В клинической практике гепатолога преобладают воспалительные заболевания печени. Во многом это обусловлено тем, что практически любое повреждающее воздействие на печень может привести к гибели гепатоцитов и развитию воспалительной реакции, а частично связано с тем, что воспалительные заболевания часто имеют длительное течение. Воспалительные заболевания печени чаще всего вызваны вирусами.
Поражение печени наблюдается при следующих системных вирусных заболеваниях:
(1) инфекционном мононуклеозе, острая фаза которого может сопровождаться легким гепатитом;
(2) цитомегаловирусной инфекции, особенно у новорожденных или иммунокомпрометированных пациентов;
(3) желтой лихорадке, которая является основной причиной гепатита в тропических странах.
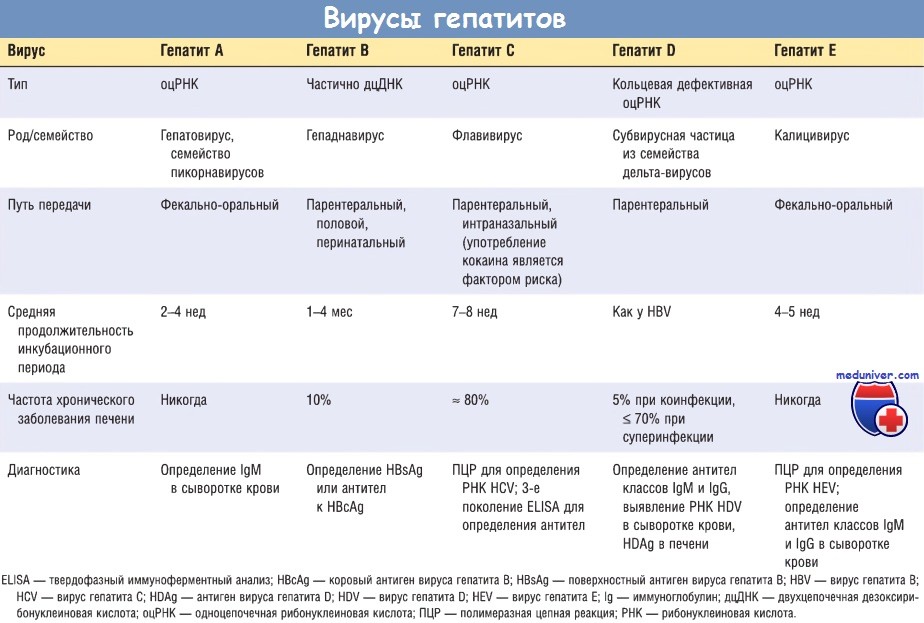
Изредка у детей и иммунокомпрометированных пациентов поражение печени может развиться при краснухе, аденовирусной, герпес-вирусной и энтеровирусной инфекциях. Однако в большинстве случаев термин «вирусный гепатит» используют для обозначения инфекционного поражения печени, вызванного группой гепатотропных вирусов (вирусов гепатита А, В, С, D и Е), которые обладают высокой аффинностью к клеткам печени. Вначале будут описаны основные признаки каждого гепатотропного вируса, а затем — клинико-патологические характеристики острого и хронического вирусных гепатитов.
Вирус гепатита А (HAV) вызывает прогностически благоприятное, самопроизвольно проходящее заболевание с инкубационным периодом 3-6 нед. НAV не вызывает хронический гепатит и не сопровождается вирусоносительством, а также крайне редко является причиной молниеносного гепатита, в связи с чем смертность от HAV-инфекции составляет 0,1%. HAV распространен повсеместно и является возбудителем эндемичного заболевания в странах с неблагоприятными санитарно-гигиеническими условиями, у многих жителей которых уже к 10-летнему возрасту определяются антитела к HAV.
Заболевание обычно протекает в легкой форме или вообще бессимптомно, редко наблюдается у взрослых. В развитых странах количество лиц, серопозитивных по антителам к HAV (признак предшествующего контакта с вирусом), увеличивается с возрастом и в возрастной группе 50 лет достигает 50%. В этой популяции острый гепатит, вызванный HAV, обычно проявляется спорадической лихорадкой. У заболевших появляются неспецифические симптомы, такие как недомогание и потеря аппетита, достаточно часто развивается желтуха. В целом HAV является причиной « 25% острых гепатитов в мире, а в США ежегодно регистрируют 30-50 тыс. новых случаев этого заболевания.
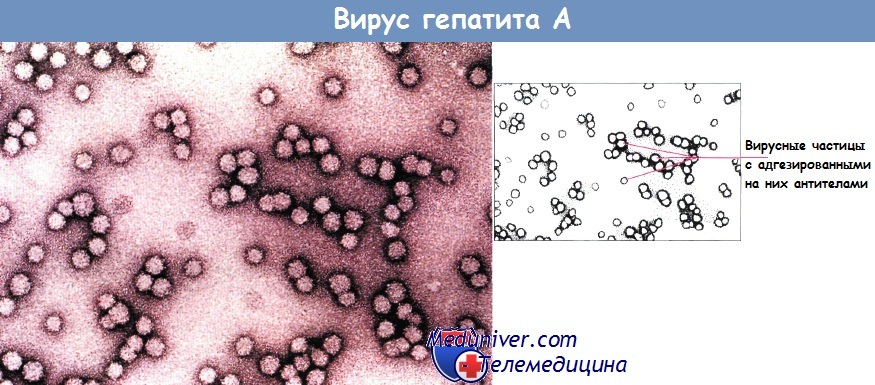
Вирус гепатита А (HAV), открытый в 1973 г., представляет собой небольшой безоболочечный пикорнавирус из рода Неpatovirus, имеющий одноцепочечную РНК, которая содержит все его гены. Вирус можно культивировать in vitro. Капсид HAV представляет собой икосаэдр (двадцатигранник) диаметром 27 нм. Рецептором для HAV является HAVcr-1 — внутримембранный муциноподобный гликопротеин I, содержащий 451 аминокислотную последовательность, физиологическая функция которого неизвестна. Инфицирование HAV происходит при употреблении зараженной воды или пищи, при этом вирус присутствует в фекалиях за 2-3 нед до и в течение 1 нед после развития желтухи.
Таким образом, большинство заражений происходит после тесного контакта с инфицированным человеком или в результате фекально-орального пути передачи возбудителя в течение указанного периода времени, что объясняет вспышки заболевания в школах и детских садах и эпидемии в густонаселенных областях с антисанитарными условиями. HAV также может обнаруживаться в сыворотке крови и слюне. Поскольку при вирусном гепатите А виремия кратковременна, гематогенная передача HAV отмечается крайне редко, поэтому скрининг донорской крови на этот вирус не проводят. В развитых странах спорадические случаи данного заболевания могут быть связаны с употреблением в пищу сырых или обработанных паром устриц, мидий и других моллюсков, в которых может накапливаться вирус, попавший в морскую воду с нечистотами.
Инфицированные работники пищевой промышленности также могут быть источником вспышек вирусного гепатита A. HAV не обладает прямым цитопатическим действием. В повреждении печени при HAV-инфекции ключевую роль играет система клеточного иммунитета, особенно Т-лимфоциты CD8+.
Специфические антитела к HAV, относящиеся к классу IgM, появляются в крови одновременно с первыми симптомами, выступая в роли достоверных маркеров острой инфекции. Об окончании выделения вируса с фекалиями свидетельствует повышение титра IgM. Уровень IgM обычно снижается в течение нескольких месяцев; позднее их сменяют антитела класса IgG. Последние циркулируют годами, возможно, обеспечивая пожизненный иммунитет ковсем штаммам HAV. До сих пор отсутствуют тест-системы для определения анти-HAV IgG, но об их наличии косвенно свидетельствует разница между количеством общих анти-HAV антител и количеством анти-HAV IgM.
Вакцинация против HAV, ставшая общедоступной с 1992 г., является эффективным способом профилактики инфицирования.
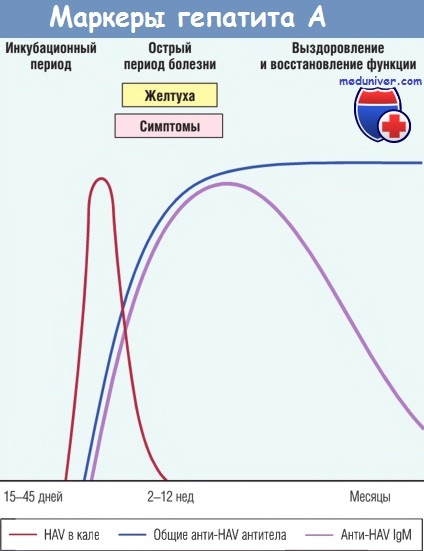
HAV — вирус гепатита A; Ig — иммуноглобулин.
источник
С 1998 г. ВОЗ выделяет 8 нозологических форм вирусных гепатитов – А, В, С, Д, Е, F, G и TTV, причем 2 из них имеют фекально-оральный механизм передачи. Это вирусные гепатиты А и Е.
Вирус гепатита А (HAV) открыт в 1973 г. Возбудитель содержит РНК, относится к роду энтеровирусов, семейству пикорнавирусов. Размеры его 27 — 32 нм. Известен только один серотип ВГА, в состав которого входят 7 генотипов вируса, имеющих один и тот же антиген – HAVAg.
Из специфических маркеров важнейшими являются anti-HAV класса иммуноглобулинов «М», которые появляются в начале заболевания и сохраняются до 6 месяцев и анти-HAV класса IgG, которые появляются с 4-5 недели болезни и длительно сохраняются, свидетельствуюя о ранее перенесенном ВГА. Антиген ВГА появляется в фекалиях в конце инкубационного периода, обнаруживается в течение продромального периода болезни и первые дни после появления желтухи. Длительного носительства вируса не бывает. Во внешней среде вирус устойчив – при комнатной температуре может сохраняется несколько месяцев, зато он быстро (в течение 5 минут) инактивируется при кипячении.
Вирус гепатита Е открыт в 1983 г., относится к РНК-содержащим вирусам размерами 24-34 нм. По сравнению с ВГА вирус менее устойчив к физическим и химическим воздействиям. Из специфических маркеров инфекции важнейшими являются anti-HEV класса иммуноглобулинов «М», которые появляются рано и сохраняются до 4-6 месяцев и класса «G», которые появляются поздно и сохраняются длительное время.
Вирусные гепатиты А и Е относятся к убиквитарным инфекциям, причем уровень заболеваемости коррелирует с санитарно-гигиеническим состоянием местности. Источником инфекции являются больные, особенно безжелтушными, стертыми или бессимптомными формами ВГА и ВГЕ. Выделение вирусов с фекалиями начинается в конце инкубационного периода с максимальной заразительностью в преджелтушном периоде. При появлении желтухи выделение вируса с фекалиями резко уменьшается. Вирусемия очень кратковременная и эпидемиологического значения не имеет.
Сезонность ВГА осенне-зимняя. Фекально-оральный механизм передачи реализуется алиментарным, водным и контактно-бытовым путями. Заража-ющая доза крайне мала и составляет от 100 до 500 вирусных частиц. Наиболее восприимчивы к ВГА дети после 1 года. К группам повышенного риска относятся организованные детские и воинские коллективы. Иммунитет после перенесенного заболевания напряженный, длительный, часто пожизненный.
ВГЕ характеризуется фекально-оральным механизмом заражения с доминирующей водного пути передачи. Отмечается у лиц молодого возраста, проживающих в тропических или субтропических регионах. Эпидемиологическими особенностями ВГЕ являются неравномерность территориального распределения, «взрывной» характер вспышек в районах с неудовлетворительным водоснабжением, частое поражение лиц мужского пола из-за купания в открытых водоемах.
Клиника и клиническая классификация ВГ с фекально-оральным механизмом передачи.
Клиника вирусного гепатита А.Инкубационный период от 7 до 50 дней, в среднем составляет 35 дней. Преджелтушный период продолжается от 4 до 8 дней, протекает в виде катарального (гриппоподобного), диспептического (гастроэнтеритического) или астеновегетативного вариантов. Желтушный период проявляется желтушным окрашиванием склер, слизистой полости рта, затем – желтушностью кожи. Желтуха быстро нарастает, достигая максимума в первые дни. Продолжает темнеть моча, обесцвечивается кал. Печень увеличивается в размерах, край ее чувствительный при пальпации. У части больных увеличивается селезенка (по данным пальпации и/или перкуссии). Характерны брадикардия и гипотония.
За периодом разгара болезни следует фаза реконвалесценции, когда улучшается самочувствие, ослабевают признаки нарушения пигментного обмена. Хронизации процесса не бывает. Вирусоносительство не формируется.
Клиника вирусного гепатита Е. Инкубационный период составляет 20 — 60 дней, в среднем 30 суток. Преджелтушный период протекает 5-7 дней по диспептическому (гастроэнтеритическому) или астеновегетативному варианту на фоне симптомов общей интоксикации. Лихорадочная реакция в преджелтушный период отсутствует или слабо выражена. С появлением желтухи симптомы общей интоксикации не уменьшаются. Желтуха нарастает 3-7 дней, она более интенсивная и длительная, чем при ВГА. Обычно желтуха появляется на фоне болевого синдрома в правом подреберье или эпигастрии. Часто затяжное течение желтухи с преобладанием синдрома холестаза. Хронизации процесса не отмечается.
Гепатолиенальный синдром более выражен и длителен, чем при ВГА. Характерен зуд кожи, расчесы или следы расчесов на коже. ВГЕ тяжело протекает у беременных, в раннем послеродовом периоде у кормящих грудью. Заболевание может приобретать злокачественное течение с быстрым развитием массивного некроза печени и острой печеночной энцефалопатией. При этом часто возникает ДВС-синдром, гемолиз эритроцитов, гемоглобинурия, что приводит к острой почечной недостаточности. Другим грозным осложнением болезни является геморрагический синдром, проявляющийся желудочно-кишечным, маточным и др. кровотечением, что также может привести к летальному исходу.
В классификации вирусных гепатитов выделяют.
1. Этиологический фактор:
— манифестная (желтушная с преобладанием синдрома цитолиза или холестаза и безжелтушная формы);
— бессимптомная (латентная) — субклиническая и инаппарантная.
источник
ВИРУСНЫЕ ГЕПАТИТЫ
Термином «гепатит» обозначают воспалительные заболевания печени различной этиологии.
Функции печени:
Пищеварительная.
Клетки печени вырабатывают желчь, поступающую в 12-перстную кишку. Желчь эмульгирует жиры, способствует их расщеплению и усвоению.
Клетки печени нейтрализуют множество ядовитых веществ, поступающих с кровью и лимфой (как экзогенных, так и эндогенных), также микроорганизмы (вирусы, бактерии), погибшие в результате работы иммунной системы, утилизируются печенью. Печень обезвреживает и множество живых микроорганизмов, не допуская их размножения.
Депонирующая
Печень является своеобразным «депо» для запасов крови и гликогена и, при возникновении дефицита крови или глюкозы, сразу компенсирует их недостаток.
Синтезирующая.
Помимо синтеза гликогена и глюкозы, печень синтезирует белки плазмы (глобулины и альбумин).
При гепатите все эти функции нарушаются.
Особенное значение поражение печени имеет в детском возрасте, поскольку печень у детей функционально незрелая, её антитоксическая и внешнесекреторные функции несовершенны. Поэтому слабость барьерной функции часто служит причиной развития токсикозов, а малое количество желчи ограничивает усвоение жиров.
Этиология и эпидемиология.
Возбудитель – вирус семейства Picornaviridae, содержит однонитевую РНК, не имеет оболочки.
Устойчив во внешней среде
Сохраняется в течение нескольких часов при температуре 60°C
Сохраняет жизнеспособность под воздействием формальдегида при температуре 37°C в течение 72-х часов
Чувствителен к ультрафиолетовым лучам и активированному хлору
Распространение вируса:
Источник инфекции – больной или вирусоноситель
Механизм передачи – фекально-оральный
Факторы передачи:
Пища (термически не обработанная)
Особая опасность – употребление в пищу устриц
Семейство не определено. Содержит однонитевую РНК, не имеет оболочки.
Свойства схожи со свойствами вируса гепатита А
Распространение вируса и факторы передачи – см. гепатит А
Особое значение имеет водный путь передачи (естественные источники воды)
Семейство Hepadnaviridae. Содержит двунитевую ДНК, имеет оболочку.
Устойчивость
Высокая устойчивость во внешней среде
При комнатной температуре сохраняет жизнеспособность в течение 3-6 месяцев
В холодильнике – 6-12 месяцев
В замороженном виде – до 20 лет
В высушенном состоянии – до 25 лет
Устойчив к воздействию химических веществ: хлорамин, формалин
Чувствительность
При автоклавировании (120°C) – активность вируса подавляется через 5 минут
При воздействии сухого жара (160°C) – активность подавляется через 2 часа
При кипячении (100°C) – инактивация через 2-10 минут
Вирус разрушается в щелочной среде, для него губительно действие перекиси водорода.
Особенности вируса гепатита В
В состав вируса входят три антигена, имеющие большое значение для лабораторной диагностики:
НВсAg (ядерный сердцевидный антиген белковой природы)
НВеAg (трансформированный НВсAg — или антиген инфекционности)
НВsAg (поверхностный австралийский антиген, расположенный на оболочке вируса)
Распространение вируса:
Резервуаром и источником инфекции являются лица с манифестными или атипичными формами болезни.
Механизм передачи – гемоконтактный.
Пути передачи:
Через молоко больной матери
Факторы передачи:
Незащищённый половой контакт
Медицинские инструменты (шприцы, иглы и др.)
Семейство Flaviviridae, содержит однонитевую РНК, имеет оболочку
Свойства вируса:
Относительно неустойчив во внешней среде.
При температуре 60°C сохраняет жизнеспособность в течение 10-ти часов
При кипячении инактивируется в течение 2-х минут
Чувствителен к хлороформу и формалину
Распространение вируса:
Резервуаром и источником инфекции является больной острой или хронической формой гепатита
Механизм передачи – гемоконтактный
Пути передачи:
Через молоко больной матери
Факторы передачи:
Незащищённый половой контакт
И другие факторы (см. гепатит В)
Семейство Togaviridae, род Deltavirus.Содержит РНК, имеет оболочку.
Свойства вируса:
Устойчив к нагреванию, действию кислот, ультрафиолетовому облучению.
Инактивируется щелочами и протеазами.
Репликация вируса происходит только в присутствии вируса гепатита В
Внешней оболочкой вируса является HBsAg вируса гепатита В (вирус-паразит)
Распространение вируса:
Резервуаром и источником инфекции являются больные острой и хронической D-инфекцией и здоровые носители.
Механизм передачи – гемоконтактный
Пути передачи – такие же, как у гепатита В
К вирусу очень восприимчивы дети раннего возраста.
Семейство Flaviviridae (условно), содержит однонитевую РНК, имеет оболочку.
Чувствительность и устойчивость вируса слабо изучены.
По свойствам близок к вирусу гепатита С, но для него не храрактерно прогрессирование инфекционного процесса с последубщим развитием цирроза и рака печени.
Механизм и пути передачи такие же как у гепатита С.
Патогенез вирусных гепатитов
Вирусный гепатит А
Входные ворота – слизистые оболочки ротоглотки и тонкой кишки
Основные звенья патогенеза:
Накопление вируса в эпителиальных клетках ЖКТ
Проникновение в лимфоидные образования входных ворот (кольцо Пирогова, мезентериальные лимфатические узлы кишечника)
Первичная презентация вируса иммунокомпетентным клеткам
Проникновение вируса в кровь (первичная вирусемия)
Накопление вируса в гепатоцитах
Репликация вируса в гепатоцитах, высвобождение вируса в желчь без разрушения клеток
Вторичное попадание вируса в кровоток (вторичная вирусемия)
Взаимодействие АГ вируса с иммунокомпетентными клетками в месте входных ворот
Развитие реакции гиперчувствительности замедленного типа
Клинически это проявляется катаральными изменениями в ротоглотке и слизистой оболочке ЖКТ, температурной реакцией, диспепсическими расстройствами и знаменует окончание инкубационного периода.
Вирус не оказывает прямого цитотоксического действия. Разрушение гепатоцита происходит в результате развития Т-клеточного иммунного ответа.
После разрушения 70% (и более) гепатоцитов развивается гипербилирубинемия, что соответствует появлению желтухи.
Антигены к гепатиту А (IgM) появляются в крови уже в конце инкубационного периода, в результате вирус быстро исчезает из крови.
Исчезновение вируса из сыворотки крови и появление антигенов соответствует завершению преджелтушного периода и разгару заболевания.
Вирусный гепатит Е
Патогенез аналогичен патогенезу вирусного гепатита А
Вирусный гепатит В
Входные ворота – повреждённые кожные покровы и слизистые оболочки, а также – сосуды при инъекциях.
Основные звенья патогенеза:
Проникновение вируса в печень с кровотоком
Фиксация вируса на гепатоцитах
Проникновение вируса в клетку
Высвобождение вирусной ДНК
Проникновение ДНК в ядро гепатоцита
Начало синтеза нуклеиновых кислот и «сборка» вируса
Репликация вируса в гепатоцитах (возможна репликация в клетках костного мозга, макрофагах и Т-хелперах)
Дочерние популяции вируса накапливаются на поверхности гепатоцита
Разрушение гепатоцитов, содержащих вирус, происходит за счёт трёх механизмов:
Воздействие иммунокомпетентных клеток — Т-цитотоксические клетки, естественные киллеры и макрофаги.
Действие лизосомальных ферментов, разрушающих мембрану клетки.
Действие противопечёночных гуморальных аутоантител
источник
Вирусный гепатит А-острая циклическая инфекция, характеризующаяся четкой сменой периодов.После заражения ВГА из кишечника проникает в кровь и далее в печень, где после фиксации к рецепторам гепатоцитов проникает внутрь клеток. На стадии первичной репликации отчетливых повреждений гепатоцитов не обнаруживается. Новые поколения вируса выделяются в желчные канальцы, далее поступают в кишечник и выделяются с фекалиями во внешнюю среду. Часть вирусных частиц проникает в кровь, обусловливая развитие интоксикационной симптоматики продромального периода. Повреждения гепатоцитов, возникающие в ходе дальнейшего течения ГА, обусловлены не репликацией вируса, а иммуноопосредованным цитолизом. В периоде разгара ГА морфологическое исследование позволяет выявить воспалительные и некробиотические процессы, происходящие преимущественно в перипортальной зоне печеночных долек и портальных трактах. Эти процессы лежат в основе развития трех основных клинико-биохимических синдромов: цитолитического, мезенхимально-воспалительного и холестатического. К лабораторным признакам цитолитического синдрома относятся: повышение активности ферментов АлАТ и АсАТ (аланинамино- и аспартатаминотрансферазы), уровня железа в сыворотке крови, снижение синтеза альбумина, протромбина и других факторов свертывания крови, эфиров холестерина. Начальным этапом цитолитического синдрома является повышение проницаемости мембраны гепатоцитов. Это обусловливает выход в кровь, прежде всего АлАТ — фермента, находящегося в цитоплазме печеночной клетки. Повышение активности АлАТ — ранний и надежный индикатор повреждения гепатоцита. Мезенхимально-воспалительный синдром характеризуется повышением уровня бета- и гаммаглобулинов, изменением коллоидных проб (снижение сулемового титра и повышение тимоловой пробы). Холестатический синдром проявляется повышением в крови уровня связанного билирубина, желчных кислот, холестерина, меди, активности щелочной фосфатазы, а также билирубинурией, уменьшением (исчезновением) уробилиновых тел в моче. Вследствие комплексных иммунных механизмов (усиление интерферонопродукции, активизации естественных киллеров, антителопродукции и активности антителозависимых киллеров) репликация вируса прекращается, и происходит его элиминация из организма человека. Для ГА не характерны ни длительное присутствие вируса в организме, ни развитие хронической формы болезни. Однако иногда течение заболевания может быть модифицировано в случаях ко-инфекции или суперинфекции другими гепатотропными вирусами. У лиц же с генетической предрасположенностью возможно развитие хронического активного аутоиммунного гепатита 1-го типа
Вирусный гепатит В Из места внедрения ВГВ гематогенно достигает печени, где в гепатоцитах происходит репликация вирионов. ВГВ не обладает цитотоксичностью. Сам вирус гепатита В проникнув в клетку, оставляет свой антиген на поверхности гепатоцита. Эти клетки опознаются Т-лимфоцитами как чужеродные и подвергаются агрессии. Таким образом, поражение клеток печени при гепатите В является иммуннообусловленными. Кроме этого при хроническом гепатите В в процесс вовлекаются Т-супрессоры. Они находятся в подавленном состоянии и поэтому формируются условия для развития аутоиммунных реакций, направленных против собственных клеточных антигенов.Следствием этого является развитие некробиотических и воспалительных изменений в паренхиме печени. В результате патологических изменений в печеночной ткани возникают цитолитический, мезенхимально-воспалительный и холестатический синдромы с определенными клиническими и лабораторными проявлениями .
При морфологическом исследовании обнаруживают дистрофические изменения гепатоцитов, зональные некрозы, активизацию и пролиферацию звездчатых эндотелиоцитов (клеток Купфера); в более тяжелых случаях — субмассивные и массивные некрозы печени, которые, как и распространенные «мостовидные» и мультилобулярные некрозы, являются нередко патологоанатомическим субстратом печеночной комы. Холестатические варианты ГВ сопровождаются вовлечением в патологический процесс внутрипеченочных желчных ходов с образованием в них «желчных тромбов», увеличением содержания билирубина в гепатоцитах.
В патогенезе ГВ, кроме репликативной, выделяют также интегративную форму течения инфекции. При этом происходит встраивание всего генома вируса в геном клетки хозяина или его фрагмента, отвечающего, например, за синтез HBsAg. Последнее приводит к присутствию в крови лишь HBsAg.Интеграция генома ВГВ в геном гепатоцита является одним из механизмов, обусловливающих развитие персистирующих (ациклических) форм течения ГВ и первичной гепатоцеллюлярной карциномы.
Вирусный гепатит С После проникновения в организм человека ВГС, обладая гепатотропностью, реплицируется преимущественно в гепатоцитах. ВГС обладает слабой иммуногенностью, что определяет замедленный, неинтенсивный Т-клеточный и гуморальный ответ иммунной системы на инфекцию. Так, в острой стадии ГС сероконверсия возникает на 1-2 мес. позже появления признаков цитолиза гепатоцитов (повышения активности АлАТ). Лишь через 2-10 нед. от начала заболевания в крови больных начинают определяться антитела к ядерному антигену классов M, затем G. Однако они обладают слабым вируснейтрализующим действием. Антитела же к неструктурным белкам ВГС в острой фазе инфекции обычно не выявляются. Зато в крови в течение острой стадии болезни (и при реактивации — в хронической) определяется присутствие РНК вируса. Устойчивость ВГС к специфическим факторам иммунитета обусловлена его высокой способностью к «ускользанию» из-под иммунологического надзора. Таким образом, слабость иммунного реагирования и мутационная изменчивость вируса во многом обусловливают высокий хрониогенный потенциал данного заболевания.
Вирусный гепатит D Этот вирус является дефектным, так как он на своей поверхности не имеет рецепторов для гепатоцитов. Поэтому он не может проникнуть в клетку и реплицироваться в ней. Для репродукции данного вируса необходимо участие «вируса-помощника». Роль этого помощника играет вирус гепатита В. таким образом, заболевание может возникнуть при одновременном заражении обоими вирусами или при инфицировании лиц уже имеющих вирус гепатита В (суперинфекция). Сочетанное действие обоих вирусов приводит к развитию более тяжелых форм заболевания с выраженными явлениями печеночно-клеточной недостаточности. В большинстве случаев заболевание приобретает прогрессирующее течение с быстрым переходом в цирроз печени и смертью.
Вирусный гепатит Е изучен недостаточно. Большинство исследователей полагают, что центральным звеном патогенеза является цитопатическое действие вируса. Не исключается и участие иммунных механизмов в некробиотических изменениях печеночной ткани.
источник
Обычными входными воротами для вируса вирусного гепатита А служат слизистые оболочки ротоглотки и тонкой кишки. В месте внедрения развивается воспалительный процесс, обусловливающий формирование катарального синдрома, диспептических явлений и температурной реакции. Проникновение возбудителя в кровь приводит к вирусемии, благодаря которой он достигает печени. В настоящее время предполагают, что повреждение гепатоцитов обусловлено клеточными цитотоксическими иммунными реакциями. Вместе с тем не исключают прямое цитопатическое действие вируса на гепатоциты. У больных вирусным гепатитом А при биопсии печени установлено значительное повреждение портальной зоны с интенсивной клеточной инфильтрацией и разрушением пограничной пластины, выраженными признаками холестаза.
Даже при небольшом поражении гепатоцитов формируется гепатолиенальный синдром, развивается дискинезия желчевыводящих путей; при более выраженном поражении печени возникает желтуха. В дальнейшем для восстановления гепатоцитов требуется несколько недель, а для восстановления полной цитоархитектоники печени — несколько месяцев.
Антигены вируса вирусного гепатита А проявляют высокую иммуногенность: активация иммунной системы и специфическая сенсибилизация лимфоцитов начинаются с момента внедрения возбудителя.
Антигены вируса (оболочечные белки) экспрессируются на мембранах гепатоцитов в комплексе с антигенами главного комплекса гистосовместимости (HLA) I типа, и инфицированные клетки уничтожаются цитотоксическими Т-лимфоцитами и Т-киллерами.
Сходство антигенов вируса и антигенов гепатоцитов определяет развитие общих аутоиммунных процессов, от интенсивности которых во многом зависит исход заболевания. У лиц с генетической предрасположенностью вследствие вирусного гепатита А может развиться хронический аутоиммунный гепатит I типа. Описаны нефротический синдром с развитием мезангиопролиферативного гломерулонефрита, артриты, васкулиты, криоглобулинемии; при этом вирусный гепатит А выступал в качестве провоцирующего фактора. В очень редких случаях (0,1%) возможно развитие фульминантных форм вирусного гепатита А.
Уже в инкубационный период выявляют специфические IgM; длительность инкубации объясняют индивидуальные особенности иммунного ответа. При быстром нарастании титров антител желтуха не развивается.
В результате иммунных реакций в большинстве случаев довольно быстро, в течение 2-3 нед, наступает выздоровление с полным освобождением организма от вируса. Вирусоносительство и хронические формы при вирусном гепатите А не наблюдают.
Инкубационный период продолжается 3-4 нед. Вирусный гепатит А протекает как острое циклическое заболевание и характеризуется последовательной сменой нескольких периодов — продромального (дожелтушного), разгара (желтушного) и периода реконвалесценции.
Дожелтушный период. Характеризуется достаточно широким разнообразием симптомов, условно сгруппированных в несколько вариантов его течения.
1. Гриппоподобный (лихорадочный, катаральный) вариант при вирусном гепатите А встречается наиболее часто. Обычно заболевание начинается достаточно остро с повышения температуры тела (от субфебрильных до высоких цифр), слабости, недомогания, мышечных болей, развития лёгких катаральных симптомов (заложенность носа, боли или першение в горле, покашливание). Однако гриппоподобная симптоматика у большинства больных сопровождается диспептическими расстройствами различной степени выраженности.
2. Диспептический вариант. Катаральные явления отсутствуют, и на первый план выступают симптомы вовлечения ЖКТ. Больных беспокоят дискомфорт в эпигастральной области, снижение аппетита до полной анорексии, тошнота, иногда рвота, возникающая чаще после приёма пищи. Возможны тупые боли в правом подреберье, горечь во рту, отрыжка, запоры или послабление стула.
3. Астеновегетативный вариант. Характеризуется рядом неспецифических симптомов: развитием общей слабости, потерей работоспособности, раздражительностью или безразличием, стойкой бессонницей или, наоборот, сонливостью.
Вирусный гепатит А может клинически проявиться сразу же с развития желтухи; в этом случае продромальные признаки отсутствуют (латентный вариант начального периода).
Следует подчеркнуть, что клиническая симптоматика, отнесённая к различным вариантам дожелтушного периода, может сочетаться в различных комбинациях. В этих случаях говорят о смешанном варианте.
Осложнения вирусного гепатита А.
Развиваются сравнительно редко. К ним можно отнести обострения воспалительных процессов в жёлчных путях (холециститы, холангиты, дискинезии), а также развитие вторичных инфекций (пневмонии и др.). Острая печёночная энцефалопатия при вирусном гепатите А развивается крайне редко.
Диагностика вирусного гепатита А в начальный его период крайне затруднена. Необходимо опираться на данные эпидемиологического анамнеза (контакт с желтушными больными). При осмотре больных уже в это время можно обнаружить увеличенную в размерах печень и повышение показателей аминотрансфераз.
Начальный период заболевания продолжается от 2 до 7-10 дней и плавно переходит в желтушный. К этому моменту нормализуется температурная реакция, исчезают катаральные явления, однако диспептические симптомы сохраняются или даже могут возрастать по интенсивности.
Начало желтушного периода необходимо считать с момента появления тёмной мочи. Вслед за этим появляется иктеричность на уздечке языка, мягком нёбе, склерах, затем на кожных покровах. Её интенсивность быстро прогрессирует, обычно через 3-4 дня достигая максимума; при этом желтуха часто приобретает шафранный оттенок. Принято считать, что интенсивность желтухи прямо пропорциональна тяжести заболевания, однако при этом необходимо больше ориентироваться на выраженность синдрома интоксикации: повторную рвоту, диспептические расстройства, степень снижения аппетита. При более тяжёлом течении болезни на кожных покровах можно отметить появление синяков, особенно в местах инъекций. У части больных наблюдают носовые кровотечения.
Язык, как правило, обложен. Пальпаторно определяют увеличенную в размерах печень, чувствительную при пальпации; степень её увеличения может быть различной. В 30-40% случаев к этому времени обнаруживают спленомегалию. У части больных в разгар желтухи появляется обесцвеченный стул. Со стороны сердечно-сосудистой системы достаточно характерны брадикардия и тенденция к снижению артериального давления. На фоне желтухи помимо диспептических явлений больные отмечают адинамию, головокружение, иногда расстройства сна.
Продолжительность желтушного периода при вирусном гепатите А не превышает 30 дней. Чаще он длится около 2 нед и переходит в период реконвалесценции. К этому времени происходит постепенное снижение интенсивности желтушного синдрома, уменьшается в размерах печень, исчезают признаки интоксикации. Период реконвалесценции значительно более длителен, чем период желтухи, и может затягиваться до 3-6 мес.
У 5-10% больных вирусным гепатитом А может приобрести более длительное течение, характеризующееся малыми проявлениями или отсутствием интоксикации, небольшими цифрами билирубинемии и гиперферментемии, стойким увеличением в размерах печени. Чаще всего это объясняет развитие холестаза. Несмотря на увеличенную продолжительность заболевание заканчивается благоприятно.
Вирусный гепатит А обычно протекает в лёгкой или средне-тяжёлой формах, но не исключены и тяжёлые варианты, и обострения.
Диагностика вирусного гепатита А в основном осуществляется при выраженном желтушном синдроме, однако накопилось большое количество сообщений о том, что вирусный гепатит А зачастую может протекать в безжелтушной форме, которая в большинстве случаев не диагностируется. По мнению ряда исследователей, соотношение желтушных и безжелтушных форм может достигать 3:7.
В дожелтушный период вирусный гепатит А необходимо проводить дифференциальную диагностику с острыми респираторными и кишечными инфекциями. Определённую помощь в дифференциальной диагностике могут оказать данные эпидемиологического анамнеза: контакт с желтушными больными, пребывание больного в районах, неблагополучных по гепатиту А. В некоторых случаях уже в дожелтушный период можно обнаружить увеличенную в размерах печень, а также повышение активности аминотрансфераз.
В желтушный период заболевание дифференцируют с обтурационными и гемолитическими желтухами, мононуклеозом, иерсиниозом, лептоспирозом. Клиническая картина, во многом сходная с перечисленными заболеваниями, требует определения маркёров гепатита с помощью ИФА и ПЦР, определения в крови билирубина и его фракций.
Лабораторные исследования приобретают особое значение для установления этиологии гепатита и оценки его тяжести. При анализе крови необходимо учитывать наличие лейкопении, относительного лимфоцитоза и замедление СОЭ.
Интенсивность желтухи устанавливают на основании определения уровня билирубина в крови (особенно его связанной фракции). Активность аминотрансфераз [аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (ACT)] увеличивается в несколько раз, и степень её повышения свидетельствует об интенсивности цитолиза гепатоцитов. Нарушения белоксинтетической функции печени отражают изменения показателей коллоидных проб (снижение сулемовой и повышение тимоловой проб), снижение уровня альбуминов и преальбуминов в крови, а также уменьшение показателей протромбинового индекса.
Возможно выделение вируса вирусного гепатита А из фекалий, однако в широкой медицинской практике вирусологические исследования не применяют. Для верификации диагноза используют серологические реакции — ИФА, РИА, выявляющие нарастание специфических IgM в желтушный период и нарастание титров IgG к периоду реконвалесценции. Наиболее достоверный метод диагностики — обнаружение в крови РНК вируса с помощью ПЦР.
После установления факта заболевания вирусным гепатитом А лечение больного можно проводить в амбулаторных условиях. Госпитализируют больных с тяжёлым течением заболевания, затяжными формами, при наличии тяжёлых сопутствующих заболеваний, а также лиц декретированных групп. Больным назначают постельный режим на период выраженного интоксикационного синдрома и полноценное питание. В диете исключают тугоплавкие жиры, трудно усвояемые сорта мяса (баранина, свинина, мясо водоплавающей птицы), жареные блюда, консервы, маринады, лук, чеснок и пряности. Категорически запрещено употребление алкоголя. Рекомендована молочно-растительная пища. Дополнительно в пищевые продукты добавляют витамины групп С и В. В связи с отсутствием средств этиотропной терапии проводят патогенетическое лечение. Для снятия интоксикации в зависимости от её степени применяют обильное питье или инфузионные растворы. Для ежедневного очищения кишечника и подавления анаэробной флоры рекомендовано назначать производные лактулозы, дозы которых подбирают индивидуально. Для купирования холестатического компонента применяют спазмолитики (но-шпа, эуфиллин) и производные урсодезоксихолевой кислоты.
После завершения заболевания больной подлежит диспансерному наблюдению в течение 3-6 мес.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Многие вопросы патогенеза гепатита А до настоящего времени окончательно не решены. В общей патогенетической концепции, которую можно принять за основу, допускается существование прямого цитопатического действия вируса гепатита А непосредственно на паренхиму печени.
Заражение практически всегда происходит через рот. Вирус со слюной, пищевыми массами или водой проникает вначале в желудок, а затем в тонкую кишку, где, по-видимому, внедряется шли всасывается в портальный кровоток. Ответить на вопрос, что происходит с вирусом в желудке, а .затем в тонкой кишке, не представляется возможным. Можно допустить, что в некоторых случаях действие желудочною сока оказывается губительным для вируса и, следовательно, возможна полная санация от возбудителя уже на уровне заражения. Однако такой исход заражения хотя теоретически и возможен, но все же маловероятен, поскольку вирус гепатита А подобно другим энтеровирусам, устойчив в диапазоне pH 3,0-9,0, что гарантирует ему выживание, дальнейшее продвижение в двенадцатиперстную кишку, а затем и в тонкий отдел кишечника. По современным представлениям, вирус гепатита А в тонкой кишке не задерживается и, тем более, не оказывает на слизистую оболочку повреждающего действия. Эта фаза патогенетической цепи (энтеральная), по-видимому; больше свойственна вирусным гепатитам животных.
Механизм проникновения вируса гепатита А из кишечника в кровь точно не известен. Более вероятно активное внедрение вируса через слизистую оболочку в лимфатическую систему, а затем в регионарные лимфатические узлы, но не исключена возможность пассивного транспорта с участием особых «переносчиков», облегчающих проникновение вируса через липидную мембрану.
Однако независимо от механизма проникновения через стенку тонкой кишки вирус, скорее всего, не задерживается в регионарных лимфатических узлах и, тем более, не размножается, как это предполагалось до недавнего времени, а довольно быстро оказывается в общем кровотоке и паренхиме печени. Эту фазу патогенетической цепи условно можно назвать паренхиматозной диффузией. О механизме проникновения вируса гепатита А в печеночную паренхиму существуют различные представления. Широко распространенное мнение о первичном поражении вирусом гепатита А ретикулоэндотелиальной системы печени в настоящее время можно считать ошибочным. По современным представлениям, вирус сразу проникает в гепатоциты, где находит оптимальные условия для размножения. Высказывается мнение, что проникновение вируса через мембрану гепатоцита может осуществляться путем пиноцитоза, но более вероятен активный процесс через родственный рецептор. Наличие таких рецепторов на мембране гепатоцитов будет означать восприимчивость конкретного индивидуума к инфекции гепатита А, тогда как их отсутствие, наоборот, полную невосприимчивость. Такое направление в научных исследованиях авторам этой книги кажется особенно перспективным.
Внутриклеточно расположенный вирус начинает взаимодействовать с биологическими макромолекулами, принимающими участие в процессах детоксикации. Следствием такого взаимодействия является высвобождение свободных радикалов, выступающих инициаторами процессов перекисного окисления липидов мембран клеток. Усиление процессов перекисного окисления липидов приводит к изменению структурной организации липидных компонентов мембран за счет образования гидроперекисных групп, что обусловливает появление «дыр» в гидрофобном барьере биологических мембран и, следовательно. повышение их проницаемости. Возникает центральное звено в патогенезе гепатита А — синдром цитолиза. Становится возможным движение биологически активных веществ по градиенту концентрации. Поскольку концентрация ферментов внутри гепатоцитов в десятки и даже сотни тысяч раз превышает их содержание во внеклеточном пространстве, в сыворотке крови повышается активность ферментов с цитоплазматической, митохондриальной, лизосомальной и другой локализацией, что косвенно указывает на снижение их содержания во внутриклеточных структурах, а следовательно, на пониженный биоэнергетический режим химических превращений. Нарушаются все виды обмена (белковый, жировой, углеводный, пигменгный и др.), вследствие чего возникает дефицит богатых энергией соединений, а биоэнергетический потенциал гепатоцитов падает. Нарушается способность гепатоцитов синтезировать альбумин, факторы свертывания крови (протромбин, проконвертин, проакцелерин, фибриноген и др.), различные витамины; ухудшается использование глюкозы, аминокислот для синтеза белка, сложных белковых комплексов, биологически активных соединений; замедляются процессы переаминирования и дезаминирования аминокислот; возникают затруднения в экскреции конъюгированного билирубина, эстерификации холестерина и глюкуронизации многих соединений. Все это свидетельствует о резком нарушении детоксицирующей функции печени.
Повышенная проницаемость всех субклеточных мембран, надо полагать, приводит к замене внутриклеточного калия ионами натрия и кальция в митохондриях, что еще больше усиливает «поломки» в системе окислительного фосфорилирования и способствует развитию внутриклеточного, а затем и внеклеточного ацидоза — накоплению Н-ионов.
Изменившаяся реакция среды в гепатопитах и нарушение структурной организации субклеточных мембран приводят к активации кислых гидролаз (РНК-азы, лейцинаминопептидазы, катепсинов О, В, С и пр.), чему в известной степени способствует и падение активности ингибитора протеолиза а2-макроглобул. Завершающим действием протеолитических ферментов становится гидролиз некротизированных печеночных клеток с возможным высвобождением белковых комплексов, которые могут выступать в роли ауто-антигенов и, наряду с гепатотропным вирусом, стимулировать Т- и В-системы иммунитета, активируя, с одной стороны, сенсибилизированные клетки — киллеры, с другой — вызывая образование специфических антител, способных атаковать паренхиму печени, Следует, однако, сказать, что механизмы аутоагрессии при гепатите А в полной мере не реализуются, поэтому тяжелые формы при этом виде гепатита встречаются редко.
Фаза реконвалесценции характеризуется реализацией факторов защиты и репаративных процессов, полной элиминацией вируса и восстановлением функционального состояния печени. Практически у всех пациентов наступает выздоровление с полным восстановлением структуры и функций органа в сроки от 1,5 до З мес от начала болезни. Только у некоторых пациентов (3-5%) первоначальные факторы зашиты могут оказаться недостаточными, и может наблюдаться относительно длительная (от 3 до 6-8 мес и дольше) репликативная активность вируса в гепатоцитах с нарушением их структуры и функции. В таких случаях формируется затяжное течение болезни с пролонгированным механизмом структурно-функциональных изменений. Однако и у этих больных в конечном итоге механизмы защиты побеждают — вирусная активность блокируется, и наступает полное выздоровление. Формирования хронического процесса в исходе инфекции гепатита А не происходит.
Приведенные данные, разумеется, не исчерпывают сложный патогенез гепатита А, при котором страдают все органы и системы. С первых дней инфицирования поражается ЦНС, о чем свидетельствует появление таких симптомов, как вялость, адинамия, головная боль, бессонница, раздражительность и другие расстройства. Причиной нарушений со стороны ЦНС служит интоксикация, возникающая, с одной стороны, в результате вирусемии и действия вируса на ЦНС, с другой — в результате распада пораженных печеночных клеток и высвобождения эндогенных токсинов, а также нарушения функциональной способности печени.
С первых дней заболевания нарушается функция ЖКТ, при этом имеется угнетение желудочной секреции и функции поджелудочной железы. Результатом этого становятся снижение аппетита, вплоть до анорексии, нередко тошнота, рвота, расстройство стула, что обычно наблюдается в самом начале заболевания.
Обобщенно можно сказать, что при гепатите А патологический процесс проходит ряд последовательных, взаимообусловленных этапов, причем на первых этапах ведущим является действие вируса, вызывающее появление общетоксического синдрома, а на последующих — обменные нарушения с возможным возникновением так называемого вторичного метаболического токсикоза. Однако, независимо от стадии заболевания, печень служит главной ареной патологического процесса.
Хотя некоторые исследователи и сообщают о прямом цитопатическом действии вируса гепатита А, но фактических материалов, подтверждающих это положение, в работах не приводится. В опытах на обезьянах и клеточных культурах показана локализация вирусного антигена в цитоплазме гепатоцитов при полном отсутствии его в ядрах. При изучении динамики размножения вируса гепатита А выявлено, что максимальная продукция внутриклеточного вирусного антигена отмечается на 3-4-й неделе от начала заражения, что совпадает с динамикой обнаружения вируса у больных. Однако полностью переносить результаты, полученные in vitro, на заболевание у человека не представляется возможным. Есть мнение, что своеобразие репродукции вируса гепатита А in vitro состоит в том, что он исключительно долго репродуцируется в культуре и у него полностью отсутствует цитопатический эффект. Если все же допустить, что вирус гепатита А не обладает цитопатическим действием, то придется признать, что поражение гепатоцитов при гепатите А связано в первую очередь с сенсибилизацией лимфоцитов к антигенам вируса-возбудителя и, возможно, денатурированным белкам гепатоцитов.
В настоящее время в патогенезе вирусных гепатитов, в том числе гепатита А, большое значение придают иммунологическим механизмам повреждения печеночных клеток. В исследованиях последних лет установлено, что поражение инфицированных печеночных клеток при гепатите А осуществляется сенсибилизированными цитотоксическими Т-лимфоцитами.
Другими дополнительными механизмами гепатодеструкции при гепатите А могут быть К-клеточный цитолиз и иммунокомплексное поражение гепатоцитов.
По нашим наблюдениям и с учетом данных литературы, можно считать, что для гепатита А востром периоде болезни характерны Т-лимфопения, Т-лимфоцитоз — активных, термостабильных и ауторозеткообразующих клеток. При этом соотношение Т-лимфоцитов с хелперной активностью и Т-лимфоцитов с супрессорной активностью снижается.
Содержание В-клеток существенно не меняется. Указанные сдвиги в показателях иммунологического реагирования существенно зависят от тяжести заболевания. Особенно значительное снижение Т-клеток отмечается при тяжелых формах болезни, и, наоборот, содержание Т-активных, Т-многорепепторных, термостабильных и ауторозеткообразующих клеток бывает тем больше, чем тяжелее патологический процесс в печени. Пропорционально нарастанию тяжести заболевания усиливается специфическая сенсибилизация к печеночному липопротеину, и возрастают показатели активности натуральных киллеров и антителозависимая клеточная цитотоксичность.
Отмеченные сдвиги иммунологического реагирования отражают адекватность иммунного ответа у больных гепатитом А, направлены на элиминацию инфицированных гепатоцитов и обеспечение полноценного иммунитета и полного выздоровления.
При развитии затяжного гепатита А отмечается более выраженное снижение числа Т-лимфоцитов при относительно слабой мобилизации функционально активных субпопуляций Т-клеток и умеренном сдвиге соотношения хелперных и супрессорных Т-лимфоцитов в сторону преобладания первых, что в конечном итоге приводит к увеличению синтеза продукции IgМ, а также повышению сенсибилизации Т-клеток к ЛП4. Такой тип иммунологического реагирования предопределяет замедленный цикл инфекционного процесса. В этих случаях можно предполагать, что антигены вируса гепатита А, расположенные на поверхности гепатоцитов, вызывают слабую активацию Т-клеток индукторов иммунного ответа и столь же слабое подавление супрессорных Т-клеток. Это взаимодействие иммунокомпетентных клеток создает условия для замедленного специфического иммуногенеза, завершающегося (через замедленный цикл) формированием достаточно стойкого протективного иммунитета.
В полном соответствии с характером клеточного иммунологического реагирования находятся изменения в механизмах иммунокомплексообразования.
Проведенные исследования показали, что у всех больных гепатитом А на высоте клинических проявлений в крови резко повышается концентрация иммунных комплексов и возрастает их комплементсвязываюшая активность. Важно отметить, что в этот период болезни в крови циркулируют преимущественно комплексы крупных размеров, в чьем составе преобладают иммуноглобулины класса М. Такие иммунные комплексы, как известно, легко связывают комплемент, быстро выводятся из организма клетками мононуклеарно-фагоцитарной системы. При гладком течении гепатита А динамика ЦИК в сыворотке крови строго коррелирует с характером патологического процесса в печени, тогда как у больных с затяжным течением болезни высокий уровень иммунных комплексов служит предвестником неблагоприятного исхода. При этом в составе ЦИК резко возрастает доля средних и мелких иммунных комплексов, обладающих слабой комплементсвязывающей активностью, и, кроме того, в их составе возрастает доля иммуноглобулинов G, что затрудняет их элиминацию клетками макрофагальной системы и, следовательно, может стать решающей причиной затяжного течения гепатита А.
Таким образом, фактические материалы позволяют считать гепатит А, как и гепатит В, иммунопатологическим заболеванием. Однако сходство этих заболеваний лишь внешнее и просматривается преимущественно по характеру иммунологического реагирования. Иммунологические сдвиги при гепатите А возникают на мембранные антигены гепатоцитов с экспрессированными вирусными антигенами, что отражает некрозогенный эффект возбудителя. Кроме того, хотя при гепатите А и возникает специфическая сенсибилизация иммунокомпетентных клеток к липопротеину гепатоцитов, но все же выраженного иммунного цитолиза гепатоцитов не происходит, поскольку вирус гепатита А не интегрируется в геном клетки. В связи с этим реакции иммунного цитолиза не пролонгированы во времени, а отражают всего-лишь адекватность иммунного ответа, способствуя быстрой элиминации инфицированных гепатоцитов и элиминации вируса, чему в известной степени способствуют также адекватные механизмы иммунокомплексообразования, обеспечивающие быстрое связывание антигенов вируса преимущественно антителами класса IgM, с образованием крупных комплексов, легко элиминирующихся макрофагальной системой, Совокупность всех этих механизмов обеспечивает самолимитируюшийся процесс без риска развития фульминантного или хронического гепатита.
По образному выражению гепатологов, патогенез вирусного гепатита — это патогенез нарушений обмена веществ. Хотя с современных позиций такое определение и нельзя признать полностью правильным, нарушения в обмене веществ играют важную роль в патогенезе заболевания.
При гепатите А нарушаются все виды обмена (белкового, жирового, углеводного, пигментного и др.). Биохимической основой этих процессов служат освобождение внутриклеточных ферментов и переход их из гепатоцитов в кровь Первоначально клетки покидают ферменты цитоплазматической локализации (AЛT, ACT, Ф-1-ФА, сорбитдегидрогенеза и др.), затем митохондриальной (глутаматдегидрогеназа, уроканиназа, малатдегидрогеназа и др.) и лизосомальной локализации (катепсины D, С, лейцинаминoneптидаза и др.). Потеря гепатоцитами ферментов, являющихся основными катализаторами обменных превращений, приводит к нарушениям окислительного фосфорилиоования, а следовательно, к снижению синтеза доноров энергии (АТФ, НАДФ и др.), что и лежит в основе прохрессируюшего нарушения обмена веществ. Снижается синтез альбумина, факторов свертывания крови, витаминов, нарушается обмен микроэлементов, гормонов, углеводов, жиров и др. Следовательно, нарушения обмена веществ при вирусных гепатитах всегда возникают вторично, вслед за массивной потерей печеночно-клеточных ферментов.
Схематично происходящее на уровне гепатоцитов можно представить как взаимообусловленный каскад обменных нарушений, проходящих три стадии: ферментативных нарушений, функциональных сдвигов, некроза и лизиса гепатоцитов с их аутолитическим распадом. Важнейшую роль в аутолитическом распаде пораженных гепатоцитов играют протеолитические ферменты, высвобождающиеся из субклеточных органелл — лизосом. Под их действием происходит распад белковых структур с высвобождением большого количества аминокислот, играющих существенную роль в возникновении симптомов интоксикации.
В механизме развития патологического процесса важную роль играют и нарушения в пигментном обмене. Известно, что печень служит важнейшим органом, осуществляющим превращения билирубина, в результате которых пигмент теряет токсические свойства и выводится из организма. В физиологических условиях билирубин образуется в ретикулоэндотелиальной сети из гемоглобина, высвобождающегося при гемолизе эритроцитов.
При вирусных гепатитах нарушения в пигментном обмене возникают прежде всего на уровне экскреции гепатоцитом связанного билирубина. При этом функции захвата и конъюгации свободного билирубина на первых этапах заболевания практически не страдают. Главной причиной нарушения экскреции билирубина следует считать поражение ферментных систем и снижение энергетического потенциала гепатоцитов. Образующийся в ходе обменных превращений связанный билирубин в конечном итоге поступает не в желчный капилляр, а непосредственно в кровь (парахолия). Другие механизмы, например механическое препятствие вследствие образования желчных тромбов или сдавление желчных ходов, при гепатите А не имеют существенного значения. Исключение составляют лишь холестатические формы болезни, при которых механические факторы могут приобретать значение в патогенезе длительно сохраняющейся желтухи.
Морфология гепатита А изучена на основании данных прижизненных пункционных биопсий печени. Изменения отмечаются во всех тканевых компонентах печени — паренхиме, соединительнотканной строме, ретикулоэндотелии, желчевыводящих путях. Степень поражения органа может варьировать от незначительных дистрофических и единичных некротических изменений эпителиальной ткани дольки печени при легких формах до более выраженных очаговых некрозов печеночной паренхимы при среднетяжелых и тяжелых формах. Распространенных некрозов печеночной паренхимы и, тем более, массивного некроза печени при гепатите А не бывает.
По характеру морфологических изменений можно различать острую и затяжную формы болезни.
При острой циклической форме в печени обнаруживается диффузное поражение гепатоцитов, эндотелиальных и мезенхимальных элементов. Отмечается пестрота микроскопических изменений за счет дискомплексации балочного строения и различного характера поражения гепатоцитов, их значительного полиморфизма: наряду с распространенными дистрофическими изменениями имеются и выраженные пронесен регенерации. Характерно наличие рассеянных по дольке некротизированных гепатоцитов, а также присутствие отдельных печеночных клеток с гомогенизированной ацидофильной цитоплазмой с пикнотичным ядром (эозинофильное тельце). Ожирения печеночных клеток не отмечается. Теряют гликоген лишь некротизированные клетки.
Изменения мезенхимальных элементов внутри дольки выражаются в пролиферации звездчатых ретикулоэндотелиоцитов (купферовских клеток) с превращением их в макрофаги, обнаруживаемые в просвете капилляров. Цитоплазма этих клеток базофильна, содержит желчный пигмент и липофусцин. Мелкие лимфогистиоцитарные скопления отмечаются на месте рассеянных по дольке некротизированных гепатоцитов. Капилляры в центре долек расширены. Строма без видимых изменений. В портальном тракте отмечается пролиферация лимфогистиоцитарных элементов с примесью плазматических клеток, эозинофилов и нейтрофилов.
Морфологические изменения в печени цикличны. К концу 1-й — началу 2-й недели болезни в портальных трактах и вокруг вегвеи печеночных вен на фоне отека соединительнотканных структур уже имеется рыхлый обильный инфильтрат. В разгаре заболевания (2-3-я неделя болезни) растет интенсивность альтеративно-дегенеративных процессов вплоть до появления очаговых некрозов с одновременным нарастанием пролиферативной реакции.
Структура паренхимы печени в этом периоде максимально нарушена за счет дискомплексации и резко выраженных дистрофических изменений печеночных клеток. В более тяжелых случаях преобладают поля «просветленных» (баллонных) клеток и обнаруживаются многочисленные мумифицированные клетки (тельца Каунсильмена). Могут определяться мелкоочаговые или даже фокальные некрозы, рассеянные по всей дольке,
При гепатите А, в отличие от гепатита В, воспалительно-дистрофические и пролиферативные изменения локализуются по периферии долек, распространяясь к центру, внутрь паренхимы, в виде тонкой сеточки и дорожек. В периферических зонах долек возможно появление многоядерных клеток со склонностью к образованию симпластоподобных структур: характерно нарастание количества плазматических клеток
В желчных капиллярах могут появляться желчные тромбы, возможны следы некоторого огрубения и коллагенизации ретикулярного каркаса, но еще по периферии долек могут сохраняться мелкие некрозы с регенератами из многоядерных клеток и разрастанием ложных желчных ходов, что следует расценивать как проявления регенерации печеночной паренхимы.
На протяжении 4-й недели некротически-дистрофические изменения паренхимы исчезают, мезенхимальная инфильтрация существенно уменьшается. Полностью исчезают «просветления» цитоплазмы (баллонная дистрофия).
В бывших очажках некроза видны зоны разрежения — «изъяны» паренхимы. Преобладают явления регенерации и восстановления.
Поданным большинства морфологов, к концу 5-6-й недели болезни исчезают все воспалительные явления, а к концу 2-3-го месяца патологический процесс в печени при гепатите А в подавляющем большинстве случаев полностью завершается. Наступает восстановление структуры и функции печени.
Степень деструктивных изменений в паренхиме печени соответствует тяжести клинических проявлений болезни.
Из внепеченочных изменений при гепатите А отмечают увеличение портальных лимфатических узлов и селезенки с ретикулярной гиперплазией стромы и миелозом пульпы селезенки. Возможны также реактивные изменения со стороны ретикулоэндотелиальной системы поджелудочной железы, почек и других органов. Описаны изменения и со стороны ЦНС.
У пациентов с легкими формами гепатита А, погибших от случайных причин, в ЦНС обнаружены циркуляторные расстройства, изменения эндотелиальных клеток, серозный и серозно-продуктивный менингит, дегенеративные изменения нервных клеток.
По данным патологов, поражение ЦНС возникает при всех вирусных гепатитах. При этом первичное воздействие вируса на ЦНС выражается поражением прежде всего эндотелия сосудов (венул). В нервных клетках появляются патологические изменения различной выраженности, вплоть до некробиоза отдельных клеток.
Высказывается мнение, что изменения со стороны ЦНС при вирусных гепатитах аналогичны гепатоцеребральному синдрому при гепатолентикулярной дегенерации.
Возбудитель гепатита А передается исключительно фекально-оральным путем, через инфицированные продукты питания, воду и посредством бытового контакта. Вирус выделяется только с фекалиями, при этом он попадает в пищу обычно при нарушении элементарных правил гигиены в момент ее обработки и приготовления; инфицирование воды происходит путем загрязнения водоисточников бытовыми сбросами.
источник