Первичная и вторичная профилактика острой ревматической лихорадки.
Основные цели первичной профилактики заключаются в следующем.
1. Мероприятия, направленные на повышение уровня естественного иммунитета и адаптационных возможностей организма по отношению к неблагоприятным условиям внешней среды. К ним относятся:
полноценное витаминизированное питание;
максимальное пребывание на свежем воздухе;
рациональная физкультура и спорт;
борьба со скученностью в жилищах, детских дошкольных учреждениях, школах, училищах, вузах, общественных учреждениях;
проведение комплекса санитарно-гигиенических мер, снижающих возможность стрептококкового инфицирования коллективов, особенно детских.
2. Своевременное и эффективное лечение острой и хронической рецидивирующей БГСА-инфекции глотки: тонзиллита (ангины) и фарингита.
Вопросы диагностики и дифференциального диагноза острого и хронического рецидивирующего БГСА-тонзиллита/фарингита широко освещены в отечественной медицинской литературе. Точный диагноз и обязательная рациональная антибиотикотерапия БГСА-тонзиллита/фарингита по-прежнему играют важнейшую роль в профилактике ОРЛ.
Несмотря на то, что БГСА по-прежнему сохраняет практически полную чувствительность к β-лактамным антибиотикам, в последние годы отмечаются определенные проблемы в терапии тонзиллитов, вызванных этим микроорганизмом. По данным разных авторов, частота неудач пенициллинотерапии БГСА-тонзиллитов составляет 24–30% и даже достигает 38%. Одной из возможных причин этого явления может быть низкая комплаентность (исполнительность) больных. Известно, что более чем у половины пациентов на 4-й день болезни исчезает лихорадка и боль в горле, а к концу 6-х суток клиническая симптоматика БГСА-тонзиллита купируется практически полностью. В связи с этим многие больные самостоятельно прекращают прием антибиотика. По имеющимся данным, при назначении стандартной 10-дневной схемы пенициллинотерапии на 9-е сутки продолжали прием препарата всего лишь 8% больных [5]. Более того, анализ причин упомянутой вспышки ОРЛ в США позволил выявить, что в 10–15% случаев имело место несоблюдение сроков лечения пенициллином предшествовавшей заболеванию БГСА-инфекции глотки.
В качестве другой не менее важной причины может выступать гидролиз пенициллина специфическими ферментами-β-лактамазами, которые продуцируются микроорганизмами — ко-патогенами (S. aureus, H. influenzae, M. catarrhalis и др.), присутствующими в глубоких тканях миндалин при хроническом тонзиллите. Известно, что у здоровых лиц миндалины в норме колонизированы ротоглоточной микрофлорой, представляющей около 100 различных видов микробов-комменсалов. При наличии хронического воспалительного процесса в миндалинах и под влиянием антибиотиков (особенно — пенициллина) состав оральной флоры претерпевает изменения, выражающиеся в нарастании числа штаммов бактерий, способных продуцировать бета-лактамазы (феномен селективного прессинга). Показано, что к концу XX в. частота выявляемости ко-патогенов, продуцирующих β-лактамазы, у детей с хроническим рецидивирующим тонзиллитом повысилась до 94% [6].
Препараты пенициллинового ряда остаются средствами выбора при лечении острых форм БГСА-тонзиллита (табл. 1). Оптимальным препаратом из группы оральных пенициллинов представляется амоксициллин, который по противострептококковой активности аналогичен ампициллину и феноксиметилпенициллину, но существенно превосходит их по своим фармакокинетическим характеристикам, отличаясь большей биодоступностью (95, 40 и 50% соответственно) и меньшей степенью связывания с сывороточными белками (17, 22 и 60%, соответственно).
К несомненным достоинствам следует отнести наличие амоксициллина в диспергируемой лекарственной форме — Солютаб (Флемоксин Солютаб), обладающей благоприятными фармакокинетическими свойствами (высокая биодоступность, равномерное нарастание концентраций, действующего вещества в крови), минимальным воздействием на микрофлору кишечника и, следовательно, более редкими диспептическими расстройствами. Не менее важным представляется удобство в применении данной лекарственной формы (проглатывание целиком, разжевывание или предварительное растворение в воде), что повышает исполнительность пациентов в соблюдении схемы лечения.
Применение феноксиметилпенициллина представляется оправданным только у младшего контингента больных с учетом наличия лекарственной формы в виде суспензии, а также несколько большей комплаентности, контролируемой со стороны родителей, чего нельзя сказать о подростках.
Назначение однократной инъекции бензатин-пенициллина целесообразно при наличии следующих факторов:
низкая комплаентность больных;
ОРЛ и/или ХРБС в анамнезе у ближайших родственников;
неблагоприятные социально-бытовые условия (фактор скученности);
вспышки БГСА-инфекции в организованных коллективах;
невозможность перорального приема.
Наряду с пенициллинами заслуживает несомненного внимания представитель оральных цефалоспоринов первого поколения цефадроксил, высокая эффективность которого в терапии А-стрептококковых тонзиллитов, а также хорошая переносимость подтверждены в многочисленных клинических исследованиях.
При непереносимости β-лактамных антибиотиков целесообразно назначение макролидов (спирамицин, азитромицин, рокситромицин, кларитромицин, джозамицин, мидекамицин), противострептококковая активность которых сопоставима с таковой для пенициллина. Эти препараты также обладают способностью создавать высокую тканевую концентрацию в очаге инфекции и хорошей переносимостью. Заслуживает внимания препарат из группы 16-членных макролидов джозамицин (Вильпрафен, Вильпрафен Солютаб), который активен в отношении некоторых эритромицин-резистентных штаммов стрептококков и стафилококков и обладает вышеуказанными преимуществами диспергируемой лекарственной формы. Применение эритромицина — первого представителя антибиотиков данного класса — в настоящее время существенно снизилось, особенно в терапевтической практике, поскольку он наиболее часто, по сравнению с другими макролидами, вызывает нежелательные эффекты со стороны желудочно-кишечного тракта, обусловленные его стимулирующим действием на моторику желудка и кишечника.
Как уже указывалось, при наличии хронического рецидивирующего БГСА-тонзиллита вероятность колонизации очага инфекции микроорганизмами, продуцирующими β-лактамазы, достаточно высока. В этих случаях целесообразно проведение курса лечения ингибитор-защищенными пенициллинами (амоксициллин/клавуланат) или оральными цефалоспоринами II поколения (цефуроксим аксетил), а при непереносимости b-лактамных антибиотиков — линкозамидами (табл. 2). Указанные антибиотики также рассматриваются как препараты второго ряда для случаев безуспешной пенициллинотерапии острого БГСА-тонзиллита (что чаще встречается при использовании феноксиметилпенициллина). Следует заметить, что в ходе сравнительного фармакокинетического исследования выявлено важное преимущество диспергируемой лекарственной формы амоксициллин/клавуланата (Флемоклав Солютаб) над стандартным таблетированным препаратом, заключающееся в значительном снижении (почти в 2 раза) вариабельности концентраций клавулановой кислоты в сыворотке крови [7], что должно способствовать улучшению переносимости лечения. Показано, что при назначении Флемоклава Солютаб существенно снижается частота диареи, которая при применении обычных форм амоксициллина/клавуланата достигает 24% [8].
Необходимо подчеркнуть, что применение тетрациклинов, сульфаниламидов, ко-тримоксазола (Бисептола) и хлорамфеникола при БГСА-инфекции глотки в настоящее время не оправдано по причине высокой частоты резистентности и, следовательно, низких показателях эффективности терапии. Назначение ранних фторхинолонов (ципрофлоксацин, пефлоксацин, офлоксацин, ломефлоксацин) также не является обоснованным по причине низкой природной противострептококковой активности этих препаратов.
Вторичная профилактика направлена на предупреждение повторных атак и прогрессирования заболевания у лиц, перенесших ОРЛ, и предусматривает регулярное круглогодичное введение пенициллина пролонгированного действия (бензатина бензилпенициллин). Препарат вводят глубоко внутримышечно детям с массой тела до 27 кг в дозе 600 000 ЕД 1 раз в 3 нед, детям с массой тела > 27 кг —1200 000 ЕД 1 раз в 3 нед, подросткам и взрослым — 2 400 000 ЕД 1 раз в 3 нед.
Длительность вторичной профилактики (которую следует начинать еще в стационаре) для каждого пациента устанавливается индивидуально и, в соответствии с рекомендациями ВОЗ, определяется наличием факторов риска повторных атак ОРЛ. К этим факторам относятся:
время от момента первой атаки ОРЛ;
фактор скученности в семье;
семейный анамнез, отягощенный по ОРЛ/ХРБС;
социально-экономический и образовательный статус больного;
риск стрептококковой инфекции в регионе;
профессия и место работы больного (школьные учителя, врачи, лица, работающие в условиях скученности).
Как правило, длительность вторичной профилактики должна составлять:
а) для лиц, перенесших ОРЛ без кардита (артрит, хорея) — не менее 5 лет после последней атаки или до 18-летнего возраста (по принципу «что дольше»);
б) в случаях излеченного кардита без формирования порока сердца — не менее 10 лет после последней атаки или до 25-летнего возраста (по принципу «что дольше»);
в) для больных с пороком сердца (в том числе после оперативного лечения) — пожизненно.
Наиболее эффективной лекарственной формой бензатина бензилпенициллина является экстенциллин. Исследования, проведенные в Институте ревматологии РАМН и Государственном научном центре по антибиотикам, показали, что экстенциллин обладает явными фармакокинетическими преимуществами в сравнении с Бициллином-5 по основному параметру — длительности поддержания адекватной противострептококковой концентрации бензилпенициллина в сыворотке крови пациентов. Из отечественных препаратов рекомендуется Бициллин-1, который назначается в вышеуказанных дозах 1 раз в 7 дней.
В настоящее время препарат Бициллин-5 (смесь 1,2 млн ЕД бензатина бензилпенициллина и 300 тыс. ЕД новокаиновой соли бензилпенициллина) рассматривается как не соответствующий фармакокинетическим требованиям, предъявляемым к превентивным препаратам, и не является приемлемым для проведения полноценной вторичной профилактики ОРЛ.
Широко практиковавшееся ранее ежедневное применение эритромицина у больных с ОРЛ в анамнезе и непереносимостью β-лактамных антибиотиков на сегодняшний день нуждается в пересмотре из-за повсеместного нарастания резистентности БГСА к макролидам. В качестве альтернативы у данной категории пациентов может рассматриваться своевременное курсовое лечение макролидами каждого случая БГСА-тонзиллита/фарингита.
источник
Профилактика ревматической лихорадки
Как родители могут защитить своего ребенка от заболевания ревматической лихорадкой?
Специалисты делят профилактику ревматической лихорадки на первичную и вторичную.
Первичная профилактика направлена на предупреждение развития ревматизма и включает в себя мероприятия, направленные на укрепление иммунитета.
В первую очередь иммунитет ребенка обеспечивает полноценное питание с правильным соотношением в рационе белков, жиров и углеводов. Каких бы новомодных диет ни придерживались взрослые члены семьи, на детей это распространяться не должно! Ребенку обязательно надо ежедневно давать мясо или рыбу, овощные салаты с растительным маслом, ежедневно в питании должно присутствовать сливочное масло, овощи, фрукты, крупяные изделия. Обязательно надо давать ребенку различные кисломолочные продукты, куриные яйца.
Необходимо соблюдение правильного режима дня, чередование нагрузки и отдыха. С маленькими детьми нужно обязательно ежедневно гулять, а более старших, хоть насильно, но отрывать от телевизоров и компьютеров и отправлять дышать свежим воздухом. Полезны различные водные процедуры – регулярный прохладный душ, в летнее время купание в реке, озере, море, в зимнее время занятия в плавательном бассейне. Полезны занятия физкультурой и спортом.
У детей необходимо своевременно выявлять и лечить очаги хронической инфекции – хронический тонзиллит, отит, синусит, кариозные зубы. Важным является правильное лечение ангин. Что под этим подразумевается? Катаральная ангина обычно хорошо поддается лечению препаратами пенициллина. Их применяют 3–5 дней и часто на этом заканчивают лечение. Такие меры снимают острую лихорадку, подавляя стрептококк, но оставляют его в жизнеспособном, т. е. потенциально опасном, состоянии.
Для достижения стойкого бактерицидного эффекта требуется антибактериальная терапия на протяжении 9-10 дней, особенно это важно для детей из семей, в которых имеются больные ревматизмом. Детям, переболевшим ангиной, перед выпиской в школу желательно сделать общий анализ крови, чтобы убедиться в полном долечивании заболевания.
Вторичная профилактика направлена на предупреждение повторного развития заболевания ревматизмом. Для подавления стрептококковой инфекции используются препараты пенициллина пролонгированного действия, преимущественно бициллин-5, первые введения которого осуществляются еще в стационаре, а затем рекомендуется введение бициллина-5 1 раз в 2–4 недели круглогодично в течение 5 лет.
В качестве иллюстрации развития острой ревматической лихорадки может служить такая выписка из истории болезни ребенка.
«Мальчик Б., 12 лет, поступил в больницу с жалобами на резкие боли в животе, с подозрением на аппендицит. После осмотра хирургом диагноз аппендицита был снят, и с предположительным диагнозом «ревматизм» больной был положен в соматическое отделение. Из анамнеза известно, что мальчик рос и развивался нормально, болел редко. Мать ребенка в детстве перенесла ревматизм. За 10 дней до настоящего заболевания ребенок перенес нетяжелую катаральную ангину, в течение 3 дней принимал парацетамол, состояние быстро улучшилось, и на 7-й день мальчик был выписан в школу. Накануне заболевания, возвращаясь домой из плавательного бассейна, мальчик очень замерз. Вечером он плохо себя почувствовал, появилась слабость, головная боль. Мальчик выпил чай с медом и лег спать. На следующее утро самочувствие ребенка было плохим – температура тела поднялась до 37,5 о С, появилось общее недомогание, слабость, боли в коленных суставах и сильные боли в животе разлитого характера. Днем температура повысилась до 38,5 о С, боли в животе продолжали беспокоить, и мальчик был госпитализирован. При осмотре врач обнаружил, что коленные суставы опухли, горячие на ощупь, движения в них ограничены и болезненны. Живот мягкий, при ощупывании болезненный. Кожа бледная, температура тела 38,8 о С, пульс 120 в минуту, число дыханий 27 в минуту. Тоны сердца приглушены, на верхушке сердца выслушивается нежный систолический шум. В анализе крови увеличено количество лейкоцитов до 12 000, СОЭ 45 мм/час. Был поставлен диагноз – острая ревматическая лихорадка, миокардит, полиартрит, абдоминальный синдром».
Таким образом, в данном случае непосредственной причиной развития ревматизма явилась стрептококковая инфекция. Она активизировалась в результате плохого лечения ангины у ребенка, наследственно предрасположенного к развитию заболевания. Способствовал возникновению болезни и фактор охлаждения ребенка.
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Острая ревматическая лихорадка (ОРЛ) – постинфекционное осложнение тонзиллита (ангины) или фарингита, вызванных b–гемолитическим стрептококком группы А (БГСА), в виде системного воспалительного заболевания соединительной ткани с преимущественной локализацией в сердечно–сосудистой системе (кардит), суставах (мигрирующий полиартрит), мозге (хорея) и коже (кольцевидная эритема, ревматические узелки), развивающегося у предрасположенных лиц, главным образом молодого возраста (7–15 лет), в связи с аутоиммунным ответом организма на антигены стрептококка и их перекрестной реактивностью со схожими аутоантигенами перечисленных поражаемых тканей человека (феномен молекулярной мимикрии).
Хроническая ревматическая болезнь сердца (ХРБС) – заболевание, характеризующееся стойким поражением сердечных клапанов в виде поствоспалительного краевого фиброза клапанных створок или сформированного порока сердца (недостаточность и/или стеноз) после перенесенной ОРЛ.
Во второй половине XX столетия заболеваемость ОРЛ и ХРБС и обусловленная ими смертность снизились, а продолжительность жизни больных увеличилась. Снижение заболеваемости было тесно связано с проведением социально–экономических преобразований, повышением уровня жизни, улучшением качества медико–профилактических мероприятий. Тем не менее в последние годы стало очевидным, что упомянутые мероприятия хотя и способствуют сокращению заболеваемости ОРЛ и ХРБС, но полностью проблему борьбы с этими болезнями не решают.
В современной России в силу известных негативных общественно–социальных изменений существует опасность появления истинных вспышек ОРЛ. В частности, в 1994 году по сравнению с предыдущим 1993 годом отмечен подъем первичной заболеваемости (выявляемости) ОРЛ с 0,06 до 0,16‰ среди детей и с 0,08 до 0,17‰ у подростков. Этот рост произошел преимущественно в Северокавказском регионе, особенно в республиках Ингушетия и Дагестан. Однако и в целом по стране должна быть постоянной настороженность врачей в отношении возможных вспышек ОРЛ в связи с неснижающимися показателями первичной заболеваемости (выявляемости) ХРБС. Подавляющее большинство в данной категории составляют пациенты с приобретенными ревматическими пороками сердца (РПС). К концу последнего десятилетия прошлого века в России ежегодно диагностировалось на 2,5 тыс. больных с ХРБС больше, чем в начале регистрации (1994 г.). При этом распространенность ХРБС наиболее значимо (с 1,4 до 2,3 на 1000) увеличилась за счет населения Северного Кавказа, т.е. там, где в 1994 г. была зарегистрирована вспышка ОРЛ. Следовательно, проблемы ОРЛ и ХРБС по–прежнему должны быть в центре внимания ученых–медиков, организаторов здравоохранения и практических врачей.
По данным статистического отчета Минздравсоцразвития РФ за 2006 г., распространенность ХРБС остается высокой и составляет 2,21 на 1000 населения. При этом около 220 тыс. больных нуждаются в регулярной круглогодичной вторичной профилактике ОРЛ.
Программа предупреждения ОРЛ и повторных атак заболевания включает первичную и вторичную профилактику.
Основные цели первичной профилактики заключаются в следующем.
1. Мероприятия, направленные на повышение уровня естественного иммунитета и адаптационных возможностей организма по отношению к неблагоприятным условиям внешней среды. К ним относятся:
– раннее закаливание;
– полноценное витаминизированное питание;
– максимальное использование свежего воздуха;
– рациональная физкультура и спорт;
– борьба со скученностью в жилищах, детских дошкольных учреждениях, школах, училищах, вузах, общественных учреждениях;
– проведение комплекса санитарно–гигиенических мер, снижающих возможность стрептококкового инфицирования коллективов, особенно детских.
2. Своевременное и эффективное лечение острой и хронической рецидивирующей БГСА–инфекции глотки: тонзиллита (ангины) и фарингита.
БГСА передается воздушно–капельным путем. Вероятность заражения увеличивается при высокой обсемененности и тесном контакте. Источниками инфекции являются больные и (реже) бессимптомные носители. Характерна быстрота распространения инфекции, особенно в организованных коллективах. Поражаются преимущественно дети в возрасте 5–15 лет и лица молодого возраста. Точные данные официальной статистики по БГСА–инфекциям отсутствуют. Однако, как свидетельствуют результаты американских исследователей, практически каждый ребенок, достигший 5–летнего возраста, имеет в анамнезе перенесенную БГСА–инфекцию глотки, а в возрасте 13 лет количество эпизодов заболевания достигает трех [1]. Наибольшая заболеваемость БГСА–тонзиллитом/фарингитом наблюдается ранней весной. Фарингиты, вызванные вирусом гриппа, коронавирусами, респираторно–синцитиальными вирусами, возникают преимущественно в осенне–зимний период.
Клиническая картина БГСА–тонзиллита хорошо известна и представлена в ряде публикаций, доступных для российских врачей [2–4]. В рамках данной статьи хотелось бы еще раз подчеркнуть, что диагноз БГСА–тонзиллита должен быть подтвержден микробиологическим исследованием мазка с поверхности миндалин и/или задней стенки глотки. Однако культуральный метод не позволяет дифференцировать активную инфекцию от БГСА–носительства, а современным экспресс–тестам, несмотря на их высокую специфичность, свойственна сравнительно низкая чувствительность, т.е. отрицательный результат быстрой диагностики не исключает стрептококковую этиологию заболевания.
В настоящее время канадскими авторами [5] разработан и апробирован на большой группе пациентов клинический алгоритм, позволяющий при первом осмотре больного предположить наличие БГСА–инфекции глотки и, соответственно, решить вопрос о назначении эмпирической антимикробной терапии при невозможности выполнения микробиологического исследования (табл. 1).
Необходимо иметь в виду, что в 1/3 случаев ОРЛ является следствием БГСА–тонзиллита, протекающего со стертой клинической симптоматикой (удовлетворительное общее состояние, температура тела нормальная или субфебрильная, небольшое чувство першения в глотке, исчезающее через 1–2 дня), когда большинство больных не обращается за медицинской помощью, а проводит лечение самостоятельно без применения соответствующих антибиотиков.
Учитывая возможность спонтанного купирования клинической симптоматики БГСА–тонзиллита и выздоровления без каких–либо осложнений, некоторые врачи при курации таких больных совершенно необоснованно отдают предпочтение местному лечению (полоскание, ингаляции и т.д.) в ущерб системной антибиотикотерапии. Подобный подход представляется совершенно неправильным и даже вредным для больного из–за угрозы развития весьма серьезных последствий.
В связи с вышеизложенным следует подчеркнуть, что точный диагноз и обязательная рациональная антибиотикотерапия БГСА–тонзиллита по–прежнему играют важнейшую роль как в контроле за распространением данной инфекции, так и в профилактике ОРЛ.
В 1931 г. A. Coburn и A. Moor впервые применили сульфаниламидные препараты с профилактической целью у больных ХРБС. Далее последовал целый ряд сообщений о положительном профилактическом их действии в небольших дозах (в частности, по 1 г сульфадимезина в сутки). Однако, несмотря на некоторые позитивные результаты, использование этих препаратов оказалось малоэффективным в связи с нарастанием резистентных БГСА–штаммов.
В середине 40–х гг. прошлого века мировая клиническая медицина получила в свое распоряжение первый антибиотик – пенициллин G. В 1948 г. опубликована работа датских авторов, свидетельствовавшая об успешном применении этого препарата при БГСА–инфекции. Однако истинная значимость пенициллина была установлена несколькими годами позже в исследованиях, выполненных с привлечением солдат–новобранцев одной из баз ВВС США в штате Вайоминг. Применение депо–формы пенициллина G позволило добиться эрадикации БГСА из глотки у 93% пациентов. При этом частота развития ОРЛ среди лиц, пролеченных пенициллином, снизилась на 90% (!!) по сравнению с группой, не получавшей лечения [6,7].
В конце 1950–х годов в клиническую практику была внедрена кислотоустойчивая лекарственная форма препарата (пенициллин V, феноксиметилпенициллин), что позволило проводить успешную терапию БГСА–инфекций глотки при пероральном приеме антибиотика. В дальнейшем эффективность и безопасность пенициллинов была подтверждена в многочисленных клинических исследованиях с вовлечением большого количества пациентов (детей и взрослых).
Несмотря на то что БГСА по–прежнему сохраняет практически полную чувствительность к b–лактамным антибиотикам, в последние годы отмечаются определенные проблемы в терапии тонзиллитов, вызванных этим микроорганизмом. По данным разных авторов, частота неудач пенициллинотерапии БГСА–тонзиллитов составляет 24–30% и даже достигает 38%. В качестве возможных причин этого явления называются следующие.
1. Низкая комплаентность (исполнительность) больных. Известно, что более чем у половины пациентов на 4–й день болезни исчезает лихорадка и боль в горле, а концу 6–х суток клиническая симптоматика БГСА–тонзиллита купируется практически полностью. В связи с этим многие больные самостоятельно прекращают прием антибиотика. По имеющимся данным, при назначении стандартной 10–дневной схемы пенициллинотерапии на 9–е сутки продолжали прием препарата всего лишь 8% больных [8]. Более того, анализ причин вспышки ОРЛ в США в середине 1980–х гг. позволил выявить, что в 10–15% случаев имело место несоблюдение сроков лечения пенициллином предшествовавшей заболеванию БГСА–инфекции глотки.
2. Гидролиз пенициллина специфическими ферментами – b–лактамазами, которые продуцируются микроорганизмами – ко–патогенами (S. aureus, H. influenzae, M. catarrhalis и др.), присутствующими в глубоких тканях миндалин при хроническом тонзиллите. Известно, что у здоровых лиц миндалины в норме колонизированы ротоглоточной микрофлорой, представляющей около 100 различных видов микробов–комменсалов. При наличии хронического воспалительного процесса в миндалинах и под влиянием антибиотиков (особенно пенициллина) состав оральной флоры претерпевает изменения, выражающиеся в нарастании числа штаммов бактерий, способных продуцировать b–лактамазы (феномен селективного прессинга). Показано, что к концу XX века частота выявляемости ко–патогенов, продуцирующих b–лактамазы, у детей с хроническим рецидивирующим тонзиллитом повысилась до 94%.
3. Реинфицирование БГСА. Риск реинфекции особенно велик в закрытых и полузакрытых коллективах (детские сады, школы, училища, дневные стационары и т.д.) Сообщают, что реинфекция может развиваться при контакте как с инфицированным лицом, так и с контаминированными предметами. Среди 104 детей, получивших 10–дневный курс пенициллина по поводу БГСА–тонзиллита, А–стрептококки были выделены повторно на съемных ортодонтических приспособлениях (19% случаев) и на зубных щетках (11% случаев). Авторы делают вывод о том, что упомянутые предметы, вероятно, могут быть источником реинфекции у некоторых больных [8].
4. Нарушение колонизационной резистентности. a–стрептококки, являющиеся представителями сапрофитной микрофлоры глотки, защищают последнюю от колонизации БГСА. Показано, что после курса антибиотикотерапии у больных, ротоглотку которых колонизировали a–стрептококками (в виде орального спрея), отмечалась более низкая частота рецидивов БГСА–тонзиллита, чем в контрольной группе (2 и 23% соответственно) [9]. Следовательно, бактерицидное действие пенициллина на a–гемолитические стрептококки может нарушить этот протективный механизм.
5. Носительство БГСА. Увеличивающееся число неудач пенициллинотерапии может быть отражением нарастания в популяции носителей БГСА – лиц, у которых ротоглотка колонизирована А–стрептококками, но клинические симптомы инфекции отсутствуют. Распространенность БГСА–носительства среди школьников в регионах с умеренным климатом может достигать 20%, в то время как в жарких странах она превышает 40%. В одном исследовании частота БГСА–носительства среди здоровых детей составляла 2,5%, среди детей с инфекциями верхних дыхательных путей предположительно вирусной этиологии – 4,4%, среди детей с инфекцией верхних дыхательных путей с верифицированной вирусной этиологией – 6,9% [10].
6. Феномен интернализации. В ряде исследований показано, что БГСА, являющиеся по сути внеклеточными патогенами, могут проникать внутрь эпителиальных клеток слизистой оболочки дыхательных путей и таким образом быть защищенными от действия b–лактамных антибиотиков [11,12].
Как видно из таблицы 2, препараты пенициллинового ряда остаются средствами выбора при лечении острых форм БГСА–тонзиллита. Оптимальным препаратом из группы оральных пенициллинов представляется амоксициллин, который по противострептококковой активности аналогичен ампициллину и феноксиметилпенициллину, но существенно превосходит их по своим фармакокинетическим характеристикам, отличаясь большей биодоступностью (95, 40 и 50% соответственно) и меньшей степенью связывания с сывороточными белками (17, 22 и 80% соответственно).
Назначение ампициллина в пероральной форме для лечения БГСА–тонзиллита, а также инфекций дыхательных путей иной локализации в настоящее время большинством авторов признано нецелесообразным по причине неудовлетворительных фармакокинетических характеристик препарата (в первую очередь низкой биодоступности).
Применение феноксиметилпенициллина представляется оправданным только у младшего контингента больных, учитывая наличие лекарственной формы в виде суспензии, а также несколько большую комплаентность, контролируемую со стороны родителей, чего нельзя сказать о подростках.
Назначение однократной инъекции бензатин–пенициллина целесообразно в следующих ситуациях:
– низкая исполнительность больных;
– ОРЛ и/или хроническая ревматическая болезнь сердца в анамнезе у ближайших родственников;
– неблагоприятные социально–бытовые условия (фактор скученности);
– вспышки БГСА–инфекции в организованных коллективах;
– невозможность перорального приема.
Наряду с пенициллинами заслуживает несомненного внимания представитель оральных цефалоспоринов I поколения цефадроксил, высокая эффективность которого в терапии А–стрептококковых тонзиллитов, а также хорошая переносимость подтверждены в многочисленных клинических исследованиях.
При непереносимости b–лактамных антибиотиков целесообразно назначение макролидов (спирамицин, азитромицин, джозамицин, рокситромицин, кларитромицин, мидекамицин), противострептококковая активность которых сопоставима с таковой для пенициллина. Эти препараты также обладают способностью создавать высокую тканевую концентрацию в очаге инфекции и хорошей переносимостью. Применение эритромицина – первого представителя антибиотиков данного класса – в настоящее время существенно снизилось, особенно в терапевтической практике, поскольку он наиболее часто, по сравнению с другими макролидами, вызывает нежелательные эффекты со стороны желудочно–кишечного тракта, обусловленные его стимулирующим действием на моторику желудка и кишечника.
Следует отметить, что в конце XX века из Японии и ряда стран Европы стали поступать сообщения о нарастании резистентности БГСА к эритромицину и другим макролидам. В современной действительности приобретенная устойчивость БГСА к эритромицину распространена достаточно широко, и в отдельных европейских регионах она превышает 40%. Основные механизмы устойчивости (метилирование и активное выведение) представлены примерно в равной степени. На примере Финляндии было показано, что эта резистентность является управляемым процессом [13]. После того как устойчивость БГСА к макролидам в этой стране достигла 19%, органы здравоохранения предприняли ряд административных мер и провели широкую разъяснительную кампанию среди населения. Это привело к двукратному снижению потребления макролидов и, как следствие, двукратному снижению частоты БГСА–штаммов, устойчивых к упомянутым антибиотикам. В России резистентность БГСА к макролидам колеблется от 4,8 (Центральный регион) до 14% (Урал) [14].
В литературе имеются сообщения о высокой эффективности 5–дневных курсов кларитромицина, цефуроксима, цефиксима и других антибиотиков при лечении БГСА–тонзиллита у детей и взрослых. Однако результаты этих исследований еще не получили официального признания со стороны контролирующих организаций и, по мнению экспертов, должны быть подтверждены в ходе дальнейших крупномасштабных исследований с тщательной микробиологической верификацией и серологическим типированием выделенных БГСА–штаммов.
Антибиотики–линкозамиды (линкомицин, клиндамицин) также обладают высокой противострептококковой активностью, но их назначают больным БГСА–тонзиллитом только при непереносимости как b–лактамов, так и макролидов. Широкое применение этих препаратов при данной нозологической форме не рекомендуется. Известно, что при частом применении оральных пенициллинов чувствительность к ним со стороны зеленящих стрептококков, локализующихся в ротовой полости, существенно снижается. Поэтому у данной категории пациентов, среди которых достаточное количество больных с ревматическими пороками сердца, линкозамиды рассматриваются как препараты первого ряда для профилактики инфекционного эндокардита при выполнении различных стоматологических манипуляций.
Как уже указывалось, при наличии хронического рецидивирующего БГСА–тонзиллита вероятность колонизации очага инфекции микроорганизмами, продуцирующими b–лактамазы, достаточно высока. В этих случаях целесообразно проведение курса лечения ингибитор–защищенными пенициллинами (амоксициллин/ клавуланат) или оральными цефалоспоринами II поколения (цефуроксим–аксетил), а при непереносимости b–лактамных антибиотиков – линкозамидами (табл. 3). Указанные антибиотики также рассматриваются как препараты второго ряда для случаев безуспешной пенициллинотерапии острого БГСА–тонзиллита (что чаще встречается при использовании феноксиметилпенициллина). Универсальной же схемы, обеспечивающей 100%–ную элиминацию БГСА из носоглотки, в мировой клинической практике не имеется.
Необходимо отметить, что применение тетрациклинов, сульфаниламидов, ко–тримоксазола и хлорамфеникола при БГСА–инфекции глотки в настоящее время не оправдано по причине высокой частоты резистентности и, следовательно, низких показателях эффективности терапии. Назначение ранних фторхинолонов (ципрофлоксацин, пефлоксацин, офлоксацин, ломефлоксацин) также не обосновано по причине низкой природной противострептококковой активности этих препаратов.
Вторичная профилактика направлена на предупреждение повторных атак и прогрессирования заболевания у лиц, перенесших ОРЛ, и предусматривает регулярное круглогодичное введение пенициллина пролонгированного действия (бензатин бензилпенициллина). Препарат вводят глубоко внутримышечно детям с массой тела до 27 кг в дозе 600000 ЕД 1 раз в 3 недели, детям с массой тела > 27 кг – 1200000 ЕД 1 раз в 3 недели, подросткам и взрослым – 2400000 ЕД 1 раз в 3 недели.
Длительность вторичной профилактики (которую следует начинать еще в стационаре) для каждого пациента устанавливается индивидуально и, в соответствии с рекомендациями ВОЗ, определяется наличием факторов риска повторных атак ОРЛ. К этим факторам относятся:
• Возраст больного
• Наличие ХРБС
• Время от момента первой атаки ОРЛ
• Число предыдущих атак
• Фактор скученности в семье
• Семейный анамнез, отягощенный по ОРЛ/ХРБС
• Социально–экономический и образовательный статус больного
• Риск стрептококковой инфекции в регионе
• Профессия и место работы больного (школьные учителя, врачи, лица, работающие в условиях скученности).
Как правило, длительность вторичной профилактики должна составлять:
а) для лиц, перенесших ОРЛ без кардита (артрит, хорея), не менее 5 лет после последней атаки или до 18–летнего возраста (по принципу «что дольше»);
б) в случаях излеченного кардита без формирования порока сердца – не менее 10 лет после последней атаки или до 25–летнего возраста (по принципу «что дольше»);
в) для больных с пороком сердца (в т.ч. после оперативного лечения) – пожизненно.
Наиболее эффективной лекарственной формой бензатин бензилпенициллина является экстенциллин. Исследования, проведенные в Институте ревматологии РАМН и Государственном научном центре по антибиотикам, показали, что экстенциллин обладает явными фармакокинетическими преимуществами в сравнении с бициллином–5 по основному параметру – длительности поддержания адекватной противострептококковой концентрации бензилпенициллина в сыворотке крови пациентов. Из отечественных препаратов рекомендуется бициллин–1, который назначается в вышеуказанных дозах 1 раз в 7 дней.
В настоящее время препарат бициллин–5 (смесь 1,2 млн. ЕД бензатин бензилпенициллина и 300 тыс. ЕД новокаиновой соли бензилпенициллина) рассматривается как не соответствующий фармакокинетическим требованиям, предъявляемым к превентивным препаратам, и не является приемлемым для проведения полноценной вторичной профилактики ОРЛ.
Широко практиковавшееся ранее ежедневное применение эритромицина у больных с ОРЛ в анамнезе и непереносимостью b–лактамных антибиотиков на сегодняшний день нуждается в пересмотре из–за повсеместного нарастания резистентности БГСА к макролидам. В качестве альтернативы у данной категории пациентов может рассматриваться своевременное курсовое лечение макролидами каждого случая БГСА–тонзиллита/фарингита.
Следует особо подчеркнуть, что схема приема антибиотиков, назначаемых с целью профилактики рецидивов ОРЛ, не соответствует таковой для предупреждения ИЭ. Кроме того, у этих больных, особенно при длительном пероральном приеме пенициллиновых препаратов, существует высокая вероятность носительства зеленящих стрептококков, являющихся относительно устойчивыми к антибиотикам этой группы. В подобных ситуациях для профилактики ИЭ рекомендуется назначать клиндамицин.
Несмотря на то что появившиеся в последние годы новые антибактериальные средства существенно расширили возможности антимикробной терапии БГСА–тонзиллита, они не решили данную проблему полностью. В связи с этим многими исследователями возлагаются большие надежды на вакцину, содержащую эпитопы М–протеинов высоковирулентных БГСА–штаммов, не вступающих в перекрестную реакцию с тканевыми антигенами человеческого организма. Недавно были опубликованы первые данные клинических испытаний 26–валентной вакцины, содержащей эпитопы М–протеинов так называемых «ревматогенных» штаммов БГСА, которые не вступали в перекрестную реакцию с тканевыми антигенами человеческого организма. Результаты исследований с участием 30 здоровых добровольцев показали, что созданная рекомбинантная вакцина против А–стрептококка стимулирует иммунный ответ без каких–либо признаков токсичности. По мнению создателей, она способна обеспечивать защиту против большинства А–стрептококковых штаммов, в том числе вызывающих острый тонзиллит, синдром стрептококкового токсического шока и некротизирующий фасциит [15].
Упомянутые результаты вселяют определенный оптимизм, но при этом возникает как минимум один вопрос: не приведет ли вызванная вакциной активация иммунной системы пациента к первичной или повторной атаке ОРЛ? Ответ, по всей вероятности, должен быть получен в дальнейших крупномасштабных проспективных исследованиях.
источник
Медикаментозная терапия заключается в назначении антибиотиков, к которым чувствителен р-гемолитический стрептококк группы А, нестероидных противовоспалительных препаратов (НПВП), глюкокортикоидов, аминохинолиновых препаратов, витаминов, препаратов, улучшающих метаболические процессы в миокарде, и лекарств для проведения симптоматической терапии.
Антибактериальные средства используются для ликвидации очага стрептококковой инфекции в носоглотке. До настоящего времени стрептококк остается высокочувствительным к антибиотикам пенициллиновой группы. Начинают терапию с курса бензилпенициллина в суточной дозе от 1,5 до 4 млн ЕД в виде внутримышечных инъекций в течение 10—14 дней. При отсутствии факторов риска (отягощенная наследственность, неблагоприятные социально-бытовые условия) возможно использование 10-дневного курса оральных препаратов пенициллиновой группы: феноксиметилпенициллина по 0,5—1,0 г 4 раза в день, ампициллина по 0,5 г 4 раза в день, амоксициллина по0,5 г 3 или 1,0 г 2 раза в день. Лучшим препаратом из перечисленных является амоксициллин, так как он не уступает по эффективности феноксиметилпенициллину и ампициллину, но обладает большей биодоступностью и меньшей степенью связывания с сывороточными белками.
При непереносимости (аллергия) вышеперечисленных препаратов рекомендовано применение:
1. Макролидов:
■ спирамицин (ровамицин) 6-9 млн ME за 2-3 приема, длительность курса 5—8 дней;
■ азитромицин, рокситромицин, кларитромицин, эритромицин (в дозе 0,25—0,5 г внутрь через 4-6 ч в течение 5-8 дней).
2. Комбинированных препаратов (амоксициллин-клавунат, ампициллинсульбактам).
3. Оральных цефалоспоринов (цефалексин, цефаклор, цефиксим). Антибиотики этих групп рассматриваются как препараты второго ряда в
случае неэффективности пенициллинотерапии. Эти антибиотики высокоактивны в отношении стрептококка и способны создавать высокую концентрацию в очаге инфекции. Не рекомендуется лечить ОРЛ тетрациклинами, левомицетином (хлорамфениколом), фторхинолонами, сульфаниламидами, так как к этим препаратам стрептококк мало чувствителен или полностью резистентен.
В качестве нового средства профилактики и этиотропного лечения стрептококковой инфекции рекомендован томицид. Препарат представляет собой антагонистическую субстанцию, основным действующим началом которой является бактериоциноподобное вещество (смесь лизатов бактерий), оказывающее ингибирующее действие на многие микроорганизмы, в том числе стрептококки.
Аналогичным действием обладает имудон (таблетки), представляющий собой поливалентный комплекс, в состав которого входят вещества, действующие на микроорганизмы, наиболее часто вызывающие воспалительный процесс в полости рта. Активным действующим компонентом препарата является смесь лизатов бактерий: 50 мг сухого вещества для местного применения. Имудон активирует фагоцитоз, способствует увеличению содержания лизоцима и секреторного IgA в слюне, а также иммунокомпетентных клеток. Препарат показан при остром и хроническом фарингите, хроническом тонзиллите, стоматите, до и после тонзиллэктомии, при удалении зубов. Суточная доза препарата 8 таблеток, которые рассасываются во рту с интервалом 2—3 ч. Средняя продолжительность лечения 10 дней.
После окончания лечения антибиотиками короткого действия сразу начинают вторичную профилактику заболевания путем внутримышечного введения препаратов пенициллина пролонгированного действия.
НПВП назначают при ревматическом артрите, хорее, кардите легкой и средней степени тяжести, при легкой и умеренной степени активности. В настоящее время предпочтение отдается диклофенаку (75 мг в сутки), ацетилсалициловой кислоте (3,0-4,0 г в сутки). При их непереносимости возможно применение ибупрофена по 800—1200 мг в день. Терапевтическая доза назначается на период стационарного лечения, но не меньше месяца, затем дозу постепенно снижают. НПВП обладают выраженной противовоспалительной активностью, в течение 10—14 дней приводят к исчезновению лихорадки, болей в суставах, уменьшению одышки, сердцебиения, положительной динамике ЭКГ, рентгенологических изменений, ЭхоКГ, реактантов острой фазы, снижению СОЭ. Общая длительность противовоспалительной терапии должна составлять 9—12 недель. Период противовоспалительного лечения определен тем, что 95% ревматических атак купируется в срок 12 недель. Отмена лечения в более ранние сроки или быстрое снижение дозы противовоспалительных препаратов приводит к возврату клинических и лабораторных признаков болезни, т. е. развитию так называемого «рибаунд-синдрома», что влечет за собой удлинение атаки до 7 и более месяцев.
Глюкокортикоиды применяют в случае тяжелого, угрожающего жизни кардита, при максимальной, а в ряде случаев и умеренной степени активности процесса с выраженным экссудативным компонентом воспаления. ГКС не применяют при минимальной степени активности ревматического воспаления и слабо выраженном кардите. Чаще из данной группы препаратов используют преднизолон. Начальная доза препарата составляет 0,5—0,6, максимально — 1,0 мг/кг массы тела, обычно не более 30-40 мг/сут. Терапевтическая доза назначается примерно в течение 2 недель до достижения выраженного клинико-лабораторного улучшения. Затем дозу снижают по 2,5-5,0 мг один раз в 5-7 дней до полной отмены препарата. При снижении дозы преднизолона необходимо назначить НПВП для продления противовоспалительного лечения до 9—12 недель.
Аминохинолиновые препараты применяют в зависимости от выраженности иммунологических процессов при ОРЛ. Эти препараты являются слабыми иммунодепрессантами, стабилизаторами лизосомальных мембран, за счет чего уменьшается протеолитическое действие лизосомальных ферментов. Используется делагил по 0,25 г или плаквенил по 0,2 г 2 раза в день в течение месяца, а затем делагил — по 1 таблетке на ночь, плаквенил — по 1 таблетке 2 раза в день длительно, до 8—12 месяцев, иногда — дольше (до 2 лет).
Витаминотерапия и метаболическая терапия являются компонентом комплексной терапии ОРЛ. Назначают большие дозы витамина С (до 1,0 г в сутки в течение 1 — 1,5 месяцев, а далее — в половинной дозе до 12 недель), витамин В1 по 1,0 мл 6% раствора и витамин В6 по 1,0 мл 5% раствора в/м через день, рибоксин по 0,4 г 3 раза в день, милдронат, неотон, продектин (триметацидин), триметазидин (предуктал) длительно. Эти препараты улучшают метаболические процессы в миокарде, способствуют активизации синтеза белка, обладают антиоксидантной активностью.
Симптоматические средства применяют при развитии осложнений ОРЛ. При развитии недостаточности кровообращения назначают малые дозы сердечных гликозидов, иАПФ, мочегонные средства, препараты калия, при развитии аритмий — антиаритмические препараты.
Профилактика ОРЛ. Согласно рекомендациям Комитета экспертов ВОЗ профилактика ревматической лихорадки подразделяется на первичную (профилактика первичной заболеваемости) и вторичную (профилактика повторных случаев болезни).
Цель первичной профилактики — организация комплекса индивидуальных, общественных и общегосударственных мер, направленных на ликвидацию первичной заболеваемости ОРЛ, — санация хронического тонзиллита, лечение родственников больных РЛ, закаливание, организация здорового быта, санаторное лечение, своевременная и адекватная терапия острых заболеваний верхних дыхательных путей (ангин и фарингитов), вызванных стрептококком группы А. Лечение острой стрептококковой инфекции проводят бензилпенициллином в суточной дозе 2—4 млн ЕД/сут для подростков и взрослых в/м в 4 приема. Курс лечения составляет не менее 10 дней.
Возможно использование пероральных препаратов при менее выраженной клинической картине заболевания: феноксиметилпенициллин по 250 мг 4 раза в сутки или полусинтетические пенициллины, цефалоспорины, макролиды в тех же дозах, которые были указаны выше (см. раздел «лечение») не менее 10 дней. Для лечения стрептококкового фарингита исследовательская группа ВОЗ предлагает использовать бициллин-1 внутримышечно 1,2 млн ЕД или феноксиметилпенициллин внутрь по 250 мг 4 раза в сутки в течение 10 дней.
Вторичная профилактика направлена на предупреждение рецидивов у лиц, уже перенесших ОРЛ, путем регулярного введения пенициллинов пролонгированного действия (бициллинов, бензатин-пенициллина). В России они выпускаются в виде бициллина-1 и бициллина-5, содержащего 1 часть бензилпенициллина новокаиновой соли и 4 части бициллина-1. В то же время ряд авторов указывают на недостаточную эффективность бициллинопрофилактики у 13—37% пациентов. В связи с чем для вторичной профилактики ОРЛ в настоящее время рекомендуется введение бензатинбензилпенициллина, аналогами которого в других странах являются пендепон (Чехия), тардоциллин (Германия), ретарпен (Австрия), экстенциллин (Франция), бензациллин (Болгария).
Необходимость проведения бициллиновой профилактики больным ОРЛ обусловлена тем, что они отличаются особой чувствительностью к повторным стрептококковым инфекциям. Известно, что после стрептококковой инфекции опасность обострения ревматического процесса в 10—20 раз выше вероятности впервые заболеть ревматизмом. К тому же стрептококковая инфекция нередко протекает в виде субклинических или ассоциированных с вирусом форм, которые трудно своевременно диагностировать. Длительное непрерывное введение препаратов пенициллина больным, перенесшим ОРЛ, позволяет достаточно надежно предупредить у них развитие любых стрептококковых инфекций и тем самым резко снизить опасность рецидивирования и прогрессирования ревматического процесса. Профилактику начинают уже в стационаре сразу после окончания курса-пенициллинотерапии.
Вторичная профилактика ОРЛ в нашей стране проводится в соответствии с методическими рекомендациями, разработанными в Институте ревматологии АМН. В основном они соответствуют рекомендациям ВОЗ. Бициллин-1 вводят внутримышечно в дозе 1,2 млн ЕД 1 раз в неделю. Бициллин-5 вводят внутримышечно в дозе 1,5 млн ЕД 1 раз в 2 недели.
Бициллинопрофилактика должна проводиться круглогодично без перерывов. Сезонная бициллинопрофилактика (в весенне-осенний период) не позволяет предотвратить рецидивы ОРЛ. Эффективность сезонной бициллинопрофилактики в 10 раз ниже, чем круглогодичной.
Длительность бициллинопрофилактики экспертами ВОЗ определяется в соответствии со следующими правилами: при отсутствии клинических симптомов поражения сердца и очагов активной хронической инфекции — не менее 3 лет после последней атаки ОРЛ (именно в этот период опасность рецидива ревматизма наиболее реальна — 95%), но прекращается не ранее, чем по достижении пациентом 18 лет, после перенесенного кардита — до 25-летнего возраста и более. Больным с ХРБС и тем, кому выполнялась хирургическая коррекция порока сердца, эксперты ВОЗ рекомендуют проводить вторичную профилактику ОРЛ в течение всей жизни.
В условиях вторичной профилактики обязательным является проведение текущей профилактики ОРЛ. Она заключается в назначении антибактериальных препаратов, к которым чувствителен стрептококк, всем больным, перенесшим ОРЛ, при интеркуррентных инфекционных заболеваниях и малых операциях (экстракция зуба, аборт, тонзиллэктомия и др.). При малых операциях пероральный прием антибиотиков может быть заменен парентеральным введением бензилпенициллина в течение 5 дней с последующим введением бициллина-1 или бициллина-5 в стандартных дозах. Целью текущей профилактики является не только предотвращение ОРЛ, но и предотвращение развития инфекционного эндокардита.
При беременности у женщин, перенесших ОРЛ, проводящаяся бициллинопрофилактика не отменяется. Но если к моменту беременности бициллинопрофилактика была уже прекращена, то ее возобновляют с 12-14-недельного срока беременности и проводят до родов.
источник
Распространенность острой ревматической лихорадки (ОРЛ) в развитых странах составляет 3 – 8 случаев на 10 тысяч населения. Максимальная заболеваемость отмечается у детей в возрасте от 7 до 15 лет, причем мальчики и девочки болеют с одинаковой частотой. Это объясняется тем, что в данном возрасте обычно происходят первые контакты детского организма со стрептококком, что и обуславливает соответствующую реакцию иммунной системы. У 10 – 15% пациентов первые проявления заболевания могут возникать и в более позднем возрасте.
Интересные факты
- Ревматическая лихорадка развивается у 3% людей, перенесших стрептококковую инфекцию.
- Поражение сердца при ревматической лихорадке является одной из самых распространенных причин инвалидности среди людей трудоспособного возраста.
- В начале 20 века более 40% людей, заболевших ревматической лихорадкой, умирали. У 70% развивались необратимые пороки сердца.
- Сегодня, ввиду широкого распространения антибиотиков, частота развития ревматической лихорадки и ее осложнений снизилась в несколько раз.
- Поражение суставов при ревматической лихорадке является полностью обратимым.
Иммунная система – комплекс органов и тканей человека, которые обеспечивают иммунитет, то есть сопротивляемость организма по отношению к чужеродным бактериям, вирусам, грибкам и другим органическим структурам. Эта функция осуществляется благодаря наличию и совместной работе, так называемых, иммунокомпетентных клеток.
После рождения организм ребенка защищен врожденным иммунитетом, который осуществляется посредством циркуляции в его крови иммунных факторов (антител), перешедших от матери. Примерно через 6 месяцев жизни функциональная активность материнских антител истощается, и у ребенка начинает активно развиваться собственная иммунная система (вырабатывается приобретенный иммунитет).
Органами иммунной системы являются:
- Красный костный мозг. Располагается преимущественно в губчатых костях (таза, грудины, тел позвонков). Является основным органом кроветворения, в котором также образуются клетки иммунной системы.
- Тимус (вилочковая железа). В нем происходит образование и дифференциация (обучение) Т-лимфоцитов.
- Селезенка. В данном органе происходит дифференциация иммунокомпетентных клеток, а также разрушение «старых» и поврежденных клеток крови, чужеродных бактерий и других инородных частиц.
- Лимфатические узлы. Располагаются по ходу лимфатических сосудов во всем организме и содержат Т-лимфоциты и В-лимфоциты. В лимфоузлах происходит уничтожение различных бактериальных и вирусных частиц, что предотвращает их дальнейшее распространение по организму.
В центральных органах иммунной системы (в костном мозге и тимусе) происходит образование и дифференцировка всех иммунокомпетентных клеток. После этого они поступают в общий кровоток и в другие органы, где выполняют свои функции.
Клетками, обеспечивающими иммунитет, являются:
- Лимфоциты (Т и В) – основные иммунокомпетентные клетки, регулирующие деятельность всей иммунной системы.
- Нейтрофилы – мигрируют в очаг воспаления, где фагоцитируют (то есть поглощают и разрушают) небольшие фрагменты бактерий, грибов.
- Эозинофилы – участвуют в поглощении и нейтрализации фрагментов бактерий и грибов, а также оказывают токсическое действие на других паразитов в очаге воспаления (посредством выработки антител).
- Базофилы – играют важную роль в развитии аллергических реакций.
- Моноциты – находятся в тканях различных органов, поглощая и уничтожая чужеродные микроорганизмы и опухолевые клетки.
В общих чертах принцип работы иммунной системы человека заключается в следующем. Любой микроорганизм (бактерия, вирус, грибок и так далее) имеет на своей поверхности определенные структуры, называемые антигенами, причем антигенный набор каждой клетки уникален и специфичен. При попадании в организм человека бактериальные антигены распознаются иммунокомпетентными клетками (лимфоцитами) как «чужие» и уничтожаются посредством различных механизмов.
Важно отметить, что клетки собственного организма человека также содержат определенные антигены, однако в процессе синтеза лимфоцитов данные антигены программируются как «свои» и не разрушаются.
С функциональной точки зрения иммунная система человека включает:
- клеточный иммунитет;
- гуморальный иммунитет.
Данный вид иммунитета подразумевает непосредственное участие иммунокомпетентных клеток в выявлении и уничтожении чужеродного агента, попавшего в организм. Клеточный иммунитет регулируется различными подвидами Т-лимфоцитов (Т-хелперами, Т-киллерами, Т-супрессорами и Т-клетками памяти), а также другими клетками иммунной системы.
В чистом виде «чужой» антиген не способен взаимодействовать с иммунной системой человека, поэтому он поглощается так называемыми антигенпрезентирующими клетками, обрабатывается и представляется на поверхности их клеточных мембран. В таком виде микробные антигены распознаются Т-хелперами. Это приводит к ускоренному образованию и активации Т-киллеров (особых лимфоцитов, способных разрушать клетки, на поверхности которых имеется чужеродный антиген), моноцитов и других клеток иммунной системы, которые распространяются по всему организму, находя и уничтожая «чужие» антигены.
Результатом описанных реакций является разрушение всех клеток, содержащих бактериальные антигены (как чужих, так и собственных, пораженных инфекцией).
Антигенпрезентирующие клетки, на поверхности которых находится чужеродный антиген, попадают в лимфатическую систему. С током лимфы они доставляются в ближайший лимфатический узел, являющийся местом скопления большого количества В-лимфоцитов. При контакте с чужеродным антигеном (прямом либо опосредованном Т-хелперами) В-лимфоциты превращаются в так называемые плазматические клетки, в которых синтезируется большое количество особых антител (иммуноглобулинов класса M, G и других), строго специфичных к распознанному антигену. Данные антитела выделяются в кровь, связываются с чужеродными антигенами и активируют целый ряд неспецифических иммунных реакций (систему комплемента, фагоцитоз, синтез нейтрофилов и моноцитов), что приводит к разрушению «чужого» антигена и всех клеток, на мембране которых он расположен.
Весь процесс активации В-лимфоцитов и синтеза антител занимает около 2 недель. Как только чужеродный антиген полностью удаляется из организма, прекращается и образование плазматических клеток. Однако определенная часть В-лимфоцитов превращается в так называемые В-клетки памяти, которые могут циркулировать в крови на протяжении многих лет. Они несут в себе информацию об инфекционном агенте, вызвавшем иммунный ответ. При повторном его проникновении в организм клетки памяти обуславливают быструю (в течение нескольких минут или часов) активацию В-лимфоцитов и синтез большого количества специфических антител.
Как говорилось ранее, ревматическая лихорадка развивается в результате попадания в организм человека В-гемолитического стрептококка группы А. Этот микроорганизм обладает огромным набором различных антигенов (м-протеином, полисахаридами), а также вырабатывает множество токсинов (стрептолизины S и О, протеиназу, гиалуронидазу и другие), каждый из которых активирует образование специфических антител.
Центральным звеном патогенеза ревматической лихорадки является тот факт, что некоторые антигены В-гемолитического стрептококка структурно схожи с антигенами определенных тканей человеческого организма. В результате этого антитела, вырабатываемые с целью уничтожения чужеродных агентов, взаимодействуют и с клетками тканей человека, вызывая их разрушение.
Важно отметить, что системные поражения обусловлены не только нарушениями в работе иммунной системы, но и способностью некоторых токсинов В-гемолитического стрептококка непосредственно повреждать ткани человеческого организма.
Антитела против стрептококковых антигенов поражают:
- Соединительную ткань. Это особый тип ткани, имеющийся практически во всех органах человека и выполняющий поддерживающую и защитную функции. При ревматической лихорадке поражается преимущественно соединительная ткань сердца, стенок сосудов и суставов, что и приводит к соответствующим клиническим проявлениям заболевания.
- Кардиомиоциты. После того как клетки сердечной мышцы поражаются стрептококковыми токсинами, некоторые их антигены начинают распознаваться иммунной системой как «чужие», в результате чего к ним также могут вырабатываться антитела.
- Нервные клетки (нейроны). Нейроны определенных зон мозга (субталамического и хвостатого ядер) также имеют сходство с антигенами стрептококков и могут поражаться антителами.
Все описанные выше явления приводят к тому, что в различных органах развиваются характерные воспалительные процессы, исходом которых является некроз (гибель) поврежденного участка. Вокруг очага некроза образуется так называемая гранулема, представляющая собой компенсаторное разрастание соединительной ткани. Гранулема развивается в течение 3 – 4 месяцев, после чего она склерозируется, то есть на месте повреждения образуется плотный рубец. Множественные рубцовые изменения вызывают необратимые нарушения функций пораженного органа, что может являться причиной инвалидности.
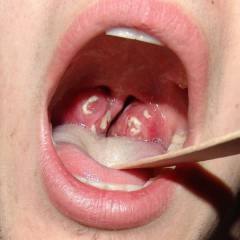
Важно отметить, что ОРЛ возникает только после инфицирования лимфоидных образований глотки. Гемолитические стрептококки могут поражать и другие участки тела (кожу, мягкие ткани), однако развивающиеся в данном случае заболевания не осложняются острой ревматической лихорадкой. Это объясняется различиями в иммунных реакциях, которые активируются в ответ на поражение кожи и глотки, а также различным антигенным составом стрептококков, участвующих в развитии данных инфекционных заболеваний.
Причиной ревматической лихорадки может быть:
- Острый тонзиллит (ангина). Это инфекционное воспаление лимфоидных образований глотки, чаще небных миндалин (гланд). Заболевание проявляется болью в горле, повышением температуры тела, покраснением слизистой оболочки небных миндалин. Иногда на них может появляться белый налет или язвочки.
- Фарингит. Данным термином обозначается воспаление слизистой оболочки глотки, развивающееся при попадании стрептококка в дыхательные пути. Заболевание проявляется першением и болью в горле, сухим, мучительным кашлем и повышением температуры тела до 37,5 – 38,5ºС.
- Скарлатина. Инфекционное заболевание, проявляющееся мелкой сыпью на коже, симптомами общей интоксикации (повышением температуры, ознобом, мышечными и головными болями), а также поражением лимфоидных образований глотки по типу ангины.
Все перечисленные заболевания могут быть вызваны и другими факторами – различными бактериями, вирусами, слизистая оболочка глотки может воспалиться при вдыхании холодного или горячего воздуха или различных химикатов, однако острая ревматическая лихорадка развивается только после инфицирования В-гемолитическим стрептококком группы А.
Для развития острой ревматической лихорадки недостаточно единичного попадания стрептококка в организм. Дело в том, что при первичном инфицировании (которое обычно происходит до 3 – 5 лет) клетки иммунной системы взаимодействуют со стрептококковыми антигенами, однако освобождение организма от инфекции и выздоровление наступает быстрее, чем развиваются патологические иммунные реакции.
Для возникновения ревматической лихорадки необходимы повторные и длительные контакты иммунной системы с антигенами и развитие так называемой сенсибилизации (или повышенной чувствительности) к микроорганизму. Если организм человека сенсибилизирован к стрептококку, то при очередном инфицировании развивается длительная, выраженная иммунная реакция (как клеточная, так и гуморальная). Этим объясняется тот факт, что дети до трехлетнего возраста болеют ревматической лихорадкой в исключительно редких случаях.
Многие проведенные исследования указывают на наличие генетической предрасположенности к ОРЛ. Это подтверждается более частым развитием ревматической лихорадки у близнецов, а также у братьев и сестер, если один или оба их родителя страдали данным заболеванием.
Точный механизм наследования науке неизвестен, однако предполагается участие генов так называемого главного комплекса гистосовместимости (MHC). Исследованиями последних лет установлено, что у детей с генетической предрасположенностью, часто страдающих стрептококковыми инфекциями, в области небных миндалин образуются специальные рецепторы к поверхностным антигенам В-гемолитического стрептококка, что и обуславливает развитие выраженного иммунного ответа при контакте с данным микроорганизмом.
Появлению симптомов ОРЛ обычно предшествует так называемый период мнимого благополучия, когда признаки перенесенной инфекции выражены минимально (может отмечаться слабость, повышенная утомляемость, безболезненное увеличение подчелюстных лимфоузлов). В это время происходит превращение В-лимфоцитов в плазматические клетки и синтез специфических антител. Когда антитела начинают выделяться в кровь в больших количествах, наступает период развернутых клинических проявлений заболевания.
Клинические проявления ОРЛ различаются в зависимости от возраста больного, поражаемых органов и проводимого лечения. У детей дошкольного и младшего школьного возраста симптомы возникают остро, ярко выражены и существенно сказываются на общем состоянии ребенка. У взрослых заболевание характеризуется более медленным началом и менее выраженной симптоматикой.
Острая ревматическая лихорадка может проявляться:
- повышением температуры тела;
- поражением сердца (кардитом);
- воспалением суставов (полиартритом);
- подкожными ревматическими узелками;
- кольцевидной эритемой (специфической сыпью);
- поражением центральной нервной системы (малой хореей);
- поражением других органов и систем.
Как только антитела начинают поступать в кровь, они взаимодействуют со стрептококками и с антигенами соединительной ткани организма хозяина, вызывая системный воспалительный процесс. В очаг воспаления мигрируют лейкоциты (нейтрофилы, моноциты, базофилы), которые выделяют биологически активные вещества (главным образом серотонин и гистамин), что и обуславливает повышение температуры.
Чем сильнее больной человек сенсибилизирован к инфекции, тем быстрее будет развиваться воспалительный процесс и тем выраженнее будет температурная реакция организма. В тяжелых случаях температура тела может повышаться до 38 — 39ºС и выше, сопровождаясь обильным потоотделением, общей слабостью, сонливостью, головными и мышечными болями.
Стоит отметить, что у взрослых людей данный симптом менее выражен, а у пожилых может и вовсе отсутствовать, что связано с уменьшением активности иммунной системы в старческом возрасте.
Поражение сердца встречается у 50 – 80% больных при первом эпизоде ревматической лихорадки и почти у 100% больных при рецидивах заболевания.
Сердце представляет собой мышечный орган, состоящий из четырех камер — двух предсердий (правого и левого) и соответствующих им желудочков. Камеры сердца разделены между собой клапанами, которые открываясь и закрываясь в определенной последовательности обеспечивают циркуляцию крови в организме.
Насыщенная кислородом (артериальная) кровь из легких поступает в левое предсердие, а из него через митральный клапан – в левый желудочек. Через аортальный клапан артериальная кровь изгоняется из левого желудочка в системный кровоток, отдавая кислород тканям и превращаясь в венозную. Венозная кровь собирается в венах и впадает в правое предсердие, а затем (через трикуспидальный клапан) в правый желудочек, откуда (через клапан легочной артерии) перекачивается в легкие.
В структуре сердца различают три оболочки, которые в равной степени могут повреждаться антистрептококковыми антителами, что и будет обуславливать клиническую картину заболевания.
Поражение сердца при ОРЛ может проявляться:
- эндокардитом;
- миокардитом;
- перикардитом.
Эндокардит
Данным термином обозначается воспаление внутренней оболочки сердца, непосредственно контактирующей с кровью. В норме она идеально гладкая, что предотвращает тромбообразование (прилипание и склеивание клеток крови). При развитии воспаления целостность ее поверхности нарушается, что создает препятствия протекающей через сердце крови (клинически это проявляется появлением патологических шумов при выслушивании сердца) и предрасполагает к образованию тромбов.
Результатом воспалительного процесса является образование рубцов на эндокарде, причем наиболее опасным является поражение клапанов сердца. Их рубцовые изменения могут привести к стенозу (сужению просвета) либо к недостаточности (неполному смыканию створок клапанов), в результате чего может нарушаться кровоснабжение всего организма.
Чаще всего поражаются митральный и аортальный клапаны, что может проявляться общей и мышечной слабостью, частыми головокружениями и обмороками, а в тяжелых случаях – кашлем, одышкой, отеком легких и другими симптомами сердечной недостаточности.
Миокардит (воспаление сердечной мышцы)
Возникает как в результате прямого токсического влияния стрептококков на сердце, так и вследствие поражения кардиомиоцитов антителами. Насосная функция сердечной мышцы при этом сильно снижается и организм не получает достаточного количества крови, в связи с чем человек может жаловаться на колющие боли в области сердца, одышку (чувство нехватки воздуха), общую слабость и быструю утомляемость при физических нагрузках.
Перикардит
Редкое проявление ОРЛ (встречается не более чем у 10% больных), при котором воспаляется наружная оболочка сердца (перикард). Перикард состоит из двух листков, один из которых прилегает непосредственно к сердечной мышце, а второй фиксирует орган в грудной клетке. В норме между этими листками существует небольшое щелевидное пространство, позволяющее им смещаться друг относительно друга во время сердечных сокращений.
При воспалении перикарда в этом пространстве скапливается больше количество воспалительной жидкости (экссудата), либо откладывается особый белок – фибрин, который склеивает наружный и внутренний листки перикарда между собой. В обоих случаях происходит сдавливание сердца и снижение его насосной функции, что может проявляться болями в грудной клетке, одышкой в покое или при физической нагрузке, кашлем.
Полиартрит встречается более чем у 70% больных ревматической лихорадкой. Поражение суставов развивается остро и часто сочетается с другими проявлениями заболевания.
В норме любой сустав состоит из суставных поверхностей двух костей, на концах которых располагается суставной хрящ. Полость сустава окружена плотно прилегающей оболочкой – синовиальной мембраной. Она содержит небольшое количество синовиальной жидкости, которая выполняет питательную и защитную функции. При поражении синовиальной мембраны антителами в ней развивается выраженный воспалительный процесс, который сопровождается миграцией лейкоцитов к очагу воспаления и выделением гистамина и серотонина. В полость сустава выделяется большое количество экссудата, что повышает внутрисуставное давление и нарушает подвижность в нем.
Полиартрит при острой ревматической лихорадке характеризуется:
- Поражением множества суставов. Признаки воспаления возникают одновременно в обоих симметричных суставах, что является характерной особенностью ревматической лихорадки. Вначале поражаются наиболее крупные суставы (коленный, плечевой). Через некоторое время присоединяется поражение средних суставов – локтевых, голеностопных. Воспаление мелких суставов (кистей, стоп) встречается реже и свидетельствует о тяжелом течении заболевания.
- Болью. Боль обусловлена выделением медиаторов воспаления и носит острый характер, усиливается при любых активных или пассивных движениях в пораженном суставе и при его пальпации (прощупывании).
- Покраснением. В очаге воспаления происходит расширение кровеносных сосудов (обусловленное выделением гистамина), в результате чего цвет кожных покровов становится более красным.
- Припухлостью. Гистамин и серотонин повышают проницаемость мелких сосудов, в результате чего жидкая часть крови выходит из сосудистого русла в окружающие ткани. Этим обусловлено развитие отека и припухлости пораженных суставов.
- Местным повышением температуры. Расширение сосудов приводит к увеличению количества крови, поступающей в очаг воспаления. В результате этого температура кожи над пораженным суставом повышается на 1 – 2 градуса по сравнению с соседними участками (что определяется при пальпации).
- Нарушением функции пораженных суставов. Выделение экссудата в полость синовиальной оболочки, а также выраженная болезненность при любых движениях заставляют больного максимально снизить нагрузку на пораженные суставы, что может повлиять на повседневный образ жизни.
Важно отметить, что полиартрит при первой атаке ревматической лихорадки является обратимым. Без лечения воспалительные явления самостоятельно стихают через 2 – 3 недели, не оставляя после себя никаких признаков структурного поражения суставов. При назначении противовоспалительной терапии боли исчезают гораздо быстрее – в течение нескольких часов или дней.
В легких случаях заболевания поражение суставов может проявляться только болезненностью (артралгией) без других признаков воспаления.
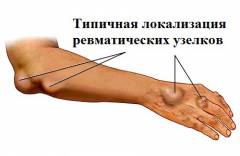
Подкожные узелки встречаются крайне редко (в 1 – 3 % случаев). Они развиваются в результате разрушения соединительной ткани и компенсаторного разрастания непораженных участков, расположенных вокруг зоны воспаления. При пальпации ревматические узелки определяются как плотные, малоподвижные и безболезненные образования, от 1 мм до 2 см в диаметре. Чаще всего они обнаруживаются над костными выступами, в местах прикрепления сухожилий (на разгибательных поверхностях крупных суставов, в области лодыжек, затылка, позвоночника).
Данные образования появляются позже других симптомов болезни (обычно через 5 – 10 дней после начала клинических проявлений). Узелки рассасываются медленно (в течение 2 – 4 недель), однако исчезают без остаточных явлений.
Обычно возникает на пике клинических проявлений заболевания, на фоне выраженной лихорадки и полиартрита. Характеризуется появлением на коже в области туловища или верхних частей рук и ног красных или розовых пятен различных размеров (до нескольких сантиметров в диаметре). Они не возвышаются над поверхностью кожи, имеют четкие края, безболезненны, не чешутся, бледнеют при надавливании. Пятна постепенно увеличиваются в размерах, при этом в центре появляется относительно бледное пятно (внешне напоминает кольцо). Они могут сливаться друг с другом, появляться и исчезать в различных областях тела, но никогда не располагаются в области лица.
Развитие данного симптома связывают с поражением кожи специфическими антителами, в результате чего развивается воспалительная реакция, сопровождающаяся расширением кровеносных сосудов. После стихания воспалительного процесса кольцевидная эритема исчезает без каких-либо остаточных явлений.
Механизм поражения центральной нервной системы (ЦНС) при ревматической лихорадке окончательно не установлен. Считается, что основную роль в этом играет выработка антител, которые поражают нервные клетки. Первые признаки поражения ЦНС появляются через 2 – 4 месяца после стихания лихорадки, редко сопровождаются артралгиями или другими симптомами заболевания.
Типичным проявлением ревматической лихорадки является малая хорея, которая характеризуется появлением неконтролируемой, беспорядочной двигательной активности. Внешне движения ребенка напоминают нормальные, однако характеризуются чрезмерно выраженной амплитудой и интенсивностью. Данное состояние развивается постепенно — родители замечают, что ребенок начинает ронять предметы из рук, нарушается его почерк, позже появляются непроизвольные подергивания мышц лица и конечностей. Несмотря на повышенную двигательную активность мышечный тонус у таких детей снижен, что является характерным признаком ревматической хореи.
В тяжелых случаях может отмечаться нарушение походки, трудности при общении, нарушение процессов глотания. Ребенок становится агрессивным, раздражительным, плаксивым. Обычно данное состояние длится от 2 до 4 месяцев, однако при назначении противострептококковой терапии симптомы регрессируют довольно быстро.
Помимо разрушения нейронов специфическими антителами, нарушения в работе центральной нервной системы могут быть обусловлены поражением сосудов, питающих головной и спинной мозг.
Поражения ЦНС при ревматической лихорадке могут проявляться:
- Энцефалитом – воспалением головного мозга.
- Менингитом – воспалением оболочек головного и/или спинного мозга.
- Невралгиями – болезненностью определенного участка тела, иннервируемого пораженным нервом.
- Нарушением умственного развития – ухудшением памяти, снижением успеваемости в школе и так далее.
Перечисленные выше симптомы являются наиболее характерными проявлениями ревматической лихорадки, однако при данном заболевании поражаться может практически любой орган и любая ткань, что будет отражаться на состоянии пациента.
Менее частыми проявлениями ревматической лихорадки являются:
- Поражение легких. Развивается на пике лихорадки. Характеризуется воспалительным повреждением легочной ткани (пневмонией) либо легочных сосудов (васкулитом), а также экссудативным плевритом (скоплением экссудата в плевральной полости – щелевидном пространстве между легкими и грудной клеткой). Это может проявляться болью в груди, одышкой, кашлем с небольшим количеством мокроты. Ревматический характер пневмонии подтверждается полным отсутствием эффекта при применении антибиотиков и быстрым улучшением состояния пациента после назначения противоревматических препаратов.
- Поражение желудочно-кишечной системы (абдоминальный синдром). Проявляется резкими острыми болями в животе. Их возникновение может быть связано с воспалением сосудов брыжейки (особой ткани, фиксирующей кишечник в животе), перитонитом (воспалением брюшины – тонкой пленки, покрывающей поверхность внутренних органов). Кроме этого, больные могут жаловаться на диарею или запоры, тошноту, рвоту. Как и при поражении легких, симптомы полностью исчезают после назначения противоревматических препаратов.
- Поражение почек. В норме в почках происходит фильтрация крови, в результате чего побочные продукты обмена веществ и часть жидкости превращаются в мочу и выводятся из организма. При ОРЛ функция почек нарушается, следствием чего может стать появление в моче клеток крови и других веществ (например, белков), которые обычно в ней отсутствуют.
- Поражение печени. Воспаление ткани печени (гепатит) встречается довольно редко. Гораздо чаще поражение печени обусловлено развитием сердечной недостаточности – состояния, при котором сердце не может перекачивать необходимое количество крови, в результате чего она скапливается в печени. Это приводит к перерастяжению органа и нарушению его функций, что проявляется тяжестью и болями в правом подреберье.
- Поражение глаз. Характеризуется воспалением радужной оболочки (иритом), роговицы (кератитом) и других структур глаза. Это может проявляться режущей болью в глазах, усиленным слезотечением, светобоязнью, помутнением роговицы и другими симптомами, вплоть до нарушения зрения.
- Поражение сосудов. Как уже говорилось, воспалительный процесс может поражать любые сосуды организма, приводя к самым разнообразным проявлениям – кровотечениям, нарушению кровоснабжения и некрозу (гибели) части органа и так далее.
При подозрении на ревматическую лихорадку назначается:
- выделение стрептококка из носоглотки;
- общий анализ крови;
- биохимический анализ крови;
- иммунологическое исследование крови;
- общий анализ мочи;
- электрокардиография (ЭКГ);
- эхокардиография (Эхо-КГ);
- фонокардиография (ФКГ);
- рентгенография органов грудной клетки.
Выделение В-гемолитического стрептококка группы А из носоглотки является обязательным условием для подтверждения диагноза ревматической лихорадки. Забор материала на анализ производится в лаборатории, где медсестра стерильной ватной палочной несколько раз проводит по слизистой оболочке зева, глотки, полости рта и носа. Затем производится посев полученного материала на специальных питательных средах, на которых стрептококк растет и размножается лучше всего.
Рост колоний В-гемолитического стрептококка подтверждает наличие данного микроорганизма на слизистой оболочки носоглотки, однако не дает информацию о давности инфицирования и степени активности заболевания. Стоит отметить, что культура стрептококка может выделяться при полном отсутствии клинических проявлений инфекции (у так называемых бессимптомных носителей), однако это не исключает возможность развития ревматической лихорадки у таких пациентов.
Данное исследование позволяет подтвердить наличие инфекции в организме, а также выявить некоторые признаки системного воспалительного процесса.
Изменения в общем анализе крови характеризуются:
- Увеличением количества лейкоцитов. При наличии стрептококковой инфекции и в течение нескольких дней после нее может определяться повышение общего числа лейкоцитов (более 9,0 х 10 9 /л), преимущественно за счет молодых (палочкоядерных) форм нейтрофилов. Это обусловлено активацией иммунной системы в ответ на наличие чужеродной бактерии в организме, в результате чего лейкоциты не успевают полностью дифференцироваться в лимфоидных органах и выделяются в кровоток в незрелом виде.
- Повышением скорости оседания эритроцитов (СОЭ). Данный показатель определяется путем помещения крови в пробирку и измерения времени, за которое более тяжелые эритроциты осядут на дно пробирки. В нормальных условиях поверхность эритроцитов заряжена отрицательно, что препятствует их сближению и поддерживает клетки крови во взвешенном состоянии. При наличии воспалительного процесса в кровь выделяется большое количество белков острой фазы воспаления, что способствуют более быстрому оседанию эритроцитов. СОЭ при этом может увеличиваться в несколько раз (при норме не более 10 мм в час у мужчин и 15 мм в час у женщин).
| Название | Норма |
| С-реактивный белок | Менее 5 мг/л. |
| А-1 антитрипсин | 0,9 – 2 г/л |
| А-2 глобулин | Мужчины: 1,5 – 3,5 г/л. |
| Женщины: 1,75 – 4,2 г/л. | |
| Фибриноген | 2 – 4 г/л. |
| Церулоплазмин | 0,15 – 0,6 г/л. |
| Лактоферрин | 190 – 750 нг/мл |
| Гаптоглобин | 0,8 – 2,7 г/л. |
| Название | Что обозначает | Норма |
| Иммуноглобулин М (IgM) | Концентрация IgM в крови начинает повышаться через несколько часов после инфицирования. По мере освобождения организма от инфекции их концентрация будет снижаться. | 0,5 – 3,5 г/л. |
| Иммуноглобулин G (IgG) | Появляются в крови через 10 – 14 дней после инфицирования и нарастают по мере развития заболевания. Могут оставаться в крови на протяжении длительного времени, обеспечивая защиту от перенесенной инфекции. | 7,0 – 17,0 г/л. |
Более информативным является определение специфических антител, образующихся к стрептококковым антигенам. Их концентрация достигает максимума к 3 – 4 неделе после инфицирования, а по мере удаления стрептококков из организма снижается, что является надежным маркером выздоровления.
| Название | Допустимые значения |
| Антистрептолизин-О (АСЛ-О) | Взрослые: до 200 Международных Единиц в 1 мл (МЕ/мл). |
| Дети: до 150 МЕ/мл. | |
| Антистрептогиалуронидаза (АСГ) | до 335 МЕ/мл. |
| Антистрептокиназа (АСК) | до 300 МЕ/мл. |
| Анти-дезоксирибонуклеаза-В (анти-ДНКаза-В) | Взрослые: до 120 МЕ/мл. |
| Дети: до 200 МЕ/мл. |
В процессе диагностики и лечения необходимо многократное определение титра иммуноглобулинов и антистрептококковых антител в крови. Их повышение будет говорить о нарастании активности воспалительного процесса, в то время как снижение будет свидетельствовать о выздоровлении.
При ревматической лихорадке специфических изменений в общем анализе мочи не наблюдается.
При повреждении почек или на пике лихорадки может отмечаться:
- Протеинурия – наличие белка в моче в концентрации более 0,033 г/л.
- Гематурия – наличие в моче более 2 – 3 эритроцитов в поле зрения (при исследовании под микроскопом).
Данное исследование назначается при подозрении на ревматическую лихорадку в обязательном порядке, так как поражение сердца является частым осложнением заболевания.
При ревматической лихорадке ЭКГ может выявить:
- Признаки миокардита – снижение (брадикардию) или увеличение (тахикардию) частоты сердечных сокращений, нарушение их ритма, нарушение проводимости в сердечной мышце.
- Признаки поражения клапанов – на них может указывать гипертрофия (увеличение размеров) сердечной мышцы, развивающаяся при наличии стеноза или недостаточности аортального клапана.
- Признаки перикардита – снижение вольтажа (высоты зубцов) на ЭКГ и подъем сегмента RS-T (отражает переход воспалительного процесса с перикарда на верхние слои миокарда).
Суть данного метода заключается в использовании ультразвуковых волн для исследования строения и функции сердца. Определяются размеры стенок и объемы камер сердца, а также количество крови, изгоняемой во время сердечного сокращения (ударный объем).
При ревматической лихорадке Эхо-КГ позволяет выявить:
- Экссудативный перикардит. В данном случае воспалительная жидкость скапливается в перикарде, уменьшая наполнение сердца кровью, вследствие чего снижается ударный объем.
- Стеноз аортального клапана. Проявляется наличием рубцовых изменений в области клапана, а также уменьшением ударного объема. При длительном течении возможно развитие гипертрофии (утолщения) стенки левого желудочка.
- Недостаточность аортального клапана. Проявляется регургитацией (обратным током) крови через не полностью сомкнувшиеся створки клапана во время расслабления сердечной мышцы (диастолы).
- Стеноз митрального клапана. Проявляется наличием рубцов в области клапана и гипертрофией левого предсердия (при длительном существовании порока).
- Недостаточность митрального клапана. Проявляется регургитацией крови из левого желудочка в левое предсердие во время систолы.
Суть данного метода заключается в следующем. С помощью высокочувствительного микрофона производится определение тонов и шумов сердца, которые после компьютерной обработки отображаются в виде графика (на бумаге или на мониторе).
Фонокардиография может определить:
- Шум трения перикарда – появляется при фибринозном перикардите в результате трения листков перикарда друг об друга.
- Систолические шумы – могут появляться при стенозе аортального клапана либо при недостаточности митрального.
- Диастолические шумы – возникают при недостаточности аортального клапана либо при стенозе митрального.
При сочетанном поражении обоих клапанов шумы будут определяться как во время систолы, так и во время диастолы.
| Большие критерии | Малые критерии |
|
|
Диагноз ревматической лихорадки считается подтвержденным, если у больного выявлено хотя бы два больших критерия либо один большой и два малых, при этом лабораторное подтверждение перенесенной стрептококковой инфекции носоглотки является обязательным условием для постановки диагноза.

При выраженном воспалительном процессе с вовлечением сердца, суставов и центральной нервной системы пациентам показан постельный режим на срок от 5 до 14 дней. Расширять режим возможно только в том случае, если устранены признаки кардита, полиартрита и малой хореи.
Выписка пациента из стационара производится после стихания клинических проявлений и нормализации лабораторных показателей (снижения СОЭ и белков острой фазы воспаления). В дальнейшем пациенту показано санаторно-курортное и амбулаторное лечение (на дому), при этом он должен регулярно посещать лечащего врача и сдавать необходимые анализы, чтобы контролировать процесс выздоровления и предотвратить развитие осложнений.
Лекарственная терапия является основным методом лечения острой ревматической лихорадки. С этой целью применяются средства, снижающие активность воспалительного процесса и предупреждающие дальнейшее повреждение тканей и органов (включая антибактериальную терапию, направленную на уничтожение В-гемолитического стрептококка).
Важно помнить, что чем раньше начато адекватное лечение, тем больше будет его эффективность и тем меньше вероятность развития осложнений заболевания, поэтому при появлении первых признаков ревматической лихорадки необходимо немедленно обратиться к врачу.
| Группа медикаментов | Основные представители | Механизм лечебного действия и показания к использованию | Способ применения и дозы |
| Противовоспалительная терапия | |||
| Нестероидные противовоспалительные препараты (НПВП) | Диклофенак | Ингибируют циклооксигеназу и синтез простагландинов, тем самым угнетая образование и высвобождение медиаторов воспаления. Оказывают противовоспалительное, обезболивающее и жаропонижающее действие. | |
Применяются при умеренном воспалительном процессе (СОЭ 30 мм/час), при тяжелых поражениях сердца, суставов, ЦНС, а также при неэффективности нестероидных противовоспалительных препаратов.
Рекомендуемые дозы:
- Взрослым– по 10 – 20 мг 2 раза в день после еды.
- Детям – 0,7 – 0,8 мг/кг/сутки, разделенные на три приема.
Ожидаемый эффект развивается в среднем через 2 недели после приема. Отменять препарат следует очень медленно, снижая дозу на 2,5 мг 1 рад в 5 – 7 дней. После прекращения лечения следует принимать НПВП в течение как минимум 4 – 6 недель.
(Ремикейд)
(Оренсия)
(Мабтера)
Эффективность данного препарата при ревматической лихорадке продолжает изучаться.
Рекомендуемые дозы:
- Взрослым — по 400 000 – 1 000 000 Единиц Действия (ЕД) 4 раза в сутки.
- Детям – по 100 – 150 тысяч ЕД 4 раза в сутки.
Длительность лечения не менее 10 дней. При тяжелой инфекции суточная доза может быть увеличена до 10 миллионов ЕД.
Рекомендуемые дозы:
- Взрослым –300 – 600 тысяч ЕД 1 раз в неделю.
- Детям –5 – 10 тысяч ЕД/кг 1 раз в неделю.
Рекомендуемые дозы:
- Взрослым – 250 мг 2 раза в стуки.
- Детям – 10 мг/кг 2 раза в сутки.
Длительность лечения не менее 10 дней.
Рекомендуемые дозы:
- Взрослым – 500 мг 2 раза в стуки.
- Детям – 30 мг/кг 1 раз в сутки.
Длительность лечения не менее 10 дней.
(используются при неэффективности либо при непереносимости пенициллинов и цефалоспоринов)
Поражение различных органов и систем обычно не требует специфического лечения и устраняется при использовании стандартной противовоспалительной терапии, однако в некоторых случаях (при нарушении работы сердца либо при выраженных неврологических симптомах) требуется назначение целого ряда других лекарственных средств.
Для лечения сердечной недостаточности применяются:
- мочегонные препараты – фуросемид, спиронолактон;
- сердечные гликозиды – дигоксин, дигитоксин;
- медикаменты, снижающие артериальное давление – лизиноприл, атенолол;
- при развитии аритмии применяются антиаритмические средства – лидокаин, амиодарон и другие.
Для лечения малой хореи назначаются:
- успокоительные препараты – мидазолам, фенобарбитал;
- антипсихотики – галоперидол, дроперидол;
- ноотропные препараты (улучшающие умственную активность) – пирацетам (ноотропил);
- психотерапия.
Санаторно-курортное лечение назначается после стихания острого воспалительного процесса, подтвержденного клинически и лабораторно (нормализацией СОЭ и белков острой фазы, снижением общего количества лейкоцитов).
Пациент направляется в специализированный ревматологический санаторий на 1,5 – 2 месяца, где продолжает принимать противовоспалительное и антистафилококковое лечение. Кроме того, для каждого пациента разрабатывается специальная диета и индивидуальный комплекс лечебной физкультуры, направленный на нормализацию работы сердечно-сосудистой и легочной систем и предотвращение дальнейшего поражения суставов.
Санаторно-курортное лечение противопоказано:
- в остром периоде ревматической лихорадки;
- при наличии активного инфекционного процесса в носоглотке – пациент является переносчиком и распространителем инфекции;
- в случае выраженного поражения органов и систем – при сердечной недостаточности, отеке легких и так далее;
- при наличии тяжелых сопутствующих заболеваний – опухолей, туберкулеза, психических отклонений.
Все больные, перенесшие острую ревматическую лихорадку, должны в обязательном порядке продолжать лечение на дому, систематически посещая врача и сдавая необходимые анализы (общий анализ крови и мочи, посев из носоглотки) раз в 3 – 6 месяцев.
Кроме этого, больные должны принимать профилактические дозы антибиотиков в течение нескольких лет (вторичная профилактика), чтобы предотвратить прогрессирование заболевания и его рецидивы. С этой целью чаще всего используется бензатина бензилпенициллин, вводимый внутримышечно, 1 раз в 3 недели. Взрослым препарат вводится в дозе 2,4 миллиона ЕД, детям с массой тела менее 25 кг – 600 тысяч ЕД, а с массой тела более 25 кг – 1,2 миллиона ЕД.
Длительность такого лечения после неосложненной ревматической лихорадки должна продолжаться до 5 лет, а в случае развития пороков сердца – до 10 лет и более (иногда пожизненно).
Специальной диеты при данном заболевании не требуется. Тем не менее, пациентам во время обострения ревматической лихорадки, а также на протяжении всего периода выздоровления необходимо полноценное, сбалансированное питание, чтобы организм мог адекватно сопротивляться инфекции (стрептококку) и в то же время восстанавливать поврежденные органы и ткани.
Больным ревматической лихорадкой рекомендуется:
- Употреблять не менее 1 грамма белков на килограмм массы тела в сутки (белки являются строительным материалом, за счет которого происходит восстановление поврежденных тканей).
- Употреблять фрукты и овощи, содержащие витамины С (шиповник, красную смородину, яблоки), В1 (орехи, фасоль), В2 (молоко, яйца) и В5 (зеленые овощи, яичный желток). Данные витамины участвуют в восстановлении тканей организма после различных повреждений.
- При развитии сердечной недостаточности назначается диета (стол) номер 10 по Певзнеру, при этом рекомендуется потреблять не более 3 – 5 г соли в сутки (включая соль в различных продуктах питания). Это объясняется тем, что соль задерживает жидкость в организме, тем самым увеличивая объем циркулирующей крови и нагрузку на сердце.
Основными показаниями к хирургическому лечению при ревматической лихорадке являются развившиеся пороки сердца (стеноз и/или недостаточность митрального и/или аортального клапанов), при которых нарушается функция органа (развивается сердечная недостаточность, отек легких). Вид хирургического вмешательства зависит от типа порока сердца и общего состояния пациента (операция производится только при отсутствии активного воспалительного процесса).
Для устранения клапанных пороков сердца может применяться:
- Баллонная вальвулопластика. Через артерию вводится катетер с баллончиком на конце. Когда баллончик оказывается на уровне пораженного (стенозированного) клапана – в него накачивается воздух, в результате чего спайки и рубцы на створках клапана разрываются.
- Открытая вальвулопластика. Через разрез в передней стенке грудой клетки производится рассечение спаек на пораженном клапане (при его стенозе). Частота рецидивов поражения клапана после данного метода довольно высока.
- Протезирование клапана. Производится удаление пораженного клапана и пересадка нового, механического либо биологического (от свиньи, коровы либо от доноров).
Изменения в суставах при ревматической лихорадке носят обратимый характер, поэтому их хирургическая коррекция требуется в исключительно редких случаях.

Опасными осложнениями ревматической лихорадки являются:
- Стеноз или недостаточность клапанов сердца. Один или несколько клапанных пороков развивается более чем у 60% людей, впервые перенесших ревматическую лихорадку, в то время как после рецидива данный показатель приближается к 90%.
- Аритмия. Нарушение ритма и частоты сердечных сокращений может возникать из-за формирования рубцов непосредственно в миокарде, что нарушает распространение нервных импульсов по сердечной мышце и ток крови в ней.
- Хроническая сердечная недостаточность. Развивается в результате выраженных повреждений сердечной мышцы или клапанного аппарата, при которых сердце оказывается не в состоянии перекачивать необходимые объемы крови. При этом состоянии кровь скапливается в венах организма и может выходить из сосудистого русла, что проявляется отеками ног, увеличением печени, одышкой, отеком легких и другими симптомами.
- Тромбоэмболия (закупорка просвета артерии тромбом). Нарушение целостности эндокарда предрасполагает к тромбообразованию. Иногда тромбы могут отрываться от эндокарда и с током крови разноситься по всему организму, застревая в артериях мелкого диаметра и закупоривая их. Это приводит к инфаркту (гибели участка ткани, который кровоснабжался пораженной артерией) и формированию рубца. При множественных инфарктах какого-либо органа его функция значительно снижается, что может проявляться соответствующими симптомами. Наиболее опасной считаются тромбоэмболия легочной артерии, сосудов головного мозга и почек, которые могут привести к смерти больного.
Ревматическая лихорадка у детей и подростков характеризуется:
- Обязательным наличием инфекции верхних дыхательных путей (ангины, скарлатины, фарингита) за 2 – 3 недели до начала заболевания.
- Выраженным повышением температуры (до 39 – 41ºС). Ребенок становится вялым, плаксивым, жалуется на сильные головные боли и боли в мышцах.
- Более тяжелым течением у девушек в подростковом возрасте (от 14 до 17 лет), чем у детей и взрослых. Это связано с особыми изменениями (нервными и эндокринными), происходящими в женском организме в период полового созревания.
- Быстрым формированием клапанных пороков сердца. Почти в 70% случаев первая атака острой ревматической лихорадки сочетается с кардитом (поражением сердца) и осложняется развитием митрального стеноза (сужения левого предсердно-желудочкового отверстия).
- Частым вовлечением суставов в воспалительный процесс (отеком, покраснением, болезненностью при движениях), причем одновременно поражаются как крупные (коленные и локтевые), так и мелкие суставы кистей и стоп.
- Поражением центральной нервной системы при первом обострении заболевания (отмечается более чем у 25% подростков).
- Трудностями в лечении подростков, связанными с нетипичными реакциями их организма на принимаемые медикаменты, частым нарушением режима лечения, отказом от приема лекарственных средств. Этим обусловлен тот факт, что рецидивы ревматической лихорадки у подростков наблюдаются почти в два раза чаще, чем у детей и взрослых.
Все дети после первой атаки острой ревматической лихорадки должны принимать профилактические дозы пенициллинов длительного действия до 21 года, а иногда и дольше.

Сразу после установления диагноза инфекции верхних дыхательных путей необходимо назначить антибиотики широкого спектра действия и взять мазок со слизистой носоглотки с целью определения конкретного микроорганизма, вызывавшего заболевание. Также в лаборатории проводится антибиотикограмма (определение чувствительности бактерии к различным антибиотикам), на основании результатов которой подбирается наиболее эффективный антибактериальный препарат.
| Название медикамента | Механизм лечебного действия | Способ применения и дозы |
| Амоксициллин | Пенициллиновые антибиотики широкого спектра действия. Нарушают синтез клеточной стенки бактерий, что приводит к их гибели. | Внутрь, после еды, не менее 10 дней подряд. |
Рекомендуемые дозы:
- Детям – 250 мг 3 раза в сутки.
- Взрослым – 500 мг 3 раза в сутки.
Рекомендуемые дозы:
- Детям с весом до 25 кг – по 125 мг 3 раза в сутки.
- Детям с весом более 25 кг – 250 мг 3 раза в сутки.
- Взрослым – 500 мг 3 раза в сутки.
Рекомендуемые дозы:
- Детям с весом до 25 кг – 600 тысяч ЕД (единиц действия).
- Детям с весом более 25 кг – 1,2 миллиона ЕД.
- Взрослым – 2,4 миллиона ЕД.
Рекомендуемые дозы:
- Детям – 12 миллиграмм на килограмм массы тела в сутки за 1 прием.
- Взрослым – в первый день лечения 500 мг (за 1 прием), а в дальнейшем по 250 мг 1 раз в день.
Длительность лечения 5 – 7 дней.
Рекомендуемые дозы:
- Взрослым – по 150 мг каждые 6 часов.
- Детям – по 7 мг/кг 3 раза в сутки.
Длительность лечения не менее 10 дней подряд.

При вторичной профилактике обычно используется бензатина бензилпенициллин (синонимы: экстенциллин, ретарпен), который назначается:
- Детям с весом менее 25 кг – в дозе 600 000 ЕД.
- Детям с весом более 25 кг – в дозе 1 200 000 ЕД.
- Взрослым – в дозе 2 400 000 ЕД.
| Особенности течения РЛ | Рекомендуемая длительность профилактики |
| Во время первой атаки заболевания не отмечалось клинических и лабораторных признаков поражения сердца (кардита). |
|
| Во время первой атаки имелись признаки кардита, но клапанный порок сердца (стеноз и/или недостаточность одного из клапанов) не сформировался. | В течение 10 лет либо до 21 года (по принципу «что дольше»). |
| После острого периода заболевания сформировался клапанный порок сердца. | Не менее 10 лет после последнего обострения заболевания, иногда пожизненно (если после отмены профилактики отмечаются рецидивы). |
Если у больного, перенесшего ревматическую лихорадку, сформировался клапанный порок сердца, то ему необходимо принимать антибиотики в профилактических целях каждый раз, когда производятся различные медицинские манипуляции, связанные с риском инфицирования (стоматологические процедуры, эндоскопические исследования желудочно-кишечной или мочеполовой систем). С этой целью обычно назначается антибиотик амоксициллин в дозе 2 грамма для взрослых или 50 мг/кг для детей. Препарат назначается однократно (внутрь, внутримышечно или внутривенно), за 30 – 40 минут до проведения медицинской процедуры.

В зависимости от времени появления различают:
- впервые возникшую ревматическую лихорадку;
- повторную ревматическую лихорадку (рецидив).
В зависимости от преобладающих клинических проявлений различают:
- Латентное (скрытое) течение – клинические проявления заболевания отсутствуют, однако в крови определяются антитела к В-гемолитическому стрептококку (бактерии, являющейся причиной развития заболевания) – антистрептолизин-О, антистрептокиназа, антистрептогиалуронидаза и другие.
- Ревмокардит – поражение сердца, обусловленное действием антистрептококковых антител.
- Артрит – поражение суставов с вовлечением или без вовлечения сердца.
- Малую хорею – нарушение функции центральной нервной системы (ЦНС), которое может сочетаться с поражением других систем либо быть единственным проявлением заболевания.
- Поражение кожи и мягких тканей – кольцевидную эритему, подкожные узелки.
- Артралгию – характеризуется болезненностью в суставах, без других проявлений заболевания.
- Поражение внутренних органов (абдоминальный синдром).
В зависимости от выраженности воспалительного процесса различают ревматическую лихорадку минимальной, умеренной и высокой степени активности.
| Степень активности | Клинические проявления | Лабораторные проявления |
| Минимальная | Характеризуется легкими клиническими проявлениями заболевания, которые полностью исчезают после завершения лечения. Прогноз благоприятен (при своевременном и адекватном лечении наблюдается полное выздоровление). |
|
| Умеренная | Характеризуется поражением сердца, суставов и других систем. Почти всегда формируются клапанные пороки сердца. |
|
| Высокая | Характеризуется выраженным повышением температуры (более 40 ºС), тяжелым ревмокардитом и признаками сердечной недостаточности II – IV степени. Прогноз неблагоприятен. |
|
Исходом ревматической лихорадки может быть:
- Выздоровление (полное исчезновение всех симптомов заболевания после проведения лечения и отсутствие осложнений).
- Хроническая ревматическая болезнь сердца без клапанного порока.
- Хроническая ревматическая болезнь сердца с клапанным пороком.
Кроме этого, при формулировке диагноза обычно указывается степень сердечной недостаточности (I, II, III или IV), определяемая в зависимости от характера поражения сердца и его функциональных возможностей.

Наиболее опасным во время беременности (с точки зрения развития осложнения) считается наличие клапанных пороков сердца. Они формируются при поражении эндокарда (внутренней оболочки сердца), что приводит к снижению функциональной активности сердечной мышцы и нарушению циркуляции крови во всем организме.
Ревматическая лихорадка может осложниться:
- Митральным стенозом – сужением просвета митрального клапана, пропускающего кровь из левого предсердия в левый желудочек.
- Митральной недостаточностью – неполным смыканием створок митрального клапана при его закрытии.
- Аортальным стенозом или недостаточностью – поражением клапана аорты, который пропускает кровь из левого желудочка сердца в аорту (самую крупную артерию организма) и далее в системный кровоток.
Так как во время беременности (и особенно во время родов) нагрузка на сердце женщины увеличивается в несколько раз, наличие описанных выше поражений может привести к развитию острой сердечной (левожелудочковой) недостаточности и отеку легких, что часто заканчивается смертельным исходом.
| Беременность и роды допускаются без ограничений | Беременность и роды допускаются при условии, что женщина будет наблюдаться в специализированном отделении стационара | Беременность и роды абсолютно противопоказаны |
|
|
|
При выявлении признаков сердечной недостаточности легкой степени в третьем триместре беременности поднимается вопрос о кесаревом сечении с целью предотвращения чрезмерных нагрузок на сердце, которые переносит женщина во время естественных родов. Срок операции определяется врачами индивидуально в зависимости от состояния женщины.
Если при наличии абсолютных противопоказаний женщина настаивает на сохранении беременности, она должна быть госпитализирована в специализированное кардиоакушерское отделение, где будет проводиться специфическое лечение на протяжении всей беременности, а при необходимости могут быть оказаны реанимационные мероприятия.
Беременные женщины, хотя бы раз в жизни перенесшие ревматическую лихорадку, но не имеющие абсолютных противопоказаний к беременности, должны систематически госпитализироваться и обследоваться, чтобы врачи могли вовремя обнаружить и предотвратить различные осложнения.
| Период госпитализации | Цель госпитализации |
| 8 – 12 недели беременности | Выявление пороков сердца и оценка резервов сердечно-сосудистой системы (то есть определяется, сможет ли женщина выносить и родить ребенка). При необходимости на данном этапе может быть поднят вопрос о прерывании беременности по медицинским показаниям. |
| 28 – 32 недели беременности | Женщина госпитализируется в кардиоакушерское отделение, где повторно оценивается функциональное состояние сердечно-сосудистой системы и проводится укрепляющее и поддерживающее лечение. |
| С 34 недели до родов | На данном этапе решается вопрос о способе родоразрешения (через естественные родовые пути или с помощью кесарева сечения). |
Выписывать женщину из роддома рекомендуется не ранее, чем через 2 недели после родов (или кесарева сечения), так как к этому времени нормализуется работа сердечно-сосудистой системы и снижается риск развития осложнений.
В любом случае, женщине, хотя бы раз в жизни перенесшей ревматическую лихорадку, рекомендуется принимать профилактические дозы пенициллинов длительного действия до наступления беременности. С этой целью назначается бензатина бензилпенициллин в дозе 2,4 миллиона единиц действия. Препарат вводится внутримышечно, 1 раз в 3 недели, что предупреждает инфицирование В-гемолитическим стрептококком (бактерией, вызывающей обострение заболевания).
источник