Вирусный гепатит А (болезнь Боткина) является острой энтеровирусной инфекцией с преимущественно фекально-оральным механизмом заражения («болезнь грязных рук»). Причиной инфекции является вирус гепатита А (HAV — Hepatitis A virus, ВГА). Заболеванию подвержены все люди, не имеющие антитела к вирусу гепатита А. Почти все заболевшие выздоравливают, после заболевания у них вырабатывается стойкая невосприимчивость к повторным заражениям. В редких случаях регистрируются молниеносные формы заболевания, нередко заканчивающиеся смертельным исходом. Болезнь Боткина тяжело протекает у детей грудного возраста и пожилых людей.
Ежегодно в мире регистрируется около 1,4 млн. случаев заболевания, которое наиболее распространено среди детей 4 — 15 лет. Среди всех вирусов HAV считается одним из самых устойчивых к воздействию факторов внешней среды. Основным источником инфицирования является больной в острой фазе заболевания. Опасность представляют больные со стертыми и безжелтушными формами гепатита. В организм человека вирусы попадают с загрязненной водой и продуктами питания, существуют так же контактно-бытовой и половой механизмы заражения. Способствуют распространению гепатита А антисанитария и ненадлежащая личная гигиена. Заболевание широко распространено в странах Азии, Южной Америки, Средиземноморья и Африки. Безопасное водоснабжение, безопасность пищевых продуктов, соблюдение правил личной гигиены и вакцинация — основные меры профилактики гепатита А.
Вирус гепатита А является гепатотропным. Он способен размножаться только в клетках печени. Обладает слабым повреждающим действием. На его долю приходится до 50% всех вирусных гепатитов.
Возбудитель гепатита А относится к семейству Picornaviridae (пикорнавирусы), роду Hepatovirus. По морфологии близок к энтеровирусам. HAV — это РНК-содержащий вирус 72-го типа, организован просто, имеет один вирусоспецифический антиген.
Предположение о том, что «желтуха» (гепатит А) имеет инфекционную природу, сделал С. П. Боткин в 1888 году. Вирусная природа заболевания впервые была доказана в 1937 году американскими учеными Д. Финдлеем и Ф. Мак Коллюмом. Сам вирус выделен совсем недавно — в 1979 году С. Фейстоуном из фекалий больных с применением метода иммунной электронной микроскопии.
HAV — просто организованный вирус.
- Зрелые вирионы имеют сферическую форму с кубическим типом симметрии (икосаэдр), размером 25 — 27 нм.
- Геном представлен однонитчатой несегментированной молекулой +РНК, находящейся в центре вириона. Имеет белок VPg.
- Поверхность капсида не имеет выступов, состоит из 32 капсомеров. Суперкапсид отсутствует.
- В составе вирусов находятся структурные белки в количестве 4-х: VP1, VP2, VP3, VP4.
Рис. 2. Схема строения HAV (вируса гепатита А).
Репродукция вирусов гепатита А происходит в цитоплазме печеночных клеток. Прямое повреждающее воздействие усиливается иммунными механизмами. Геномная +РНК на рибосомах печеночных клеток связывается и транслируется в полипептид-предшественник, который в последствии нарезается протеазами (ферментами) на отдельные фрагменты Р1 — Р3, являющиеся предшественниками структурных белков VР1 — VР4. Из фрагмента Р3 образуются неструктурные белки РНК: зависимая РНК-полимераза и протеаза. Под воздействием РНК-полимеразы нить +РНК подвергается транскрипции (переписыванию) в комплементарную -РНК, которая будет служить матрицей для синтеза +РНК — точной копии вирусного генома. Далее происходит сборка вирусных частиц и выход вирионов из клетки.
Вирус гепатита А имеет один антиген (НА-антиген), по которому проводится его идентификация. Вирусспецифический антиген имеет, как и все антигены, белковую природу.
Вирусы HAV не культивируются на обычных питательных средах, так как они репродуцируются в цитоплазме печеночных клеток. В культурах клеток репродуцируются с трудом. В основном, это перевиваемые линии клеток почек обезьян (зеленых мартышек) и человека. В эксперименте инфекция воспроизводится только на обезьянах павианах, мармозетах, шимпанзе и гамадрилах. НAV не обладают выраженным цитопатическим эффектом.
Вирусы гепатита А обладают повышенной устойчивостью к факторам внешней среды:
- воздействию детергентов и растворителей;
- низким температурам;
- устойчивы в средах с низким рН (кислые среды);
- долгое время сохраняются в водопроводной воде, сточных водах, на пищевых продуктах и объектах внешней среды;
- в культурах клеток вирусы сохраняют инфекционность 4 — 12 часов при температуре +60 0 С.
- HAV проявляют чувствительность к хлору, формалину и УФО;
- в течение 5 минут погибают при кипячении;
- при автоклавировании (120 0 С) погибают в течение 20 минут, при воздействии сухого жара при 180 0 С погибают в течение часа.
Рис. 3. На фото возбудители гепатита А — HAV.
Болезнь Боткина является классическим антропонозом. Человек является единственным резервуаром (источником) инфекции. HAV интенсивно выделяются с калом во внешнюю среду в конце инкубационного периода и до развития желтухи. Заразными являются больные с безжелтушными и стертыми формами заболевания, что особенно часто встречается среди детей. С появлением желтухи заразность больных уменьшается.
Способствует распространению заболевания высокая устойчивость HAV во внешней среде. В России пик заболеваемости гепатитом А приходится на октябрь-январь месяцы.
Рис. 5. На фото вирусы гепатита А (вид в электронном микроскопе).
Механизм заражения гепатитом А фекально-оральный. Пищевые продукты, в том числе те, которые не подвергаются до продажи термической обработке (замороженные фрукты и овощи, морепродукты и др.), загрязненная фекалиями вода, грязные руки и обсемененные предметы быта, в том числе детские игрушки — основные факторы передачи инфекции. Вирусы могут передаваться при употреблении инъекционных наркотиков и половых контактах.
Рис. 6. В экономически и социально неразвитых странах с низким уровнем санитарной гигиены инфицирование вирусами происходит уже в раннем детстве.
Случаи гепатита А и эпидемии заболевания регистрируются во всех странах мира. В Европейских странах 80% населения до 40 лет имеет сывороточные антитела против HAV. В экономически и социально неразвитых странах с низким уровнем санитарной гигиены инфицирование вирусами происходит уже в раннем детстве. В ряде стран до 100% населения имеют в крови защитные антитела. Широкое распространение HAV регистрируется в странах Африки, Латинской Америки и Юго-Восточной Азии. Способствуют распространению заболевания массовая миграция, туризм, дефицит воды, плохое системное водоснабжение и канализация, низкий уровень гигиены населения.
В РФ распространению инфекции способствует высокий уровень организации детей (детские ясли и сады, школы-интернаты, спортивные лагеря) и миграционные процессы.
Рис. 7. Географическое распространение гепатита А.
Гепатит А протекает поэтапно:
- В организм человека вирусы гепатита А попадают, в основном, с пищей или водой. Размножаются в эпителиальных клетках кишечника и лимфоидной ткани.
- Далее возбудители попадают в кровь, вызывая кратковременную вирусемию. Их максимальное количество в крови регистрируется в конце инкубационного периода и начальном периоде заболевания.
- Из крови HAV проникают в клетки печени, где интенсивно размножаются, вызывая острый диффузный гепатит. Цитопатогенный эффект при этом выражен слабо. Не исключается возможность повреждения клеток печени натуральными киллерами — NK-клетками. У больных развивается желтуха и повышается уровень трансаминаз. До появления желтухи вирусы в огромном количестве выделяются с желчью в 12-и перстную кишку и далее с калом наружу. При появлении желтухи интенсивность выделения HAV снижается (эпидемический парадокс).
- В большинстве случаев под воздействием иммунной системы (антител) репликация вирусов прекращается и наступает выздоровление. Тяжелые (молниеносные) формы и летальный эффект регистрируются крайне редко.
- Иммунитет после перенесенного заболевания стойкий, пожизненный, связан с IgG. IgM появляются в сыворотке крови вначале заболевания и исчезают через 3 — 4 месяца. Параллельно развитию гуморального, в кишечнике развивается местный иммунитет (синтезируются секреторные иммуноглобулины SIgA.
Рис. 4. Гепатит А (болезнь Боткина) называют «болезнью грязных рук».
источник
1.Таксономия, классификация
Гепатит А(инфекционный гепатит, эпидемический гепатит, болезнь Боткина, катаральная желтуха) — острое инфекционное антропонозное заболевание с фекально-оральным механизмом передачи, характеризующееся преимущественным поражением печени и проявляющееся клинически гепатомегалией, интоксикацией и желтухой.
Вирус гепатита А (ВГА, HAV) относится к семейству Picornaviridae,роду Hepatovirus(ранее этот вирус считался серотипом 72 рода Enterovirus).
2. Морфология, размеры, особенности генома
Строение вириона. Диаметр вириона равен 27 нм, капсид имеет икосаэдрический тип симметрии (рис. 23), содержит 60 капсомеров и не имеет наружной суперкапсидной оболочки, поэтому не содержит липидов и углеводов. Каждая структурная единица капсида (протомер) построена из 4-х полипептидов: VP1, VP2, VP3, VP4, из них VP1, VP2, VP3 располагаются на поверхности вириона, a VP 4, вероятно, лежит внутри вирусной частицы и имеет тесный контакт с геномной РНК.
Рис. 23 Схема вируса гепатита А
Геном вируса представлен линейной однонитевой молекулой плюс-РНК, выполняющей также функции информационной РНК и обладающей инфекционностью.
Антигены. В антигенном отношении ВГА является однородным, его антигенная активность обусловлена тремя поверхностными капсидными белками, которые представляют собой единый вирусспецифический антиген вируса гепатита A (HAV-Ag).
Резистентность. ВГА относительно устойчив к низким значениям рН (до 1.0), низким температурам (при -20°С сохраняется годами), жирорастворителям (эфиру, хлороформу, детергентам), высушиванию. При комнатной температуре вирус выживает несколько недель.
Чувствителен к формалину (0,35%), хлору, ультрафиолетовым лучам. Вирус инактивируется при 60°С в течение нескольких часов, полностью теряет свою инфекционность при автоклавгировании (120°С) за 20 мин, при обработке сухим жаром (180°С) — через 1час.
3.Этапы репродукции
Репродукция. Вирус размножается в организме обезьян шимпанзе и мармозет, а также в отдельных первичных и перевиваемых линиях культур клеток человека и обезьян, в которых происходит репродукция лабораторных и вакцинных штаммов вируса гепатита А, но использование культур клеток для выделения вируса из клинического материала затруднено.
Считается, что цикл репродукции ВГА сходен с репродукцией других пикорнавирусов. Первично вирион взаимодействует со специфическими рецепторами на плазматической мембране чувствительных клеток (эпителиоциты, гепатоциты) и проникает в их цитоплазму, при этом теряется капсид и вирусная РНК освобождается.
Далее геномная РНК связывается с рибосомами клетки и транслируется с образованием гигантского белка-предшественника. Этот полипептид нарезается протеазами на три фрагмента: PI, P2 и РЗ. Фрагмент Р1 является предшественником для структурных белков (VP1 — VP4), из РЗ образуются неструктурные вирусспецифические белки — протеаза и РНК-полимераза, фрагмент Р2 разрушается.
В дальнейшем РНК-полимераза обеспечивает синтез дочерних геномов вируса. При этом вирионная плюс-РНК транскрибируется в комплементарную минус-РНК, которая и служит матрицей для синтеза дочерних геномов. Процесс репликации РНК идет на гладком эндоплазматическом ретикулуме.
При накоплении достаточного количества структурных белков и вирусных дочерних геномов на мембранах эндоплазматического ретикулума осуществляется самосборка вирионов (идет упаковка плюс-РНК в белковые капсиды).
Выход вируса из клетки осуществляется путем экзоцитоза и, возможно, при разрушении гепатоцитов цитолитическими Т-лимфоцитами.
4. Эпидемиология
Гепатит А является антропонозной инфекцией, преимущественно поражает детей. Распространен повсеместно. Характеризуется сезонностью с максимумом заболеваемости в осенне-зимний период, периодичностью с циклами подъема заболеваемости. Для гепатита А характерны отдельные вспышки, мелкие и средние, реже крупные эпидемии. В странах с высоким уровнем общественной гигиены и санитарной культуры заболеваемость гепатитом А ниже, чем в развивающихся странах. Летальность не превышает 0,1 — 0,5%.
Источником и резервуаром инфекции служат больные в инкубационном периоде желтушной и безжелтушной формы инфекции. Наиболее заразительны больные в последние 7-10 дней инкубационного периода и в течение 2-х недель преджелтушного периода заболевания. В это время наблюдается массированное выделзние вируса с фекалиями, которое прекращается в период разгара заболевания (желтушный период).
Основной механизм передачи при гепатите А — фекально-оральный. Заражение происходит через контаминированную вирусами воду, пищу и контактным путем. Передача вируса возможна от больных и через кровь в период вирусемии при проведении парентеральных манипуляций.
5. Клинические проявления
Входными воротами для ВГА являются слизистые ротоглотки и тонкого кишечника, в эпителиоцитах которых, возможно, происходит первичная репродукция, откуда вирус проникает в мезентериальные лимфатические узлы и далее в кровь, вызывая кратковременную вирусемию. С кровотоком через портальную вену вирус заносится в печень, где активно размножается в гепатоцитах.
Поражение клеток печени при гепатите А обусловлено клеточными цитотоксическими иммунными реакциями, их сущность заключается в том, что вирусные антигены появляются на мембране гепатоцитов вместе с антигенами главного комплекса гистосовместимости (HLA) 1-го типа. Далее пораженные вирусом клетки узнаются цитотоксическими Т-лимфоцитами и уничтожаются. Таким образом, организм освобождается от вируса, уничтожая клетки, пораженные ВГА. Но не исключается и частичное прямое цитопатическое действие этого вируса на клетки печени.
Гибель гепатоцитов ведет к развитию воспалительных и некробиотических процессов и, как следствие, к снижению дезинтоксикационной и барьерной функций печени.
Основными признаками вирусного гепатита А являются дистрофические изменения клеток печени, набухание гепатоцитов, отек портальных трактов. В тяжелых случаях развиваются некрозы. Воспалительные некробиотические процессы приводят к возникновению цитолитического, мезенхимально-воспалительного и холестатического клинико-биохимических синдромов.
Клиника. При типичном течении гепатита А характерна четкая смена периодов: инкубационный, продромальный (преджелтушный), разгар болезни (желтушный период) и реконвалесценция.
Инкубационный период при гепатите А продолжается в среднем 21-28 дней, а продромальный период 2-14 дней и характеризуется катаральными и диспептическими явлениями с токсическим синдромом. Разгар болезни продолжается в среднем 2-3 недели и знаменуется появлением желтухи.
Далее заболевание переходит в стадию реконвалесценции продолжительностью 1-12 месяцев, во время которой происходит постепенное угасание всех клинических симптомов. Болезнь, как правило, заканчивается полным выздоровлением. В результате развития иммунного ответа вирус элиминируется из организма.
Наиболее типичной формой является острая желтушная циклическая форма, возможен безжелтушной и бессимптомный варианты гепатита А. Хронические формы и вирусоносительство гепатита А не возникают.
6. Лабораторная диагностика, характер исследуемого материала
Вирусный гепатит А диагносцируется преимущественно с помощью иммунологических методов исследования, реже применяют иммунную электронную микроскопию (ИЭМ), в последнее время начали применять ПЦР. Вирусологические исследования проводят ограничено, главным образом для научных целей, что связано с трудностью культивирования ВГА на клеточных культурах.
Исследуемый материал — сыворотка крови, фекалии, реже моча икровь.
На ранней стадии заболевания — в продромальном (безжелтушном) периоде обнаруживают вирусспецифические антигены и/или антитела класса IgM в сыворотке крови.
ВГА-антиген (HAV-Ag) выявляют в фильтрате фекалий, используя соответствующую тест-систему ИФА или РИА.
ИЭМ, основанная на связывании специфических антител с находящимися в фекалиях вирусами и последующим образовании агрегатов вирионов, выявляемых при электронноскопии, в настоящее время применяется реже.
В то же время расширяется применение ПЦР.
Наиболее распространенным и доступным способом диагностики, позволяющим диагносцировать гепатит А как в раннем периоде, так и в более поздние сроки, является серологическое исследование испытуемой сыворотки с целью обнаружения антител класса IgM. Эти антитела появляются в безжелтушном периоде, их титр значительно нарастает в период разгара заболевания, а затем в течение нескольких месяцев постепенно снижается. Антитела класса IgM (ранняя диагностика) обнаруживаются с помощью ИФА (используя тест-систему ИФА-анти-HAV-M), применяют также РПГА и РГА.
Постановка этих же реакций с парными сыворотками позволяет выявить четырехкратное и более увеличение титра антител, характерное для желтушного периода и реконвалесценции.
Ретроспективный диагноз, а также наличие постинфекционного иммунитета, устанавливают путем обнаружения специфических IgG антител, которые сохраняются в организме в течение многих лет.
Дата добавления: 2015-06-27 ; Просмотров: 3720 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
источник
Вирусный гепатит А-острая циклическая инфекция, характеризующаяся четкой сменой периодов.После заражения ВГА из кишечника проникает в кровь и далее в печень, где после фиксации к рецепторам гепатоцитов проникает внутрь клеток. На стадии первичной репликации отчетливых повреждений гепатоцитов не обнаруживается. Новые поколения вируса выделяются в желчные канальцы, далее поступают в кишечник и выделяются с фекалиями во внешнюю среду. Часть вирусных частиц проникает в кровь, обусловливая развитие интоксикационной симптоматики продромального периода. Повреждения гепатоцитов, возникающие в ходе дальнейшего течения ГА, обусловлены не репликацией вируса, а иммуноопосредованным цитолизом. В периоде разгара ГА морфологическое исследование позволяет выявить воспалительные и некробиотические процессы, происходящие преимущественно в перипортальной зоне печеночных долек и портальных трактах. Эти процессы лежат в основе развития трех основных клинико-биохимических синдромов: цитолитического, мезенхимально-воспалительного и холестатического. К лабораторным признакам цитолитического синдрома относятся: повышение активности ферментов АлАТ и АсАТ (аланинамино- и аспартатаминотрансферазы), уровня железа в сыворотке крови, снижение синтеза альбумина, протромбина и других факторов свертывания крови, эфиров холестерина. Начальным этапом цитолитического синдрома является повышение проницаемости мембраны гепатоцитов. Это обусловливает выход в кровь, прежде всего АлАТ — фермента, находящегося в цитоплазме печеночной клетки. Повышение активности АлАТ — ранний и надежный индикатор повреждения гепатоцита. Мезенхимально-воспалительный синдром характеризуется повышением уровня бета- и гаммаглобулинов, изменением коллоидных проб (снижение сулемового титра и повышение тимоловой пробы). Холестатический синдром проявляется повышением в крови уровня связанного билирубина, желчных кислот, холестерина, меди, активности щелочной фосфатазы, а также билирубинурией, уменьшением (исчезновением) уробилиновых тел в моче. Вследствие комплексных иммунных механизмов (усиление интерферонопродукции, активизации естественных киллеров, антителопродукции и активности антителозависимых киллеров) репликация вируса прекращается, и происходит его элиминация из организма человека. Для ГА не характерны ни длительное присутствие вируса в организме, ни развитие хронической формы болезни. Однако иногда течение заболевания может быть модифицировано в случаях ко-инфекции или суперинфекции другими гепатотропными вирусами. У лиц же с генетической предрасположенностью возможно развитие хронического активного аутоиммунного гепатита 1-го типа
Вирусный гепатит В Из места внедрения ВГВ гематогенно достигает печени, где в гепатоцитах происходит репликация вирионов. ВГВ не обладает цитотоксичностью. Сам вирус гепатита В проникнув в клетку, оставляет свой антиген на поверхности гепатоцита. Эти клетки опознаются Т-лимфоцитами как чужеродные и подвергаются агрессии. Таким образом, поражение клеток печени при гепатите В является иммуннообусловленными. Кроме этого при хроническом гепатите В в процесс вовлекаются Т-супрессоры. Они находятся в подавленном состоянии и поэтому формируются условия для развития аутоиммунных реакций, направленных против собственных клеточных антигенов.Следствием этого является развитие некробиотических и воспалительных изменений в паренхиме печени. В результате патологических изменений в печеночной ткани возникают цитолитический, мезенхимально-воспалительный и холестатический синдромы с определенными клиническими и лабораторными проявлениями .
При морфологическом исследовании обнаруживают дистрофические изменения гепатоцитов, зональные некрозы, активизацию и пролиферацию звездчатых эндотелиоцитов (клеток Купфера); в более тяжелых случаях — субмассивные и массивные некрозы печени, которые, как и распространенные «мостовидные» и мультилобулярные некрозы, являются нередко патологоанатомическим субстратом печеночной комы. Холестатические варианты ГВ сопровождаются вовлечением в патологический процесс внутрипеченочных желчных ходов с образованием в них «желчных тромбов», увеличением содержания билирубина в гепатоцитах.
В патогенезе ГВ, кроме репликативной, выделяют также интегративную форму течения инфекции. При этом происходит встраивание всего генома вируса в геном клетки хозяина или его фрагмента, отвечающего, например, за синтез HBsAg. Последнее приводит к присутствию в крови лишь HBsAg.Интеграция генома ВГВ в геном гепатоцита является одним из механизмов, обусловливающих развитие персистирующих (ациклических) форм течения ГВ и первичной гепатоцеллюлярной карциномы.
Вирусный гепатит С После проникновения в организм человека ВГС, обладая гепатотропностью, реплицируется преимущественно в гепатоцитах. ВГС обладает слабой иммуногенностью, что определяет замедленный, неинтенсивный Т-клеточный и гуморальный ответ иммунной системы на инфекцию. Так, в острой стадии ГС сероконверсия возникает на 1-2 мес. позже появления признаков цитолиза гепатоцитов (повышения активности АлАТ). Лишь через 2-10 нед. от начала заболевания в крови больных начинают определяться антитела к ядерному антигену классов M, затем G. Однако они обладают слабым вируснейтрализующим действием. Антитела же к неструктурным белкам ВГС в острой фазе инфекции обычно не выявляются. Зато в крови в течение острой стадии болезни (и при реактивации — в хронической) определяется присутствие РНК вируса. Устойчивость ВГС к специфическим факторам иммунитета обусловлена его высокой способностью к «ускользанию» из-под иммунологического надзора. Таким образом, слабость иммунного реагирования и мутационная изменчивость вируса во многом обусловливают высокий хрониогенный потенциал данного заболевания.
Вирусный гепатит D Этот вирус является дефектным, так как он на своей поверхности не имеет рецепторов для гепатоцитов. Поэтому он не может проникнуть в клетку и реплицироваться в ней. Для репродукции данного вируса необходимо участие «вируса-помощника». Роль этого помощника играет вирус гепатита В. таким образом, заболевание может возникнуть при одновременном заражении обоими вирусами или при инфицировании лиц уже имеющих вирус гепатита В (суперинфекция). Сочетанное действие обоих вирусов приводит к развитию более тяжелых форм заболевания с выраженными явлениями печеночно-клеточной недостаточности. В большинстве случаев заболевание приобретает прогрессирующее течение с быстрым переходом в цирроз печени и смертью.
Вирусный гепатит Е изучен недостаточно. Большинство исследователей полагают, что центральным звеном патогенеза является цитопатическое действие вируса. Не исключается и участие иммунных механизмов в некробиотических изменениях печеночной ткани.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Многие вопросы патогенеза гепатита А до настоящего времени окончательно не решены. В общей патогенетической концепции, которую можно принять за основу, допускается существование прямого цитопатического действия вируса гепатита А непосредственно на паренхиму печени.
Заражение практически всегда происходит через рот. Вирус со слюной, пищевыми массами или водой проникает вначале в желудок, а затем в тонкую кишку, где, по-видимому, внедряется шли всасывается в портальный кровоток. Ответить на вопрос, что происходит с вирусом в желудке, а .затем в тонкой кишке, не представляется возможным. Можно допустить, что в некоторых случаях действие желудочною сока оказывается губительным для вируса и, следовательно, возможна полная санация от возбудителя уже на уровне заражения. Однако такой исход заражения хотя теоретически и возможен, но все же маловероятен, поскольку вирус гепатита А подобно другим энтеровирусам, устойчив в диапазоне pH 3,0-9,0, что гарантирует ему выживание, дальнейшее продвижение в двенадцатиперстную кишку, а затем и в тонкий отдел кишечника. По современным представлениям, вирус гепатита А в тонкой кишке не задерживается и, тем более, не оказывает на слизистую оболочку повреждающего действия. Эта фаза патогенетической цепи (энтеральная), по-видимому; больше свойственна вирусным гепатитам животных.
Механизм проникновения вируса гепатита А из кишечника в кровь точно не известен. Более вероятно активное внедрение вируса через слизистую оболочку в лимфатическую систему, а затем в регионарные лимфатические узлы, но не исключена возможность пассивного транспорта с участием особых «переносчиков», облегчающих проникновение вируса через липидную мембрану.
Однако независимо от механизма проникновения через стенку тонкой кишки вирус, скорее всего, не задерживается в регионарных лимфатических узлах и, тем более, не размножается, как это предполагалось до недавнего времени, а довольно быстро оказывается в общем кровотоке и паренхиме печени. Эту фазу патогенетической цепи условно можно назвать паренхиматозной диффузией. О механизме проникновения вируса гепатита А в печеночную паренхиму существуют различные представления. Широко распространенное мнение о первичном поражении вирусом гепатита А ретикулоэндотелиальной системы печени в настоящее время можно считать ошибочным. По современным представлениям, вирус сразу проникает в гепатоциты, где находит оптимальные условия для размножения. Высказывается мнение, что проникновение вируса через мембрану гепатоцита может осуществляться путем пиноцитоза, но более вероятен активный процесс через родственный рецептор. Наличие таких рецепторов на мембране гепатоцитов будет означать восприимчивость конкретного индивидуума к инфекции гепатита А, тогда как их отсутствие, наоборот, полную невосприимчивость. Такое направление в научных исследованиях авторам этой книги кажется особенно перспективным.
Внутриклеточно расположенный вирус начинает взаимодействовать с биологическими макромолекулами, принимающими участие в процессах детоксикации. Следствием такого взаимодействия является высвобождение свободных радикалов, выступающих инициаторами процессов перекисного окисления липидов мембран клеток. Усиление процессов перекисного окисления липидов приводит к изменению структурной организации липидных компонентов мембран за счет образования гидроперекисных групп, что обусловливает появление «дыр» в гидрофобном барьере биологических мембран и, следовательно. повышение их проницаемости. Возникает центральное звено в патогенезе гепатита А — синдром цитолиза. Становится возможным движение биологически активных веществ по градиенту концентрации. Поскольку концентрация ферментов внутри гепатоцитов в десятки и даже сотни тысяч раз превышает их содержание во внеклеточном пространстве, в сыворотке крови повышается активность ферментов с цитоплазматической, митохондриальной, лизосомальной и другой локализацией, что косвенно указывает на снижение их содержания во внутриклеточных структурах, а следовательно, на пониженный биоэнергетический режим химических превращений. Нарушаются все виды обмена (белковый, жировой, углеводный, пигменгный и др.), вследствие чего возникает дефицит богатых энергией соединений, а биоэнергетический потенциал гепатоцитов падает. Нарушается способность гепатоцитов синтезировать альбумин, факторы свертывания крови (протромбин, проконвертин, проакцелерин, фибриноген и др.), различные витамины; ухудшается использование глюкозы, аминокислот для синтеза белка, сложных белковых комплексов, биологически активных соединений; замедляются процессы переаминирования и дезаминирования аминокислот; возникают затруднения в экскреции конъюгированного билирубина, эстерификации холестерина и глюкуронизации многих соединений. Все это свидетельствует о резком нарушении детоксицирующей функции печени.
Повышенная проницаемость всех субклеточных мембран, надо полагать, приводит к замене внутриклеточного калия ионами натрия и кальция в митохондриях, что еще больше усиливает «поломки» в системе окислительного фосфорилирования и способствует развитию внутриклеточного, а затем и внеклеточного ацидоза — накоплению Н-ионов.
Изменившаяся реакция среды в гепатопитах и нарушение структурной организации субклеточных мембран приводят к активации кислых гидролаз (РНК-азы, лейцинаминопептидазы, катепсинов О, В, С и пр.), чему в известной степени способствует и падение активности ингибитора протеолиза а2-макроглобул. Завершающим действием протеолитических ферментов становится гидролиз некротизированных печеночных клеток с возможным высвобождением белковых комплексов, которые могут выступать в роли ауто-антигенов и, наряду с гепатотропным вирусом, стимулировать Т- и В-системы иммунитета, активируя, с одной стороны, сенсибилизированные клетки — киллеры, с другой — вызывая образование специфических антител, способных атаковать паренхиму печени, Следует, однако, сказать, что механизмы аутоагрессии при гепатите А в полной мере не реализуются, поэтому тяжелые формы при этом виде гепатита встречаются редко.
Фаза реконвалесценции характеризуется реализацией факторов защиты и репаративных процессов, полной элиминацией вируса и восстановлением функционального состояния печени. Практически у всех пациентов наступает выздоровление с полным восстановлением структуры и функций органа в сроки от 1,5 до З мес от начала болезни. Только у некоторых пациентов (3-5%) первоначальные факторы зашиты могут оказаться недостаточными, и может наблюдаться относительно длительная (от 3 до 6-8 мес и дольше) репликативная активность вируса в гепатоцитах с нарушением их структуры и функции. В таких случаях формируется затяжное течение болезни с пролонгированным механизмом структурно-функциональных изменений. Однако и у этих больных в конечном итоге механизмы защиты побеждают — вирусная активность блокируется, и наступает полное выздоровление. Формирования хронического процесса в исходе инфекции гепатита А не происходит.
Приведенные данные, разумеется, не исчерпывают сложный патогенез гепатита А, при котором страдают все органы и системы. С первых дней инфицирования поражается ЦНС, о чем свидетельствует появление таких симптомов, как вялость, адинамия, головная боль, бессонница, раздражительность и другие расстройства. Причиной нарушений со стороны ЦНС служит интоксикация, возникающая, с одной стороны, в результате вирусемии и действия вируса на ЦНС, с другой — в результате распада пораженных печеночных клеток и высвобождения эндогенных токсинов, а также нарушения функциональной способности печени.
С первых дней заболевания нарушается функция ЖКТ, при этом имеется угнетение желудочной секреции и функции поджелудочной железы. Результатом этого становятся снижение аппетита, вплоть до анорексии, нередко тошнота, рвота, расстройство стула, что обычно наблюдается в самом начале заболевания.
Обобщенно можно сказать, что при гепатите А патологический процесс проходит ряд последовательных, взаимообусловленных этапов, причем на первых этапах ведущим является действие вируса, вызывающее появление общетоксического синдрома, а на последующих — обменные нарушения с возможным возникновением так называемого вторичного метаболического токсикоза. Однако, независимо от стадии заболевания, печень служит главной ареной патологического процесса.
Хотя некоторые исследователи и сообщают о прямом цитопатическом действии вируса гепатита А, но фактических материалов, подтверждающих это положение, в работах не приводится. В опытах на обезьянах и клеточных культурах показана локализация вирусного антигена в цитоплазме гепатоцитов при полном отсутствии его в ядрах. При изучении динамики размножения вируса гепатита А выявлено, что максимальная продукция внутриклеточного вирусного антигена отмечается на 3-4-й неделе от начала заражения, что совпадает с динамикой обнаружения вируса у больных. Однако полностью переносить результаты, полученные in vitro, на заболевание у человека не представляется возможным. Есть мнение, что своеобразие репродукции вируса гепатита А in vitro состоит в том, что он исключительно долго репродуцируется в культуре и у него полностью отсутствует цитопатический эффект. Если все же допустить, что вирус гепатита А не обладает цитопатическим действием, то придется признать, что поражение гепатоцитов при гепатите А связано в первую очередь с сенсибилизацией лимфоцитов к антигенам вируса-возбудителя и, возможно, денатурированным белкам гепатоцитов.
В настоящее время в патогенезе вирусных гепатитов, в том числе гепатита А, большое значение придают иммунологическим механизмам повреждения печеночных клеток. В исследованиях последних лет установлено, что поражение инфицированных печеночных клеток при гепатите А осуществляется сенсибилизированными цитотоксическими Т-лимфоцитами.
Другими дополнительными механизмами гепатодеструкции при гепатите А могут быть К-клеточный цитолиз и иммунокомплексное поражение гепатоцитов.
По нашим наблюдениям и с учетом данных литературы, можно считать, что для гепатита А востром периоде болезни характерны Т-лимфопения, Т-лимфоцитоз — активных, термостабильных и ауторозеткообразующих клеток. При этом соотношение Т-лимфоцитов с хелперной активностью и Т-лимфоцитов с супрессорной активностью снижается.
Содержание В-клеток существенно не меняется. Указанные сдвиги в показателях иммунологического реагирования существенно зависят от тяжести заболевания. Особенно значительное снижение Т-клеток отмечается при тяжелых формах болезни, и, наоборот, содержание Т-активных, Т-многорепепторных, термостабильных и ауторозеткообразующих клеток бывает тем больше, чем тяжелее патологический процесс в печени. Пропорционально нарастанию тяжести заболевания усиливается специфическая сенсибилизация к печеночному липопротеину, и возрастают показатели активности натуральных киллеров и антителозависимая клеточная цитотоксичность.
Отмеченные сдвиги иммунологического реагирования отражают адекватность иммунного ответа у больных гепатитом А, направлены на элиминацию инфицированных гепатоцитов и обеспечение полноценного иммунитета и полного выздоровления.
При развитии затяжного гепатита А отмечается более выраженное снижение числа Т-лимфоцитов при относительно слабой мобилизации функционально активных субпопуляций Т-клеток и умеренном сдвиге соотношения хелперных и супрессорных Т-лимфоцитов в сторону преобладания первых, что в конечном итоге приводит к увеличению синтеза продукции IgМ, а также повышению сенсибилизации Т-клеток к ЛП4. Такой тип иммунологического реагирования предопределяет замедленный цикл инфекционного процесса. В этих случаях можно предполагать, что антигены вируса гепатита А, расположенные на поверхности гепатоцитов, вызывают слабую активацию Т-клеток индукторов иммунного ответа и столь же слабое подавление супрессорных Т-клеток. Это взаимодействие иммунокомпетентных клеток создает условия для замедленного специфического иммуногенеза, завершающегося (через замедленный цикл) формированием достаточно стойкого протективного иммунитета.
В полном соответствии с характером клеточного иммунологического реагирования находятся изменения в механизмах иммунокомплексообразования.
Проведенные исследования показали, что у всех больных гепатитом А на высоте клинических проявлений в крови резко повышается концентрация иммунных комплексов и возрастает их комплементсвязываюшая активность. Важно отметить, что в этот период болезни в крови циркулируют преимущественно комплексы крупных размеров, в чьем составе преобладают иммуноглобулины класса М. Такие иммунные комплексы, как известно, легко связывают комплемент, быстро выводятся из организма клетками мононуклеарно-фагоцитарной системы. При гладком течении гепатита А динамика ЦИК в сыворотке крови строго коррелирует с характером патологического процесса в печени, тогда как у больных с затяжным течением болезни высокий уровень иммунных комплексов служит предвестником неблагоприятного исхода. При этом в составе ЦИК резко возрастает доля средних и мелких иммунных комплексов, обладающих слабой комплементсвязывающей активностью, и, кроме того, в их составе возрастает доля иммуноглобулинов G, что затрудняет их элиминацию клетками макрофагальной системы и, следовательно, может стать решающей причиной затяжного течения гепатита А.
Таким образом, фактические материалы позволяют считать гепатит А, как и гепатит В, иммунопатологическим заболеванием. Однако сходство этих заболеваний лишь внешнее и просматривается преимущественно по характеру иммунологического реагирования. Иммунологические сдвиги при гепатите А возникают на мембранные антигены гепатоцитов с экспрессированными вирусными антигенами, что отражает некрозогенный эффект возбудителя. Кроме того, хотя при гепатите А и возникает специфическая сенсибилизация иммунокомпетентных клеток к липопротеину гепатоцитов, но все же выраженного иммунного цитолиза гепатоцитов не происходит, поскольку вирус гепатита А не интегрируется в геном клетки. В связи с этим реакции иммунного цитолиза не пролонгированы во времени, а отражают всего-лишь адекватность иммунного ответа, способствуя быстрой элиминации инфицированных гепатоцитов и элиминации вируса, чему в известной степени способствуют также адекватные механизмы иммунокомплексообразования, обеспечивающие быстрое связывание антигенов вируса преимущественно антителами класса IgM, с образованием крупных комплексов, легко элиминирующихся макрофагальной системой, Совокупность всех этих механизмов обеспечивает самолимитируюшийся процесс без риска развития фульминантного или хронического гепатита.
По образному выражению гепатологов, патогенез вирусного гепатита — это патогенез нарушений обмена веществ. Хотя с современных позиций такое определение и нельзя признать полностью правильным, нарушения в обмене веществ играют важную роль в патогенезе заболевания.
При гепатите А нарушаются все виды обмена (белкового, жирового, углеводного, пигментного и др.). Биохимической основой этих процессов служат освобождение внутриклеточных ферментов и переход их из гепатоцитов в кровь Первоначально клетки покидают ферменты цитоплазматической локализации (AЛT, ACT, Ф-1-ФА, сорбитдегидрогенеза и др.), затем митохондриальной (глутаматдегидрогеназа, уроканиназа, малатдегидрогеназа и др.) и лизосомальной локализации (катепсины D, С, лейцинаминoneптидаза и др.). Потеря гепатоцитами ферментов, являющихся основными катализаторами обменных превращений, приводит к нарушениям окислительного фосфорилиоования, а следовательно, к снижению синтеза доноров энергии (АТФ, НАДФ и др.), что и лежит в основе прохрессируюшего нарушения обмена веществ. Снижается синтез альбумина, факторов свертывания крови, витаминов, нарушается обмен микроэлементов, гормонов, углеводов, жиров и др. Следовательно, нарушения обмена веществ при вирусных гепатитах всегда возникают вторично, вслед за массивной потерей печеночно-клеточных ферментов.
Схематично происходящее на уровне гепатоцитов можно представить как взаимообусловленный каскад обменных нарушений, проходящих три стадии: ферментативных нарушений, функциональных сдвигов, некроза и лизиса гепатоцитов с их аутолитическим распадом. Важнейшую роль в аутолитическом распаде пораженных гепатоцитов играют протеолитические ферменты, высвобождающиеся из субклеточных органелл — лизосом. Под их действием происходит распад белковых структур с высвобождением большого количества аминокислот, играющих существенную роль в возникновении симптомов интоксикации.
В механизме развития патологического процесса важную роль играют и нарушения в пигментном обмене. Известно, что печень служит важнейшим органом, осуществляющим превращения билирубина, в результате которых пигмент теряет токсические свойства и выводится из организма. В физиологических условиях билирубин образуется в ретикулоэндотелиальной сети из гемоглобина, высвобождающегося при гемолизе эритроцитов.
При вирусных гепатитах нарушения в пигментном обмене возникают прежде всего на уровне экскреции гепатоцитом связанного билирубина. При этом функции захвата и конъюгации свободного билирубина на первых этапах заболевания практически не страдают. Главной причиной нарушения экскреции билирубина следует считать поражение ферментных систем и снижение энергетического потенциала гепатоцитов. Образующийся в ходе обменных превращений связанный билирубин в конечном итоге поступает не в желчный капилляр, а непосредственно в кровь (парахолия). Другие механизмы, например механическое препятствие вследствие образования желчных тромбов или сдавление желчных ходов, при гепатите А не имеют существенного значения. Исключение составляют лишь холестатические формы болезни, при которых механические факторы могут приобретать значение в патогенезе длительно сохраняющейся желтухи.
Морфология гепатита А изучена на основании данных прижизненных пункционных биопсий печени. Изменения отмечаются во всех тканевых компонентах печени — паренхиме, соединительнотканной строме, ретикулоэндотелии, желчевыводящих путях. Степень поражения органа может варьировать от незначительных дистрофических и единичных некротических изменений эпителиальной ткани дольки печени при легких формах до более выраженных очаговых некрозов печеночной паренхимы при среднетяжелых и тяжелых формах. Распространенных некрозов печеночной паренхимы и, тем более, массивного некроза печени при гепатите А не бывает.
По характеру морфологических изменений можно различать острую и затяжную формы болезни.
При острой циклической форме в печени обнаруживается диффузное поражение гепатоцитов, эндотелиальных и мезенхимальных элементов. Отмечается пестрота микроскопических изменений за счет дискомплексации балочного строения и различного характера поражения гепатоцитов, их значительного полиморфизма: наряду с распространенными дистрофическими изменениями имеются и выраженные пронесен регенерации. Характерно наличие рассеянных по дольке некротизированных гепатоцитов, а также присутствие отдельных печеночных клеток с гомогенизированной ацидофильной цитоплазмой с пикнотичным ядром (эозинофильное тельце). Ожирения печеночных клеток не отмечается. Теряют гликоген лишь некротизированные клетки.
Изменения мезенхимальных элементов внутри дольки выражаются в пролиферации звездчатых ретикулоэндотелиоцитов (купферовских клеток) с превращением их в макрофаги, обнаруживаемые в просвете капилляров. Цитоплазма этих клеток базофильна, содержит желчный пигмент и липофусцин. Мелкие лимфогистиоцитарные скопления отмечаются на месте рассеянных по дольке некротизированных гепатоцитов. Капилляры в центре долек расширены. Строма без видимых изменений. В портальном тракте отмечается пролиферация лимфогистиоцитарных элементов с примесью плазматических клеток, эозинофилов и нейтрофилов.
Морфологические изменения в печени цикличны. К концу 1-й — началу 2-й недели болезни в портальных трактах и вокруг вегвеи печеночных вен на фоне отека соединительнотканных структур уже имеется рыхлый обильный инфильтрат. В разгаре заболевания (2-3-я неделя болезни) растет интенсивность альтеративно-дегенеративных процессов вплоть до появления очаговых некрозов с одновременным нарастанием пролиферативной реакции.
Структура паренхимы печени в этом периоде максимально нарушена за счет дискомплексации и резко выраженных дистрофических изменений печеночных клеток. В более тяжелых случаях преобладают поля «просветленных» (баллонных) клеток и обнаруживаются многочисленные мумифицированные клетки (тельца Каунсильмена). Могут определяться мелкоочаговые или даже фокальные некрозы, рассеянные по всей дольке,
При гепатите А, в отличие от гепатита В, воспалительно-дистрофические и пролиферативные изменения локализуются по периферии долек, распространяясь к центру, внутрь паренхимы, в виде тонкой сеточки и дорожек. В периферических зонах долек возможно появление многоядерных клеток со склонностью к образованию симпластоподобных структур: характерно нарастание количества плазматических клеток
В желчных капиллярах могут появляться желчные тромбы, возможны следы некоторого огрубения и коллагенизации ретикулярного каркаса, но еще по периферии долек могут сохраняться мелкие некрозы с регенератами из многоядерных клеток и разрастанием ложных желчных ходов, что следует расценивать как проявления регенерации печеночной паренхимы.
На протяжении 4-й недели некротически-дистрофические изменения паренхимы исчезают, мезенхимальная инфильтрация существенно уменьшается. Полностью исчезают «просветления» цитоплазмы (баллонная дистрофия).
В бывших очажках некроза видны зоны разрежения — «изъяны» паренхимы. Преобладают явления регенерации и восстановления.
Поданным большинства морфологов, к концу 5-6-й недели болезни исчезают все воспалительные явления, а к концу 2-3-го месяца патологический процесс в печени при гепатите А в подавляющем большинстве случаев полностью завершается. Наступает восстановление структуры и функции печени.
Степень деструктивных изменений в паренхиме печени соответствует тяжести клинических проявлений болезни.
Из внепеченочных изменений при гепатите А отмечают увеличение портальных лимфатических узлов и селезенки с ретикулярной гиперплазией стромы и миелозом пульпы селезенки. Возможны также реактивные изменения со стороны ретикулоэндотелиальной системы поджелудочной железы, почек и других органов. Описаны изменения и со стороны ЦНС.
У пациентов с легкими формами гепатита А, погибших от случайных причин, в ЦНС обнаружены циркуляторные расстройства, изменения эндотелиальных клеток, серозный и серозно-продуктивный менингит, дегенеративные изменения нервных клеток.
По данным патологов, поражение ЦНС возникает при всех вирусных гепатитах. При этом первичное воздействие вируса на ЦНС выражается поражением прежде всего эндотелия сосудов (венул). В нервных клетках появляются патологические изменения различной выраженности, вплоть до некробиоза отдельных клеток.
Высказывается мнение, что изменения со стороны ЦНС при вирусных гепатитах аналогичны гепатоцеребральному синдрому при гепатолентикулярной дегенерации.
Возбудитель гепатита А передается исключительно фекально-оральным путем, через инфицированные продукты питания, воду и посредством бытового контакта. Вирус выделяется только с фекалиями, при этом он попадает в пищу обычно при нарушении элементарных правил гигиены в момент ее обработки и приготовления; инфицирование воды происходит путем загрязнения водоисточников бытовыми сбросами.
источник
Возбудитель. HAV – РНК-содержащий вирус из группы Picornaviridae (подкласс Hepatovirus), не имеющий оболочки, диаметром 27-28 нм, с кубической симметрией (рис. 3.2). Белки капсида образуют 60 центромер. Одноцепочечная линейная молекула РНК кодирует структуру белков капсида, протеаз Р2, Р3 и РНК- полимеразы. Идентифицирован один серотип и несколько генотипов HAV.
Рис. 3.2. Схематическое изображение строения вируса гепатита А
Эпидемиология. Источником заражения является больной ОВГ А. Вирус выделяется в течение одной-двух недель преджелтушного и, по меньшей мере, одной недели желтушного периода. HAV обладает устойчивостью во внешней среде.
Механизм передачи инфекции — преимущественно фекально-оральный. Вклад парентерального (при переливании крови инфицированного донора) и полового пути (у гомосексуалистов, рассматриваемый как фекально-оральный) в общее число случаев заражения небольшой. Нельзя полностью исключить возможность воздушно-капельной передачи. Вертикальная передача вируса (от матери плоду) не установлена.
Восприимчивость к инфекции высокая. Уровень заболеваемости значительно отличается в разных регионах. В странах Восточной Европы он составляет в среднем 250 случаев на 100.000 населения в год. В северных широтах выражена сезонность заболеваемости с нарастанием в осенне-зимний период. ОВГ А регистрируется спорадически, в виде вспышек, или в виде эпидемий. Эпидемии наблюдаются в развивающихся странах с 4-5 летней периодичностью.
Основные факторы риска развития ОВГ А: перенаселенность в условиях несоблюдения правил гигиены, поездки за рубеж, контакты с больным в быту, гомосексуальные контакты, контакты с детьми из детских садов, наркомания.
Инкубационный период длится в среднем 30 дней (15-50 дней).
Патогенез. Из желудочно-кишечного тракта вирус попадает в печень. Вирионы реплицируются в цитоплазме гепатоцита и выделяются в желчь (рис. 3.3).
Рис. 3.3. Репликация HAV в клетках печени
Лизис гепатоцитов опосредован иммунным ответом на инфекцию при участии цитотоксических Т-лимфоцитов и/или механизма антителозависимой клеточно-опосредованной цитотоксичности. Предполагается, что HAV не обладает значительной прямой цитопатогенностью.
Клиническая картина. Субклиническое течение, часто под маской острого гастроэнтерита, наблюдается особенно часто у детей (до 90% случаев). У взрослых ОВГ А обычно протекает в манифестной форме. В продромальном периоде возможно появление лихорадки (до 39°С). С появлением желтухи характерно улучшение самочувствия. В острый период может наблюдаться кореподобная или сходная с крапивницей кожная сыпь. В целом, частота внепеченочных проявлений существенно ниже, чем при ОВГ В или С. В фазе реконвалесценции у незначительного числа больных появляется преходящий асцит, не являющийся неблагоприятным прогностическим признаком, а также преходящая протеинурия и гематурия. Происхождение этих симптомов не установлено.
Для ОВГ А наиболее характерно развитие холестатических форм с мучительным кожным зудом. Чаще, чем при других ОВГ, наблюдаются рецидивы, особенно в детском возрасте. Они развиваются спустя 30-90 дней от начала болезни, что связано, как предполагается, с повторным заражением или реактивацией первичной инфекции. Картина рецидива напоминает первую атаку, с повторным выделением вируса. Рецидивы заканчиваются выздоровлением, изредка сопровождаются артритом, васкулитом, криоглобулинемией. Предсказать развитие рецидива можно по отсутствию тенденции к снижению уровня АЛТ.
Серологическая диагностика (рис. 3.4). В крови, кале, дуоденальном содержимом в острый период может быть обнаружен HAAg с использованием реакции иммунофлюоресценции, метода фиксации комплемента, радиоиммунного метода или ELISA. Однако в клинической практике эти методики не нашли широкого применения.
Показатели острой инфекции:
наличие Ig M анти-
HAV
в диагностическом
титре;
обнаружение HA-Ag в кале
(в широкой практике не используется)
появление Ig G анти-HAV,
исчезновение Ig M анти-HAV
Рис. 3.4. Изменения серологических показателей при ОВГ А
Высокоспецифичные для ОВГ А анти-HAV класса IgM обнаруживаются в сыворотке на протяжении всей острой фазы болезни и в течение следующих 3-6 мес. (до года в низком титре). Анти-HAV класса IgG, по всей вероятности, обеспечивают стойкий иммунитет и сохраняются в течение всей жизни.
Течение и прогноз. Длительность заболевания в среднем составляет 6нед. Как правило, больные выздоравливают без специального лечения. Вероятность летального исхода не превышает 0,001%. Хронизация инфекции не наблюдается. Функция и гистологическая картина печени обычно нормализуется в течение 6мес.
Среди осложнений описано развитие мезангиопролиферативного гломерулонефрита с нефротическим синдромом. Имеются отдельные данные о пусковой роли ОВГ А в патогенезе аутоиммунного гепатита I типа у лиц с нарушением функции Т-супрессоров.
Профилактика. Неспецифические методы профилактики включают изоляцию больных и контактировавших с ними лиц на протяжении двух последних недель преджелтушного и одной недели желтушного периода, дезинфекцию предметов пользования больного, мытье рук, соответствующую кулинарную обработку пищи в течение всего срока болезни.
Иммунопрофилактика. Профилактические меры до контакта с больным (“отсроченный эффект”). Инактивированная HAV- вакцина. Вакцинация проводится в областях с низким и средним уровнем заболеваемости лицам, входящим в группы риска: выезжающим в эндемичные районы; пациентам, часто прибегающим к инъекциям лекарств; детям и молодым людям, проживающим в условиях скученности; военнослужащим; пациентам с хроническими заболеваниями печени; работникам лабораторий, контактирующим с HAV; гомосексуалистам; иногда — работникам детских учреждений и пищевой промышленности.
Режим введения: взрослым старше 19 лет — два введения по 1440 Elisa Units (EU) с перерывом в 6-12 мес. Детям старше 2 лет вакцинация осуществляется по трехэтапному режиму — 360 EU c перерывом в 1 и 6-12 мес. или по двухэтапному режиму — 720 EU с перерывом в 6-12 мес. Однократная вакцинация обеспечивает иммунитет в течение одного года, повторная (“усиливающая”) в течение 5-10 лет. Профилактическая эффективность — 95-100%. Иммуногенность: почти у 100% здоровых вакцина пациентов вызывает продукцию анти-HAV (у 85% пациентов в течение 15 дней). Переносимость хорошая. Нет опасности заражения других лиц после вакцинации.
Живая аттенуированная вакцина служит эффективным способом профилактики ОВГ А. Однако она еще не нашла широкого применения.
Профилактические меры после контакта с больным (“немедленный эффект”). Пассивная иммунизация сывороточным иммуноглобулином. Показания: внутрисемейные и близкие контакты с больным ОВГ А (иммунизируются в т.ч. грудные дети). Не применяется при случайных спорадических контактах вне дома. Иммунизация больших групп оправдана при реальной опасности эпидемий.
Режим иммунизации: 0,02 мл/кг вводятся в дельтовидную мышцу не позднее 14 дней после контакта с больным. Может также использоваться для быстрой иммунизации лиц, выезжающих в эндемичные районы, в дозе 0,06 мл/кг (предварительно желательно определить анти-HAV). При сохранении напряженной эпидемиологической обстановки возможна повторная иммунизация.
Эффективность — 100% в предупреждении клинически манифестных форм ОВГ А при введении до контакта и 80-90% — при введении в пределах 6 дней после контакта. Переносимость хорошая.
Возможно одновременное применение активной и пассивной иммунизации с контралатеральным введением (при выезде в эндемичные районы), а также одновременная активная вакцинация против гепатитов А и В.
источник
Определение. Доброкачественное остроциклическое энтеровирусное заболевание, характеризующееся цитопатическим действием вируса на гепатоциты и клинически проявляющееся синдромом интоксикации, гепатоспленомегалией и часто желтухой. Этиология и патогене
Определение. Доброкачественное остроциклическое энтеровирусное заболевание, характеризующееся цитопатическим действием вируса на гепатоциты и клинически проявляющееся синдромом интоксикации, гепатоспленомегалией и часто желтухой.
Этиология и патогенез. Возбудитель — энтеровирус тип 72 (род Enterovirus, семейство Picornavir >
Эпидемиология. Источником инфекции является человек с любыми проявлениями болезни. Существенная часть заразившихся переносит болезнь в бессимптомной, а потому и нерегистрируемой форме. Величина этой доли составляет у детей 90-95%, а у взрослых — 25-50%. Больной человек опасен для окружающих начиная со второй недели инкубационного периода болезни с пиком в течение первой недели болезни. Вероятность заражения с появлением желтухи значительно уменьшается: в первую неделю желтушного периода частота положительных находок составляет 30-50%, во вторую — 15-25%, позже выделение вируса наблюдается лишь у единичных больных. Хроническое носительство вируса не установлено.
Механизм передачи — фекально-оральный. Вирус выделяется с фекальными массами. Заражение людей происходит при употреблении воды и пищи, инфицированной вирусом ГА, иногда контактно-бытовым путем. Передача возбудителя через медицинский инструментарий существенного значения не имеет. Роль каждого пути передачи неодинакова в разных условиях. Водный путь, как правило, приводит к вспышкам заболевания среди лиц, пользовавшихся инфицированной водой. Пищевые вспышки чаще всего связаны с контаминацией продуктов на пищевых предприятиях персоналом с легкой формой болезни. Возможно также заражение овощей и ягод при использовании в качестве удобрения фекалий человека. Бытовой путь передачи, как правило, имеет место в условиях организованных дошкольных детских учреждений.
Проявления эпидемического процесса. Болезнь характеризуется рядом особенностей: повсеместным распространением, неравномерной интенсивностью на отдельных территориях, цикличностью в многолетней динамике, выраженной осенне-зимней сезонностью, преимущественным поражением детей дошкольного возраста, подростков и лиц молодого возраста.
Вирусный гепатит А относится к числу наиболее широко распространенных в мире кишечных инфекций. ВОЗ сообщает о приблизительно 1,4 млн. случаев гепатита А, регистрируемых ежегодно.
Наибольшая восприимчивость к ГА характерна для детей от 2 до 14 лет. Определяет уровень детской заболеваемости возрастная группа 3-6 лет, в 1998 году он составил 82,7 в 1999 году — 77,0 на 100 тыс. населения. Заболеваемость среди городского и сельского населения практически сравнялась, показатели составляют соответственно 30,0 и 32,6. В 1999 году зарегистрирована 91 крупная вспышка ВГА с числом пострадавших 1422 человека. Из них детей — 1040 человек.
В 1999 году проведено исследование на антиген вируса гепатита А 14 152 объектов внешней среды. Из них положительных 474 (3,4%); причем наибольшее число положительных результатов получено из воды источников децентрализованного водоснабжения — 9,6%, фекально-бытовых сточных вод — 6,4%, что свидетельствует о широкой циркуляции возбудителя во внешней среде [2].
Вследствие этого повышенная заболеваемость наблюдается в регионах с неудовлетворительным состоянием санитарно-коммунального благосостояния, где отмечаются эпидемические вспышки, в основном водного происхождения. В многолетней динамике характерны периодические (через 4-6 лет) подъемы заболеваемости. Последние годы характеризуются очередным подъемом заболеваемости (см. рисунок).
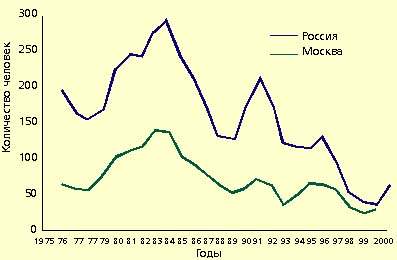 |
Подъем заболеваемости отмечен во всех возрастных группах населения, но наиболее выражен среди детей (рост — в 2,5 раза). Особенностью этого процесса в 2000 году в Москве явилось возникновение эпидемических вспышек с пищевым путем передачи. Восприимчивость к инфекции высокая, после перенесенной болезни вырабатывается стойкий напряженный иммунитет.
Клиника. Инкубационный период продолжается 3-4 недели. Начальный период заболевания (продромальный, дожелтушный) характеризуется достаточно большим разнообразием симптомов. Наиболее часто встречается лихорадочное (гриппоподобное) состояние. Одновременно больные отмечают явления дискомфорта в эпигастрии, снижение аппетита, тошноту, иногда рвоту, возникающую чаще после приема пищи. Возможны и другие проявления, в том числе по астеновегетативному варианту. В ряде случаев уже в этом периоде можно обнаружить увеличенную в размере печень и повышение показателей аминотрансфераз. Продолжительность начального периода в среднем около недели. Наблюдается плавный переход от дожелтушного к желтушному периоду. К этому моменту нормализуется температурная реакция, исчезают катаральные явления, однако диспепсические симптомы сохраняются или даже возрастают по интенсивности. Первым признаком наступления желтушного периода является потемнение мочи. Вскоре развивается желтуха, которую прежде всего можно заметить на слизистой ротовой полости (под уздечкой языка) и на склерах, а затем на кожных покровах. Язык обложен, стул может обесцвечиваться. Печень увеличена в размерах, достаточно плотной консистенции, слегка болезненная при пальпации. В половине случаев можно обнаружить спленомегалию. На фоне желтухи помимо диспепсических явлений больные отмечают адинамию, головокружение, иногда расстройства сна. Проявляется брадикардия, АД склонно к снижению.
Течение гепатита А обычно легкое или среднетяжелое, но не исключены и тяжелые варианты, и обострения. В некоторых случаях заболевание может приобрести затяжной характер. Фулминантная (злокачественная) форма гепатита встречается не более чем у 0,5% заболевших [1].
Дифференциальная диагностика. В продромальном периоде необходимо проводить дифференциальную диагностику с острыми респираторными и кишечными инфекциями, гриппом. В желтушном периоде заболевание дифференцируют с обтурационными и гемолитическими желтухами, мононуклеозом, иерсиниозом, лептоспирозом.
Лабораторная диагностика. Для установления этиологии гепатита и оценки его тяжести особое значение имеют лабораторные исследования. Возможно выделение вируса гепатита А из фекалий, но в широкой медицинской практике вирусологические исследования не применяются. Для верификации диагноза используют серологические реакции — ИФА, РИА, при проведении которых обнаруживается нарастание титров IgM-anti-HAV в желтушном периоде и нарастание титров IgG-anti-HAV к периоду реконвалесценции. Антитела класса М сохраняются в крови больного не дольше 6-8 месяцев и их наличие однозначно свидетельствует о текущей (или недавно перенесенной) гепатитной инфекции. При анализе крови необходимо учитывать наличие лейкопении, относительного лимфоцитоза и замедление СОЭ. Интенсивность желтухи устанавливается путем определения уровня билирубина в крови (особенно его связанной фракции). Активность аминотрансфераз (АлАТ, АсАТ) увеличивается в несколько раз, и степень их повышения говорит об интенсивности цитолиза гепатоцитов. Нарушение белково-синтетической функции печени отражает изменения показателей коллоидных проб (снижение сулемовой и повышение тимоловой проб), снижение уровня альбуминов в крови, а также уменьшение показателей протромбинового индекса.
Осложнения при вирусном гепатите А нечасты, однако могут манифестироваться воспалительные процессы в желчных путях (холециститы, холангиты, дискинезии), а также другие вторичные инфекции — пневмонии и т. д. Летальность, по данным мировой литературы, невысокая и составляет 0,1-0,4%, имеет место главным образом среди лиц с сопутствующими патологическими состояниями.
Лечение. При установлении этиологического фактора (ВГА) лечение больного можно проводить в амбулаторных условиях путем назначения постельного режима на период выраженного интоксикационного синдрома, обеспечения полноценного питания с исключением тугоплавких жиров и дополнительного введения в пищевые продукты витаминов групп С и В. Для снятия интоксикации в зависимости от ее степени назначаются обильное питье или инфузионные растворы. Для ежедневного очищения кишечника и подавления анаэробной флоры рекомендуется принимать препараты — производные лактулозы, вызывающие осмотическую диарею. С целью купирования холестатического компонента применяют спазмолитики (но-шпа, эуфиллин) и производные урсодезоксихолевой кислоты.
Профилактика и меры борьбы. Основными профилактическими мерами являются обеспечение населения доброкачественной водой и создание условий, гарантирующих выполнение санитарных правил, предъявляемых к заготовке, хранению, приготовлению и реализации продуктов питания. Важное значение имеет обеспечение надлежащего противоэпидемического режима в организованных детских коллективах. В период предсезонного повышения заболеваемости эффективна иммуноглобулинопрофилактика, обеспечивающая защиту в течение 3-4 месяцев. Вакцинация 50-60% детей дошкольных учреждений и 70-80% школьников обеспечивает снижение заболеваемости среди этих категорий населения. Детям дошкольного возраста вводят иммуноглобулин в дозе 0,75 мл, школьникам начальных классов — в дозе 1,5 мл (не более четырех раз в течение жизни с интервалом не менее одного года).
Заболевшие гепатитом подлежат госпитализации по клиническим и эпидемиологическим показаниям. Выписку реконвалесцентов и допуск их на работу (в том числе работников пищевых предприятий и лиц к ним приравненных) или детей в детские учреждения осуществляют в зависимости от состояния здоровья. В очаге инфекции устанавливают 35-дневное медицинское наблюдение за лицами, находившимися в контакте с больным. В дошкольных коллективах в течение этого периода запрещается перевод детей и персонала в другие группы, прием новых детей осуществляется только с разрешения эпидемиолога. Детям, которые общались с больными, и беременным вводят иммуноглобулин в дозе 1 мл — до 10 лет и 1,5 мл — лицам старше 10 лет. В очаге с использованием химических дезсредств проводится текущая и заключительная дезинфекция.
- Профилактические мероприятия осенью (время высокого риска) должны иметь статус противоэпидемических (в частности, дошкольные и школьные учреждения даже при отсутствии заболеваний следует рассматривать как потенциальные очаги ГА), направленных на активный поиск источников инфекции, в том числе с помощью антител класса IgM в ИФА), усиление дезинфекционного режима, предметное санитарное воспитание детей и взрослых в отношении реальной опасности заражения ГА.
В настоящее время в качестве специфической профилактики предложена вакцина против гепатита А. Введение иммуноглобулинов обеспечивает быструю, но кратковременную защиту. Вакцинопрофилактика формирует активный иммунитет, сопровождающийся продолжительной циркуляцией собственных антител. В настоящее время выпускаются эффективные и безвредные вакцины против гепатита А для детей и взрослого населения, обеспечивающие иммунитет до 10 лет [3]. Учитывая высокую поражаемость детей и тот факт, что они являются основным источником инфекции для взрослых, перспективным направлением является вакцинопрофилактика гепатита А среди детей младшего возраста и школьников, которая уже широко используется в США и ряде стран Европы (Израиль, Испания, Италия).
В России зарегистрированы следующие вакцины:
- ГЕП-А-ин-ВАК, Россия;
- Аваксим фирмы «Авентис Пастер», Франция;
- ВАКТА фирмы «Мерк, Шарп и Доум», США;
- Хаврикс 1440 и 720 фирмы «Смит Кляйн Бичем», Бельгия.
Все вакцины представляют собой инактивированные формалином вирионы гепатита А, адсорбированные на гидроокиси алюминия, вводятся внутримышечно [3]. ГЕП-А-ин-ВАК назначается детям с 3 лет и взрослым. Взрослым вакцину вводят в дозе 0,5 мл в дельтовидную мышцу. Курс — три прививки по схеме 0-1 и 6 месяцев. Детям вводят 0,25 мл в дельтовидную мышцу дважды с интервалом в 1 месяц.
Аваксим рекомендован детям с 2 лет и взрослым однократно внутримышечно, ревакцинация проводится через 6-18 месяцев однократно, последующие ревакцинации — каждые 10 лет.
ВАКТА вводится с 2 лет как однократная первичная доза (детям 25 антигенных ед. — 0,5 мл, взрослым 50 антигенных ед. — 1,0 мл) с повторной дозой через 6-18 месяцев.
Хаврикс применяется как у детей начиная с одного года, так и у взрослых. Выпускается в ампулах по 0,5 мл (720 ед.) для детей и по 1,0 мл (1440 ИФА ед.) для взрослых.
Вакцинация стимулирует развитие иммунитета через 21-28 суток. Титры антител, хотя и ниже, чем после заболевания, обеспечивают надежную защиту от инфекции.
В ряду упомянутых зарегистрированных вакцин против гепатита А вакцина ВАКТА обладает рядом исключительных характеристик, а именно:
1. ВАКТА — единственная вакцина, обеспечивающая 100%-ную защиту после введения первой дозы [4, 5].
Протективная эффективность, иммуногенность и безопасность вакцины были оценены в рамках рандомизированного двойного слепого плацебо-контролируемого исследования, в котором приняли участие 1037 восприимчивых здоровых детей и подростков в возрасте от 2 до 16 лет в одном из американских населенных пунктов с повторяющимися вспышками гепатита А (исследование эффективности вакцины «Монро»). Население г. Монро (штат Нью-Йорк) религиозно и там наблюдался редкий для США эндемический уровень вирусного гепатита А, более 3000 случаев заболевания на 100 тыс. населения — в 60 с лишним раз выше, чем в среднем по США в то время [4].
Проспективные конечные точки исследования были установлены в 50 и 30 дней. Случаев гепатита А не наблюдалось ни в один из указанных временных промежутков, что говорит о 100%-ной защитной эффективности вакцины. Учитывая, что инкубационный период гепатита А составляет 20-30 (а у детей, возможно, и более) дней, был сделан вывод о том, что любой участник исследования, имевший контакт с вирусом уже через 10 дней после иммунизации вакциной ВАКТА, был защищен. Следует отметить, что в действительности клинически подтвержденных случаев заболевания гепатитом А не наблюдалось не только после первой конечной точки исследования (30 дней), но уже на 14-й день после иммунизации, по сравнению с 34 случаями в группе плацебо.
2. ВАКТА — высокоочищенная вакцина, не содержащая консервантов (см. таблицу).
В целях усиления борьбы с вирусным гепатитом А в Москве осенью 2000 года была проведена работа по селективной вакцинации школьников в очагах этой инфекции и показана высокая эффективность данного мероприятия. Учитывая полученные результаты, а также продолжающийся рост заболеваемости, издано Постановление главного государственного врача по г. Москве, предусматривающее вакцинацию против гепатита А работников пищевых предприятий, коммунального хозяйства и транспорта. Организация и проведение целенаправленных профилактических мероприятий во многом зависят от финансовой поддержки правительства Москвы.
источник