Современная лабораторная диагностика HCV-инфекции основана на нескольких основных методиках исследования, которые делят на две группы в зависимости от технологии проведения – серологические и молекулярные. Эти анализы направлены на то, чтобы выявить основные маркеры гепатита С максимально точно и в кратчайшие сроки. В большинстве лабораторий сейчас применяют современные реагенты и оборудование, что позволяет поставить диагноз через 14–20 дней после заражения.
Эксперты не могут озвучить точное количество инфицированных HCV, так как в подавляющем большинстве случаев через несколько недель после заражения происходит хронизация вирусного процесса. В дальнейшем болезнь часто протекает в скрытой, латентной форме годами. Более чем у половины пациентов патологию диагностируют случайно при обращении к врачу по другому поводу, прохождении диспансеризации, оформлении медицинской книжки, постановке на учет по причине беременности и т.д.
По данным Всемирной организации здравоохранения, более полумиллиона человек ежегодно умирают от осложнений, вызванных HCV. Данная патология лидирует в перечне показаний для трансплантации печени.
Несмотря на меры по профилактике распространения заболевания, появление высокоэффективных лекарственных препаратов и методов диагностики, позволяющих своевременно выявить и полностью излечить болезнь, остановить рост количества инфицированных не удается ни в одной стране мира.
Возбудитель гепатита С, Hepatitis C Virus, относится к семейству Flaviviridae. Основу генома вируса составляет одноцепочечная РНК, включающая более 10 000 нуклеотидных остатков. Из-за неоднородности структуры специалисты выделили несколько генотипов HCV. Их распространенность не одинакова в различных уголках планеты. Но в большей степени диагностируют первый генотип (более 46% инфицированных), на втором месте – третий (треть случаев).
Еще одной характерной особенностью возбудителя гепатита Ц является мутационная активность. Так, у пациента в рамках одного генотипа идентифицируют до 40 подвидов HCV. По этой причине специалисты не могут создать вакцину для пожизненной защиты от инфицирования.
Заражение часто происходит при использовании одного шприца несколькими людьми для введения внутривенных наркотиков. Путь передачи болезни может быть также связан с применением уже использованных или недостаточно стерилизованных медицинских и/или косметологических инструментов. Возможно заражение при половом контакте, не исключен и вертикальный путь инфицирования.
В 80% случаев болезнь протекает без выраженных клинических проявлений.
Только у незначительного количества пациентов возникает один или несколько из таких симптомов:
- повышение температуры без катаральных признаков;
- усталость;
- снижение аппетита;
- тошноту с приступами рвоты;
- боли в животе;
- потемнение мочи;
- появление у фекальных масс сероватого оттенка;
- боли в суставах;
- желтизна склер и кожных покровов (встречается относительно редко, только при желтушной форме заболевания).
Что касается хронического течения патологии, период отсутствия симптомов может продолжаться вплоть до развития цирроза печени, печеночной недостаточности либо злокачественного онкологического образования.
Острую форму HCV диагностируют крайне редко, что связывают с бессимптомным прогрессированием заболевания. Для выявления патологии используют серологические методы, направленные на определение ряда специфических иммуноглобулинов, которые являются обязательной частью иммунного ответа на попадание вирусного патогена внутрь гепатоцитов. Другим методом диагностики является определение структурных частиц вируса при помощи молекулярно-химических реакций.
Что значит маркеры гепатита С? В медицинской литературе этот термин означает ряд высокоспецифичных лабораторных параметров, свидетельствующих о наличии острого либо хронического ВГС. Это, в частности, иммуноглобулины G и M (и их суммарный титр без дифференцирования на классы) и РНК (определенная часть генома) вириона. Соответственно, результаты, полученные в ходе выполнения ИФА и ПЦР (данные оценивают только в комплексе), и являются маркерами HCV.
В настоящее время существуют законодательно определенные критерии (на основе рекомендаций ВОЗ и Министерства здравоохранения), кому нужно обязательно сдавать анализ крови для выявления возможной HCV-инфекции:
- в период вынашивания ребенка (в I и III триместре);
- реципиентам донорского биологического материала (вне зависимости от его вида и количества), особенно если процедура и/или операция была проведена до 1992 года (именно тогда появились достоверные методы исследования, позволяющие выявить основные маркеры гепатита C);
- работникам медицинской, косметологической, торговой сферы (в соответствии со сроками оформления медкнижки);
- пациентам, регулярно проходящим процедуру гемодиализа, регулярно подвергающихся разнообразным инвазивным вмешательствам;
- перед назначением операционных вмешательств;
- перед началом курса химиотерапии;
- при отклонениях в показателях печеночных проб (для исключения или подтверждения гепатита);
- пациенты, состоящие на учете в специализированных клиниках и диспансерах на предмет пристрастия к наркотическим веществам;
- персонал детских образовательных учреждений, интернатов (при регулярном прохождении диспансеризации);
- члены семей и находящиеся в близком контакте с человеком с диагностированным ВГС;
- лица с повышенным риском инфицирования (инъекционные наркоманы, люди, отдающие предпочтение гомосексуальным, случайным или коммерческим половым связям);
- осужденные и пребывающие в местах лишения свободы;
- доноры биологического материала, органов;
- дети до достижения годовалого возраста (если выявлены положительные серологические маркеры вирусных гепатитов, то дольше) при наличии у матери диагностированного ВГС во время беременности;
- у людей с ВИЧ.
HCV-инфекция – серьезный диагноз, требующий немедленного начала терапии. Поэтому положительные маркеры, выявленные в одном из исследований, не являются показанием к приему лекарственных препаратов. Подтверждают наличие инфекции по нескольким специфическим анализам.
Где сдать кровь на выявление HCV, решает пациент. Можно обратиться в поликлинику по месту жительства, записавшись на консультацию к терапевту или инфекционисту. Врач выдаст направление на проведение анализа, но перед этим придется сделать клиническое исследование крови, печеночные пробы. Стоимость тестов компенсируется по полису ОМС.
Можно выполнить анализы в платной лаборатории. Там не требуется направление от врача. Стоимость в клиниках Москвы колеблется в пределах 3000–7000 тысяч рублей и выше в зависимости от разновидности диагностического теста и того, сколько маркеров необходимо определить.
Все исследования, применяемые для диагностики HCV-инфекции, можно разделить на несколько групп. Проведение каждого анализа является обязательным до начала терапии, а некоторые исследования выполняются и на определенных этапах лечебного цикла для оценки правильности и эффективности подобранной противовирусной схемы.
Для постановки диагноза врачу нужны следующие данные:
- Серологические маркеры вирусных гепатитов. Обнаруживаются вне зависимости от генотипа HCV. Это специфические антитела (anti-HCV) разновидностей G и/или M. Выявляются иммуноферментными методами (ИФА), технологиями иммунохемилюминисценции, иммуноблотинга и т.д. Изначально определяют суммарное количество антител (IgG + IgM) А подтверждающее исследование направлено на выявление антител к специфическим протеинам HCV, входящим в структуру капсида и оболочки, при помощи ИФА или иммуноблотинга.
- Молекулярные маркеры. Назначаются в качестве подтверждающих тестов для определения наличия РНК возбудителя патологии, оценки его количественного содержания. К этой же группе исследований относят генотипирующие анализы, предназначенные для установления разновидности вируса. Для проведения тестов используются различные методики постановки полимеразной цепной реакции (ПЦР).
Следующий этап диагностики проводят только при положительном результате предыдущих тестов. По мнению специалистов у пациентов с первым генотипом HCV целесообразно определение уровня IL28B. Подобное исследование помогает прогнозировать эффективность противовирусного лечения. Но такая схема диагностики подходит при использовании интерфероновых схем терапии. Связь между показателем IL28B и действием современных лекарственных средств (Софосбувира, Асунапревира и т.д.) не установлена, потому необходимость в проведении такого исследования остается под вопросом.
Первичная лабораторная диагностика HCV начинается с определения в сыворотке крови параметра anti-HCV. Положительный результат свидетельствует об активном течении патологического процесса (то есть заражении гепатитом С) либо о встрече иммунной системы организма с инфекцией в прошлом.
В большинстве лабораторий Москвы и других крупных городов серологический маркер определяется при помощи иммуноферментных систем (ИФА) II и III поколения. Суть анализа состоит в захвате рекомбинантными белками антител к HCV из исследуемой сыворотки. Впоследствии они определяются вторичными антителами против Ig класса G и V, мечеными ферментами, которые катализируют течение цветной реакции.
Тест-системы I поколения имели низкую специфичность, так как были способны обнаружить антитела, вырабатываемые к белку NS4. Чувствительность ИФА не превышала 70%, а сроки обнаружения иммуноглобулинов – минимум 16 недель с момента инфицирования.
ИФА II поколения способны выявить антитела к участку генома core, NS3 и NS4, что повышает специфичность теста до 95%, снижает риск получения ложноположительных результатов и сокращают срок обнаружения иммуноглобулинов до 10 недель от дня попадания РНК вируса в кровь человека.
Тест-системы ИФА III поколения разработаны на основе антигена NS5 и высокоиммуногенного эпитопа (части молекулы антигена) NS3. Подобная техника выполнения анализа обеспечивает срок сокращения серологического окна: положительные маркеры (либо отрицательный результат) можно получить уже на 4–6 неделе после заражения. Чувствительность ИФА последнего поколения достигает 99%.
Несмотря на то, что серологическое исследование является одним из золотых стандартов диагностики HCV, возможно получение ложноположительных или ложноотрицательных результатов, связанных не с качеством тест-систем, а особенностями состояния пациента.
Так, на проведение ИФА могут повлиять:
- аутоиммунные поражения суставов, особенно при положительном ревматоидном факторе, и другие заболевания подобного генеза;
- беременность;
- регулярное проведение гемодиализа;
- тяжелые иммуносупрессивные состояния (например, на фоне ВИЧ);
- гематологические злокачественные новообразования.
Современные тест-системы, дополненные рекомбинантными NS5, специфичны и чувствительны на 99,95% не реагируют на наличие в крови ревматоидного фактора и/или С-реактивного белка.
Серологический скриннинг является обязательным, но недостаточным компонентом диагностики HCV. Для подтверждения результатов анализа обязательно назначают исследование методом полимеразной цепной реакции.
Сейчас доступны качественные и количественные способы выявления РНК возбудителя вирусного гепатита С. Первая методика предназначена для подтверждения диагноза HCV-инфекции у лиц с положительным anti-HCV и для обследования донорского материала.
Количественный анализ служит основным маркером определения вирусной нагрузки. Является ключевым для оценки активности патологического процесса и эффективности противовирусной терапии. Применяемые тест-системы позволяют провести полимеразную цепную реакцию в режиме «real time». Диапазон вирусной нагрузки колеблется в пределах от 10–15 до 10 млн. МЕ/мл.
Техника количественной полимеразной цепной реакции – маркер репликации хронического вирусного гепатита С. Согласно современным рекомендациям, анализ проводят на 4–12–24 неделе лечения (и дополнительно на 48 при проведении интерфероновой терапии). Повторно исследование делают через 24 и 48 недель после окончания приема и/или инъекций медикаментов.
Отрицательный результат количественной ПЦР на 4 неделе лечения – один из основных факторов быстро вирусологического ответа и благоприятного исхода заболевания. Отсутствие РНК вируса на 24 неделе после завершения терапии является признаком выздоровления.
После базовых диагностических тестов и подтверждения положительных маркеров гепатита С обязательно проведение генотипирования. От результатов этого исследования зависит тактика дальнейшей терапии и прогноз развития риска осложнений. Определение генотипа HCV выполняется путем анализа нуклеотидной последовательности участка NS5 протеина вируса.
Но применяемые для генотипирования тест-системы недостаточно совершенны и не могут точно идентифицировать недавно выявленные, редко встречающиеся генотипы (в частности, 7,8 и 9).
В последних клинических исследованиях доказана роль определения полиморфизма гена IL28B у пациентов с генотипом 1а и 1b HCV. Проведение анализа важно для выбора между интерфероновыми схемами терапии и приемом комбинации противовирусных лекарственных препаратов.
Пункционная биопсия печени также входит в перечень необходимых для пациента с вирусом гепатита С анализов. Процедура позволяет оценить тяжесть структурных изменений в печеночной ткани, установить локализацию и распространенность фибротического процесса, некроза гепатоцитов, наличие злокачественной малигнизации клеток (при длительном течении хронического гепатита С), роль сопутствующих осложнений в повреждениях печени.
Но перед выполнением процедуры необходимо принять во внимание несколько факторов:
- Оценивают соотношение целесообразности проведения биопсии и потенциального вреда здоровью пациента.
- Перед манипуляцией делают УЗИ для оценки риска возможных осложнений. В идеале пункцию также нужно проводить под ультразвуковым контролем.
- За несколько дней до процедуры выполняют коагулограмму, определяют протромбиновое время и протромбиновый индекс. Если количество тромбоцитов менее 90 тыс. клеток/мм3, биопсию откладывают или выполняют при наличии строгих жизненных показаний.
- Перед манипуляцией необходимо взять письменное согласие пациента на процедуру.
- При необходимости (например, перевозбуждении) больному дают седативные средства (при отсутствии противопоказаний).
- После проведения забора ткани оценивают количество и качество биоптата. При необходимости процедуру сразу же повторяют.
- На протяжении 8 часов после манипуляции пациент должен оставаться под медицинским наблюдением.
Еще одним сравнительно новым методом оценки состояния печени является эластометрия, проводимая с использованием приборов ФиброСкан, ФиброТест, ФиброМетр и др. Преимуществом данного способа диагностики служит неинвазивность, быстрое получение результатов и безболезненность, что важно в педиатрической практике. Но проведение исследования затруднительно при избыточном весе пациента, наличии стеатоза, превышении уровня печеночных ферментов в 3 раза и более.
Для получения точных результатов важно соблюдать правила, предписывающие, как сдавать кровь и готовиться к проведению исследования.
Все аспекты необходимо уточнить у врача, но перечень стандартных рекомендаций включает:
- соблюдение диеты (№5 или №5а) с ограничением жирного, жареного, копченого за 7–10 дней до процедуры;
- строгое ограничение алкоголя за 2–2,5 недели до выполнения анализа;
- отказ от курения за 12–14 часов до забора крови;
- сдачу крови строго натощак (последний прием пищи за 12 часов до посещения лаборатории).
Результаты может быть искажены при приеме некоторых лекарственных препаратов. Поэтому при расшифровке данных необходимо сообщить врачу о каких-либо принимаемых медикаментах.
Сколько ждать результатов исследования зависит от загруженности лаборатории, технологической оснащенности (иногда требуется транспортировка биологического материала). В среднем постановка полимеразной цепной реакции или выполнение ИФА занимает от 2 до 5 дней. Некоторые клиники предлагают услугу платного срочного исследования.
Диагностика гепатита С проводится в несколько этапов.
Показанием для определения серологических маркеров методом ИФА (anti-HCV Total) служат:
- беременность (первый и третий семестр);
- отношение к группам риска по ВГС;
- ежегодное оформление медицинской книжки;
- повышение уровня печеночных трансаминаз и/или билирубина;
- самостоятельное желание пациента.
Для подтверждения диагноза HCV при положительных результатах серологического исследования назначают качественный анализ ПЦР. Обнаружение РНК вируса свидетельствует об остром или хроническом течении вирусной инфекции, что требует дальнейшего обследования пациента для подготовки к проведению терапии.
Назначают следующие диагностические тесты:
- определение иммуноглобулинов G и М для установления стадии заболевания (острая, хроническая, рецидив латентного течения инфекции);
- оценка вирусной нагрузки;
- генотипирование;
- • определение степени поражения печени.
Обязательны и другие исследования: клинические анализы крови, мочи и кала, выявление возможных сопутствующих коинфекций (ВИЧ, аутоиммунные заболевания), исключение или подтверждение беременности.
Биологическим материалом для проведения ИФА и ПЦР является сыворотка крови. Реже исследование проводят на биоптате печени, но такой тест трудоемкий, дорогостоящий и требует выполнение инвазивных медицинских процедур.
В 2017 году на фармацевтическом рынке появились экспресс-тесты, позволяющие проводить предварительную диагностику гепатита С по образцу слюны. Преимуществом набора является возможность выполнения самостоятельно в домашних условиях. Но результат экспресс-теста также требует подтверждения, несмотря на то, что его специфичность достигает 96%.
Расшифровка серологических маркеров на гепатит С обязательно проводится в тандеме с данными полимеразной цепной реакции. Значение полученных результатов приведено в таблице ниже.
| Определяемый показатель | Возможный диагноз |
| Положительный anti-HCV | |
| На фоне отрицательного результата полимеразной цепной реакции | |
| На фоне положительного результата качественной ПЦР | Подтверждение диагноза острого или хронического гепатита |
| Положительные данные качественного анализа методом полимеразной цепной реакции – маркер HCV-инфекции | |
| При IgM «+» и отрицательном титре IgG | Свидетельствует об остром течении заболевания и недавнем заражении (до полугода). Прогноз благоприятный, лечение могут отсрочить на несколько недель (4–6) из-за вероятности самостоятельного излечения без медикаментозного вмешательства |
| При IgG «+» и отсутствии IgM | Указывает на наличие хронической инфекции. Иногда такой результат – маркер носителя гепатита С, когда болезнь протекает без выраженной клинической картины |
| При IgG «+» и IgM «+» | Симптом острого рецидива хронического патологического процесса |
Иногда пациенты и врачи сталкиваются с ситуацией, когда качественный анализ методом ПЦР на РНК отрицательный, а маркеры положительные (при проведении серологического обследования).
В таком случае доктора придерживаются следующей тактики:
- Повторная постановка полимеразной цепной реакции для исключения ошибочного результата вследствие лабораторной ошибки.
- Исключение/подтверждение заболеваний, синдромов и состояний, которые могут быть вероятной причиной ложноположительного результата ИФА.
- Сбор анамнеза. Такая картина характерна после перенесенного острого гепатита С. При этом человек может сам не знать о прошедшем заболевании. Сопоставление симптоматики (в том числе неспецифической), предположение пути заражения и данных клинических исследований позволяют доктору предположить такой исход патологического процесса.
- Повтор анализа через 3–4 недели, когда можно исключить вероятность диагностического окна.
Но вне зависимости от результатов исследований трактовать полученные данные должен только врач. Специалисты предостерегают от самостоятельной терапии. Комбинация противовирусных препаратов и длительность их применения подбирается с учетом генотипа HCV наличия или отсутствия коинфекций и ряда других факторов.
источник
Со времени открытия серологических маркеров инфекций данный анализ является основным в лабораторных исследованиях. Цель его проведения – помощь в распознавании заболеваний инфекционного происхождения, а также выявление недугов, обусловленных нарушением защитных функций иммунной системы.
Диагностирование гепатитов, краснухи, сифилиса, ВИЧ и многих других болезней в наше время стало доступно благодаря анализам на серологические маркеры инфекций. Расшифровка результатов исследований помогает достаточно быстро определить наличие заболеваний, которые иногда бывает трудно выявить обычными способами.
Анализ свойств и эффектов сывороток
Происхождение наименования «серология» — от лат. названия сыворотки (serum). Сочетание с известным logos означает «учение о сыворотке». Под серологией подразумевается раздел иммунологии, изучающий специфику взаимодействия антител сыворотки с антигенами.
Основа серологической диагностики – выявление специфических антител, образующихся в ответ на инфицирование определенным антигеном. По наличию в крови определенных антител делается заключение о характере и степени активности инфекции.
Серологический метод используется в диагностике:
- герпеса
- кишечных инфекций
- цитомегаловируса
- эпидемического паротита
- атипичной пневмонии
- краснухи
- хламидиоза
- токсоплазмоза
- сифилиса
- ВИЧ
- кори
- вирусных гепатитов В и C
Исследование применяют и в случаях, когда требуется выявление причин миокардитов.
Серологические реакции могут быть применены:
- В случае если нужно подтвердить диагноз. Практикуется добавление в сыворотку крови соответствующего антигена. Наличие антител доказывается либо опровергается характером ответной реакции.
- В случае, когда о характере заболевания ничего не известно, видовая принадлежность антигенов, находящихся в крови, выявляется добавлением антител.
Для проведения анализа из крови предварительно удаляют компонент, ответственный за свертываемость (фиброген).
Таким образом, цель проведения серологического анализа крови:
- Постановка диагноза. Исследование показано в случае, когда требуется лабораторное подтверждение присутствия в сыворотке крови возбудителя.
- Назначение лечения. Анализ поможет выявить реакцию возбудителя на различные лекарства.
Использование серологического анализа практикуется и при диагностике аутоиммунных заболеваний. Проведение процедуры помогает выявить антитела к тканям организма.
Вирусные гепатиты относятся к тому виду серьёзных инфекционных заболеваний, которые могут достаточно долго протекать, ничем себя особенно не проявляя. В трудности своевременного обнаружения и заключается его главная опасность.
Проведение анализа на маркеры, появляющиеся в крови как следствие введения вакцины или перенесенного заболевания, позволяет выявить гепатит в ранней фазе, в которой он лучше поддается излечению.
Этот вид (так называемая желтуха) встречается достаточно часто. Передается при употреблении инфицированных продуктов и воды. При его диагностике анализ делается на наличие антител:
- Аnti-НАV IgМ. Существование в крови ранних антител свидетельствует о наличии вируса в организме не менее 25-30 дней.
- Аnti-НАV IgG. Его наличие – свидетельство того, что пациент переболел данной формой гепатита в прошлом.
Передается половым путем. Вирус может попасть в кровь и при использовании нестерильных инструментов. Распространен широко, при своевременном выявлении хорошо поддается лечению. По выздоровлении организм приобретает к вирусу пожизненный иммунитет. Нелеченый гепатит В, вероятнее всего, перейдет в хроническую форму, которая грозит осложнениями в виде цирроза и рака печени.
При выявлении гепатита В ищут следующие маркеры:
- HВsAg. Специфический антиген, показывающий наличие заболевания.
- Аnti-НВs. Его появление свидетельствует о завершении процесса.
- Аnti-НВс IgG. Его длительное нахождение в организме указывает на течение процесса.
- Аnti-НВс IgM. Его обнаружение является признаком начальной фазы заболевания.
- Аnti-НВе. Его присутствие – признак вялотекущей формы гепатита.
Наиболее тяжёлая форма заболевания. Поддается лечению лишь на ранних стадиях. Исход несвоевременно выявленной болезни – летальный.
По результатам исследований выявляются следующие маркеры:
- Аnti-НСV. Свидетельствует о наличии заболевания.
- Аnti-НСV IgM. Позволяет судить о достаточно недавнем заражении, что дает основания для благоприятного прогноза.
Симптоматика та же, что и у гепатита В. Диагностируется присутствием аnti-НDV Ig G, характерного для гепатита В, дополненного аnti-НDV Ig M.
В целом подобен гепатиту А, но более опасен для беременных. Выявляется присутствием anti-HEV lg.
По свойствам близок к гепатиту С, но менее опасен.
Необходимые анализы во время беременности
Беременность – период, когда подверженность инфекциям становится достаточно острой проблемой для организма. Существует группа инфекций, которые опасны для беременных, в то время как для остальных групп пациентов не представляет угрозы. Названа эта группа ТОRСН-инфекциями. Название образовано из первых букв входящий в группу названий инфекций:
- токсоплазмоз
- другие инфекции (сифилис, листериоз, хламидиоз и др.)
- краснуха
- цитомегаловирусная инфекция
- герпес
Выявленные антитела IgG означают наличие иммунитета к заболеванию. Препятствием для планирования беременности не являются.
Обнаружение IgM возможно лишь в острой стадии. Беременность можно планировать лишь после выздоровления.
Краснуха. Относится к инфекциям, передающимся внутриутробно. Перенесенное заболевание формирует пожизненный иммунитет. Тяжесть, с которой протекает заболевание, прямо пропорциональна возрасту больного. У плода инфицированной женщины велика вероятность развития тяжелых пороков. Сегодня есть возможность привиться от краснухи, тем самым избежав вероятности заболеть во время беременности. После прививки в течение некоторого времени в крови сохраняются титры IgM, поэтому от планирования беременности лучше воздержаться в течение 3 мес.
Перед прививкой нужно сделать серологический анализ, после которого можно принимать решение о проведении прививки.
- IgМ-, IgG-: обозначает отсутствие антител и необходимость вакцинации.
- IgМ-, IgG+: показывает наличие иммунитета. Вакцинация не требуется.
- IgМ+, IgG-: заболевание в ранней стадии, период обострения.
- IgМ+, IgG+: период обострения.
Динамика отслеживается по степени понижения IgM и увеличения IgG. Заболевание опасно в острой фазе при положительном значении IgM.
Появление в крови IgM либо IgG, если ранее их у данной пациентки не наблюдалось, означает развитие заболевания. Такой же вердикт можно вынести при 4-кратном повышении за две-три недели количества IgG. Срок давности предыдущего обследования также имеет значение: антитела могут присутствовать в крови в течение 2 лет от начала заболевания. Поэтому наличие IgM не может интерпретироваться как признак острой инфекции. Наличие IgG в снижающемся количестве – не считается заболеванием и не представляет опасности.
Если заражение произошло во II или III триместре, заболевание излечимо.
Диагностические анализы при аллергии проводят с помощью количественного определения иммуноглобулина Е. При этом способе аллергены связываются с антителами, образуя единый комплекс. В исследовании используется более 200 аллергенов.
Более тщательные исследования проводятся, когда нужно выявить тип и степень остроты реакции. Преимущество этого метода заключается в отсутствии прямого контакта пациента с аллергеном. При этом определяются общие и аллергенспецифические IgE.
В определении диагноза важны не только лабораторные исследования, но и другие данные. Сопоставить их и правильно диагностировать наличие заболевания может только врач, специализирующийся в данной области. Самолечением на основании расшифровки серологических анализов заниматься нельзя.
Заметили ошибку? Выделите ее и нажмите Ctrl+Enter, чтобы сообщить нам.
источник
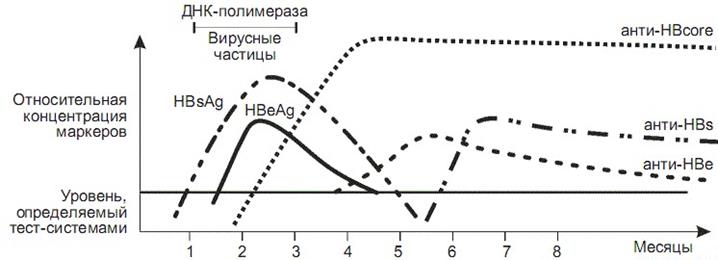
HBsAg — наружный компонент вируса гепатита В, появляется в крови больных острым гепатитом в продромальном периоде болезни, сохраняется около 1-4 мес, исчезает при выздоровлении. Определение HBsAg в крови — признак персистенции вируса гепатита В. Это наблюдается у Уз больных хроническими заболеваниями печени. Могут быть случаи «здорового носительства» HBsAg.
HBeAg — определяется в крови больных с положительным HbsAg, выявляется на ранних стадиях острого вирусного гепатита В вскоре после появления HBsAg и исчезает к периоду развернутой клинической картины.
При хронизации воспалительного процесса в печени HBeAg сохраняется вместе с HBsAg в крови в течение длительного срока.
Наличие HBeAg отражает фазу репликации вируса гепатита В и коррелирует с высокой активностью воспалительного процесса в печени и контагиозностью больного.
HBcAg — в крови не обнаруживается, располагается в ядрах гепатоцитов. В последние годы с помощью иммуноэлекгронной микроскопии HBcAg обнаружен также и в цитоплазме гепатоцитов больных.
После заражения вирусом гепатита В в процессе иммунного ответа в крови появляются антитела к антигенам вируса.
Первыми появляются антитела к HbcAg — HBcAb (НbсАgAbо-dy), уже через 2-4 недели после появления HBsAg. Большая часть антител в это время представлена классом IgM (HBcAblgM), которые сохраняются в сыворотке крови больных 6-9 мес. Наличие HBcAblgM свидетельствует об остром или хроническом гепатите с продолжающейся репликацией вируса гепатита В. Несколько позже в крови появляются НВсАb класса IgG, которые могут определяться в течение многих лет. Выявление HBcAblgG может указывать как на перенесенный и полностью разрешившийся острый вирусный гепатит В, так и на персистенцию вируса гепатита В.
Антитела к HbeAg — НВеАb — появляются приблизительно через 2 недели от начала острого вирусного гепатита В и по мере уменьшения концентрации HBeAg остаются в крови от 1 до 5 лет и более. Появление НВеАb свидетельствует о выздоровлении больного или о переходе острого вирусного гепатита в хронический, при этом репликация вируса гепатита В прекращается или значительно снижается, происходит интеграция генома вируса гепатита В в геном гепатоцита, что сопровождается снижением активности воспалительного процесса.
Антитела к HBsAg — HBsAb — обнаруживаются через 3-5 месяцев после начала острого гепатита В. Они могут определяться в крови больного в течение 5-10 и более лет. Появление этих антител говорит об иммунном разрешении инфекции, но при этом не исключается наличие вируса гепатита В в гепатоцитах.
Некоторые доктора считают, что только эти антитела обладают защитными свойствами, обеспечивают иммунитет к вирусу гепатита В.
Непосредственным цитопатическим действием сам вирус гепатита В не обладает (т.е. сам вирус гепатоциты не разрушает), поражение печени объясняется выраженным иммунным ответом организма на внедрение в гепатоцит вируса.
В жизнедеятельности вируса гепатита В различают две фазы: фазу репликации и фазу интеграции.
В фазу репликации происходит воспроизведение (размножение) вируса. Гепатотропность вируса гепатита В, способность его проникать в гепатоцит определяется белками внешней оболочки области pre-S. На мембранах гепатоцитов имеются зоны полимеризированного альбумина, соответствующие рецепторам pre-S 1.
Благодаря взаимодействию белков pre-S с рецепторами к ним на поверхности гепатоцита вирус прикрепляется к гепатоциту. В фазе репликации ДНК вируса проникает в ядро гепатоцита и на ней, как на матрице, с помощью ДНК-полимеразы, синтезируется нуклеокапсид вируса, содержащий ДНК вируса, антигены HBcAg, HBeAg, HBxAg. Антигены HBcAg и HBeAg являются основной мишенью иммунной системы. Затем нуклеокапсид мигрирует из ядра в цитоплазму, где реплицируются белки внешней оболочки (HBsAg) и таким образом, происходит сборка полного вириона. При этом избыток HBsAg, не использованный для сборки вируса, через межклеточное пространство попадает в кровь. Полная сборка (репликация) вируса заканчивается презентацией его растворимого нуклеокапсидного антигена — HBeAg на мембране гепатоцита, где происходит его «узнавание» иммуноцитами. В защите вируса от воздействия иммунной системы огромную роль играет секреция HBeAg в кровь. Установлено, что циркулирующий HBeAg подавляет оба звена иммунитета. Клеточный иммунитет ингибируется путем снижения синтеза у-интерферона (именно он играет важнейшую роль в процессе распознавания антигенов вируса гепатита В Т-лимфоцитами), гуморальный — благодаря подавлению образования антител В-лимфоцитами. Таким образом HBeAg способен вызывать состояние иммунотолерантности и это замедляет его удаление из инфицированных гепатоцитов.
В настоящее время установлена способность вируса гепатита В к мутациям. Мутации с разной частотой могут возникать практически во всех генах вируса гепатита В, но наиболее часто — в области гена, кодирующего синтез HBeAg. В результате мутации вирус теряет способность синтезировать HBeAg и это позволяет вирусу избавиться от надзора иммунной системы и избежать элиминации. Таким образом, можно считать, что мутация вируса может рассматриваться как способ защиты от иммунной системы и выживания (сохранения) вируса в организме человека. Bonino (1994) определяет мутировавший вирус гепатита В как «HBVминус HBeAg». Он нередко выявляется при наиболее тяжело протекающих заболеваниях печени, вызванных вирусом гепатита В, в частности, при HbeAg-негативном варианте хронического гепатита, который имеет следующие особенности:
- отсутствие в крови HBeAg при наличии маркеров репликации HBV;
- обнаружение ДНК HBV в сыворотке крови и HBcAg в гепатоцитах;
- наличие в инфицированных гепатоцитах как цитоплазматических, так и ядерных антигенов нуклеокапсида HBV;
- более тяжелое клиническое течение заболевания;
- менее выраженный ответ на лечение интерфероном по сравнению с HBeAg-позитивным вариантом хронического гепатита В.
Следовательно, вирус типа «HBV минус HBeAg» более патогенен, чем немутировавший тип HBV, возможно, это обусловлено более высокой цитопатогенностью или большей эффективностью цитоксических Т-лимфоцитов.
В настоящее время более обоснована точка зрения, согласно которой «HBV минус HBeAg» обычно обнаруживают при отсутствии толерантности к вирусу, а популяции немутировавшего («дикого») вируса преобладают при наличии толерантности к нему. Неузнаваемость мутантных HBV обусловливает неполноценность иммунного ответа, что меняет течение и исход вирусного гепатита В.
Маркерами фазы репликации вируса гепатита В являются:
- выявление в крови HBeAg, HBcAblgM (коэффициент HBcAbG/HBcAbM 200 нг/л (определяется с помощью полимеразной цепной реакции), ДНК-полимеразы и антигенов pre-S (характеризующих функциональную активность альбуминчувствительности рецепторов);
- выявление в гепатоцитах HBeAg и HBV-ДНК.
У 7-12% больных хроническим вирусным гепатитом В возможен спонтанный переход фазы репликации в нерепликативную фазу (при этом из крови исчезает HBeAg и появляются НВеАb). Именно фаза репликации обусловливает тяжесть поражения печени и контагиозность больного.
Установлено, что репликация вируса гепатита В происходит не только в печени — в гемопоэтических клетках-предшественниках (в костном мозге); эндотелии; моноцитах, макрофагах лимфатических узлов и селезенки, эндотелии сосудов почек; железистом эпителии и фибробластах стромы желудка и кишечника; в стромальных фибробластах яичек; нейроцитах и стромальных фибробластах периферических, нервных ганглиев; фибробластах дермы. В 1995-1996 г. была показана репликация вируса гепатита В в тканях сердца, легких, головного мозга, половых желез, надпочечников, щитовидной и поджелудочной желез.
Внепеченочная репликация вируса гепатита В может быть причиной развития разнообразных внепеченочных (системных) проявлений заболевания — хронической генерализованной инфекции.
В фазу интеграции происходит интегрирование (встраивание) фрагмента вируса гепатита В, несущего ген HBsAg, в геном (ДНК) гепатоцита с последующим образованием преимущественно HBsAg. При этом репликация вируса прекращается, однако генетический аппарат гепатоцита продолжает синтезировать HBsAg в большом количестве.
Вирусная ДНК может быть интегрирована не только в гепатоцитах, но и в клетки поджелудочной железы, слюнных желез, лейкоциты, сперматозоиды, клетки почек.
Фаза интеграции сопровождается становлением клинико-морфологической ремиссии. В этой фазе в большинстве случаев формируется состояние иммунологической толерантности к вирусу, что приводит к купированию активности процесса и носительству HBsAg. Интеграция делает вирус недосягаемым для иммунного контроля.
Серологические маркеры фазы интеграции:
- наличие в крови только HBsAg или в сочетании с HBcAblgG;
- отсутствие в крови вирусной ДНК-полимеразы и ДНК-вируса;
- сероконверсия HBeAg в НВеАb (т.е. исчезновение из крови HBeAg и появление НВеАb).
В последние годы установлено, что при гепатите В интеграция генома вируса с геномом гепатоцита не облигатна, а факультативна. У подавляющего большинства больных острым гепатитом В она не развивается. В редких случаях хронизация HBV-инфекции может протекать без интеграции с геномом инфицированных гепатоцитов. У таких больных регистрируется продолжающаяся активная репликация HBV.

источник
Вирусные гепатиты – тяжелые заболевания печени, лечение которых требует много времени и сил. При этом терапевтический эффект во многом зависит от того, на какой стадии была диагностирована данная болезнь. Раннюю диагностику может обеспечить анализ на маркеры гепатитов.
Особенность гепатита С и В заключается в том, что ранние стадии развития инфекции не имеют характерных симптомов, и когда пациент обращается в клинику с жалобами, его печень сильно поражена и ее функции нарушены. Избежать такого развития поможет ранняя диагностика.
Маркеры являются специфическими антигенами и антителами к этим заболеваниям. Выявление специфических антител в кровяной сыворотке может подтвердить наличие у человека того или иного типа гепатита. Важная особенность состоит в том, что маркеры выявляются даже на раннем этапе заболевания при отсутствии симптомов.
Для выявления специфических и серологических маркеров к гепатитам используют несколько видов исследования.
- Диагностика, основанная на иммунологических методах исследования.
- С помощью реакции иммунитета на вирусы.
- С помощью специализированного скринингового исследования.
- Путем проведения иммуноферментного анализа.
В зависимости от методов и цели диагностики выполняют 2 вида анализов на маркеры гепатита:
В ходе такого исследования удается определить тип вируса, который стал причиной болезни. Специфическими маркерами являются антигены гепатитов.
Антиген представляет собой отдельные элементы вируса. При попадании в благоприятную среду эти антигены участвуют в продуцировании новых клеток вируса. Незадействованные фрагменты разносятся по организму током крови.
К этому типу маркеров относят антитела к существующим антигенам. Этот способ диагностики становится возможным благодаря особенности человеческого организма вырабатывать антитела (клетки, направленные на борьбу с возбудителями болезней). Выявление таких антител к антигенам гепатита свидетельствует о наличии патологических процессов в тканях печени.
В случае заражения гепатитом В у людей в организме присутствуют несколько маркеров:
- антигены гепатита – к таким относятся HBeAg и HBsAg;
- антитела к антигенам – в эту группу включают анти-HBs, анти-HBe, анти-HBc.
По результатам проведенного иммуноферментного анализа врачи могут не только выявить тип гепатита, но и определить его стадию. Благодаря этому появляется возможность прогнозировать развитие болезни и выбирать наиболее эффективное лечение.
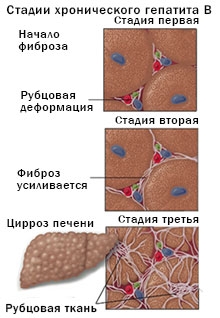
Если в крови присутствуют сразу 2 антигена (HBsAg и HBeAg), то это свидетельствует о наличии воспалительных процессов в тканях печени.
Данный маркер репликации вируса начинает распространяться в организме с момента проникновения инфекции в организм. Его выявление у пациента в крови свидетельствует о высокой концентрации вируса. На этот период приходится активное распространение болезни. Подтверждением этого факта становятся некоторые симптомы, например желтый оттенок кожных покровов.
Обнаружение HBeAg в крови спустя 4 и более недели после заражения является признаком перехода болезни в хроническое течение.
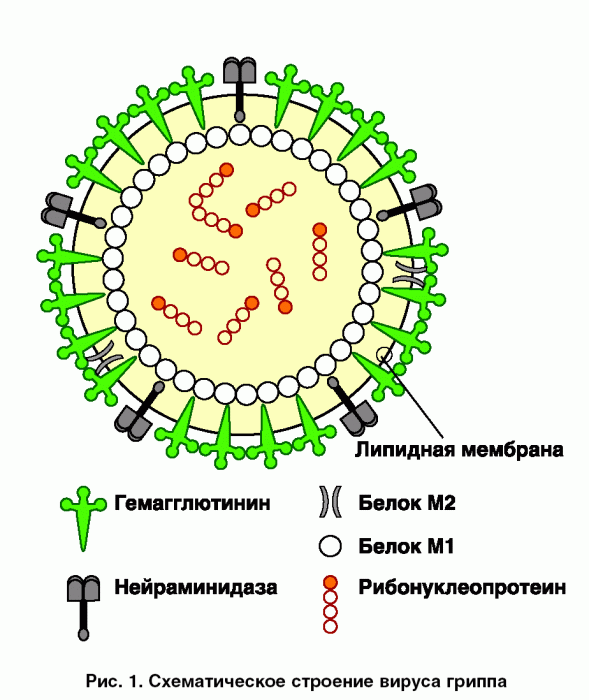
Особенностью данного антигена является высокая иммуногенность. По этой причине антитела к нему начинают вырабатываться в числе первых. Таким образом, диагностировать гепатит по наличию антител можно уже спустя 3-5 недель после заражения. При этом выраженные симптомы на этой стадии отсутствуют.
Суммарные маркеры анти-HBc являются антителами, активно вырабатываемыми организмом для эффективной борьбы с вирусами. Обнаружить эти маркеры можно после окончания острой стадии болезни. Сохраняться в организме они могут на протяжении 10 лет после заражения. Иными словами, обнаружение в крови антител в некоторых случаях свидетельствует лишь о ранее перенесенной болезни.
Такой тип маркера представляет собой антитела к антигену HBcAg. Они возникают в начале болезни, поэтому их наличие в крови – показатель острого течения данного заболевания. К этому моменту у большинства пациентов еще отсутствуют симптомы. Длительность пребывания антител в сыворотке достигает 5-6 месяцев. Спустя этот промежуток времени Анти-HBc IgM исчезают.
Положительный анти-HBe регистрируется в организме в период активного развития вируса. Это помогает более точно определить стадию болезни. Чаще всего для этой цели изучают показатели анти-HBe совместно с данными о маркере HBeAg.
Маркер анти-HBs относится к антителам, которые обнаруживаются уже после прохождения острой стадии болезни. Их наличие в крови говорит об активном противостоянии иммунной системы и защите организма от вируса. Этот тип маркера может присутствовать в крови пациентов спустя 10 лет с момента заражения.
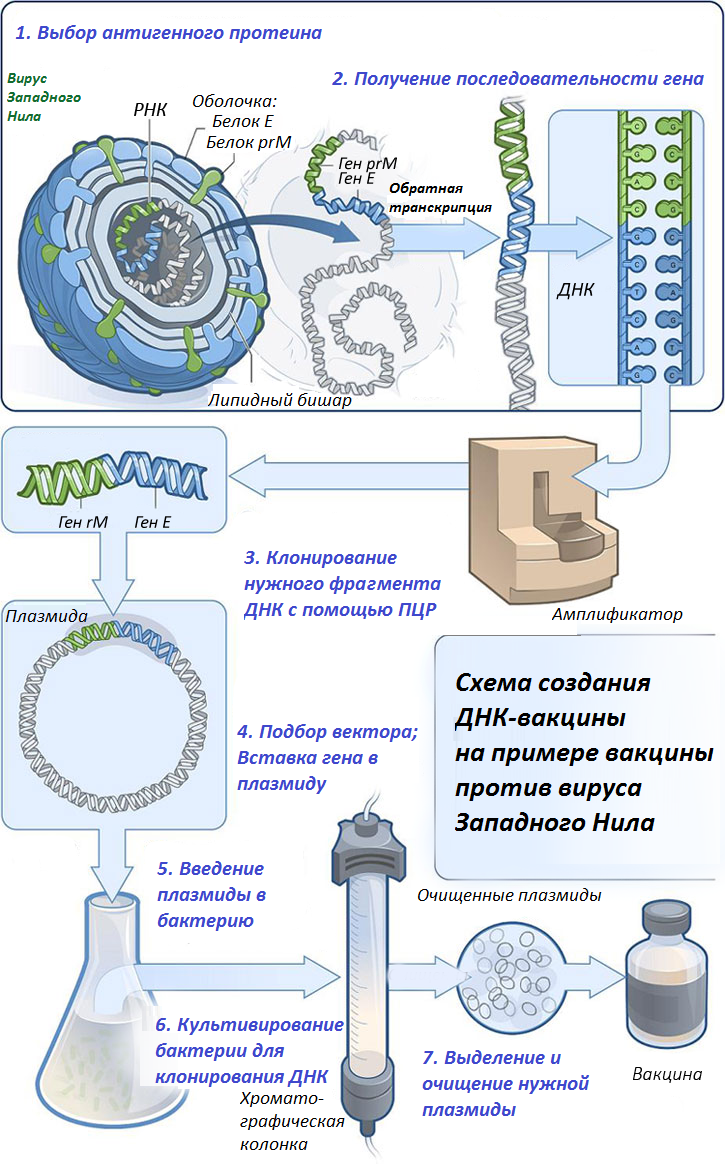
Результаты анализов содержат в себе данные о присутствии или отсутствии маркеров в крови. При этом разные сочетания свидетельствуют о разных диагнозах. Более детально разобраться в референсных значениях поможет таблица с расшифровкой.
| Интерпретация результата | HBsAg | HBeAg | Анти-HBc IgM | Анти-HBc | Сумм анти-HBe | Анти-HBs | HBV-ДНК |
| Острая фаза заболевания. Дикий штамм. | + | + | + | + | — | — | + |
| Острая инфекция. Мутантный штамм. | + | — | + | + | — | — | + |
| Острый разрешившийся вирус. Сероконверсия. | + | — | -/+ | + | + | — | -/+ |
| Активный хронический тип течения | + | + | -/+ | + | -/+ | — | + |
| Интегративное хроническое течение | +/- | -/+ | -/+ | + | -/+ | — | -/+ |
| Признак «здорового» носительства | + | — | — | + | — | -/+ | — |
| Ранее перенесенная инфекция | — | — | — | + | -/+ | + | — |
| Перенесенная инфекция при отсутствии иммунного ответа Хроническая латентная инфекция Разрешение острой инфекции | — | — | — | + | -/+ | — | — |
| Состояние, наступающее после иммунизации | — | — | — | — | — | + | — |
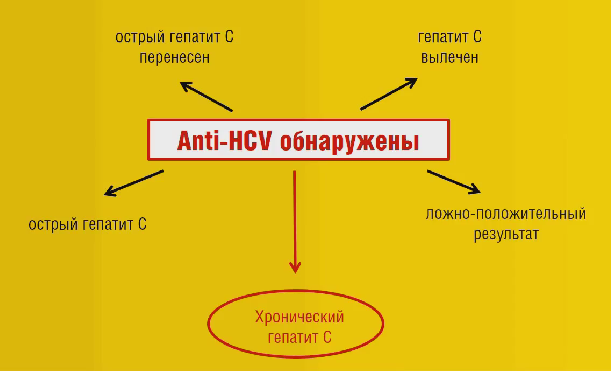
Такая статистика обусловлена длительным инкубационным периодом болезни, отсутствием симптомов или их слабым проявлением. Повышение температуры и хроническая усталость часто принимаются за симптомы других заболеваний. Единственным эффективным способом диагностики в таких случаях является анализ на маркеры.
Существует несколько маркеров, позволяющих выявить наличие гепатита С в организме:
- HCV-RNA. РНК (рибонуклеиновая кислота) вируса обнаруживается в крови или тканях печени в тех случаях, когда болезнь находится в стадии активного развития. Присутствие такого маркера будет выявлено с самого начала заболевания.
- Anti-HCV total (или суммарные антитела). Иммуноглобулины такого типа появляются в организме спустя около 6 недель после заражения. Их выявление свидетельствует о наличии вируса в теле пациента. При этом такие маркеры могут присутствовать в крови даже после излечения.
- Anti-HCV core IgG. Обнаружить данные тела можно несколько позже (начиная с 11 недели). Anti-HCV core IgG относят к антителам класса G. Присутствие таких маркеров характерно для больных с хроническим течением гепатита.
- Anti-NS3. Маркер этого вида сопутствует гепатиту С острой формы.
- Маркеры anti-NS4 и anti-NS5 часто обнаруживаются в тех случаях, когда инфекция находится на поздних стадиях развития с поражением тканей печени. После полного излечения их количество сокращается.
Положительный или отрицательный результат на гепатит С можно выявить с помощью таблицы:
| Возможные диагнозы | Анти-HCV IgM | Анти-HCV IgG | Анти-NS4 | РНК HCV |
| Острое течение гепатита С | +/- | +/- | — | + |
| Острое течение – реконвалесценция | — | + | — | — |
| Хроническое течение гепатита С | +/- | + | + | + |
| Хроническое течение гепатита С при отсутствии репликации | — | + | + | — |
Гепатит А представляет собой заболевание печени с острой формой течения. Способов передачи существует несколько, наиболее частая причина заражения – несоблюдение правил гигиены. Среди характерных симптомов:
- желтуха;
- нарушение работы печени;
- повышенная температура тела;
- болевые ощущения в суставах;
- слабость и тошнота.
Данный вид гепатита характеризуется быстротечностью, отсутствием тяжелых последствий и простым лечением.
При лабораторном исследовании выявляется несколько маркеров:
- РНК вируса. Является признаком наличия инфекции в организме и ее стремительного распространения.
- Ag. Маркер является показателем наличия вируса.
- Анти-ВГА IgG. Обнаружение такого антитела свидетельствует о перенесенном заболевании и наличии иммунитета к гепатиту А.
- Анти-ВГА IgM. Показатель характеризует острую форму заболевания.
Гепатит Е широко распространен в жарких странах. Причиной заражения является антисанитария. Эта форма гепатита легко передается через грязную воду, продукты питания. Основными симптомами являются:
- расстройство пищеварительного тракта;
- болевые ощущения в правом подреберье.
Течение болезни характеризуется как тяжелое с высоким процентом смертности. Диагностировать гепатит Е можно с помощью выявления следующих маркеров.
- РНК вируса. Наличие такого антигена – признак активного распространения вируса в организме.
- Ag. Маркер подтверждает наличие гепатита Е в крови пациента.
- Анти-ВГЕ IgM. Антитела этого типа присутствуют во время острого течения болезни.
- Анти-ВГЕ IgG. Если в крови найден такой маркер, значит, человек ранее уже болел гепатитом Е и организм выработал иммунитет к вирусу.
Вирус гепатита D относится к антропонозным инфекциям. Заражение происходит посредством любых жидкостей зараженного человека, однако ему подвержены лишь те, кто болен гепатитом B. Симптомы этих заболеваний во многом похожи, однако вирус типа D часто вызывает асцит и отеки. Анализы назначают в первую очередь пациентам с гепатитом В и тем, кто принимает наркотические средства.
Выявить болезнь можно по антигенам и антителам к ним:
- РНК данного вируса. Этот маркер присутствует в организме в период активного распространения инфекции.
- Анти-ВГД IgM появляется в период острого течения.
- HDAg. Наличие антигена в крови подтверждает заражение.
- Анти-ВГД IgG. Человек уже перенес болезнь в прошлом, и теперь у него есть иммунитет к данному типу вируса.
Вирус гепатита G распространяется половым путем и через многократное использование одноразовых шприцев. Реже передача вируса происходит при иглоукалывании или пирсинге. Как и тип D, этот вид болезни может возникнуть лишь у людей с наличием гепатита C, B или D. Длительное отсутствие симптомов приводит к хроническому течению и повышает риск развития цирроза печени.
Ранняя диагностика возможна путем исследования крови для обнаружения маркеров:
- РНК вируса. В этом случае ставят диагноз острого течения гепатита G.
- Анти-ВГG. Признак того, что пациент перенес гепатит и теперь в организме у него есть иммунитет к этому заболеванию.
Для получения максимально точных результатов исследования пациенту нужно правильно подготовиться к процедуре забора крови:
- За неделю до исследования исключают прием всех противовирусных лекарственных средств.
- За двое суток до сдачи крови желательно отказаться от тяжелых физических нагрузок. Важно также перейти на диетическое питание. Для этого исключают из рациона острые, копченые, жирные, жареные блюда.
- В день сдачи анализов с утра не завтракают – кровь нужно сдавать натощак.
После процедуры остается лишь ждать результаты.
источник
Гепатит В – это воспалительное заболевание печени, которое провоцирует вирус гепатита B (HBV). Этот опасный недуг имеет тяжёлое течение и грозит серьёзными осложнениями. Когда происходит инфицирование, вирус быстро размножается, провоцируя разрушение печеночных клеток (гепатоциты).
По медицинской статистике, у 10% пациентов с гепатитом процесс хронизируется. Тогда повышается вероятность цирроза и рака печени. Выявить патологию на ранних этапах проблематично, так как выраженные симптомы не наблюдаются. Нередко инфекция протекает без признаков желтухи (окрашивание кои и видимых слизистых оболочек в жёлтый цвет), из-за чего диагностика ещё больше затрудняется.
Вирус проникает в организм через кровь, например, при незащищённом сексе, приёме внутривенных наркотиков, посещении медицинских учреждений или салонов красоты, где используют не продезинфицированные инструменты и т. д.
Во время диагностики большое значение имеют маркеры гепатита B. С их помощью можно выявить заболевание на ранних этапах, определить степень его тяжести и составить грамотную схему лечения.
HBV устойчив к перепадам температуры, замораживанию, кислотной среде. Вирус содержит дезоксирибонуклеиновую кислоту в отличие от других возбудителей заболевания, геном которых представлен РНК (рибонуклеиновая кислота). Инфекционный агент встраивается в структуру гепатоцитов, блокирует синтез нормальных белков, вызывая воспаление печеночных клеток. Патогенные микроорганизмы могут поражать селезёнку, лимфоузлы, костный мозг. HBV тяжело отличить от клеток собственного организма, поэтому он может стать причиной аутоиммунного гепатита.
Анализы на маркеры вирусного гепатита B (ВГВ) и точная их интерпретация даёт возможность подтвердить инфекцию, спрогнозировать её течение, а также оценить силу иммунной реакции.
Цели диагностики для выявления маркеров ВГВ:
- Первичное выявление носителей вируса. Для этой цели определяют показатель HBsAg (показатель заболевания до появления первых симптомов), а также иммуноглобулины класса М (IgM), которые свидетельствуют об острой фазе инфекции.
- Подозрение на гепатит B с хроническим течением. Для выявления антител класса G (IgG), при которых болезнь имеет вялотекущее течение, назначают лабораторные исследования.
- Оценка напряжённости иммунитета. Анализ поможет определить пациентов из группы риска, которые нуждаются в вакцинации, и выявить силу реакции против HBV после иммунизации.
- Контроль над динамикой терапии. После исследования врач может вовремя скорректировать схему лечения.
Чтобы диагностировать болезнь, используют клинические анализы или экспресс-тесты. Они позволяют выявить разные стадии недуга: заражение, выздоровление, развитие.
Справка. Антигены – это чужеродные вещества для организма, при появлении которых образуются антитела. Это белковые молекулы или фрагменты HBV, которые появляются после инфицирования организма. Антитела – это белковые соединения, которые препятствуют размножению вируса и нейтрализуют его токсины.
| Вид маркера | Клиническое значение |
| HBs-Ag | Поверхностный антиген вируса гепатита B. Это компонент оболочки HBV выявляет гепатоциты, в которые будет внедряться вирус. |
| HBe-Ag | Белок вируса, который указывает на его активное размножение. Если результаты диагностики положительные, то это свидетельствует о том, что болезнь обострилась или вероятность инфицирования высокая. |
| HBcore-Ag | Это ядерный антиген ВГВ (размещается в клеточных ядрах), который выявляют во время биопсии печени (прижизненный забор фрагментов тканей). |
| Анти-HBs | Антитела к HBsAg. Когда иммунитет контактирует с белком, то начинают формироваться иммуноглобулины (ИГ), которые мешают ему проникнуть в печеночные клетки. |
| HBe-антиген | Суммарные антитела к HBe, которые обнаруживаются в начале выздоровления. |
| Анти-Hbcor-Ag | Общие антитела к HBcore-Ag. Применяется для выявления гепатита, который давно завершился. |
| Иммуноглобулины класса М к HBcore-Ag | Этот маркер указывает на наличие острой инфекции. |
| Антитела класса G к Hbcor-Ag | При их выявлении речь идёт о текущем или завершившемся ВГВ. |
ДНК вируса гепатита B свидетельствует о присутствии инфекционного агента. При длительном наличии этого маркер инфекция переходит в хроническую форму. Этот показатель указывает на то, что HBV стремительно размножается и разрушает печень. ДНК вируса гепатита B можно выявить на ранних этапах патологии.
HBs Ag – это ранний маркер гепатита В. Его ещё называют австралийским антигеном по той причине, что впервые его выявили у коренных жителей Австралии. Как упоминалось ранее, это внешняя белковая оболочка патогена. У этого генотипа выделяют несколько субтипов: ayw, aur, adw, adrq, adrq+, которые незначительно отличаются строением.
Этот маркер можно обнаружить во время инкубации гепатита или на протяжении 1 – 1,5 месяца после проявления первых симптомов. Если этот показатель обнаруживается в кровотоке более полугода, то повышается вероятность развития хронического ВГВ.
Донорскую кровь рекомендуется проверять на наличие HBs Ag. Однако многие иммуноферментные тесты не позволяют с точностью обнаружить данный маркер у пациентов. Тогда повышается вероятность ложноотрицательного или ложноположительного анализа на гепатит B. Ложноотрицательный результат получают, если исследование проводят через 3 – 4 недели после возможного инфицирования, если болезнь имеет пассивное течение, у пациента низкая концентрация HBs Ag либо редкие субтипы. Ложноположительный результат провоцируют различные факторы: неправильный забор биологического материала, онкологические заболевания и т. д.
Чтобы оценить течение патологии, а также спрогнозировать его исход, важно контролировать систему HBs Ag – анти-HBs. Антитела к поверхностному антигену вируса при гепатите B (острая форма) обнаруживают через длительный промежуток времени после исчезновения HBs Ag.
Если анти-HBs вновь обнаруживаются, то это свидетельствует о том, что постинфекционный иммунитет сформировался. То есть пациент выздоровел после ВГВ.
Если антитела обнаружили во время острого течения инфекции или сразу после того, как исчез HBsAg, то это плохой признак. Тогда повышается риск тяжёлого гепатита B, который сопровождается признаками печеночной энцефалопатии (нервно-психические нарушения вследствие дисфункции печени).
При хроническом ВГВ оба маркеры могут появляться одновременно.
Антитела к HBs могут присутствовать до конца жизни.
Анти-HBsAg – это единственные составляющие иммунной системы, которые обладают защитными свойствами. То есть эти иммуноглобулины защищают организм от повторного инфицирования гепатитом Б.
Сейчас для профилактики инфекции типа В применяют вакцины рекомбинантного HBsAg. Раствор вводят внутримышечно, после чего антитела начинают выделяться спустя 14 дней. Для формирования полноценного иммунитета прививку делают 3 раза.
Вакцинация считается успешной, если уровень антител превышает 100 мМЕ/мл. Через 9 – 12 лет их концентрация может немного снизиться. Если количество иммуноглобулинов не превышает 99 мМЕ/мл, то такая реакция иммунитета считается отрицательной или слабой.
Резистентность к вакцине наблюдается у пациентов с ВИЧ или весом выше 70 кг. По мнению медиков, чтобы достичь адекватных результатов иммунопрофилактики гепатита B, дозу препарата нужно увеличить.
Осторожно . Проводить вакцинацию лиц, которые перенесли ВГВ, не рекомендуется, так как это чрезмерная нагрузка на и без того, ослабленный иммунитет. Поэтому перед прививкой нужно провести исследования на наличие HBsAg, анти-HBs, а также HB core-антител. Если хотя бы один из маркеров присутствует в крови, то вакцинация противопоказана.
При снижении количества антител после иммунизации рекомендуется провести ревакцинацию (повторная прививка). Хотя в большинстве случаев поствакцинальный иммунитет сохраняется, даже если концентрация анти-HBsAg снижается. В дополнительной дозе препарата нуждаются только пациенты с ВИЧ, хронической недостаточностью почек, болезнями печени, а также лица, которым назначили гемодиализ (внепочечное очищение крови).
Этот антиген локализуется только в ядрах печеночных клеток заражённого человека. Обнаружить его можно при биопсии печени, в кровотоке HBcore-Ag не циркулирует. Из-за того что антиген занимает сердцевинное положение в вирусной частице, он обладает высокой иммуногенностью. Именно по этой причине антитела к нему начинают выделяться практически с первых дней болезни, когда внешние симптомы ещё отсутствуют.
Антитела к HBcore-Ag делят на 2 вида: иммуноглобулины класса М (IgM) и G (IgG). IgM выявляют ещё во время латентного периода, когда клинические проявления отсутствуют. Этот маркер свидетельствует о ВГВ с острым течением. Его можно наблюдать от 6 месяцев до 1 года, а после излечения он исчезает. IgM обнаруживают, когда хронический процесс обостряется.
Анализ на IgM и IgG помогает диагностировать гепатит B в «серонегативный» период, когда отсутствую другие HBS-маркеры.
Справка. Иногда HBcore-IgM и IgG могут указывать на заболевания костно-мышечной системы.
Такой антиген гепатита B, как HBeAg обнаруживается в кровотоке во время инкубации или при первых симптомах болезни. Если у больного определяют высокую концентрацию этого маркера, то он требует особого внимания. Если его активность сохраняется на протяжении 3–4 недель, то повышается вероятность перехода инфекции в хроническую форму. Снижение его уровня или полное отсутствие свидетельствует о выздоровлении.
При появлении этого антигена повышается заразность крови и других биологических жидкостей больного. Если острый гепатит протекает легко, то уровень HBeAg уменьшается спустя 20–40 дней после заражения. При этом одновременно повышается концентрация анти-HBe, пока они полностью не замещают антигены.
Быстрое увеличение количества антител свидетельствует о скором выздоровлении, которое исключает возможность перехода инфекции в хроническую форму. Если концентрация данных маркеров низкая или они отсутствуют, то повышается риск хронизации патологического процесса.
Если при гепатите B с хроническим течением количество HBeAg и ДНК вируса повышается, то это говорит о том, что его активная репликативность (способность к воспроизведению подобного себе потомства) сохраняется. Когда уровень антигена и ДНК снижается, речь идёт об интегративном гепатите, когда генный аппарат вируса и гепатоцита объединяются.
Иногда при инфицировании штаммом «е» или мутации инфекционного агента HBeAg может не проявляться, при этом его антитела присутствуют, а способность к размножению сохраняется. Тогда уровень ДНК HBV превышает 10˄5 копий/мл.
После того как человек выздоравливает, антитела к HbeAg сохраняются от полугода до 5 лет.
Лабораторная диагностика гепатита B помогает обнаружить серологические маркеры, ДНК, определить стадию инфекции и спрогнозировать её исход. Наиболее информативным считается анализ крови. Перед исследованием запрещено принимать пищу на протяжении 8 часов до назначенного времени.
Чтобы выявить HBV, применяют следующие анализы:
- ПЦР (полимеразная цепная реакция) для выявления ДНК вируса.
- Качественное выявление антител класса Ig G к Hbc и HBsAg.
- Исследование крови, которое позволяет определить HBeAg и иммуноглобулины класса М к HBcor.
С помощью иммунологических тестов по нескольким маркерам можно дополнить картину:
- Обнаружение вирусных частиц HBsAg может указывать на наличие вируса, хотя нередко их обнаруживают у здоровых людей. Отрицательный результат – до 0,05 МЕ/мл, положительный – более 0,05 МЕ/мл.
- HBe-антиген обнаруживают почти у каждого больного. Этот маркер свидетельствует об остром гепатите и высокой заразности больного. Отсутствие белка – это норма.
- Антитела класса М указывают на острый BГВ, кровь и другие биологические жидкости больного заразны, существует вероятность хронизации процесса. У здорового человека этот маркер отсутствует. Иммуноглобулины класса G свидетельствуют о том, что иммунитет против болезни сформировался.
- Антитела к HBe – это признак благоприятного течения инфекции и формирования иммунной защиты. Такое же значение имеет маркер анти-Hbs.
Метод ПЦР – это современный и высокоинформативный анализ на гепатит Б, который позволяет выявить ДНК HBV в гепатоцитах. Медики выделяют следующие виды исследования:
- Качественное ПЦР назначается при подозрении на ВГВ. Если результаты колеблются от 10 до 500 МЕ/мл, а уровень ДНК низкий, то HBV не обнаружен.
- Количественное ПЦР дает представление о том, насколько показатели крови больного далеки от норм. Это исследование позволяет определить фазу заболевания и составить тактику лечения. Количественный анализ более чувствительный, чем качественный. Врач подсчитывает обнаруженные ДНК, которые выражают в копиях на мл или МЕ/мл.
Чтобы правильно расшифровать анализы, нужно сравнить результаты с нормальными показателями и сопоставить их с присутствующими симптомами гепатита B. При правильной расшифровке качественных и количественных характеристик маркеров гепатита врач выявит инфекцию, определит её стадию, форму и составит прогноз.
| HBsAg | Анти-HBs | HBeAg | Анти-HBe | Антитела класса М к HBc | Антитела класса G к Hbc | HBV ДНК | Заключение |
| +/- | -/+ | +/- | -/+ | + | + | +/- | Гепатит B протекает в острой форме |
| + | — | — | + | — | + | Менее 10? | Пациент является носителем HBV |
| + | — | +/- | -/+ | +/- | + | Более 10? | Инфекция в хронической форме |
| — | + | — | — | — | — | — | У пациента выработался иммунитет после вакцинации |
| — | + | — | +/- | — | + | — | Сформировался иммунитет после перенесённого гепатита |
Гепатит B – это опасная патология, которая не имеет яркой выраженности и часто приобретает хроническое течение. Серологические маркеры помогут выявить недуг даже на ранней стадии, когда вероятность осложнений ещё минимальная. Предупредить ВГВ поможет вакцинация. Чтобы подстраховать себя, рекомендуется время от времени сдавать анализ на маркеры гепатита B.
источник