Это заболевание связано с воспалением печени. Последствия недуга хронический гепатит зависят от степени и активности поражения главного «фильтра организма», о чем не всегда сигнализируют симптомы и признаки. Страшными последствиями болезни является цирроз печени и развитие опухолей. Избежать этого можно, узнав причины возникновения, разновидности и способы лечения.
Недуг характеризуется наличием диффузных воспалительных заболеваний в печени (фильтре организма) на протяжении периода от 6 месяцев и более. Часто это проходит бессимптомно, поэтому человек может и не подозревать о наличии поражения гепатоцитов паренхимы. Если вовремя это не диагностировать, клетки печени замещаются соединительной тканью. Проявляется цирроз, развиваются острые онкологические, желчные расстройства. Не все разновидности заболевания перерастают в хроническую стадию, например, тип А. Инфекционные вариации B и C могут стать такими.
Если ненадлежащим методом проводить лечение реактивного гепатита В, С, D, G, заболевание переходит в хроническую стадию. Тип А стандартно лечится за несколько недель, в организме вырабатывается стойкий иммунитет до конца жизни. Его еще называют болезнью Боткина – желтухой. Основную опасность таит тип С (80%). Помимо этого, недуг развивается по причине таких факторов:
- нарушение обмена веществ;
- аутоиммунный гепатит – передается наследственным путем, сбои в защитных процессах;
- токсические – на организм длительное время воздействуют вредные вещества: алкоголь, лекарственные препараты (тетрациклины, наркотики, противотуберкулезные, седативные), соль, бензолы, тяжелые металлы, радиоактивные элементы.
Три основных типа поражения печени – А, B, C. Первый является распространенным, сначала похож на грипп. Через 2-4 дня кал становится бесцветным, а моча, наоборот, темнеет. Профилактика – соблюдение гигиенических норм. Разновидность Е похожа на А, но тяжелая форма поражает печень и почки. Тип F мало изучен. При вирусной этиологии гепатита D наблюдаются острые внепеченочные симптомы: поражение легких, почек, суставов, мышц. Тип G схож с С, но не приводит к раку, циррозу. Острая форма поражает организм быстро. Классификация хронических гепатитов:
- криптогенный – не изучены запускающие механизмы;
- хронический персистирующий (малоактивный) – развивается при медикаментозных, алкогольных и токсических поражениях печени;
- лобулярный – вариант первого с локализацией патологий в печеночных дольках;
- агрессивный гепатит (хронический активный) – характеризуется некрозами, есть склонность к возникновению цирроза, возникает из-за вирусов гепатитов В, редко С, может иметь медикаментозную, хроническую алкогольную этиологию (природу происхождения).
Для выявления патогенеза хронической болезни врач проводит первичный осмотр. У зараженного человека наблюдается мелкоточечная сыпь, желтоватый цвет кожи, малиновый язык, красные ладони, сосудистые звездочки. Вместе с осмотром производится пальпация в области селезенки, печени: если они увеличены, будут неприятные ощущения при надавливании. Потом назначается УЗИ этих органов для установления неоднородности их структуры. Диагностика хронического гепатита включает в себя в некоторых случаях:
- биопсию печени, чтобы определить тип заболевания, есть цирроз/фиброз или нет;
- общий анализ крови, который подтверждает наличие воспалительных процессов;
- лабораторное серологическое исследование – выявляет определенные маркеры вирусных антигенов;
- биохимический анализ крови – определяет уровень билирубина, печеночных ферментов, из-за которых кожа меняет цвет;
- иммунологическое обследование – выявление антител к печеночным клеткам.
Это жалобы на горечь во рту при холестазе, нарушения испражнения, головные боли, кровоточивость с гематомами, ощущение разбитости, усталости. Чувствуется тяжесть, дискомфорт в области печени – под правым подреберьем. Ноющая боль усиливается после употребления жареной, жирной пищи. Возможно развитие астеновегетативного синдрома – снижение умственной концентрации, работоспособности, сонливость. Клинические проявления иногда включают уменьшение массы тела вследствие нарушений метаболизма, холестатического синдрома.
Терапия разрабатывается с учетом индивидуальных особенностей каждого пациента. Лечебный комплекс определяется степенью активности заболевания, причинами возникновения. Лекарственная терапия дополняется специальной диетой, двигательным режимом. Используются препараты интерферона для того, чтобы подавить хронический вирусный гепатит C. Печень защищается гепатопротекторами, которые восстанавливают структуру ткани в комплексе с витаминами и антиоксидантами, снимают иммунное воспаление. Цель – ремиссия болезни (ослабление).
Он еще называется сывороточным типом. Заражение происходит через кровь, семенную жидкость при половых актах, во время родовой деятельности. Назначаются иммуностимуляторы (к примеру, Тималин, Метилурацил), витамины группы B и С, фолиевая, никотиновая кислота. Печень восстанавливается анаболическими, кортикостероидными гормонами. Дополняется лечение хронического гепатита этого типа лекарствами для защиты печени. После выписки из больницы ежегодно нужно проходить оздоровление в санатории, всю жизнь придерживаться диет.
После анализа степени поражения печени, стадии цирроза, рака, оценки сопутствующих заболеваний назначается индивидуальный курс длительной терапии. В современной практике применяется интерферон и Рибавирин, которые эффективны против всех генотипов недуга. Основная проблема больного инфекцией HCV (тип С) – плохая переносимость препаратов, их высокая стоимость.
Лечение должно начинаться после полного удостоверения в правильности диагноза хронической формы. Выждав 3-6 месяцев, повторно проводится гистологический контроль. Главные элементы терапии – иммуносупрессоры и кортикостероиды. Если лечение прерывается до устранения всех клинических симптомов, возможен рецидив со стадией обострения заболевания. Терапия должна проводиться под строгим контролем врача.
Хронический вирусный гепатит с минимальной степенью активности лечится путем снижения физических и нервных нагрузок. Обеспечивается здоровый сон, спокойная обстановка, правильное питание. При благоприятном протекании заболевания специальная медикаментозная помощь не нужна. Используются противовирусные и иммуномодулирующие препараты. Диспансеризация необходима как профилактическая мера.
Репликация не происходит воздушно-капельным и бытовым способом, поэтому носители вирусов заболевания не представляют опасность. Для защиты важно использовать барьерную контрацепцию, не брать чужие предметы гигиены. Экстренная профилактика типа B – применение иммуноглобулина человека, вакцин. Лекарственные поражения и аутоиммунные формы излечимы, а вирусный хронический гепатит трансформируется в цирроз. Избежать алкогольных поражений поможет исключение спиртного из рациона.
источник
Гепатит С является самым коварным недугом, поражающим печень, поскольку сопровождается долгим скрытым периодом и опасными осложнениями. Софосбувир относится к категории новейших противовирусных препаратов, широко используемых в лечении этого заболевания с 2013 года. По сравнению с предыдущими классами аналогичных медикаментов, он показывает высокую безопасность и эффективность – от 80 до 100% в зависимости от тяжести течения болезни, генотипа вируса, сопутствующих недугов. Однако рецидив гепатита С после лечения Софосбувиром иногда все же случается.
После правильно проведенного курса лечения Софосбувиром пациент в подавляющем большинстве случаев полностью излечивается от того подвида гепатита, которым он был инфицирован. Однако от заражения другим типом того же заболевания он не застрахован.
Вирус гепатита С отличается своей способностью к генетическим мутациям. Всемирная организация здравоохранения насчитывает 6 генотипов возбудителя (ученые говорят об 11), каждый из которых содержит подтипы и квазивиды общим количеством более 100. Поэтому вылечившись от одного вида, человек может быть инфицирован повторно другим генотипом вируса, в результате чего развивается рецидив.
Риск возврата гепатита С после лечения Софосбувиром выше у следующих лиц:
- медицинских работников, имеющих дело с кровью по долгу службы;
- пациентов, находящихся на диализе;
- наркозависимых, из-за многократного использования шприцев;
- детям инфицированных матерей;
- семей заболевших или лиц, имеющих частые контакты с инфицированными людьми;
- ведущих активную половую жизнь со множеством партнеров, гомосексуалистов;
- пациентов, постоянно нуждающихся в переливании крови.

Вероятность повторного инфицирования гепатитом С возрастает в случаях наличия сопутствующих заболеваний, сопровождающихся тяжелым течением (например, ВИЧ), второго типа сахарного диабета, недугов пищеварительного тракта, особенно при хроническом течении. Риск рецидива повышается у пациентов с лишним весом, со значительными повреждениями печени, у женщин в период климакса.
Рецидив гепатита С может произойти в случаях переливания зараженной крови, незащищенных половых актов, при использовании нестерильных шприцев, проведении некоторых процедур, сопровождающихся повышенной травматичностью (маникюр, педикюр, нанесение татуировок, пирсинг).
Иногда возникают ситуации, когда после терапии Софосбувиром пациент не излечивается, поскольку оказывается невосприимчив к лечению. Это бывает нечасто (примерно в 1% случаев), причины такого явления не установлены. Однако даже при том, что болезнь не поддавалась излечению полностью, вирусная нагрузка существенно снижалась. В этих случаях рекомендуется изменить препарат, идущий в паре с Софосбувиром, и скорректировать дозу.
Заболевание может возвращаться также при нарушениях режима лечения Софосбувиром, установленного врачом, неправильных дозировках медикамента, незаконченности курса терапии. При пропуске приема препарата концентрация действующих веществ падает, осложняя лечебный процесс, и гепатит С может вернуться.
После окончания терапевтического курса пациенту положено сдавать анализы на гепатит С каждые три месяца. При возникновении подозрительных признаков необходимо обратиться к врачу, чтобы не упустить время и сразу начать лечиться.
При повторном инфицировании гепатитом С наблюдаются те же симптомы, что и первоначально:

- утомляемость, нервозность, слабость;
- тошнота, рвота, абдоминальные боли, диарея или запор, плохой аппетит;
- субфебрильные значения температуры тела;
- желтушность кожи, склер, слизистых;
- обесцвечивание каловых масс, потемнение урины;
- увеличение печени в размерах.
Рецидив гепатита С после Софосбувира, то есть повторное заражение, протекает в более тяжелой форме. Обострение заболевания связано с ослаблением организма после борьбы с первоначальным возбудителем.
Рецидивирующий гепатит С грозит развитием следующих осложнений:
- Фиброз печени. При недуге наблюдается замещение тканей органа соединительной рубцовой, в результате чего нарушается его функция.
- Гломерулонефрит. Представляет собой поражение почек, ведущее к формированию почечной недостаточности.
- Жировой гепатоз. Обратимая патология, которая сопровождается заменой гепатоцитов на жировые клетки. Может приводить к фиброзу и циррозу печени.
- Онкология. Наличие злокачественных новообразований в органе с плохим прогнозом в случае несвоевременного лечения.
- Неврологические расстройства. Сюда относятся депрессии, ухудшения памяти, внимания и умственной работоспособности.
В случае если гепатит С снова диагностируется у того же человека, назначается повторный курс лечения Софосбувиром или другим противовирусным препаратом. Длительность приема медикамента обычно увеличивается по сравнению с первым разом. Лечить пациента продолжают с учетом тяжести недуга, генотипа вируса, индивидуальных особенностей.
Помимо Софосбувира или других противовирусных средств, направленных на подавление возбудителя гепатита С, назначаются также:
- гепатопротекторы – препараты, останавливающие разрушение клеток печени и способствующие их восстановлению;
- сорбенты для выведения токсинов и устранения признаков интоксикации, иногда назначают совместный прием антибактериальных препаратов, которые призваны блокировать всасывание токсинов кишечником;
- кислота урсодезоксихолевая, чье действие помогает нормализировать уровень билирубина и справиться с неприятными симптомами;
- поливитамины, включающие в себя фолиевую кислоту, витамины С, Е, группы В для поддержания и укрепления иммунитета.

Обязательной частью лечения гепатита С является соблюдение диеты №5 по Певзнеру для того, чтобы максимально разгрузить печень и насытить организм необходимыми витаминами и микроэлементами. Она предусматривает дробное питание около 5 раз в день. Уменьшается процент жира, соли в рационе, исключаются продукты, провоцирующие брожение и гнилостные процессы в кишечнике, копченые, консервированные, слишком холодные или горячие блюда, алкоголь. В основе питания должны лежать нежирные сорта мяса и рыбы, крупы, овощи и фрукты, молочные продукты, каши.
Для недопущения развития рецидива гепатита С после лечения Софосбувиром необходимо соблюдать меры предосторожности:
- предохраняться барьерными методами контрацепции при интимных контактах;
- перед проведением травмоопасных процедур необходимо убедиться в том, что используются одноразовые или хорошо простерилизованные инструменты;
- пользоваться услугами надежных стоматологических клиник и салонов красоты;
- исключить многократное использование шприцев;
- избегать контактов с биологическими жидкостями инфицированных людей;
- пользоваться индивидуальными гигиеническими и другими личными принадлежностями (щетками для чистки зубов, ножницами, бритвами).

Поскольку после прохождения курса лечения гепатита С организм пациента ослаблен, для снижения вероятности повторного инфицирования необходимо придерживаться таких профилактических рекомендаций, как соблюдение режима умеренных физических нагрузок, диеты для восстановления работы пищеварительного тракта, отказ от алкоголя.
источник
Сокращения: EASL — Европейская ассоциация по изучению печени; EMA — Европейское агентство по лекарственным средствам; FDA — Управление по контролю за качеством пищевых продуктов и лекарственных средств США; HBcAg — сердцевинный антиген вируса гепатита B; HBsAg — поверхностный антиген вируса гепатита B; ВГВ — вирус гепатита B; ВГС — вирус гепатита C; АлАТ — аланинаминотрансфераза; IFN — интерферон; НА — нуклеоз(т)идные аналоги; пгРНК — прегеномная РНК; ПППД — противовирусные препараты прямого действия; ПЦР — полимеразная цепная реакция.
Европейская ассоциация по изучению печени (EASL) опубликовала рекомендации по лечению гепатитов C и B [1, 2]. Безинтерфероновая терапия противовирусными препаратами прямого действия (ПППД) сегодня служит стандартом лечения гепатита C на всех стадиях болезни, однако связана с риском реактивации вируса гепатита В (ВГВ) как у HBsAg-позитивных, так и у HBsAg-негативных пациентов со скрытым гепатитом B [3]. Реактивация ВГВ у пациентов с гепатитом C, получающих лечение ПППД, биологически возможна, поскольку ПППД прекращают репродукцию вируса гепатита С (ВГС), удаляя его из гепатоцитов в течение нескольких недель, если не дней, в зависимости от эффективности неспецифического противовирусного иммунного ответа. В связи с этим любое прямое вмешательство ВГС в репродукцию ВГВ внезапно блокируется, вызывая потенциальное нарушение равновесия при наличии внутрипеченочного репродуктивного пространства для последнего. Более того, гепатоцеллюлярная регенерация вследствие элиминации ВГС может еще больше расширить количество клеток, доступных для инфицирования ВГВ. Этот эффект был менее выражен при терапии на основе интерферона (IFN) за счет свойственной IFN активности против ВГВ [4]; отсутствие действия ПППД, направленных против ВГС, на ВГВ означает, что этот вопрос сегодня вызывает беспокойство и ведет к соответствующим предупреждениям от Управления по контролю за качеством пищевых продуктов и лекарственных средств США (FDA) и Европейского агентства по лекарственным средствам (EMA).
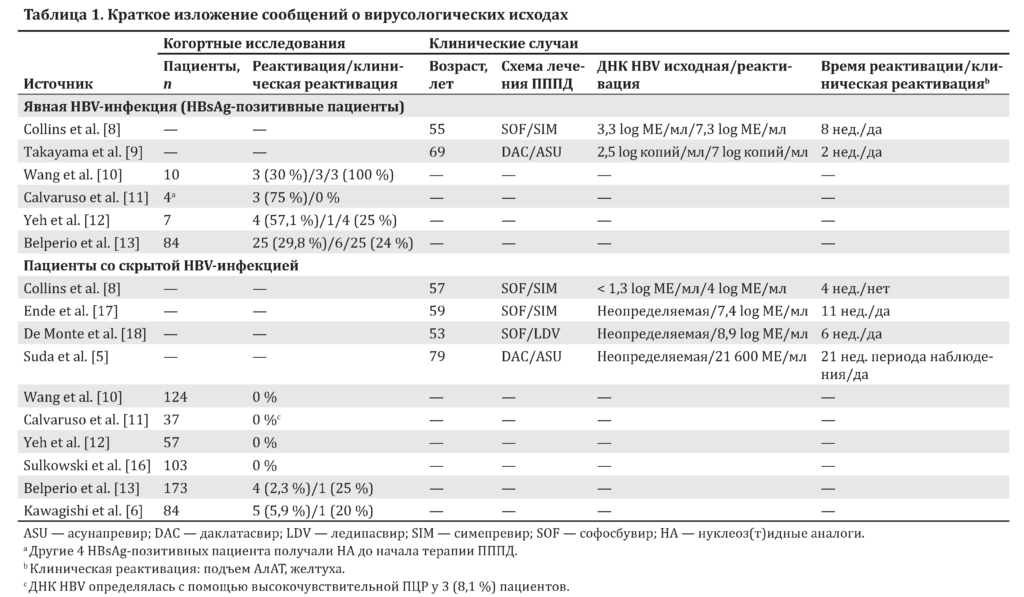
Suda et al. [5] и Kawagishi et al. [6] сообщают о новых случаях реактивации ВГВ у пациентов с гепатитом C, получающих лечение ПППД. Чтобы прояснить риск реактивации и оценить наилучший подход к лечению таких пациентов, необходимо разделение между двумя различными группами пациентов с гепатитом C: теми, у кого гепатит B очевиден (HBsAg-позитивные), и теми, у кого инфекция ВГВ скрыта (по большей части позитивность по антителам к HBcAg в отсутствие HBsAg).
В целом распространенность смешанной инфекции, вызванной ВГВ и ВГС, колеблется от 2 до 10 % у пациентов, позитивных на антитела к ВГС [7]. На заре безинтерфероновой эры некоторые группы ученых сообщали о реактивации ВГВ у лиц со смешанной инфекцией, получающих ПППД [8–11]. Collins et al. [8] описали пациента со смешанной инфекцией, у которого после 8 нед. применения софосбувира и симепревира имел место подъем активности аланинаминотрансферазы (АлАТ) до 1495 МЕ/л и появилась желтуха (общий билирубин 12,2 мг/дл). Takayama et al. описывали реактивацию ВГВ на 15-е сутки применения даклатасвира и асунапревира с подъемом активности АлАТ до 237 МЕ/мл и повышением уровня ДНК ВГВ с 2,5 до 7 log копий/мл [9]. В обоих случаях терапия нуклеоз(т)идными аналогами (НА) купировала обострение гепатита B. После этих случаев FDA и EMA выпустили предупреждения о риске реактивации у пациентов, получающих ПППД по поводу гепатита C (сообщение FDA по безопасности препаратов «Реактивация ВГВ у некоторых пациентов, получающих ПППД для лечения гепатита C» от 4 октября 2016 г. и информационное письмо EMA 263596/2016 от 5 апреля 2016 г.).
После сообщений о первом случае 4 обсервационных исследования проанализировали распространенность явной ВГВ-инфекции у пациентов с гепатитом C, которых планировали лечить ПППД, и оценили частоту реактивации ВГВ. Wang et al. сообщили о распространенности 3,1 % у пациентов, позитивных на HbsAg, из группы 327 пациентов, получающих ПППД для приема внутрь для лечения гепатита C. 3 (30 %) из 10 пациентов, позитивных на HBsAg, имели гепатит: один — без желтухи, другой — с желтухой и третий — с печеночной недостаточностью; и все эти случаи были связаны с реактивацией ВГВ [10]. Второе исследование [11] сообщило о 8 (7,7 %) случаях у пациентов, позитивных на HBsAg из группы 104 пациента с гепатитом C и циррозом, получавших лечение ПППД. 4 пациента получали НА и оставались негативными на ДНК ВГВ во время и после терапии гепатита C. 3 (75 %) из 4 неактивных носителей, оставленных без лечения по поводу гепатита B на момент начала терапии ПППД, стали позитивными на ДНК ВГВ в течение первых 4 нед. терапии гепатита C, и уровень ДНК ВГВ у них вырос на 2–3 log без биохимических признаков обострения. Немедленно была начата терапия НА и достигнуто подавление ДНК ВГВ.
Третье исследование за авторством Yeh et al. [12] проанализировало 64 пациентов с хроническим гепатитом C с ВГВ-инфекцией в настоящем (7 пациентов) и прошлом (57 пациентов). Из 7 пациентов с текущей ВГВ-инфекцией вирусологическая реактивация ВГВ была обнаружена у 4 (57,1 %); 1 пациент имел клиническую реактивацию ВГВ, которая прошла после назначения энтекавира. В самом последнем исследовании, проведенном Belperio et al. [13], были ретроспективно оценены 62 290 больных гепатитом С после завершения терапии ПППД. Из 377 (0,6 %) пациентов, которые были HBsAg-позитивными до начала терапии ПППД, 96 (25,5 %) получали лечение от гепатита B на момент начала терапии ПППД.
Во время лечения ПППД тестирование на ДНК ВГВ было проведено у 22,3 % (84 из 377) пациентов, позитивных на HBsAg, и у 30 (35,7 %) из них ДНК ВГВ определялась.
Всего у 25 (29,8 %) пациентов имело место повышение уровня ДНК ВГВ, у 8 пациентов была реактивация ВГВ, определяемая как повышение уровня ДНК ВГВ > 1000 МЕ/мл от исходного, 6 из них также имели высокую активность аминотрансфераз. На эту тему также опубликован метаанализ [14]. Авторы сравнили пациентов с гепатитом C и явной ВГВ-инфекцией, получавших IFN vs ПППД, и сделали вывод, что объединенная частота реактивации ВГВ была одинаковой у пациентов, получавших терапию на основе IFN и ПППД (14,5 vs 12,2 %), но у пациентов, получавших ПППД, она возникала значительно раньше (во время лечения), чем у пациентов, получавших терапию на основе IFN (в конце лечения и во время периода наблюдения).
Исходя из этих данных, EASL рекомендует рассматривать пациентов, позитивных на HBsAg, получающих терапию ПППД, как кандидатов на одновременную профилактику с помощью НА и требующих тщательного наблюдения (степень рекомендации 2). Однако следует заметить, что большинство пациентов с ВГС/ВГВ-коинфекцией и выраженным поражением печени получают эффективную терапию НА, что устраняет риск реактивации.
Оценки риска реактивации ВГВ у пациентов с гепатитом C и предшествовавшим контактом с ВГВ более противоречивы, а рекомендации менее строги. Возможности, предлагаемые ПППД в лечении пациентов с тяжелым поражением печени, имеющих высокую вероятность носительства скрытой ВГВ-инфекции, делают вопрос еще более релевантным. Действительно, доля пациентов с хроническим гепатитом C и серологическими свидетельствами предшествующего контакта с ВГВ, определяемыми наличием антител к HBcAg в отсутствие HBsAg, колеблется от 30 до 60 % [7, 15].
Данные первых 3 когортных исследований, проведенных с учетом этих обстоятельств, могут быть суммированы следующим образом: эпизодов вирусологической реактивации ВГВ во время терапии ПППД не было у 124, 37 и 57 пациентов с инфекцией ВГВ в прошлом, наблюдавшихся Wang et al., Calvaruso et al. и Yeh et al. соответственно. Дальнейший анализ с использованием высокочувствительной ПЦР показал определяемый уровень ДНК ВГВ у 8 % пациентов итальянской когорты [11]. Кроме того, анализ образцов сыворотки 103 пациентов, ранее инфицированных ВГВ и пролеченных в клиническом исследовании ледипасвира-софосбувира в Тайване и Корее, не обнаружил ни одного случая реактивации ВГВ [16]. Согласно этим результатам, мы можем сделать вывод, что реактивация ВГВ не представляет проблему у пациентов без активного гепатита B.
Однако 2 наблюдения в Японии (1 клинический случай и 1 когортное исследование) содержат новейшие сообщения о реактивации ВГВ у пациентов, излеченных от гепатита B [8, 17, 18].
Suda et al. [5] сообщают о случае у 79-летней женщины, инфицированной ВГС генотипа 1b, у которой случилась реактивация ВГВ через 21 нед. после эрадикации ВГС с помощью ПППД. Исходная оценка показала, что пациентка была HBsAg-негативна, имела антитела к HBsAg и HBcAg и неопределяемый уровень ДНК ВГВ. В отличие от прежде опубликованных сообщений, показавших, что репродукция ВГВ происходит в первые недели терапии ПППД, в данном случае наблюдалась поздняя реактивация ВГВ. Авторы измерили количество прегеномной РНК (пгРНК), транскрибируемой с генома ВГВ в образцах печени, полученных до начала терапии ПППД. Они выявили пгРНК ВГВ как до, так и после лечения даклатасвиром/асунапревиром, что подтверждает диагноз реактивации.
Kawagishi et al. [6] проанализировали данные 84 пациентов, которые были излечены от гепатита B (HBsAg- и ДНК ВГВ-негативные и позитивные на антитела к HBcAg и HBsAg), и выявили 5 (5,9 %) случаев с определяемой ДНК ВГВ во время лечения, но только 1 случай с повышением активности аминотрансфераз.
Несмотря на то что гепатит, вызванный реактивацией ВГВ, не наблюдался, 2 пациента с повторным появлением ВГВ и эрадикацией ВГС имели виремию ВГВ на 8-й и 12-й неделях после завершения терапии соответственно, что позволяет предположить персистенцию репродукции ВГВ после элиминации ВГС. В этом исследовании пациенты были старше 65 лет и не имели факторов иммунной недостаточности. Ретроспективное исследование, проведенное Belperio et al. [13], показало частоту определяемости ДНК ВГВ 2,3 % (4 из 173 пациентов) у пациентов, позитивных только на антитела к HBcAg на фоне терапии ПППД.
Клинически реактивация ВГВ часто протекает легко. Между тем в 2015 г. у 59-летней женщины с хроническим гепатитом C генотипа 1b и изолированной позитивностью на антитела к HBcAg, начавшей лечение симепревиром, софосбувиром и рибавирином, развилась фульминантная форма реактивации ВГВ , приведшая к трансплантации печени на 11-й неделе запланированного 12-недельного курса [17]. В силу ранее обсуждавшихся данных пациентам, позитивным на антитела к HBsAg и HBcAg, показан мониторинг активности сывороточных аминотрансфераз.
В заключение отметим, что реактивация ВГВ — частое явление у пациентов со смешанной инфекцией, вызванной ВГВ и ВГС, но она может возникать и у пациентов, излечившихся от гепатита B (табл. 1). Таким образом, пациентов важно проверять на HBsAg, антитела к HBcAg и HBsAg, чтобы назначить терапию НА, если определяется HBsAg или если ДНК ВГВ определяется у пациентов со скрытым гепатитом B. Низкий риск реактивации у пациентов, ранее контактировавших с ВГВ, позволяет ограничиться отслеживанием активности сывороточных аминотрансфераз и оценкой уровня ДНК ВГВ в случае повышения активности печеночных ферментов.
Реактивация ВГВ часто происходит во время терапии гепатита C ПППД, однако описаны и случаи поздней реактивации (после окончания терапии), что означает, что нужно продолжать наблюдение пациентов после элиминации ВГС. Схемы ПППД и генотип ВГС, по-видимому, не влияют на риск реактивации. В литературе не описаны случаи реактивации ВГВ у пациентов с недостаточностью иммунитета, и роль количественного уровня HBsAg у HBsAg-позитивных пациентов остается неясной.
Целесообразны дальнейшие исследования, направленные на выявление надежных прогностических факторов реактивации ВГВ.
VC — гранты на поездки; выступления и участие в консультативных комиссиях для компаний AbbVie, BMS, Gilead Sciences и Intercept; грант и поддержка исследований от MSD.
AC — исследовательские гранты, гонорары за чтение лекций, участие в консультативных комиссиях, научные консультации для компаний Abbvie, Gilead Sciences, BMS, MSD, Intercept.
источник
Особенности структуры и репликации вируса гепатита В описаны в главе 3.
Эпидемиология. Примерно 5% населения Земли – это хронические носители HBV. Распространенность этого вируса широко варьирует в различных отделах земного шара и составляет от 8% до 15% на Дальнем, Среднем Востоке и в Африке и только 0,2% — 1% — в Западной Европе и США (рис.4.1). Россия относится к странам со средней степенью распространенности HBV инфекции (
7%). Заболеваемость гепатитом В в России растет: в 1991 г. она составляла 17.9 на 100 тыс. населения, а к 1999 г. увеличилась до 43.5 на 100 тыс. населения. Параллельно увеличивается частота носительства HBV инфекции: с 2.1. на 100 тыс. в 1992 г. до 82.0 на 100 тыс. в 1999г. В эпидемический процесс интенсивно вовлекаются люди молодого возраста (15 — 30 лет), на долю которых приходится около 90% от общего количества заболевших этой инфекцией. Объяснить такой возрастной состав могут доминирующие пути передачи HBV инфекции в настоящее время: внутривенная наркомания и половой путь. В 1999 г. половым путем заразилось 51.5%, при внутривенном введении наркотиков – 30.1% лиц. Молодые люди в возрасте до 30 лет по данным формы Госстатучета №2 составляют 80% умерших от гепатита В. 42% летальных исходов обусловлено одновременным инфицированием HBV, HCV и HDV. Следует отметить, что удельный вес внутрибольничной заболеваемости HBV-инфекцией в структуре общей заболеваемости населения ежегодно снижается: от 34.1% в 1993г. до 3.3% в 1999г.
Рис. 4.1. Географическое распределение хронических носителей HBC-инфекции
Пути передачи HBV и группы риска инфицирования описаны в главе 3.
Риск хронизации острого гепатита В напрямую связан с возрастом пациента в момент инфицирования. У взрослых с нормальной иммунной системой ХГВ развивается менее, чем в 5% случаев. Среди детей, инфицированных в возрасте от 1 до 5 лет, хронический процесс возникает в 30% случаев, для новорожденных эта цифра возрастает до 90%. Приблизительно у 0,1 – 0,5% больных с острым гепатитом В развивается фульминантная печеночная недостаточность, смертность от которой без трансплантации печени составляет 80%.
Течение HBV инфекции. Естественное течение HBV-инфекции определяется взаимоотношениями вируса и иммунного ответа организма. Дополнительное значение имеет возраст пациента в момент его инфицирования. Прогрессированию заболевания могут способствовать пол (см. ниже), употребление алкоголя и сочетание HBV с другими вирусами гепатитов.
В целом, хроническая HBV инфекция разделяется на две фазы: ранняя репликативная фаза с острым процессом в печени и поздняя нерепликативная фаза с ремиссией заболевания (рис. 4.2).
Рис. 4.2. Естественное течение хронической HBV-инфекции
Для детей, инфицированных внутриутробно, выделяют дополнительную фазу — иммунной толерантности, при которой репликация вируса не сопровождается какими-либо симптомами заболевания.
У внутриутробно инфицированных больных первая фаза инфекции характеризуется высоким уровнем репликации HBV (наличие HBeAg и HBV DNA в сыворотке крови) без клинических признаков болезни, с нормальным уровнем АЛТ и минимальными изменениями при биопсии печени. Это объясняется иммунной толерантностью организма к HBV, причины которой окончательно не известны.
Переход ко второй фазе (иммунного клиренса) у этих больных происходит в возрасте от 15 до 35 лет. Данный процесс сопровождается спонтанным клиренсом HBeAg, средняя частота которого составляет 10% -20% в год (рис. 4.2, б). Иммунный клиренс может протекать бессимптомно, или сопровождаться клиническими признаками ОГВ. Иногда в этот период появляются антитела класса IgM к HBcAg, что может быть причиной неправильной диагностики ОГВ у ранее нераспознанных носителей инфекции. Такие обострения заболевания приблизительно в 2,5% случаев приводят к его декомпенсации или фульминантной печеночной недостаточности. Предполагается, что пусковым фактором иммунного клиренса инфекции является увеличение вирусной нагрузки или изменения в презентации вирусных антигенов иммунокомпетентным клеткам.
Клинические обострения не всегда сопровождаются сероконверсией HBeAg и исчезновением HBV DNA. Недостаточный иммунный ответ в некоторых случаях приводит к прекращению иммунного клиренса инфекции, в результате чего формируется хроническое рецидивирующее заболевание. Повторные эпизоды некровоспалительной активности могут приводить к формированию цирроза печени и повышать риск развития гепатоцеллюлярной карциномы (ГЦК). Рецидивирующее течение заболевания чаще встречается у мужчин, чем у женщин. Причина этого факта не ясна.
Инфицированные во взрослом возрасте пациенты чаще имеют следующий тип течения хронической инфекции (рис. 4.2, а): во время первой репликативной фазы имеются клинические признаки заболевания, повышение уровня АЛТ и наличие HBeAg и HBV DNA в сыворотке крови; при гистологическом исследовании ткани печени — картина хронического гепатита. Частота спонтанной сероконверсии HBeAg также составляет в среднем 10 – 20% в год. Однако, рецидивы обострений значительно реже сопровождаются сероконвесией HBeAg в anti-HBe.
Во время третьей фазы заболевания у перинатально инфицированных и второй фазы у инфицированных взрослых происходит сероконверсия, т.е. пациенты становятся HBeAg-негативными и у них появляются anti-HBe. В этот период заболевание входит в фазу ремиссии, хотя в сыворотке крови может сохраняться и циркулировать HBsAg. Частота отсроченного клиренса HBsAg в среднем составляет 0,5 – 2% в год.
В целом, при заражении HBV последовательность событий такова: из числа всех инфицированных лиц приблизительно 70% — 80% становятся бессимптомными носителями, у 10 – 30% формируется хронический гепатит; самостоятельное разрешение хронической HBV инфекции также возможно. За 10 – 50 лет существования хронического гепатита у пациента может сформироваться цирроз печени, что служит фоном для развития ГЦК. Риск развития ГЦК составляет, в среднем, 4% в год у больных с ЦП (рис. 4.3).
Рис. 4.3. Течение гепатита B
Клиническая картина. В странах с низкой и средней частотой распространенности HBV инфекции приблизительно 1/3 –1/2 больных ХГВ в прошлом переносят клинически манифестный ОГВ, который постепенно прогрессирует в хроническую форму. Оставшиеся пациенты, а также лица с ХГВ, проживающие в эндемичных для этой инфекции зонах, часто не имеют анамнестических указаний на острую фазу инфекции.
В эндемичных районах основной путь заражения HBV – вертикальный: от инфицированной матери к ребенку. В результате в таких регионах у 9 человек из 10 от всех инфицированных к моменту достижения ими взрослого состояния уже имеется хроническая инфекция.
Специфических симптомов хронической HBV инфекции не существует (табл. 4.1). У большинства больных вообще отсутствуют какие-либо клинические признаки заболевания.
Таблица 4.1. Симптомы HBV инфекции (большинство пациентов с ХГВ не имеют никаких клинических симптомов заболевания)
| Острый гепатит В | Хронический гепатит В |
|---|---|
| Утомляемость или гриппоподобный синдром | Симптомы, аналогичные ОГВ |
| Тошнота, эпигастральная боль | Мышечные и суставные боли |
| Диарея | Слабость |
| Кожная сыпь | Симптомы и стигмы цирроза печени |
| Желтуха | Симптомы и стигмы рака печени |
| Темная моча, светлый кал |
Основной симптом хронического гепатита – немотивированная слабость или недомогание. Иногда пациенты ощущают боль или дискомфорт в правом верхнем отделе живота или эпигастральной области. ХГВ в фазе репликации HBV по своему течению может походить на острый гепатит В. В таких случаях больные ощущают утомляемость, отсутствие аппетита, тошноту, появляется желтуха. Иногда развивается печеночная декомпенсация.
При физикальном осмотре можно не обнаружить никаких специфических признаков или выявить стигмы хронического заболевания печени, например, пальмарную эритему, сосудистые звездочки или умеренную гепатомегалию. Для больных с циррозом печени характерна спленомегалия. Прогрессирование заболевания приводит к появлению осложнений цирроза печени в виде варикозного расширения вен пищевода и желудка с возможностью кровотечений из них, асцита, периферических отеков, энцефалопатии.
Внепеченочные проявления хронической HBV инфекции. Приблизительно у 10-20% больных встречаются внепеченочные проявления хронической HBV инфекции. Считается, что они вызываются циркулирующими иммунными комплексами, хотя их истинное происхождение окончательно не известно.
Сывороточная болезнь. Иногда начало острого гепатита В подобно сывороточной болезни с лихорадкой, артралгиями, артритами и кожной сыпью. При кожной и суставной манифестации болезни быстро присоединяется желтуха.
Нодозный периартериит. У 10 – 50% больных с нодозным периартериитом обнаруживается HBsAg. Иммунные комплексы, содержащие антигены и антитела к HBV рассматриваются в качестве триггера поражения сосудов. В патологический процесс могут вовлекаться крупные, средние и мелкие артерии с поражением сердечно-сосудистой системы (перикардит, артериальная гипертензия, сердечная недостаточность), почек (гематурия, протеинурия), гастроинтестинального тракта (васкулит мезентериальных сосудов с болями в животе), костно-мышечной системы (артралгии и артриты), нервной системы (мононевриты или поражения ЦНС), кожи (сыпь).
Гломерулонефрит. HBV-опосредованный гломерулонефрит чаще встречается у детей. Морфологически это мембранозная, мембранознопролиферативная формы или IgA-опосредованная нефропатия. При манифестации заболевания поражением почек изменения в печени редко бывают тяжелыми. Приблизительно у 30 – 60% детей с HBV опосредованным мембранозным гломерулонефритом развиваются спонтанные ремиссии. Лечение кортикостероидами, как правило, неэффективно и способствуют репликации HBV. Положительные результаты лечения интерфероном показаны в нескольких клинических исследованиях, но они значительно ниже у взрослых, чем у детей. Приблизительно у 30% больных заболевание может прогрессировать с развитием почечной недостаточности, в среднем,10% их них будут требовать постоянного гемодиализа.
Эссенциальная смешанная криоглобулинемия. Смешанная крио-
глобулинемия – системное заболевание с вовлечением в патологический процесс преимущественно мелких сосудов, проявляющееся гломерулонефритом, артритом и пурпурой. В криоглобулинах обнаруживают HBsAg, HBsAb и HBV -подобные частицы. Однако, последние исследования ставят под сомнение связь эссенциальной смешанной криоглобулинемии с HBV и указывают на строгую ассоциацию между этим состоянием и хронической HCV инфекцией.
Болезнь Джанотти (папулезный акродерматит). Клинически проявляется симметричной макулопапулезной эритематозной сыпью на ногах, ягодицах, предплечьях, сохраняющейся от 15 до 20 дней, иногда сопровождающейся лимфоаденопатией. В патогенезе патологического процесса играют роль циркулирующие иммунные комплексы, содержащие HBsAg и антитела к нему. У детей эта форма заболевания всегда строго ассоциируется с выявлением HBsAg в сыворотке крови.
Апластическая анемия. В литературе описаны тяжелые случаи апластической анемии в ранней фазе ОГВ. Однако, результаты недавних исследований показали, что ассоциированная с гепатитом апластическая анемия развивается по иммунопатологическому механизму и патогенетически напрямую не связана с вирусом.
источник
Вирусный гепатит – это инфекционное заболевание, сопровождающееся сильной интоксикацией организма и поражением печени. Вирусный гепатит вызывается вирусом инфекционного гепатита. Его возбудители довольно устойчивы, выдерживают нагревание до 56 °С в течение 30 минут, не поддаются высушиванию, устойчивы к воздействию низких температур, ультрафиолетовых лучей и химических веществ. В крови больного вирусы могут сохраняться достаточно продолжительное время. Источниками инфекции являются вирусоноситель и больной человек.
Больные представляют опасность с конца инкубационного периода, в преджелтушный период и первую декаду желтушного периода. Вирус инфекционного гепатита имеет оральный путь передачи. В организм он попадает через загрязненные руки, предметы быта и т. д. Кроме того, встречаются вспышки вирусного гепатита в результате употребления инфицированных продуктов и воды.
Следует отметить, что особенно высока восприимчивость к данному заболеванию у детей 2-10 лет. У грудных детей имеется врожденный иммунитет к данному заболеванию.
Когда в организм проникает вирус инфекционного гепатита, он попадает в желудочно-кишечный тракт, задерживается в тонком кишечнике, после чего проходит в регионарные лимфатические узлы, где и размножается. После этого вирус попадает в кровь, а через нее – в печень. Именно в этом органе протекает основной патологический процесс.
Инкубационный период при вирусном гепатите может продолжаться 15-45 дней, однако в основном он длится 20 дней. Принято выделять 4 периода заболевания: преджелтушный, желтушный, послежелтушный и восстановительный. Первый период характеризуется симптомами, свойственными многим вирусным инфекциям (острая интоксикация организма, сопровождающаяся поражением центральной нервной системы). Больные жалуются на общую слабость и головную боль, у них поднимается температура, наблюдается тахикардия. В отдельных случаях на фоне высокой температуры начинается рвота.
На этом этапе поражений печени не наблюдается. Нередко больные жалуются на боли в области правого подреберья. Довольно редко заболевание начинается проявлениями «острого живота». После окончания инфекционной стадии температура больного опускается до нормальной. В то же время продолжается интоксикация с симптомами печеночной недостаточности. Следует отметить, что патологические явления наблюдаются на фоне нормальной температуры тела.
В этот период наблюдается снижение аппетита, тошнота, рвота и головокружение. Одновременно происходит увеличение печени, больной жалуется на ощущение тяжести в правом подреберье.
Затем наступает желтушный период, симптомом которого является желтуха. В этот период печень и селезенка сильно увеличены в размерах, усилена пигментация кожи, нарушен белковый и углеводный обмен, а также обмен жиров и витаминов. В результате в организме больного нарушается водно-солевой баланс, а печень не может выполнять дезинтоксикационные функции.
Температура в начале желтушного периода, как правило, нормальная. Потом начинаются так называемые температурные свечи, сопровождающиеся сопутствующими осложнениями воспалительного характера.
В результате развития заболевания поражается сердечно-сосудистая система: у больных отмечается тахикардия, брадикардия, систолический шум, глухость сердечных тонов. Исследование крови показывает снижение гемоглобина и понижение СОЭ. У взрослых пациентов наиболее заметны изменения количества белых кровяных телец, проявляющиеся лейкопенией или лейкоцитозом.
Показатель выздоровления больного – снижение содержания билирубина до нормы в сыворотке крови. В послежелтушный период самочувствие больных улучшается, билирубин находится в пределах нормы, однако еще некоторое время наблюдается ряд клинических и биохимических изменений в организме. Этот период может продолжаться до 3 месяцев, а период выздоровления, как правило, затягивается еще на несколько месяцев. Без оказания своевременной медицинской помощи заболевание принимает хронический характер.
Вирусный гепатит может проявляться в легкой, среднетяжелой и тяжелой форме. В первом случае признаки интоксикации организма выражены слабо, а изменения биохимических показателей незначительны. Среднетяжелая форма характеризуется резким ухудшением состояния больного. Он быстро утомляется, чувствует вялость и сонливость, при аускультации прослушивается глухость сердечных тонов. Печень болезненна, а биохимические изменения сохраняются очень долго.
Что касается тяжелой формы вирусного гепатита, она длится достаточно долго. Преджелтушный период в этом случае короткий, сопровождается явлениями острой интоксикации. Кроме того, быстро нарастают симптомы печеночной недостаточности. Больные беспокойны, раздражительны, жалуются на сильную головную боль и болезненные ощущения в правом подреберье.
У них наблюдаются нарушения аппетита и сна, сердечная недостаточность и тахикардия, интенсивные проявления желтухи. Следует учитывать, что на фоне данного заболевания может развиться злокачественная форма гепатита, осложнениями которой являются прекома и кома.
Прекоматозное состояние больных сопровождается учащенным дыханием, тахикардией, тошнотой и рвотой. Затем в результате печеночной недостаточности развивается коматозное состояние с выраженными изменениями со стороны центральной нервной системы. У больных возникает психомоторное возбуждение, бред, клонические судороги, а также рвота с примесью крови.
Затем могут возникнуть носовые и кишечные кровотечения. Язык больного сухой и обложенный, лицо отечное, кожные покровы имеют желтый цвет. Живот больного мягкий, но вздутый, печень заметно уменьшена в размерах. При перечисленных симптомах может наступить смерть из-за токсической дистрофии печени. В случае медленного развития процесса летальный исход наступает несколько позже.
Следует учитывать, что у переболевших вирусным гепатитом возможны рецидивы данного заболевания. При этом отмечается повторный синдром гепатита. Обострения в основном появляются после внедрения в организм вирусной или микробной инфекции, нарушения режима питания или использования медикаментозных средств, непереносимых поврежденными клетками печени.
Наиболее опасны ранние рецидивы, которые могут возникнуть в первые три месяца после заболевания. Такие рецидивы приводят к развитию комы. Рецидивы вирусного гепатита способствуют его переходу в хроническую форму, течение которой существенно осложняется такими сопутствующими заболеваниями, как отит, ангина, ринит, пневмония.
Прогноз при вирусном гепатите, как правило, благоприятный. У большинства больных наступает полное выздоровление. Этиотропной терапии данного заболевания не существует. В этом случае важным условием является соблюдение больным правильного режима питания. Категорически запрещается употреблять жирную, жареную, копченую, пряную пищу, а также шоколад и алкоголь.
Переболевший желтухой первое время должен пить как можно больше жидкости (до 3 л в сутки) и получать комплексную витаминотерапию. При тяжелых формах вирусного гепатита проводится инфузионная терапия: внутривенно вводят 5%-ный раствор глюкозы, гемодез.
В случае развития печеночной недостаточности используются кортикостероиды. Необходимо также проводить профилактические мероприятия, которые включают тщательное соблюдение правил личной гигиены, контроль за качеством продуктов питания и водоснабжением.
В статье использованы материалы из открытых источников: Автор: Виктор Зайцев
По материалам: health-medicine.info
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
источник
Этиология. В настоящее время уже доказано существование семи относящихся к различным группам вирусов, которые являются возбудителями одноименных вирусных гепатитов (ВГ): A, B, C, D, E, F, G
Особенности вирусов – возбудителей вирусных гепатитов
| Особенности | A | B | C | D | E |
| Групповая принадлежность | Пикорна-вирус (энтеровирус 72) | Гепадна-вирус | Флави-вирус | Рибозин (дефектный вирус) | Калици-вирус |
| Нуклеиновая кислота вируса | РНК | ДНК | РНК | РНК | РНК |
| Устойчивость при кипячении | погибает через 5 мин | 30–40 мин | 30–40 мин | 3–5 мин | 3–5 мин |
| Место репликации вируса | в протоплазме пораженной клетки | в ядре | в протоплазме | в ядре | в протоплазме |
| Связь с онкологическими заболеваниями | – | + | + | + | – |
Эпидемиология. Все вирусные гепатиты являются антропонозами (источник инфекции — исключительно человек). При ВГА и ВГЕ максимум заразительности приходится на последние дни инкубационного периода и первые дни преджелтушного периода, механизм передачи фекально-оральный (чаще факторами передачи являются вода и пища). При ВГВ и ВГС больные заразны все время, пока в крови у них присутствует вирус (при хроническом течении годами), основной путь передачи — парентеральный (через кровь), при ВГВ регистрируются также вертикальный и половой пути. Для гепатитов А и Е характерна летне-осенняя сезонность. Иммунитет после перенесенного заболевания пожизненный типоспецифичесикй.
Патогенез. Основные патогенетические особенности ВГ обусловлены нарушением функции гепатоцитов главной мишени вирусов. Механизм повреждения гепатоцитов различен при ВГ различной этиологии. При ВГА происходит непосредственное воздействие вируса, проникшего в клетку, размножение вируса приводит к ее гибели. В случаях ВГВ главная роль принадлежит иммунным реакциям иммунный цитолиз с участием Т-лимфоцитов-киллеров, в дальнейшем антителозависимый иммунный цитолиз, аутоиммунные реакции. При ВГС многие механизмы сходны с таковыми при ВГВ, но HCV способен, в отличие от HBV, и сам вызывать цитопатогенное действие, подобно HAV. Кроме того, велика роль аутоиммунных реакций, а вот антителозависимый иммунный цитолиз выражен слабее. Вирус гепатита D оказывает прямое цитопатогенное действие, иммунное воспаление слабо выражено, что и объясняет отсутствие эффекта от применения иммуносупрессивных препаратов. При ВГЕ, как и при ВГА, преобладает непосредственное цитопатогенное действие вируса на клетку, но холестазы и железистая трансформация клеток встречаются чаще.
Желтуха, один из наиболее ярких симптомов ВГ, обусловлена тем, что при повреждении гепатоцита нарушается разделение его функций (в норме через билиарный полюс клетки в желчные канальцы выделяются различные компоненты желчи, через синусоидальный продукты метаболизма в кровь и лимфу), все продукты поступают непосредственно в кровь. Нарушается отток желчи, возникает отек печеночной паренхимы.
Очищение организма от возбудителя происходит благодаря действию специфических противовирусных антител, но HBV, HCV, HDV могут длительное время (пожизненно) сохраняться в гепатоците.
Клиническая классификация:
| острый (до 3 мес) | ||
| По длительности | затяжной (до 6 мес) | |
| хронический (свыше 6 мес)* | ||
| бессимптомные формы | носительство* | |
| По выраженности | субклиническое течение | |
| клинических проявлений | манифестные формы | безжелтушные |
| желтушные | ||
| циклическое | ||
| По характеру течения | ациклическое | с обострениями |
| с рецидивами* | ||
| легкое течение | ||
| среднетяжелое | ||
| По тяжести течения | тяжелое | |
| фульминантные формы | ранние (возникают в первые 2–3 недели болезни) | |
| поздние (на 7–8 неделе) | ||
| По характеру патологического | с преобладанием цитолитического синдрома | |
| процесса в печени | с преобладанием холестатического синдрома | |
| холестатические формы |
Клиника. Для вирусных гепатитов характерна цикличность течения. Выделяют следующие периоды: инкубационный, преджелтушный, желтушный (период нарастания, разгара и угасания желтухи), реконвалесценции и остаточных явлений.
Инкубационный период при ВГА составляет 7-50 дней, ВГВ — 1,5-6 мес., ВГС — до 14 нед., ВГЕ — 14-50 дней.
Преджелтушный период имеет несколько вариантов течения.
1) Астено-вегетативный (встречается при всех ВГ).
2) Диспептический (снижение аппетита, тошнота, рвота, дискомфорт в животе; встречается при всех ВГ, но чаще при ВГА и ВГЕ, т.к. именно для этих гепатитов характерна энтеральная фаза).
3) Артралгический (характерен для ВГВ, ВГС, ВГD). Боли в суставах при этом не сопровождаются их деформацией, признаками воспаления.
4) Псевдогриппозный или гриппоподобный (характерен для ВГА и ВГЕ). Лихорадка держится не более 23 дней, катаральные симптомы отсутствуют.
5) Аллергический (бывает, хотя и редко, при ВГВ, ВГС, ВГD). При этом появляются зудящие уртикарные высыпания, может повышаться температура.
Чаще всего встречается смешанный вариант, когда сочетаются признаки двух-трех вариантов.
Желтушный период наступает тогда, когда уровень билирубина в 1,52 раза превышает норму. Но обычно за 12 дня до этого больные обращают внимание на изменение цвета мочи (темнеет) и кала (светлеет). Снижение аппетита, утомляемость типичные проявления этого периода. Могут возникать боли в животе, свидетельствующие в большей степени о холецистите, дискинезии желчевыводящих путей, панкреатите. В разгаре болезни четко определяются увеличение печени и селезенки. Артериальное давление имеет тенденцию к снижению, нередко выявляется брадикардия. С момента мочевого криза (количество мочи увеличивается, она светлеет) желтуха начинает уменьшаться.
Следует помнить об особенностях различных ВГ, помогающих распознать этиологию болезни еще до проведения специальных методов исследования.
Вирусный гепатит А:
· болеют преимущественно дети и люди молодого возраста;
· заболевание может возникать в виде вспышек;
· максимум заболеваемости приходится на конец лета осень; обычно заболевание начинается остро;
· у большинства больных в преджелтушном периоде наблюдается кратковременная (13 дня) лихорадка без катаральных явлений;
· с момента появления желтухи состояние обычно улучшается;
· в большинстве случаев заболевание протекает легко;
· хронизация, рецидивы не характерны.
Вирусный гепатит В:
· имеются указания на перенесенные в прошлом (за 1,56 мес до данного заболевания) операции, парентеральные манипуляции;
· заболевание обычно возникает в виде единичных случаев, но следует помнить о возможности групповых заболеваний среди наркоманов, у половых партнеров;
· заболевание развивается постепенно, медленно;
· преджелтушный период чаще протекает по типу артралгического, диспептического, выраженного астено-вегетативного синдромов без лихорадки;
· с момента появления желтухи самочувствие не только не улучшается, но часто ухудшается, интоксикация может сохраняться до мочевого криза;
· в преджелтушном и желтушном периодах возможны различные аллергические проявления;
· заболевание чаще протекает в среднетяжелой форме;
· возможны затяжное течение, переход в хроническую форму, носительство.
Вирусный гепатит С:
· заболевание чаще возникает у лиц, перенесших переливание крови или ее компонентов, реципиентов органов и тканей, наркоманов, ВИЧ-инфицированных;
· начинается очень постепенно, часто без четко выраженного преджелтушного периода;
· протекает преимущественно в виде легких форм, тем не менее, в большинстве случаев дает хронизацию (эта особенность послужила основанием для того, чтобы ВГС называть “ласковый убийца”);
· на фоне “легкого течения” у больных могут выявляться значительно увеличенные печень и селезенка, не соответствующие по своим размерам и плотности ни тяжести течения, ни остроте процесса;
· HCV-инфекция иногда распознается лишь тогда, когда у больного уже сформировался цирроз печени;
· заболевание нередко протекает с периодическими ферментативными обострениями, которые обычно не распознаются клинически.
Дельта гепатит:
· группы риска те же, что ВГВ, особое внимание имеющим маркеры ВГВ; у 60% больных еще в преджелтушном периоде возникает лихорадка, сохраняющаяся и в желтушном периоде;
· часто появляются боли в правом подреберье;
· если заболевание протекает по типу коинфекции, то протекает достаточно тяжело, но заканчивается чаще полным очищением организма от возбудителя; если по типу суперинфекции то характерны обострения, рецидивы, хронизация;
· применение кортикостероидов отягощает течение заболевания.
Вирусный гепатит Е:
· особую группу риска представляют лица, посещавшие страны Азии, Африки, Южной Америки. (В 1996 году были вспышки и в Украине!);
· типичен взрывной характер эпидемий, связанных с определенными источниками водоснабжения;
· заболевают преимущественно люди молодого возраста (1518 лет);
· заболевание начинается остро, как при ВГА, но самочувствие после снижения температуры и появления желтухи не улучшается;
· у большинства больных еще в преджелтушном периоде появляется выраженный болевой синдром (боль локализуется в правом подреберье и эпигастральной области), он сохраняется и при появлении желтухи;
· вирус поражает не только гепатоциты, но и почечную ткань, поэтому гепатит нередко сочетается с гломерулонефритом;
· у беременных очень тяжелое течение с высокой летальностью (от 30 до 60%);
· наблюдается двухфазное повышение активности трансфераз, что не имеет, как правило, клинического отображения;
· кортикостероиды отягощают течение ВГЕ.
Осложнения и исходы вирусных гепатитов. Острая печеночная энцефалопатия, острая почечная недостаточность, ДВС-синдром. Исходами вирусных гепатитов В, С, D могут быть хронический гепатит (при В и D — 10-15%, при С — 50-80%), цирроз печени, рак печени.
Лабораторная диагностика. Обычные клинические анализы крови, мочи, кала каких-либо специфических изменений не выявляют. В крови могут наблюдаться лейкопения и относительный лимфоцитоз. В моче при развитии желтухи становится положительной реакция на желчные пигменты. В разгаре болезни кал может приобретать серую окраску, а реакция на стеркобилин становится отрицательной. Особая роль при обследовании принадлежит биохимическим методам обследования.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Да какие ж вы математики, если запаролиться нормально не можете. 8250 — 

195.133.146.119 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник
С позиции современных знаний рецидив вируса после лечения гепатита с представляет собой непростую клиническую задачу, которая требует всестороннего анализа, поиска причин рецидива HCV и принятия решения о повторном лечении гепатита (перелечивании). Чаще всего рецидив HCV-инфекции возникает в течение первых 3-12 месяцев (12-48 недель) после окончания курса противовирусной терапии. Срок возникновения рецидива не зависит от того чем пациент лечился, устаревшими режимами на основе интерферона-альфа или самыми современными безинтерфероновыми препаратами. В то же время рецидивы HCV после лечения интерфероном и рибавирином возникают чаще чем после безинтерфероновой терапии ингибиторами прямого противовирусного действия.
При контрольном вирусологическом обследовании после окончания курса противовирусной терапии РНК HCV в плазме крови у пациента не определяется. Однако через некоторое время, иногда через год после терапии, результаты анализа ПЦР вновь становятся положительными, в крови вновь повышается уровень активности АЛТ и могут вновь появиться явные симптомы и клинические признаки обострения гепатита. Иногда бывают случаи, когда рецидив HCV регистрируют только спустя много лет после окончания курса лечения. Подобные ситуации чаще всего связаны с развитием иммунодефицитных состояний, когда иммунная система перестает «контролировать» процесс размножения (репликации) вируса. Вирусная репликация при этом многократно усиливается и РНК HCV вновь появляется в крови.
О такой сложной клинической ситуации как рецидив гепатита с через несколько лет после лечения можно говорить в тех случаях, когда по результатам контрольного анализа ПЦР после длительной авиремии в плазме крови повторно обнаруживают виремию РНК HCV. Рецидив виремии может сочетаться с повышением уровня активности АЛТ в крови и появлением характерных клинических симптомов. В части случаев никаких клинических симптомов и гиперферментемии АЛТ вообще не бывает. Однако в любом случае возврат вируса гепатита с и виремию следует рассматривать в качестве неблагоприятного состояния, которое требует повторного противовирусного лечения с целью предотвратить цирроз и рак печени, а также различные тяжелые системные лимфопролиферативные и аутоиммунные заболевания.
Многие пациенты с HCV-инфекцией, у которых удается достичь УВО (устойчивый вирусологический ответ) после успешной безинтерфероновой терапии оригинальными препаратами или дженериками нередко задают вопрос о том может ли алкоголь спровоцировать возврат гепатита с и через какое время после окончания курса лечения это может случиться. Ответ на данный вопрос довольно прост. Алкоголь не является «стимулятором» процесса вирусной репликации и поэтому не может стать причиной рецидива даже в том случае, если после лечения гепатит С «перешел» в незаметную оккультную форму, вирус HCV остался в организме и «затаился» глубоко в клетках печени гепатоцитах и иммунных клетках крови В-лимфоцитах.
Ответ на другой часто задаваемый вопрос . возможен ли рецидив гепатита с после лечения, к сожалению, утвердительный. Рецидив гепатита свидетельствует о том, что сразу после лечения вирус HCV на какое-то время «спрятался» в гепатоцитах и В-лимфоцитах и затем в результате действия той или иной причины вновь стал активно размножаться.
Наиболее часто встречающиеся причины рецидива гепатита с хорошо известны многим пациентам и практикующим врачам-гепатологам. Эти причины давно установлены, их довольно много, но в числе наиболее значимых нужно выделить следующие:
- прием дженериков сомнительного происхождения, не очень высокого качества или с истекшим сроком годности;
- наличие у пациента сопутствующих гепатотропных «виремических» вирусных инфекций – HBV, HDV, HGV, CMV, TTV, которые «отвлекают на себя» внимание иммунной системы, не давая возможности сосредоточиться на борьбе с вирусом HCV;
- самолечение, отсутствие во время лечения лабораторного контроля и клинического контроля со стороны врача-гепатолога;
- досрочное прекращение курса лечения или недостаточная продолжительность курса лечения;
- неправильный выбор препаратов для лечения и режима терапии;
- далеко зашедшая стадия фиброзных изменений в печени или цирроз печени на момент начала лечения;
- наличие тяжелых внепеченочных проявлений HCV-инфекции, в первую очередь криоглобулинемии с полиорганными проявлениями, а также аутоиммунных, нефрологических, гематологических, ревматологических или лимфопролиферативных заболеваний;
- несоблюдение пациентом во время курса лечения строгих правил хранения и введения интерферона или правил приема рибавирина (например, полное прекращение приема рибавирина при появлении первых нежелательных явлений или побочных реакций);
- несоблюдение пациентом во время курса лечения строгих правил приема препаратов-ингибиторов;
- неоднократные пропуски приема лекарственных препаратов во время курса лечения;
- наличие у вируса HCV мутаций лекарственной устойчивости (резистентности), которые могут быть или «первичными», или возникшими на фоне приема препаратов-ингибиторов;
- несоблюдение пациентом во время курса лечения строгих правил контроля межлекарственных взаимодействий и лекарственной совместимости.
Вышеперечисленные причины рецидива HCV позволяют дать утвердительный ответ на вопрос может ли гепатит с вернуться, хорошо объясняют почему возвращается гепатит с после лечения и как этого можно избежать. На самом деле возврат гепатита с после пвт (противовирусной терапии) это нередко встречающаяся в клинической практике ситуация, особенно в тех случаях, если пациенты занимаются бесконтрольным самолечением, не соблюдают правила приема лекарственных препаратов или в качестве препаратов для противовирусной терапии принимают дженерики сомнительной репутации и не очень высокого качества. Поэтому всем пациентам с HCV-инфекцией, которые начинают курс лечения гепатита С, следует знать о том, что возврат гепатита с после дженериков более вероятен, чем после лечения оригинальными препаратами. При прочих равных условиях эффективность дженериков все-таки уступает эффективности оригинальных препаратов.
Эффективное лечение рецидива гепатита с гарантией достижения УВО (устойчивого вирусологического ответа) после повторного курса лечения всегда представляет определенные трудности для пациента и врача-гепатолога. Необходим правильный выбор конкретного режима повторного лечения (перелечивания), который зависит от генотипа/субтипа HCV, характеристики противовирусных лекарственных препаратов, которыми пациент неудачно лечился и стадии фиброзных изменений в печени.
Всех пациентов с рецидивом гепатита С в зависимости от стадии фиброза условно разделяют на 3 группы:
- 1-я группа – это пациенты с F0, F1, F2 и F3 стадиями фиброза, у которых для повторного лечения HCV можно применять короткий 8-ми недельный курс двух новых ингибиторов glecaprevir/pibrentasvir (оригинальная торговая марка «Мавирет»);
- 2-я группа – это пациенты с F4 стадией фиброза (то есть с компенсированным циррозом печени класса Child-A не более 6 баллов по шкале Child-Pugh); лечение рецидива гепатита С у таких пациентов представляет определенные трудности и требует сопровождения опытного врача-гепатолога;
- 3-я группа – это пациенты с субкомпенсированным циррозом печени класса Child-B (7-9 баллов по шкале Child-Pugh) и декомпенсированным циррозом печени класса Child-C (10-15 баллов по шкале Child-Pugh); повторное лечение HCV у таких пациентов является чрезвычайно трудной задачей и требует слаженных действий команды врачей нескольких специальностей.
Перелечивание гепатита и лечение рецидива HCV у пациентов, получавших «простые» режимы интерферон с рибавирином и/или софосбувир с рибавирином
Лечение рецидива HCV после любого из трех «простых» режимов противовирусной терапии .
- Peg_IFN-alfa + RBV_ribavirin
- Peg_IFN-alfa + RBV_ribavirin + SOF_sofosbuvir
- SOF_sofosbuvir + RBV_ribavirin
… является не очень сложной клинической задачей и подробно описано в общих рекомендациях EASL. В клинике ЭКСКЛЮЗИВ для повторного лечения HCV у таких пациентов успешно применяют различные по составу и продолжительности безинтерфероновые режимы, которые подробно представлены на сайте . здесь.
Значительно более трудной клинической задачей по сравнению с предыдущей представляется лечение рецидива гепатита С у пациентов, не достигших УВО после различных комбинированных безинтерфероновых режимов, в состав которых входили те или иные ингибиторы протеазы NS3/4A 1-го и 2-го поколений и/или ингибиторы NS5A 1-го поколения, такие как .
- ингибиторы сериновой протеазы NS3/4A – Telaprevir (препарат 1-го поколения «Инсиво»), Boceprevir (препарат 1-го поколения «Виктрелис»), Simeprevir (препарат 2-го поколения «Олисио»), Asunaprevir (препарат 2-го поколения «Сунвепра»), Paritaprevir (препарат 2-го поколения, входит в состав 3D-режима «Викейра Пак»);
- ингибиторы репликазы NS5A – Ledipasvir (препарат 1-го поколения, входит в состав 2D-режима «Харвони»), Daclatasvir (препарат 1-го поколения, входит в состав 2D-режимов «Даклинза» + «Сунвепра» и «Даклинза» + «Совальди»), Ombitasvir (препарат 1-го поколения, входит в состав 3D-режима «Викейра Пак»).
Несколько групп исследователей высказали предположение, что эффективность повторного лечения гепатита (рецидива HCV) у «пациентов-неудачников» может быть повышена при правильном подборе безинтерфероновых ингибиторов с учетом результатов определения мутаций лекарственной устойчивости, которые могут снижать восприимчивость вируса HCV к соответствующему классу ингибиторов. Наиболее неблагоприятные мутации были выявлены у больных, которые получали безинтерфероновые режимы, но не достигли УВО. Однако до сих пор в клинической гепатологии так и не выработаны какие-либо определенные рекомендации по конкретным режимам перелечивания в зависимости от выявленных мутаций. Поэтому выбор наиболее оптимальной схемы повторного лечения пациентов с рецидивом HCV после безинтерфероновой терапии должен быть основан в первую очередь на установлении и анализе причин рецидива гепатита (см. выше), информации о применявшихся ингибиторах и клиническом опыте врача-гепатолога.
На сегодняшний день известны результаты первых двух многоцентровых клинических испытаний III фазы (POLARIS-I и POLARIS-IV), показавших безопасность и эффективность принципиально новой 12-ти недельной комбинации трех ингибиторов sofosbuvir (ингибитор NS5B 1-го поколения) + velpatasvir (ингибитор NS5A 2-го поколения) + voxilaprevir (ингибитор NS3/4A 3-го поколения) у пациентов, которые не достигли УВО после различных безинтерфероновых режимов, включавших те или иные ингибиторы протеазы NS3/4A 1-го и 2-го поколений и/или ингибиторы NS5A 1-го поколения.
В исследование POLARIS-I было включено 263 пациента с рецидивом HCV, в том числе 143 пациента с циррозом печени. С целью перелечивания эти пациенты в течение 12-ти недель получали тройную комбинацию sofosbuvir/velpatasvir/voxilaprevir . Итоговый показатель УВО составил 96% (253 из 263). В исследовании был зарегистрирован всего лишь один случай вирусологического прорыва во время курса перелечивания и 9 случаев повторного рецидива виремии HCV после его окончания. Показатель УВО у пациентов без цирроза печени составил 99% и был показательно выше, чем у пациентов с циррозом печени (93%).
Врачи-исследователи POLARIS-I особо отметили, что ни генотип HCV, ни профиль мутаций лекарственной устойчивости на момент начала курса повторного лечения не имели никакого влияния на конечный результат терапии у наблюдавшихся пациентов.
В параллельное исследование РOLARIS-IV было включено в общей сложности 333 пациента с рецидивом HCV. Всех пациентов разделили на 2 сопоставимые группы. В первую группу вошли 182 пациента (46% с циррозом печени), которые начали получать 12-ти недельную комбинацию трех ингибиторов sofosbuvir/velpatasvir/voxilaprevir (SOF/VEL/VOX) . Во вторую группу включили 151 пациента (44% с циррозом печени), которые начали получать 12-ти недельную комбинацию двух ингибиторов sofosbuvir/velpatasvir (SOF/VEL) . Итоговый показатель УВО в 3D-группе SOF/VEL/VOX составил 98% (178 из 182) и был достоверно выше итогового показателя УВО в 2D-группе SOF/VEL (всего лишь 90%, 136 из 151).
Врачи-исследователи POLARIS-IV также отметили, что ни генотип HCV, ни профиль мутаций лекарственной устойчивости на момент начала курса перелечивания не оказывали никакого влияния на конечный результат у больных, получавших новый безинтерфероновый 3D-режим тремя мощными ингибиторами SOF/VEL/VOX . Важно подчеркнуть, что у тех немногих пациентов, которые на этом режиме также испытали неудачу, не было обнаружено никаких мутаций лекарственной устойчивости ни перед началом курса лечения, ни при вирусологическом прорыве во время курса лечения, ни при рецидиве HCV после окончания курса лечения.
Результаты еще одного обсервационного исследования MAGELLAN-I по лечению «пациентов-неудачников» с рецидивом HCV после безинтерфероновых режимов, включавших различные ингибиторы NS5A 1-го поколения, показали недостаточную эффективность стандартного 12-ти недельного и пролонгированного 16-ти недельного двойного режима glecaprevir/pibrentasvir (GLE/PIB) в преодолении барьера вирусологической устойчивости у таких пациентов. Новая комбинация GLE/PIB включала в себя два новых ингибитора – glecaprevir/GLE (ингибитор протеазы NS3/4A 3-го поколения) и pibrentasvir/PIB (ингибитор NS5A 2-го поколения). Итоговый показатель УВО среди пациентов в исследовании MAGELLAN-I даже при 16-ти недельном режиме не превысил 80%, поэтому в настоящее время комбинация GLE/PIB («Maviret/Мавирет») не рекомендована к применению для повторного лечения пациентов с рецидивом HCV после безинтерфероновой терапии, содержавшей тот или иной ингибитор NS5A.
С учетом результатов исследований РOLARIS-I, POLARIS-IV и MAGELLAN было высказано предположение о том, что для перелечивания пациентов с рецидивом HCV после безинтерфероновой терапии, включавшей тот или иной ингибитор NS5A 1-го поколения может применяться 3D-комбинация из ингибиторов NS5B sofosbuvir/SOF , NS3/4А glecaprevir/GLE и NS5A pibrentasvir/PIB , поскольку новый ингибитор NS5A 2-го поколения pibrentasvir обладает более высокой противовирусной эффективностью и способностью преодолевать барьер вирусологической устойчивости, чем все другие известные ингибиторы NS5A. Тройная комбинация sofosbuvir + glecaprevir/pibrentasvir рассматривается в качестве альтернативы при перелечивании «трудных» пациентов со сложными мутациями лекарственной устойчивости в регионе NS5A и/или с прогрессирующими стадиями заболевания печени (кроме декомпенсированного цирроза класса Child-C), включая пациентов, испытавших несколько неудачных курсов лечения. Первый случай успешного перелечивания такого пациента с помощью 12-ти недельной 3D комбинации SOF + GLE/PIB в клинике ЭКСКЛЮЗИВ уже наблюдали и зарегистрировали.
Таким образом, на сегодняшний день для перелечивания самых сложных пациентов, не достигших УВО после первого курса безинтерфероновой терапии, в состав которой входили тот или иной ингибитор протеазы NS3/4A 2-го поколения ( Simeprevir, Asunaprevir, Paritaprevir ) и/или ингибитор NS5A 1-го поколения ( Ledipasvir, Daclatasvir, Ombitasvir ), рекомендованы две новые 12-ти недельные 3D-комбинации:
- sofosbuvir/velpatasvir/voxilaprevir (оригинальное торговое название «Vosevi»);
- sofosbuvir («Sovaldi») + glecaprevir/pibrentasvir («Mavyret», «Maviret»).
Если случилась неприятная для пациента ситуация и гепатит С вернулся после окончания курса лечения препаратом софосбувир значит нужно принимать соответствующее решение и начинать повторный курс противовирусной терапии. Начинать повторное лечение можно в любое время вне зависимости от того, как давно был закончен предыдущий курс терапии.
Следует обратить особое внимание на такую неоднозначную клиническую задачу как рецидив после лечения софосбувиром. Данную ситуацию и прогноз эффективности повторного лечения следует рассматривать с двух сторон, с учетом того, в комбинации с какими препаратами пациент получал ингибитор NS5B софосбувир. Во-первых, это может быть рецидив HCV после двух «простых» режимов, в состав которых входил софосбувир (см. ниже):
- комбинированный режим «пегилированный IFN-альфа в сочетании с рибавирином и софосбувиром» ( Peg_IFN-alfa + Ribavirin + Sofosbuvir );
- полностью безинтерфероновый режим «софосбувир в сочетании с рибавирином» ( Sofosbuvir + Ribavirin ).
Режимы перелечивания таких пациентов в клинике ЭКСКЛЮЗИВ представлены на сайте здесь.
Во-вторых, рецидив HCV может случиться после полностью безинтерфероновых комбинированных режимов, в состав которых кроме ингибитора NS5B софосбувира входил тот или иной ингибитор NS5A 1-го поколения, например, ледипасвир/ledipasvir (в составе комбинированного препарата «Харвони»), велпатасвир/velpatasvir (в составе комбинированного препарата « Эпклуза ») или даклатасвир/daclatasvir (комбинация препаратов «Совальди» + «Даклинза»). Вирусологическая неудача после таких сложных безинтерфероновых схем требует перелечивания (повторного лечения) с помощью новых лекарственных режимов, в состав которых должны входить три мощных ингибитора. Самыми эффективными режимами перелечивания на сегодняшний день являются 12-ти недельные пангенотипные режимы «Восеви» («Vosevi») и «Мавирет» + «Совальди» («Maviret» + «Sovaldi»).
Возврат гепатита после софосбувира в последнее время регистрируют, к сожалению, все чаще. В большинстве случаев рецидив виремии РНК HCV происходит у пациентов, которые принимали сомнительного качества дженерик софосбувира, особенно в комбинации с препаратом рибавирин, или в тех случаях когда схема лечения на основе софосбувира не являлась оптимальной.
Очень неприятной ситуацией для пациента и врача-гепатолога является рецидив после софосбувира и даклатасвира, который отличается тем, что у вируса HCV на фоне терапии этими двумя ингибиторами, скорее всего, возникли мутации лекарственной устойчивости к этим ингибиторам и для эффективного перелечивания HCV-инфекции у пациента-неудачника потребуются уже не два, а три более мощных ингибитора следующих поколений (см. ниже итоговые рекомендации по лечению рецидива HCV).
С позиции современных знаний ситуацию когда вернулся вирус гепатита после Харвони, в состав которого входит ингибитор репликазы NS5A 1-го поколения ледипасвир/ledipasvir, нужно рассматривать как неудачу после безинтерферонового режима, содержавшего ингибитор NS5A.
Рецидив гепатита после курса Харвони требует перелечивания и назначения мощного 12-ти недельного безинтерферонового режима, включающего в свой состав три ингибитора, например:
- 3D-режим «Восеви» (ингибитор NS5B софосбувир + ингибитор NS5A велпатасвир + ингибитор NS3/4A воксилапревир в одной таблетке);
- комбинированный 3D-режим «Мавирет» + «Совальди» (соответственно, ингибитор NS3/4A глекапревир + ингибитор NS5A пибрентасвир в одной таблетке в комбинации с ингибитором NS5B софосбувиром).
Ответ на вопрос: Может ли вернуться вирус гепатита С после лечения Викейра Пак, к сожалению, утвердительный. Но это бывает очень редко. По данным клиники ЭКСКЛЮЗИВ рецидив виремии РНК HCV зарегистрирован у 2% пациентов, которые получали 3D-режим «Викейра Пак».
Возврат вируса гепатита после лечения викейра пак является трудной клинической задачей для повторного лечения (перелечивания), так как комбинированный препарат «Викейра Пак» содержит в своем составе три ингибитора всех трех белков-ферментов (NS3/4A, NS5A и NS5B), которые играют важную роль на этапах процесса репликации HCV. Перелечивание пациентов с вирусологической неудачей в виде рецидива виремии РНК HCV после 3D-режима «Викейра Пак» представляется значительно более сложной задачей по сравнению с перелечиванием пациентов с неудачей после двойных 2D-режимов «Харвони» ( LED/ледипасвир и SOF/софосбувир ), « Эпклуза » (VEL/велпатасвир + SOF/софосбувир) или «Совальди» ( SOF/софосбувир ) + «Даклинза» ( DAC/даклатасвир ).
На сегодняшний день для эффективного перелечивания пациентов с неудачей после 3D-режима «Викейра Пак» рекомендованы два новых 3D-безинтерфероновых режима, в состав каждого из которых входят по 3 мощных ингибитора. Первый рекомендуемый режим перелечивания – это 12-ти недельная 3D-комбинация «Восеви» ( SOF/софосбувир + VEL/велпатасвир + VOX/воксилапревир ) в одной таблетке от фармацевтической компании Gilead Sciensis, Inc. Второй возможный режим перелечивания – это 12-ти недельная 3D-комбинация «Мавирет» ( GLE/глекапревир и PIB/пибрентасвир ) + «Совальди» ( SOF/софосбувир ) в разных таблетках от фармацевтических компаний AbbVie, Inc. и Gilead Sciensis, Inc.
Следует знать, что антитела к вирусу гепатита С после курса Викейра Пак будут сохраняться в организме и определяться в плазме крови в реакции ИФА (иммуноферментный анализ) в течение неопределенно длительного времени даже после успешного окончания курса терапии. Антитела к HCV при отсутствии виремии РНК HCV (иными словами при отрицательных результатах ПЦР) после окончания курса лечения свидетельствуют только лишь о том, что вирус HCV «оставил свой след» в организме в результате контакта с иммунной системой.
Возврат вируса HCV после лечения чаще всего происходит в течение первых 3-12 месяцев после окончания курса Викейра Пак или какого-либо иного курса противовирусной терапии. Такую ситуацию регистрируют не очень часто, обозначают специальным термином «рецидив виремии РНК HCV» и рассматривают как один из четырех возможных вариантов вирусологической неудачи, перечисленных ниже, а именно:
- отсутствие вирусологического ответа;
- частичный вирусологический ответ;
- «вирусологический прорыв» виремии РНК HCV во время курса терапии;
- рецидив виремии РНК HCV после окончания курса терапии.
Рецидив HCV и перелечивание гепатита у пациентов после неудачи «Мавирет»
Предварительные результаты продолжающегося клинического испытания 3D-комбинации sofosbuvir + glecaprevir/pibrentasvir («Совальди» + «Мавирет») были официально объявлены в самом начале 2018 г. Первых 23 пациентов, которые ранее не достигли УВО после 8-ми или 12-ти недельных курсов терапии в 2D-режиме GLE/glecaprevir и PIB/pibrentasvir , перелечивали усиленной рибавирином комбинацией sofosbuvir + glecaprevir/pibrentasvir + ribavirin в течение 12-ти (2 пациента) или 16-ти (21 пациент) недель. УВО зарегистрирован в 96% случаев (у 22 из 23 пациентов). У одного пациента повторно возник рецидив HCV после окончания курса перелечивания. Таким образом, 3D-комбинация SOF + GLE/PIB + RBV (три мощных ингибитора с добавлением рибавирина) показала высокую эффективность, хороший профиль безопасности и хорошую переносимость.
Есть обоснованные предположения, что у особо «трудных» для перелечивания пациентов, которые ранее получали безинтерфероновую терапию, включавшую тот или иной ингибитор NS5A 1-го поколения, комбинированные 3D-режимы sofosbuvir/velpatasvir/voxilaprevir и sofosbuvir + glecaprevir/pibrentasvir могут быть эффективны даже без добавления рибавирина и/или увеличения продолжительности курса лечения до 16-24 недель. Однако пока нет никаких убедительных данных, чтобы поддержать эти показания, которые должны быть отдельно рассмотрены и решены командами опытных врачей-гепатологов с учетом многих клинических параметров на момент начала курса перелечивания. Необходимо обязательно учитывать стадию и характер хронического заболевания печени, наличие внепеченочных проявлений HCV, например, криоглобулинемию, информацию о предыдущих неудачных курсах лечения и профиль мутаций лекарственной устойчивости. Также следует помнить, что наличие у пациента субкомпенсированного (класса Child-B) или декомпенсированного (класса Child-C) цирроза печени полностью исключает при повторном лечении HCV использование ингибиторов протеазы NS3/4A, но в то же время требует как можно более быстрого начала терапии.
Тестирование мутаций лекарственной устойчивости HCV в программе обследования перед началом курса повторного лечения у пациентов с возвратом вируса гепатита С после предыдущего лечения представляется полезным (но не обязательным) для выбора наиболее оптимального режима терапии и повышения вероятности успеха.
- Пациенты, у которых ранее не был достигнут УВО с помощью «простых» режимов Peg_IFN-alfa+RBV, Peg_IFN-alfa+RBV+SOF или SOF+RBV должны перелечиваться с учетом генотипа/субтипа HCV и стадии фиброза (цирроза) согласно общим рекомендациям, представленным на сайте . здесь;
Для получения профессиональной консультации по лечению гепатита С в нашей клинике заполните поля ниже и нажмите кнопку «Отправить». Мы перезвоним вам в кратчайшие сроки.
источник