Однажды заразившись вирусом гепатита С, большинство инфицированных приобретают хронический гепатит С. Вероятность этого составляет около 70%.
Хронический гепатит С развивается у 85 % больных с острой формой инфекции. В процессе развития заболевания вполне вероятна цепочка острый вирусный гепатит →хронический гепатит→цирроз печени→ гепатоцеллюлярный рак.
Обратите внимание на то, что эта статья содержит только общие современные представления о хроническом гепатите С.
Хронический вирусный гепатит С — симптомы Намного опаснее хроническая форма — болезнь долгое время длится бессимптомно, сигнализируют о болезни лишь хроническая усталость, упадок сил и нехватка энергии.
Хронический гепатит С — это воспалительное заболевание печени, вызванное вирусом гепатита С, текущее без улучшения в течение 6 мес и более. Синонимы: Хронический вирусный Гепатит C (хвгс), Хроническая HCV-инфекция (от англ. hepatitis С virus), хронический гепатит С.
Вирусный гепатит С был открыт только в 1989 году. Заболевание опасно тем, протекает практически бессимптомно и клинически себя никак не проявляет. Острый вирусный гепатит C лишь в 15-20% случаев завершается выздоровлением, остальные переходят в хроническую форму.
В зависимости от степени активности инфекционного процесса выделяют хронические вирусные гепатиты с минимальной, слабо выраженной, умеренно выраженной, выраженной активностью, фульминантный гепатит с печеночной энцефалопатией.
Хронический вирусный гепатит C с минимальной степенью активности (хронический персистирующий вирусный гепатит) возникает в условиях генетически обусловленного слабого иммунного ответа.
КОД ПО МКБ-10 В18.2 Хронический вирусный гепатит С.
Распространённость хронической HCV-инфекции в мире составляет 0,5-2%. Выделяют области с высокой распространённостью вирусного гепатита С: изолированные поселения в Японии (16%), Заир и Саудовская Аравия (>6%) и др. В России заболеваемость острой HCV-инфекцией — 9,9 на 100 000 населения (2005 г.).
Хронический вирусный гепатит С за последние 5 лет вышел на первое место по заболеваемости и тяжести осложнений.
Существует 6 основных генотипов вируса гепатита С и более 40 подтипов. Именно с этим связана высокая частота развития хронического вирусного гепатита С.
Неспецифическая профилактика — см. «Хронический гепатит В».
Результаты исследований свидетельствуют о низкой вероятности передачи HCV-инфекции половым путем. Вакцина для профилактики гепатита С находится в стадии разработки.
Хронический гепатит C является одной из главных причин, приводящих к пересадке печени.
Определяют суммарные антитела к вирусу гепатита С (анти-HCV). Рекомендовано подтверждение положительного результата иммуноферментного анализа методом рекомбинантного иммуноблоттинга.
Возбудитель — покрытый оболочкой РНК-содержащий вирус диаметром 55 нм семейства Flaviviridae. Вирус характеризуется высокой частотой мутаций участков генома, кодирующих белки Е1 и E2/NS1, что обусловливает значительную изменчивость HCV-инфекции и возможность одновременного инфицирования разными типами вируса.
Передача инфекции происходит гематогенным путем, реже половым путем или от инфицированной матери плоду (3-5% случаев).
Вирус гепатита С передается через кровь. Половой путь является не актуальным и заражение вирусом гепатита С половым путем происходит редко. Передача вируса от матери во время беременности происходит, также, крайне редко. Кормление грудью не запрещено при гепатите С, но следует соблюдать осторожность при появлении крови на сосках.
Заразиться вирусом можно при нанесении татуировок, пирсинге, посещении маникюрного кабинета, медицинских манипуляциях с кровью, в том числе при переливании крови, введении препаратов крови, операциях, у стоматолога. Возможно также заразиться при общем использовании зубных щеток, бритвенных приборов, маникюрных принадлежностей.
При бытовых контактах заразиться вирусом гепатита С невозможно. Вирус не передается воздушно-капельным путем, при рукопожатии, объятиях и использовании общей посуды.
После попадания вируса в кровь человека, он с током крови поступает в печень, заражает печеночные клетки и там размножается.
Хронический вирусный гепатит С протекает, как правило, со скудной клинической картиной и преходящим уровнем трансаминаз.
В большинстве случаев заболевание протекает бессимптомно. У 6% больных выявляют астенический синдром. Часто наблюдается тупая непостоянная боль или тяжесть в правом подреберье (эти симптомы напрямую не связаны с HCV-инфекцией), реже — тошнота, снижение аппетита, кожный зуд, артралгии и миалгии.
Внепечёночные клинические проявления вирусного гепатита С:
- часто смешанная криоглобулинемия — проявляется пурпурой, артралгиями.
- поражением почек и редко нервной системы;
- мембранозный гломерулонефрит;
- синдром Шегрена;
- красный плоский лишай;
- аутоиммунная тромбоцитопения;
- поздняя кожная порфирия.
Анамнез позволяет получить сведения о возможном пути инфицирования и иногда о перенесённом остром гепатите С.
На доцирротической стадии малоинформативно, может быть незначительная гепатомегалия. Появление желтухи, спленомегалии, телеангиэказий указывает на декомпенсацию функции печени или присоединение острого гепатита другой этиологии (HDV, алкогольный, лекарственный гепатиты и др.).
Биохимический анализ крови при гепатите C: Цитолитический синдром отражает активность трансаминаз (АЛТ и АСТ). Однако их нормальные показатели не исключают цитологическую активность гепатита. При хроническом гепатите С активность АЛТ редко достигает высоких значений и подвержена спонтанным колебаниям. Постоянно нормальная активность трансаминаз и 20% случаев не коррелирует с выраженностью гистологических изменений. Только при повышенной активности АЛТ в 10 раз и больше можно (высокой степенью вероятности предполагать наличие мостовидных некрозов печени)
Согласно данным проспективных исследований, примерно у 30% пациентов с хроническим вирусным гепатитом С (ХВГС) активность аминотрансфераз сохраняется в пределах нормальных значений
Серологические исследования при гепатите C: основной маркер наличия вируса гепатита C в организме — HCV-PHK. Аити-HCV могут не выявляться у лиц с врождённым или приобретенным иммунодефицитом, у новорождённых от матерей-носителей или прииспользовании недостаточно чувствительных методов диагностики.
Перед началом противовирусной терапии необходимо определить генотип HCV и вирусную нагрузку (количество копий вирусной РНК в 1 мл крови; показатель также может быть выражен в ME). Например, генотипы 1 и 4 хуже поддаются лечению интерферонами. Значение вирусной нагрузки особенно велико при инфицировании HCV с генотипом 1, поскольку при ее значении ниже 2х10^6 копий/мл либо 600 МЕ/млвозможно сокращение курса лечения.
Лечению хронического гепатита C подлежат пациенты с высоким риском формирования цирроза печени, определяемому по биохимическим и гистологическим признакам. Терапия хронического гепатита С направлена на достижение устойчивого вирусологического ответа, то есть элиминации сывороточной HCV-PHK через 6 месяцев после окончания противовирусной терапии, поскольку в этом случае рецидивы заболевания редки.
Вирусологический ответ сопровождают биохимические (нормализация АЛТ и ACT) и гистологические (снижение индекса гистологической активности ииндекса фиброза) изменения. Гистологический ответ может быть отсроченным, особенно при исходном фиброзе высокой степени. Отсутствие биохимического и гистологического ответа при достижении вирусологического требует тщательного исключения других причин повреждения печени.
- Нормализация активности сывороточных трансаминаз.
- Элиминация сывороточной HCV-PHK.
- Нормализация или улучшение гистологической структуры печени.
- Предотвращение осложнений (цирроз, рак печени).
- Снижение смертности.
Противовирусная терапия хронического гематита C включает применение интерферонов альфа (простых или пегилированиых) в комбинации с рибавирином.
Схема фармакотерапии гепатита C зависит от генотипа HCV и массы тела пациента.
Препараты применяются в комбинации.
• Рибавирин внутрь 2 раза в сутки во время еды в следующей дозе: при массе тела до 65 кг — 800 мг/сут, 65-85 кг — 1000 мг/сут, 85-105 кг 1200 мг/сут. выше 105 кг — 1400 мг/сут.
• Интерферон альфа в дозе 3 млн ME З раза в неделю в виде внутримышечных или подкожных инъекций. Или подкожно пегинтерферон альфа-2а в дозе 180 мкг 1 раз в неделю. Или подкожно пегинтерферон альфа-2b в дозе 1,5 мкг/кг 1 раз в неделю.
При инфицировании HCV с генотипом 1 или 4 продолжительность курса комбинированного лечения составляет 48 нед.При инфицировании HCV с другим генотипом эту схему лечения применяют в течение 24 нед.
В настоящее время идет разработка новых противовирусных препаратов ингибиторов ферментов HCV (протеаз, геликаз, полимераз). При компенсированном циррозе печени в исходе хронического гепатита С противовирусное лечение проводят по общим принципам. При этом вероятность для снижения устойчивого вирусологического ответа ниже, а частота побочных эффектов лекарственных средств выше, чем при лечении пациентов без цирроза печени.
Частота развития цирроза печени при ее типичном течении хронического гепатита С достигает 20-25%. Однако возможны колебания этого показателя в значительных пределах, потому что развитие цирроза печени зависит от индивидуальных особенностей течения болезни и дополнительных повреждающих факторов (особенно алкоголя). Процесс формирования цирроза печени длится от 10 до 50 лет (в среднем — 20 лет). При инфицировании в возрасте 50 лет и старше прогрессирование заболевания ускорено.
Риск развития гепатоцеллюлярной карциномы у больных с циррозом печени составляет от 1,4 до 6,9%. Единственным способом предотвращения тяжёлых осложнений хронического гепатита С у пациентов с высоким риском прогрессирования болезни служит противовирусная терапия.
Даже при декомпенсированномциррозе она снижает риск развития гелатоцеллюлярной карциномы до 0,9-1,4% вгод, а потребность в трансплантации печени — со 100 до 70%.
источник
Структура и механизм повреждающего действия HCV описаны в главе 3.
Эпидемиология. Распространенность хронической HCV-инфекции варьирует от 0.5% до 2% во всем мире. Существуют области с ее высоким распространением: более 6% в Заире и Саудовской Аравии, выше 16% в изолированных поселениях Японии. В России заболеваемость гепатитом С впервые официально регистрировалась в 1994 г. и составила 3.2 на 100 тыс. населения. В 1999 г. эта цифра выросла до 19.3 на 100 тыс. населения.
В настоящее время чаще всего инфицируются HCV молодые люди, преимущественно мужчины, в возрасте около 20 лет. 38% — 40% из них заражаются при внутривенном введении наркотиков. Приблизительно у половины больных путь инфицирования HCV определенно выяснить не удается.
Пути передачи HCV. Основной путь передачи HCV – парентеральный: трансфузии, трансплантация органов от инфицированных доноров, внутривенная наркомания. Возможно инфицирование половым путем, от матери к ребенку и при бытовых контактах (см. ниже).
В прошлом HCV был основной причиной развития посттрансфузионного гепатита (минимум – 85% случаев). В пользу этой точки зрения свидетельствует тот факт, что 37% — 58% больных с ХГС старше 50 лет имеют в анамнезе переливания крови до 1990 года. В настоящее время гемотрансфузии ответственны менее, чем за 4% острых случаев гепатита С.
В течение последних 10 лет ведущим фактором риска инфицирования HCV стала внутривенная наркомания. Заражение происходит очень быстро после начала применения наркотиков: 50% — 80% наркоманов становятся anti-HCV позитивными в течение 12 месяцев от первой инъекции. Кроме того, выявлена ассоциация HCV-инфекции с интраназальным введением кокаина (например, совместное использование одной трубочки для вдыхания порошка). Риск инфицирования HCV существует при выполнении татуировок, пирсинга, маникюра и прочих подобных манипуляций.
Работники здравоохранения представляют собой группу риска инфицирования HCV . По данным американских авторов риск заражения HCV у стоматологов составляет 1.75% по сравнению с 0.14% у их пациентов. Для хирургов-стоматологов эта цифра возрастает до 9.3%.
Нозокомиальное распространение инфекции происходит при несоблюдении мер безопасности, неправильной дезинфекции и обработке медицинского оборудования.
Риск инфицирования HCV половым путем намного ниже в сравнении с HBV, ВИЧ и другими передающимися половым путем инфекциями. Моногамные пары могут не использовать методов барьерной контрацепции. Половой путь инфицирования HCV более актуален для лиц, ведущих беспорядочную половую жизнь и гомосексуалистов, его частота по данным авторов составляет 0.8% — 22%.
Перинатальное инфицирование также не имеет ведущего значения. В среднем, только 5% детей от anti-HCV позитивных матерей имеют маркеры HCV-инфекции.
Спорадические случаи (путь инфицирования выявить не удается) острого гепатита С составляют 30 – 40%.
Течение HCV-инфекции. В нескольких проспективных исследованиях показано, что у 60% — 70% от всех инфицированных HCV лиц развивается хронический гепатит с повышением сывороточных трансаминаз и виремией. Однако, реальная цифра выше, т.к. нормализация АЛТ после острой инфекции не всегда сопряжена с ее разрешением: персистенция HCV RNA наблюдается приблизительно у половины больных. Если она сохраняется более 3 или 6 месяцев, то ее спонтанное разрешение представляется мало вероятным.
Клиническая картина. У большинства пациентов с ХГС на фоне высоких сывороточных трансаминаз заболевание протекает бессимптомно. Только 6% больных ощущают слабость. Достаточно частый симптом — тупая непостоянная или связанная с положением тела боль в верхнем правом квадранте живота. Реже встречаются тошнота, потеря аппетита, кожный зуд, артралгии и миалгии. Клинические признаки поражения печени или внепеченочные знаки отсутствуют. Физикальный осмотр пациента помогает в диагнозе только на стадии ЦП.
Уровень АЛТ обычно изменяется незначительно и только у четверти больных превышает верхний лимит нормы в 2 раза. Однако колебания этого показателя могут быть очень широкими, но периоды его повышения не сопровождаются клиренсом HCV. В целом, сывороточные трансаминазы у пациентов с ХГС имеют ограниченное клиническое значение за исключением периода противовирусного лечения. Несмотря на то, что общепринято традиционное мнение о корреляции между уровнем печеночных ферментов с тяжестью гистологических изменений в ткани печени, АЛТ не является основным ориентиром для оценки воспалительной активности у конкретного больного. Только при ее десятикратном и более повышении можно достоверно предполагать существование мостовидных некрозов. Подобно этому, уровень вирусной нагрузки HCV также плохо коррелирует с гистологическими изменениями.
Проспективные и ретроспективные исследования показали, что пациенты с ХГС представляют собой группу риска развития ЦП и ГЦК. Достаточно часто прогрессирование заболевания протекает бессимптомно, и пациент обращается к врачу уже на конечной стадии патологического процесса. Однако, относительно течения ХГС мнения ученых расходятся. Одни считают, что это заболевание неизбежно прогрессирует в свою конечную стадию и потенциально летально, другие не разделяют эту точку зрения. По данным проведенных исследований частота ЦП в результате ХГС колеблется от 2.4% до 24%. В среднем, процесс формирования ЦП занимает около 20 лет, иногда удлиняясь до 50. Скорость развития цирроза в основном зависит от воспалительной активности и фиброза (гистологические признаки), и в меньшей степени от других факторов (табл. 4.8).
Таблица 4.8. Вероятность развития цирроза печени в зависимости от степени гистологических изменений.
| Диагноз при выявлении ХГС в зависимости от степени воспалительной активности | Риск развития цирроза печени (%) через | ||
| 5 лет | 10 лет | 20 лет | |
| ХГС с минимальной или слабо выраженной активностью | 7 | 7 | 30 |
| ХГС с умеренной активностью | 25 | 44 | 95 |
| Тяжелый ХГС | 68 | 100 | 100 |
| Выраженный фиброз | 58 | 100 | 100 |
ГЦК является достоверным осложнением HCV-инфекции, хотя очень редко встречается в отсутствие цирроза печени. В США и большинстве стран Европы для больных с ЦП ежегодный риск развития ГЦК составляет 1.4% . В Италии и Японии он выше и колеблется от 2.6% до 6.9%. Средняя продолжительность развития ГЦК для больных с HCV-инфекцией составляет 28 – 29 лет.
Другие факторы, способствующие прогрессированию HCV-инфекции.
Алкоголь. Ассоциация между алкогольным повреждением печени и HCV-инфекцией впервые была отмечена в эпидемиологических исследованиях по изучению выживаемости носителей anti-HCV. В настоящее время четко определено, что регулярный прием алкоголя увеличивает повреждение печени у лиц с HCV-инфекцией. Механизм этого процесса остается не вполне ясным: усиливает алкоголь репликацию HCV, или является дополнительным фактором повреждения печени. Однако, прием алкоголя лицами, инфицированными HCV, запрещается.
Роль таких факторов окружающей среды, как токсины, курение и т.д. четко не доказана в прогрессировании HCV.
Возраст может играть роль в прогрессировании заболевания, если инфицирование произошло до 50-55 лет.
Предварительные данные свидетельствуют о том, что фенотип HLA DRB1 может отвечать за восприимчивость к инфекции, а другие фенотипы играют роль в регуляции репликации HCV.
Такие факторы, как этническая принадлежность требуют дальнейших исследований, так как прогрессирование заболевания и развитие ГЦК чаще всего встречается в Японии и Италии.
Есть предположения, что женщины реже болеют тяжелыми формами HCV-инфекции, но этот факт требует дальнейших исследований.
Роль генотипа вируса в прогрессии заболевания обсуждается.
Морфологические признаки ХГС. Для этой формы довольно характерны участки крупнокапельной жировой дистрофии гепатоцитов (рис. 4.9), плотное расположение, агрегация лимфоидных клеток в портальных трактах с образованием в части случаев лимфоидных узелков ( с или без центров размножения) (рис. 4.10), негнойный холангит с лимфоидной и плазмоклеточной инфильтрацией стенок протоков. Клеточная инфильтрация перипортальной зоны наблюдается часто (рис. 4.11), но ступенчатые некрозы выражены обычно довольно слабо. Мостовидные некрозы наблюдаются нечасто. Несмотря на относительно слабую выраженность некротических и воспалительных изменений, отмечается тенденция к прогрессированию фиброза, нередко приводящая к циррозу (рис. 4.12, 4.13). Этому, возможно, способствуют быстро протекающие очаговые некротически-воспалительные изменения в дольках. Для идентификации антигенов вируса гепатита С используют полимеразную цепную реакцию.
Рис. 4.9. Хронический вирусный гепатит B (биоптат печени, окраска г/э, х200). Расширение, деформация, фибриоз портального тракта, выраженная лимфоидная инфильтрация с распространением инфильтрата на периферию дольки. Рядом — небольшой участок крупнокапельной жировой дистрофии гепатоцитов
Рис. 4.10. Хронический вирусный гепатит C (биоптат печени, окраска по Ван Гизону, х200). Фиброзные септы окружают формирующуюся ложную дольку. В одной из септ виден лимфоидный узелок
Рис. 4.11. Хронический вирусный гепатит C (биоптат печени, окраска г/э, х200). Портальный тракт со слабой лимфо-гистиоцитарной инфильтрацией, без фиброзных изменений. Минимальная активность гепатита
Рис. 4.12. Хронический вирусный гепатит C (биоптат печени,). Фиброзная порто-портальная септа. В портальном тракте — выраженная лимфо-гистиоцитарная инфильтрация с аггрегацией лимфоидных элементов
Рис. 4.13. Хронический вирусный гепатит C (биоптат печени, окраска по Ван Гизону, х200). Фиброзные изменения и выраженная клеточная инфильтрация портального тракта и периферии дольки с развитием ступенчатого некроза. Ложная долька слева. Гидропическая дистрофия гепатоцитов.
Внепеченочные проявления HCV. Внепеченочные проявления HCV-инфекции перечислены в табл. 4.9, истинный патогенез их развития не известен. Предполагается, что большинство из них иммуноопосредованы и проявляют себя через следующие события: индукция моноклональных или поликлональных лимфоцитов, отложение в тканях иммунных комплексов, образование аутоантител или активация специфических лимфоцитов, эффекты вирусиндуцированых цитокинов или высвобождение медиаторов воспаления и.д.
Таблица 4.9. Внепеченочные проявления HCV-инфекции.
| Механизм развития | Клинические проявления |
|---|---|
| Продукция или отложение иммуноглобулинов |
|
| Аутоиммунный |
|
| Неизвестный механизм |
|
У пациентов с ХГС часто обнаруживают различные аутоантитела. Антиядерный фактор (ANF), антитела к гладкой мускулатуре (SMA), антитела к щитовидной железе встречаются в 40-65% случаев. Однако, их присутствие не влияет ни на клинические проявления, ни на течение заболевания и ответ на противовирусную терапию. Антитела к печеночно-почечным микросомам-1(anti-LKM-1) заслуживают особого внимания, т.к. считаются маркером аутоиммунного гепатита 2 типа. Однако, при исследовании европейских пациентов с anti-LKM-1 в 48% — 88% случаев у них были обнаружены anti-HCV. Более того, выявлено несколько очень важных различий между пациентами позитивными к anti-LKM-1 и anti-HCV и позитивными только к anti-LKM-1 (аутоиммунный гепатит тип 2). У пациентов с аутоиммунным гепатитом 2 типа anti-LKM-1 реагируют с сегментом 33АА цитохрома Р450 IID6, в то время как у anti-HCV-позитивных пациентов anti-LKM-1 связываются с клеточным протеином GOR 47-1.Iia. Это предполагает молекулярную мимкрию между Р450 IID6 и HCV, хотя гомологичных эпитопов не обнаружено. В заключение необходимо отметить, что иногда у пациентов с аутоиммунным гепатитом 1 типа и высоким уровнем гаммаглобулинов встречается ложно позитивный тест на анти-HCV.
Смешанная криоглобулинемия относится к лимфопролиферативным расстройствам. В ее основе лежит отложение иммунных комплексов в сосудах мелкого и среднего калибра. Наиболее часто она проявляется триадой симптомов: пальпируемой пурпурой, артралгиями и слабостью. Однако, в патологической процесс могут быть вовлечены различные органы и нервная система. В последние годы отмечена четкая связь смешанной криоглобулинемии с HCV-инфекцией. Anti-HCV и HCV RNA выявляют в 42-54% и 84% соответственно у больных со смешанной криоглобулинемией II типа. Криоглобулины обнаруживают у 19 – 54% больных с гепатитом С, особенно, на стадии цирроза. Однако, клиническая симптоматика имеется только в 25% случаев. Более часто криоглобулины встречаются у пациентов с высокой вирусной нагрузкой, генотип не имеет клинического значения. Лечение ИФ приводит к уменьшению или исчезновению криоглобулинов, кожных и других симптомов. Клиническое улучшение не всегда сочетается с вирусологическим ответом и наоборот. Однако, положительный вирусологический ответ и нормализация АЛТ сочетаются с исчезновением криоглобулинов, и, в свою очередь рецидив виремии часто сочетается с рецидивом криоглобулинемии.
Мембранозный гломерулонефрит. HCV четко ассоциируется с развитием мембранопролиферативного гломерулонефрита и нефротического синдрома. Anti-HCV и HCV RNA у таких пациентов обнаруживаются в циркулирующих иммунных комплексах; их депозиты, криоглобулиноподобные структуры и сердцевинный протеин HCV локализуются в гломерулах. ИФ-терапия часто приводит к уменьшению протеинурии, однако, рецидив виремии сочетается с обострением гломерулонефрита. Есть предположения о том, что в таких ситуациях высокие дозы ИФ более эффективны.
Лимфома. Получены данные о широком распространении HCV у больных с В-клеточной не-Ходжкинской лимфомой (20 – 40%). Также описана ассоциация HCV с MALT-лимфомами. Есть результаты об эффективности лечения ИФ HCV-ассоциированных лимфом, однако, этот опыт ограничен.
Аутоиммунные расстройства встречаются в среднем у 23% больных с HCV, ассоциации с генотипом вируса не отмечается.
Наиболее часто наблюдаются расстройства со стороны щитовидной железы. Антитела к щитовидной железе встречаются в 5.2-12.5% случаев. Среди расстройств функции преобладает гипотироидизм (3.1 – 5.5%), преимущественно — у пожилых женщин и пациентов с высоким титром антител к пероксидазе. Лечение ИФ, в свою очередь, может индуцировать заболевание щитовидной железы и выработку к ней антител. Однако, прекращение лечения останавливает этот процесс.
Синдром Съегрена (сухой синдром) связан с прогрессирующей деструкцией экзокринных желез (слюнных и слезных) в связи с их хронической лимфоцитарной инфильтрацией активированными Т- и иногда – В-клетками. HCV-инфекция не связана с первичным синдромом Съегрена, однако, в одном из исследований у 57% больных с ХГС был обнаружен лимфоцитарный сиалоденит, подобный таковому при синдроме Съегрена.
Аутоиммунная идиопатическая тромбоцитопеническая пурпура. У 10-19% больных с аутоиммунной идиопатической тромбоцитопенической пурпурой обнаруживаются anti-HCV. Причинно-следственные связи этих состояний находятся в процессе исследований.
Плоский лишай (Lichen planus). Anti-HCV присутствуют у 10-38% с этой патологией. Механизм ассоциации HCV с Lichen planus не ясен. В процессе ИФ-терапии часто наблюдается обострение Lichen planus.
Поздняя кожная порфирия. Причиной поздней кожной порфирии является снижение активности уропорфириноген декарбоксилазы. Прием алкоголя, эстрогенов и перегрузка железом приводят к клиническим проявлениям этого патологического состояния. Поздняя кожная порфирия ассоциируется с алкогольной болезнью печени и гемосидерозом. Сообщается о выявлении anti-HCV у 62-91% больных с поздней кожной порфирией, что заставляет рассматривать anti-HCV как важнейший фактор развития этого заболевания, хотя конкретная роль HCV в его патогенезе в настоящее время не ясна.
источник
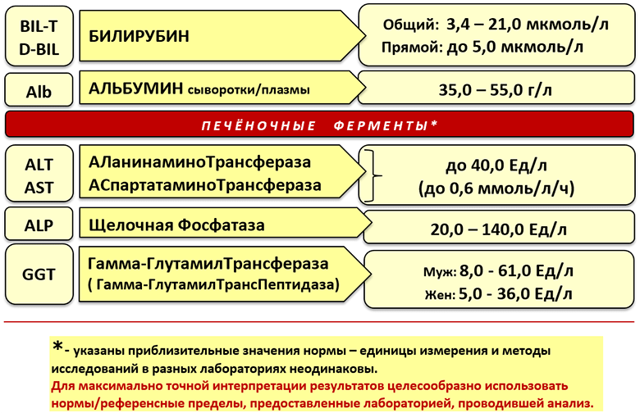
АЛТ и АСТ при гепатите С — те показатели, которые наиболее точно укажут на степень поражения органа и прогрессирование заболевания. С их помощью удается более точно подбирать препараты для комплексной терапии, обеспечивать своевременную помощь больному. Вместе с тем не всегда их увеличение показывает заболевания печени. Часто АСТ и АЛТ позволяют заподозрить проблемы с почками и сердцем. Больным гепатитом анализ на ферментные печеночные вещества нужно сдавать периодически, в соответствии с рекомендациями лечащего врача-инфекциониста либо гепатолога.
Аспартатаминотрансферазы и аминотрансферазы — те ферментные вещества, которые связаны с преобразованием целого ряда аминокислот. Их синтез может осуществляться только в человеческом организме. В некоторой степени эти ферменты содержатся в тканях таких органов, как сердце, почки, в мышечных тканях, но наибольшее их количество производится в печени. Именно поэтому при обнаружении нарушения нормы этих гормонов врачи сначала приступают к комплексному обследованию печени.
Норма для мужчин — иметь таких гормонов немного больше. Это связано с некоторыми гормональными процессами, происходящими в их организме.
Так, уровень АЛТ и АСТ у здорового мужчины должен находиться в пределах 41 ед./Л и 37 ед./Л. У представительниц женского пола такие цифры значительно меньше. Норма для них: АЛТ — 31 ед./Л максимум, АСТ — 30 ед./Л.

Повышается ферментное содержание в крови при таких факторах:
- некрозе тканей печени;
- циррозе;
- доброкачественных образованиях;
- гепатитах;
- миокардите;
- панкреатите;
- инфаркте миокарда;
-
инфекционном мононуклеозе в период обострения;
- серьезных воспалительных процессах.
Другими причинами, которые влияют на степени активности АЛТ и АСТ, являются:
- злоупотребление алкоголем;
- лечение химиотерапией;
- резкое увеличение физической или умственной нагрузки;
- психологический шок;
- прием наркотических веществ;
- отравления свинцом;
- прием некоторых препаратов, в частности Аспирина, комбинированных оральных контрацептивов, Варфарина.
Систематически проверяя ферментную активность, врачи смогут следить за прогрессированием заболевания, при необходимости корректировать схему лечения, вводить дополнительные методы борьбы. Если показатели повышены в 1,5–5 раз, то они трактуются медиками как умеренная гиперферментемия, в 6–10 раз — средней тяжести, в 10 раз — гиперферментемия тяжелой степени. Показатели АЛТ и АСТ редко бывают пониженными.
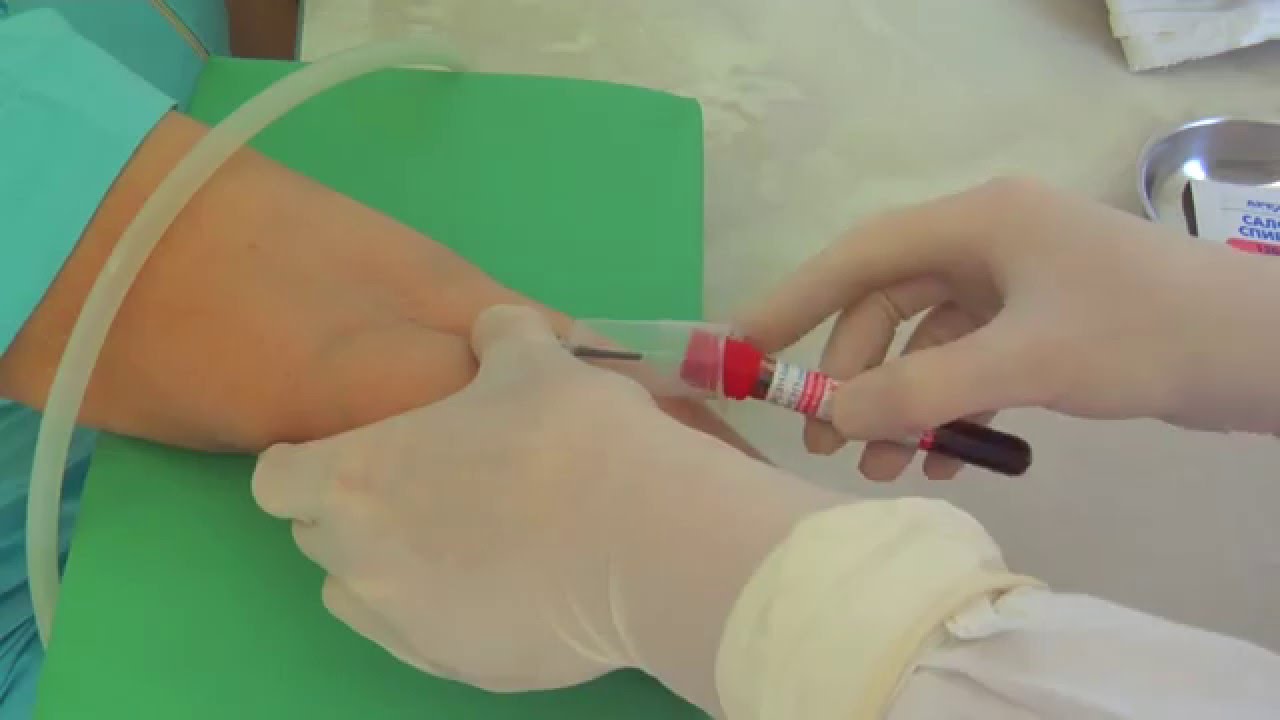
Вирусный гепатит С, как правило, развивается в течение длительного времени — нескольких месяцев и даже лет. Именно поэтому ферментная активность проявляется не сразу. Показатели остаются нормальными, а тем временем заболевание разрушает клетки органа. Заподозрить наличие гепатита врач может по коэффициенту де Ритиса. По своей сути, это соотношение АЛТ и АСТ. Если коэффициент увеличен в 1,33 раза (увеличенная норма АЛТ), тогда можно говорить о патологии со стороны печени. Если же коэффициент меньший, тогда имеется подозрение на сердечные болезни.

Именно тогда завершается инкубационный период, начинается активное размножение и деятельность вирусов в середине клеток, поэтому анализ крови фиксирует увеличение этих цифр. Через несколько дней (недель) таких данных уже заметить не удастся.
Второй пик приходится на этап манифестаций, то есть того момента, когда впервые проявляются неспецифические симптомы гепатита (слабость, потеря аппетита, усталость и т. д.). Это случается в основном через 1,5 месяца с момента заражения. Волнообразные подъемы значений указывают на выход вирусных патогенов в кровь и повторное заражение ими печеночных клеток.
При желтушном гепатите С одновременно с увеличением АЛТ наблюдается и увеличение уровня прямого и общего билирубина. Если же заболевание протекает без желтизны, то анализ укажет только на увеличение выработки ферментных веществ.
После полного выздоровления и исчезновения вируса значения приходят в норму. Вместе с тем встречаются и другие клинические случаи, когда в связи с элиминацией вируса сохранятся стабильно высокие значения. Не всегда снижение показателей трактуется как уменьшение опасности и полное выздоровление.
При хроническом течении заболевания могут проявляться стабильно завышенные показатели или наблюдаться периодические всплески ферментов. Относительное увеличение АСТ указывает на ухудшение ситуации и присоединение дополнительных (вторичных) изменений. К таким, в частности, можно отнести цирроз печени, наличие опухоли.
Увеличение уровня АСТ и АЛТ при появлении гепатита наблюдается в 100% случаев.
Также показатели используются для определения степени активности гепатита.
- нарушение пищеварительного процесса;
- появление диареи и метеоризма;
- изменение цвета кожных покровов (в основном кожа становится желтой);
- частые неприятные срыгивания;
- дискомфорт и боли со стороны печени.
Чтобы выявить уровень трансаминазы и других показателей, забор крови осуществляют из вены. Лучше проводить обследование в утреннее время. Именно тогда показатели наиболее точно соответствуют реальному состоянию здоровья. Поскольку печень — тот орган, который просто мгновенно реагирует на любые изменения питания, пациенту лучше отказаться от еды хотя бы за 8 часов до момента забора материала. Кроме того, запрещается за несколько дней до анализа употреблять алкогольные напитки, за несколько недель нужно отказаться от некоторых видов медикаментов.

Обязательно нужно сообщить лаборанту или врачу обо всех препаратах, принимаемых накануне. Важно указать свой привычный образ жизни, заболевания, которые ранее уже диагностировались, симптомы, проявляющиеся в течение последнего периода. Долго ждать получения результатов не приходится. Большинство лабораторий готовы сообщить полученные данные через 2–3 дня с момента забора материала.
Конечно, многих интересует, как уменьшить уровень ферментов. Понижение ферментной выработки происходит, если заболевание будет полностью вылечено или же вирус гепатита переведен в «неактивное» состояние.
Снизить АЛТ и АСТ удается с помощью диеты. В первую очередь человек должен отказаться от жирной и белковой пищи. Среди продуктов питания, которые нужно ограничить при увеличении печеночных ферментов, следует назвать:
-
лук, чеснок;
- шпинат;
- редьку;
- шоколад;
- кислые фрукты;
- газированные напитки;
- щавель;
- жирные молочные продукты;
- маринованные, соленые продукты;
- сдобную выпечку.

Из ежедневного питания у больных гепатитом должны исключаться: кофе, крепкий чай, шоколадные напитки. От алкогольных продуктов в случае, когда меняется уровень ферментных веществ, нужно обязательно отказаться. Ограничения касаются и количества соли и сахара.
Как снизить АЛТ и АСТ, помимо правильного питания? Здоровый сон, хороший психологический климат, частые прогулки на свежем воздухе — основные факторы, которые дают возможность корректировки количества АЛТ и АСТ показателей. Иногда уменьшить продуцирование ферментов удается благодаря антибактериальной терапии (но редко), иммуномодулирующим медикаментозным препаратам.
Если результат анализов показал присутствие вируса гепатита С, врач, скорее всего, будет рекомендовать проведение противовирусной терапии. Какие препараты использовать и как долго, должен определять специалист, исходя из каждого конкретного случая.
В 2012 году произошел прорыв в лечении гепатита С. Новые противовирусные препараты подтвердили возможность полного выздоровления от гепатита С с вероятностью в 97%. Сколько времени нужно для того, чтобы запустить эти препараты в свободную продажу в России, еще точно не известно, на сегодняшний день проходят экспериментальные исследования по поводу их длительного использования.
Обязательно каждый человек, биохимический анализ у которого подтвердил отклонение от нормальных показателей, должен обратиться к специалисту. Важно понять, что негативные последствия любого заболевания, в том числе и гепатита, будут значительно меньшими, если лечение начнется своевременно. В современной фармацевтике достаточно средств, способных обеспечить снижение печеночных ферментов.
источник
Три обстоятельства определяют серьезность HCV-инфекции.
- Бессимптомное течение острой инфекции: пациенты могут не подозревать о наличии у них инфекции и служить невольным источником заражения окружающих.
- Прогрессирование в хронический гепатит: более чем у 60% инфицированных вирусом после острой фазы не происходит элиминация вируса и развивается ХГС. 2, 40
- Риск развития цирроза печени и ГЦК: ХГС является потенциально фатальным заболеванием. Неуклонно прогрессирующее поражение печени протекает часто бессимптомно, проявляясь клинически только на стадии цирроза печени или ГЦК, когда лечение становится неэффективным.
ОСТРЫЙ ГЕПАТИТ С
Время появления anti-HCV различно: в одних случаях — через 2-4 недели после начала гепатита (прежде всего anti-c22 и anti-с33), в других — через месяцы после повышения уровня аминотрансфераз. 89 У ряда больных с самоограничивающимся течением инфекции anti-HCV никогда не появляются, возможно, вследствие низкой концентрации циркулирующих вирусных антигенов, 2, 14 при этом в сыворотке у них выявляется HCV РНК методом ПЦР. 2 У больных с посттрансфузионным гепатитом ни А, ни В и отсутствием HCV (гепатит ни А, ни В, ни С) кратковременное выявление anti-HCV непосредственно после трансфузии может быть обусловлено пассивным переносом anti-HCV от донора. 89
Принимая во внимание вышеуказанные обстоятельства, а также ограниченную доступность исследования HCV РНК методом ПЦР, диагноз ОГС в настоящее время основывается на данных анамнеза, в том числе эпидемиологического, и исключении других причин острого гепатита (табл. 4). (Ситуация должна измениться по мере введения в широкую практику коммерческих тест-систем для определения HCV РНК методом ПЦР32).
Табл. 4 Критерии исключения ОГС / ни А, ни В, ни С в отсутствие anti-HCV (по Alberti и Realdi 89 )
| Возможные причины острого гепатита | Диагностические критерии |
| Вирус гепатита А Вирус гепатита В Вирус гепатита Е Цитомегаловирус Вирус Эпштейна-Барр | специфические антитела класса IgМ |
| Токсические факторы Алкоголь Лекарства Сердечная недостаточность | анамнез, симптомы и объективные признаки |
| Заболевания желчных путей | объективные, ультразвуковые признаки |
| Аутоиммунный гепатит | антитела (антинуклеарные, к гладкой мускулатуре и микросомам печени и почек, к растворимому печеночному антигену, антимитохондриальные) |
Некоторые морфологические признаки являются характерными для HCV-инфекции (см. «Морфологическое исследование печени»), но не специфичными, поэтому биопсия печени не рекомендуется в качестве рутинного метода диагностики ОГС.
Инкубационный период ОГС длится от 6 до 12 недель, 90 однако может быть укорочен до 2-24 дней у больных, инфицированных при переливании крови и ее продуктов (таких, как VIII фактор); в среднем инкубационный период составляет 7-8 недель. 89
В отличие от острого гепатита А и В, симптоматика которых сходна, ОГС протекает с менее тяжелым поражением печени, мягко или бессимптомно. 89 У небольшой части пациентов имеются продромальные явления (лихорадка), слабость, тошнота, дискомфорт в животе, потемнение мочи и желтуха.
Биохимические показатели, сывороточные маркеры HCV
При ОГС уровень АЛТ может быстро повышаться и затем резко падать, или оставаться повышенным на протяжении некоторого времени — «плато», или (что более характерно) колебаться в течение нескольких недель или месяцев.
На рис. 2 показаны 4 примера сероконверсии в anti-c100 (у двух больных гепатит развился после гемотрансфузии, у двух других факторы риска заражения установить не удалось). 89
Фульминантная печеночная недостаточность — это «острая тяжелая печеночная недостаточность с развитием печеночной энцефалопатии менее чем через 2 недели после начала желтухи» (лабораторным маркером при этом является снижение уровня V фактора свертывания, или проакцелерина, более чем на 50%). 91 Если после начала желтухи до развития указанных проявлений прошло более 2 недель, но менее 3 месяцев, говорят о субфульминантной печеночной недостаточности. 91 При тяжелой печеночной недостаточности помимо желтухи могут наблюдаться нарушения свертывания крови, признаки портальной гипертензии, почечная недостаточность, дыхательные и сердечно-сосудистые расстройства, метаболические нарушения, бактериальные и грибковые инфекции (с повышенной частотой). Проявления энцефалопатии включают в порядке нарастания тяжести хлопающий тремор кистей, нарушения сознания и кому. 91
Частота. Данные о роли HCV в развитии фульминантного гепатита ни А, ни В остаются противоречивыми. Частота выявления anti-HCV у больных фульминантным гепатитом в Японии составила 50%, в то время как в западных странах была крайне низкой. 91, 92 Обстоятельствами, затрудняющими интерпретацию данных, являются отсроченное появление сывороточных маркеров при HCV-инфекции и одновременное наличие маркеров других вирусов (таких как вирусы гепатита В и Е). 91 По мнению японских авторов, повышенная частота фульминантного гепатита С в Японии по сравнению с западными странами может быть связана со следующими факторами:
- относительно высокой частотой HCV в популяции (по сравнению с другими индустриальными странами);
- наличием иммуносупрессивной терапии у некоторых из этих больных и феноменом «иммунного рикошета» при отмене лечения;
- особенностями генотипов HCV, распространенных в Японии.
Тяжесть течения. Сообщается, что фульминантный гепатит ни А, ни В имеет более тяжелое и часто фатальное течение по сравнению с фульминантным гепатитом А или В. 93 Однако, по данным исследования, проведенного в Японии, фульминантный anti-HCV положительный гепатит (составлявший большинство случаев фульминантного гепатита ни А, ни В) характеризовался менее острым и тяжелым, но в то же время более длительным повреждением печени, чем фульминантный гепатит B. 92 По мнению других авторов, риск фульминантного гепатита повышается при сочетанной инфекции HBV и HCV, 94 а также у пожилых ииммунокомпрометированных больных.
Рис 2. Сероконверсия в anti-HCV при ОГС (по Alberti и Realdi, 89 воспроизведено с разрешения)
| Пример 1 | Пример 2 |
 |  |
| Пример 3 | Пример 4 |
 |  |
Примеры 1 и 2 — посттрансфузионный гепатит, 0 — время гемотрансфузии
Примеры 3 и 4 — спорадический гепатит, 0 — начало гепатита.
Пример 1: кратковременное выявление anti-HCV непосредственно после трансфузии, обусловленное, вероятно, пассивным переносом anti-HCV от донора; ранняя сероконверсия на 19-й день.
Пример 2: поздняя сероконверсия на 127-й день.
Пример 3: кратковременное выявление anti-HCV, полное выздоровление.
Пример 4: выраженное и длительное персистирование anti-HCV, прогрессирование в хроничеcкий гепатит.
В исходе ОГС может наблюдаться:
- Выздоровление: полная нормализация АЛТ и исчезновение anti-HCV и HCV РНК в течение 6-12 месяцев от начала заболевания — наблюдается только у 20% больных ОГС.
- Нормализация АЛТ и сохранение HCV РНК в сыворотке, наблюдается примерно у 20% больных, заболевание печени может прогрессировать, несмотря на нормальный уровень аминотрансфераз (см. «Хронический гепатит С. Изменения биохимического анализа крови, сывороточные маркеры HCV»).
- Сохранение повышенного уровня АЛТ и HCV РНК в сыворотке: прогрессирование в хронический гепатит с персистированием anti-HCV — наблюдается примерно у 60% больных.
Отдаленные исходы ОГС у двух последних категорий больных описаны ниже. Предпринимались попытки оценить эффективность лечения ОГС ИФН альфа-2b с целью предотвращения хронизации (результаты обсуждаются в разделе «Лечение острого гепатита С»). Течение HCV-инфекции представлено на рис. 3.
Рис. 3 Течение НСV-инфекции(По Sclimilovitz-Weiss и соавт., 14 воспроизведено с разрешения)
ХРОНИЧЕСКИЙ ГЕПАТИТ С
Если у больных на протяжении 6 месяцев после острой инфекции в сыворотке крови сохраняется повышенный уровень АЛТ и/или маркеры HCV, следует предполагать хроническую HCV-инфекцию; колебания уровня АЛТ с периодической нормализацией могут затруднять диагностику. Как указывалось выше, течение ХГС вариабельно и может приводить к серьезному поражению печени в отсутствие симптомов, с последующим развитием печеночной недостаточности, ГЦК и смерти. Некоторые генотипы, по-видимому, определяют более тяжелое течение хронического гепатита, однако необходимы дальнейшие исследования для окончательного подтверждения предварительных результатов (см. «Хронический гепатит С. Зависимость тяжести течения от генотипа HCV»). 7
Причины высокой частоты хронизации инфекции не ясны. Lau предположил влияние двух факторов вируса: 1) низкий уровень репликации вируса приводит к недостаточной стимуляции клеточного иммунитета; 2) высокая частота мутаций генома HCV позволяет вирусу избегать иммунного надзора. 95
Кроме того, в хронизации гепатита С предполагается участие целого ряда факторов, не относящихся к вирусу.
Факторы риска хронизации HCV-инфекции 89
- Посттрансфузионное заражение (попадание большого количества вируса, в отличие от спорадических случаев)
- Парентеральное заражение
- Массивные гемотрансфузии
- Трансфузии коммерческой крови
- Тяжелое течение острой инфекции
- Высокий уровень АЛТ во время острой инфекции
- 3начительные колебания уровня АЛТ во время острой инфекции
- Выявление anti-HCV
- Мужской пол
Выявление больных
Наблюдение за больными ОГС (с наличием anti-HCV) или ни А, ни В, ни C позволяет выявить больных хронической HCV-инфекцией. Примерно у 90% больных посттрансфузионным гепатитом обнаруживаются anti-HCV. 2 В отсутствие anti-HCV наличие виремии подтверждается определением HCV РНК методом ПЦР. Некоторые гистологические признаки являются характерными (но не специфичными) для ХГС и используются в качестве критериев, позволяющих проводить дифференциальный диагноз с аутоиммунным гепатитом и хроническим гепатитом В (см. «Морфологическое исследование печени»).
Диагностика спорадических случаев ХГС более трудна, основная часть больных выявляется при тестировании донорской крови, при обследовании по поводу неспецифических проявлений (слабость, отсутствие аппетита) или лабораторных изменений (повышение АЛТ).
В большинстве случаев ХГС имеет бессимптомное или мягкое течение вплоть до поздних стадий, когда развивается цирроз печени и тяжелые осложнения хронического заболевания печени; желтуха при этом является плохим прогностическим признаком. 96 У некоторых больных клинические проявления наблюдаются только при развитии ГЦК. 14 Несмотря на это, качество жизни, связанное со здоровьем и физическим статусом, у больных хроническим гепатитом С оказалось существенно ниже, чем в общей популяции. 97, 98 Специальное анкетирование выявило ухудшение качества жизни во всех категориях: работа, сон, отдых, развлечения. 97 Больные хроническим гепатитом С, по данным обзора SF-36 Health Survey, были сопоставимы по тяжести заболевания с больными сахарным диабетом II типа (7 баллов по 8-балльной шкале) и по сравнению со здоровыми лицами имели гораздо худшие показатели физиологических функций, общего здоровья и жизнеспособности. 98
У большинства больных наблюдается медленное прогрессирование заболевания, однако в ряде случаев цирроз печени развивается быстро, в особенности у инфицированных в более старшем возрасте, при наличии сопутствующего алкоголизма, лейкоза, коинфекции HBV и ВИЧ. 14
Биохимические показатели, сывороточные маркеры HCV
На рис. 4 показана динамика уровня АЛТ и anti-HCV наряду с данными морфологического исследования печени у больного хроническим посттрансфузионным гепатитом С прогрессирующего течения и формированием цирроза печени в течение 8 лет. 89 Существуют значительные различия в скорости прогрессирования болезни, динамике биохимических показателей и вирусологических маркеров.
Уровень АЛТ: имеет тенденцию к значительным колебаниям в течение многих месяцев и лет (от 2 до 8 верхних пределов нормы), наблюдаются и более высокие, и нормальные значения. 14
Даже в отсутствие повышения активности АЛТ может наблюдаться прогрессирование поражения печени (в присутствии HCV). 5, 99 Частота данного феномена остается неясной.
Уровень ГГТ: более высок, чем при других формах вирусного гепатита. 89
Фракция IgG иммуноглобулинов сыворотки: часто повышена. 89
Активность ACT больше, чем АЛТ: предполагает наличие цирроза печени. 14
Снижение уровня альбумина сыворотки: предполагает наличие цирроза печени. 14
Удлинение протромбинового времени: предполагает наличие цирроза печени. 14
Уровень HCV РНК сыворотки: наличие HCV РНК даже в отсутствие повышения ACT, АЛТ может отражать повреждение печени. 5, 99 (Повышение уровня аминотрансфераз не всегда коррелирует с гистологической активностью). 100 В исследовании, проведенном в Италии, из бессимптомных лиц, серопозитивных по anti-HCV, HCV РНК выявлялась только у больных с морфологически подтвержденным ХГС (т.е. признаками воспаления) даже при нормальном уровне аминотрансфераз, а у лиц с отсутствием изменений при биопсии печени HCV РНК в сыворотке отсутствовала. 99 По данным другого исследования, титры HCV РНК были гораздо выше при умеренном и тяжелом ХГС (см. «Морфологическое исследование печени»), чем при мягком гепатите или циррозе. 101 Необходимы дальнейшие исследования по установлению связи титра HCV РНК с активностью печеночного процесса и прогнозом заболевания.
Рис. 4 Длительное наблюдение посттрансфузионного гепатита С (по Alberti и Realdi, 89 воспроизведено с разрешения)
стрелка — биопсии печени: (1) — мягкий-умеренный гепатит, (2) — тяжелый гепатит, (3) — активный цирроз печени
Прогрессирование в цирроз печени
По меньшей мере у 20% больных хроническим гепатитом в течение примерно 20 лет развивается цирроз печени, ассоциируемый с повышенным риском развития ГЦК. 90 В ряде случаев прогрессирование в цирроз происходит более быстрыми темпами. 102, 103 Итальянские исследователи показали, что цирроз печени формируется у 32% больных хроническим посттрансфузионным гепатитом С к концу 7,5-летнего периода наблюдения. 102 По данным наблюдения 155 больных ХГС в Японии, цирроз развился в среднем через 8 лет у 30%, ГЦК — у 15%. Частота спонтанной ремиссии составила 2% (для сравнения, из 173 больных хроническим гепатитом В спонтанная ремиссия наступила у 38%). 103
Зависимость тяжести течения от генотипа HCV
При инфицировании разными генотипами вируса не выявляется каких-либо различий в уровне АЛТ или альбумина (см. «Географическое распределение генотипов HCV»). 7 Однако, пациенты, инфицированные генотипом 1 вируса имеют более тяжелое течение болезни по сравнению с имеющими генотипы 2, 3, 4 (табл. 5).
Табл. 5 Генотипы HCV при хроническом гепатите разной степени тяжести
| Генотип | Мягкий-умеренный хронический гепатит | Тяжелый хронический гепатит | р |
| 1 | 8(27,5%) | 21(72,4%) | 0,03 |
| 2 | 4(44,4%) | 5(55,5%) | — |
| 3 | 5(62,2%) | 3(37,5%) | — |
| 4 | 8(42,1%) | 11(57,8%) | — |
| Всего | 26(38%) | 41(61,1%) | — |
— различие не достоверно
Смешанные вирусные инфекции
В ряде случаев имеет место коинсрекция HBV и HCV с/без HDV. 104-108 HCV, по-видимому, подавляет HBV, а также HDV 105-108 и может являться причиной активности заболевания печени в отсутствие репликации HBV и HDV. 107 При коинфекции HBV и HCV повышается не только вероятность более тяжелого течения гепатита и развития цирроза, но и риск ГЦК. 109, 110
Морфологическое исследование печени
Биопсия печени: показания, противопоказания
Больным с подозрением на ХГС рекомендуется проведение биопсии печени для исключения других возможных причин заболевания печени и для оценки активности и стадии поражения печени (наличие цирроза). У больных циррозом печени при «слепой» чрескожной биопсии морфологические признаки цирроза примерно в 20% случаев могут не выявляться вследствие крупноузлового поражения печени или недостаточного забора материала. 111 Биопсия печени противопоказана при нарушениях свертывающей системы крови или расширении внутрипеченочных желчных протоков. 112 В отдельных случаях биопсия выполняется при лапароскопии или трансвенозным путем.
Морфологические признаки ХГС
Характерными морфологическими признаками ХГС являются лимфоидные скопления или фолликулы в портальных трактах, 2 которые могут встречаться изолированно или в сочетании с воспалительной инфильтрацией портальных трактов и повреждением желчных протоков той или иной степени выраженности. Обычно наблюдаются мелкоочаговые некрозы и лимфоидноклеточные инфильтраты внутри долек, жировая дистрофия гепатоцитов (у 3/4 больных). 2 Гистохимический анализ позволяет выявить антиген HCV в ткани печени, 2 с помощью ПЦР обнаруживают HCV РНК. Чем выше содержание HCV в печени, тем более выражены признаки воспаления. Высокие концентрации вируса выявляются в поздних стадиях хронического заболевания печени. 2, 113
Таким образом, наиболее частыми морфологическими признаками ХГС являются:
- мягкий хронический гепатит (см. ниже)
- лимфоидные фолликулы
- лобулярные некрозы и лимфоидные инфильтраты, жировая дистрофия, ацидофильные тельца
- HCV-антиген в ткани печени (гистохимическое свечение)
- HCV РНК (ПЦР)
Определение степени активности и стадии заболевания
Использовавшаяся до недавнего времени классификация хронического гепатита, основанная на гистологических критериях (согласно которым выделялись хронический персистирующий, хронический активный и хронический лобулярный гепатит), отражает скорее степень тяжести заболевания, чем самостоятельные формы болезни. В зависимости от репликации вируса, состояния иммунной системы организма и других факторов эти «формы» могут переходить друг в друга 114 и каждая из них — в цирроз печени и/или ГЦК. В настоящее время хронический гепатит клинически определяется более общими терминами: «мягкий», «умеренный» или «тяжелый».
Современная классификация хронического гепатита, разработанная совместно гепатологами Европы и США, основана на определении степени активности (оценка тяжести) и стадии (оценка прогрессирования) заболевания. 114 Для оценки тяжести хронического гепатита наиболее широко используется индекс гистологической активности Кноделя, 115 имеющий четыре компонента, каждый из которых оценивается по балльной системе (табл. 6). На основании суммарного индекса, полученного при оценке трех первых компонентов, выделяется «мягкий», «умеренный» или «тяжелый» хронический гепатит (табл. 7). Четвертый компонент (отсутствие или наличие фиброза, цирроз) в действительности характеризует стадию заболевания (табл. 8), коррелируя с другими методами оценки фиброза. 114
Табл. 6 Оценка индекса гистологической активности 115
| Компоненты индекса | Пределы баллов |
| 1. Перипортальные некрозы с или без мостовидных некрозов | 0-10 |
| 2. Внутридольковая дегенерация и фокальные некрозы | 0-4 |
| 3. Портальное воспаление | 0-4 |
| 4. Фиброз | 0-4 |
Табл. 7 Соответствие индекса гистологической активности прежней классификации хронического гепатита
| Индекс | Определение | Прежняя терминология |
| 1-3 | Минимальный хронический гепатит | Неспецифичный реактивный гепатит; ХЛГ; ХПГ |
| 4-8 | Слабовыраженный хронический гепатит | Тяжелый ХЛГ, ХПГ; мягкий ХАГ |
| 9-12 | Умеренный хронический гепатит | Умеренный ХАГ |
| 13-18 | Тяжелый хронический гепатит | Тяжелый ХАГ с мостовидными некрозами |
ХЛГ-хронический лобулярный гепатит
XПГ-хронический персистирующий гепатит
ХАГ-хронический активный гепатит
Табл. 8 Стадии хронического гепатита 114
| Индекс фиброза | Описание |
| Отсутствие фиброза | |
| 1 | Слабый фиброз |
| 2 | Умеренный фиброз |
| 3 | Тяжелый фиброз |
| 4 | Цирроз |
Окончательный диагноз хронического гепатита, согласно предложенной классификации, должен основываться на определении этиологии, степени активности и стадии заболевания. 44 Пример формулировки диагноза: хронический гепатит С (этиология) умеренной степени активности (тяжесть) с выраженным фиброзом (стадия).
ГЕПАТОЦЕЛЛЮЛЯРНАЯ КАРЦИНОМА
Связь с хронической HCV-инфекцией
Эпидемиологические исследования показали прямую связь ХГС с развитием ГЦК. 110, 116, 117 В Европе, США и Японии HCV имеет, возможно, большее значение, чем HBV, в данном контексте. 103, 118 Предполагается, что риск развития ГЦК при ХГС превышает риск печеночно-клеточной недостаточности или кровотечения из варикозно-расширенных вен пищевода, в связи с чем больные должны регулярно проходить ультразвуковое обследование и контроль уровня альфа-фетопротеина сыворотки. 2
Цирроз печени является важным фактором риска развития рака печени и обнаруживается примерно у 97% больных ГЦК с наличием сывороточных маркеров HCV. 2 В отличие от вируса гепатита В не получено доказательств интеграции генома HCV в геном печеночной клетки. Однако канцерогенное действие вируса несомненно. 119 Имеются сообщения о развитии ГЦК при хроническом гепатите С без цирроза печени. 116, 120
Прогноз больных ГЦК с наличием anti-HCV значительно хуже по сравнению с больными, имеющими в сыворотке HBsAg или с алкоголь-индуцированным раком печени, так как опухоль при HCV-инфекции имеет тенденцию к мультифокальному росту и часто поздно диагностируется. 2, 121 В связи с этим представляется чрезвычайно важным регулярный скрининг больных HCV-инфекцией (особенно на стадии цирроза печени) в отношении ГЦК. 2
СОЧЕТАНИЕ HCV-ИНФЕКЦИИ С ДРУГИМИ ЗАБОЛЕВАНИЯМИ И СИНДРОМАМИ
HCV-инфекция вовлекается в патогенез других заболеваний и синдромов, помимо аутоиммунного гепатита.
Синдром Шегрена. HCV-инфекция у больных хроническим гепатитом может выступать в роли пускового механизма локальных иммунных реакций, приводящих к развитию морфологических изменений в слюнных железах, характерных для синдрома Шегрена — лимфоцитарного сиалоаденита. 122
Эссенциальная смешанная криоглобулинемия(ЭСК). Иммунный ответ на HCV может приводить к развитию ЭСК. У больных ЭСК в сыворотке с высокой частотой обнаруживаются anti-HCV и HCV РНК, 123 вирионы HCV и комплексы HCV антиген-антитело в криопреципитатах. 124, 125 Предлагается лечение интерфероном альфа при данном заболевании. 125-129 (см. «Особенности применения ИФН альфа-2b А. Эссенциальная смешанная криоглобулинемия»).
Поздняя кожная порфирия (ПКП). Роль HCV-инфекции обсуждается в патогенезе поражения печени при ПКП. 130-132 В исследовании, проведенном в Испании, 75 из 95 больных спорадической ПКП имели anti-HCV, в то время как из 5 больных семейной ПКП anti-HCV не были выявлены ни у одного. 130 При этом частота выявления anti-HCV возрастала пропорционально степени активности по гистологическим признакам. Авторы предположили, что HCV может выступать в роли триггера ПКП у предрасположенных лиц, поскольку примерно у 2/3 больных признаки HCV-инфекции имелись до развития ПКП. Был сделан вывод о необходимости тестирования на HCV всех больных ПКП и у серопозитивных больных при наличии активности печеночного процесса обсуждать лечение интерфероном альфа. Связь между HCV-инфекцией и ПКП выявлена также исследователями из Ирландии и Франции. 131, 132
Алкогольное поражение печени. Примерно у 1/3 больных с алкогольным поражением печени выявляются anti-HCV и/или HCV РНК. 133, 134 Наличие HCV РНК не обязательно влияет на морфологическую картину печени, 134 однако, по-видимому, повышает вероятность прогрессирования заболевания и развития цирроза печени 133, 135 и, что более важно, оказывает влияние на выживаемость больных. Четырехлетняя выживаемость больных алкогольным гепатитом с наличием HCV-маркеров была на 50% меньше пo сравнению с больными, не имевшими маркеров HCV (24% против 49%, р=0,08). 136
источник
 инфекционном мононуклеозе в период обострения;
инфекционном мононуклеозе в период обострения;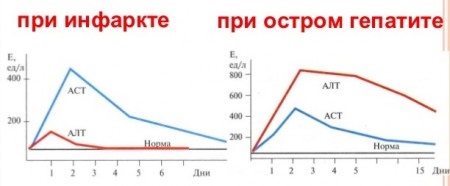
 лук, чеснок;
лук, чеснок;
