Многие годы безуспешно боретесь с БОЛЯМИ в ПЕЧЕНИ?
Глава Института заболеваний печени: «Вы будете поражены, насколько просто можно вылечить печень просто принимая каждый день.
Диагностика вирусного гепатита B основывается на характерном анамнезе заболевания, клинических данных (желтуха, гепатомегалия) и лабораторных (серологических) данных (выявление в крови специфических антител к вирусу, антигенов вируса). Кроме того, для выявления генетического вирусного материала можно использовать метод ПЦР (молекулярно-генетический анализ на гепатит B).
При сборе анамнеза у пациентов с вирусным гепатитом B принимаются во внимание следующие данные: были ли за несколько месяцев до манифестации болезни переливания крови, любые другие медицинские манипуляции, введение наркотиков (особенно совместное, нестерильным инструментом), незащищенные половые акты (особенно с новыми партнерами), другие контакты с носителями вируса гепатита B.
Кроме анализов на гепатит B большое значение в его диагностике имеет специфическая клиническая картина: постепенное начало болезни, выраженность периода, предшествующего появлению желтухи, наличие периода выраженной диспепсии, наличие артралгий (боли в суставах) и характерная сыпь на коже.
Достоверно верифицируется вирусный гепатит B только путем выявления специфических антигенов вируса в крови методом ИФА или РИА. Это — HBsAg, HBeAg, HBcAg. Кроме того, достоверным маркером гепатита B является обнаружение иммуноглобулина анти-HBc, анти-HBs, анти-HBe (IgM, IgG). Так, HBsAg обнаруживается в крови в инкубационном периоде заболевания, буквально через 2–4 недели после инфицирования у приблизительно 80% пациентов. При адекватном лечении через 3–4 месяца антиген HBs в крови исчезает, и к этому моменту концентрация антител (иммуноглобулин M) к антигену HBs (анти-HBs) в крови становится максимальной.
Концентрация антигенов (HBsAg) тем ниже, чем тяжелее течение болезни. Так, при молниеносном течении вследствие массовой гибели вирусов HBsAg выявляется только самыми чувствительными методами, в то время как антитела (анти-HBs) к частицам вируса обнаруживаются раньше. Таким образом, факт выявления в крови пациента антигенов вируса и антител к ним необходимо увязывать с клинической симптоматикой, чтобы не прийти к ложным выводам относительно стадии болезни и тяжести ее течения.
Выявление специфического маркера гепатита B (анти-HBc, который относится к иммуноглобулинам группы M) считается наиболее достоверным признаком заболевания и практически с полной вероятностью подтверждает диагноз. IgM сохраняется в крови на протяжении всей болезни вплоть до полного выздоровления. Иммуноглобулин группы M является маркером острой фазы заболевания. Затем его концентрация в крови идет на спад, и через 2–3 месяца после выздоровления выявляются уже иммуноглобулины группы G (анти-HBc), обеспечивающие длительный иммунитет (практически пожизненный) у более чем 80% пациентов.
Кроме HBsAg в период инкубации в крови может обнаруживаться HBeAg, однако он не стоек и быстро разрушается при воздействии факторов иммунитета (уже в среднем через неделю после появления). К концу данного периода нарастает концентрация антител к HBe. Но если уровень антител нарастает медленно, а антигены HBe выявляются на протяжении месяца и более, это свидетельствует о переходе болезни в хроническую фазу.
Для диагностики гепатита B используется метод ПЦР. С его помощью можно достоверно обнаружить генетический материал (ДНК) вируса в клетках организма: в крови, в гепатоцитах, в лимфоцитах — во всех местах, где происходит процесс репликации вирусных частиц. Метод ПЦР очень точный. При диагностике вирусного гепатита, вызванного мутантными штаммами вируса, которые зачастую не определяются стандартными серологическими методами, ПЦР считается крайне эффективным способом диагностики.
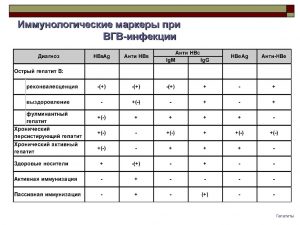
В таблице представлены различные варианты и комбинации антигенов и антител (полученные методом ИФА, РИА) и ДНК вируса (ПЦР), характерные для определенных периодов болезни.
Используя метод ПЦР в совокупности с методами серологической диагностики гепатита B, можно не только достоверно констатировать наличие генетического вирусного материала в организме, но и отличить острый период заболевания от хронического, определить момент выздоровления, судить о сформировавшемся иммунитете, об эффективности лечения, давать прогнозы.
Многие люди, у которых диагностируют этот вирус, находятся в полной растерянности от этого известия. Ведь очень часто многие виды гепатитов проходят без малейших симптомов. К таким видам относится и вирусный гепатит В. На сегодняшний день численность заболевания им возрастает. Это связано с распространенной наркоманией, проституцией, алкоголизмом. Поэтому для излечения данного вируса необходимо вовремя его диагностировать и понять основные причины его возникновения и степень сложности ее течения.
Поставить точный диагноз можно только при клинических исследованиях или с помощью экспресс-тестов. С помощью диагностики можно увидеть разные стадии заболевания: инфицирование вирусом, выздоровление или прогрессирование заболевания.
Раньше обнаружение инфекции было большой проблемой, но сегодня, благодаря качественной диагностике, его возможно обнаружить в самых начальных стадиях.
Можно выделить следующие антигены вирусного гепатита:
- HBsAg представлена в виде вирусной белковой молекулы. Ее белок необходим для того, чтобы определять клетки печени, к которым он будет прикрепляться. В основном он выявляется по прошествии нескольких недель. Его можно выявить с помощью лабораторных исследований посредством проведения серологических анализов на маркеры гепатита. Если выявляется этот антиген, в таком случае он может свидетельствовать о:
- Острой форме заболевания, которая будет сочетаться с HBsAg,HBeAg, Anti-HBc суммарных.
- Хронической форме, если идет сочетание с положительным HBeAg, Anti-HBc суммарных.
- Неопасное инфицирование, при взаимодействии Anti-HBc суммарных.
- HBeAg под ней понимается вирусный белок. Если выявят этот маркер, значит вирус достаточно активный. Этот антиген инфицируется в основном кровью. При положительном диагнозе этого вируса, можно говорить, о том, что началась активная фаза обострения гепатита или большая возможность заражения.
- HbcoreАg, — это ядерный белок, его можно диагностировать во время обследования печени, по маркерам крови его выявить невозможно. Однако если проводить анализ крови, можно выявить антитела к этому белку. После заражения организма, он начинает активную выработку антигенов, в то время как иммунитет выделяет антитела, для борьбы с ними. Антигены и антитела, полностью соответствуют друг другу, а наличие их в крови определяется положительным результатом.
Также, кроме антигенов, существуют антитела при гепатите В, они бывают следующие:
- Анти-HBs – это антитела к белку поверхностному гепатита В. Во время контакта иммунитета и белка, начинаются всевозможные помехи в виде образования антител, которые затрудняют ему внедриться в клетки организма. Благодаря антителам, клетки иммунитета смогут быстро обнаружить проникший в организм вирус и быстро его уничтожить.
- анти-НВс представлен антителами к белку ядерному вируса. Если в анализах находят маркер этих антител, это расшифровывается так, что у организма есть иммунитет к этому вирусу либо после вакцинации, либо самостоятельного излечения. Если его находят при исследованиях, это не означает, что человек инфицирован, просто организм сталкивался с ним и выработал к нему иммунитет. А об инфицировании можно судить, только после результатов других маркеров.
- IgM анти-НВс, в основном они проявляются на начальных этапах заболевания. Обнаружение положительного диагноза может означать присутствие острой и активной формы болезни при неправильном его лечении и высокой вероятности его заражения.
- анти-НВe, помогает препятствовать распространению ядерного белка вируса. Благодаря им иммунитет может активно бороться с вирусом, останавливая его распространение на начальных этапах.
При выявлении определенного антигена, обозначается форма болезни, его активность и дальнейшее его лечение.
Проведение расшифровки заболевания проводится по обнаруженным антигенам:
- так называемый австралийский антиген (HBsAg) можно обнаружить в период обострения. Положительный результат может обозначиться через месяц после попадания вируса в организм. А проявление активности антител свидетельствуют о том, что больной выздоровел и сформировал иммунитет к этой болезни. Его диагностика проводится с помощью иммуноферментного анализа, по-другому ИФА
- антиген HBcAg нельзя определить по крови, а только после обследования печени. А антитела появляются во время начала обострения и находятся все время в крови;
- антиген НВеAg свидетельствует о высокой активности вируса, а антитела появляются сразу после снижения активности антигена.
Сейчас существует множество клинических исследований, которые позволяют на ранней стадии определить антиген вируса и состояние активности вируса в крови. Это позволяет назначить правильную схему лечения, которая поможет справиться с вирусом.
Можно выделить основные причины заражения:
- Употребляя наркотики в виде инъекций.
- Во время половых актов.
- В стоматологии и тату-салонах, если приборы плохо дезинфицируются.
- После переливания крови и хирургических операциях.
В основном им болеют родственники инфицированного человека, наркоманы, люди, которые занимаются секс услугами, медработники, заключенные, дети, которые родились от больной матери. Существует специальная таблица, которая в полной мере раскрывает суть всех вирусов гепатита, определяет пути передачи и их симптоматику.
источник
В основе всех серологических реакций лежит взаимодействие антигена и антитела.
Метод обнаружения с диагностической целью антител в сыворотке крови обследуемого .
В этом случае из двух компонентов реакции (антитело, антиген) неизвестным является сыворотка крови, так как постановка реакции проводится с заведомо известными антигенами. Положительный результат реакции свидетельствует о наличии в крови антител, соответствующих применяемому антигену; отрицательный результат указывает на отсутствие таковых.
Достоверные результаты получают при исследовании «парных» сывороток крови больного, взятой вначале заболевания (3-7 день) и через 10-12 дней. В этом случае удается наблюдать динамику нарастания антител. При вирусных инфекциях лишь четырехкратное и более повышение титра антител во второй сыворотке имеет диагностическое значение.
С внедрением в практику лабораторий метода иммуноферментного анализа (ИФА) стало возможным определять в крови больных антитела, относящиеся к различным классам иммуноглобулинов (JgM и JgG), что существенным образом повысило информативность серологических методов диагностики.
При первичном иммунном ответе, когда иммунная система человека взаимодействует с инфекционным агентом в первый раз, синтезируются преимущественно антитела, относящиеся к иммуноглобулинам класса М ( JgM ) . Лишь позднее, на 8-12-й день после попадания антигена в организм, в крови начинают накапливаться антитела иммуноглобулинов класса G ( JgG ) . При иммунном ответе на инфекционные агенты вырабатываются также и антитела класса А ( JgA ), которые играют важную роль в защите от инфекционных агентов кожи и слизистых оболочек.
Полимеразная цепная реакция (ПЦР), являющаяся одним из методов ДНК-диагностики, позволяет увеличить число копий детектируемого участка генома (ДНК) бактерий или вирусов в миллионы раз с использованием фермента ДНК-полимеразы. Тестируемый специфический для данного генома отрезок нуклеиновой кислоты многократно умножается (амплифицируется), что позволяет его идентифицировать. Сначала молекула ДНК бактерий или вирусов нагреванием разделяется на 2 цепи, затем в присутствии синтезированных ДНК-праймеров (последовательность нуклеинов специфична для определяемого генома) происходит связывание их с комплементарными участками ДНК, синтезируется вторая цепь нуклеиновой кислоты вслед за каждым праймером в присутствии термостабильной ДНК-полимеразы. Получается две молекулы ДНК. Процесс многократно повторяется.
Для диагностики достаточно одной молекулы ДНК, т. е. одной бактерии или вирусной частицы. Введение в реакцию дополнительного этапа — синтеза ДНК на молекуле РНК при помощи фермента обратной транскриптазы — позволило тестировать РНК-вирусы, например вирус гепатита С.
ПЦР — это трехступенчатый процесс , повторяющийся циклично: денатурация, отжиг праймеров, синтез ДНК (полимеризация). Синтезированное количество ДНК идентифицируют методом иммуноферментного анализа или электрофореза.
- Преимущество ПЦР в диагностике инфекционных заболеваний перед другими методами исследований заключается в следующем:
- возбудитель инфекции может быть обнаружен в любой биологической среде организма, в том числе и в материале, получаемом при биопсии;
- возможна диагностика инфекционных болезней на самых разных стадиях заболевания;
- возможность количественной оценки результатов исследований ( сколько вирусов или бактерий содержится в исследуемом материале);
- высокая чувствительность метода.
В настоящее время выделяют следующие формы вирусных гепатитов: гепатит А, гепатит В, гепатит С, гепатит D, гепатит Е, гепатит G и гепатит ТТ. Для диагностики каждой из перечисленных форм вирусных гепатитов используется определенный перечень маркеров.
Гепатит А — острая энтеровирусная инфекция. Возбудитель — вирус гепатита А (ВГА,HAV) — энтеровирус типа 72. Геном вируса представлен однонитчатой РНК. Вирус гепатита А содержит единственный антиген (HA-Ag). Удельный вес гепатита А в суммарной заболеваемости вирусными гепатитами составляет 70-80%. В структуре заболеваемости гепатитом А дети составляют до 80%, причем основная масса — дошкольники и школьники начальных классов.
Гепатит В – вирусная антропонозная инфекция. Возбудитель вирус гепатита В (ВГВ, HBV) – относится к семейству гепаднавирусов, ДНК-содержащих вирусов, поражающих клетки печени. Вирионы ВГВ имеют наружную липопротеидную оболочку и нуклеокапсид, содержащий двунитчатую ДНК и ДНК-зависимую ДНК-полимеразу.
- В структуре ВГВ (HBV) выделяют следующие антигенные системы:
- поверхностный («австралийский») антиген, HBsAg, находящийся в составе липопротеидной оболочки ВГВ, является маркером ВГВ, указывая на инфицированность вирусом;
- ядерный (core), HBcAg – обнаруживается в составе нуклеокапсида вирионов, свидетельствует об активной репродукции вируса;
- HBeAg – входит в состав ядра ВГВ, указывая на активность вируса и, кроме того, на его высокую вирулентность и инфицированность;
- HBxAg – расположен вблизи оболочки вириона, его роль в генезе инфекции изучается.
В диагностике вирусного гепатита В ведущее значение имеет определение комплекса маркеров гепатита. Свыше 5% населения планеты охвачено этой инфекцией, а частота безжелтушных форм ВГВ составляет, по данным разных авторов, от 60 до 82%.
Гепатит С (ВГС) – вирусное заболевание, наиболее часто протекающее в виде посттрансфузионного гепатита с преобладанием безжелтушных и легких форм и склонное к хронизации процесса.
Возбудитель — вирус гепатита С – имеет сходство с флавовирусами, содержит РНК. На основе филогенетического анализа выделено 6 генотипов ВГС и более 80 субтипов.
Генотип 1 — наиболее распространенный генотип во всем мире (от 40 до 80%). Генотип 1а является доминирующим для США, а 1b преобладает в Западной Европе и Южной Азии.
Генотип 2 распространен во всем мире, однако встречается с меньшей частотой, чем генотип 1 (от 10 до 40%).
ВГС тип 3 характерен для Индии, Пакистана, Австралии и Шотландии. Генотип 4 распространен преимущественно в Средней Азии и Египте, генотип 5 – в Южной Африке, а генотип 6 – в Гонконге и Мокао.
Примерно 90% всех случаев посттрансфузионных гепатитов связано с ВГС. Среди доноров антитела к вирусу гепатита С (анти-ВГС) обнаруживают в 0,2-5% случаев.
У 40-75% пациентов регистрируется бессимптомная форма болезни, у 50-75% больных острым ВГС формируется хронический гепатит, у 20% из них развивается цирроз печени. Важная роль ВГС отводится и в этиологии гепатоклеточной карциномы.
Геном вируса гепатита С представлен одноцепочечной положительно заряженной РНК, которая кодирует 3 структурных и 5 неструктурных белков. К каждому из этих белков вырабатываются антитела, обнаруживаемые в крови больных гепатитом С.
Отличительной чертой ВГС является волнообразное течение заболевания, в котором разграничивают 3 фазы: острую, латентную и фазу реактивации.
Для острой фазы характерно повышение активности печеночных ферментов в сыворотке крови, уровня антител класса IgM и IgG к ВГС с нарастанием титров, а также РНК ВГС.
Латентная фаза характеризуется отсутствием клинических проявлений, наличием в крови антител класса IgG к ВГС в высоких титрах, отсутствием антител класса IgM и РНК ВГС либо их присутствием в низких концентрациях на фоне незначительного повышения активности печеночных ферментов в периоды обострения.
Для фазы реактивации характерно появление клинических признаков, повышение активности печеночных ферментов, наличие антител класса IgG (к нуклеокапсидному белку core и неструктурным белкам NS) в высоких титрах, присутствие РНК ВГС и нарастание титров антител класса IgM к ВГС в динамике.
Гепатит D – вирусная инфекция, вследствие биологических особенностей вируса протекающая исключительно в виде ко- или суперифекции при гепатите В, характеризующаяся тяжелым течением,
часто неблагоприятным исходом.
Самостоятельно, без вируса В, вирус гепатита D не может попасть в организм человека
Возбудитель – вирус гепатита D (ВГD), по своим биологическим свойствам приближается к вироидам – обнаруженным молекулам нуклеиновых кислот. Печень человека – единственное место размножения (репликации) ВГD.
Известно существование двух вариантов инфекции: коинфекция (одновременное заражение ВГВ и ВГD) и суперинфекция (заражение HBsAg-позитивных пациентов). Сочетание ВГВ и ВГD сопровождается развитием более тяжелых форм патологического процесса, что определяется главным образом действием ВГD.
Летальность при суперинфекции достигает 15-20%. Инфицирование дельта-вирусом может вызывать острое заболевание, заканчивающееся выздоровлением, или формировать хроническое носительство ВГD.
При гепатите D могут отсутствовать в крови маркеры гепатита В – анти НВс и НВs-антиген – и наблюдается угнетение ДНК-полимеразной активности, так как ВГD ингибирует репликацию вируса гепатита В.
источник
Для определения вируса гепатита, получения информации о происхождении болезни, условиях и причинах возникновения проводится серодиагностика гепатита с, b, a. Выявление серологических маркеров позволяет поставить диагноз и предпринять правильное лечение. К маркерам относятся вирусные белки, специфичные антитела, которые вырабатывает организм как ответ на инфекцию и нуклеиновые кислоты вируса.
ВАЖНО ЗНАТЬ! Даже «запущенная» печень или желчный пузырь лечатся дома, без операций и уколов. Просто прочитайте что сделала Ольга Кричевская читать далее.
Серодиагностика — распознавание этиологии заболеваний способом выявления антител в крови. Серологические маркеры относятся к поздней диагностике, так как реакции возможны на 10−12 дней от начала болезни. Серодиагностические исследования проводят, чтобы:
- диагностировать заболевание — определить наличие антител в крови, используя стандартные антигены;
- определить возбудитель — выявить неизвестные антигены.
Для проведения серодиагностики используют: бактериальные клетки; плазмоциты и лимфоциты, опухолевые и пораженные клетки; растворимые компоненты. Выделяют 6 групп серологических реакций:
- Реакции, которые происходят с укрупнением частиц Ag.
- Реакции связывания комплемента и иммунный гемолиз.
- Реакция иммунофлюоресценции.
- Реакции нейтрализации Anti.
- Реакция с фагоцитозом.
- Реакции иммуносорбентного анализа с применением антигенов и антител.
Вернуться к оглавлению
Проведение серодиагностики назначают больным, если по каким-то причинам нет возможности провести диагностику, исключающую заболевание. Анализ выявляет тип возбудителя инфекции и помогает поставить диагноз. Также серодиагностика позволяет подобрать наилучший вариант лечения. Симптомы для сдачи анализа: необоснованные приступы слабости, плохой аппетит, тошнота, изменение цвета каловых масс и урины, желтизна кожи. Своевременная серодиагностика подтверждает или опровергает инфицирование и определяет стадию заболевания.
Оболочка каждого вируса имеет собственный набор белков. А аминокислоты, которые составляют белок, считаются своеобразным кодовым набором. Этот код и является маркером при серодиагностике. Маркерами гепатита А являются anti-НАV IgM и IgG. Маркерами гепатит В — HBcAg, HBsAg, HBeAg. Маркерами вируса С — HBCAg. Для проведения серодиагностики на вирус А применяют: ИЭМ (иммуноэлектронную микроскопию), РСК (связывания комплемента), РИА (применение меченых Anti и Ag), РЭМА (реакцию энзим антител). Серодиагностика на вирус В использует РИА, РЭМА, РПГ (преципитация в геле) и РИГА (непрямая гемагглютинация). При реакции РИГА используют эритроциты, которые нагружены HBsAg. Для серодиагностики гепатита С применяют иммуноферментный анализ.
Исследование при гепатите А нацелено на определение IgM и IgG. Данные показатели появляются в крови как только уровень сывороточных ферментов в организме увеличивается. Anti-НАV IgМ — является показателем уровня антител М к вирусу гепатита. После инфицирования показатель вырастает и пока не появятся первые симптомы, анализ крови будет показывать положительный результат. Аnti-НАV IgG — данный класс определяется через 10 недель после попадания инфекции в организм. Показатель чаще всего остается высоким и после выздоровления, он свидетельствует о том, что начинается процесс формирования иммунитета к вирусу типа А.
С помощью маркера HBsAg можно выявить гепатит B на самом раннем этапе, антиген проявляется на 27−41 день после попадания инфекции в организм.
Исследование нацелено на выявление антигенов и антител. Серодиагностика позволяет поставить диагноз и спрогнозировать исход болезни. Для каждой стадии, обнаруживается разный маркер HBV. На протяжении инкубационного периода антиген сохраняется в крови от 2 до 5 месяцев. Показателем инфицирования является одновременное определение HBs и НВс. В начале восстановления из крови исчезают HBc и HBe, образуется anti-НВс, позже в крови определяются антитела ко всем типам антигена. Наличие HbsAg говорит о заражении, если антиген есть в крови больше полугода, значит, заболевание находится в хронической стадии. Anti-HbsAg — показывает, что в организме образовались антитела и иммунная система активно борется с вирусом. HbsAg выявляется еще некоторое время после выздоровления. Anti-HbcAg выявляется с проявления симптомов и продолжается на протяжении всего периода.
Вирус гепатита С размножается неактивно, поэтому возникают трудности в диагностике инфицирования. Единственный способ выявления вируса С — определение РНК. Его определение проводят способом иммуноферментного анализа, выявляя количество Anti-HCV. Антитела определяются через 4−6 недель после попадания вируса в кровь. В этот период начинается формирование и циркуляция IgM. Через 3 месяца начинается синтез IgG. Длительное обнаружение IgM говорит об активности вируса и хронической стадии болезни. При хронической форме выявление IgM свидетельствует о поражении печени. Результат иммуноферментного анализа не является основанием для постановки диагноза, метод используется как скрининговый тест для выявления хронической формы. Обнаружив антитела к HCV и при подозрении на гепатит С необходимо пройти комплексное лабораторное обследование.
Иммуноферментный анализ серодиагностики позволяет обнаружить антитела к гепатиту С в 95% случаев хронической формы, при острой форме — точность метода 50−70%.
Серодиагностика не имеет 100% специфичности и чувствительности при диагностике вирусных гепатитов. Поэтому при оценке результатов необходимо учитывать симптоматику и использовать для диагностики несколько тестов, подтверждающих полученный результат. При оценке результатов серологических исследований следует учитывать анамнез заболевания, сведения о перенесенных заболеваниях и вакцинации, а также возможный контакт с источником инфекции.
Судя по тому, что вы сейчас читаете эти строки — победа в борьбе с заболеваниями печени пока не на вашей стороне.
И вы уже думали о хирургическом вмешательстве? Оно и понятно, ведь печень — очень важный орган, а его правильное функционирование — залог здоровья и хорошего самочувствия. Тошнота и рвота, желтоватый или сероватый оттенок кожи, горечь во рту, потемнение цвета мочи и диарея. Все эти симптомы знакомы вам не понаслышке.
Но возможно правильнее лечить не следствие, а причину? Рекомендуем прочитать историю Ольги Кричевской, как она вылечила печень и очистила желчный пузырь. Читать статью >>
источник
Современная лабораторная диагностика HCV-инфекции основана на нескольких основных методиках исследования, которые делят на две группы в зависимости от технологии проведения – серологические и молекулярные. Эти анализы направлены на то, чтобы выявить основные маркеры гепатита С максимально точно и в кратчайшие сроки. В большинстве лабораторий сейчас применяют современные реагенты и оборудование, что позволяет поставить диагноз через 14–20 дней после заражения.
Эксперты не могут озвучить точное количество инфицированных HCV, так как в подавляющем большинстве случаев через несколько недель после заражения происходит хронизация вирусного процесса. В дальнейшем болезнь часто протекает в скрытой, латентной форме годами. Более чем у половины пациентов патологию диагностируют случайно при обращении к врачу по другому поводу, прохождении диспансеризации, оформлении медицинской книжки, постановке на учет по причине беременности и т.д.
По данным Всемирной организации здравоохранения, более полумиллиона человек ежегодно умирают от осложнений, вызванных HCV. Данная патология лидирует в перечне показаний для трансплантации печени.
Несмотря на меры по профилактике распространения заболевания, появление высокоэффективных лекарственных препаратов и методов диагностики, позволяющих своевременно выявить и полностью излечить болезнь, остановить рост количества инфицированных не удается ни в одной стране мира.
Возбудитель гепатита С, Hepatitis C Virus, относится к семейству Flaviviridae. Основу генома вируса составляет одноцепочечная РНК, включающая более 10 000 нуклеотидных остатков. Из-за неоднородности структуры специалисты выделили несколько генотипов HCV. Их распространенность не одинакова в различных уголках планеты. Но в большей степени диагностируют первый генотип (более 46% инфицированных), на втором месте – третий (треть случаев).
Еще одной характерной особенностью возбудителя гепатита Ц является мутационная активность. Так, у пациента в рамках одного генотипа идентифицируют до 40 подвидов HCV. По этой причине специалисты не могут создать вакцину для пожизненной защиты от инфицирования.
Заражение часто происходит при использовании одного шприца несколькими людьми для введения внутривенных наркотиков. Путь передачи болезни может быть также связан с применением уже использованных или недостаточно стерилизованных медицинских и/или косметологических инструментов. Возможно заражение при половом контакте, не исключен и вертикальный путь инфицирования.
В 80% случаев болезнь протекает без выраженных клинических проявлений.
Только у незначительного количества пациентов возникает один или несколько из таких симптомов:
- повышение температуры без катаральных признаков;
- усталость;
- снижение аппетита;
- тошноту с приступами рвоты;
- боли в животе;
- потемнение мочи;
- появление у фекальных масс сероватого оттенка;
- боли в суставах;
- желтизна склер и кожных покровов (встречается относительно редко, только при желтушной форме заболевания).
Что касается хронического течения патологии, период отсутствия симптомов может продолжаться вплоть до развития цирроза печени, печеночной недостаточности либо злокачественного онкологического образования.
Острую форму HCV диагностируют крайне редко, что связывают с бессимптомным прогрессированием заболевания. Для выявления патологии используют серологические методы, направленные на определение ряда специфических иммуноглобулинов, которые являются обязательной частью иммунного ответа на попадание вирусного патогена внутрь гепатоцитов. Другим методом диагностики является определение структурных частиц вируса при помощи молекулярно-химических реакций.
Что значит маркеры гепатита С? В медицинской литературе этот термин означает ряд высокоспецифичных лабораторных параметров, свидетельствующих о наличии острого либо хронического ВГС. Это, в частности, иммуноглобулины G и M (и их суммарный титр без дифференцирования на классы) и РНК (определенная часть генома) вириона. Соответственно, результаты, полученные в ходе выполнения ИФА и ПЦР (данные оценивают только в комплексе), и являются маркерами HCV.
В настоящее время существуют законодательно определенные критерии (на основе рекомендаций ВОЗ и Министерства здравоохранения), кому нужно обязательно сдавать анализ крови для выявления возможной HCV-инфекции:
- в период вынашивания ребенка (в I и III триместре);
- реципиентам донорского биологического материала (вне зависимости от его вида и количества), особенно если процедура и/или операция была проведена до 1992 года (именно тогда появились достоверные методы исследования, позволяющие выявить основные маркеры гепатита C);
- работникам медицинской, косметологической, торговой сферы (в соответствии со сроками оформления медкнижки);
- пациентам, регулярно проходящим процедуру гемодиализа, регулярно подвергающихся разнообразным инвазивным вмешательствам;
- перед назначением операционных вмешательств;
- перед началом курса химиотерапии;
- при отклонениях в показателях печеночных проб (для исключения или подтверждения гепатита);
- пациенты, состоящие на учете в специализированных клиниках и диспансерах на предмет пристрастия к наркотическим веществам;
- персонал детских образовательных учреждений, интернатов (при регулярном прохождении диспансеризации);
- члены семей и находящиеся в близком контакте с человеком с диагностированным ВГС;
- лица с повышенным риском инфицирования (инъекционные наркоманы, люди, отдающие предпочтение гомосексуальным, случайным или коммерческим половым связям);
- осужденные и пребывающие в местах лишения свободы;
- доноры биологического материала, органов;
- дети до достижения годовалого возраста (если выявлены положительные серологические маркеры вирусных гепатитов, то дольше) при наличии у матери диагностированного ВГС во время беременности;
- у людей с ВИЧ.
HCV-инфекция – серьезный диагноз, требующий немедленного начала терапии. Поэтому положительные маркеры, выявленные в одном из исследований, не являются показанием к приему лекарственных препаратов. Подтверждают наличие инфекции по нескольким специфическим анализам.
Где сдать кровь на выявление HCV, решает пациент. Можно обратиться в поликлинику по месту жительства, записавшись на консультацию к терапевту или инфекционисту. Врач выдаст направление на проведение анализа, но перед этим придется сделать клиническое исследование крови, печеночные пробы. Стоимость тестов компенсируется по полису ОМС.
Можно выполнить анализы в платной лаборатории. Там не требуется направление от врача. Стоимость в клиниках Москвы колеблется в пределах 3000–7000 тысяч рублей и выше в зависимости от разновидности диагностического теста и того, сколько маркеров необходимо определить.
Все исследования, применяемые для диагностики HCV-инфекции, можно разделить на несколько групп. Проведение каждого анализа является обязательным до начала терапии, а некоторые исследования выполняются и на определенных этапах лечебного цикла для оценки правильности и эффективности подобранной противовирусной схемы.
Для постановки диагноза врачу нужны следующие данные:
- Серологические маркеры вирусных гепатитов. Обнаруживаются вне зависимости от генотипа HCV. Это специфические антитела (anti-HCV) разновидностей G и/или M. Выявляются иммуноферментными методами (ИФА), технологиями иммунохемилюминисценции, иммуноблотинга и т.д. Изначально определяют суммарное количество антител (IgG + IgM) А подтверждающее исследование направлено на выявление антител к специфическим протеинам HCV, входящим в структуру капсида и оболочки, при помощи ИФА или иммуноблотинга.
- Молекулярные маркеры. Назначаются в качестве подтверждающих тестов для определения наличия РНК возбудителя патологии, оценки его количественного содержания. К этой же группе исследований относят генотипирующие анализы, предназначенные для установления разновидности вируса. Для проведения тестов используются различные методики постановки полимеразной цепной реакции (ПЦР).
Следующий этап диагностики проводят только при положительном результате предыдущих тестов. По мнению специалистов у пациентов с первым генотипом HCV целесообразно определение уровня IL28B. Подобное исследование помогает прогнозировать эффективность противовирусного лечения. Но такая схема диагностики подходит при использовании интерфероновых схем терапии. Связь между показателем IL28B и действием современных лекарственных средств (Софосбувира, Асунапревира и т.д.) не установлена, потому необходимость в проведении такого исследования остается под вопросом.
Первичная лабораторная диагностика HCV начинается с определения в сыворотке крови параметра anti-HCV. Положительный результат свидетельствует об активном течении патологического процесса (то есть заражении гепатитом С) либо о встрече иммунной системы организма с инфекцией в прошлом.
В большинстве лабораторий Москвы и других крупных городов серологический маркер определяется при помощи иммуноферментных систем (ИФА) II и III поколения. Суть анализа состоит в захвате рекомбинантными белками антител к HCV из исследуемой сыворотки. Впоследствии они определяются вторичными антителами против Ig класса G и V, мечеными ферментами, которые катализируют течение цветной реакции.
Тест-системы I поколения имели низкую специфичность, так как были способны обнаружить антитела, вырабатываемые к белку NS4. Чувствительность ИФА не превышала 70%, а сроки обнаружения иммуноглобулинов – минимум 16 недель с момента инфицирования.
ИФА II поколения способны выявить антитела к участку генома core, NS3 и NS4, что повышает специфичность теста до 95%, снижает риск получения ложноположительных результатов и сокращают срок обнаружения иммуноглобулинов до 10 недель от дня попадания РНК вируса в кровь человека.
Тест-системы ИФА III поколения разработаны на основе антигена NS5 и высокоиммуногенного эпитопа (части молекулы антигена) NS3. Подобная техника выполнения анализа обеспечивает срок сокращения серологического окна: положительные маркеры (либо отрицательный результат) можно получить уже на 4–6 неделе после заражения. Чувствительность ИФА последнего поколения достигает 99%.
Несмотря на то, что серологическое исследование является одним из золотых стандартов диагностики HCV, возможно получение ложноположительных или ложноотрицательных результатов, связанных не с качеством тест-систем, а особенностями состояния пациента.
Так, на проведение ИФА могут повлиять:
- аутоиммунные поражения суставов, особенно при положительном ревматоидном факторе, и другие заболевания подобного генеза;
- беременность;
- регулярное проведение гемодиализа;
- тяжелые иммуносупрессивные состояния (например, на фоне ВИЧ);
- гематологические злокачественные новообразования.
Современные тест-системы, дополненные рекомбинантными NS5, специфичны и чувствительны на 99,95% не реагируют на наличие в крови ревматоидного фактора и/или С-реактивного белка.
Серологический скриннинг является обязательным, но недостаточным компонентом диагностики HCV. Для подтверждения результатов анализа обязательно назначают исследование методом полимеразной цепной реакции.
Сейчас доступны качественные и количественные способы выявления РНК возбудителя вирусного гепатита С. Первая методика предназначена для подтверждения диагноза HCV-инфекции у лиц с положительным anti-HCV и для обследования донорского материала.
Количественный анализ служит основным маркером определения вирусной нагрузки. Является ключевым для оценки активности патологического процесса и эффективности противовирусной терапии. Применяемые тест-системы позволяют провести полимеразную цепную реакцию в режиме «real time». Диапазон вирусной нагрузки колеблется в пределах от 10–15 до 10 млн. МЕ/мл.
Техника количественной полимеразной цепной реакции – маркер репликации хронического вирусного гепатита С. Согласно современным рекомендациям, анализ проводят на 4–12–24 неделе лечения (и дополнительно на 48 при проведении интерфероновой терапии). Повторно исследование делают через 24 и 48 недель после окончания приема и/или инъекций медикаментов.
Отрицательный результат количественной ПЦР на 4 неделе лечения – один из основных факторов быстро вирусологического ответа и благоприятного исхода заболевания. Отсутствие РНК вируса на 24 неделе после завершения терапии является признаком выздоровления.
После базовых диагностических тестов и подтверждения положительных маркеров гепатита С обязательно проведение генотипирования. От результатов этого исследования зависит тактика дальнейшей терапии и прогноз развития риска осложнений. Определение генотипа HCV выполняется путем анализа нуклеотидной последовательности участка NS5 протеина вируса.
Но применяемые для генотипирования тест-системы недостаточно совершенны и не могут точно идентифицировать недавно выявленные, редко встречающиеся генотипы (в частности, 7,8 и 9).
В последних клинических исследованиях доказана роль определения полиморфизма гена IL28B у пациентов с генотипом 1а и 1b HCV. Проведение анализа важно для выбора между интерфероновыми схемами терапии и приемом комбинации противовирусных лекарственных препаратов.
Пункционная биопсия печени также входит в перечень необходимых для пациента с вирусом гепатита С анализов. Процедура позволяет оценить тяжесть структурных изменений в печеночной ткани, установить локализацию и распространенность фибротического процесса, некроза гепатоцитов, наличие злокачественной малигнизации клеток (при длительном течении хронического гепатита С), роль сопутствующих осложнений в повреждениях печени.
Но перед выполнением процедуры необходимо принять во внимание несколько факторов:
- Оценивают соотношение целесообразности проведения биопсии и потенциального вреда здоровью пациента.
- Перед манипуляцией делают УЗИ для оценки риска возможных осложнений. В идеале пункцию также нужно проводить под ультразвуковым контролем.
- За несколько дней до процедуры выполняют коагулограмму, определяют протромбиновое время и протромбиновый индекс. Если количество тромбоцитов менее 90 тыс. клеток/мм3, биопсию откладывают или выполняют при наличии строгих жизненных показаний.
- Перед манипуляцией необходимо взять письменное согласие пациента на процедуру.
- При необходимости (например, перевозбуждении) больному дают седативные средства (при отсутствии противопоказаний).
- После проведения забора ткани оценивают количество и качество биоптата. При необходимости процедуру сразу же повторяют.
- На протяжении 8 часов после манипуляции пациент должен оставаться под медицинским наблюдением.
Еще одним сравнительно новым методом оценки состояния печени является эластометрия, проводимая с использованием приборов ФиброСкан, ФиброТест, ФиброМетр и др. Преимуществом данного способа диагностики служит неинвазивность, быстрое получение результатов и безболезненность, что важно в педиатрической практике. Но проведение исследования затруднительно при избыточном весе пациента, наличии стеатоза, превышении уровня печеночных ферментов в 3 раза и более.
Для получения точных результатов важно соблюдать правила, предписывающие, как сдавать кровь и готовиться к проведению исследования.
Все аспекты необходимо уточнить у врача, но перечень стандартных рекомендаций включает:
- соблюдение диеты (№5 или №5а) с ограничением жирного, жареного, копченого за 7–10 дней до процедуры;
- строгое ограничение алкоголя за 2–2,5 недели до выполнения анализа;
- отказ от курения за 12–14 часов до забора крови;
- сдачу крови строго натощак (последний прием пищи за 12 часов до посещения лаборатории).
Результаты может быть искажены при приеме некоторых лекарственных препаратов. Поэтому при расшифровке данных необходимо сообщить врачу о каких-либо принимаемых медикаментах.
Сколько ждать результатов исследования зависит от загруженности лаборатории, технологической оснащенности (иногда требуется транспортировка биологического материала). В среднем постановка полимеразной цепной реакции или выполнение ИФА занимает от 2 до 5 дней. Некоторые клиники предлагают услугу платного срочного исследования.
Диагностика гепатита С проводится в несколько этапов.
Показанием для определения серологических маркеров методом ИФА (anti-HCV Total) служат:
- беременность (первый и третий семестр);
- отношение к группам риска по ВГС;
- ежегодное оформление медицинской книжки;
- повышение уровня печеночных трансаминаз и/или билирубина;
- самостоятельное желание пациента.
Для подтверждения диагноза HCV при положительных результатах серологического исследования назначают качественный анализ ПЦР. Обнаружение РНК вируса свидетельствует об остром или хроническом течении вирусной инфекции, что требует дальнейшего обследования пациента для подготовки к проведению терапии.
Назначают следующие диагностические тесты:
- определение иммуноглобулинов G и М для установления стадии заболевания (острая, хроническая, рецидив латентного течения инфекции);
- оценка вирусной нагрузки;
- генотипирование;
- • определение степени поражения печени.
Обязательны и другие исследования: клинические анализы крови, мочи и кала, выявление возможных сопутствующих коинфекций (ВИЧ, аутоиммунные заболевания), исключение или подтверждение беременности.
Биологическим материалом для проведения ИФА и ПЦР является сыворотка крови. Реже исследование проводят на биоптате печени, но такой тест трудоемкий, дорогостоящий и требует выполнение инвазивных медицинских процедур.
В 2017 году на фармацевтическом рынке появились экспресс-тесты, позволяющие проводить предварительную диагностику гепатита С по образцу слюны. Преимуществом набора является возможность выполнения самостоятельно в домашних условиях. Но результат экспресс-теста также требует подтверждения, несмотря на то, что его специфичность достигает 96%.
Расшифровка серологических маркеров на гепатит С обязательно проводится в тандеме с данными полимеразной цепной реакции. Значение полученных результатов приведено в таблице ниже.
| Определяемый показатель | Возможный диагноз |
| Положительный anti-HCV | |
| На фоне отрицательного результата полимеразной цепной реакции | |
| На фоне положительного результата качественной ПЦР | Подтверждение диагноза острого или хронического гепатита |
| Положительные данные качественного анализа методом полимеразной цепной реакции – маркер HCV-инфекции | |
| При IgM «+» и отрицательном титре IgG | Свидетельствует об остром течении заболевания и недавнем заражении (до полугода). Прогноз благоприятный, лечение могут отсрочить на несколько недель (4–6) из-за вероятности самостоятельного излечения без медикаментозного вмешательства |
| При IgG «+» и отсутствии IgM | Указывает на наличие хронической инфекции. Иногда такой результат – маркер носителя гепатита С, когда болезнь протекает без выраженной клинической картины |
| При IgG «+» и IgM «+» | Симптом острого рецидива хронического патологического процесса |
Иногда пациенты и врачи сталкиваются с ситуацией, когда качественный анализ методом ПЦР на РНК отрицательный, а маркеры положительные (при проведении серологического обследования).
В таком случае доктора придерживаются следующей тактики:
- Повторная постановка полимеразной цепной реакции для исключения ошибочного результата вследствие лабораторной ошибки.
- Исключение/подтверждение заболеваний, синдромов и состояний, которые могут быть вероятной причиной ложноположительного результата ИФА.
- Сбор анамнеза. Такая картина характерна после перенесенного острого гепатита С. При этом человек может сам не знать о прошедшем заболевании. Сопоставление симптоматики (в том числе неспецифической), предположение пути заражения и данных клинических исследований позволяют доктору предположить такой исход патологического процесса.
- Повтор анализа через 3–4 недели, когда можно исключить вероятность диагностического окна.
Но вне зависимости от результатов исследований трактовать полученные данные должен только врач. Специалисты предостерегают от самостоятельной терапии. Комбинация противовирусных препаратов и длительность их применения подбирается с учетом генотипа HCV наличия или отсутствия коинфекций и ряда других факторов.
источник
Основой лабораторной диагностики вирусных гепатитов служат:
— знания об их возбудителях и репликации
— информация о появлении и исчезновении маркеров инфицирования
— современные иммунохимические и молекулярно- биологические методы детекции антигенов, антител и нуклеиновых кислот/
Лабораторная диагностика гепатита В (ГВ)
Лабораторная диагностика ГВ — основана на выявлении специфических для ГВ антигенов и соответствующих антител в крови, а также вирусных нуклеиновых кислот, основными из которых являются:
анти-НВс класса Ig М и IgG
Наиболее широко в диагностике ГВ используется определение НВsAg. Данный антиген выявляется как при остром, так и при хроническом заболевании (однако острая инфекция обычно подтверждается наличием высоких титров анти-НВс IgМ). При остром ГВ поверхностный антиген вируса обнаруживается через 3-5 недель от момента инфицирования, то есть задолго до появления клинических признаков болезни и в этих случаях является единственным серологическим маркером. НВsAg постоянно выявляется в преджелтушном и желтушном периодах болезни. Персистирование НВsAg в течение 6 месяцев и более указывает на затяжное или хроническое течение болезни, и позволяет предположить хроническое носительство вируса. Элиминация НВsAg и появление антител к нему является непременным условием выздоровления. Серологическими маркерами репликации ВГВ являются — анти-НВс класса IgМ, НВеAg, ДНК и ДНК-полимераза, которые обнаруживаются при остром ГВ с первых дней клинических проявлений и могут обнаруживаться при обострении хронического ГВ. Серологические маркеры репликации ВГВ определяют как в целях общей диагностики, так и для оценки эффективности применяемой терапии. НВсAg выявляется в ткани печени и не определяется в сыворотке крови. Опосредовано его присутствие в организме отражают циркулирующие антитела – анти-НВс класса IgМ и IgG. В острый период ГВ наличие анти-НВс класса IgМ является дополнительным маркером этого заболевания. Однако необходимо учитывать, что около 50% больных хроническим ГВ также могут иметь эти антитела в периоде обострения, но чаще в низких концентрациях. Наличие в сыворотке крови только анти-НВс класса IgG наблюдается в период между исчезновением НВsAg и образованием анти-НВs. Сочетанное выявление анти-НВс класса IgG в низком титре с анти-НВs указывает на перенесенную ГВ-инфекцию и наличие иммунитета. Все применяемые методы исследования для определения специфических маркеров ГВ можно разделить на 2 группы – иммунохимический и молекулярно-биологические. Иммунохимические – основное место принадлежит иммуноферментному анализу (ИФА) с его высокой чувствительностью и специфичностью, простотой проведения и стабильностью реактивов. Молекулярно-биологические – точечная и жидкостная гибридизация, а также цепная полимеразная реакция (ПЦР) – позволяет выявлять наличие ДНК-ВГВ непосредственно, либо с помощью определения вирусоспецифического фермента – ДНК- полимеразы..
Лабораторная диагностика гепатита Д (ГД) Вирус гепатита Д (ВГД) – это дефектный вирус, содержащий одно-спиральную РНК, которому для репликации необходимо помощь вируса ГВ для синтеза оболочечных белков, состоящих из HBsAg, который используется для инкапсуляции генома ВГД. Маркером активной репликации ВГД также является анти-ВГД класса IgМ. Серологические маркеры инфекции ГД зависят от того, как был приобретен вирус – в виде коинфекции с ВГВ (у большинства больных заболевание имеет острое течение и заканчивается выздоровлением) или суперинфекции у больных с хронической ГВ-инфекцией (протекает тяжелее, чем коинфекция — в 10% развивается фульминантный гепатит). При коинфекции в большинстве случаев антитела — анти-ВГД класса IgМ и IgG — обнаруживаются в течение заболевания. Титр анти-ВГД обычно снижается до практически неопределяемых уровней после выздоровления, и не сохраняется никаких серологических маркеров того, что человек был когда-либо инфицирован ВГД. Антиген ВГД определяется только у 25% больных и обычно исчезает вместе с исчезновением HВsAg. При суперинфекции у больных с хронической ГВ-инфекцией серологическая картина имеет следующие характерные особенности: – титр HBsAg снижается к моменту появления антигена ВГД в сыворотке; — антиген ВГД и РНК-ВГД продолжают определяться в сыворотке, так как обычно у большинства пациентов с суперинфекцией ГД (70-80%) развивается хроническая инфекция, в отличие от случаев коинфекции; — определяются высокие титры антител (анти-ВГД) как класса IgМ, так и IgG, которые сохраняются неопределенное время. Серологические маркеры вируса ГД определяют методом иммуноферментного и радиоиммунного анализа, а РНК-ВГД — методом полимеразной цепной реакции.
Лабораторная диагностика гепатита С (ГС) Открытие Геном вируса ГС (ВГС) представлен однонитчатой позитивной РНК, состоящих из 10 000 нуклеотидных оснований, образующих регионы, которые кодируют три структурных белка (С, Е1, Е2) и пять неструктурных (NS2, NS3, NS4, NS5). Лабораторная диагностика ГС основывается на обнаружении серологических маркерв ВГС: антител к вирусу ГС (анти-ВГС, анти-ВГС класса IgМ, IgG) методом ИФА и РНК-ВГС методом ПЦР. К настоящему времени разработаны 4 поколения тест-систем для выявления анти-ВГС в иммуноферментном методе, но ИФА первого поколения сейчас не используется из-за низкой чувствительности. РНК-ВГС является показателем активной репликации ВГС и самым ранним маркером инфекции, и может быть обнаружена методом полимеразной цепной реакции уже через 1- 2 недели после инфицирования, незадолго до повышения уровня сывороточных трансаминаз. Анти-ВГС обнаруживаются к 5-6 неделе после начала гепатита в 80% случаев и к 12 неделе у 90% лиц методом иммуноферментного анализа. При определении анти-ВГС в некоторых случаях регистрируется ложноположительная реакция. Для разграничения ложноположительных образцов от образцов действительно содержащих антитела к ВГС, разработаны дополнительные тесты – рекомбинантный иммуноблотинг, определение спектра белков анти-ВГС. Иммуноблотинговые диагностикумы позволяют исключить неспецифический результат, полученный методом ИФА, однако визуальная оценка иммуноблотинговых полос может быть неоднозначной в разных диагностических центрах. Диагноз хронического ГС у лиц с наличием анти-ВГС обычно ставится на основании повышенных печеночных проб в течение более 6 месяцев.
Лабораторная диагностика гепатита А (ГА) Вирус ГА — это РНК- содержащий вирус, размером 27 нм, классифицированный как пикорнавирус. Лабораторная диагностика ГА основана на выявлении маркеров вируса ГА – антигена ВГА, антител (анти-ВГА класса IgМ и IgG ), а также РНК ВГА. Окончательным доказательством о текущей или недавней инфекции служит наличие в сыворотке крови (даже в одной пробе сыворотки) антител к ВГА класса IgM (анти-ВГА IgM) и наличие ВГА в фекалиях. На перенесенную инфекцию ГА, а также на длительный иммунитет, указывает наличие антител к ВГА класса IgG (анти-ВГА IgG). Диагноз острого ГА подтверждается в острой или ранней стадии выздоровления при наличии анти-ВГА класса IgM, которые появляются в последние 5-10 дней инкубационного периода и продолжают выявляться на протяжении 6-7 месяцев от начала заболевания. Кроме того, эти антитела могут быть выявлены в первые месяцы у лиц (20-30%), вакцинированных инактивированной вакциной против ГА. Их образование связано с первичным иммунным ответом на введение антигена, а не на инфекцию, вызванную вакциной. РНК ВГА может быть выявлена за несколько дней до повышения активности АлАТ и в течение 5 — 59 дней заболевания при типичном течении ГА; при затяжных случаях — РНК ВГА в среднем может определяться до 95 дней. Антиген вируса ГА (ВГА-Ag) обнаруживается в фекалиях больных за 7-10 дней до проявления клинических симптомов и в первые дни заболевания, что используется также для ранней диагностики и выявления источников возбудителя инфекции. Концентрация ВГА в фекалиях является наивысшей на протяжении 2-х нед. перед появлением желтухи. У взрослых выделение вируса с фекалиями продолжается обычно менее одной недели после появления желтухи. Вирус, однако, был обнаружен также через 2 мес. от начало заболевания (во время обострения). Дети могут выделять вирус более длительно, чем взрослые, возможно в течение нескольких недель после клинического проявления заболевания. Хроническое выделения ВГА из фекалий не отмечается. Определение антигена ВГА нашло также применение в санитарной вирусологии при исследовании воды на наличие вируса. Анти-ВГА класса IgG также появляются рано в начале заболевания (с 3-4 недели), сохраняются на протяжении всей жизни и обеспечивают пожизненную защиту от этого заболевания. Определение анти-ВГА IgG используется для изучения иммуноструктуры населения, динамики специфического гуморального иммунитета. Определение анти-ВГА класса IgG важно также для пред- и поствакцинального скрининга (минимальная протективная концентрация анти-ВГА соответствует 20 МЕ/л).
Для диагностики гепатита А прежде всего проводится расспрос больного, во время которого врач выясняет, не было ли у пациента за 7-50 дней до начала заболевания контакта с больными желтухой, не употреблял ли он сырую воду из случайных источников, немытые овощи и фрукты.Во время осмотра пациента учитываются такие симптомы гепатита А: острое начало болезни с резким повышением температуры и расстройством пищеварения, присоединение через несколько дней желтухи и улучшение на этом фоне самочувствия, увеличение печени и селезенки. Наконец, в обязательном порядке проводятся анализы крови на гепатит А, которые указывают на недавнюю инфекцию или на наличие уже выработанного в результате предыдущего инфицирования иммунитета к вирусу гепатитаА.Анализы на гепатит А могут показать повышение в крови больного билирубинаи печёночных ферментов; существуют анализы на антитела (иммуноглобулины) к вирусу гепатита А класса М (анти-НАV IgМ или анти-ВГА IgМ), которые выявляются с помощью иммуноферментного анализа (ИФА) в сыворотке крови с первых дней болезни и далее в течение 3-6 месяцев. Анти-ВГА IgМ вырабатываются у всех больных гепатитом А, их обнаружение — ранний надёжный тест, позволяющий выявить любые варианты гепатита А и поставить диагноз до наступления желтухи. В диагностике гепатита В большое внимание уделяется опросу пациента и выявлению факторов риска гепатита В: факты внутривенного введения наркотических средств, случаи переливания крови, оперативные вмешательства и другие манипуляции, связанные с нарушением целостности кожных покровов или слизистых, случайные половые связи, тесный контакт с носителями вируса гепатита В или с больными хроническими заболеваниями печени в сроки от 6 недель до 6 месяцев до начала заболевания. Для диагностики гепатита В очень важны результаты анализов на антигены. Вирус гепатита В содержит 3 основных антигена: поверхностный НВsАg, внутренний НВcАg (который можно определить только в клетках печени) и связанный с ним НВеАg. Ко всем этим антигенам в ходе инфекционного процесса образуются антитела. Для их определения используется иммуноферментный анализ(ИФА). Кроме анализов на антитела, важную роль в диагностике гепатита В играет анализ на ДНК вируса гепатита В, который осуществляется методом полимеразной цепной реакции (ПЦР). Исходя из результатов анализов крови на гепатит В можно определить стадию заболевания, наличие хронического гепатитаВ, а также наличие иммунитета к заболеванию гепатитом В. При положительных анализах на гепатит В проводится обследование методом ИФА на наличие в крови больного маркеров дельта-вирусной инфекции, то есть гепатита D. Для постановки диагноза вирусного гепатита С, как правило, используется несколько лабораторных тестов. Среди них биохимический анализ крови и анализ крови на антитела к вирусу гепатита С (анти-HCV). Положительные результаты анализов на вирус гепатита С могут означать развитие хронической инфекции или инфекцию, перенесенную в прошлом.При первом анализе крови у некоторых больных может определяться положительный результат, который не подтверждается при более углублённом обследовании. Такая реакция может быть связана с другими причинами, а не с вирусом гепатита С. Для более точного диагноза определяется ДНК вируса гепатита С с использованием метода полимеразной цепной реакции (ПЦР). При необходимости, врач назначает УЗИили биопсию печени.
Дата добавления: 2018-05-09 ; просмотров: 109 ; ЗАКАЗАТЬ РАБОТУ
источник



