Гепатит В (ГВ, hepatitis В) – вирусная антропонозная инфекция с перкутанным механизмом заражения; характеризуется преимущественным поражением печени и протекает в различных клинико-патогенетических вариантах – от вирусоносительства до прогрессирующих форм с развитием острой печеночной недостаточности, цирроза печени и гепатомы.Этиология. Возбудитель – вирус гепатита В (ВГВ, НВv) – относится к нетаксономической группе Hepadnaviridae. Вирионы ВГВ («частицы Дейна») – сферические, диаметром 42 нм (до 45 нм), имеют наружную липопротеидную оболочку и нуклеокапсид, содержащий двунитчатую циркулярную ДНК, одна нить которой короче другой почти на 1/3 и ДНК-зависимую ДНК-полимеразу В структуре ВГВ выделяют ряд антигенных систем: 1) поверхностный («австралийский», surface) антиген, НВsАg, находящийся в составе липопротеидной оболочки ВГВ
2) сердцевидный (соrе), НВсАg, выявляется в составе нуклеокапсида вирионов, в ядрах и иногда в перинуклеарной зоне инфицированных гепатоцитов;3) НВеАg, связанный с НВсАg и представленный тремя подтипами, отражает активность ДНК-полимеразы ВГВ. 4) НВхАg, расположенный вблизи оболочки вириона.В поверхностных слоях оболочки ВГВ расположены рецепторы для человеческого полимеризированного альбумина.ВГВ отличается высокой устойчивостью к низким и высоким температурам, многим дезинфектантам. Вирус устойчив к длительному (18 ч) воздействию кислой среды (рН 2,3), сохраняет антигенную активность в течение 7 дней при воздействии 1,5 % раствора формалина, 24 ч при воздействии 2 % раствора фенола и 5 ч – эфира и хлороформа. Инактивируется при автоклавировании в течение 30 мин, при воздействии ?-пропиолактона.Эпидемиология. Вирусный гепатит В – антропонозная инфекция с перкутанным механизмом заражения.Основным резервуаром и источником ВГВ являются лица с субклинической формой инфекционного процесса, так называемые вирусоносители.
В распространении возбудителей весьма велика роль наркоманов, гомосексуалистов и проституток, большая часть которых инфицирована ВГВ. Источниками инфекции являются также больные острыми и хроническими формами ГВ.Ведущий механизм передачи ВГВ – перкутанный, который вследствие чрезвычайно малой инфицирующей дозы вируса (для заражения ВГВ достаточно 10 -7 мл инфицированной крови) реализуется преимущественно естественными путями – половым и вертикальным. Наряду с естественными путями ВГВ распространяется искусственными (артифициальными) путями – при гемотрансфузиях инфицированной крови, в ходе операций, при стоматологических, гинекологических, инструментальных лечебно-диагностических манипуляциях, разнообразных парентеральных процедурах, производимых недостаточно тщательно обеззараженными инструментами многоразового пользования (ятрогенная инфекция). Высокий риск заражения артифициальным путем имеется у наркоманов и у лиц, подвергающихся татуировкам и обрядовым процедурам.Наиболее часто заболевания регистрируются среди детей 1-го года жизни, как правило, с сопутствующей патологией или от ВГВ-инфицированных матерей, среди людей зрелого и пожилого возраста, обычно при наличии у них сопутствующих болезней. У реконвалесцентов острого ГВ развивается стойкий, возможно, пожизненный иммунитет
Вирус проникает в организм человека через повреждённые кожные покровы или слизистые оболочки, затем гематогенно диссеминирует в печень, где фиксируется на гепатоцитах благодаря поверхностным рецепторам, содержащим HBsAg. Экспрессия HBsAg происходит на мембране печёночных клеток. При этом возбудитель не оказывает прямого цитопатического действия на клетки печени.
Процесс репродукции в гепатоцитах обусловлен активностью ДНК-полимеразы, активно участвующей в «достройке» неполноценной цепочки вирусной ДНК за счёт антигенов гистосовместимости, общих для различных клеток организма хозяина. Дочерние популяции накапливаются в поверхностной мембране гепатоцитов. Цитолиз печёночных клеток происходит под действием цитотоксических иммунных механизмов. Мишенями для последних являются антигенные детерминанты вируса вирусного гепатита В, ассоциированные с антигенами главного комплекса гистосовместимости (HLA) на поверхности гепатоцитов.
Существенную роль в патогенезе вирусного гепатита В играют иммунные комплексы (HBsAg-антитела), оседающие на эндотелии сосудов различных органов и в лимфатических узлах, обусловливая внепечёночные поражения (например, гломерулонефрит и узелковый периартериит).
Аутоиммунные реакции возникают также в ответ на воздействие фрагментов гепатоцитов после их гибели. Это ведёт не только к элиминации указанных фрагментов, но и к повреждению здоровых печёночных клеток.
Морфологические изменения характеризуются дистрофическими и некробиотическими процессами в центролобулярных и перипортальных зонах печёночной дольки с последующим развитием фиброза. Одновременно в процесс вовлекаются внутрипечёночные жёлчные ходы, что ведёт к формированию холестаза.
Дата добавления: 2014-12-09 ; просмотров: 5845 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
источник
НВV не обладает прямым цитопатическим действием. Повреждение печени при ГВ иммуноопосредовано, обусловлено силой и характером иммунного ответа на экспрессию антигенов HBV на печеночно-клеточных мембранах и определяется степенью инфекционности, вирулентности, генотипом и дозой вирусов, активностью системы интерферона, иммуногенетическими свойствами инфицированного человека.
В генезе цитолиза наряду с саногенными иммунными процессами существенная роль отводится иммунопатологическим реакциям, индуцированным антигенами вирусов, локализованными в мембранах гепатоцитов, и фиксацией на них антител и комплемента. Происходят усиление перекисного окисления липндов клеточных мембран с повышением их проницаемости, выход лизосомальных гидролаз в цитоплазму гепатоцитов, нарушение структуры и повреждение митохондрий, увеличение внутриклеточного содержания ионов натрия и кальция, а также другие процессы, определяющие нарушение внутриклеточного метаболизма и повреждение печеночных клеток
Развитие острой циклической формы гепатита В отражает нормальную иммунную реакцию организма в ответ на внедрение возбудителя. Цитолиз гепатоцитов иммунокомпетентны-ми клетками (лимфоцитами-киллерами, сенсибилизированными к экспрессированным на гепатоцитарных мембранах антигенным детерминантам HBV), А-клетками и др. приводит к повторной гематогенной диссеминации вирусов, нарастанию иммунного ответа, сенсибилизации В-лимфоцитов, продукции антител и при циклическом течении процесса к элиминации возбудителей.
Исчезновение вируса из организма—результат разрушения всех инфицированных клеток и подавления различных фаз репликации вируса вырабатываемым интерфероном. Реакция гуморального звена иммунитета проявляется накоплением специфических антител к антигенам вируса ГВ. В острую фазу болезни в крови обнаруживают анти-HBc-IgM, затем анти-ABc-IgG, позже — анти-НВе и последними, обычно через несколько месяцев после клинического выздоровления — анти-HBs. Образующиеся иммунные комплексы, включающие антигены, антитела и С3-компонент комплемента, фагоцитируются макрофагами и выделяются из организма.
Вместе с тем, циркулирующие иммунные комплексы могут участвовать в иммунопатологических реакциях. В большинстве случаев — 80-85% НВV-инфекция завершается выздоровлением.
Молниеносные, злокачественные формы гепатита В в значительной степени обусловлены генетически детерминированной гиперергической реакцией иммуноцитов на достаточно чужеродные в антигенном отношении вирусы при низком интерфероновом ответе.
Вместе с тем, низкая патогенность и антигенная чужеродность вирусов, неэффективность клеточного и гуморального иммунитета, дефектность интерфероновой системы обеспечивают персистенцию вируса, развитие HBV-носительства и хронического гепатита.
Механизмы хронизации и прогрессирования гепатита В могут быть представлены недостаточным (неадекватным) иммунным ответом в сочетании с высокой репликативной активностью вируса или низкой репликативной активностью вируса с интеграцией генетического аппарата НВV в геном гепатоцита, мутацией вирусов, снижением продукции интерферона, аутоиммунными механизмами, внепеченочной репликацией вируса, иммуногенетической предрасположенностью индивидуума.
Аутоиммунные механизмы обусловлены интерференцией вирусспецифических белков возбудителя и структурных субъединиц печеночных клеток.
Генетическая предрасположенность к HBV нашла подтверждение в эпидемиологических характеристиках инфекции у представителей разных рас. Hbs-антигенемия максимально распространена среди эскимосов Аляски, в странах Центральной Африки, Юго-Восточной Азии, Латинской Америки, Австралии, Океании, где преобладают лица со слабым иммунным ответом. Эти регионы отличаются наиболее высокой заболеваемостью гепатоцеллюлярной карциномой. Вместе с тем, частота острых манифестных форм в гиперэндемичных регионах небольшая.
В странах Европы и Северной Америки преобладание лиц с адекватной силой иммунного ответа определяет большую частоту острой манифестной инфекции с выздоровлением.
Наблюдающиеся при прогрессирующих формах острого и хронического ГВ острая токсическая дистрофия, массивный и субмассивный некроз печени приводят к развитию острой печеночной недостаточности (ОПН), сопровождающейся накоплением в крови токсичных метаболитов (аминокислоты, ароматические соединения, фальш-медиаторы, свободный билирубин, бактериальные токсины, продукты распада клеток и др.) — так называемая метаболическая буря, с поражением ЦНС в виде неврологических и психических расстройств.
источник
ВИРУСНЫЕ ГЕПАТИТЫ
Термином «гепатит» обозначают воспалительные заболевания печени различной этиологии.
Функции печени:
Пищеварительная.
Клетки печени вырабатывают желчь, поступающую в 12-перстную кишку. Желчь эмульгирует жиры, способствует их расщеплению и усвоению.
Клетки печени нейтрализуют множество ядовитых веществ, поступающих с кровью и лимфой (как экзогенных, так и эндогенных), также микроорганизмы (вирусы, бактерии), погибшие в результате работы иммунной системы, утилизируются печенью. Печень обезвреживает и множество живых микроорганизмов, не допуская их размножения.
Депонирующая
Печень является своеобразным «депо» для запасов крови и гликогена и, при возникновении дефицита крови или глюкозы, сразу компенсирует их недостаток.
Синтезирующая.
Помимо синтеза гликогена и глюкозы, печень синтезирует белки плазмы (глобулины и альбумин).
При гепатите все эти функции нарушаются.
Особенное значение поражение печени имеет в детском возрасте, поскольку печень у детей функционально незрелая, её антитоксическая и внешнесекреторные функции несовершенны. Поэтому слабость барьерной функции часто служит причиной развития токсикозов, а малое количество желчи ограничивает усвоение жиров.
Этиология и эпидемиология.
Возбудитель – вирус семейства Picornaviridae, содержит однонитевую РНК, не имеет оболочки.
Устойчив во внешней среде
Сохраняется в течение нескольких часов при температуре 60°C
Сохраняет жизнеспособность под воздействием формальдегида при температуре 37°C в течение 72-х часов
Чувствителен к ультрафиолетовым лучам и активированному хлору
Распространение вируса:
Источник инфекции – больной или вирусоноситель
Механизм передачи – фекально-оральный
Факторы передачи:
Пища (термически не обработанная)
Особая опасность – употребление в пищу устриц
Семейство не определено. Содержит однонитевую РНК, не имеет оболочки.
Свойства схожи со свойствами вируса гепатита А
Распространение вируса и факторы передачи – см. гепатит А
Особое значение имеет водный путь передачи (естественные источники воды)
Семейство Hepadnaviridae. Содержит двунитевую ДНК, имеет оболочку.
Устойчивость
Высокая устойчивость во внешней среде
При комнатной температуре сохраняет жизнеспособность в течение 3-6 месяцев
В холодильнике – 6-12 месяцев
В замороженном виде – до 20 лет
В высушенном состоянии – до 25 лет
Устойчив к воздействию химических веществ: хлорамин, формалин
Чувствительность
При автоклавировании (120°C) – активность вируса подавляется через 5 минут
При воздействии сухого жара (160°C) – активность подавляется через 2 часа
При кипячении (100°C) – инактивация через 2-10 минут
Вирус разрушается в щелочной среде, для него губительно действие перекиси водорода.
Особенности вируса гепатита В
В состав вируса входят три антигена, имеющие большое значение для лабораторной диагностики:
НВсAg (ядерный сердцевидный антиген белковой природы)
НВеAg (трансформированный НВсAg — или антиген инфекционности)
НВsAg (поверхностный австралийский антиген, расположенный на оболочке вируса)
Распространение вируса:
Резервуаром и источником инфекции являются лица с манифестными или атипичными формами болезни.
Механизм передачи – гемоконтактный.
Пути передачи:
Через молоко больной матери
Факторы передачи:
Незащищённый половой контакт
Медицинские инструменты (шприцы, иглы и др.)
Семейство Flaviviridae, содержит однонитевую РНК, имеет оболочку
Свойства вируса:
Относительно неустойчив во внешней среде.
При температуре 60°C сохраняет жизнеспособность в течение 10-ти часов
При кипячении инактивируется в течение 2-х минут
Чувствителен к хлороформу и формалину
Распространение вируса:
Резервуаром и источником инфекции является больной острой или хронической формой гепатита
Механизм передачи – гемоконтактный
Пути передачи:
Через молоко больной матери
Факторы передачи:
Незащищённый половой контакт
И другие факторы (см. гепатит В)
Семейство Togaviridae, род Deltavirus.Содержит РНК, имеет оболочку.
Свойства вируса:
Устойчив к нагреванию, действию кислот, ультрафиолетовому облучению.
Инактивируется щелочами и протеазами.
Репликация вируса происходит только в присутствии вируса гепатита В
Внешней оболочкой вируса является HBsAg вируса гепатита В (вирус-паразит)
Распространение вируса:
Резервуаром и источником инфекции являются больные острой и хронической D-инфекцией и здоровые носители.
Механизм передачи – гемоконтактный
Пути передачи – такие же, как у гепатита В
К вирусу очень восприимчивы дети раннего возраста.
Семейство Flaviviridae (условно), содержит однонитевую РНК, имеет оболочку.
Чувствительность и устойчивость вируса слабо изучены.
По свойствам близок к вирусу гепатита С, но для него не храрактерно прогрессирование инфекционного процесса с последубщим развитием цирроза и рака печени.
Механизм и пути передачи такие же как у гепатита С.
Патогенез вирусных гепатитов
Вирусный гепатит А
Входные ворота – слизистые оболочки ротоглотки и тонкой кишки
Основные звенья патогенеза:
Накопление вируса в эпителиальных клетках ЖКТ
Проникновение в лимфоидные образования входных ворот (кольцо Пирогова, мезентериальные лимфатические узлы кишечника)
Первичная презентация вируса иммунокомпетентным клеткам
Проникновение вируса в кровь (первичная вирусемия)
Накопление вируса в гепатоцитах
Репликация вируса в гепатоцитах, высвобождение вируса в желчь без разрушения клеток
Вторичное попадание вируса в кровоток (вторичная вирусемия)
Взаимодействие АГ вируса с иммунокомпетентными клетками в месте входных ворот
Развитие реакции гиперчувствительности замедленного типа
Клинически это проявляется катаральными изменениями в ротоглотке и слизистой оболочке ЖКТ, температурной реакцией, диспепсическими расстройствами и знаменует окончание инкубационного периода.
Вирус не оказывает прямого цитотоксического действия. Разрушение гепатоцита происходит в результате развития Т-клеточного иммунного ответа.
После разрушения 70% (и более) гепатоцитов развивается гипербилирубинемия, что соответствует появлению желтухи.
Антигены к гепатиту А (IgM) появляются в крови уже в конце инкубационного периода, в результате вирус быстро исчезает из крови.
Исчезновение вируса из сыворотки крови и появление антигенов соответствует завершению преджелтушного периода и разгару заболевания.
Вирусный гепатит Е
Патогенез аналогичен патогенезу вирусного гепатита А
Вирусный гепатит В
Входные ворота – повреждённые кожные покровы и слизистые оболочки, а также – сосуды при инъекциях.
Основные звенья патогенеза:
Проникновение вируса в печень с кровотоком
Фиксация вируса на гепатоцитах
Проникновение вируса в клетку
Высвобождение вирусной ДНК
Проникновение ДНК в ядро гепатоцита
Начало синтеза нуклеиновых кислот и «сборка» вируса
Репликация вируса в гепатоцитах (возможна репликация в клетках костного мозга, макрофагах и Т-хелперах)
Дочерние популяции вируса накапливаются на поверхности гепатоцита
Разрушение гепатоцитов, содержащих вирус, происходит за счёт трёх механизмов:
Воздействие иммунокомпетентных клеток — Т-цитотоксические клетки, естественные киллеры и макрофаги.
Действие лизосомальных ферментов, разрушающих мембрану клетки.
Действие противопечёночных гуморальных аутоантител
источник
Вирусный гепатит А-острая циклическая инфекция, характеризующаяся четкой сменой периодов.После заражения ВГА из кишечника проникает в кровь и далее в печень, где после фиксации к рецепторам гепатоцитов проникает внутрь клеток. На стадии первичной репликации отчетливых повреждений гепатоцитов не обнаруживается. Новые поколения вируса выделяются в желчные канальцы, далее поступают в кишечник и выделяются с фекалиями во внешнюю среду. Часть вирусных частиц проникает в кровь, обусловливая развитие интоксикационной симптоматики продромального периода. Повреждения гепатоцитов, возникающие в ходе дальнейшего течения ГА, обусловлены не репликацией вируса, а иммуноопосредованным цитолизом. В периоде разгара ГА морфологическое исследование позволяет выявить воспалительные и некробиотические процессы, происходящие преимущественно в перипортальной зоне печеночных долек и портальных трактах. Эти процессы лежат в основе развития трех основных клинико-биохимических синдромов: цитолитического, мезенхимально-воспалительного и холестатического. К лабораторным признакам цитолитического синдрома относятся: повышение активности ферментов АлАТ и АсАТ (аланинамино- и аспартатаминотрансферазы), уровня железа в сыворотке крови, снижение синтеза альбумина, протромбина и других факторов свертывания крови, эфиров холестерина. Начальным этапом цитолитического синдрома является повышение проницаемости мембраны гепатоцитов. Это обусловливает выход в кровь, прежде всего АлАТ — фермента, находящегося в цитоплазме печеночной клетки. Повышение активности АлАТ — ранний и надежный индикатор повреждения гепатоцита. Мезенхимально-воспалительный синдром характеризуется повышением уровня бета- и гаммаглобулинов, изменением коллоидных проб (снижение сулемового титра и повышение тимоловой пробы). Холестатический синдром проявляется повышением в крови уровня связанного билирубина, желчных кислот, холестерина, меди, активности щелочной фосфатазы, а также билирубинурией, уменьшением (исчезновением) уробилиновых тел в моче. Вследствие комплексных иммунных механизмов (усиление интерферонопродукции, активизации естественных киллеров, антителопродукции и активности антителозависимых киллеров) репликация вируса прекращается, и происходит его элиминация из организма человека. Для ГА не характерны ни длительное присутствие вируса в организме, ни развитие хронической формы болезни. Однако иногда течение заболевания может быть модифицировано в случаях ко-инфекции или суперинфекции другими гепатотропными вирусами. У лиц же с генетической предрасположенностью возможно развитие хронического активного аутоиммунного гепатита 1-го типа
Вирусный гепатит В Из места внедрения ВГВ гематогенно достигает печени, где в гепатоцитах происходит репликация вирионов. ВГВ не обладает цитотоксичностью. Сам вирус гепатита В проникнув в клетку, оставляет свой антиген на поверхности гепатоцита. Эти клетки опознаются Т-лимфоцитами как чужеродные и подвергаются агрессии. Таким образом, поражение клеток печени при гепатите В является иммуннообусловленными. Кроме этого при хроническом гепатите В в процесс вовлекаются Т-супрессоры. Они находятся в подавленном состоянии и поэтому формируются условия для развития аутоиммунных реакций, направленных против собственных клеточных антигенов.Следствием этого является развитие некробиотических и воспалительных изменений в паренхиме печени. В результате патологических изменений в печеночной ткани возникают цитолитический, мезенхимально-воспалительный и холестатический синдромы с определенными клиническими и лабораторными проявлениями .
При морфологическом исследовании обнаруживают дистрофические изменения гепатоцитов, зональные некрозы, активизацию и пролиферацию звездчатых эндотелиоцитов (клеток Купфера); в более тяжелых случаях — субмассивные и массивные некрозы печени, которые, как и распространенные «мостовидные» и мультилобулярные некрозы, являются нередко патологоанатомическим субстратом печеночной комы. Холестатические варианты ГВ сопровождаются вовлечением в патологический процесс внутрипеченочных желчных ходов с образованием в них «желчных тромбов», увеличением содержания билирубина в гепатоцитах.
В патогенезе ГВ, кроме репликативной, выделяют также интегративную форму течения инфекции. При этом происходит встраивание всего генома вируса в геном клетки хозяина или его фрагмента, отвечающего, например, за синтез HBsAg. Последнее приводит к присутствию в крови лишь HBsAg.Интеграция генома ВГВ в геном гепатоцита является одним из механизмов, обусловливающих развитие персистирующих (ациклических) форм течения ГВ и первичной гепатоцеллюлярной карциномы.
Вирусный гепатит С После проникновения в организм человека ВГС, обладая гепатотропностью, реплицируется преимущественно в гепатоцитах. ВГС обладает слабой иммуногенностью, что определяет замедленный, неинтенсивный Т-клеточный и гуморальный ответ иммунной системы на инфекцию. Так, в острой стадии ГС сероконверсия возникает на 1-2 мес. позже появления признаков цитолиза гепатоцитов (повышения активности АлАТ). Лишь через 2-10 нед. от начала заболевания в крови больных начинают определяться антитела к ядерному антигену классов M, затем G. Однако они обладают слабым вируснейтрализующим действием. Антитела же к неструктурным белкам ВГС в острой фазе инфекции обычно не выявляются. Зато в крови в течение острой стадии болезни (и при реактивации — в хронической) определяется присутствие РНК вируса. Устойчивость ВГС к специфическим факторам иммунитета обусловлена его высокой способностью к «ускользанию» из-под иммунологического надзора. Таким образом, слабость иммунного реагирования и мутационная изменчивость вируса во многом обусловливают высокий хрониогенный потенциал данного заболевания.
Вирусный гепатит D Этот вирус является дефектным, так как он на своей поверхности не имеет рецепторов для гепатоцитов. Поэтому он не может проникнуть в клетку и реплицироваться в ней. Для репродукции данного вируса необходимо участие «вируса-помощника». Роль этого помощника играет вирус гепатита В. таким образом, заболевание может возникнуть при одновременном заражении обоими вирусами или при инфицировании лиц уже имеющих вирус гепатита В (суперинфекция). Сочетанное действие обоих вирусов приводит к развитию более тяжелых форм заболевания с выраженными явлениями печеночно-клеточной недостаточности. В большинстве случаев заболевание приобретает прогрессирующее течение с быстрым переходом в цирроз печени и смертью.
Вирусный гепатит Е изучен недостаточно. Большинство исследователей полагают, что центральным звеном патогенеза является цитопатическое действие вируса. Не исключается и участие иммунных механизмов в некробиотических изменениях печеночной ткани.
источник
Вирусный гепатит В. Этиология, патогенез, эпидемиологические особенности и клиника. Маркерная диагностика, принципы лечения и профилактики
Вирусный гепатит В (ВГВ) – антропонозная вирусная инфекционная болезнь, передающаяся преимущественно парентеральным и половым путями, характеризующаяся развитием циклически протекающего паренхиматозного гепатита.
Этиология: вирус гепатита В (ВГВ, HBV) — ДНК-овый гепаднавирус; содержит ряд АГ: поверхностный АГ на наружной липопротеиновой оболочке (HBsAg, «австралийский» АГ), сердцевинный АГ (HBcAg, коровский АГ) и АГ инфекциозности (HBeAg) на наружной части ядра; каждый из АГ вызывает гуморальный иммунный ответ, проявляющийся выработкой соответствующих АТ (анти-HBs, анти-НВс, анти-НВе).
Эпидемиология: единственный источник – человек (больные всеми формами острого и хронического ГВ и носители), основные пути передачи: парентеральный (при гемотрансфузии, гемодиализе, в/в наркомании), половой (при половых контактах с инфицированным человеком), контактно-бытовой (через предметы, загрязненные кровью – бритвы, ножницы, зубные щетки), вертикальный (от матери к ребенку через плаценту) и интранатальный (при прохождении ребенка через родовые пути инфицированной матери)
Патогенез: попадание вируса в кровь —> инфицирование гепатоцитов —> репликация ВГВ в гепатоцитах с развитием острого или хронического ВГВ или интеграция вируса в геном клетки с развитием вирусоносительства —> сборка в цитоплазме гепатоцита вирусной частицы после репликации ВГВ —> презентация АГ или полного вируса на поверхности мембраны гепатоцитов —> распознавание ВГВ NK-клетками, Т-киллерами и др. —> атака клетками иммунной системы инфицированных гепатоцитов —> цитолиз —> высвобождение АГ ВГВ (HBc, HBe, HBs) —> образование против АГ ВГВ АТ (анти-НВс, анти-НВе, анти-HBs) —> взаимодействие АГ и АТ с образованием иммунных комплексов, их циркуляцией в крови и отложением на мембранах неинфицированных гепатоцитов и др. клеток —> иммуноопосредованный цитолиз гепатоцитов, развитие аутоиммунных поражений (кожных высыпаний, артралгий, гломерулонефрита и др.); при адекватной ИС развивается острый ВГВ с циклическим течением процесса, заканчивающегося выздоровлением, при слабой реакции ИС болезнь протекает легко, но полной элиминации вируса не происходит и создаются условия для хронизации процесса, при гиперергической реакции ИС поражаются не только инфицированные клетки, но и клетки с фиксированными на них ИК, что может обусловить обширный некроз печени и фульминантную печеночную недостаточность.
1. инкубационный период в среднем 60-120 дней (от 42 до 180 дней)
2. преджелтушный период (7-14 дней):
— умеренные симптомы интоксикации (общее недомогание, слабость, разбитость, утомляемость, головная боль к вечеру, нарушение сна) без значительного повышения температуры тела
— умеренно выраженные диспепсические явления (ухудшение аппетита, горечь во рту, снижение вкусовых ощущений, тошнота, иногда рвота, тяжесть и тупые боли в эпигастральной области и правом подреберье)
— у четверти больных – артралгии в крупных суставах (чаще ночью), уртикарные высыпания и зуд кожи
3. желтушный период (3-4 нед):
— нарастание явлений интоксикации
— нарастание диспепсических явлений (обложенность и отечность языка, горечь во рту, тошнота, реже рвота, снижение аппетита вплоть до анорексии, болезненность в правом подреберье более выраженная и продолжительная, иногда вплоть до резких болей)
— постепенное нарастание желтухи с максимумом на 2-3-й неделе; желтуха интенсивная, на высоте сопровождается ахоличным калом, темной мочой
— печень всегда увеличена, консистенция несколько уплотнена, при пальпации гладкая; у трети больных отмечается увеличение селезенки
— могут быть проявления геморрагического синдрома (петехиальная сыпь на коже, носовые кровотечения, кровоизлияния в местах инъекций, «дегтеобразный» стул, рвота с примесью крови)
— в ОАК лейкопения с лимфо- и моноцитозом, сниженное до 2-4 мм/ч СОЭ
— в БАК стойкая и выраженная гипербилирубинемия (особенно на 2-3-й неделе желтушного периода), повышение активности АлАТ и АсАТ, снижение ПТИ
— при серологическом исследовании крови обнаруживаются HBsAg, анти-НВс IgM
— при тяжелом течении постепенно нарастают признаки печеночной недостаточности
4. период реконвалесценции (от 3-4 нед до 6 мес) – сопровождается появлением аппетита, уменьшением желтухи, окрашиванием кала и посветлением мочи, могут сохраняться астенизация, гепатомегалия, гипербилирубинемия, гиперферментемия (при легкой форме аминотрансферазы нормализуются к 30-35 дню, при среднетяжелой – к 40-50 дню, при тяжелой – к 60-65 дню)
1) данные эпидемиологического анамнеза (гемотрансфузии, хирургические вмешательства и др.) и особенности клинической картины (постепенное начало, длительный преджелтушный период, аллергические высыпания на коже, отсутствие улучшения самочувствия или его ухудшение с появлением желтухи, длительный желтушный период с медленным исчезновением симптомов заболевания в периоде реконвалесценции)
2) серологические реакции: наиболее ранний маркер ВГВ, появляющийся в крови в инкубационном периоде, HBsAg, также рано обнаруживают ДНК HBV (указывает на вирусемию), HBeAg, анти-НВс IgM; при благоприятном течении быстро исчезает вначале HBeAg с появлением анти-НВе, затем HBsAg с появлением анти-HBs, вместо ранних анти-НВс IgM появляются поздние анти-НВс IgG (могут циркулировать в крови годами, часто являясь единственным маркером перенесенного ГВ, т.к. antiHBs при остром ВГВ не развиваются у 15% реконвалесцентов, а в течение 6 лет после заболевания могут исчезать у 20% переболевших).
Длительная циркуляция (более 3 мес) HBeAg, ДНК HBV, а также анти-НВс IgM и HBsAg в стабильно высоком титре свидетельствуют о затяжном течении инфекционного процесса и высокой вероятности хронизации; о развитии хронического ВГВ следует также думать при выявлении HBsAg в стабильном титре на протяжении 6 мес. и более от начала заболевания даже при отсутствии маркеров активной вирусной репликации (HBeAg, ДНК HBV, анти-НВс IgM), клинической симптоматики и при нормальных биохимических показателях, в этом случае для уточнения диагноза показана пункционная биопсия печени
При адекватном ответе на вакцинацию против ВГВ в крови обнаруживают анти-HBs на уровне 10 mIU/мл и выше в сочетании с отсутствием анти-НВс.
Анти-НВс IgG могут циркулировать в крови годами, часто являясь единственным маркером перенесенного ГВ, т.к. серологическое исследование может попасть в фазу «серонегативного окна», когда HBsAg уже отсутствует, a antiHBs еще не появились, кроме того)
1. При легких и среднетяжелых формах – полупостельный режим, при тяжелых – постельный; диета № 5, пища механически и химически щадящая, без экстрактивных веществ, подается в теплом виде
2. Строгое соблюдение гигиены полости рта и кожи, при зуде — протирание кожи р-ром пищевого уксуса (1:2), 1% р-ром ментолового спирта, горячий душ на ночь
3. Дезинтоксикационная терапия: в/в капельные инфузии 0,5-1,5 л 5% р-ра глюкозы, полиионных р-ров, гемодеза, реополиглюкина, форсированный диурез под контролем суточного баланса жидкости
4. Противовирусные и иммуномодулирующие ЛС показаны только при тяжелом течении ВГВ с наличием маркеров активной вирусной репликации, угрозой развития острой печеночной недостаточности или хронизации:
— рекомбинантный (ИФН альфа / реаферон, ИФН альфа – 2a / роферон А, ИФН альфа – 2b / интрон) и нативный (вэллферон, человеческий лейкоцитарный ИФН) a-ИФН, пегилированные ИФН (Пег-ИФН а2а / пегасис и Пег-ИФН а2b / Пег-интрон), индукторы ИФН (циклоферон / неовир, амиксин)
— синтетические нуклеозиды (фамцикловир, ламивудин / эпивир, зидовудин / ретровир)
— ингибиторы протеазы (саквинавир/ инвираза, индинавир)
— иммуномодуляторы (лейкинферон, ИЛ-1 / беталейкин, ИЛ-2 / ронколейкин)
5. При выраженном холестазе — энтеросорбенты (полифепан, билигнин, угольные гранулированные сорбенты), экстракорпоральная детоксикация (гемосорбция, плазмаферез, плазмосорбция и др.), при налии длительной постгепатитной гипербилирубинемии – фенобарбитал.
6. Ферментые препараты (панкреатин, креон, мезим форте, фестал, панзинорм, юниэнзайм) для усиления пищеварительной функции желудка и поджелудочной железы; при запорах – слабительные растительного просхождения, магния сульфат внутрь.
7. Гепатопротекторы в течение 1-3 мес: производные силимарина (легален, карсил, силимар), препараты из экстрактов растений (гепалив, гепатофальк, гепабене), эссенциале.
8. Лечение признаков печеночной недостаточности и печеночной энцефалопатии (см. вопрос 191)
Профилактика ВГВ: изоляция источников ВГВ (выявление носителей HBs-АГ, контроль за донорами крови и др.), прерывание путей передачи возбудителя (использование одноразовых шприцев, игл, систем инфузий, соблюдение правил стерилизации инструментария), пропаганда здорового образа жизни (половая гигиена, борьба с наркоманией), ограничение показаний для гемотрансфузий, плановая вакцинация контингентов риска (вакцины Энджерикс В, Н-В-ВАКС II и др.)
ВГС — заболевание, вызываемое ВГС – РНК-овым флавивирусом, сходное по эпидемиологическим и клиническим признакам с ВГВ, однако протекающее более легко и отличающееся при желтушных формах сравнительно быстрым обратным развитием болезни
Отличительные особенности ВГС:
— преимущественно парентеральный путь передачи (гепатит наркоманов), реже – другие пути (контактно-бытовой, половой, вертикальный)
— вирус ГС обладает прямым цитопатическим действием; биологические свойства вируса доминируют над иммунным ответом, что предрасполагает к хронизации процесса
— клинически чаще встречаются безжелтушные, субклинические и инаппарантные формы острого ВГС, которые переносятся без стационарного лечения и остаются нераспознанными, однако в 80-90% случаев переходят в хронический гепатит и у 20-30% больных — в цирроз печени
— серологически характерно обнаружение в крови РНК HCV (методом ПЦР), несколько реже – анти-HCV IgM и IgG
— при лечении острого ВГС во всех случаях необходима этиотропная противовирусная терапия
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Для студента самое главное не сдать экзамен, а вовремя вспомнить про него. 9746 — 

195.133.146.119 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
источник
Что такое гепатит Б? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александров П. А., инфекциониста со стажем в 11 лет.
Вирусный гепатит В (Б) — острое и хроническое инфекционное заболевание, вызываемое вирусом гепатита В, с гемоконтактным механизмом передачи (через кровь), протекающее в различных клинико-морфологических вариантах, и возможным развитием цирроза печени и гепатоцеллюлярной карциномы. Всего в мире, по самым скромных оценкам, инфицировано более 250 млн человек.
вид — вирус гепатита В (частица Дейна)
Развитие вируса происходит в гепатоцитах (железистых клетках печени). Он способен к интеграции в ДНК человека. Имеются 9 генотипов вируса с различными подтипами — генетическая изменчивость позволяет вирусу образовывать мутантные формы и ускользать от действия лекарств.
Имеет ряд собственных антигенов:
- поверхностный HbsAg (австралийский). Появляется за 15-30 дней до развития болезни, свидетельствует об инфицировании (не всегда). Антитела к HbsAg выявляются через 2-5 месяцев от начала заболевания, а сам HbsAg исчезает из крови (при благоприятном течении процесса);
- сердцевинный HbcorAg (ядерный, коровский). Появляется в инкубационном периоде и совместно с ним появляются антитела (HbcorAb). Длительное присутствие HbcorAg в крови свидетельствует о вероятной хронизации процесса (неадекватный иммунный ответ);
- антиген инфекциозности и активного размножения вируса (HbeAg). Появляется совместно с HbsAg и отражает степень инфицированности. Его продолжительная циркуляция в крови является свидетельством развития хронизации процесса, а антитела к нему являются благоприятным прогностическим признаком (не всегда, но по меньшей мере указывают на возможность более благоприятного процесса, срок их циркуляции после выздоровления окончательно не определён, но не более пяти лет после благоприятного разрешения процесса);
- HbxAg — регулятор транскрипции, способствует развитию гепатокарциномы.
Вирус гепатита В чрезвычайно устойчив к действию всевозможных естественных факторов окружающей среды, инактивируется при 60 °C за 10 часов, при 100 °C за 10 минут, при оптимальной температуре сохраняется до 6 месяцев, при автоклавировании погибает за 5 минут, в сухожаровом шкафу — через 2 часа, 2% раствор хлорамина убивает вирус за 2 часа. [1] [3]
Источник инфекции — только человек, больной острой или хронической формой инфекции.
Механизм передачи: гемоконтактный и вертикальный (от матери к ребёнку), не исключается трансмиссивный механизм передачи (например, при укусах комаров в результате раздавливания и втирания инфицированного тела комара в поврежденную ткань человека).
Пути передачи: половой, контактно-бытовой, гемотрансфузионный (например, при переливании крови или медицинских манипуляциях). Восприимчивость всеобщая. Заболеваемость — 30-100 человек на 100 тысяч населения (зависит от страны). Летальность от острых форм — до 2%. После перенесённого острого заболевания при условии выздоровления иммунитет стойкий, пожизненный.
Для заражения характерна малая заражающая доза (невидимые следы крови). [1] [2]
Инкубационный период — от 42 до 180 дней (следует иметь в виду, что наличие клинической симптоматики характеризует лишь незначительную долю всех случаев заболевания).
Начало постепенное. Характерные синдромы:
- общей инфекционной интоксикации (проявляется как астеноневротический синдром);
- холестатический (нарушение секреции желчи);
- артрита;
- нарушения пигментного обмена (появление желтухи при уровне общего билирубина свыше 40 ммоль/л);
- геморрагический (кровоточивость кровеносных сосудов);
- экзантемы;
- отёчно-асцитический (скопление жидкости в брюшной полости);
- гепатолиенальный (увеличение печени и селезёнки).
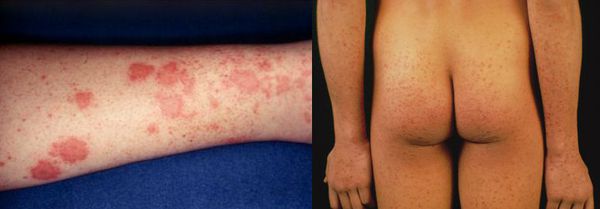
Начальный (преджелтушный) период продолжается 7-14 дней. Чаще протекает по многообразному типу с болевыми ощущениями в различных суставах по ночам и утром, уртикарными высыпаниями, астеновегетативными проявлениями (снижение аппетита, апатия, нервозность, слабость, разбитость, повышенная утомляемость). Изредка развивается синдром Джанотти-Крости — симметричная, яркая пятнисто-папулёзная сыпь. Не исключены умеренные диспептические явления (расстройства пищеварения). К концу периода происходит потемнение мочи, обесцвечивание кала.
Желтушный период продолжительностью около одного месяца характеризуется возникновением желтушного окрашивания кожи (различных оттенков) на фоне продолжающегося или ухудшающегося общего состояния. Характерна длительность и стойкость симптоматики. Появляется тяжесть и болезненность в правом подреберье, горечь во рту, тошнота, выражённый зуд кожи (практически не снимаемый никакими средствами). На фоне усиления астеноневротического компонента появляются геморрагические проявления, урежение пульса, гипотензия, отёки (отражает степень интоксикации и нарушения функций печени).
Следующим этапом в развитии болезни является нормализации общего состояния, спадение желтухи и реконвалесценция, которая в зависимости от конкретной ситуации и состояния иммунной системы может закончиться как выздоровлением, так и движением развития заболевания в хроническое течение, характеризующееся маловыраженой неусточивой симптоматикой, преимущественно в виде слабости, периодического дискомфорта в правом подреберье, бурно сигнализирующим лишь на стадии цирроза и полиорганных осложнений.
- гепатиты другой этиологии;
- желтухи другой этиологии (например, гемолитическая болезнь, токсическое поражение, опухоли);
- малярия;
- инфекционный мононуклеоз;
- лептоспироз;
- ревматоидный артрит.
В первое десятилетие 21 века произошло возникновение концепции «оккультной» (стёртой) ВГВ-инфекции (далее ОкВГВ), характеризующейся наличием вируса при недетектируемом уровне HbsAg. Механизм данного состояния связывают с мутацией в регионе домена полимеразы, что ведёт к уменьшению вирусной репликации и отсутствию экспрессии HbsАg, также вероятны дефекты гена Pol, что является следствием противовирусной терапии (Рахманова А.Г. и соавторы, 2015). При этом единственными серологическими маркером ВГВ могут быть HBcor антитела (чаще в сочетании с HbeAb), в особенности тогда, когда недоступны высокочувствительные и затратные методы определения HBV ДНК (Цинзерлинг В.А., Лобзин Ю.В., Карев В.Е., 2012). Это обуславливает сохраняющийся риск инфицирования пулов плазмы ВГВ при донорстве крови и трансплантации органов, внутрибольничного инфицирования в роддомах, хирургических стационарах, стоматологии.
Острый гепатит характеризуется более тяжёлым течением у беременной, возникновении повышенного риска преждевременных родов, аномалий развития плода на ранних сроках и кровотечений. Вероятность передачи при острой форме зависит от сроков беременности: в первом триместре риск 10% (но более тяжёлые проявления), в третьем триместре — до 75% (чаще бессимптомное течение после родов). У большинства детей при заражении во внутриутробном и постнатальном периодах происходит хронизация инфекции. [1] [3] [6]
Входные ворота — мельчайшие повреждения кожи и слизистых оболочек.
С движением кровяной массы вирус попадает в печеночную ткань, где локализуется в гепатоцитах и теряет свою протеиновую сферу в лизосомах. Происходит выход вирусной ДНК с последующим ресинтезом аномальных протеинов LSP, а параллельно образование новых частиц Дейна.
В процессе эволюции вирусчеловеческого взаимодействия возможно развитие двух вариантов:
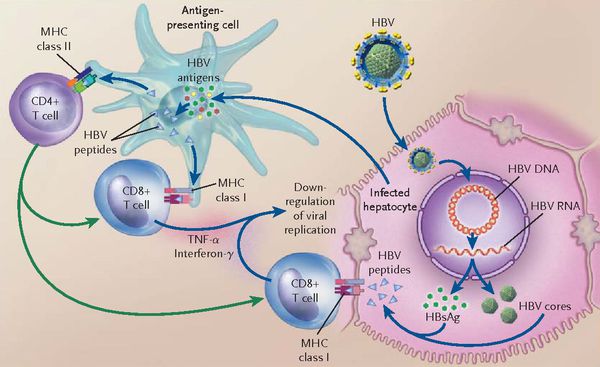
При репликативном пути происходит следующее: белки LSP совместно с HbcorAg вызывают увеличение продукции гамма-интерферона, что приводит к активации главного комплекса гисотсовместимости (HLA), проистекает преобразование молекул гистосовместимости 1 и 2 классов, в результате чего клетка становиться для организма враждебной в антигенном формате.
Антигенпрезентирующие макрофаги содействуют изменению В-лимфоцитов в плазматические клетки и экспрессии ими агрессивных белков-антител к посторонним антигенам. В итоге на поверхности печёночных клеток формируются вирусспецифические иммунные комплексы (антиген + антитело + фракция комплемента С3в).
В динамике может реализоваться два сценария:
- в первом варианте запуск каскада комплимента ведёт к появлению в составе иммунных комплексов агрессивной фракции С9 (мембранатакующий комплекс) — наблюдается значительный некроз гепатоцитов без участия лимфоцитов (молниеносная форма гепатита В);
- при альтернативной варианте (наблюдающимся в большинстве случаев) каскад комплемента в силу иммуноиндивидуалистических свойств не активируется — тогда идёт умеренное разрушение Т-киллерами меченых антителами заражённых вирусом гепатоцитов. Образуются ступенчатые некрозы с образованием на месте гибели гепатоцитов соединительной ткани — рубцов (то есть острый гепатит В при плохом иммунном ответе постепенно переходит в хронический).
Непременным атрибутом патогенеза является формирование иммунопатологического процесса. Гибель гепатоцитов, инфицированных вирусом гепатита В, следует за счёт иммунокомпетентных частиц, Т-киллеров и макрофагальных элементов.
Серьёзным значением является нарушение свойств мембраны клеток печени, что сопровождается экскрецией (выделением) лизосомальных ферментов, разрушающих гепатоциты. Сообразно этому, гибель гепатоцитов происходит за счёт иммунокомпетентных клеток, лизосомальных ферментов и противопечёночных гуморальных аутоантител, то есть острая болезнь наступает (и благоприятно заканчивается) только при хорошем иммунитете, а при плохом идёт хронизация.
При тяжёлом цитолитическом синдроме (массивные некрозы гепатоцитов) возникает гипокалиемический алкалоз, острая печёночная недостаточность, печёночная энцефалопатия (ПЭП), церебротоксическое действие, нарушение функции обмена нервной ткани. [2] [3] [6]
По клиническим проявлениям:
- субклинический (инаппарантный);
- клинически выраженный (желтушный, безжелтушный, холестатический, фульминантный).
По фазам хронического процесса:
- HBeAg-положительная хроническая инфекция HBV (фаза «иммунной толерантности»);
- HBeAg-положительный хронический гепатит B;
- HBeAg-негативная хроническая инфекция HBV;
- HBeAg-отрицательный хронический гепатит B;
- отрицательная HBsAg фаза HBV-инфекции («оккультная фаза»). [1][2]
Острая печеночная недостаточность (синдром острой печеночной энцефалопатии):
- Первая стадия (ОПЭ-1). Предвестники — астения (слабость) и адинамия, инверсивное настроение, эйфория, нарушение сна, «тряска» конечностей, агрессивность, печёночный запах изо-рта, рвота, сонливость, нарастание желтухи, сжатие размеров печени, ухудшение лабораторных данных.
- Вторая стадия (ОПЭ-2). Прекома — моторное возбуждение перетекает в сопор (субкома), появляются судороги, сознание спутано, дезориентация во времени и месте, хлопающая дрожь кистей, тахикардия, повышение кровоточивости, рвота «кофейной гущей», дёгтеобразный стул, уменьшение диуреза (объёма мочи).
- Третья стадия (ОПЭ-3). Кома I — исчезновение словесной связи и адекватной реакции на болевые раздражители, выявление патологических рефлексов (Бабинского). Наблюдается спазм подбородочной мышцы со смещением кожи подбородка кверху при раздражении кожи в области возвышения одного пальца кисти на той же стороне тела. Появляются симптомы орального автоматизма — хоботковый. Дефекация и акт мочеиспускания не контролируются. Глотание сохранено, зрачки узкие со слабой реакцией на яркий свет, усиление желтухи, геморрагических проявлений, размеров печени, кисло-сладкий печёночный запах изо-рта, олиго или анурия.
- Четвёртая стадия (ОПЭ-4). Кома II — абсолютная потеря реакции на все раздражители, арефлексия, симптом плавающих глазных яблок, зрачки расширены и без реакции на свет, нет корнеального рефлекса, исчезает хлопающий тремор, нарушается глотание, дыхание типа Куссмауля или Чейн-Стокса, пульс нитевидный, недержание мочи и кала, резкое увеличение уровня билирубина в крови. [1][5]
Многообразие форм, тесная взаимосвязь с иммунной системой человека и зачастую достаточно высокая стоимость исследований часто затрудняют принятие конкретного решения и диагноза в стационарный отрезок времени, поэтому во избежание роковых (для больного) ошибок следует подходить к диагностике с учётом всех получаемых данных в динамическом наблюдении:
- общеклинический анализ крови с лейкоцитарной формулой (лейкопения, лимфо- и моноцитоз, уменьшение СОЭ, тромбоцитопения);
- общий анализ мочи (появление уробилина);
- биохимический анализ крови (гипербилирубинемия в основном за счёт связанной фракции, повышение уровня АЛТ и АСТ, ГГТП, холестерина, щелочной фосфатазы, снижение протромбинового индекса, фибриногена, положительная тимоловая проба);
- специфические серологические тесты достаточно многообразны и зависят от стадии и формы гепатита В (HbsAg, HbeAg, HbcorAg, HbcorAb IgM и суммарные, HbeAb, anti-Hbs, ПЦР гепатита В в качественном и количественном измерении);
- УЗИ органов брюшной полости, КТ и МРТ диагностика;
- фиброскан (применяется для оценки степени фиброза). [3][4]
Лечение острых форм гепатита В должно осуществляться в стационаре (учитывая возможность быстрых и тяжёлых форм болезни), хронических — с учётом проявлений. В острый период показан постельный режим, печёночная диета (№ 5 по Певзнеру): достаточное количество жидкости, исключение алкоголя, жирной, жареной, острой пищи, всё в мягком и жидком виде.
При лёгкой и средней тяжести острого гепатита этиотропная противовирусная терапия (ПВТ) не показана. При тяжёлой степени и риске развития осложнений назначается специфическая противовирусная терапия на весь период лечения и возможно более длительное время.
В лечении хронических форм гепатита показаниями к назначению ПВТ является наличие уровня DNA HBV более 2000 МЕ/мл (при циррозе печении независимо от уровня), умеренное и высокое повышение АЛТ/АСТ и степени фиброза печёночной ткани не менее F2 по шкале METAVIR, высокая вирусная нагрузка у беременных женщин. В каждом конкретном случае показания определяются индивидуально, в зависимости от выраженности процесса, временной тенденции, пола, планирования беременности и другого.
Существует два пути противовирусного лечения:
- терапия пегилированными интерферонами (имеет ряд существенных противопоказаний и серьёзных побочных эффектов — не менее 12 месяцев);
- нуклеозидно-аналоговой терапии NA (используются препараты с высоким порогом резистентности вируса, длительно — не менее пяти лет, удобство применения, хорошая переносимость).
В отдельных случаях может рассматриваться применение комбинированной терапии.
Из средств патогенетической терапии в острый период используются внутривенно вводимые растворы 5% глюкозы, дезинтоксикантов, антиоксидантов и витамины. Показан приём энтеросорбентов, ферментных препаратов, при выраженном холестазе применяются препараты Урсодезоксихолевой кислоты, при тяжёлом течении — глюкокортикостероиды, методы аппаратного плазмофереза.
В хронической стадии заболевания при наличии соответствующей активности процесса и невозможности назначения ПВТ может быть показан приём групп гепатопротекторов и антиоксидантов. [1] [3]
Основное направление профилактики на сегодняшний день — это проведение профилактической вакцинации в младенческом возрасте (в том числе усиленная вакцинация детей, рождённых от матерей с гепатитом В) и далее периодические ревакцинации раз в 10 лет (или индивидуально по результатам обследования). Достоверно показано, что в странах, где была введена вакцинация, резко сократилось количество вновь выявленных случаев острого гепатита В.
Вызывает некоторые вопросы эффективность вакцинации при заражении «оккультными» формами гепатита В, так как действие вакцины направлено на нейтрализацию HbsAg, которого в данном случае нет, или он видоизменён — окончательного решения пока не определено, ведутся поиски.
Вторая составляющая стратегии профилактики включает обеспечение безопасности крови и её компонентов, использование одноразового или стерилизованного инструментария, ограничение числа половых партнёров и использование барьерной контрацепции. [1] [2]
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
В патогенезе гепатита В можно выделить несколько ведущих звеньев патогенетической цепи:
- внедрение возбудителя — заражение;
- фиксация на гепатоците и проникновение внутрь клетки;
- размножение вируса и «выталкивание» его на поверхность гепатоцита, а также в кровь;
- включение иммунологических реакции, направленных на элиминацию возбудителя;
- иммунокомплексное поражение органов и систем;
- формирование иммунитета, освобождение от возбудителя, выздоровление.
Поскольку заражение при гепатите В всегда происходит парентеральным путем, можно считать, что момент инфицирования практически равнозначен проникновению вируса в кровь. Попытки некоторых исследователей выделять при гепатите В энтеральную и региональную фазу малообоснованы. Больше оснований считать, что с током крови вирус сразу попадает в печень.
Тропизм вируса гепатита В к ткани печени предопределен наличием в составе НВsАg специального рецептора — полипептида с молекулярной массой 31 000 Да (РЗ1), обладающего альбумин связывающей активностью. Аналогичная зона альбумина находится и на мембране гепатоцитов печени человека и шимпанзе, чем по существу и определяется тропизм НВV к печени человека и шимпанзе.
При проникновении вируса внутрь гепатоцита происходит высвобождение вирусной ДНК, которая, попадая в ядро гепатоцита и исполняя роль матрицы для синтеза нуклеиновых кислот, запускает ряд последовательных биологических реакций, чьим итогом становится сборка нуклеокапсида вируса. Нуклеокапсид мигрирует через ядерную мембрану в цитоплазму где и происходит окончательная сборка частиц Дейна — полного вируса гепатита В.
Следует, однако, отметить, что при заражении гепатоцита процесс может пойти двумя путями — репликативным и интегративным. В первом случае развивается картина острого или хронического гепатита, а во втором — вирусоносительство.
Причины, предопределяющие два вида взаимодействия вирусной ДНК и гепатоцита, точно не установлены. Вероятнее всего, тип реагирования генетически детерминирован.
Итогом репликативного взаимодействия становятся сборка структур коровского антигена (в ядре) и сборка полного вируса (в цитоплазме) с последующей презентацией полного вируса или его антигенов на мембране или в структуре мембраны гепатоцитов.
Принято считать, что репликация вируса не приводит к поражению клетки на уровне гепатоцита, поскольку вирус гепатита В не обладает цитопатическим действием. Это положение нельзя считать бесспорным, так как оно основывается на экспериментальных данных, которые, хотя и свидетельствуют об отсутствии цитопатического действия вируса гепатита В, но получены на культурах тканей и поэтому не могут быть полностью экстраполированы на вирусный гепатит В у человека. Во всяком случае, вопрос об отсутствии поражения гепатоцитов в ходе репликативной фазы нуждается в дополнительном изучении.
Однако, независимо от характера взаимодействия вируса с клеткой, в дальнейшем печень обязательно включается в иммунопатологический процесс. При этом поражение гепатоцитов связано с тем, что в результате экспрессии вирусных антигенов на мембране гепатоцитов и выхода вирусных антигенов в свободную циркуляцию происходит включение цепи последовательных клеточных и гуморальных иммунных реакций, направленных в конечном итоге на удаление вируса ил организма. Этот процесс осуществляется в полном соответствии с общими закономерностями иммунного ответа при вирусных инфекциях. Для элиминации возбудителя включаются клеточные цитотоксические реакции, опосредованные различными классами клеток-эффекторов: К-клеток, Т-клеток, естественных киллеров, макрофагов. В ходе этих реакций происходит разрушение инфицированных гепатоцитов, что сопровождается высвобождением вирусных антигенов (НВсАg, НВeАg, НВsАg), запускающих систему антителогенеза, вследствие чего в крови накапливаются специфические антитела, прежде всего к коровому — анти-НВс и е-антигену — анти-НВЕ. Следовательно, освобождение печеночной клетки от вируса происходит в процессе ее гибели за счет реакций клеточного цитолиза.
Одновременно с этим накапливающиеся в крови специфические антитела связывают антигены вируса, образуя иммунные комплексы, фагоцитируемые макрофагами и выделяющиеся почками. При этом могут возникать различные иммунокомплексные поражения в виде гломерулонефрита, артериита, артралгий, кожных высыпаний и др. С участием специфических антител происходит очищение организма от возбудителя и наступает полное выздоровление.
В соответствии с изложенной концепцией патогенеза гепатита В все многообразие клинических вариантов течения болезни принято объяснять особенностями взаимодействия вируса и кооперацией иммунокомпетентных клеток, иначе говоря, силой иммунного ответа на присутствие вирусных антигенов. По современным представлениям, сила иммунного ответа генетически детерминирована и сцеплена с антигенами гистосовместимости локуса НLA первого класса.
Принято считать, что в условиях адекватного иммунного ответа на антигены вируса клинически развивается острый гепатит с циклическим течением и полным выздоровлением. На фоне снижения иммунного ответа к антигенам вируса иммуноопосредованный цитолиз выражен незначительно, поэтому не происходит эффективной элиминации инфицированных клеток печени, что приводит к слабовыраженным клиническим проявлениям с длительной персистенцией вируса и, возможно, развитию хронического гепатита. При этом, наоборот, в случае генетически детерминированною сильного иммунного ответа и массивности инфицирования (гемотрансфузии) возникают обширные зоны поражения печеночных клеток, чему клинически соответствуют тяжелые и злокачественные формы болезни.
Представленная схема патогенеза гепатита В отличается стройностью, тем не менее в ней имеется ряд спорных и малоисследованных моментов.
Если следовать концепции гепатита В как иммунопатологического заболевания, можно было бы ожидать усиления реакций клеточной цитотоксичности с нарастанием тяжести заболевания. Однако, при тяжелых формах показатели клеточного звена иммунитета резко снижены, в том числе отмечается многократное падение, по сравнению с таковыми у здоровых детей, и показателя К-клеточной цитотоксичности. При злокачественной форме в периоде развития массивного некроза печени и особенно печеночной комы отмечается полная неспособность лимфоцитов к бластной трансформации под влиянием фитогематтлютинина, стафилококкового эндотоксина и НВsAg. Кроме того, отсутствует способность лейкоцитов к миграции по данным реакции торможения миграции лейкоцитов (РТМЛ), и выявляется резкое увеличение проницаемости мембран лимфоцитов по результатам исследований их с помощью флюоресцентного зонда тетрациклина.
Так, если показатели флюоресценции лимфоцитов здоровых людей составляют 9,9±2%, а при типичном гепатите В с доброкачественным течением они повышаются до 22,3±2,7%, то при злокачественных формах число флюоресцирующих лимфоцитов достигает в среднем 63,5±5,8%. Поскольку повышение проницаемости клеточных мембран однозначно оценивается в литературе как достоверный показатель их функциональной неполноценности, можно заключить, что при гепатите В, особенно при злокачественной форме, возникает грубое повреждение лимфоцитов. Об этом же свидетельствуют и показатели К-клеточной цитотоксичносги. При тяжелой форме на 1-2-й неделе заболевания цитотоксичность составляет 15,5±8,8%, а при злокачественной форме на 1-й неделе — 6.0±2,6, на 2-й — 22.0±6,3% при норме 44,8±2,6%.
Представленные данные однозначно свидетельствуют о выраженных нарушениях в клеточном звене иммунитета у больных с тяжелыми формами гепатита В. Очевидно также, что эти изменения возникают вторично, в результате поражения иммунокомпетентных клеток токсическими метаболитами и, возможно, циркулирующими иммунными комплексами.
Как показали исследования, у больных с тяжелыми формами гепатита В, особенно в случае развития массивного некроза печени, в сыворотке крови происходит падение титра HВsАg и НВeАg и одновременно начинают обнаруживаться в высоких титрах антитела к поверхностному антигену, что совершенно нехарактерно для доброкачественных форм болезни, при которых анти-НВV появляются лишь на 3-5-м месяцев болезни.
Быстрое исчезновение антигенов вируса гепатита В при одновременном появлении высоких титров противовирусных антител позволяет предполагать интенсивное образование иммунных комплексов и возможное их участие в патогенезе развития массивного некроза печени.
Таким образом, фактические материалы не позволяют однозначно трактовать гепатит В только с позиций иммунопатологической агрессии. И дело не только в том, что при этом не обнаруживается связи между глубиной и распространенностью морфологических изменений в печени, с одной стороны, и выраженностью клеточных факторов иммунитета — с другой. Теоретически это обстоятельство можно было бы объяснить поздними сроками исследования показателей клеточного иммунитета, когда иммунокомпетентные клетки подверглись мощному токсическому воздействию в связи с нарастающей функциональной недостаточностью печени. Можно, конечно, допустить, что иммунный цитолиз гепатоцитов происходит на самых ранних этапах инфекционного процесса, возможно, еще до появления клинических симптомов тяжелого поражения печени. Однако такое предположение маловероятно, поскольку у больных с острейшим (молниеносным) течением болезни выявлялись аналогичные показатели клеточного иммунитета и, кроме того, при морфологическом исследовании ткани печени не обнаруживалось массивной лимфоцитарной инфильтрации, в то же время выявлялись сплошные поля некротизированного эпителия без явлений резорбции и лимфоцитарной агрессии.
Объяснить морфологическую картину при остром гепатите только с позиций иммунного клеточного цитолиза весьма сложно, поэтому в ранних работах не исключали цитотоксическое действие вируса гепатита В.
В настоящее время это предположение нашло частичное подтверждение благодаря открытию вируса гепатита В. Как показали исследования, частота обнаружения маркеров гепатита D находится в прямой зависимости от тяжести заболевания: при легкой форме они обнаруживаются у 14%, среднетяжелой — у 18, тяжелой — 30, злокачественной — у 52% больных. Учитывая, что вирус гепатита D обладает некрозогенным цитопатическим эффектом, можно считать установленным, что в развитии фульминантных форм гепатита В большое значение имеет коинфекция вирусами гепатита В и D.
Патогенез гепатита В можно представить следующим образом. После проникновения вируса гепатита В в гепатоциты индуцируется иммунологическая атака на инфицированные гепатоциты Т-киллеров, выделяющих лимфотоксины в направлении печеночных клеток.
Интимные механизмы поражения гепатоцигов при гепатите В до настоящего времени не установлены. Ведущую роль играют активированные процессы перекисного окисления липидов и лизосомальные гидролазы. Пусковым моментом могут быть лимфотоксины, высвобождающиеся из эффекторных клеток при их контакте с гепатоцитами, но не исключено, что инициатором процессов переоксидации может выступать и сам вирус. В дальнейшем патологический процесс вероятнее всего развивается в следующей последовательности.
- Взаимодействие фактора агрессии (лимфотоксины или вирус) с биологическими макромолекулами (возможно, с компонентами мембран эндоплазматической сети, способными принимать участие в процессах детоксикации, по аналогии с другими повреждающими агентами, как это было показано по отношению к четыреххлористому углероду).
- Образование свободных радикалов, активация процессов перекисного окисления липидов и повышение проницаемости всех гепатоцеллюлярных мембран (синдром цитолиза).
- Движение биологически активных веществ по градиенту концентрации — потеря ферментов различной внутриклеточной локализации, донаторов энергии, калия и др. Накопление в клетках натрия, кальция, сдвиг pH в сторону внутриклеточного ацидоза.
- Активация и выход лизосомальных гидролаз (РНК-аза, ДНК-аза, катепсины и др.) с распадом печеночной клетки и высвобождением аутоантигенов.
- Стимуляция Т- и В-систем иммунитета с формированием специфической сенсибилизации Т-лимфоцитов к печеночному липопротеину, а также образование противопеченочных гуморальных аутоантител.
В предложенной схеме патогенеза гепатита В в качестве пускового фактора выступают вирусные антигены, чья интенсивная продукция наблюдается на самых ранних этапах заболевания и весь острый период, за исключением злокачественных форм, при которых продукция вирусных антигенов практически прекращается в момент развития массивного некроза печени, что и предопределяет быстрое снижение репликации вируса.
Очевидно также, что вирусные антигены активируют Т- и В-системы иммунитета. В ходе этого процесса возникает характерное перераспределение субпопуляций Т-лимфоцитов, направленное на организацию адекватного иммунного ответа, элиминацию инфицированных гепатоцитов, нейтрализацию вирусных антигенов, саногенез и выздоровление
При взаимодействии иммунокомпетентных клеток с вирусными антигенами на мембранах гепатоцитов или в ходе репродукции вируса внутри гепатоцита, возникают условия для активации процессов перекисного окисления липидов, управляющий как известно, проницаемостью всех клеточных и субклеточных мембран,
С этих позиций становится понятным столь закономерное и в высшей степени характерное для вирусных гепатитов возникновение синдрома цитолиза — повышенной проницаемости клеточных мембран
Конечным исходом синдрома цитолиза может быть полное разобщение окислительного фосфорилирования, истечение материала клетки, гибель печеночной паренхимы.
Однако в подавляющем большинстве случаев эти процессы не приобретают столь фатального развития. Только при злокачественных формах болезни патологический процесс протекает лавинообразно и необратимо, поскольку возникают массивное заражение, выраженный иммунный процесс, чрезмерная активация процессов переоксидации и лизосомальных гидродаз, явления аутоиммунной агрессии.
Эти же механизмы наблюдаются и при благоприятном течении гепатита В, с той лишь особенностью, что все они реализуются на качественно ином уровне. В отличие от случаев массивного некроза печени, при благоприятном течении болезни количество инфицированных гепатоцитов, а следовательно, зона иммунопатологического цитолиза меньше, процессы перекисного окисления липидов усиливаются не столь значительно, активация же кислых гидролаз приводит лишь к ограниченному аутолизу с несущественным высвобождением аутоантигенов, а следовательно, без массивной аутоагрессии, то есть все этапы патогенеза при благоприятном течении осуществляются в рамках сохраняющейся структурной организации паренхимы печени и сдерживаются защитными системами (антиоксиданты, ингибиторы и др.) и поэтому не имеют столь разрушительного действия.
Причины возникновения симптомов интоксикации при вирусных гепатитах исследованы не до конца. Предложение различать так называемую первичную, или вирусную, интоксикацию и вторичную (обменную, или метаболическую) можно считать позитивным, хотя это не раскрывает интимного механизма возникновения общетоксического синдрома. Во-первых, вирусы гепатитов не обладают токсическими свойствами, а, во-вторых, концентрация многих метаболитов далеко не всегда коррелирует с тяжестью заболевания и степенью выраженности симптомов токсикоза. Известно также, что и концентрация вирусных антигенов строго не коррелирует с тяжестью интоксикации. наоборот, с увеличением тяжести заболевания, а следовательно, нарастания степени токсикоза, концентрация НВsАg снижается и бывает самой низкой при злокачественных формах в момент возникновения глубокой печеночной комы. Вместе с тем частота обнаружения и титры специфических противовирусных антител прямо зависят от тяжести заболевания.
Интоксикация появляется не в момент регистрации вирусных антигенов, а в периоде циркуляции в крови противовирусных антител класса IgМ к коровскому антигену и антигену системы E. Более того, при тяжелых и особенно злокачественных формах у значительной части больных в крови появляются даже анти-НВs, чего обычно никогда не наблюдается при легких и среднетяжелых формах болезни.
Представленные данные дозволяют заключить, что синдром токсикоза при вирусных гепатитах, и гепатите В в частности, не возникает в результате появления в крови вирусных антигенов, а становится следствием взаимодействия вирусных антигенов с противовирусными антителами класса IgМ. Результат такого взаимодействия, как известно, — образование иммунных комплексов и, возможно, активных токсичных веществ.
Симптомы интоксикации возникают в момент появления в свободной циркуляции иммунных комплексов, но в дальнейшем такой корреляции не прослеживается.
Частичное объяснение этому можно найти при исследовании состава иммунных комплексов. У больных с тяжелыми формами в крови циркулируют преимущественно комплексы среднего размера, а в их составе на высоте токсического синдрома преобладают антитела класса тогда как в периоде спада клинических проявлений и реконвалесценции комплексы становятся более крупными, а в их составе начинают преобладать антитела класса IgG.
Представленные данные касаются механизмов развития токсического синдрома в начальном периоде заболевания, но при токсикозе, возникающем на высоте клинических проявлений, они имеют лишь частичное значение и особенно — при развитии печеночной комы.
Методом гемокультур удалось показать, что при гепатите В в крови постоянно накапливаются токсины, высвобождающиеся из пораженной распадающейся печеночной ткани. Концентрация этих токсинов пропорциональна тяжести заболевания,они имеют белковую природу.
В периоде реконвалесценции в крови появляются антитела к этому токсину; но в случае возникновения печеночной комы концентрация токсина в крови резко возрастает, а антитела в крови не обнаруживаются.
По характеру морфологических изменений различают три формы острого гепатита В:
- циклическая форма,
- массивный некроз печени;
- холестатический перихолангиолитический гепатит.
При циклической форме гепатита В дистрофические, воспалительные и пролиферативные изменения более выражены в центре долек, в то время как при гепатите А они локализуются по периферии дольки, распространяясь к центру. Эти различия объясняются разными путями проникновения вируса в паренхиму печень. Вирус гепатита А попадает в печень через воротную вену и распространяется к центру долек, вирус гепатита В проникает через печеночную артерию и разветвления капилляров, равномерно снабжающие все дольки, вплоть до их центра.
Степень поражения паренхимы печени в большинстве случаев соответствует тяжести клинических проявлений болезни. При легких формах обычно наблюдается фокальный некроз гепатоцитов, а при среднетяжелых и тяжелых формах — зональный некроз (с тенденцией к слиянию и образованию мостовидных некрозов при тяжелых формах болезни).
Наибольшие морфологические изменения в паренхиме наблюдаются на высоте клинических проявлений, что обычно совпадает с 1-й декадой заболевания. В течение 2-й и особенно 3-й декады усиливаются процессы регенерации. К этому периоду уже практически полностью исчезают некробиотические изменения и начинают преобладать процессы клеточной инфильтрации с медленным последующим восстановлением структуры печеночно-клеточных пластинок. Однако полное восстановление структуры и функции печеночной паренхимы наступает только через 3-6 мес от начала заболевания и далеко не у всех больных.
Генерализованный характер инфекции при гепатите В подтверждается и обнаружением НВsAg не только в гепатоцитах, но и в почках, легких, селезенке, поджелудочной железе, клетках костного мозга и др.
Холестатический (перихолангиолитический) гепатит — особая форма заболевания, при которой наибольшие морфологические изменения обнаруживаются со стороны внутрипеченочных желчных ходов, с картиной холангиолита и перихолангиолита. При холестатической форме возникают холестазы с расширением желчных капилляров со стазом желчи в них, с пролиферацией холангиол и клеточными инфильтратами вокруг них. Печеночные клетки при данной форме гепатита поражаются незначительно. Клинически заболевание характеризуется затяжным течением с длительной желтухой. Показано, что причиной такого своеобразного течения болезни служи преимущественное действие вируса на стенки холангиол при несущественном воздействии на гепатоциты.
источник