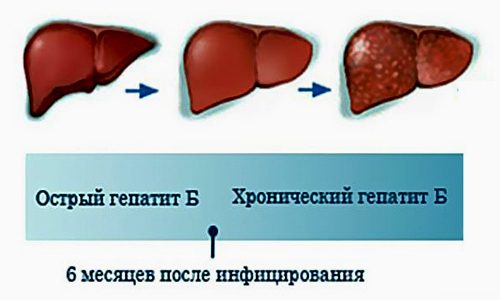
Хронический вирусный гепатит В — это серьезное заболевание печени, которому подвержены только люди. Согласно медицинской статистике, треть населения земного шара имеет в своей крови маркеры HBV-инфекции, свидетельствующие о перенесенном недуге, и более 350 млн человек, которые в настоящее время являются носителями вируса, могут даже не догадываться об этом. Эти показатели указывают на разнообразие клинической картины и исход заболевания. Именно поэтому важно знать признаки недуга, как передается и есть ли возможность вылечить хронический гепатит.
Вирус гепатита В устойчив к воздействию внешней среды и передается только от человека к человеку.
В препаратах крови его жизнеспособности практически ничего не угрожает и он может быть активным на протяжении нескольких лет. Период существования вируса на предметах личной гигиены, белье и медицинских инструментах значительно меньше и при нормальной температуре составляет всего несколько месяцев. Высокие температуры (120–180 ºC) и дезинфицирующие препараты позволяют уничтожить частички гепатита В всего лишь в течение часа.
Переносчиками вируса считаются не только заболевшие люди, но и лица, являющиеся носителями. Биологический материал больного человека опасен уже в период инкубационного периода, когда симптомы хронического гепатита В еще незаметны. Несмотря на то что эпидемиологическую опасность представляют только кровь и сперма больного человека (именно здесь наибольший процент скопления клеток вируса), наблюдались случаи, когда гепатитом В заражались через слюну, мочу или грудное молоко вирусоносителя.
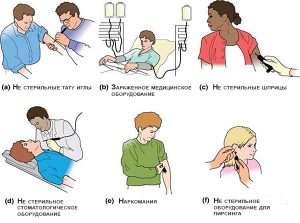
Возможные пути передачи вирусного гепатита В:
- Парентеральный путь. При переливании крови или плазмы больного человека, при многократном использовании без стерилизации медицинских инструментов после контакта с вирусоносителем.
- Бытовой путь. При использовании общих предметов гигиены (полотенец, бритв, зубных щеток). Однако здесь имеется некоторая особенность: вирус может попасть к здоровому человеку только при наличии ранок или микротрещин, сквозь которые в организм попадут зараженные биологические частички.
- Заражение гепатитом половым путем.
-
В редких случаях наблюдается вертикальный путь передачи инфекции, который регистрируется при родах.
- Часто вирус гепатита В передается через маникюрные приборы в салонах, при использовании общих шприцев или нанесении татуировок необработанными инструментами.
Различают несколько видов данного недуга:
- Позитивный репликативный хронический гепатит В, симптомы и лечение этого варианта соответствуют острой фазе заболевания. Больной ощущает сильную слабость, быструю утомляемость, горечь во рту, боли в правом подреберье. Наблюдается повышение температуры тела, вздутие живота, неустойчивый стул. Причем чем выше активность патологического процесса, тем более выражены признаки болезни. При осмотре врач наблюдает желтушность кожи, а в наиболее тяжелых случаях — носовые кровотечения и геморрагические высыпания.
-
Негативный хронический интегративный гепатит В. Это неактивная фаза заболевания, которая, как правило, протекает без особых симптомов и имеет благоприятный исход. При визуальном обследовании больного каких-либо существенных изменений, например желтушности кожи, не наблюдается. Селезенка также не увеличена, анализы в норме или на высшей границе нормы. Однако практически всегда заметно увеличение печени.
- Интегративный микст-гепатит характеризуется отсутствием маркеров патологии, но при этом сохраняются высокие уровни аланиновой аминотрансферазы в крови, что указывает на продолжающийся выраженный процесс разрушения печени.
О том, как лечить хронический гепатит В, пациенту должен рассказать лечащий врач. Не стоит пытаться излечить заболевание самостоятельно, поскольку патология может спровоцировать серьезные осложнения.
Лечение заболевания направлено на уменьшение воспаления и степени фиброза в печени, подавление вируса и улучшение качества жизни больного. При выраженной фазе рекомендуется противовирусная терапия, основой которой станет подавление активности вируса. При интегративном хроническом гепатите В терапевтические мероприятия не позволяют инфекционному процессу перейти в стадию активности.
Для подавления вируса используются следующие группы препаратов:
- Интерфероны, которые быстро подавляют вирус и приводят к длительной ремиссии.
- Нуклеозидные ингибиторы обратной транскриптазы. Очень мощные препараты, влияющие на вирус на клеточном уровне. Как правило, применяют при неэффективности интерферонов.
- Глюкокортикостероиды. Рекомендуются непосредственно перед противовирусной терапией для усиления иммунной реакции.
Помимо противовирусной терапии, используется симптоматическое лечение, благодаря которому функции печени быстрее восстанавливаются, а больной ощущает значительное облегчение состояния.

- Разогретый мед смешивают с яблочным соком и пьют непосредственно перед сном. Такой вариант лечения не позволяет клеткам печени разрушаться и деформироваться. Однако использовать его можно только при отсутствии аллергии на продукты пчеловодства.
- Смешивают в равных пропорциях тысячелистник, мяту и семена укропа. Готовую массу заливают 2 стаканами кипятка и проваривают пару минут. Отвар настаивают под крышкой 7–8 часов, после чего процеживают. Выпивают смесь в течение дня равными порциями.
- Горсть цветка маргаритки в течение 10 часов настаивают в 2 стаканах воды комнатной температуры (лучше кипяченой). По истечении времени настой фильтруют и употребляют по 100–120 мл трижды в день.
- 5 г измельченного корня девясила залить 200 мл крутого кипятка, настоять 8 часов, профильтровать через 2 слоя марли. Пить по четверти стакана 4 раза в день. Средство считается отличным желчегонным вариантом.
-
1 ч. л. цветков бессмертника заливают стаканом кипятка и настаивают в течение часа в термосе. Готовую жидкость фильтруют и употребляют по полстакана трижды в день после основных приемов пищи.
- Смешивают семена моркови, свеклы и сельдерея в пропорциях 1:3:4. 3 ст. л. смеси заливают 1 л кипятка и дают настояться полчаса, после чего фильтруют. Употребляют средство по полстакана 6 раз в день.
- 0,5 г мумие разводят в 500 мл кипяченой воды. Готовый раствор употребляют по 1 ст. л. за 30 минут до еды. Длительность лечения — 24 дня.
Обострение хронического гепатита В наблюдается, как правило, вследствие нарушений предписаний врача и после контакта с провоцирующими факторами. В период обострения больному рекомендуется соблюдать постельный режим. Причем до тех пор, пока не нормализуется работа печени.
Еще одно обязательное правило — соблюдение правильной системы питания. Часто врачи назначают диету №5. Рацион больного должен включать в себя пищу, богатую белками и углеводами. Жиры рекомендуется максимально сократить, а некоторые и вовсе исключить. Категорически противопоказан алкоголь (в том числе и в минимальных дозах). Рекомендуется есть часто, но порция не должна превышать 200–250 г.
Больным, у которых наблюдается данная патология, следует оберегать себя и от сопутствующих недугов. Особую опасность представляют болезни сердца, ЖКТ и инфекционные заболевания. Нежелательны также переохлаждения или длительное пребывание на солнце.
источник
Опасное заболевание – хронический гепатит В – приводит к разрушению клеток и ухудшению работы печени. Вирус, вызывающий болезнь, передается через биологические жидкости организма. В большинстве случаев хронический гепатит является результатом недолеченного острого. Комплексное лечение дальнейших обострений включает противовирусную терапию, использование гепатопротекторов, иммуномодуляторов, витаминов. Несоблюдение назначенной схемы лечения может привести к циррозу и даже раку. В этих случаях проводят трансплантацию печени.
Хронический гепатит В вызывает вирус, обладающий рядом признаков:
- встречается только у человека;
- имеет высокую устойчивость к неблагоприятным факторам среды;
- местом его размножения является печень.
- парентеральный (через кровь);
- половой;
- от матери к ребенку при беременности или родах.
Наиболее восприимчивы к вирусу дети до 5 лет и люди с ослабленным иммунитетом.
Особенность хронического гепатита В – наличие фазы иммунной толерантности. Симптомы болезни отсутствуют, а анализы не показывают изменений.
По статистике, гепатитом В болеет почти треть населения Земли. Хронический гепатит В (ХГВ) возникает у 5-10% лиц, перенесших острый процесс. Развитие болезни включает несколько фаз:
- Период иммунной толерантности, когда вирус живет в клетках без их повреждения, проходит бессимптомно.
- В период активности начинается быстрое размножение вируса гепатита В (ВГВ) и разрушение гепатоцитов. Налицо все симптомы заболевания.
- Этап вирусоносительства (ремиссии) протекает длительно, признаки болезни отсутствуют. Больной представляет опасность для окружающих.
Обострение хронического заболевания могут спровоцировать факторы среды: попадание в организм вируса герпеса, злоупотребление алкоголем, несоблюдение правил гигиены.

Симптомы обострения гепатита обусловлены нарушением работы печени и проявляются:
- общей слабостью, повышенной раздражительностью, утомляемостью;
- болями в области правого подреберья;
- появлением признаков крапивницы, зудом;
- брадикардией и гипотонией;
- образованием тромбов или кровоточивостью;
- тошнотой, жидким стулом, похудением;
- увеличением размеров органа, пожелтением кожи.
Симптомы проявляются слабо, например, может отсутствовать желтушность. Первым признаком обострения хронической болезни может стать кожный зуд в ладонях, нарушения стула или тяжесть в подреберье.
Диагностика ХГВ назначается врачом-гастроэнтерологом. Обследование включает лабораторные (исследование крови) и инструментальные методы (УЗИ, биопсия).
При хроническом течении гепатита разрушаются клетки печени, изменяется белковый состав крови. На этом основана диагностика ХГВ.
Для определения наличия и степени повреждения органа исследуют:
- Уровень аминотрансфераз (АЛТ и АСТ) – ферментов печеночных тканей. Повышение АЛТ указывает на вирусное поражение, АСТ – на разрушение клеток.
- Содержание альбумина – белка, который вырабатывается в органе. Снижение его концентрации в крови указывает на гепатит.
- Количество ферритина – железосодержащего белка. Его повышение характерно для повреждения клеток.
Информативным является показатель количества билирубина – главного компонента желчи. Рост его содержания в крови свидетельствует о нарушении работы печени.
На стадии хронического вирусоносительства разрушенные гепатоциты замещаются соединительной тканью. Это явление называется фиброз. Для определения его степени используют биохимический метод – фибротест. Он позволяет выявить хроническую патологию на самой ранней стадии. При диагностике хронического воспаления его проводят совместно с биохимическим исследованием крови.
Используют обычный ФиброТест или ФиброМакс. В первом случае определяют белковые фракции, ферменты, АЛТ и билирубин. Если этого недостаточно, назначают ФиброМакс, который дополнительно включает определение:
Подготовиться к этому обследованию непросто: два дня пред этим запрещено курить и есть мясо, накануне нельзя пить.
Метод маркеров при диагностике гепатита основан на определении наличия антигенов ВГВ, которые обеспечивают внедрение вируса в клетки. В стадии активности антигены попадают в кровь, что позволяет выявить наличие ВГВ. Самым известным из маркеров активной вирусной репликации является антиген HBsAg (Австралийский антиген). Больные гепатитом Б могут определить его в домашних условиях экспресс-методом.

В клинике проводят полноценный анализ венозной крови иммуноферментным методом или с помощью реакции флуоресцирующих антител. Так определяют не только наличие HBsAg, но и степень поражения гепатоцитов. Методы основаны на том, что при попадании антигена организм вырабатывает антитела, и можно выявить наличие и количество комплексов антиген-антитело.
Если на основании биохимических обследований постановка диагноза затруднена, используют аппаратные методы:
- Ультразвуковое обследование при хронической форме гепатита основано на разной степени поглощения УЗ-волн здоровыми и поврежденными тканями. На картинке монитора виден орган с участками разной интенсивности, по которым определяют наличие и степень поражения.
- Эластография (фибросканирование) – новый метод, позволяющий определить размеры и расположение пораженных участков печени. На экране получают изображение, где здоровые и больные ткани показаны разным цветом. Оба метода информативны, совершенно безболезненны, не требуют больших затрат времени.
Для уточнения диагноза назначают и другие обследования:
- Компьютерная томография с помощью снимков позволяет оценить расположение, размеры и степень повреждений.
- Магнитно-резонансная томография выявляет малейшие поражения тканей.
- Биопсия в последнее время применяется редко, так как является инвазивным методом и требует длительной подготовки. Но точность его высока, поскольку исследуется непосредственно печеночная ткань.
- Сцинтиграфия – метод, когда пациенту в вену вводят радиоактивные изотопы, а затем улавливают исходящее от органа излучение. По изображениям устанавливают наличие и степень повреждения.
В итоге получают полную информацию о состоянии печени. На основании данных обследования гастроэнтеролог назначает лечение.
Полностью излечить хроническую болезнь пока не удается. Но правильное лечение и выполнение необходимых мероприятий поможет продлить ремиссию на долгие годы.
Стратегия комплексной терапии ХГВ зависит от степени проявления патологии. Как лечить хронический гепатит на данном этапе, может определить только врач.
В стадии ремиссии, характеризующейся отсутствием специфических симптомов, болей или тяжести в области печени, необходимо наблюдаться у специалиста, своевременно сдавать анализы.
В фазе активности прописывают противовирусные средства, прежде всего интерфероны. Они повышают активность иммунитета и тормозят размножение ВГВ, препятствуют фиброзу, устраняют симптомы болезни.
Препараты обладают высокой противовирусной активностью (Реаферон, Интрон, Интерферон-Р). Их вводят 3-7 раз в неделю на протяжении 6-12 мес. Разработаны интерфероны пролонгированного действия, например, отечественный Альгерон. Их применяют раз в неделю.

В терапии хронической формы используют аналоги нуклеотидов или нуклеозидов. В период активности они встраиваются в ДНК вирусов, и те теряют способность размножаться. Высокой эффективностью обладают:
- Ламивудин – российский препарат, разрушающий не только ВГВ, но и ВИЧ;
- Энтекавир – выпускается в Словении, обладает высокой противовирусной активностью;
- Тенофовир – производится в России, рекомендован при неэффективности других средств.
Недостатком этих лекарств является постепенное развитие резистентности вирусов, что вызывает необходимость замены препарата.
Эти лекарства защищают печень от любых агрессивных факторов. Они действуют в нескольких направлениях:
- выводят токсины;
- оказывают противовоспалительный эффект;
- препятствуют развитию фиброза;
- стимулируют восстановление клеток органа;
- являются иммуномодуляторами.
Их, как правило, применяют в фазе ремиссии гепатита по окончании противовирусной терапии. Однако если интерфероны и нуклеозиды в стадии клинического обострения гепатита противопоказаны, гепатопротекторами лечится и активная стадия. Их также включают в состав комплексной терапии для снижения побочного действия интерферонов.
Эффективны при лечении гепатита В:
- Гепатофальк – средство на растительной основе с противовоспалительным и обезболивающим действием;
- Фосфоглив – российский препарат, оказывающий защитное и противовирусное действие;
- Легалон – содержит экстракт расторопши, снижает токсические проявления, восстанавливает синтез белков.
Препараты не имеют побочных эффектов, но принимать их без консультации врача нельзя – назначения проводят только на основании результатов обследования.
Когда тяжелая хроническая форма гепатита Б не поддается лечению, а гепатоциты продолжают разрушаться, развивается печеночная недостаточность, возникает угроза летального исхода. Это является показанием для трансплантации.
Печень пересаживают от умершего человека или живого донора (используют лишь часть органа). В первом случае положительный исход наблюдается в 80% случаев, во втором – в 90%.
Часто при пересадке наблюдаются осложнения:
- иммунологическая несовместимость тканей;
- образование тромбов;
- инфекционный процесс;
- истечение желчи.
Любой из этих факторов может привести к смерти. Если операция проведена успешно, длительно принимают препараты, препятствующие отторжению чужих тканей.
Пересадка не гарантирует устранения вируса. Нужно регулярно проходить обследования, соблюдать диету. Любое вирусное заболевание может спровоцировать рецидив.
Диета №5 является элементом комплексного лечения хронического процесса и исключает жирную, острую, копченую и жареную пищу. Запрещено употреблять:
- овощные, мясные, рыбные консервы;
- жирную рыбу и мясо;
- фрукты и ягоды высокой кислотности;
- изделия из сдобного теста;
- газированные напитки;
- кофе;
- алкоголь.
Питание должно быть дробным (4-5 раз в день), основа рациона – овощи и фрукты. Пища готовится дома на пару или варится.
Дополнительно в период ремиссии применяют витамины А, С, Е и группы В, которые обладают антиоксидантными свойствами и БАДы для очищения печени:
- Овесол – включает растительные экстракты, обладает противовоспалительным и желчегонным действием;
- Гепатрин – растительный БАД-гепатопротектор;
- Холесенол Артишок применяют в комплексной терапии ХГВ для улучшения работы органа.
Для лечения и профилактики гепатита используют также народные средства. Любое из них должно быть одобрено врачом, поскольку на фоне медикаментозного лечения может увеличиться нагрузка на печень.
Среди всех видов гепатита ХГВ считают самым опасным из-за риска осложнений и того, что его хронизация может проходить незаметно. Симптоматика бывает слабо выражена. Это затрудняет постановку диагноза. Поэтому лишь в 40-50% случаев лечение ХГВ приводит к полному выздоровлению.
Причины развития хронического гепатита В у людей, перенесших острую форму, обусловлены, по мнению специалистов, сбоями в работе иммунной системы. Провоцирующими факторами могут стать:
- другие вирусные инфекции;
- нездоровое питание (жирное, копченое, фаст-фуды);
- злоупотребление алкоголем;
- включение аутоиммунных механизмов;
- частый прием обезболивающих средств, антибиотиков.
По данным ВОЗ, почти у 30% хронических больных гепатит прогрессирует. У большинства в течение 3-5 лет развивается цирроз или рак печени. Предполагается, что через 10-15 лет количество этих заболеваний возрастет на 50-70%.
источник
Больной должен быть обследован на контагиозность. Это особенно важно, если он является HBeAg-положительным. Отдельно следует обследовать семью и сексуального партнёра больного на наличие HBsAg и анти-НВс, в случае отрицательных результатов исследований им рекомендуют вакцинацию против гепатита В.
Постельный режим не обязателен. Физическая нагрузка должна быть дозированной. Питание обычное. Приёма алкоголя следует избегать, так как это улучшает прогноз для носителей HBsAg. Однако 1-2 стакана вина или пива в день допустимы, если это является частью образа жизни больного.
Большинство больных с хроническим гепатитом В ведут нормальную жизнь. Необходима психологическая поддержка для предупреждения «ухода в болезнь».
Следует выяснить, насколько больной контагиозен, какова выраженность симптомов или печёночной недостаточности. Пункционная биопсия печени обычно предшествует назначению терапии. Наличие тяжёлого хронического гепатита с циррозом, очевидно, заставляет решать вопрос о лечении в срочном порядке. Подход к больным с высокой контагиозностью в репликативной фазе и больным с низкой контагиозностью в фазе интеграции вируса различен.

Лечение хронического вирусного гепатита В направлено на подавление контагиозности, уничтожение вируса, предотвращение развития цирроза печени и, возможно, гепатоцеллюлярной карциномы. Ни один метод лечения не избавляет больного от вируса, тем не менее успешная противовирусная терапия позволяет уменьшить выраженность процесса и обусловленный им некроз гепатоцитов.
Следует рассмотреть возможность применения интерферона-а (ИФН-а), как лимфобластоидного, так и рекомбинантного. Интерферон улучшает экспрессию белков HLA класса I и может увеличивать активность интерлейкина-2 (ИЛ-2) и, таким образом, разрушать поражённые гепатоциты.
Интерферон в лечении HBeAg-положительных больных: метаанализ (15 исследований)
Интерферон-а применяют только у больных с реплицирующимся HBV, что устанавливают по положительным тестам на HBeAg и HBV-ДНК и, если необходимо, HBeAg в гепатоцитах.
По схеме, принятой в США, вводят 5 млн ЕД ежедневно либо 10 млн ЕД 3 раза в неделю подкожно в течение 16 нед. Эти дозы выше принятых в Европе и вызывают множество побочных эффектов, в связи с чем высока частота прерывания лечения. Увеличение продолжительности лечения или применение более высоких доз препарата не сказываются на эффективности лечения.
Ранние системные побочные эффекты обычно имеют преходящий характер, возникают в течение 1-й недели лечения через 4-8 ч после инъекции и купируются парацетамолом. Поздние осложнения в виде психических расстройств, особенно на фоне уже существовавшего психического заболевания, являются показанием для прекращения лечения интерфероном. Наличие в анамнезе психических расстройств является противопоказанием к назначению интерферона. Аутоиммунные изменения развиваются через 4-6 мес от начала лечения и включают появление антинуклеарных, антимитохондриальных и антитиреоидных антител. Наличие антител к микросомам щитовидной железы до начала лечения является противопоказанием к назначению интерферона. Возможно также развитие бактериальной инфекции, особенно при циррозе печени.
Позитивный ответ характеризуется исчезновением HBeAg и HBV-ДНК и преходящим повышением активности сывороточных трансаминаз приблизительно на 8-й неделе, что обусловлено лизисом инфицированных гепатоцитов. Биопсия печени выявляет уменьшение воспаления и гепатоцеллюлярного некроза. Репликативные формы HBV исчезают из печени. Анти-НВе появляются примерно через 6 мес. HBsAg исчезает только у 5-10%, обычно когда лечение начинают в самые ранние сроки заболевания. Элиминация HBsAg может затягиваться на многие месяцы.
- Гриппоподобный синдром
- Миалгии, обычно преходящие
- Головная боль
- Тошнота
- Слабость
- Миалгии
- Раздражительность
- Тревожность и депрессия
- Уменьшение массы тела
- Диарея
- Алопеция
- Миелосупрессия
- Бактериальные инфекции
- Появление аутоиммунных антител
- Нейропатия зрительного тракта
- Обострение красного плоского лишая
Лечение интерфероном, несомненно, эффективно. По данным метаанализа 15 контролированных исследований эффективности интерферона, у HBeAg-положительных больных отмечается в 4 раза более частое исчезновение HBsAg и в 3 раза более частое исчезновение HBeAg по сравнению с контролем .
Больные с декомпенсированным циррозом страдают от побочных эффектов, особенно от инфекций, которые служат поводом для прекращения лечения интерфероном или снижения дозы. В группе А по Чайлду даже низкие дозы (например, 1 млн ЕД 3 раза в неделю) дробно вводимого интерферона-а могут оказаться эффективными, но в группах В или С результаты лечения плохие и наблюдается множество побочных эффектов.
Эффективность лечения интерфероном-а выражалась в длительной ремиссии заболевания печени у 8 из 15 больных с хронической HBV-инфекцией и гломерулонефритом. В течении заболевания почек обычно отмечается улучшение.
Эти результаты получены у взрослых больных белой расы с хорошим общим состоянием и компенсированным заболеванием печени. Менее благоприятные результаты получены у больных, китайцев по происхождению, среди которых обострения после ремиссии, достигнутой с помощью интерферона, наблюдаются у 25%, а HBV-ДНК перестаёт выявляться только у 17 % больных, у которых исчезает HBeAg.
Интерферон может быть эффективным у детей. Общая доза 7,5 млн ЕД/м 2 при введении 3 раза в неделю в течение 6 мес привела у 30% к развитию сероконверсии HBeAg в анти-НВе.
Низкий показатель успешных результатов в сочетании с высокой стоимостью лечения и побочными эффектами затрудняют подбор больных для лечения интерфероном. Оно показано медицинским работникам (хирурги, стоматологи, медсестры, студенты-медики, лаборанты) и лицам, часто меняющим полового партнёра. Наибольшая эффективность лечения наблюдается у лиц, перенёсших острый вирусный гепатит, имеющих высокую активность АлАТ и низкий уровень виремии.
В настоящее время исследуется эффективность аналогов нуклеозидов в лечении хронической HBV-инфекции. Аденин-арабинозид-5-монофосфат (АРА-АМФ) является синтетическим пуриновым нуклеозидом, обладающим противовирусной активностью в отношении HBV. Ранние наблюдения подтвердили этот эффект, но дальнейшие исследования не проводились из-за нейротоксичности (миалгии, периферическая невропатия), отмечавшейся на всем протяжении лечения. В недавних исследованиях было показано, что в результате лечения АРА-АМФ у 37% больных с хронической HBV-инфекцией в крови исчезает HBV-ДНК, но полный и стойкий ответ достигается только при низком уровне репликации HBV. Миалгии послужили причиной прекращения лечения у 47% больных.
Аналоги нуклеозидов не обладают собственной активностью против HBV и активируются энзимами, находящимися в клетках. Эти энзимы высокоспецифичны для каждого вида хозяина (человек или животное), каждого типа клетки и каждой стадии клеточного цикла. Это обусловливает трудности в сравнении данных экспериментальных исследований, проведённых, например, на культуре клеток животных, инфицированных гепаднавирусами, с данными, полученными при обследовании людей. Видовые особенности также могут обусловливать различия в токсичности этих соединений.
Новые пероральные аналоги нуклеозидов включают фиалуридин, ламивудин и фамцикловир. Профиль токсичности определяется их сродством к митохондриальной и ядерной ДНК. Если преобладает сродство к ядерной ДНК, то токсичность проявляется в течение нескольких недель. Однако если превалирует сродство к митохондриальной ДНК, симптомы токсического действия появляются лишь через несколько месяцев от начала лечения. Это можно объяснить большим функциональным резервом митохондрий и значительным количеством копий ДНК, приходящихся на одну митохондрию. Тяжёлые проявления токсического синдрома включают миопатию, невропатию, панкреатит, нарушения функции печени и лактацидоз.
В предварительном исследовании выявлены хорошие результаты лечения фиалуридином со значительным снижением уровня HBV-ДНК. Однако долгосрочное исследование было обоснованно приостановлено в связи с развитием тяжёлой митохондриальной токсичности и летальными исходами у добровольцев.
Ламивудин ингибирует обратную транскриптазу, необходимую для транскрипции прегенома HBV-PHK в HBV-ДНК. Лечение в дозах 100-300 мг/сут в течение 12 нед даёт обнадеживающие результаты. HBV-ДНК исчезает. Контролированные исследования в настоящее время продолжаются. Особое внимание должно уделяться возможной митохондриальной токсичности. Отмена препарата может сопровождаться обострением гепатита.
Ламивудин и фамцикловир применялись для предотвращения реинфицирования после трансплантации у HBV-ДНК-положительных больных циррозом печени.

Кортикостероиды усиливают репликацию вируса, а после их отмены отмечается «иммунный рикошет» в виде падения концентрации HBV-ДНК. После кортикостероидов назначают полный курс лечения интерфероном. Но тяжёлым больным его не назначают, так как усиление иммунного ответа может приводить к печёночно-клеточной недостаточности. Более того, контролированное исследование, сравнивающее монотерапию интерфероном с лечением преднизолоном с последующим назначением интерферона, не выявило преимуществ комбинированной терапии. Однако у больных с исходной активностью сывороточных трансаминаз менее 100 МЕ/л добавление к лечению преднизолона улучшало его результаты.

Специфические мутации core-протеина препятствуют осуществлению Т-клетками своей функции при более поздней стадии хронической HBV-инфекции и способны снизить эффективность лечения интерфероном. Эти мутации развиваются на протяжении заболевания и влияют на способность иммунного распознавания организмом хозяина. Данные некоторых исследований о связи мутаций с плохим ответом на интерферон противоречивы и не подтверждены в других исследованиях. Появление рге-core-мутантов на фоне терапии обычно предвещает неудачу в попытках избавления от вируса, но изменения в core-области не влияют на исход заболевания в целом. Pre-core-мутанты могут обусловить тяжёлые рецидивы HBV-инфекции после трансплантации печени.
- Благоприятные
- Женский пол
- Гетеросексуальность
- Приверженность лечению
- Малая давность инфекции
- Высокая активность трансаминаз сыворотки
- Наличие гистологических признаков активности
- Низкий уровень HBV-ДНК
- Неблагоприятные
- Гомосексуализм
- ВИЧ-инфекция
- Давнее инфицирование
- Восточное происхождение
При наблюдении в течение 3-7 лет за 23 больными, ответившими на лечение интерфероном, обострение выявлено у 3, в то время как 20 оставались HBeAg-отрицательными и бессимптомными, а 13 стали HBsAg-отрицательными.

Для этих больных характерны более пожилой возраст и более поздняя стадия заболевания печени. Специфического лечения для этой категории больных нет, оно в основном симптоматическое и включает весь комплекс известных средств. Урсодезоксихолевая кислота — безопасная, нетоксичная гидрофильная жёлчная кислота — ослабляет действие токсичных жёлчных кислот, задерживающихся у больных с гепатоцеллюлярным поражением. В суточной дозе 500 мг она снижает активность сывороточных трансаминаз у больных с хроническим гепатитом. В некоторых случаях выявляются анти-НВе, но при наличии в сыворотке HBV-ДНК.
HBsAg-положительные больные, страдающие хроническим гепатитом или циррозом, особенно мужчины старше 45 лет, регулярно должны проходить профилактическое обследование с целью раннего выявления гепатоцеллюлярной карциномы, когда возможна резекция печени. Исследование сывороточного а-фетопротеина и ультразвуковое исследование проводят с 6-месячными интервалами
источник
Целью проведения противовирусной терапии хронического гепатита В служит профилактика развития цирроза печени, печеночной недостаточности и печеночно-клеточного рака. Не у всех пациентов хронический вирусный гепатит В приводит к этим исходам, а если приводит, то спустя несколько десятилетий после манифестации заболевания. Именно поэтому для оценки эффективности проводимой терапии используются более удобные для измерения конечные точки, в число которых входят подавление репликации вируса, исчезновение е-антигена вируса гепатита В (HBeAg), исчезновение поверхностного антигена гепатита В (HBsAg), нормализация активности аланинаминотрансферазы (AЛT) и улучшение гистологической картины печени [1, 2]. Результаты исследований, в которых приняли участие пациенты, не получающие терапию, свидетельствуют о стойкой активной репликации вируса гепатита В или воспалении печени, что отражает высокий уровень репликации ДНК вируса гепатита В в сыворотке крови, повышение активности AЛT и выявление HBeAg. Все это указывает на повышенный риск прогрессирования патологии [3—7]. Таким образом, при определении показаний для проведения терапии по поводу хронического вирусного гепатита В необходимо отталкиваться от уровня репликации вируса, а также активности и стадии патологических изменений в печени [1,8—10]
В течение последнего десятилетия число препаратов, зарегистрированных для лечения гепатита В, выросло с 1 (интерферон) до 7, в число которых вошли 5 пероральных аналогов нуклеотидов (нуклеозидов) и 2 интерферона — стандартный и пегилированный (пегИФН). Доступность лекарственных средств с мощной противовирусной активностью, безопасных для применения у пациентов с циррозом и печеночной недостаточностью, расширила возможности врачей при назначении курса лечения гепатита В. Это в свою очередь привело к снижению числа пациентов с вирусным гепатитом В, включенных в лист ожидания на трансплантацию печени [11], а также увеличило среднюю продолжительность жизни таких больных [12]. Но несмотря на это остается еще много вопросов, точные ответы на которые не найдены: 1) когда начинать лечение, 2) какой препарат назначать первым и 3) когда можно отменить терапию. В настоящей статье рассматривается начальная терапия заболевания. Лечение пациентов с устойчивостью к противовирусным препаратам описывается в публикации Локарнини (Locarnini S.) в журнале «Clinics in Liver Disease» № 14, 2010.
Решение о начале проведения противовирусной терапии пациентам с жизнеугрожающим состоянием печени, связанным с вирусным гепатитом В, у которых предполагаемая польза от действия лекарственных средств существенно преобладает над риском для здоровья, не представляет затруднений. Сложнее принять такое решение на ранней стадии этого заболевания, поскольку современные лекарственные препараты не приводят к эрадикации вируса и большинству пациентов требуется многолетняя, а иногда и пожизненная терапия с целью предупреждения неблагоприятных клинических исходов. На схеме 1 приведены показания для назначения терапии вирусного гепатита В.
У пациентов с жизнеугрожающей патологией печени, такой как острая печеночная недостаточность, декомпенсированный цирроз печени или тяжелое обострение хронического гепатита В, решение о начале терапии является очевидным. Несмотря на отсутствие рандомизированных контролируемых клинических исследований противовирусной терапии в подобных условиях, ее положительные эффекты ранее были продемонстрированы в когортных исследованиях и сериях клинических случаев [13, 14]. Эти исследования показали, что противовирусная терапия обеспечивает стабилизацию функции печени, позволяя пациентам дождаться трансплантации органа. В некоторых случаях функция печени улучшается до уровня, позволяющего вычеркнуть таких пациентов из листа ожидания на трансплантацию. У пациентов, которым предстоит трансплантация печени, снижение уровня ДНК вируса гепатита В до операции также уменьшает риск развития рецидива гепатита после трансплантации органа.
Пациенты с жизнеугрожающим повреждением печени должны получать противовирусную терапию независимо от уровня ДНК вируса гепатита В в сыворотке и активности АЛТ. При этом лечение должно быть назначено как можно раньше, поскольку для достижения благоприятного клинического эффекта может потребоваться от 3 до 6 мес [14].
У пациентов с компенсированным циррозом существует риск развития декомпенсации функций печени или печеночно-клеточного рака. Ключевое двойное слепое рандомизированное плацебо-контролируемое клиническое исследование действия ламивудина у пациентов с мостовидным фиброзом или циррозом и высоким уровнем репликации вируса гепатита В [положительный HBeAg и/или сывороточный уровень ДНК вируса 700 ООО копий/мл (примерно 140 ООО МЕ/мл)] показало, что терапия ламивудином значимо снижает риск прогрессирования болезни, определенного как повышение оценки по шкале Чайлд—Пью (Child-Turcotte-Pugh) на 2 балла и более, начало клинической декомпенсации или развитие печеночно-клеточного рака [15]. Значимая разница в первичной конечной точке между опытной и контрольной группами (7,8 против 17,7%; наблюдалась в среднем через 32,6 мес, что послужило причиной для независимого комитета по безопасности и мониторингу данных рекомендовать прекращение исследования. В данном исследовании также была обнаружена значимая разница между группами по частоте развития печеночноклеточного рака (3,9 против 7,4%; р=0,047).
Схема 1. Показания для назначения лечения вирусного гепатита В [1]
Лечение однозначно показано:
- Острая печеночная недостаточность
- Цирроз или клинические осложнения гепатита В
- Выраженный фиброз с высоким уровнем ДНК вируса гепатита В в сыворотке крови
- Положительный HBsAg у пациента с запланированной химио- или иммуносупрессивной терапией
Лечение может быть показано:
- HBeAg-положительный или отрицательный хронический гепатит В с активным течением
Лечение обычно не показано:
- HBeAg-положительный хронический гепатит В в фазе иммунотолерантности
- HBeAg-отрицательный хронический гепатит В в фазе неактивного носительства
Полученные данные стали основанием для многих экспертов рекомендовать противовирусную терапию всем пациентам с компенсированным циррозом. Однако благоприятные эффекты противовирусной терапии на клинические исходы у пациентов с компенсированным циррозом и низким уровнем ДНК вируса гепатита В в сыворотке доказаны не были. Согласно клиническим рекомендациям Американской ассоциации по изучению заболеваний печени (AASLD, Association for the Study of Liver Diseases), противовирусную терапию должны получать пациенты с компенсированным циррозом и уровнем ДНК вируса гепатита В в сыворотке выше 2000 МЕ/мл [8]. Такая низкая граница сывороточного уровня ДНК гепатита В была выбрана в связи с тем, что недавно полученные данные свидетельствовали в пользу связи стойкого повышения уровня ДНК вируса гепатита В с ростом процента смертности, обусловленного развитием патологии печени и печеночно-клеточного рака. При этом риск повышается в случае, если сывороточный уровень ДНК вируса гепатита В превышает 10 000 копий/мл (-2000 МЕ/мл) [5, 6].
В течении хронического вирусного гепатита В, как правило, выделяют 4 фазы (хотя не у всех пациентов развиваются все фазы, и продолжительность каждой из них существенно варьирует у разных людей) [16]. Пациентам без выраженного фиброза противовирусная терапия рекомендуется только в фазе иммунного клиренса или реактивации, но не в фазе иммунотолерантности или неактивного носительства. Решение о начале терапии основывается на репликации вируса гепатита В и активности или стадии патологии печени с коррекцией на возраст пациента, статус по HBeAg и другие факторы, такие как мнение самого пациента (рис. 1, 2) [17].
Рис. 1. Алгоритм терапии пациентов с HBeAg-положительным гепатитом В Здесь и на рис. 2: AJIT — аланинаминотрансфераза; ВГВ — вирус гепатита В; ВГН — верхняя граница нормы.
Рис. 2. Алгоритм терапии пациентов с HBeAg-отрицательным гепатитом В
Фаза иммунотолерантности характеризуется наличием HBeAg, нормальной активностью AJIT и высоким уровнем ДНК вируса гепатита В в сыворотке. В этой фазе проведение противовирусной терапии не рекомендуется, поскольку у большинства пациентов выявляется небольшое воспаление с незначительным фиброзом или без такового [18, 19]. Кроме того, исследования показали, что у пациентов, остающихся в этой фазе, клинические исходы, равно как и прогрессирование фиброза, выявляются редко [ 18,20]. Еще одной причиной отсрочки назначения противовирусной терапии служит ее низкая эффективность в этой фазе. Большинство исследований показало, что индуцированная терапией (интерферон и аналог нуклеоз(т)ида) сероконверсия у пациентов с нормальной или несколько повышенной (в 1—2 раза выше верхней границы нормы) активностью AJIT встречается редко ( Фаза иммунного клиренса или типичный HBeAg-положительный гепатит
Фаза иммунного клиренса характеризуется наличием HBeAg, высоким/флуктуирующим уровнем ДНК вируса гепатита В в сыворотке, персис-тирующим или интермиттирующим повышением активности АЛТ и наличием признаков некроза и воспаления на биоптате печени. У некоторых пациентов отмечается спонтанная сероконверсия по HBeAg, при этом заболевание переходит в фазу неактивного носительства после короткой фазы иммунного клиренса. У некоторых пациентов могут выявляться повторяющиеся обострения гепатита с прогрессированием в цирроз или декомпенсация функции печени, развивающиеся на фоне фазы иммунного клиренса. Таким образом, согласно клиническим рекомендациям, пациенты в фазе иммунного клиренса должны находиться под наблюдением врача в течение 3—6 мес с целью выявления спонтанной сероконверсии по HBeAg [8, 9]. Пациентам, у которых через 3—6 мес сохраняется HBeAg, а активность АЛТ в сыворотке более чем в 2 раза превышает верхнюю границу нормы, необходимо назначить противовирусную терапию. В случае обострения с развитием желтухи или декомпенсации функции печени терапию следует назначить немедленно.
Фаза неактивного носительства
Фаза неактивного носительства характеризуется отсутствием HBeAg, стойким сохранением нормальных показателей активности АЛТ и низким или неопределимым уровнем ДНК вируса гепатита В. Прогноз для пациентов в случае диагностирования фазы неактивного носительства благоприятный, особенно если эта фаза наступает в молодом возрасте, до развития необратимых повреждений печени [24]. Недавние исследования показали, что у пациентов с высокой нормальной активностью АЛТ (0,5-1 верхней границы нормы) повышен риск смерти от патологии печени по сравнению с пациентами с низкой нормальной активностью АЛТ ( Фаза реактивации или HBeAg-отрицательный хронический гепатит
Фаза реактивации характеризуется отсутствием HBeAg, периодическим или стойким повышением активности АЛТ и уровнем ДНК вируса гепатита В, который может варьировать от неопределимого до очень высокого (8—9 log10 копий/мл). У большинства пациентов отмечаются преядерные или ядерные варианты промотера, которые препятствуют или снижают продукцию HBeAg. У пациентов в этой фазе заболевание часто носит волнообразный характер. Таким образом, чтобы определить, находится ли пациент в фазе неактивного носительства или перешел в фазу реактивации, необходимо его регулярное обследование. Лечение необходимо назначать, как только появятся данные о том, что у пациента именно хронический HBeAg-отрицательный вирусный гепатит В, поскольку при этом у многих выявляются прогрессирующие повреждения печени. Стойкая спонтанная ремиссия наблюдается редко.
На время проведения терапии вирусного гепатита В могут влиять и другие факторы. Одним из них служит возраст (суррогатный показатель продолжительности инфекции). Особенно это касается пациентов с HBeAg-положительным гепатитом при нормальном или минимальном повышении активности AJIT. Еще одним важным фактором у молодых женщин служит планирование беременности. Несмотря на то что 2 зарегистрированных аналога нуклеоз(т)идов относятся к препаратам класса В (телбивудин и тенофовир), данные о безопасности проведения противовирусной терапии в I триместре беременности ограничены. В Регистре беременных, получающих антиретровирусную терапию (Antiretroviral Pregnancy Registry), с 1989 г. идет отслеживание исходов для матери и плода у женщин, получающих пероральные нуклеоз(т)иды. На июль 2009 г. были получены данные о 10 803 случаях беременности, в течение которых мать принимала пероральные аналоги нуклеоз(т)идов по поводу вирусного гепатита В или ВИЧ-инфекции [28]. Врожденные пороки развития у детей, контактировавших с ламивуди-ном в I триместре беременности, были выявлены в 2,9% случаев (96 из 3314), а у детей, контактировавших с тенофовиром — в 2,4% случаев (18 из 756). Эти показатели сопоставимы с таковыми в контрольной популяции. Однако зарегистрированы были только данные о живорожденных. Частота спонтанных абортов и влияние контакта с нуклеоз(т)идами на рост и развитие ребенка изучены не были.
Данные о риске развития врожденных пороков, связанных с энтекавиром, адефовиром и телбивудином, ограничены по причине малого числа зарегистрированных живорожденных. Противовирусная терапия рекомендуется женщинам с жизнеугрожающей патологией печени и компенсированным циррозом с высоким уровнем ДНК вируса гепатита В в сыворотке. Для пациенток без выраженного фиброза решение о назначении противовирусной терапии должно приниматься с учетом планируемой беременности, ожидаемой продолжительности терапии и вероятности спонтанного улучшения. Так, например, у пациенток с HBeAg-положительным гепатитом с минимальным повышением активности AЛT можно отложить терапию по причине благоприятного краткосрочного прогноза и необходимости проведения многолетней терапии для достижения сероконверсии по НBeAg. Все пациентки должны находиться под наблюдением для своевременного начала терапии в случае более активного течения гепатита.
В некоторых исследованиях сообщается о семейной группировке случаев печеночно-клеточного рака. Между тем, какие факторы — генетические, вирусные или факторы окружающей среды — вносят вклад в семейную группировку печеночноклеточного рака и как оценить его риск в случае семейного анамнеза, неизвестно. Несмотря на то что назначение противовирусной терапии пациентам с хроническим гепатитом В и семейным анамнезом печеночно-клеточного рака представляется обоснованным, нет данных в поддержку благоприятных клинических эффектов такого подхода у пациентов, в остальном не отвечающих критериям назначения терапии.
У пациентов с хроническим гепатитом В, получающих иммуносупрессивную терапию или химиотерапию по поводу других заболеваний, есть риск обострения гепатита по причине реактивации репликации вируса гепатита В [29]. Профилактическая противовирусная терапия рекомендуется всем пациентам с HBsAg-положительным гепатитом, нуждающимся в долгосрочной иммуносупрессивной терапии. Реактивация репликации вируса гепатита В также возможна у пациентов с HBsAg-отрицательным гепатитом, но наличием антител к ядерному антигену вируса (анти-НВс антитела). Однако риск при этом существенно ниже [30]. Несмотря на ограниченность данных, большинство экспертов рекомендуют проведение профилактической противовирусной терапии пациентам с HBsAg-отрицательным, анти-НВс-положительным гепатитом, которым предстоит терапия высокого риска (химиотерапия по поводу злокачественных гематологических заболеваний или трансплантации костного мозга; назначение ри-туксимаба по любой причине; долгосрочная терапия глюкокортикоидами).
Как только принято решение о начале терапии, следующий вопрос, на который необходимо ответить, — какой препарат назначить. Решение об использовании аналога нуклеоз(т)ида или интерферона основывается на характеристиках и предпочтениях пациента. В табл. 1 представлены все «за» и «против» терапии интерфероном и аналогами нуклеоз(т)идов. Терапия интерфероном не рекомендуется пациентам с декомпенсацией функций печени, иммуносупрессией либо соматическими или психиатрическими противопоказаниями. Основным преимуществом интерферона служит ограниченная продолжительность его назначения. Интерферон также характеризуется более высокой частотой случаев исчезновения HBsAg, хотя этот положительный эффект преимущественно наблюдается у пациентов, инфицированных вирусом с генотипом А. В некоторых исследованиях было обнаружено что сероконверсия по HBeAg, вызванная интерфероном, более продолжительна, чем вызванная нуклеозидом, но прямые сравнения не проводились. Основными недостатками интерферона служат необходимость парентерального назначения и высокая частота развития побочных эффектов. Нуклеоз(т)идные аналоги назначают внутрь и отличаются очень хорошей переносимостью. Тем не менее в случае их отмены нередко развиваются обострения, что требует проведения длительной терапии, а это чревато развитием устойчивости к противовирусным препаратам.
Таблица 1. Сравнительная характеристика терапии интерфероном-а и аналогами нуклеоз(т)идов
| Терапия | ИФН-а | Аналоги нуклеоз(т)идов |
| Путь введения | Подкожный | Пероральный |
| Продолжительность терапии | Ограниченная (12 мес) | От нескольких лет до пожизненной |
| Противовирусная активность | Средняя | Сильная, зависит от препарата |
| Исчезновение HBsAg | 1-3% через 1 год | 0-1% через 1 год, варьирует в зависимости от препарата |
| Устойчивость | Нет | 0-25% через 1 год |
| Побочные эффекты | Частые | Редкие |
Терапия аналогами нуклеоз(т)идов
Аналоги нуклеоз(т)идов, назначаемые при гепатите В, делятся на 3 группы: L-нуклеозиды, включая ламивудин и телбивудин; нециклические фосфонаты нуклеозидов, включая тенофовир и адефовир; и аналоги дезоксигуанозина, включая энтекавир. Мутации, возникающие в результате применения препарата одной группы, приводят, по крайней мере, к некоторой устойчивости организма к другим препаратам этой группы, в некоторых случаях снижая чувствительность и к препаратам других групп. Выбор лекарственного средства для начальной терапии должен основываться на противовирусной активности и риске развития устойчивости к препарату. В табл. 2 приводится сравнение частоты ответа, а также устойчивости организма к 5 зарегистрированным аналогам нуклеоз(т)идов. Энтекавир, телбивудин и тенофовир обладают более мощной противовирусной активностью, несколько меньше у ламивудина и затем адефовира. Энтекавир и тенофовир имеют более высокий генетический барьер развития устойчивости (частота развития устойчивости к препарату ниже), затем следуют адефовир, телбивудин и ламивудин. Гистологическим улучшением считали снижение оценки по шкале некроза и воспаления на >2 балла и отсутствие ухудшения по шкале фиброза.
Все 5 зарегистрированных аналогов нуклеоз(т)идов характеризуются хорошей переносимостью, но, как и при использовании других аналогов нуклеоз(т)идов, существует потенциальный риск развития митохондриальной токсичности и лактат-ацидоза. О необходимости сохранять бдительность свидетельствует недавнее изъятие с рынка клевудина, в число побочных действий которого вошли митохондриальная токсичность и мио-патии [31, 32]. Нефротоксическое действие адефовира и тенофовира было выявлено у 3% пациентов через 3—5 лет непрерывного назначения [33, 34]. При этом наблюдалось развитие дисфункции почечных канальцев, синдром Фанкони (Fanconi). Применение телбивудина на протяжении более чем 3 лет сопровождалось миалгией/миозитом и периферической нейропатией у 1,4 и 0,28% пациентов соответственно. Риск развития периферической нейропатии существенно возрастал у пациентов, получавших комбинированную терапию телбивудином и пегинтерфероном (18,75%) [35, 36]. Недавнее исследование показало, что назначение энтекавира пациентам с декомпенсацией функций печени сопровождается высокой частотой развития лактат-ацидоза [37].
Аналоги нуклеоз(т)идов наилучшим образом подходят пациентам с декомпенсацией функции печени, противопоказаниями к назначению интерферона и пациентам, согласным на длительный прием препарата. Из 5 зарегистрированных препаратов наилучшим профилем эффективности, безопасности и лекарственной устойчивости обладают энтекавир и тенофовир. Энтекавир предпочтительнее назначать пациентам с повышенным риском развития почечной недостаточности, а тенофовир — молодым женщинам (в том числе желающим забеременеть), а также пациентам, получавшим в прошлом ламивудин. Ламивудин и телбивудин не следует назначать при проведении первой линии терапии по причине высокой частоты лекарственной устойчивости. Адефовир практически полностью вытеснен тенофовиром из-за слабой противовирусной активности.
Интерферон противопоказан пациентам с декомпенсированным циррозом печени по причине риска развития тяжелого сепсиса и прогрессирования печеночной недостаточности [38, 39]. Также не рекомендуется назначать его пациентам с тяжелыми обострениями хронического вирусного гепатита В, острой печеночной недостаточностью и пациентам, получающим имму-носупрессивную или химиотерапию. Интерферон можно назначать пациентам с компенсированным циррозом, нормальной синтетической функцией печени и отсутствием признаков портальной гипертензии. В крупном регистре клинических исследований пегИФН-а2а наблюдались всплески повышения активности АЛТ (>5 раз выше верхней границы нормы), которые не приводили к печеночной декомпенсации, несмотря на то что у 18% пациентов с Н BeAg-положительным и 31% пациентов с HBeAg-отрицательным гепатитом, получавших монотерапию пегИФН, был выявлен выраженный фиброз или компенсированный цирроз [40, 41].
Таблица 2. Частота ответа на терапию зарегистрированными препаратами НВеАд-положительного и НВеАд-отрицательного гепатита В* [2]
Примечание. ВГВ — вирус гепатита В; * — биопсию печени выполняли на 24-й неделе после прекращения терапии; ** — временная точка, в которой оценивали ответ в годах; * * * — оценку проводили после отмены терапии.
В нескольких исследованиях проводилось изучение прогностических факторов положительного ответа на терапию пегилированным интерфероном с целью более точного выбора группы пациентов. В ретроспективном анализе обобщенных данных о 721 пациенте, включенном в 2 исследования пегИФН 111 фазы, прогностическими факторами положительного ответа на терапию у пациентов с Н Be Ag-положительным гепатитом были высокая активность AJ1T, низкий уровень ДНК вируса гепатита В, женский пол, более пожилой возраст и отсутствие предшествующей терапии интерфероном. Наилучшие исходы были достигнуты у пациентов, инфицированных вирусом с генотипом А, высокой активностью AJ1T или низким уровнем ДНК вируса, а также пациентов, инфицированных вирусами генотипа В или С с высокой активностью AJIT и низким уровнем ДНК вируса [42].
Интерферон отличается от аналогов нуклеоз-(т)идов тем, что он обладает иммуномодулирую щим и противовирусным эффектом, что может обеспечивать более высокую частоту исчезновения HBsAg и более продолжительную вирусную супрессию [42, 43]. Спустя 3 года после лечения у 28% пациентов с HBeAg-отрицательным гепатитом, получавших пегИФН, уровень ДНК вируса гепатита В составил 10 000 копий/мл и менее против 15% пациентов, получавших лами-вудин (/7=0,039). Кроме того, у 8,7% пациентов, получавших пегИФН, было выявлено исчезновение HBsAg. В группе ламивудина подобный эффект не был достигнут ни у одного из пациентов [43].
Эти данные свидетельствуют о том, что лучшими кандидатами для терапии интерфероном служат молодые пациенты без сопутствующих соматических или психиатрических заболеваний, отказывающиеся от длительного приема препаратов. У пациентов с HBeAg-положительным гепатитом следует учитывать генотип вируса и назначать интерферон в случае, если выявлен генотип А [42].
Комбинированная терапия была предложена на случай развития аддитивной или синергичной противовирусной активности, а также в целях профилактики развития устойчивости к противовирусным препаратам. В большинстве клинических исследований комбинированной терапии в качестве аналога нуклеоз(т)идов применяли ламиву-дин. Результаты исследований показали, что комбинация ламивудина ни с пегИФН, ни с другими аналогами нуклеоз(т)идов не имеет явного преимущества над монотерапией в отношении скорости и степени вирусной супрессии. Основным преимуществом этих комбинаций служит снижение частоты развития устойчивости к ламивудину. Устойчивость к энтекавиру или тенофовиру при проведении монотерапии возникает редко.
Комбинация пегИФН и аналога нуклеоз(т)ида
По сравнению с монотерапией пегИФН добавление ламивудина приводило к более выраженной вирусной супрессии.
>Но это преимущество не сохранялась после прекращения терапии [40, 41, 44]. Комбинация пегИФН и ламивудина также сопровождалась более низкой частотой развития устойчивости к ламивудину по сравнению с монотерапией лами-вудином, при этом устойчивость к ламивудину не наблюдалась у пациентов, прошедших курс монотерапии пегИФН. Клиническое исследование комбинированной терапии пегИФН и телбивудином было прекращено по причине более высокой частоты развития периферической нейропатии. В настоящее время продолжаются клинические исследования комбинированной терапии пегИФН и энтекавиром с одновременным или этапным назначением 2 препаратов и различной продолжительностью приема энтекавира.
Комбинированная терапия нуклеоз(т)идами
Все зарегистрированные в настоящее время пероральные препараты, назначаемые для лечения гепатита В, действуют на полимеразу вируса. Кроме того, мутации, вызывающие устойчивость к одному препарату, могут также повлиять на развитие устойчивости к другим. Проведенные до настоящего времени клинические исследования комбинированной терапии аналогами нуклеоз(т)идов показали отсутствие аддитивной или синергичной противовирусной активности и снижение (но не полное исчезновение) устойчивости к ламивудину.
Исследование II фазы, сравнивающее действие комбинации телбивудина и ламивудина с монотерапией телбивудином или ламивудином, показало, что комбинированная терапия обладала такой же или меньшей эффективностью, чем монотерапия телбивудином [45]. Такой результат, вероятно, обусловлен тем фактом, что телбивудин и ламиву-дин представляют собой L-нуклеозиды и мутации против одного препарата вызывают перекрестную устойчивость к другому.
В другом исследовании сравнивалось действие комбинации ламивудина и адефовира с монотерапией ламивудином. В исследование вошло 115 пациентов с HBeAg-положительным гепатитом [46]. Начальное снижение уровня ДНК вируса гепатита В в сыворотке между группами не отличалось. На 104-й неделе исследования доля пациентов с неопределимым уровнем ДНК вируса гепатита В в сыворотке и сероконверсией по HBeAg также была сопоставимой. У пациентов в группе комбинированной терапии отмечалась значительно меньшая частота устойчивости к ламивудину (15%), чем в группе монотерапии ламивудином (43%). Высокая частота устойчивости к ламивудину в группе комбинированной терапии была неожиданной и, вероятно, связана со слабой противовирусной активностью адефовира.
Наблюдение пациентов в ходе терапии позволяет оценить ответ на лечение, переносимость препарата и приверженность лечению. Все пациенты во время проведения терапии и, по крайней мере, в течение 24 нед после ее отмены должны находиться под пристальным наблюдением врача на случай возможного обострения гепатита (обусловленного реактивацией вируса), что требует немедленного возобновления лечения. Долгосрочное наблюдение необходимо для выявления поздних обострений, оценки продолжительности ответа и частоты исчезновения HBsAg. Наблюдение на предмет печеночно-клеточного рака должно проводиться в соответствии с клиническими рекомендациями даже у пациентов с сохраняющейся на фоне терапии вирусной супрессией или стойким вирусологическим ответом после ее отмены.
Пациенты, получающие пегилированный интерферон, должны проходить клинический осмотр с интервалом раз в 12—24 нед. Общий анализ крови и функциональные печеночные тесты следует выполнять сначала каждые 4, а затем каждые 4—12 нед. Каждые 12 нед следует определять уровень ДНК вируса гепатита В в сыворотке. Уровень тиреоидных гормонов контролируют каждые 12 нед во время лечения и каждые 24 нед после его прекращения. Наличие HBeAg и анти-НВе антител необходимо определять каждые 12—24 нед у пациентов с HBeAg-положительным гепатитом. Наличие HBsAg контролируют каждые 24—48 нед. Ретроспективный анализ пациентов, получавших пегИФН, показал, что снижение титра HBsAg в первые 12—24 нед служит прогностическим фактором долгосрочной вирусной супрессии и исчезновения HBsAg [47]. Аналогично снижение титра HBeAg служило прогностическим фактором его исчезновения для пациентов, у которых HBeAg до начала лечения не выявлялся [48]. Эти данные свидетельствуют о том, что контроль титра HBeAg или HBsAg может помочь в оценке продолжительности терапии и выявлении пациентов с низкой вероятностью выявления положительного эффекта в случае дальнейшего применения интерферона. Однако данное предположение требует дополнительных исследований.
Пациенты, получающие терапию аналогами нуклеоз(т)идов, должны проходить клинический осмотр каждые 24 нед, при этом подчеркивается необходимость приверженности терапии. Уровень ДНК вируса гепатита В и активность AJIT в сыворотке следует контролировать через 12 и 24 нед и затем каждые 12—24 нед. У пациентов с субопти-мальным вирусологическим ответом может быть получен положительный эффект в случае добавления второго препарата. Такой подход основан на опыте применения ламивудина и телбивудина — препаратов, характеризующихся более высокой частотой развития устойчивости к ним. Между тем применимость такой стратегии и критерии субоп-тимального ответа у пациентов, получающих энте-кавир или тенофовир, не установлены. Определение HBeAg и анти-НВе антител следует проводить каждые 24—48 нед у пациентов с HBeAg-положительным гепатитом до начала лечения. У пациентов с HBeAg-отрицательным гепатитом уровень HBsAg необходимо контролировать ежегодно. У пациентов, получающих адефовир или тенофовир, необходимо контролировать уровень сывороточного креатинина каждые 24 нед (или чаще, если речь идет о пациентах более старшего возраста или повышенном риске развития почечной недостаточности).
В идеале противовирусную терапию следует проводить до исчезновения HBsAg. Однако вероятность этого события низка и составляет около 3—5% через 3—5 лет терапии аналогами нуклеоз(т)идов и 5—10% через 5 лет проведения курса терапии пегилированным интерфероном.
ПегИФН назначают ограниченным курсом, поскольку его иммуномодулирующие эффекты могут сохраняться и после прекращения терапии. На основании результатов клинических исследований III фазы рекомендуемая продолжительность терапии составляет 48 нед для пациентов с HBeAg-положительным и HBeAg-отрицательным гепатитом. В настоящее время проводятся исследования, которые позволят установить, достаточно ли более короткого курса терапии для пациентов с HBeAg-положительным гепатитом и такими «смягчающими обстоятельствами», как вирус с генотипом А, высокая активность AJIT и низкий уровень ДНК вируса гепатита В. Недавние исследования показали, что мониторинг титра HBsAg позволяет выявить популяцию пациентов с медленным ответом, у которых может быть получен положительный эффект от более длительной терапии, а также пациентов, не отвечающих на лечение, продолжение которого становится бесполезным. Но данный подход все еще требует подтверждения данными новых исследований.
Аналоги нуклеоз(т)идов назначают до достижения желаемой конечной точки. Пациентам с декомпенсированным циррозом рекомендуется пожизненная терапия в виду риска развития фатального обострения после ее отмены. Пациентам с компенсированным циррозом некоторые эксперты также рекомендуют проведение пожизненной терапии. Учитывая данные, указывающие на обратное развитие фиброза или цирроза у пациентов с сохраняющейся после 3—5 лет проведения противовирусной терапии вирусной супрессией, можно рекомендовать прекращение терапии пациентам с подтвержденным обратным развитием цирроза и исчезновением HBsAg (при условии тщательного наблюдения и возможности немедленного возобновления терапии в случае биохимического или клинического обострения).
Согласно клиническим рекомендациям Американской ассоциации по изучению заболеваний печени (AASLD, Association for the Study of Liver Diseases), у пациентов с HBeAg-положительным гепатитом без прогрессирующего цирроза лечение следует продолжать до достижения сероконвер-сии по HBeAg (HBeAg-отрицательный, анти-НВе антитела положительные, ДНК вируса гепатита В в сыворотке не определяется) и прекращать только после 6 мес проведения дополнительной терапии [8]. Многие эксперты подвергают сомнению валидность использования сероконверсии по HBeAg в качестве терапевтической конечной точки, ссылаясь на то, что у некоторых пациентов сохраняется виремия после сероконверсии по HBeAg, а после прекращения лечения до 50% пациентов вновь становятся HBeAg-положительными. Эти аргументы указывают на то, что многие пациенты переходят в фазу неактивного носительства и остаются в ней месяцами, годами и десятилетиями после сероконверсии по HBeAg. Таким образом, прекращение терапии у пациентов, завершивших консолидацию терапии после достижении сероконверсии по HBeAg, имеет смысл только в том случае, если они продолжают наблюдаться.
Для пациентов с HBeAg-отрицательным гепатитом без прогрессирования в цирроз терапевтическая конечная точка не установлена. Обострение нередко возникает у пациентов, завершивших 2-летний курс терапии с неопределимым уровнем ДНК вируса гепатита В в сыворотке, наблюдавшемся на протяжении по крайней мере 1 года [49]. Предварительные данные, полученные в одном небольшом исследовании, указывают на то, что среди 33 пациентов, прекративших терапию адефовиром (через 4—5 дет, с неопределимым уровнем ДНК вируса гепатита В, по крайней мере, в течение 3 лет) у 18 отмечалась стойкая клиническая ремиссия, а у 9 исчез HBsAg на протяжении в среднем 5 лет после отмены терапии [50]. При этом у всех пациентов вскоре после прекращения лечения отмечался вирусологический рецидив. Но в ходе последующего наблюдения (после отмены терапии) уровень ДНК вируса гепатита В в сыворотке снижался до низкого или неопределимого. Для подтверждения этих данных и выявления прогностических факторов развития стойкой клинической ремиссии необходимо проведение дополнительных исследований. Эта информация может помочь в выборе пациентов, которым можно прекратить терапию, что избавит их от необходимости пожизненного приема препаратов.
источник
 В редких случаях наблюдается вертикальный путь передачи инфекции, который регистрируется при родах.
В редких случаях наблюдается вертикальный путь передачи инфекции, который регистрируется при родах.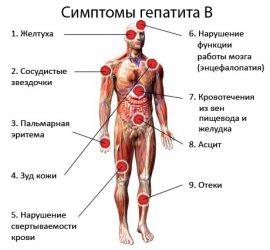 Негативный хронический интегративный гепатит В. Это неактивная фаза заболевания, которая, как правило, протекает без особых симптомов и имеет благоприятный исход. При визуальном обследовании больного каких-либо существенных изменений, например желтушности кожи, не наблюдается. Селезенка также не увеличена, анализы в норме или на высшей границе нормы. Однако практически всегда заметно увеличение печени.
Негативный хронический интегративный гепатит В. Это неактивная фаза заболевания, которая, как правило, протекает без особых симптомов и имеет благоприятный исход. При визуальном обследовании больного каких-либо существенных изменений, например желтушности кожи, не наблюдается. Селезенка также не увеличена, анализы в норме или на высшей границе нормы. Однако практически всегда заметно увеличение печени. 1 ч. л. цветков бессмертника заливают стаканом кипятка и настаивают в течение часа в термосе. Готовую жидкость фильтруют и употребляют по полстакана трижды в день после основных приемов пищи.
1 ч. л. цветков бессмертника заливают стаканом кипятка и настаивают в течение часа в термосе. Готовую жидкость фильтруют и употребляют по полстакана трижды в день после основных приемов пищи.