Этиология: вирус гепатита В (ВГВ, HBV) — ДНК-овый гепаднавирус. Белок вирусной оболочки представлен поверхностным антигеном (HBsAg) — «австралийский» АГ, нуклеокапсид содержит сердцевинный (core) антиген (HBcAg), инфекционный (HBeAg), HBxAg, ДНК и ферменты (полимеразу и протеинкиназу). Каждый из антигенов ВГВ вызывает гуморальный иммунный ответ, проявляющийся выработкой соответствующих антител (анти-HBs, анти-НВс, анти-НВе).
Эпидемиология: источник — больные как манифестными, так и бессимптомными формами острого и хронического ГВ. Механизм заражения: парентеральный; пути передачи: естественные (от матери к ребенку – вертикальный и перинатальный; при половых контактах с инфицированным человеком – половой; при других контактах с инфицированным человеком – горизонтальный) и искусственный (при нарушении целостности кожных покровов и слизистых оболочек).
Патогенез: вирусу не свойственно прямое повреждающее действие на гепатоциты, их цитолиз осуществляется иммуноопосредованно за счет реакции со стороны клеточного иммунитета через цитотоксические Т-лимфоциты.
а) инкубационный период от 42 до 180 дней, в среднем 60-120 дней.
б) начальный (преджелтушный) период— 7-14 дней; заболевание начинается с признаков смешанного варианта преджелтушного периода без значительного повышения температуры тела. Симптомы интоксикации и диспепсические проявления умеренные, у трети больных артралгический вариант начального периода (усиление болей в крупных суставах по ночам и в утренние часы). Начальный период болезни длится 7-14 дней и более, однако при заражениях, связанных с переливанием крови, он может быть короче.
в) желтушный период — 3-4 недели, более выраженная и продолжительная болезненность, иногда резкие боли в правом подреберье. Сохраняется слабость, снижение аппетита доходит до анорексии. Нередки тошнота и даже рвота. Часто зуд кожи. Печень всегда увеличена, при пальпации гладкая, с несколько уплотненной консистенцией, отмечается увеличение селезенки. Могут быть положительными желчепузырные симптомы. В периферической крови лейкопения с лимфо- и моноцитозом, иногда – с плазматической реакцией. СОЭ снижена до 2-4 мм/ч, в периоде реконвалесценции может ускоряться до 18-24 мм/ч с последующей нормализацией при отсутствии осложнений. Гипербилирубинемия более выраженная и стойкая, чем при ГА, особенно на 2-3-й неделе желтушного периода; наблюдается повышение активности аминотрансфераз в сыворотке крови при снижении сулемового теста и протромбинового индекса. При серологическом исследовании крови обнаруживаются HBsAg, анти-НВс IgM.
При тяжелом течении — признаки нарастания печеночной недостаточности и прогрессирования некротических процессов в печени – усиление общей мышечной слабости, головокружение, апатия, анорексия, тошнота, учащение рвоты, появление немотивированного возбуждения, нарушения памяти; прогрессирующее увеличение желтушной окраски кожи; уменьшение размеров печени, усиление болезненности ее края; появление геморрагического синдрома (петехиальная сыпь на коже, носовые кровотечения, кровоизлияния в местах инъекций, «дегтеобразный» стул, рвота с примесью крови); появление отечно-асцитического синдрома (отеки на стопах и нижней трети голеней, асцит); возникновение лихорадки, тахикардии, нейтрофильного лейкоцитоза; увеличение содержания общего билирубина в сыворотке крови при нарастании его непрямой фракции; уменьшение содержания холестерина ниже 2,6 ммоль/л.
г) период реконвалесценции — нормализация активности аминотрансфераз к 30-35-му дню болезни при легкой форме, при среднетяжелой – к 40-50-му, при тяжелой форме – 60-65-му дню.
Диагноз: данные анамнеза (переливание крови, операции и т.д.), клиника (постепенное начало болезни, длительный преджелтушный период, аллергические высыпания на коже, отсутствие улучшения самочувствия или его ухудшение с появлением желтухи, длительный желтушный период с медленным исчезновением симптомов заболевания в периоде реконвалесценции), серологические реакции (раннее обнаружение в крови HBsAg, HBeAg, анти-НВс IgM, а также ДНК HBV, при благоприятном течении — быстрое исчезновение сначала HBeAg с появлением анти-НВе, ДНК HBV, затем и HBsAg с появлением анти-HBs; на смену ранним анти-НВс IgM появляются поздние анти-НВс IgG).
Длительная циркуляция (более 3 мес.) в крови HBeAg, ДНК HBV, а также анти-НВс IgM и HBsAg в стабильно высоком титре свидетельствуют о затяжном течении инфекционного процесса и высокой вероятности хронизации. О возможном развитии хронического гепатита также следует думать при выявлении HBsAg в стабильном титре на протяжении 6 мес. и более от начала заболевания даже при отсутствии маркеров активной вирусной репликации (HBeAg, анти-НВс IgM, ДНК HBV), клинической симптоматики и при нормальных биохимических показателях.
Для диагностики хронизации ВГВ — пункционная биопсия.
В данном случае только результаты анализов пункционных биоптатов печени помогают установить правильный диагноз.
1. Терапия — как и при ВГА (см. вопрос 9.1.)
2. Противовирусные — альфа-интерферон (рекомбинантные: интрон А, роферон А, реальдирон и нативные: вэллферон, человеческий лейкоцитарный интерферон) при угрозе хронизации или проградиентном течении, синтетические нуклеозиды – фамцикловир (фамвир), ламивудин (эпивир), зидовудин (ретровир, азидотимидин, тимозид), ингибиторы протеазы – саквинавир (инвираза), индинавир (криксиван), индукторы интерферона – неовир (циклоферон), амиксин, иммуномодуляторы – лейкинферон, интерлейкин-1 (беталейкин), интерлейкин-2 (ронколейкин). Показаны при тяжелом течении ГВ (при наличии маркеров активной вирусной репликации) с угрозой развития острой печеночной недостаточности, особенно при появлении признаков печеночной энцефалопатии, а также при угрозе хронизации.
3. При осложнениях, связанных с энцефалопатией: купирование психомоторного возбуждения натрия оксибутиратом, седуксеном; промывания желудка (через назогастральный зонд) и высокие или сифонные клизмы для уменьшения аутоинтоксикации; пероральное применение плохо всасывающихся антибиотиков (канамицин по 0,5 г 4 раза в сутки), энтеросорбентов; дробное энтеральное питание в сочетании с парентеральным; ГКС (не менее 180-240 мг преднизолона) парентерально; инфузионная терапия; при геморрагических проявлениях — ингибиторы протеаз и фибринолиза (эпсилон-аминокапроновая кислота, контрикал, гордокс).
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Увлечёшься девушкой-вырастут хвосты, займёшься учебой-вырастут рога 9510 — 

источник
Гепатит – патология печени, распространяется разными способами, развивается в разных формах и при серьезных осложнениях приводит к смерти. Причины развития патологии – инфекция, токсины, но по статистике, у преимущественного большинства больных диагностируют вирусный гепатит или воспаление печени. Несвоевременный визит к специалисту и неоказание эффективной терапии провоцирует развитие хронической формы.
Оглавление:
- Симптомы
- Способы заражения
- Причины заболевания
- Классификация вирусных гепатитов
- Диагностика
- Биохимический анализ крови
- Поиск вирусных антигенов
- Обследования с помощью медицинского оборудования
- Лечение вирусных гепатитов в медицинском центре «Клиника К+31»
- Прогноз
- Осложнения
- Профилактика
- Питание при вирусных гепатитах
Первые серьезные симптомы гепатита начинаются после размножения вируса в достаточном количестве и его полной адаптации в организме. На это уходит от 14 дней до полугода.
До желтухи заболевание напоминает грипп:
- повышенная температура тела;
- головная боль;
- слабость.
При выявлении вируса гепатита В кожные покровы покрывает сыпь.
Развитие патологии сопровождается снижением аппетита, повышенной утомляемостью, рвотой, появляется дискомфорт в подреберье справа. Моча приобретает темный оттенок, кал светлеет. Обследование выявляет изменение размеров печени, реже заболевание затрагивает селезенку.
После симптомов желтухи состояние пациента стабилизируется. Исключением являются гепатит С и алкогольный токсический гепатит. В остальных случаях через несколько недель у пациентов наблюдается улучшение состояния.
Различают несколько степеней тяжести развития патологии:
Фульминантная или молниеносная форма заболевания сопровождается некрозом печени и приводит к смерти пациента.
Только вирусы групп В, С и D трансформируются в хроническую форму. Симптомы патологии следующие:
- усталость, проявляющаяся к концу дня;
- снижение физической активности;
- кровоточивость;
- изменение цвета мочи;
- изменение оттенка кожных покровов – характерная желтизна, вызванная повышением уровня билирубина;
- изменение размеров печени и селезенки;
- зуд;
- появление сосудистых звездочек.
Симптомы вирусных гепатитов имеют неспецифическую природу и встречаются при других патологиях. Не редко пациент даже не подозревает про болезнь, чувствуя себя здоровым. Диагностировать истинную патологию можно только на основании лабораторных исследований, которые назначит врач.
Существует два основных пути заражения гепатитом.
- Фекально-оральный для гепатита А и Е. Человек инфицируется через воду и пищу. Наиболее распространены вирусы в государствах, где наблюдаются проблемы с водоснабжением и сложно соблюдать личную гигиену.
- Попадание зараженной крови в организм для гепатита В, С, D и G.
- Переливания крови.
- Многократное использование медицинской иглы несколькими людьми.
- Незащищенные половые акты.
- Заражения в период беременности. Встречается довольно редко, наибольшую опасность вирус представляет в третьем триместре. Если у беременной выявлена ВИЧ-инфекция, вероятность инфицирования плода гепатитом составляет почти сто процентов.
- Салоны, где наносят татуировки, прокалывают уши, а также сомнительные учреждения, где проводят сеансы иглоукалывания, используя нестерильные иглы.
Примечание: в 40 % случаев заражения узнать – как передается гепатит и что стало причиной инфицирования — невозможно.
- Гепатит А – данная форма патологии встречается чаще других, известна в народе, как Болезнь Боткина. Инкубационный период – от недели до 50 дней. Самыми опасными для окружающих являются пациенты до проявления первых признаков желтухи при гепатите. Размножение вируса прекращается, когда развивается желтуха.
- Гепатит В – известен под названием Сывороточный гепатит, вирус передается через кровь. Инфицирование происходит во время интимной близости. Беременная, инфицированная гепатитом, передаст вирус ребенку. Инкубационный период – от 50 дней до полугода.
- Гепатит С – наиболее опасный вирус, известный под названием посттрансфузионный гепатит. В большинстве случаев инфицирование случается через кровь. Инкубационный период – от двух до 26 недель. Гепатит С называют «ласковым убийцей», из-за способности маскировать истинный недуг под видом менее опасных патологий. В 80 % случаев диагностики патология трансформируется в хроническую фазу и в будущем приводит к циррозу или раку печени. Именно поэтому важно своевременно выявить болезнь и провести эффективную терапию. Учитывая небольшую концентрацию вируса в крови, заражение плода в период беременности не происходит, но известны случаи передачи вируса через материнское молоко.
- Гепатит D – для размножения вируса необходим вирус гепатита В. Инкубационный период –длится до полугода. Смешанная инфекция, вызванная двумя вирусами, является причиной цирроза и смерти.
- Гепатит Е – наиболее опасен для плода во второй половине беременности. Подвержены инфицированию молодые люди в возрасте от 15 до 29 лет. В активную фазу патология переходит по окончании периода инкубации, который продолжается от двух недель до 50 дней. При условии своевременного лечения болезни прогноз благоприятный, но возможны осложнения – поражение почек и печени. Данный вирус не встречается в хронической фазе.
- Гепатит G – широкое распространение данная форма вируса получила среди наркоманов. Симптомы похожи на признаки гепатита С. Часто развивается цирроз при выявлении двух вирусов – С и G.
Диагностические мероприятия предполагают консультацию терапевта, гастроэнтеролога, а также проведение специальных исследований. Врач получает точную информацию о возбудителе патологии, течении гепатита, нарушениях в структуре, функционировании печени, сопутствующих осложнениях.
1. Определение печеночных ферментов. В результате заболевания происходит поражение тканей печени, которое сопровождается резким увеличением количества печеночных ферментов в крови.
2. Определение фракций билирубина. Резко повышается фракция билирубина – свободного и связанного. Объясняется это неспособностью печени естественным способом выводить из организма билирубин.
Биохимический анализ крови на гепатит показывает повышенное содержание холестерина и желчных кислот и снижение уровня белка. При лекарственном гепатите показатели могут быть аналогичными.
Это наиболее специфичный и точный анализ на гепатит, выявляющий возбудителя патологии и его активность. Результаты исследований основаны на выявлении вирусных частиц и антител к ним. Каждый вирус имеет определенные маркеры, по ним диагностируется патология и составляется эффективная схема терапии.
- Ультразвуковое обследование печени. Безопасная и безболезненная методика, в ходе которой определяется изменения печени и других органов, касающиеся их размеров, структуры и функционирования. Также проводится обследование сосудов и определяется оптимальное место для пункционной биопсии, если есть необходимость в таком методе диагностики.
- Пункционная биопсия. Учитывая, что УЗИ не дает полной информации о течении заболевания и его характере, часто пациенту назначают проведение пункционной биопсии. Оценка структуры печени определяется на клеточном уровне и признана наиболее точной в диагностике всех вирусов патологии. Процедура безопасна, длится 5-10 секунд. Пациенту вводят местный наркоз, при помощи иглы берут небольшой образец ткани печени. После биологический материал обследуют специалисты.
При гепатите А не требуется терапии противовирусного характера. Лечение заключается в соблюдении полупостельного режима и диетической схемы питания. Проводится терапия, направленная на устранение признаков интоксикации.
Вирусный, острый гепатит В преимущественно заканчивается полным выздоровлением. В хронической фазе полное выздоровление невозможно, но вполне возможно контролировать состояние пациента. Нужно соблюдать предписания относительно режима дня, питания, курса терапии препаратами, которые активизируют обменные процессы в печени. Противовирусная терапия необходима при клинических показаниях. Лечение интерферонами проводится только в медицинском учреждении под наблюдением врача.
Гепатит С – по статистике, у семи пациентов из десяти патология трансформируется в хроническую фазу, в будущем развиваются патологии, опасные для жизни. Главная цель терапии интерфероном-альфа – остановить заражение здоровых клеток печени. Терапия не гарантирует выздоровления, но препятствует развитию патологий, которые угрожают жизни.
После курса терапии еще нескольких месяцев нужно контролировать показания анализа крови, чтобы отреагировать на повторное проявление воспалительных процессов.
Эффективное лечение гепатита D возможно только в медицинском учреждении, назначается комплексная терапия.
Побороть вирус гепатита Е организм пациента в состоянии самостоятельно. Спустя два месяца человек выздоравливает. Курс лечения необходим для устранения неприятных симптомов болезни.
В медицинском центре «Клиника К+31» опытные врачи проведут тщательное обследование, только после этого будет назначено адекватное результатам диагностики лечение. Пациент находится под наблюдением квалифицированного, профессионального медицинского персонала. Вместе мы одолеем болезнь.
Вирус гепатитов А и Е не вызывает осложнений и проходит через несколько недель. После этого в организме формируется иммунитет.
При заболевании гепатитом В в 95 % фиксируется полное выздоровление и появляются антитела, если патология проявилась в острой форме. В остальных случаях заболевание трансформируется в хроническую фазу, пациентам в медицинском учреждении назначается поддерживающая терапия, подобранная врачом, и 10 % больных полностью выздоравливают
Только 10 % пациентов излечиваются от гепатита С, преимущественно заболевание приобретает хроническую форму. В 25 % случаях развивается цирроз или рак печени. При гепатите D прогнозы аналогичны, но осложнения протекают тяжелее.
Гепатит G приобретает хроническую форму.
- Патологии желчных путей.
- Печеночная кома опасна смертью пациента. Такое осложнение гепатита возможно при сочетании двух форм вируса – В и D.
- Цирроз.
- Злокачественная опухоль печени.
Примечание: самые серьезные осложнения гепатита, неблагоприятный прогноз врачи дают при сочетании нескольких вирусов – В и С, В и D или В, С и D.
- Профилактика гепатита – это, прежде всего, поддержание чистоты тела и окружающей обстановки.
- Мыть овощи и фрукты, употреблять хорошо приготовленные продукты.
- Свести к минимуму контакт с кровью посторонних людей. Заразиться гепатитом можно во время маникюра в салоне красоты, ведь микрочастицы крови остаются на инструментах.
- Тщательно выбирать салоны красоты, уделять пристальное внимание обработке инструментов.
- Избегать незащищенной интимной близости – это профилактика и вирусных гепатитов, и ВИЧ инфекции.
- Придерживаться специальной схемы питания.
- Вакцинация. Для защиты новорожденных от вируса первую прививку делают в роддоме. Достаточно трех вакцинаций, чтобы сформировался иммунитет.
При вирусном гепатите в острой фазе назначается специальная схема питания – стол № 5.
| Категория продуктов | Полезные | Вредные |
| Хлебобулочные изделия | Хлеб, сушки, галетное печенье | Торты, пирожные, булочки, пирожки |
| Овощи | Большинство свежих овощей можно кушать | Томаты, зеленый лук, морковь, болгарский перец, редис, чеснок, редька, грибы |
| Фрукты | Яблоки зеленых сортов, арбуз, бананы, очищенный виноград | Дыня, киви, детское питание из фруктов |
| Мясные продукты | Отварное мясо – говядина, телятина, индейка, кролик, курятина | Свинина, баранина, мясо птицы жирных сортов, колбасы, холодец |
| Молочные продукты | Творог с низким содержанием жиров, кефир, нежирные сорта сыра, молоко в составе первых блюд и каш | Сметана, сливки, творожная масса, плавленые сорта сыров |
| Первые блюда | Все супы на постных бульонах | Первые блюда на жирных бульонах |
| Сладости | Мед, сахар, варенье кроме клубничного, зефир, пастила | Особых рекомендаций нет |
| Напитки | Минеральная вода, чай, домашние соки, напитки из сухофруктов – общий объем не менее полутора литров | Томатный сок, кофе, какао, сладкие газированные напитки, магазинные соки, фруктовые воды |
| Особые рекомендации | Можно кушать отварную рыбу, каши. Ограничения установлены на сливочное масло – 40 граммов в сутки и омлет – не чаще двух раз в неделю. Запрещены: алкоголь, копчености жареные и маринованные блюда, острые пряности и консервы. | |
Примечание: приведенная диета назначается только в острой фазе. Когда гепатит трансформируется в хроническую форму, нет необходимости строго придерживаться специальной схемы в питании – запрещенные продукты разрешено употреблять не чаще одного раза в неделю.
источник
Хронический вирусный гепатит – группа инфекционных поражений печени, протекающих с воспалительными дистрофически-пролиферативными изменениями паренхимы органа. Клиническими проявлениями хронических вирусных гепатитов служат диспепсический, астеновегетативный и геморрагический синдромы, стойкая гепатоспленомегалия, нарушения функции печени. Диагностика включает определение в сыворотке маркеров гепатитов В, С, D, F и G; оценку биохимических проб печени, УЗИ печени, реогепатографию, пункционную биопсию печени, гепатосцинтиграфию. Лечение хронических вирусных гепатитов консервативное, включающее диету, прием эубиотиков, ферментов, гепатопротекторов, противовирусных препаратов.
Под хроническими вирусными гепатитами в гастроэнтерологии понимают этиологически неоднородные антропонозные заболевания, вызываемые гепатотропными вирусами (A, B, C, D, E, G), имеющие манифестное течение продолжительностью свыше 6 месяцев. Хронические вирусные гепатиты чаще встречаются в молодом возрасте и при отсутствии адекватной терапии приводят к раннему развитию цирроза, рака печени и гибели пациентов. Прогрессирование заболевания ускоряется при злоупотреблении наркотиками, алкоголем, одновременном инфицировании несколькими вирусами гепатита или ВИЧ.
Хронические гепатиты этиологически тесно связаны с острыми формами вирусных гепатитов В, С, D, Е, G, особенно протекающими в легком желтушном, безжелтушном или субклиническом варианте и принимающими затяжной характер.
Хронический вирусный гепатит обычно развивается на фоне неблагоприятных факторов – неправильного лечения острого гепатита, неполной реконвалесценции на момент выписки, отягощенного преморбидного фона, алкогольной или наркотической интоксикаций, инфицирования другими вирусами (в т. ч. гепатотропными) и т. д.
Ведущим патогенетическим механизмом при хроническом вирусном гепатите служит нарушение взаимодействия иммунных клеток с содержащими вирус гепатоцитами. При этом отмечается дефицит Т-системы, депрессия макрофагов, ослабление системы интерфероногенеза, отсутствие специфического антителогенеза в отношении антигенов вирусов, что в конечном итоге нарушает адекватное распознавание и элиминацию иммунной системой антигенов вирусов на поверхности гепатоцитов.
С учетом этиологии различают хронические вирусные гепатиты В, С, D, G; сочетания В и D, В и С и др., а также неверифицированный хронический вирусный гепатит (неясной этиологии).
В зависимости от степени активности инфекционного процесса выделяют хронические вирусные гепатиты с минимальной, слабо выраженной, умеренно выраженной, выраженной активностью, фульминантный гепатит с печеночной энцефалопатией. Минимальная степень активности (хроническая персистенция вирусного гепатита) развивается при генетически обусловленном слабом иммунном ответе, когда отмечается пропорциональное угнетение всех показателей клеточного иммунитета (Т-лимфоцитов, Т-супрессоров, Т-хелперов, Т-киллеров и др.). Низкая, умеренная и выраженная активность хронического вирусного гепатита имеет место при резком дисбалансе иммунной регуляции.
В течении хронического вирусного гепатита различают стадии:
- с отсутствием фиброза;
- с наличием слабовыраженного перипортального фиброза;
- с наличием умеренного фиброза с портопортальными септами;
- с наличием выраженного фиброза с портоцентральными септами;
- с развитием цирроза печени;
- с развитием первичной гепатоцеллюлярной карциномы.
Хронический вирусный гепатит может протекать с ведущим цитолитическим, холестатическим, аутоиммунным синдромом. Цитолитический синдром характеризуется интоксикацией, повышением активности трансаминаз, снижением ПТИ, диспротеинемией. При холестатическом синдроме преимущественными проявлениями служат кожный зуд, увеличение активности ЩФ, ГГТП, билирубина. Аутоиммунный синдром протекает с астеновегетативными явлениями, артралгиями, диспротеинемией, гипергаммаглобулинемией, повышением активности АлАТ, наличием различных аутоантител.
В зависимости от развивающихся осложнений различают хронический вирусный гепатит, отягощенный печеночной энцефалопатией, отечно-асцитическим синдром, геморрагическим синдромом, бактериальными осложнениями (пневмонией, флегмоной кишки, перитонитом, сепсисом).
Клиника хронического вирусного гепатита определяется степенью активности, этиологией заболевания, а выраженность симптоматики – сопутствующим фоном и длительностью поражения. Наиболее характерными проявлениями служат астеновегетативный, диспепсический и геморрагический синдромы, гепато- и спеномегалия. Астеновегетативные проявления при хроническом вирусном гепатите характеризуются повышенной утомляемостью, слабостью, эмоциональной лабильностью, раздражительностью, агрессивностью. Иногда отмечаются жалобы на нарушение сна, головную боль, потливость, субфебрилитет.
Явления диспепсии связаны как с нарушением нормального функционирования печени, так и с частыми сопутствующими поражениями билиарного тракта, 12-перстной кишки и поджелудочной железы, поэтому сопровождают большинство случаев хронического вирусного гепатита. Диспепсический синдром включает ощущения тяжести в эпигастрии и подреберье, метеоризм, тошноту, отрыжку, непереносимость жирной пищи, ухудшение аппетита, неустойчивость стула (склонность к поносам). Желтуха не является патогномоничным симптомом хронического вирусного гепатита; в отдельных случаях может отмечаться субиктеричность склер. Явная желтуха чаще появляется и нарастает по мере развития цирроза и печеночной недостаточности.
В половине наблюдений у больных с хроническим вирусным гепатитом отмечается геморрагический синдром, характеризующийся склонностью к кожным кровоизлияниям, носовым кровотечениям, петехиальным высыпаниям. Геморрагии обусловлены тромбоцитопенией, нарушением синтеза факторов свертываемости. У 70 % пациентов отмечается появление внепеченочных знаков: телеангиэктазий (сосудистых звездочек), пальмарной эритемы, капиллярита (расширения капилляров), усиленного сосудистого рисунка на груди.
К внепеченочным проявлениям хронического вирусного гепатита относятся миалгии и артралгии, периферическая полинейропатия, аменорея, гинекомастия, снижение либидо, поражение глаз и слюнных желез. При преобладающем аутоиммунном синдроме могут присоединяться узелковый периартериит, кардиомиопатия, антифосфолипидный синдром, дерматомиозит, гранулематоз, болезнь Такаясу, аутоиммунный гепатит, хронический гломерулонефрит, сахарный диабет и др.
При хроническом вирусном гепатите отмечается гепатомегалия: печень может выступать из-под реберной дуги на 0,5-8 см; верхняя граница определяться перкуторно на уровне VI—IV межреберий. Консистенция печени становится плотноэластической или плотной, может отмечаться повышенная чувствительность или болезненность при пальпации. У большинства пациентов также выявляется спленомегалия. Расширение вен пищевода, геморроидальных вен, развитие асцита свидетельствуют о запущенности хронического вирусного гепатита и формировании цирроза печени.
Диагноз хронического вирусного гепатита устанавливается при длительно текущем (свыше 6 месяцев) инфекционном процессе, вызванном вирусами гепатита В, С, D, F, G; наличии гепатоспленомегалии, астенического, диспепсического и геморрагического синдромов.
С целью верификации формы заболевания проводится определение маркеров вирусных гепатитов методом ИФА, обнаружение РНК вирусов с помощью ПЦР-диагностики. Из биохимических показателей функции печени наибольший интерес представляет исследование АлАт и АсАТ, щелочной фосфатазы (ЩФ), гамма-глутамилтранспептидазы (ГГТ), лецитинаминопептидазы (ЛАП), сывороточной холинэстеразы (ХЭ), лактатдегидрогеназы (ЛДГ), билирубина, холестерина и др., позволяющих судить о степени повреждения паренхимы печени при хроническом вирусном гепатите. С целью оценки состояния гемостаза производится исследование коагулограммы, определение количества тромбоцитов.
УЗИ печени позволяет увидеть изменения печеночной паренхимы (воспаление, уплотнение, склерозирование и пр.). С помощью реогепатографии изучается информация о состоянии внутрипеченочной гемодинамики. Проведение гепатосцинтиграфии показано при признаках цирроза печени.
Биопсия печени и морфологическое исследование биоптата выполняется на заключительном этапе обследования для оценки активности хронического вирусного гепатита.
В стадии ремиссии хронического вирусного гепатита необходимо придерживаться диеты и щадящего режима, проводить профилактические курсы приема поливитаминов, гепатопротекторов, желчегонных средств. Обострение хронического вирусного гепатита требует стационарного лечения.
Основу базисной терапии хронического вирусного гепатита составляет диетический стол № 5; назначение препаратов, нормализующих кишечную микрофлору (лактобактерин, бифидумбактерин, бификол); ферментов (фестал, энзистал панкреатин); гепатопротекторов (рибоксин, карсил, гептрал, эссенциале и др.). Целесообразен прием настоев и отваров, обладающих противовирусным (календула, зверобой), спазмолитическим и слабым желчегонным и действием (спорыш, мята).
При цитолитическом синдроме необходимы внутривенные инфузии белковых препаратов и свежезамороженной плазмы, проведение плазмафереза. Купирование холестатического синдрома проводится с помощью адсорбентов (активированный уголь, полифепам, билигнин), препаратов ненасыщенных жирных кислот (хенофальк, урсофальк). При аутоиммунном синдроме назначаются иммунодепрессанты, глюкокортикоиды, делагил, проводится гемосорбция.
Этиотропная терапия хронического вирусного гепатита требует назначения противовирусных препаратов: синтетических нуклеозидов (ретровир, фамвир), интерферонов (виферон, роферон А) и др.
Пациенты с хроническим вирусным гепатитом находятся на пожизненном диспансерном учете у инфекциониста-гепатолога. Неблагоприятное течение хронические вирусные гепатиты приобретают при отягощенном фоне: одновременном инфицировании несколькими вирусами, злоупотреблении алкоголя, наркотической зависимости, ВИЧ-инфекции. Исходом хронических вирусных гепатитов служит цирроз и рак печени.
Профилактика хронизации инфекционного процесса заключается в выявлении малосимптомных форм вирусного гепатита, проведении адекватного лечения и контроле за реконвалесцентами. Пациенты, перенесшие вирусные гепатиты, должны придерживаться рекомендуемой врачом диеты и образа жизни.
источник
Вирусный гепатит С — инфекционная патология, которую вызывает вирус, способный жить только в организме человека (антропонозная инфекция). Вирус гепатита C (HCV) обладает гемоконтактным путем передачи. Заболевание имеет легкое и субклиническое течение в остром периоде, с частым переходом в хроническую форму. Опасными осложнениями гепатита С являются цирроз и рак печени.
По данным Всемирной организации здравоохранения, в мире инфицировано более 200 млн человек. С каждым годом число носителей и больных гепатитом С людей увеличивается.
Вирус гепатита С относится к семейству Flaviviridae, роду Heparcivirus. В геноме вируса есть два участка, один из которых кодирует структурные белки, а другой — функциональные, обладающие свойствами для активной репликации (синтеза) HCV.
Структурные белки входят в состав наружной оболочки вируса и участвуют в проникновении HCV в клетку печени. Характерным свойством структурных белков является также участие в развитии иммунитета и ускользание от иммунного ответа организма человека на инфицирование. В участках структурных белков часто происходят мутации, из-за чего их назвали гипервариабельными.
Антитела, которые вырабатываются к белкам гипервариабельных регионов оболочки, оказывают нейтрализующее действие на вирус. Однако из-за высокой мутации в участках структурных белков, иммунная реакция на внедрение инфекции становится неэффективной из-за чего отсутствует действие интерферонотерапии в отдельных случаях.
Наиболее устойчивыми являются области, с которых считывается сердцевинный протеин — 5 UTR. Именно по генетическим различиям этого протеина определяют генотип HCV. Выделяют 6 наиболее распространенных генотипов вируса гепатита С и более 100 субтипов. Детальное изучение РНК вируса гепатита С и белков, которые участвуют в репликации, позволяет создавать новые интерфероны, которые участвуют в блокировке репликации вируса.
В России наиболее распространенными являются генотипы 1В и 3А. Генотип вируса необходимо учитывать при диагностике, так как он позволяет спрогнозировать эффективность и длительность противовирусного лечения. Доказано, что человека, инфицированного генотипами 1 или 4, тяжело лечить.
Особенности строения РНК вируса гепатита С не позволяют до конца изучить механизмы быстрой изменчивости. Поэтому и на сегодня не проводится специфическая профилактика, которая смогла бы предотвратить угрозу инфицирования гепатитом С. По этой же причине, ученые не могут создать универсальный интерферон, который препятствовал бы репликации вируса. Постоянные мутации приводят к образованию новых родственных популяций (квазивидов).
В процессе репликации и жизни в гепатоците вируса мутации происходят уже через 8 недель с момента инфицирования человека. Инфекционисты объясняют такую изменчивость ответной иммунной реакцией больного человека. Возможно, что способность HCV к мутациям позволяет ему избегать гибели в организме человека и длительное время участвовать в процессах репликации. Человек, который заразился гепатитом С, может долгое время не знать о своей болезни, в то время как вирус будет постепенно разрушать клетки печени. Поэтому гепатит С по праву считают «ласковым убийцей».
О том, как лечить острый холецистит, читайте тут.
Так как вирус гепатита С существует только в организме людей, источником инфекции является носитель или инфицированный человек. Выделены основные механизмы заражения:
- естественный (от матери к ребенку при беременности или в родах);
- контактный (бытовые предметы зараженного человека или половой акт с ним);
- искусственный (переливание зараженной крови, нестерильный инструментарий в больнице).
Естественный путь передачи HCV встречается реже, чем при вирусном гепатите В. Это связано с низкими концентрациями HCV в биологических жидкостях и мутации. Риск заразить ребенка во время родов или при вынашивании составляет всего 2 % и — 20 %, если у матери есть и ВИЧ. Если мама имеет только хронический вирусный гепатит С, ей не противопоказано кормление грудью.
В редких случаях инфекция может передаваться от ребенка к ребенку. Поэтому ребенку с HCV не запрещено посещать учебные заведения, играть с детьми (в том числе и в контактные игры). Не ограничивают и бытовые контакты людей с гепатитом С. Исключение составляют случаи, которые влекут за собой контакт с кровью инфицированного человека (бритва, зубная щетка, маникюрные ножницы и т. д.). Пациентам, у которых есть вирус гепатита С, должна быть проведена специфическая профилактика (вакцинация) от гепатита А и В.
Заражение от постоянного полового партнера также редко происходит. Однако носителям вируса надо ставить в известность партнера о своем инфицировании. Стоит отметить, что риск инфицирования через половой акт возрастает, если у человека много партнеров.
Большую угрозу инфицирования представляет внутривенное введение наркотиков через нестерильные шприцы. Наркоманы относятся к категории лиц, которые представляют наибольшую опасность в распространении инфекции. К группе риска относятся также:
- пациенты, которым проводят гемодиализ;
- лица с онкологией;
- люди с заболеваниями крови;
- врачи, медсестры, санитарки;
- доноры.
Несмотря на то что на сегодня существуют строгие требования к препаратам крови и донорству, риск заразиться при гемотрансфузии составляет 1-2 %. Это объясняется тем, что даже высокочувствительные анализы ИФА не позволяют исключить инфицирование донорской крови. Такой фактор объясняет причину внедрения метода карантинизации препаратов крови.
Важно! Человек может заразиться не только во время медицинских манипуляций, но и при выполнении татуировок, маникюра, пирсинга, порезов кожи во время проведения ритуалов.
Восприимчивость людей к инфицированию зависит от концентрации вируса, который попадает в организм. Даже выявление антител к вирусу не говорит, что у пациента есть иммунитет к HCV. Велика вероятность повторного заражения другими типами и подтипами вируса. По последним данным, хронический вирусный гепатит С сменил острый гепатит и составляет более 40 %.
Из-за изменчивости HCV специфическая профилактика не проводится. Неспецифическая профилактика заключается в проведении следующих мероприятий:
- предупреждение инфицирования в больницах и других ЛПУ;
- борьба с наркоманией;
- информирование населения о путях заражения;
- распространение информации о том, какая должна быть профилактика заражения.
После того как пациент с HCV выписывается из больницы, проводят генеральную дезинфекцию палаты. Контактные люди обследуются на наличие в крови вируса.
Развитие заболевания недостаточно изучено, так как HCV был открыт сравнительно недавно. На сегодня известны механизмы репликации вируса и терапевтические дозы интерферонов. Точных данных о механизме проникновения вируса в клетку печени нет. Предполагают что вирус после прикрепления к оболочке гепатоцита сливается с его мембраной, расплавляет ее и проникает в клетку. После сложных процессов, которые происходят в цитоплазме клетки печени, вирус начинает размножаться. Есть данные, что HCV может размножаться не только в клетках печени, но и в лимфоцитах.
Поражение гепатоцитов происходит не только под влиянием самого вируса, но и при участии аутоиммунных процессов. В ответ на внедрение HCV в гепатоциты, организм запускает механизмы уничтожения клеток печени. Исход и течение заболевания определяется состоянием иммунитета человека.
Острая фаза болезни характерна высокой концентрацией инфекции в сыворотке крови в течение первых недель после заражения. Однако в связи с мутацией HCV реакция иммунитета опаздывает на 1-2 месяца. В результате вирус успевает размножиться до ответа иммунной системы организма. При заражении гепатитом С фаза желтухи редко развивается.
Через 4 месяца может увеличиться активность трансаминазы АЛТ. Антитела к вирусу появляются еще позже и могут отсутствовать вовсе, однако отсутствие антител не означает, что человек здоров. У пациентов в 50–80 % случаев развивается хронический вирусный гепатит С. Только в 20–50 % случаев острая фаза заканчивается выздоровлением. Из крови вирус исчезает быстрее, чем из печени и других органов. Даже на сегодня не известно, полностью ли HCV исчезает из организма.
Клеточный иммунитет людей с хронической инфекцией слабый. Этот факт объясняет развитие у них хронического гепатита, цирроза и рака печени (гепатоцеллюлярной карциномы). Однако поражается не только печень. У пациентов выявляют:
- воспаления сосудов;
- гранулематоз;
- заболевания лимфатической системы;
- некрозы тканей;
- дистрофию печени;
- гломерулонефрит;
- красный плоский лишай;
- ревматизм;
- повреждения желчных протоков.
Жировая дистрофия печени наблюдается в большинстве случаев у людей с генотипом 3А. У пациентов с ХГС даже при невысокой активности вируса может развиваться фиброз печени, который в тяжелых случаях переходит в цирроз или рак. При выраженном воспалении тканей печени в 20 % случаев развивается цирроз. Прогноз болезни и тактику терапии интерферонами определяют после проведения оценки показателей анализа ИФА.
Острая стадия в 50–80 % протекает без желтухи, ее редко диагностируют. Длительность преджелтушного периода может составлять до 14 дней. У 20 % пациентов он может отсутствовать. В преджелтушный период могут наблюдаться такие симптомы:
В период желтухи появляется дискомфорт в животе, нарастает симптоматика. Пациенты могут жаловаться на головокружение или рвоту. При осмотре у больных выявляют увеличение печени и у 20 % — увеличение селезенки. Показатели билирубина при безжелтушном гепатите в норме, АЛТ увеличивается более чем в 10 раз.
Острый гепатит С протекает в 30 % случаев в легкой форме, в остальных — наблюдают средне-тяжелое течение. В редких случаях у пациента развивается тяжелое поражение печени с печеночной недостаточностью, которое заканчивается смертью.
В 70 % случаев пациенты с хроническим гепатитом С имеют невыраженное воспаление и благоприятное течение болезни. В 30 % случаев гепатит прогрессирует и приводит к фиброзу, циррозу, раку. При декомпенсированном циррозе ставят вопрос о трансплантации печени. При тяжелом прогрессивном течении причиной смерти часто являются:
- рак;
- кровотечение;
- печеночная недостаточность.
Установлено, что прогрессирование болезни и развитие тяжелых форм происходит у людей, инфицирование которых произошло после 40 лет, а также у людей с ВИЧ, гепатитом В или у тех, которые злоупотребляют алкоголем. К факторам риска относится ожирение.
ХГС может протекать длительно без симптомов и желтухи. Обнаруживают вирус случайно, иногда только после формирования цирроза. Важным диагностическим методом для пациентов с ХГС является биопсия печени. Иногда у пациентов развивается поражение желез, глаз, кожи, суставов, нервов, мышц.
Диагностика основывается на показателях анализов крови. У пациентов АЛТ превышает норму в 10 раз, выявляют маркеры ВГС. Так как не всегда по симптомам удается отличить острый гепатит от обострения хронической формы, для диагностики ОГС назначают метод ПЦР, который выявляет вирусный РНК. Появление чувствительных тестов позволяет обнаружить антитела через неделю после желтухи.
Пациентам с ХГС назначают биопсию печени для оценки степени поражения, а также стадии фиброза. На основании данных биопсии устанавливают тактику лечения и определяют показания к терапии интерферонами. Сейчас биопсия, которая считается инвазивным методом, заменяется неивазивными способами:
- тестом «Фибротест»;
- транзиентной эластографией «Фиброскан».
Однако методы не позволяют установить стадии фиброза. Биопсию проводят в таких случаях:
- пациентам в отсутствие лечения интерферонами — для определения стадии фиброза;
- пациентам с генотипом 1 вируса гепатита — для решения вопроса терапии интерферонами при выраженных стадиях фиброза.
Биопсия печени не является обязательным исследованием, поэтому человек может от нее отказаться. В особенности при генотипе 2 или 3 вируса HCV. Такие генотипы могут успешно лечиться стандартными противовирусными препаратами. Пациенты с циррозом попадают под контроль врача, так как в этом случае важна профилактика онкологических болезней печени. Дифференциальную диагностику проводят с другими гепатитами.
Лечение вирусного гепатита С проводят в стационаре. Пациентам показан постельный режим, диета № 5 с исключением раздражающей, жареной и жирной пищи. Для предотвращения прогрессирования болезни рассматривают вопрос о противовирусной терапии. При остром гепатите назначают монотерапию коротких или пегилированных (ПЕГ-ИНФ) интерферонов. Терапию рекомендуют на 8–12 неделе от начала периода желтухи.
Предпочитают проводить терапию ПЕГ-ИНФ:
- Пегинтерферон альфа 2а (Пегасис) или альфа 2b (Пегинтрон) назначают 1 раз в неделю. Длительность курса может достигать 24 недель при генотипе 1; при 4 — курс 48 недель.
- При трудностях в диагностике между острым и хроническим гепатитом к интерферонам добавляют лечение Рибавирином, который удваивает эффект интерферонов.
- Терапия, направленная на регуляцию работы ЖКТ. Назначают Панкреатин, гепатопротекторы (Эссенциале, Гептрал, Ливолин, Эсливер Форте, Карсил и т. д.), желчегонные средства, препараты для восстановления микрофлоры кишечника.
- Терапия, направленная на дезинтокискацию организма. Назначают Реополиглюкин, Реосорбилакт, солевые растворы.
На проведение противовирусной терапии настаивают при выраженном фиброзе печени. Не назначают терапию интерферонами пациентам:
- с неконтролируемой депрессией, психозами, эпилепсией;
- имеющим аутоиммунные болезни;
- при беременности;
- с неконтролируемой артериальной гипертензией;
- при обструктивных хронических болезнях легких;
- с плохо контролируемым сахарным диабетом.
Дозировку интерферонов и Рибавирина рассчитывают по массе тела пациента, учитывая генотип вируса. Критерии эффективности терапии — отсутствие РНК HCV и нормализация показателей АЛТ и АСТ. Плохо поддаются лечению пациенты после 40 лет, алкоголики, больные с инсулинозависимостью, ожирением печени, высокой вирусной нагрузкой, имеющие генотипы 1 или 4.
Повышают эффективность терапии отказ от алкоголя, курения, коррекция диеты. Если в течение 24 недель в крови у пациента выявляют РНК HCV, рассматривают вопрос о прекращении лечения в связи с неэффективностью препаратов. При достижении вирусного ответа организма курс лечения может быть продлен до 72 недель.
Важно знать! Во время терапии Рибавирином необходима контрацепция половых партнеров! Рекомендуют избегать беременности во время всего курса терапии интерферонами и спустя полгода после окончания лечения.
Во время противовирусной терапии у пациентов могут возникать побочные реакции:
- слабость;
- температура;
- головная боль;
- депрессия;
- нарушение сна;
- раздражительность;
- аутоиммунный тиреоидит;
- гемолитическая анемия.
В таких случаях проводят коррекцию дозировок интерферона или решают вопрос о прекращении лечения. Для достижения эффекта в комплекс терапии включают препараты с прямым противовирусным действием к HCV — ингибиторы протеазы (Телапревир, Боцепревир, Виктрелис). Трехкомпонентная терапия ПЕГ-ИНФ, Рибавирином и ингибиторами протеазы повышает терапевтический эффект даже у трудной категории пациентов.
Существует несколько вариантов ответа на противовирусную терапию пациентов с ХГС:
- Быстрый — наступает через 4 недели.
- Ранний.
- Полный — наступает через 12 недель.
- Частичный — в крови выявляют РНК вируса гепатита С, однако уровень виремии снижен.
- Медленный — наступает через 24 недели.
В случае когда концентрация вирусов не изменяется после терапии, говорят о полном отсутствии вирусологического ответа. Пациенты с ХГС находятся под контролем врачей всю жизнь в целях своевременного выявления осложнений, коррекции лечения и наблюдения.
источник
В настоящее время проблемой хронической HCV-инфекции интересуются как врачи-специалисты, так и люди, никак не связанные с медициной. От гепатита С во всем мире страдают по меньшей мере 200 млн человек.
В настоящее время проблемой хронической HCV-инфекции интересуются как врачи-специалисты, так и люди, никак не связанные с медициной.
От гепатита С во всем мире страдают по меньшей мере 200 млн человек. Последствиями перенесенного заболевания могут быть хронический гепатит, цирроз и первичный рак печени.
Распространенность хронической HCV-инфекции на земном шаре варьирует от 0,5 до 2%. Существуют регионы, для которых характерна более высокая распространенность этого заболевания: 6% в Заире и Саудовской Аравии, 16% в изолированных поселениях в Японии. В России наблюдается рост заболеваемости гепатитом С (3,2 на 100 тыс. населения в 1994 году и 19,3 в 1999 году). Источниками заражения вирусным гепатитом C служат больные острыми и хроническими формами HCV-инфекции, причем в основном это люди, у которых отсутствует желтуха и наблюдается бессимптомное или малосимптомное течение заболевания.
В настоящее время HCV чаще всего инфицируются молодые люди, преимущественно мужчины в возрасте около 20 лет, примерно 40% из них заражаются при внутривенном введении наркотиков. Основным путем инфицирования HCV является парентеральный. Так, у 6,1% больных, которым производилось переливание крови и ее компонентов во время кардиохирургических операций, развивался острый вирусный гепатит C, у 60% из них гепатит принимал хроническую форму.
Существует и риск заражения гепатитом C половым путем, однако он невелик (5-8%). Возможна передача HCV от матерей с острой или хронической формой инфекции; это также редкое явление, встречается не чаще чем в 5-6% случаев. Риск заражения вышеуказанными путями уступает таковому при гепатите В.
Приблизительно у половины больных путь инфицирования HCV установить не удается.
Вирус гепатита С относится к семейству флавивирусов. Геном вируса представлен однонитевой РНК протяженностью около 10 000 нуклеотидов. Вирус гепатита С вызывает заболевание только у человека. В экспериментальных условиях воспроизвести инфекцию можно у высших обезьян.
Популяция вируса неоднородна. Идентифицированы 6 генотипов (классификация по Simmonds), более 90 субтипов и множество вариантов вируса, обозначаемых как квазивиды. Зарегистрирована территориальная неравномерность циркуляции генотипов вируса гепатита С. В России чаще всего выявляются генотипы 1b и 3а этого вируса.
Определение генотипов вируса гепатита С имеет большое значение для практической медицины. Хотя до сих пор не установлено четкой корреляции между генотипами и уровнем виремии, характеристиками пациента, тяжестью течения заболевания, большинство исследователей соглашаются с выводами о значении генотипов вируса как важного фактора, влияющего на эффективность противовирусной терапии.
Вакцину против гепатита С создать пока не удалось из-за высокой изменчивости вируса гепатита С (ВГС).
Считают, что вирус оказывает прямое цитопатическое действие и вызывает иммуноопосредованное повреждение гепатоцитов. Высокая степень хронизации вирусного гепатита С обусловлена некоторыми особенностями действия вируса:
- возможностью внепеченочной репликации вируса, включая иммунокомпетентные клетки (клетки, предшественники гемопоэза, лимфоциты и моноциты периферической крови, миофибробласты);
- гетерогенностью генотипов и частыми мутациями генома вируса;
- индукцией каскада иммунопатологических реакций;
- активизацией процессов перекисного окисления липидов в печени.
В течении хронической HCV-инфекции может происходить нейтрализация мажорного варианта вируса, но тогда генерируются минорные варианты. Квазивиды HCV представляют собой движущуюся мишень, которую ограничивает иммунная система хозяина. Появление нового мажорного квазивида сопровождается повышением виремии и увеличением титра Ig M антител к вирусным белкам. Постепенно и этот новый мажорный вариант заменяется. Такой процесс приводит к периодической волнообразной виремии, сопровождающейся обострением хронического гепатита С (ХГС) и повышением уровня антител.
Возможно, антивирусному Т-клеточному ответу отведена центральная роль в элиминации ВГC, так как нейтрализующие антитела, по-видимому, очень часто оказываются неэффективными. Т-хелперные (Th) лимфоциты распознают вирусные антигенные пептиды, представленные HLA-комплексом II класса на поверхностной мембране антиген-презентирующих клеток. В зависимости от типа цитокинового профиля Th-клетки делятся на две группы: Th1 и Th2. Первые продуцируют IFNg и IL2, стимулируя Т-клеточный ответ и цитотоксическую Т-лимфоцитную активность, а вторые продуцируют IL4 и IL10, стимулируя В-клеточный ответ. Таким образом, Тh-лимфоциты играют существенную роль в регуляции иммунного ответа. У пациентов, у которых болезнь перешла в хроническую стадию, в острой фазе вирус-специфический Th ответ был ниже и преобладали цитокины типа Th2.
У хронически ВГC-инфицированных пациентов значительно увеличено содержание вирусоспецифических Th2-клеток и их цитокинов. Нарушение баланса Th1/Th2 цитокиновой продукции может играть важную роль в иммунопатогенезе хронической ВГC-инфекции. Показано снижение уровня IFNg и IL12 при ХГС. Этот дефицит является следствием повышенного уровня IL10, предполагаемого отрицательного регулятора для IFNg. Повышенное содержание Th2-клеток при ХГС может снижаться при комбинированной терапии рибавирином и IFNa. Обнаружено, что у пациентов с клинико-биохимическим улучшением после лечения IFNa произошло увеличение уровня Th1-цитокинов.
Цитотоксические лимфоциты (CTL) играют, по-видимому, некоторую роль в ограничении репликации ВГС. Этот ответ недостаточен для полной элиминации вируса при хронической инфекции и, кроме того, может вызывать повреждение печени. Известно, что CTL способны быстро опознавать и направленно лизировать клетки, несущие ВГC-антигены, не провоцируя значительного воспаления, с помощью перфоринового, FasL- и TNFα-базируемых механизмов.
ТNF, как предполагается, индуцируют апоптоз клеток, опосредуя высвобождение свободных радикалов из митохондриальных электронно-транспортных путей и модуляцию синтеза некоторых белков. Взаимодействие нуклеокапсидного белка ВГC с внутрицитоплазматической частью рецептора TNFb, вероятно, представляет собой эволюционно-отобранный механизм, с помощью которого вирус препятствует преждевременному апоптозу клетки-хозяина. В отсутствие доступных модельных клеточных культур прямая цитопатичность вируса гепатита С не может быть исследована в полном объеме.
В подавляющем большинстве случаев острого гепатита С иммунной системе не удается элиминировать вирус. До сих пор нет ясного представления о том, почему это происходит. Очевидно, ВГС обладает эволюционно-закрепленными способностями, обеспечивающими ему персистенцию.
Однако иммунная система может оказывать существенное влияние на ВГC-инфекцию. В 15% случаев острого гепатита С она эффективно уничтожает вирус, а у хронически ВГC-инфицированных обеспечивает умеренное ограничение инфекции в течение почти 20 лет. Возможно, ослабление какого-либо звена антивирусных иммунных механизмов позволяет вирусу активно воздействовать на иммунную систему. Длительная ВГC-персистенция может привести к развитию В-клеточных лимфопролиферативных нарушений, таких, как смешанная криоглобулинемия, злокачественная не-Ходжкинская лимфома и появление органоспецифических и неспецифических аутоантител. Таким образом, хроническую ВГC-инфекцию следует рассматривать как мультисистемное заболевание.
Лабораторная диагностика гепатита С основана на выявлении специфических маркеров инфицирования ВГС (анти-ВГС-IgM/G, РНК ВГС) и должна проводиться разрешенными МЗ РФ к применению диагностическими препаратами отечественного или зарубежного производства в лабораториях, имеющих лицензию на проведение данного вида лабораторных исследований.
HCV RNA — самый ранний маркер репликации вируса, определяемый с помощью полимеразной цепной реакции (ПЦР) спустя несколько недель после заражения. Для выявления анти-ВГС применяют иммуноферментный анализ (ИФА). В настоящее время используют тест-системы третьего поколения ELISA-3. Подтверждающим методом является рекомбинантный иммуноблотинг (RIBA). У 60% больных анти-ВГС определяются в острой фазе, у 35% они появляются спустя 3-6 месяцев после инфицирования, у 5% инфицированных лиц анти-ВГС не определяются.
Болезнь может протекать бессимптомно. Наиболее распространенным симптомом является слабость. Целенаправленный опрос больных часто помогает выявить такие факторы риска, как переливание крови, внутривенное введение наркотиков, хронический гемодиализ и др. Кроме слабости больной может жаловаться на быструю утомляемость, тяжесть в правом подреберье, боли в правом верхнем квадранте живота, диспепсические явления.
Критериями постановки диагноза являются увеличение печени и селезенки, гиперферментемия и анти-ВГС в крови в течение не менее 6 месяцев.
Гепатоспленомегалия выявляется не более чем у 50% обратившихся за помощью больных, активность сывороточных трансаминаз редко превышает верхнюю границу нормы в 6 раз. Следует обратить внимание на то, что активность сывороточных трасаминаз не отражает степени изменений в печени: она может быть нормальной, несмотря на значительные морфологические изменения. Концентрация РНК ВГС в сыворотке имеет существенное значение для определения контагиозности и для мониторинга результатов лечения. При наличии в крови HCV-РНК биопсия печени, как правило, выявляет ряд изменений. Концентрация HCV-РНК в сыворотке, превышающая 105 молекулярных эквивалентов (копий) в 1 мл, наблюдается в активной фазе заболевания и совпадает с пиками активности трансаминаз.
Наличие или отсутствие РНК ВГС, как правило, не является диагностическим критерием хронического гепатита С и определяет фазу процесса (активный, неактивный).
Для раннего выявления ГЦК у больных циррозом печени, особенно у мужчин старше 40 лет, каждые 6 месяцев определяют уровень сывороточного α-фетопротеина и выполняют УЗИ печени.
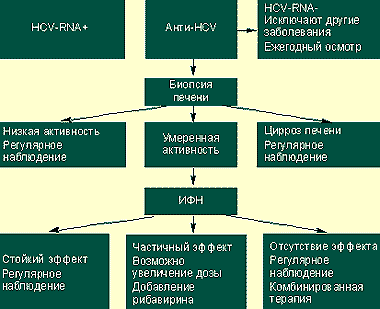 |
| Алгоритм ведения HCV-положительных больных |
Инфицирование ВГС приводит к развитию острого гепатита С, протекающего в манифестной (желтушной) или чаще в латентной (безжелтушной) формах, которые развиваются в соотношении 1:6. Около 17-25% больных острым гепатитом С выздоравливают спонтанно, у остальных 75-83% развивается хронический гепатит С. Большинство больных с биохимическими и иммунологическими признаками хронического гепатита имеют слабовыраженную или умеренную степень воспалительно-некротического поражения печени и минимально выраженный фиброз. Примерно у 26-35% больных хроническим гепатитом С в течение 10-40 лет развивается фиброз печени и может наступить смерть от цирроза печени и его осложнений. У 30-40% больных с циррозом печени высок риск заболевания раком печени.
Считается, что не более чем у 30% больных ВГС с минимальной морфологической активностью через 20 лет возможно развитие цирроза печени. Таким образом, больные, у которых при гистологическом исследовании биоптата печени выявляется наличие минимального воспаления и минимального фиброза, нуждаются в динамическом наблюдении.
Если персистенция РНК ВГС сохраняется более 6 месяцев, то спонтанное разрешение хронической HCV-инфекции маловероятно.
У большинства больных с хроническим гепатитом С заболевание протекает бессимптомно. Если жалобы существуют, то это чаще всего слабость, тупые боли в правом подреберье, тошнота, снижение аппетита, кожный зуд, артралгии и миалгии. Физикальный осмотр пациента помогает установить диагноз зачастую только на стадии цирроза печени.
Ассоциация хронического гепатита С с различными внепеченочными проявлениями — хорошо известный врачам факт. Наиболее вероятным для большинства заболеваний и синдромов, наблюдаемых при HCV-инфекции, представляется иммунный патогенез, хотя конкретные механизмы во многом еще не выяснены. Доказанные и предполагаемые иммунные механизмы включают:
- моно- или поликлональную пролиферацию лимфоцитов;
- образование аутоантител;
- отложение иммунных комплексов;
- секрецию цитокинов.
Частота иммуноопосредованных заболеваний и синдромов у больных хроническим гепатитом С достигает 23%. Наиболее характерны аутоиммунные проявления для больных с гаплотипом HLA DR4, который ассоциируется с внепеченочными проявлениями при аутоиммунном гепатите. Этот факт подтверждает гипотезу о триггерной роли вируса в инициации аутоиммунных процессов у генетически предрасположенного индивидуума.
Ассоциированные с продукцией или отложением иммуноглобулинов:
- Криоглобулинемия
- Лейкоцитокластерный васкулит
- Мембранозно-пролиферативный гломерулонефрит
- В-клеточная лимфома
- Плазмоцитома
- MALTома
- Тиреоидит
- Синдром Шегрена
- Гемолитическая анемия
- Тромбоцитопения
- Красный плоский лишай
Ассоциированные с неизвестным механизмом:
Выявление сывороточных аутоантител отражает наиболее частый феномен аутоиммунизации при HCV-инфекции, который диагностируют у 40-65% больных. Спектр аутоантител достаточно широк и включает ANA (до 28%), SMA (до 11%), анти-LKM-1 (до 7%), антифосфолипидные (до 25%), антитиреоидные (до 12,5%), ревматоидный фактор, анти-ASGP-R и др. Чаще всего титры этих антител не достигают диагностических значений, показательных для той или иной аутоиммунной патологии.
Анти-GOR являются антителами, специфичными для HCV-инфекции, и их выявляют не менее чем у 80% больных. Эпитоп, распознаваемый анти-GOR, локализуется на пока неидентифицированном ядерном белке, гиперэкспрессию которого наблюдают при гепатоцеллюлярной карциноме. Выработка анти-GOR ассоциирована только с HCV-инфекцией, но не с АИГ.
Аутоиммунные расстройства наблюдаются в среднем у 23% больных хроническим гепатитом С. Наиболее часто встречаются патология щитовидной железы.
Гистологическая картина не является патогномоничной, при этом достаточно часто выявляются характерные изменения. Отличительная особенность ее — лимфоидные агрегаты или фолликулы в портальных трактах, которые могут быть как изолированными, так и частью воспалительных изменений портальных трактов. По клеточному составу эти агрегаты напоминают первичные лимфоидные фолликулы в лимфатических узлах. Жировая дистрофия обнаруживается в 75% случаев. Кроме того, выявляются следующие характерные изменения: негнойный холангит с лимфоидной и плазмоклеточной инфильтрацией стенок протоков; лимфогистиоцитарная инфильтрация перипортальной зоны; слабовыраженные ступенчатые некрозы; мостовидные некрозы (обнаруживаются редко), пролиферация и активация сателлитных клеток печени, пролиферация эпителия желчных канальцев.
Отмечено, что индекс гистологической активности (ИГА) и индекс фиброза (ИФ) у больных хроническим гепатитом С с наличием жировой дистрофии достоверно выше, чем у пациентов без сопутствующей жировой дистрофии. У 93% больных с жировой дистрофией в гепатоцитах обнаруживался Core-протеин ВГС, при отсутствии жировой дистрофии — лишь у 39%. Этим фактом подчеркивается роль Core-протеина в развитии жировой дистрофии гепатоцитов.
Биопсия печени играет существенную роль в уточнении диагноза и оценке активности и стадии заболевания.
РНК ВГС можно определить в ткани печени методом ПЦР.
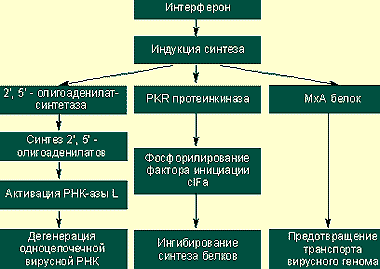 |
| Предотвращение вирусной транскрипции и трансляции |
Основная цель лечения — предотвратить прогрессирование заболевания.
Режим отдыха, диета и прием витаминов не оказывают лечебного действия.
Отбор пациентов для лечения. Показанием к назначению терапии интерфероном служит умеренное (но не минимальное) либо тяжелое воспаление и/или фиброз. Решение о лечении пациентов с циррозом печени принимают индивидуально в каждом конкретном случае. Больные, у которых гистологическая активность минимальна, должны находиться под динамическим наблюдением, так как они имеют хороший жизненный прогноз без лечения и очень низкий риск развития цирроза печени через 10-20 лет.
Факторы, связанные с благоприятным эффектом противовирусной терапии при хронической HCV-инфекции:
- Возраст моложе 45 лет
- Женский пол
- Отсутствие ожирения
- Срок инфицирования менее 5 лет
- Отсутствие коинфекции HBV
- Отсутствие иммунодепрессии
- Отсутствие алкоголизма
- Умеренное повышение АЛТ
- Отсутствие цирроза
- Низкое содержание железа в печени
- Низкий уровень HCV RNA в сыворотке
- Генотип 2 или 3
- Однородность популяции вируса
Больным с нормальным уровнем АЛТ и положительным тестом на HCV RNA без результатов гистологического исследования противовирусное лечение проводить не рекомендуется.
Основной препарат, эффективность которого в лечении гепатита С доказана, — это интерферон альфа (ИФα).
В настоящее время принята оптимальная схема монотерапии ИФ: разовая доза составляет 3 млн МЕ, ее вводят подкожно или внутримышечно 3 раза в неделю в течение 3 месяцев. Через 3 месяца необходимо исследовать РНК ВГС. Если результаты ПЦР положительные схему лечения меняют. Если же РНК не выявляется, лечение продолжают до 12 месяцев. Стойкий положительный ответ в этом случае регистрируется у 15-20% больных.
Оптимальная схема лечения хронического гепатита С в настоящее время — это комбинация ИФa и рибавирина.
Согласно рекомендации согласительной конференции Европейской ассоциации по изучению печени (1999), больным с впервые установленным диагнозом «хронический гепатит С» и показаниями к лечению необходимо назначать ИФa в комбинации с рибавирином следующими курсами:
- в течение 6 месяцев — при генотипах 2 и 3;
- в течение 6 месяцев — при генотипе 1 и низком уровне виремии;
- в течение 12 месяцев — при генотипе 1 и высоком уровне виремии.
Стойкий положительный ответ при комбинированном лечении ИФa с рибавирином наблюдается в 40-60% случаев.
Суточная масса рибавирина составляет 1000-1200 мг в зависимости от массы тела.
В последние годы для повышения эффективности интерферона применяют пегилирование, которое заключается в присоединении к молекуле интерферона полиэтиленгликоля. В итоге образуется ПЭГ-интерферон, имеющий более длительный период полураспада. Предварительные данные свидетельствуют о большей эффективности такого лечения по сравнению с терапией интерфероном альфа.
Одним из наиболее перспективных пегилированных интерферонов является пегасис — ПЭГ-интерферон альфа-2а, соединенный с разветвленной молекулой полиэтиленгликоля, молекулярная масса которого составляет 40 kDa, общий вес молекулы — около 60 kDa. Особенности химической структуры данного препарата определяют его фармакокинетические свойства и клиническую эффективность. Молекула полиэтиленгликоля присоединена к альфа-интерферону посредством самой стабильной амидной связи, это делает молекулу пегасиса чрезвычайно устойчивой к действию петидаз и позволяет выпускать препарат в виде растворенной и готовой к употреблению лекарственной формы. Особенностью молекулы полиэтиленгликоля является способность активно связывать несколько молекул воды, что создает вокруг химически структурной единицы пегасиса эффект «водного облака», делая ее устойчивой во внутренней среде и сообщая препарату относительно небольшой объем распределения. Это, в свою очередь, способствует тому, что отпадает необходимость в коррекции дозы препарата в зависимости от массы тела пациента: пегасис вводится один раз в неделю в дозе 180 мкг. Существенными преимуществами препарата пегасис являются значительно лучшая переносимость и меньшая частота побочных реакций, ассоциированных с системным действием альфа-интерферона, что значительно улучшает качество жизни пациентов, получающих лечение по поводу хронического гепатита С. Кроме того, в отличие от других пегилированных интерферонов пегасис не требует существенной коррекции дозы в зависимости от функционального состояния почек, что делает препарат незаменимым у пациентов с сопутствующей хронической почечной недостаточностью.
Клиническая эффективность пегасиса оценена солидными широкомасштабными многоцентровыми рандомизированными исследованиями. Было показано, что частота доказанного ответа на лечение значительно превышает таковую по сравнению с «короткими» интерферонами как в схемах монотерапии, так и в сочетании с рибавирином. Особенно впечатляющими в этой связи являются результаты этиопатогенетической терапии с использованием пегасиса в сочетании с рибавирином у так называемой «трудной» категории пациентов, имеющих морфологические проявления цирроза печени, 1b-генотип вируса, высокую виремию: частота доказанного ответа на лечение у данной категории пациентов при использовании пегасиса в сочетании с рибавирином может составлять около 40%, у иных категорий пациентов этот показатель может превышать 75%, что ранее было практически немыслимым результатом.
Имеются данные, свидетельствующие о положительном действии таких препаратов, как ремантадин, урсодеоксихолевая кислота, пегилированные интерфероны, препараты глициризиновой кислоты, однако эта информация нуждается в дальнейшей проверке.
По вопросам литературы обращаться в редакцию
источник