(гистологическое cytus клетка + греч. megas, megalu большой + вирус/ы/ (Вирусы); синонимы: инклюзионная болезнь, цитомегалия)
повсеместно распространенная инфекция с необычайно широким спектром клинико-патогенетических проявлений, в основе которых лежат различные варианты иммунодепрессии.
В современной клинической медицине Ц. и приобретает все большую актуальность — Европейским регионарным бюро ВОЗ она отнесена в группу болезней, которые определяют будущее инфекционной патологии. Несмотря на повсеместное распространение Ц. и., эпидемических вспышек до настоящего времени не описано. В этом своеобразном парадоксе кроется сущность проблемы — Ц. и. относится к так называемым оппортунистическим инфекциям, клиническое проявление которых становится возможным лишь в условиях первичного или вторичного иммунодефицита. В последние годы распространенность иммунодефицитов существенно повысилась в связи с появлением ВИЧ-инфекции, действием факторов, нарушающих экологическое равновесие, различными ятрогенными вмешательствами, в разной степени оправданными и вынужденными (лекарственная болезнь, применение цитостатиков, в частности после трансплантации органов и тканей, гемотрансфузии). Немалую роль играет и беременность, при которой эволюционно приспособленные механизмы физиологического иммунодефицита обеспечивают смягчение возможного иммунного конфликта между матерью и формирующимся плодом.
Все эти факторы, особенно их сочетание, создают условия для реактивации, вызываемой цитомегаловирусом латентной, хронической или инаппарантной инфекции, в возникновении которой играют роль различные механизмы передачи возбудителей инфекции среди лиц, относящихся к категории повышенного риска, новорожденных, реципиентов гемотрансфузии и трансплантатов различных органов, пациентов, систематически получающих иммунодепрессанты, а также гомосексуалистов и проституток.
Наличие инаппарантных форм и состояния вирусоносительства наряду с клинически манифестными вариантами инфекции — широко распространенное явление в инфекционной патологии (например, при полиомиелите, вирусном гепатите В, аденовирусной инфекции). В ряду таких заболеваний Ц. и. занимает особое положение по частоте вирусоносительства и преобладанию инаппарантных, субклинических форм над острыми, клинически выраженными вариантами, когда речь идет о цитомегаловирусном заболевании (ЦМВЗ).
На основании исследований, проведенных в США, 1—2% всех детей экскретируют цитомегаловирус (ЦМВ) с мочой при рождении; к 1 году количество таких детей возрастает до 10—20%, к 35 годам 40% взрослых имеют антитела к ЦМВ, а к 50 годам почти все взрослые инфицированы ЦМВ.
Этиология. ЦМВ относится к семейству герпетических вирусов (вместе с вирусами простого герпеса I и II типов, вирусом ветряной оспы и вирусом Эпстайна — Барр). Общей их чертой является прежде всего способность персистировать в организме с нерегулярной продукцией вирусных частиц и обострениями хронической инфекции. Однако ЦМВ имеет особенности, которые отличают его от других герпетических вирусов: необычайно крупная ДНК, возможность репликации ЦМВ без повреждения клетки, меньшая цитопатогенность в культуре тканей, медленная репликация вируса, сравнительно низкая вирулентность, более узкий спектр хозяев, меньшая чувствительность к аналогам нуклеозидов, резкое подавление клеточного иммунитета.
Эпидемиология. Источниками возбудителя инфекции могут являться хронические носители ЦМВ или больные с разными вариантами Ц. и. Передача возбудителя инфекции происходит через биологические жидкости и выделения: кровь, мочу, слюну, отделяемое влагалища, слезную жидкость, грудное молоко, амниотическую жидкость, сперму, фекалии. Источниками ЦМВ могут быть ткани и органы, используемые в трансплантологии, и донорская кровь, а также беременные женщины. Механизмы передачи возбудителя предполагают прежде всего непосредственный контакт между беременной (или родильницей) и плодом (или новорожденным), между сексуальными партнерами, между детьми в закрытых детских коллективах. В механизмах передачи ЦМВ, вируса гепатита В, а также возбудителя ВИЧ-инфекции много общего. При Ц. и. большая роль отводится слюне (это заболевание называют еще болезнью поцелуев). Восприимчивым объектом для Ц. и. являются лица, не встречавшиеся с вирусом в прошлом.
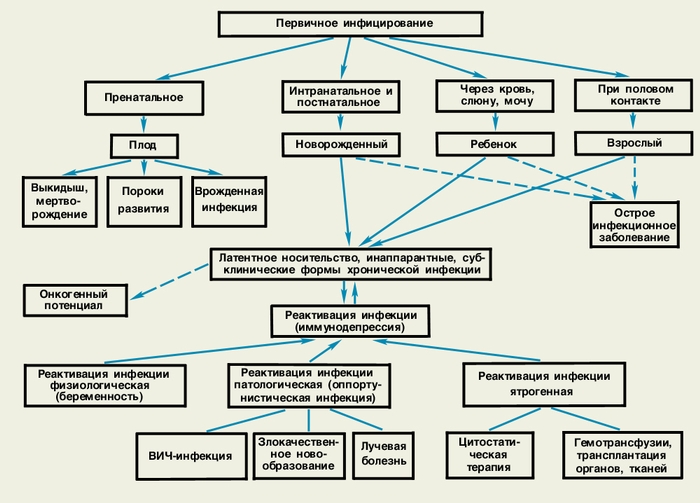
Клинико-патогенетические варианты инфекции отличаются широтой спектра, что определяется наличием различных взаимоотношений между вирусом, уровнем иммунитета (прежде всего клеточного) и механизмом инфицирования. Разрыв между цитомегаловирусной инфекцией и ЦМВЗ является разительным и уникальным — в подавляющем большинстве случаев возникают клинически бессимптомные, инаппарантные и хронические формы. В наиболее общем виде эти отношения представлены на схеме, на которой показано развитие Ц. и. и ЦМВЗ при различных путях инфицирования. Ц. и. — самая частая причина инфицирования плода; при трансплацентарном инфицировании плода обычно возникают привычные выкидыши, мертворождения, пороки развития, врожденная Ц. и. с преимущественным поражением ц.н.с. (гидроцефалия, микроцефалия и др.) и печени (фетальные гепатиты, врожденные циррозы печени, атрезии желчных путей и др.). Инфицирование ребенка при прохождении через родовые пути или в периоде новорожденности (грудное вскармливание, тесный контакт с матерью) приводит обычно к менее тяжелым последствиям, чаще к латентному вирусоносительству. Таковы же наиболее частые исходы других механизмов инфицирования, за исключением случаев трансплантации органов, тканей и гемотрансфузии, когда возникает острое инфекционное заболевание (своеобразный вирусный гепатит, без резкой интоксикации, но с гиперферментемией и холестазом; мононуклеозоподобный лимфаденит и др.). Реактивация Ц. и. наступает в условиях иммунодепрессии, связанной с эндогенными, физиологическими (беременность) или экзогенными факторами, среди которых особая роль принадлежит ятрогенным воздействиям (назначение длительных курсов цитостатиков, проведение гемотрансфузий, трансплантации органов и тканей). Наибольшую роль в качестве оппортунистической цитомегаловирусная инфекция играет при патологических состояниях, приводящих к развитию иммунодефицитов (СПИД, злокачественные новообразования, лучевая болезнь). Выделяют врожденные и приобретенные ЦМВЗ, которые различаются не только по механизмам инфицирования, но и по своей патогенетической природе.
Врожденных ЦМВЗ включают явный цитомегаловирусный синдром (мертворождения, выкидыши), недоношенность (внутриутробная гипотрофия), тромбоцитопеническую пурпуру, поражения печени с желтухой, врожденные гепатиты и циррозы печени, поражения ц.н.с. (гидроцефалия, микроцефалия, менингоэнцефалиты), цитомегаловирусный сепсис (диссеминация) с поражением и других органов и систем. Скрытый цитомегаловирусный синдром включает нарушения, которые при рождении обычно трудно распознать. Они (хориоретинит с атрофией зрительных нервов, глухота, задержка интеллектуального развития) выявляются на более поздних стадиях развития ребенка.
Приобретенные ЦМВЗ не укладываются в четкие рамки одной нозологической формы, они могут протекать с лихорадкой, интоксикацией, слабостью, миалгией, лимфаденопатией, сиаладенитом, гепатитами, пневмониями, язвами желудочно-кишечного тракта, миокардитами. При этом ЦМВЗ может принимать «образ» ВИЧ-инфекции, инфекционного мононуклеоза, острого лейкоза, лимфогранулематоза, вирусных гепатитов, сепсиса. Цитомегаловирусный гепатит, развивающийся после трансплантации печени, характеризуется лихорадкой, желтухой, гепатоспленомегалией, холестазом, при весьма умеренной интоксикации с появлением антител класса lgM к ЦМВ и выраженной гипертрансфераземии.
Диагноз устанавливают на основании данных лабораторных исследований; обнаружение в биологических жидкостях ЦМВ и его антигенов, а также специфических антител.
Лечение. Применяют противовирусные препараты и патогенетические средства иммунокорригирующего и заместительного характера. Первым противовирусным препаратом, эффективным при острой Ц. и., особенно в трансплантологии, стал ацикловир, который вводят внутривенно на протяжении 14 дней. Применение препарата требует большой осторожности, особенно у детей, в связи с возможными побочными явлениями. У больных с трансплантированными органами (почки, печень) ацикловир может быть показан при возникновении или обострении Ц. и. Левамизол (наиболее изученный иммуномодулятор в терапии Ц. и.) применяют по схеме на протяжении 12 недель (1-я неделя по 50 мг 2 раза в день на протяжении 5 дней, а в последующем — в той же дозе 2 дня в неделю). Это обеспечивает в подавляющем большинству случаев благоприятный исход последующих беременность у женщин с отягощенным акушерским анамнезом и Ц. и. В случаях, когда упорно сохраняется экскреция вируса с мочой и слюной, при наличии в крови антицитомегаловируса класса lgM проводят повторный курс лечения тем же препаратом или применяют 10-недельныи курс подкожных инъекций (2 раза в неделю по 100 мкг) тактивина. Перечисленные препараты могут применяться вне состояния беременности. При беременности приходится решать сложные проблемы, относящиеся к терапевтической и акушерской тактике. Когда искусственное прерывание беременности в ранние сроки встречает возражения прибегают к систематическому мониторингу серологических, цитологических показа гелей, а также результатов ультразвукового исследования плода в динамике. В подобных ситуациях может оказаться целесообразным применение препаратов, содержащих антитела к ЦМВ в высоких титрах.
Профилактика Ц. и. предусматривает прежде всего соблюдение правил личной гигиены, надлежащего контроля тканей и органов в трансплантологии, а также создание условий для охраны от факторов, способных вызвать иммунодепрессию. Грудное вскармливание при наличии в молоке ЦМВ нежелательно, хотя опасность такого механизма инфицирования ребенка меньше, чем в пре- и интранатальных условиях.
Библиогр.: Букринская А.Г. Вирусология, М., 1986; Демидова С. А и др. Цитомегаловирусная инфекция человека, М., 1976; Руководство по педиатрии, под ред. P.Е. Бермана и В.К. Вочана, пер. с англ., с. 3, стр. 382, М., 1987; Самохин П.А. Цитомегаловирусная инфекция у детей, М., 1987; Фарбер Н.А. и Жданов В.М. Цитомегаловирусная инфекция и синдром приобретенного иммунодефицита, Вопр. вирусол., № 4, с. 389, 1986.
Схема развития цитомегаловирусной инфекции и цитомегаловирусных заболеваний.
источник

Возбудитель – цитомегаловирус (ЦМВ) относится к семейству бета-герпесвирусов. ЦМВ отличается высоким тропизмом к клеткам слюнных желез и в локализованной форме находится только там. Цитомегаловирусная инфекция – хроническая персистирующая инфекция человека. После первичного инфицирования вирус переходит в латентное состояние и в большинстве случае себя клинически не проявляет. Развитие цитомегалии связано с потерей иммунного контроля над латентным состоянием ЦМВ. Инкубационный период составляет от 20 до 60 дней. Заболевания, обусловленные ЦМВ, регистрируются повсеместно. По данным серо-эпидемиологических исследований, 50-80% людей серопозитивны к данному вирусу. Источником заражения является человек с острой или латентной стадией заболевания. ЦМВ может находиться в слюне, отделяемом носоглотки, моче, семенной жидкости, секрете шейки матки. Пути передачи инфекции разнообразны: воздушно-капельный, контактно-бытовой, половой, транспланцентарный. У взрослых ЦМВ-инфекция встречается как сопутствующее заболевание при различных иммунодефицитных состояниях, а основными путями заражения являются: половой и парентеральный. К группам риска развития цитомегаловирусной инфекции относятся: беременные, недоношенные дети, доноры крови и органов, онкологические и гематологические больные, пациенты с различными иммунодефицитными состояниями, медицинские работники.
Различают несколько вариантов течения инфекции. Заболевание может протекать в субклинической, легкой, средней и тяжелой форме с токсикозом и летальным исходом. Выраженность симптоматики и тяжесть проявлений во многом зависят от иммунитета человека. Проявления приобретенной цитомегаловирусной инфекции у пациентов с нормальным иммунитетом может напоминать клинику простудных заболеваний. Чаще всего первичное инфицирование проявляется мононуклеозоподобным синдромом. Инкубационный период составляет 20-60 суток, продолжительность заболевания 2-6 недель. Как правило, отмечается лихорадка, слабость, явления интоксикации, увеличение лимфатических узлов, боли в мышцах. При достаточном иммунном ответе организм вырабатывает антитела против вируса и заболевание заканчивается самоизлечением. Выделение вирусов с биологическим жидкостями продолжается месяцы и годы после выздоровления. После первичного инфицирования цитомегаловирус может находится в организме десятки лет в неактивной форме или самопроизвольно исчезать из организма. В среднем у 90-95% взрослого населения обнаруживаются антитела класса G к ЦМВ. ЦМВ-инфекция у лиц с ослабленным иммунитетом. (пациенты с лимфопролиферативными заболеваниями, гемобластозами, ВИЧ-инфицированные, пациенты после трансплантации внутренних органов или костного мозга). У таких пациентов может происходить генерализация инфекции, поражаются печень, почки, легкие, сетчатка глаза, поджелудочная железа и другие органы.
Острые респираторные вирусные инфекции (ОРВИ) – пожалуй, самая обширная группа инфекций, передающихся воздушно-капельным путем и вызывающих респираторные проявления разной степени выраженности: от легкого насморка до бронхита или пневмонии. Вся группа объединена в собирательный термин в связи со схожестью клинической симптоматики. ОРВИ относят к отдельной группе респираторных инфекций, вызванных исключительно вирусами. ОРВИ болеет каждый человек, в среднем дети болеют ими от одного до пяти раз в год, взрослые от одного до двух раз в год. Известно около 250 видов вирусов, способных вызывать ОРВИ. Все они относятся к определенным группам: риновирусы, аденовирусы, коронавирусы, энтеровирусы, парвавирусы, парамиксовирусы, вирусы гриппа, вирусы парагриппа, респираторно-сентициальные вирусы, вирусы коксаки, другие респираторные вирусы. Заражение ОРВИ происходит воздушно-капельным путем. Частицы вируса передаются при кашле, разговоре, чихании. ОРВИ присуще сезонное течение, наиболее часто вспышки заболевания наблюдаются поздней осенью и ранней весной.
Для клиники ОРВИ характерно стадийное течение. Период инкубации от момента заражения до проявления первых признаков различный колеблется от нескольких часов до 3-7 суток. В период клинических проявлений все ОРВИ имеют сходные проявления той или иной степени выраженности. Клиническую картину ОРВИ составляют такие симптомы, как заложенность носа, насморк, выделения из носа (от скудных до обильных и водянистых), чихание и зуд в носу; першение в горле, дискомфорт или болезненность при глотании, краснота в горле, кашель (сухой или влажный), лихорадка – от умеренной (37,5-38?С) до выраженной (38,5-40?С). Также наблюдается общее недомогание, отказ от еды, головные боли, сонливость, покраснение глаз, жжение, слезотечение, нарушения пищеварения с послаблением стула. Иногда бывает реакция лимфоузлов в области челюсти и шеи, в виде увеличения со слабой болезненностью. Проявления ОРВИ зависят от конкретного вида вируса, и могут варьироваться от незначительного насморка и покашливания до выраженных лихорадочных и токсических проявлений. В среднем проявления длятся от 2-3 до семи и более дней, лихорадочный период длится до 2-3 дней.
ОРВИ характеризуется высокой заразностью для окружающих, сроки которой зависят от вида вируса. В среднем заразным пациент является последние дни инкубационного периода и первые 2-3 суток клинических проявлений, постепенно количество вирусов снижается и больной становится не опасным в плане распространения инфекции. В ряде случаев ОРВИ может протекать тяжело. Это может приводить к формированию таких осложнений как: острые синуситы (воспаление пазух носа с присоединением гнойной инфекции), развитие бронхитов и пневмоний, распространение инфекции на слуховую трубу с формированием отитов, присоединение вторичной бактериальной инфекции (например, развитие ангины), обострение очагов хронической инфекции как в бронхо-легочной системе, так и в других органах.
Выявление ЦМВ – инфекции базируется на трех методах:
1. Цитоскопическое исследование биологичских материалов (соскоб из уретры, моча, слюна и т.д.) – обнаружение специфичных для ЦМВ гигантских клеток («совиный глаз»).
2. Молекулярно-биологическая диагностика (ПЦР-диагностика) – основана на выявлении специфической вирусной ДНК – в настоящее время наиболее достоверный метод диагностики.
3. Иммуноферментный анализ (ИФА) – основан на выявлении специфических ЦМВ антител. При обнаружении только Ig M – острая фаза вирусного процесса, обнаружение Ig M и Ig G – свидетельствуют об обострении латентной формы инфекции, обнаружение только Ig G говорит о стихании клинических проявлений и переходе ЦМВ в латентное состояние.
Диагностика ОРВИ в остром периоде не представляет сложности – проявления типичны, иногда для исключения гнойной инфекции проводят бактериальный посев мазка из горла и носа. Дополнительных методов диагностики при неосложненных ОРВИ не проводится. В тяжелых эпизодах гриппа проводятся исследования для выявления специфического комплекса антиген—антитело, клеток крови с вирусом и т.д. В случае необходимости диагностики осложнений применяют рентген придаточных пазух носа или грудной клетки.
Основой лечения обоих инфекций является назначение противовирусной терапии. Лечение цитомегаловирусной инфекции является более сложной задачей. Терапия обычно проводится в условиях стационара. Специфического лечения и профилактики ЦМВ-инфекции нет. Рекомендуется комбинированная терапия противовирусными препаратами (ганцикловир, фоскарнет) и иммунными средствами (интерферонотерапия). В тяжелых случаях применяется посиндромальная терапия (в зависимости от вовлечения в инфекционный процесс внутренних органов).
При лечении ОРВИ необходимо соблюдать следующие правила: изоляция от других детей и взрослых, постельный режим, обильное потребление жидкости, питание по аппетиту (растительно-молочный стол). В качестве дополнительного лечения в комбинации с интерферонотерапией, назначаются симптоматические средства по показаниям: жаропонижающие средства при лихорадке выше 38,5-39?С и плохом самочувствии, препараты от насморка, антисептические и противовоспалительные средства для зева, противокашлевые, отхаркивающие и разжижающие мокроту средства. Базовой составляющей терапии ЦМВ-инфекции и ОРВИ представляется противовирусное лечение. В комплексной схеме может применяться препарат Виферон Суппозитории и Виферон Гель или Виферон Мазь. Сочетание основного действующего вещества в препарате – интерферона альфа-2b и высокоактивных антиоксидантов позволяет создать полноценную противоинфекционную защиту, улучшить собственный иммунный ответ на вирусы, повысить устойчивость организма к инфекциям.
Дерматовенеролог, аллерголог-иммунолог, член-корр. РАЕН, профессор, д.м.н., президент НП «Герпес-Форум», ведущий научный сотрудник МНПЦДВК ДЗМ, А.А. Халдин.
источник
Цитомегаловирус (другое название — ЦМВ-инфекция) – это болезнь инфекционного характера, которую относят к семейству герпесвирусов. Данный вирус поражает человека как внутриутробно, так и иными путями. Так, цитомегаловирус может передаваться половым, воздушно-капельным алиментарным путем.
Согласно существующим статистическим исследованием, антитела к цитомегаловирусу обнаруживают примерно у 10-15% подростков. Уже в возрасте 35 лет количество таких людей возрастает до 40%.
Цитомегаловирус ученые открыли в 1956 году. Особенностью этого вируса является его сродство с тканями слюнных желез. Поэтому если заболевание имеет локализованную форму, то обнаружить вирус можно исключительно в этих железах. Этот вирус присутствует в человеческом организме пожизненно. Однако цитомегаловирус не отличается высоким уровнем заразности. Как правило, для того чтобы заразиться вирусом, необходимы продолжительные и многократные контакты, тесное общение с носителем.
Сегодня выделяют три группы людей, контроль над активностью цитомегаловируса для которых является особо актуальным вопросом. Это беременные женщины, люди, у которых проявляется рецидивирующий герпес, а также пациенты, имеющие нарушенный иммунный ответ.
Человек может заразиться цитомегаловирусом разными способами. Так, заражение может произойти контактным путем, через использование зараженных вещей, в процессе пересадки органов, а также переливания крови от донора, ранее зараженного цитомегаловирусом. Заболевание передается, кроме того, при половых контактах, воздушно-капельным путем, во время беременности внутриутробно и в процессе родов. Вирус находится в крови, слюне, грудном молоке, сперме, выделениях из женских половых органов. Но вирус, который попадает в человеческий организм, нельзя распознать сразу же, ведь в данном случае длительность инкубационного периода составляет около 60 дней. В эти дни вирус может не проявляться вообще, однако по истечению инкубационного периода происходит резкое начало заболевания. Переохлаждение и последующее снижение иммунитета становятся факторами, провоцирующими цитомегаловирус. Симптомы заболевания проявляются и вследствие стресса.

При генерализованной форме цитомегаловируса происходит поражение ряда внутренних органов. Так, воспалительные процессы могут проходить в надпочечниках, селезенке, печеночной ткани, почках, поджелудочной железы, почек. В результате происходит частое проявление пневмоний, которые возникают якобы без причины, бронхитов, которые тяжело вылечить с помощью антибиотиков. Иммунный статус терпит изменения у людей с прогрессирующим цитомегаловирусом. Симптомы, которые описаны выше, дополняет соответствующая картина крови: так, в периферической крови снижается число тромбоцитов. Очень часто при данном недуге поражаются также стенки кишечника, сосуды глаза, периферические нервы и головной мозг. Возможны воспалительные процессы в суставах, сыпь на коже.
Если заболевание поражает органы мочеполовой системы, то у больного имеют место хронические неспецифические воспалительные процессы. В случае трудностей с установлением вирусной природы заболевания его очень сложно лечить с помощью антибиотиков.
Если вирус внедряется в организм, то в нем начинается перестройка иммунной системы. И после того, как острая фаза болезни закончилась, возможно проявление вегетативно-сосудистых расстройств и астенизации на протяжении длительного времени.
У людей с иммунодефицитом (у людей, перенесших химиотерапию, ВИЧ-инфицированных, а также у лиц, проходящих иммуносупрессивную терапию при пересадке органов) наличие цитомегаловируса может спровоцировать проявление очень тяжелых заболеваний. Поражения, которые проявляются у таких больных, могут стать причиной летального исхода.
После попадания этой инфекции в организм в нем начинают вырабатываться иммуноглобулины — антитела к цитомегаловирусу. Они приостанавливают развитие болезни, вследствие чего она протекает бессимптомно. В процессе лабораторного исследования крови можно выявить такие антитела. Однако однократная идентификация титра антител не позволяет различать инфекцию текущую от инфекции перенесенной. Ведь в организме носителя вируса и цитомегаловирус, и антитела присутствуют постоянно. При этом антитела не предупреждают инфицирование, и к цитомегаловирусу иммунитет не вырабатывается. В случае нерезультативной диагностики пациенту необходимо сдать анализы повторно по истечению нескольких недель.
Если у человека диагностирован цитомегаловирус, лечение болезни будет направлено на то, чтобы придушить все формы проявления заболевания и устранить неприятные симптомы. Ведь сегодня медики не располагают средством, уничтожающим вирус в человеческом организме полностью.
В случае если симптомы не проявляются у пациентов, у которых был диагностирован цитомегаловирус, лечение заболевания не требуется. Ведь это свидетельствует о нормальном иммунитете вирусоносителя.
При обнаружении вируса в крови в таком случае терапия подразумевает поддержку и укрепление иммунной системы. Следовательно, необходимо проводить иммуномодулирующее, а также общеукрепляющее лечение. Назначается также прием витаминных комплексов.
При лечении цитомегаловируса у детей и взрослых важно использовать комплексный подход к назначению терапии. Как правило, при лечении назначается прием средств с противовирусным и иммунным воздействием. При правильном подходе к лечению защитные силы организма активизируются, и активация латентной формы болезни в дальнейшем пребывает под контролем.

Лечение, направленное на поддержание иммунитета, включает в себя процедуры для укрепления и закаливания организма. Так, часто в данном случае рекомендуются банные процедуры, а тем, кто имеет определенную подготовку, можно периодически купаться в ледяной воде.
Существует много лекарственных трав, отвары которых стимулируют улучшение общего состояния организма. Подходит применение трав с желчегонным воздействием: шиповника, кукурузных рылец, бессмертника, тысячелистника. Можно полоскать рот слабым раствором йода.
Профилактика цитомегаловируса заключается главным образом в тщательном соблюдении правил как личной, так и половой гигиены. Важно соблюдать должную осторожность, контактируя с зараженными людьми. Наиболее тщательно следует соблюдать осторожность в период беременности: в данном случае нельзя допускать случайные половые связи. Еще один немаловажный момент в вопросе профилактики цитомегаловируса — поддержка иммунитета. Следует вести физически активную жизнь, правильно питаться, гулять на свежем чистом воздухе, принимать витамины, избегать стрессовых ситуаций. Детей нужно приучать к правильному образу жизни и гигиене с первых лет жизни.

Если заражение ребенка произошло на поздних сроках, то у новорожденного не наблюдается выраженных пороков, однако болезнь выражается выраженной желтухой, у ребенка увеличены селезенка и печень, возможны поражения легких и кишечника.
Если имеет место острое течение цитомегаловирусной инфекции, то у новорожденного присутствует ряд симптомов: вялость, плохой аппетит, может повышаться температура, ребенок плохо набирает вес, имеет неустойчивый стул. Возможны геморрагические высыпания на кожных покровах. Через определенное время вследствие плохого набора развивается анемия, гипотрофия. В целом отмечается очень тяжелое течение цитомегаловирусной инфекции, и в итоге часто заканчивается смертью ребенка в первый месяц жизни.
Если болезнь имеет хроническую форму или бессимптомное течение, то состояние ребенка остается удовлетворительным.
При приобретенной форме заболевания ребенок инфицируется в процессе родов, либо получает инфекцию уже в первые дни жизни во время контакта с носителем инфекции.
Возможны два варианта течения цитомегаловируса у детей в данном случае: либо изолированно поражаются слюнные железы, либо происходит поражение нескольких или одного органа. В качестве симптомов у ребенка проявляется высокая температура, увеличение лимфоузлов и на шее, и в других местах. Отекает слизистая глотки, увеличиваются миндалины, селезенка, печень. Ребенок отказывается есть, нарушается стул – проявляются запоры либо поносы. Проявляются поражения легких, ЖКТ, желтушность склер, дрожания конечностей. Возможен и сепсис, но эффект от терапии антибактериальными препаратами не проявляется. Течение болезни длительное, диагноз, как правило, установить трудно, ведь цитомегаловирус в крови и слюне иногда не обнаруживают.
Также при заражении ребенка цитомегаловирусом может проявляться цитомегаловирусный гепатит. Такие дети рождаются с тяжелым геморрагическим синдромом и рядом пороков развития, описанных выше. Очень часто течение болезни заканчивается летально.
Однако самые серьезные осложнения данного недуга проявляются у женщин, которые ожидают появления ребенка. Цитомегаловирус и беременность – достаточно опасное сочетание, ведь заражение этим заболеванием иногда приводит даже к преждевременным родам. Именно цитомегаловирус является одной из наиболее часто проявляемых причин прерывания беременности.
К тому же ребенок у больной матери может родиться с низкой массой тела, а также с серьезными поражениями легких, печени и центральной нервной системы. Цитомегаловирус и беременность – это риск того, что ребенок может вообще не выжить. Так, по разным подсчетам, от 12–30% таких новорожденных умирают. У детей, которые выжили, примерно в 90% случаев наблюдается ряд поздних осложнений: они могут терять слух, иногда присутствуют нарушения речи, атрофируются зрительные нервы.
Следовательно, очень важным шагом является обследование на наличие цитомегаловирусной инфекции в процессе планирования рождения ребенка. Если правильно подойти к применению как лечебных, так и профилактических мер, то негативное влияние цитомегаловируса на ход беременности и вероятность проявления патологий у ребенка можно предупредить.
источник
- антицитомегаловирусный иммуноглобулин
- врожденная инфекция
- врожденная цитомегаловирусная инфекция
- внутриутробная цитомегаловирусная инфекция
- вторичная цитомегаловирусная инфекция
- ганцикловир
- латентнаяцитомегаловирусная инфекция
- манифестнаяцитомегаловирусная инфекция
- первичная цитомегаловирусная инфекция
- субклиническая цитомегаловирусная инфекция
ВПР– врожденные пороки развития
ВУИ– внутриутробные инфекции
ЖКТ– желудочно-кишечный тракт
ЗВУР– задержка внутриутробного развития плода
ИГХ – иммуногистохимический анализ
ИФА – иммуноферментный анализ
ИЦХ – иммуноцитохимический анализ
ОРЗ– острое респираторное заболевание
ПЦР – полимеразная цепная реакция
ХЛИА –иммунохемилюминисцентного анализ
ЦМВИ – цитомегаловирусная инфекция
ЦНС – центральная нервная система
TORCH – Toxoplasma (токсоплазменная инфекция) — Rubella (краснуха) — Cytomegalovirus (цитомегаловирус) — Herpes (герпес)
БКМ – быстрый культуральный метод (Shellvialassay)
Ig (А, G, M) — иммуноглобулины группы (A, G, M)
Цитомегаловирусная инфекция – широко распространенная вирусная инфекция, характеризующаяся многообразными проявлениями от бессимптомного течения до тяжелых генерализованных форм с поражением внутренних органов и центральной нервной системы (у лиц с иммунодефицитом и при внутриутробном поражении плода)[1].
Врожденная цитомегаловирусная инфекция является результатом, как правило, трансплацентарнойпередачи возбудителя (при первичном заражении неиммунной беременной, реактивации ранее приобретенной инфекции во время беременности или при заражении иммунной беременной другим штаммомцитомегаловируса) от матери к плоду, реже – при заражении плода в интранатальном периоде (при наличии цитомегаловирусного поражения родовых путей).
В период новорожденности заболевание может протекать в манифестной и субклинической форме (последнее – чаще при заражении в интранатальном периоде) [5].
Иммуноглобулин человека нормальный [IgG+IgA+IgM] (Immunoglobulinum human umnormale) – представляет собой иммунологически активную белковую фракцию, содержащую широкий спектр антител, выделенную из плазмы крови человека, основным активным компонентом которой является иммуноглобулин G (Ig G), составляющий не менее 95 % общего белка и обладающий активностью антител различной специфичности против бактерий, вирусов и других возбудителей инфекционных заболеваний.
Препараты иммуноглобулина человека нормального не содержат консерванты и антибиотики.
Цитомегаловирусная инфекция (ЦМВИ) – инфекция, вызываемая возбудителем из группы бета-герпесвирусов, характеризующаяся многообразными проявлениями от бессимптомного до генерализованного течения с тяжелым поражением центральной нервной системы (ЦНС) и других органов.
ЦМВИ встречается повсеместно. Уровень пораженности населения этой инфекцией в большинстве стран мира колеблется от 50 до 90 % и значительно варьирует в различных популяциях даже в пределах одной страны в зависимости этнических и социально-экономических факторов.
В Российской Федерации частота серопозитивности составляет от 50% до 80%. Наибольший риск инфицирования плода цитомегаловирусом (ЦМВ) и развитие тяжелых форм заболевания отмечается в тех случаях, когда беременная переносит первичную ЦМВИ. Частота первичной ЦМВИ у женщин во время беременности не превышает 1%. Внутриутробное инфицирование плода ЦМВ у женщин с первичной ЦМВИ достигает 40-50%. При этом у 5-18% инфицированных детей развивается манифестная форма заболевания с тяжелым течением. Трансплацентарное инфицирование в 1 триместре приводит к порокам развития ЦНС, хориоретинитам, блокаде проводящих путей сердца. Инфицирование на более поздних сроках может приводить к развитию прогрессирующей желтухи, геморрагическому синдрому, гепатоспленомегалии, пневмонии. В дальнейшем у этих детей велика вероятность (90%) развития нарушений слуха, эпилепсии, задержки умственного и психомоторного развития, атрофии зрительного нерва, различных нарушений речи.
При вторичной инфекции в период беременности факторы специфического иммунитета у матери обеспечивают действенную защиту плода от инфицирования и развития тяжелых форм болезни. В результате риск внутриутробного инфицирования ЦМВ не превышает 2%.
Следует особо подчеркнуть, что дифференцировать реактивацию латентной ЦМВИ и суперинфекцию другим штаммом можно только с помощью молекулярного анализа выделенных изолятов.
При этом в отличие от других инфекций группы TORCH, тяжелые поражения плода при ЦМВИ могут развиваться в любом триместре беременности.
Примерно у 50 % детей с врожденной ЦМВИ наблюдаются анте- и постнатальные признаки заболевания: внутриутробная задержка развития, микроцефалия, гепатоспленомегалия, петехиальная экзантема, желтуха, хориоретинит, тромбоцитопения, анемия. До 30 % таких детей погибают в первые годы жизни (три четверти – в возрасте до 12 месяцев) на фоне нарастающей диссеминированной коагулопатии, печеночной недостаточности (первичный цирроз), вторичных бактериальных осложнений.
В 10–15 % случаев врожденной ЦМВИ, протекающей субклинически в период новорожденности, позднее развиваются клинически значимые проявления заболевания – задержка психомоторного развития, нейросенсорная глухота, нарушения функции зрения. [4;5;8].
Возбудитель ЦМВ инфекции относится к виду Cytomegalovirushominis, подцарствуDeoxyvira, классу Deoxicubika, порядку Haplovirales, семейству Herpesviridae(герпесвирус человека 5 типа), подсемейству Betahepresviridae, роду Cytomegalovirus. Зарегистрировано 4 штамма ЦМВ (АД169, Davis, Towne, Kerr), все они патогенны для человека.
Для поддержания в условиях лаборатории ЦМВ требует систематических пассажей в клеточных культурах (фибробластов гомологичных хозяев, диплоидных клеток из легких эмбриона человека).
Патогенез и патологическая анатомия
Вирус цитомегалии, поступивший в ранее неинфицированный организм, проникает внутрь клеток и начинает активно реплицироваться. Результатом репликации является формирование дочерних вирусных частиц, которые выходя из инфицированной клетки, «покрываются» внешней оболочкой. При этом внешняя оболочка вирионов образуется при участии клеточной мембраны поврежденной цитомегаловирусом клетки.
ЦМВ репродуцируется в лимфоцитах, моноцитах крови, персистирует в лимфоидных органах. Вирус имеет низкую вирулентность, выраженный тропизм к клеткам эпителия протоков слюнных желез, где медленно размножается без поражения клеток. Инфицирование слюнных желез ЦМВ происходит в результате трансэпителиальной миграции лимфоцитов и гистиоцитов. Пораженные ЦМВ клетки гипертрофируются, ядра в них увеличиваются в размерах. В результате этого инфицированные клетки приобретают типичные для цитомегалии признаки в виде «совиного глаза» – увеличенная в размерах клетка, в которой протоплазма из-за большого диаметра ядра визуализируется лишь в виде очень тонкой полоски.
После инфицирования ЦМВ присутствует в организме в латентной форме, в основном в мононуклеарных клетках периферической крови, периодически реактивируясь.
ЦМВ характеризуется значительным антигенным разнообразием. Поэтому при инфицировании серопозитивного человека другим штаммом ЦМВ формирование специфического иммунитета против данного возбудителя будет происходить, как и при первичном контакте. Следует отметить, что наработанные ранее типо- и группоспецифические антитела к другим штаммам ЦМВ будут сдерживать активную репликацию вируса. Однако действенная иммунная защита (достаточный уровень специфических анти-ЦМВ-АТ и специфических «клеток-киллеров») сформируется только к 14-28 дню от момента инфицирования данным штаммом вируса.
ЦМВИ является первичной в том случае, если инфицирование вирусом цитомегалии и развитие инфекционного процесса происходит у ранее серонегативного пациента.
Если серонегативная беременная женщина инфицируется вирусом цитомегалии, то из-за транзиторных особенностей иммунитета в этот период возможна более активная репликация ЦМВ, сопровождающаяся виремией.
Виремия, особенно при состояниях, приводящих к нарушению плацентарного барьера, способствует трансплацентарной передачи инфекции. Поступивший в организм плода вирус активно реплицируется и распространяется в организме, что обусловлено медленным нарастанием концентрации специфических Ig G (способных к трансплацентарному проникновению) в крови матери и незрелостью иммунитета плода.
Степень поражения плода при этом зависит от интенсивности размножения вируса и от периода гестации, в который происходит развитие инфекции. Соответственно, возможны как минимальные проявления заболевания (бессимптомные, субклинические формы), так и тяжелые поражения.
При вторичной инфекции (реактивации латентной ЦМВИ или реинфекцияновым штаммом ЦМВ) репликация ЦМВ происходит в условиях «иммунологического пресса», интенсивность вирусной репликации и степень виремии при этом существенно сдерживаются за счет наличия видо- и группоспецифических антител, что определяет значительно меньший риск передачи инфекции плоду, а также более легкое течение ЦМВИ у плода и новорожденного (плод одновременно с ЦМВ получает от серопозитивной матери и антитела, препятствующие репликации вируса и ограничивающие его распространение).
Патологические изменения при ЦМВИ могут иметь различную степень выраженности и носить локальный или диффузный характер. Гистопатологические изменения варьируют от фокальных паренхиматозных или перивентрикулярных некрозов до микроглиальных узелков (глиоза) и разбросанных клеток-цитомегалов. Некротические изменения на начальных стадиях сопровождаются воспалительной инфильтрацией, состоящей из циркулирующих мононуклеарныхклеток, главным образом моноцитов.
Тяжелые поражения ЦНС, обусловленные ранней вирусной диссеминацей, более часто возникают при инфицировании на ранних сроках беременности. Вероятной причиной является более высокая чувствительность нейронов, проходящих дифференцировку, к репликации ЦМВ на протяжении первого триместра гестации в отличие от уже дифференцированных нейронов, более устойчивых в эксперименте к инфицированию ЦМВ на поздних сроках беременности. [5].
Источником инфекции является человек, зараженный ЦМВ. После первичной инфекции выделение вируса из организма обычно продолжается несколько месяцев. При заражении в перинатальный период непрерывное выделение вируса продолжается 4-8 лет. Как у взрослых, так и у детей состояние латентной инфекции может прерываться периодическими рецидивами, во время которых вновь начинается выделение вируса.
У инфицированного человека вирус обнаруживается во внутренних органах, крови, ликворе, слюне, моче, влагалищном секрете, сперме, грудном молоке, слезной жидкости.
Основными механизмами заражения ЦМВ являются контактный и воздушно-капельный. Контактный механизм реализуется естественными и искусственными путями.
Естественные пути передачи возбудителя являются доминирующими. Заражение восприимчивого человека происходит при непосредственном контакте с источником инфекции (при поцелуях, половым путем) или опосредованно – через контаминированную вирусом посуду, зубные щетки, игрушки. Из-за низкой концентрации вируса в выделениях и лабильности возбудителя для передачи инфекции необходим длительный и близкий контакт.
Заражение плода реализуется при трансплацентарной передаче от матери к плоду, которая возможна в течение всей беременности. Особую опасность для плода представляет первичная ЦМВИ у беременных. При интранатальном заражении первые клинические проявления заболевания новорожденного могут манифестировать после 20 суток жизни (вплоть до 6 месяцев).
Частота случаев серонегативной беременности составляет от 10% до 30%. Реальная частота врожденной ЦМВИ среди новорожденных не превышает 0,2-2,5%, так как риск инфицирования плода, тяжесть и прогноз заболевания при врожденной ЦМВИ, зависит не столько от наличия вируса в организме, сколько от активности инфекционного процесса в период беременности.
При антенатальном инфицировании плода в подавляющем большинстве случаев имеет место трансплацентарный путь передачи ЦМВ.
При интранатальном инфицировавании вирус поступает в организм за счет аспирации, заглатывания инфицированных околоплодных вод или секретов родовых путей матери.
Новорожденный может быть заражен ЦМВ инфицированным молоком, что имеет особое значение для детей с экстремально низкой массой тела при рождении.
Инфицирование детей ЦМВ в родах или сразу после рождения обычно не ассоциируется с клинически выраженной болезнью, иначе реагируют недоношенные дети с ЭНМТ, у которых постнатальное инфицирование приводит к поражению дыхательных путей (пневмония, бронхиолит). В то же время даже при бессимптомном течении врожденной ЦМВИ у 5-17% детей в дальнейшем могут быть различные нарушения здоровья.
Искусственный путь реализуется при заражении ЦМВ реципиентов компонентов крови и органов. [2;5;8].
Р35.1 – врожденная цитомегаловирусная инфекция
Классификация острой врожденной ЦМВИ (клинические формы):
- манифестная форма (с указанием ведущих проявлений);
- субклиническая форма (с указанием способа верификации диагноза);
- осложнения [28].
Среди новорожденных с врожденной симптоматической ЦМВИ наблюдается высокая частота недоношенности (более 30%), ЗВУР в 50%, в половине случаев –микроцефалия, желтуха и гепатоспленомегалия-в 60–67%. Выявляются также, петехии, повышение аминотрансфераз, гипербилирубинемия, тромбоцитопения, неврологические отклонения(летаргия, судороги). Указанные признаки не являются патогномоничными!
Врожденная ЦМВИ, манифестная форма
Врожденная ЦМВИ, манифестная форма является результатом трансплацентарного заражения плода, как правило, при первичной ЦМВИ у беременной во втором-начале третьего триместров беременности. Наиболее тяжелым является «цитомегаловирусное заболевание с включениями», характеризующееся поражением костного мозга, печени, ЖКТ и нервной системы. Клинические симптомы: низкая масса при рождении, желтуха (гемолитическая и печеночная), гепатит, гепатоспленомегалия, геморрагический синдром (петехии, мелена и др.) как следствие тромбоцитопении и коагулопетии), пневмония, судороги, менингоэнцефалит, ВЖК, ПВЛ, интерстициальный нефрит, хориоретинит, кератоконьюнктивит.
В ликворе обнаруживается повышение белка и умеренный плеоцитоз, в моче –ЦМВ-клетки. При нейросонографии, компьютерной и магнитно-резонансной томографии мозга выявляют перивентрикулярные кальцификаты, вентрикуломегалию, микроцефалию. Наиболее частыми радиографическими отклонениями, формирующимися в дальнейшем, являются атипичный рисунок извилин коры в виделисэнцефалии или полимикрогирии, гипоплазия мозжечка, атрофия коры мозга и задержка миелинизации.
Летальность при манифестной форме составляет 10-20% [5;25].
Врожденная ЦМВИ, субклиническая форма
В этом случае клинические и инструментальные признаки заболевания у новорожденного отсутствуют, диагноз инфекционного заболевания устанавливается на основании лабораторных исследований (см. Диагностика врожденной ЦМВИ). Узначительной части таких детей (до 15 %) в течение первых 3-6 месяцев жизни постепенно начинают формироваться задержка психомоторного развития, нейросенсорная тугоухость, хориоретинит, дефекты зубов («поздние» проявления врожденной ЦМВИ). Снижение слуха (вплоть до глухоты) может прогрессировать в течение нескольких лет [17].
При ЦМВИ возможны следующие осложнения: микроцефалия, детский церебральный паралич, эпилепсия, атрофия зрительных нервов, задержка развития и низкий IQ, хронические гепатиты и циррозы печени, поражения почек (кистозные дисплазии, нефротический синдром), пневмосклероз.
Цитомегаловирус также поражает внутреннее ухо, приводя к глухоте примерно у 60% детей с симптомной неонатальной цитомегалией и у 6% инфицированных, не имеющих в неонатальном периоде какой-либо клинической симптоматики. Согласно Red Book (2015) около 25% всех потерь слуха обусловлено перенесенной внутриутробно цитомегалией. Вирус также может поражать зубы, вызывая аномалии прикуса, желтый цвет эмали зубов. [5; 28].
При сборе анамнеза рекомендовано обратить внимание на:
- отягощенный акушерский анамнез (выкидыши, мертворождения, невынашивание предыдущих беременностей, рождение детей с множественными пороками развития или умерших в раннем возрасте);
- аномалии течения настоящей беременности и родов (угроза прерывания беременности, многоводие, преждевременное отхождение вод, преждевременные роды, приращение плаценты, преждевременная отслойка плаценты);
- перенесенные матерью во время беременности инфекционные процессы, в том числе ОРВИ.
При осмотре новорожденного рекомендовано обратить внимание на наличие следующих признаков:
- рождение ребенка с признаками ЗВУР, ВПР;
- острая неонатальная гидроцефалия;
- кожные экзантемы при рождении;
- желтуха неясного генеза;
- неврологическая симптоматика, появляющаяся впервые через несколько дней после рождения;
- геморрагический синдром;
- гепатоспленомегалия.
2.3.1 Лабораторная диагностика врожденной ЦМВИ в антенатальном периоде
- Рекомендовано обследование беременной с целью выявления первичной ЦМВИ или реактивации латентной инфекции, или факта суперинфекции новым штаммом ЦМВ [2;13;21;22;30].
Уровень убедительности рекомендаций B (уровень достоверности доказательств-2а)
- Рекомендовано определение величины специфических антител классов Ig M и Ig G, величины авидности Ig G в сыворотке крови методами иммуноферментного (ИФА) или иммунохемилюминисцентного анализов (ХЛИА), выполняемых первично при постановке диагноза «беременность» [2; 27; 29;30;32].
Комментарии: Первичная ЦМВИ у беременной диагностируется на основании обнаружения сероконверсии (появление и нарастание специфических IgG). У беременной IgM сохраняются до 5 недель и/или в сочетании с низкоавидными (менее 30 %) IgG [23; 24; 30].
Уровень убедительности рекомендаций B (уровень достоверности доказательств-2а)
- Рекомендован контроль специфических антител IgG и IgM в динамике с интервалом в 4-6 недель.
Уровень убедительности рекомендаций С (уровень достоверности доказательств-3)
Комментарии: Реактивация латентной ЦМВИ или суперинфекция новым штаммом ЦМВ диагностируется в случае выявления 4-хкратного нарастания величины специфических IgG с авидностью более 60 %, независимо от наличия/отсутствия специфических IgM методами ИФА/ХЛИА [23; 24; 27; 30].
- Рекомендуется проводить скрининговые обследования на наличие ЦМВ антител всем беременным, при постановке на учет в женскую консультацию [30].
Уровень убедительности рекомендаций С (уровень достоверности доказательств-3)
- Рекомендовано повторное проведение исследований через 3-4 недели для подтверждения сероконверсии у женщин с симптомами первичной инфекции [7; 10; 23; 24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств-3)
- Рекомендовано проведение обследования на наличие ЦМВ антител у беременных из групп риска:
- перенесших (особенно, в первой половине беременности) ОРЗ-подобное заболевание с незначительными катаральными проявлениями, в сочетании с лимфаденопатией, гепатолиенальным синдромом [10; 12; 16; 18;24];
Уровень убедительности рекомендаций С (уровень достоверности доказательств-3)
- в возрасте младше 20 лет [7; 23; 24];
Уровень убедительности рекомендаций С (уровень достоверности доказательств-3)
- в периферической крови которых выявлены атипичные мононуклеары [11; 24; 26];
Уровень убедительности рекомендаций С (уровень достоверности доказательств-3)
- работающих в организованных детских коллективах (детский сад, школа), а также беременных, чьи дети посещают эти коллективы [18;24; 26].
Уровень убедительности рекомендаций С (уровень достоверности доказательств-3)
2.3.2.Лабораторная диагностика в постнатальном периоде
- Рекомендован необходимый минимум первичных исследований для этиологической верификации заболевания при подозрении на врожденную ЦМВИ у новорожденных:
- исследование сыворотки крови (слюны, мочи, ликвора) новорожденного (и матери, субстрат – сыворотка крови) одновременно количественно на Ig M и Ig G к ЦМВ методом ИФА (или ХЛИА) с указанием пороговых значений чувствительности по данной тест-системе (для Ig G – в МЕ/мл, для Ig M – в условных единицах, в виде коэффициента позитивности или величин оптической плотности исследуемого образца и положительной контрольной сыворотки) [2;24;25;28].
Уровень убедительности рекомендаций C (уровень достоверности доказательств –3)
- ПЦР (кровь, моча, слюна, ликвор) – качественный и количественный анализ с определением числа копий вируса [6;9;11;12; 17;26].
Уровень убедительности рекомендаций А (уровень достоверности доказательств –1а)
- быстрый культуральный метод – БКМ (Shell vial assay) [2;27;28].
Уровень убедительности рекомендаций В (уровень достоверности доказательств –2а)
- Для этиологической верификации рекомендовано использовать определение авидности Ig G ПЦР (кровь, лейкоконцентрат, моча, слюна, ликвор) ИЦХ с использованием моноклональных сывороток (кровь, ликвор) [6;17;23;27;28].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3)
Первичное обследование выполняется в максимально ранние сроки жизни (в родильном доме). При переводе новорожденного в отделение патологии новорожденных (детской больницы, перинатального центра и др.) результаты исследований, выполненных в родильном доме, вносятся в переводной эпикриз с обязательным указанием даты забора биологических образцов, порогов чувствительности тест-систем и контактной информации лабораторий, проводивших исследование.
2.3.3 Критерии диагностики врожденной ЦМВИ
Диагноз «Врожденная острая ЦМВИ, манифестная форма» устанавливается новорожденному при наличии клинических проявлений заболевания, и этиологической верификации одним из следующих рекомендованных способов:
- Обнаружение специфических Ig M (выявленных дважды с интервалом между исследованиями 5 — 7 суток методами ИФА или ХЛИА) [24;26;27;28].
Уровень убедительности рекомендаций С (уровень достоверности доказательств –3)
- Положительной ПЦР или выявлении антигенов ЦМВ методом ИЦХ в заведомо стерильных субстратах (кровь, ликвор) [6;15;24;26;28].
Уровень убедительности рекомендаций В (уровень достоверности доказательств –2а)
- Идентификации ЦМВ вирусологическим методом в заведомо стерильных образцах – БКМ [15;27;28].
Уровень убедительности рекомендаций В (уровень достоверности доказательств –2а)
- Отсутствием снижения величины специфических Ig G в сыворотке крови ребенка при их определении в возрасте 6 недель (в сравнении с исходным уровнем величина снижается менее, чем на 40%) [23;24;27;28].
Уровень убедительности рекомендаций С (уровень достоверности доказательств –2а)
- Сероконверсии (появлении и нарастании специфических Ig M или Ig G) при условии выполнения исследования в одной и той же лаборатории, одним и тем же методом [23;27;28].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2а)
Диагноз «Врожденная острая ЦМВИ, субклиническая форма» устанавливается ребенку первого года жизни при отсутствии клинических проявлений заболевания в период новорожденности, и этиологической верификации одним из способов, перечисленных для манифестной формы врожденной острой ЦМВИ.
Диагноз «Врожденная ЦМВИ» не может быть установлен на основании однократного выявления у ребенка первого года жизни специфических Ig G любой авидности.
Врожденный характер заболевания может быть подтвержден путем выделения вируса из глоточного мазка или пробы мочи, взятых в течение первых 3 недель жизни новорожденного (на монослойных культурах фибробластов эмбриона человека или диплоидных культур клеток легких человека с последующим микроскопическим определением цитопатогенного действия вируса), либо путем выявления генетического материала ЦМВ (в ПЦР), его антигенов (в ИЦХ) в заведомо стерильных субстратах (оптимально – со 2-х по 7-е сутки жизни).
- При наличии у беременной лабораторных признаков первичной (обострения латентной, суперинфекции) ЦМВИ рекомендуется исследование амниотической жидкости, полученной при амниоцентезе методом ПЦР или вирусологическим методом (культивирование ЦМВ) [3;21;22;]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3)
Комментарии: Исследование выполняется не ранее 7 недель от предполагаемого времени начала заболевания/обострения/суперинфекции и не ранее 21-й недели гестации.
- Не рекомендуется кордоцентез [23; 26; 27].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2а)
Комментарии: Кордоцентез не имеет диагностических преимуществ перед амниоцентезом для диагностики врожденной ЦМВИ.
3.1.1 Антенатальная терапия
- При отсутствии возможности выполнения амниоцентеза беременной рекомендуется проведение этиотропной терапии ЦМВИ [19;20;21;22;24].
Уровень убедительности рекомендаций C (уровень достоверности доказательств –3)
- Для антенатальной терапии врожденной ЦМВИ рекомендуется использовать Иммуноглобулин человека антицитомегаловирусный.
Уровень убедительности рекомендаций В (уровень достоверности доказательств –2а)
Комментарии: в дозе 200 МЕ/кг/сут внутривенно в течение 3 дней – нивелирует УЗ-маркеры заболевания, а также способствует элиминации вируса к возрасту 6 месяцев по данным лабораторного обследования [7;25;31].
3.1.2 Постнатальная терапия
Лечение новорожденных с манифестной формой острой врожденной ЦМВИ проводится в стационарных условиях.
Ребенок должен быть переведен в отделение патологии новорожденных (детской многопрофильной больницы, регионального перинатального центра – в зависимости от принятой в регионе практики) в максимально возможные ранние сроки.
Лечение на амбулаторном этапе проводится специалистами поликлиники (врач-педиатр, врач-инфекционист – обязательно, другие специалисты – при наличии показаний) с учетом установленного окончательного диагноза, рекомендаций родильного дома, специалистов отделения патологии новорожденных, сформулированных в соответствующих выписках, а так же специалистов перинатальных центров или других учреждений, определенных локальными руководящими документами, осуществляющих полноценное обследование и лечение детей, больных врожденными инфекциями).
Рекомендации по организации питания и режиму определяются наличием и степенью выраженности нарушений со стороны органов и систем.
Этиотропная терапия в постнатальном периоде
Для терапии врожденной ЦМВИ рекомендуются следующие противовирусные препараты:
- Иммуноглобулин человека антицитомегаловирусный рекомендован в качестве препарата 1-го выбора, как безопасный и достаточно эффективный метод лечения при субклинической форме врожденной ЦМВИ [25;26;31].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2а)
Комментарии: 1 мл антицитомегаловирусного иммуноглобулина человека содержит 100 МЕ нейтрализующей активности внутривенно в дозе 1 мл/кг массы тела через 1 день или 4 мл/кг каждые 4 дня до обратного развития симптомов заболевания. Обычный курс не менее 6 введений.
- Валганцикловир** рекомендован в качестве препарата резерва новорожденным при врожденной ЦМВИ [25;26;31].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2а)
Комментарии: Нейтропения развивается у 34% больных, леченных ганцикловиром** и у 20%, получавших валганцикловир**.
Валганцикловир** назначается энтерально, внутрь16 мг/кг 2 раза в сутки в течении 6 месяцев. При невозможности назначить внутрь Валганцикловир**, внутривенно назначают ганцикловир**.
- Ганцикловир** рекомендован лишь при жизнеугрожающем течении болезни у новорожденных, который ингибирует ДНК-полимеразу ЦМВ и тем самым его репликацию [25;26;31].
Уровень убедительности рекомендаций В (уровень достоверности доказательств –2а)
Комментарии: Вводят внутривенно медленно в течении 1 часа 6 мг/кг (разовая доза) 2 раза в день. Курс 14-21 день, затем при необходимости продолжения терапии, переходят на прием внутрь 6 мг/кг в сутки. Препарат токсичен, вызывает миелотоксический эффект с развитием тяжелой нейтропении, тромбоцитопении, обладает тератогенной, мутагенной и канцерогенной активностью.
- Иммуноглобулин человека нормальный** [IgG+IgA+IgM] рекомендован в качестве препарата резерва [14].
Уровень убедительности рекомендаций В (уровень достоверности доказательств –2а)
Комментарии: Эффективность препарата обусловлена не только содержанием в нем антител к ЦМВ 15-20 МЕ/мл, но и тем, что ЦМВ, угнетая иммунитет, способствует развитию на фоне ЦМВИ тяжелых бактериальных инфекций.
- Интерферон альфа-2b# рекомендован в комплексной терапии врожденной ЦМВИ с высокоактивными антиоксидантами (суппозитории) в качестве препарата резерва [14].
Уровень убедительности рекомендаций В (уровень достоверности доказательств –2а)
Комментарии: препарат рекомендован в качестве иммуномодулирующего противовирусного средства в комплексной терапии ЦМВИ новорожденным:
>34 недель по 150 000 МЕ 2 раза/сутки курсом 5 суток. Рекомендованы 2-5 курсов терапии с интервалом между курсами в 5 суток;
источник