Вирусные гепатиты – тяжелые заболевания печени, лечение которых требует много времени и сил. При этом терапевтический эффект во многом зависит от того, на какой стадии была диагностирована данная болезнь. Раннюю диагностику может обеспечить анализ на маркеры гепатитов.
Особенность гепатита С и В заключается в том, что ранние стадии развития инфекции не имеют характерных симптомов, и когда пациент обращается в клинику с жалобами, его печень сильно поражена и ее функции нарушены. Избежать такого развития поможет ранняя диагностика.
Маркеры являются специфическими антигенами и антителами к этим заболеваниям. Выявление специфических антител в кровяной сыворотке может подтвердить наличие у человека того или иного типа гепатита. Важная особенность состоит в том, что маркеры выявляются даже на раннем этапе заболевания при отсутствии симптомов.
Для выявления специфических и серологических маркеров к гепатитам используют несколько видов исследования.
- Диагностика, основанная на иммунологических методах исследования.
- С помощью реакции иммунитета на вирусы.
- С помощью специализированного скринингового исследования.
- Путем проведения иммуноферментного анализа.
В зависимости от методов и цели диагностики выполняют 2 вида анализов на маркеры гепатита:
В ходе такого исследования удается определить тип вируса, который стал причиной болезни. Специфическими маркерами являются антигены гепатитов.
Антиген представляет собой отдельные элементы вируса. При попадании в благоприятную среду эти антигены участвуют в продуцировании новых клеток вируса. Незадействованные фрагменты разносятся по организму током крови.
К этому типу маркеров относят антитела к существующим антигенам. Этот способ диагностики становится возможным благодаря особенности человеческого организма вырабатывать антитела (клетки, направленные на борьбу с возбудителями болезней). Выявление таких антител к антигенам гепатита свидетельствует о наличии патологических процессов в тканях печени.
В случае заражения гепатитом В у людей в организме присутствуют несколько маркеров:
- антигены гепатита – к таким относятся HBeAg и HBsAg;
- антитела к антигенам – в эту группу включают анти-HBs, анти-HBe, анти-HBc.
По результатам проведенного иммуноферментного анализа врачи могут не только выявить тип гепатита, но и определить его стадию. Благодаря этому появляется возможность прогнозировать развитие болезни и выбирать наиболее эффективное лечение.
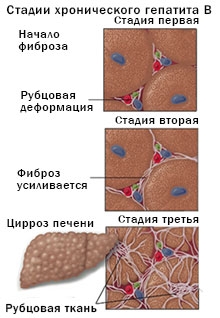
Если в крови присутствуют сразу 2 антигена (HBsAg и HBeAg), то это свидетельствует о наличии воспалительных процессов в тканях печени.
Данный маркер репликации вируса начинает распространяться в организме с момента проникновения инфекции в организм. Его выявление у пациента в крови свидетельствует о высокой концентрации вируса. На этот период приходится активное распространение болезни. Подтверждением этого факта становятся некоторые симптомы, например желтый оттенок кожных покровов.
Обнаружение HBeAg в крови спустя 4 и более недели после заражения является признаком перехода болезни в хроническое течение.
Особенностью данного антигена является высокая иммуногенность. По этой причине антитела к нему начинают вырабатываться в числе первых. Таким образом, диагностировать гепатит по наличию антител можно уже спустя 3-5 недель после заражения. При этом выраженные симптомы на этой стадии отсутствуют.
Суммарные маркеры анти-HBc являются антителами, активно вырабатываемыми организмом для эффективной борьбы с вирусами. Обнаружить эти маркеры можно после окончания острой стадии болезни. Сохраняться в организме они могут на протяжении 10 лет после заражения. Иными словами, обнаружение в крови антител в некоторых случаях свидетельствует лишь о ранее перенесенной болезни.
Такой тип маркера представляет собой антитела к антигену HBcAg. Они возникают в начале болезни, поэтому их наличие в крови – показатель острого течения данного заболевания. К этому моменту у большинства пациентов еще отсутствуют симптомы. Длительность пребывания антител в сыворотке достигает 5-6 месяцев. Спустя этот промежуток времени Анти-HBc IgM исчезают.
Положительный анти-HBe регистрируется в организме в период активного развития вируса. Это помогает более точно определить стадию болезни. Чаще всего для этой цели изучают показатели анти-HBe совместно с данными о маркере HBeAg.
Маркер анти-HBs относится к антителам, которые обнаруживаются уже после прохождения острой стадии болезни. Их наличие в крови говорит об активном противостоянии иммунной системы и защите организма от вируса. Этот тип маркера может присутствовать в крови пациентов спустя 10 лет с момента заражения.
Результаты анализов содержат в себе данные о присутствии или отсутствии маркеров в крови. При этом разные сочетания свидетельствуют о разных диагнозах. Более детально разобраться в референсных значениях поможет таблица с расшифровкой.
| Интерпретация результата | HBsAg | HBeAg | Анти-HBc IgM | Анти-HBc | Сумм анти-HBe | Анти-HBs | HBV-ДНК |
| Острая фаза заболевания. Дикий штамм. | + | + | + | + | — | — | + |
| Острая инфекция. Мутантный штамм. | + | — | + | + | — | — | + |
| Острый разрешившийся вирус. Сероконверсия. | + | — | -/+ | + | + | — | -/+ |
| Активный хронический тип течения | + | + | -/+ | + | -/+ | — | + |
| Интегративное хроническое течение | +/- | -/+ | -/+ | + | -/+ | — | -/+ |
| Признак «здорового» носительства | + | — | — | + | — | -/+ | — |
| Ранее перенесенная инфекция | — | — | — | + | -/+ | + | — |
| Перенесенная инфекция при отсутствии иммунного ответа Хроническая латентная инфекция Разрешение острой инфекции | — | — | — | + | -/+ | — | — |
| Состояние, наступающее после иммунизации | — | — | — | — | — | + | — |
Такая статистика обусловлена длительным инкубационным периодом болезни, отсутствием симптомов или их слабым проявлением. Повышение температуры и хроническая усталость часто принимаются за симптомы других заболеваний. Единственным эффективным способом диагностики в таких случаях является анализ на маркеры.
Существует несколько маркеров, позволяющих выявить наличие гепатита С в организме:
- HCV-RNA. РНК (рибонуклеиновая кислота) вируса обнаруживается в крови или тканях печени в тех случаях, когда болезнь находится в стадии активного развития. Присутствие такого маркера будет выявлено с самого начала заболевания.
- Anti-HCV total (или суммарные антитела). Иммуноглобулины такого типа появляются в организме спустя около 6 недель после заражения. Их выявление свидетельствует о наличии вируса в теле пациента. При этом такие маркеры могут присутствовать в крови даже после излечения.
- Anti-HCV core IgG. Обнаружить данные тела можно несколько позже (начиная с 11 недели). Anti-HCV core IgG относят к антителам класса G. Присутствие таких маркеров характерно для больных с хроническим течением гепатита.
- Anti-NS3. Маркер этого вида сопутствует гепатиту С острой формы.
- Маркеры anti-NS4 и anti-NS5 часто обнаруживаются в тех случаях, когда инфекция находится на поздних стадиях развития с поражением тканей печени. После полного излечения их количество сокращается.
Положительный или отрицательный результат на гепатит С можно выявить с помощью таблицы:
| Возможные диагнозы | Анти-HCV IgM | Анти-HCV IgG | Анти-NS4 | РНК HCV |
| Острое течение гепатита С | +/- | +/- | — | + |
| Острое течение – реконвалесценция | — | + | — | — |
| Хроническое течение гепатита С | +/- | + | + | + |
| Хроническое течение гепатита С при отсутствии репликации | — | + | + | — |
Гепатит А представляет собой заболевание печени с острой формой течения. Способов передачи существует несколько, наиболее частая причина заражения – несоблюдение правил гигиены. Среди характерных симптомов:
- желтуха;
- нарушение работы печени;
- повышенная температура тела;
- болевые ощущения в суставах;
- слабость и тошнота.
Данный вид гепатита характеризуется быстротечностью, отсутствием тяжелых последствий и простым лечением.
При лабораторном исследовании выявляется несколько маркеров:
- РНК вируса. Является признаком наличия инфекции в организме и ее стремительного распространения.
- Ag. Маркер является показателем наличия вируса.
- Анти-ВГА IgG. Обнаружение такого антитела свидетельствует о перенесенном заболевании и наличии иммунитета к гепатиту А.
- Анти-ВГА IgM. Показатель характеризует острую форму заболевания.
Гепатит Е широко распространен в жарких странах. Причиной заражения является антисанитария. Эта форма гепатита легко передается через грязную воду, продукты питания. Основными симптомами являются:
- расстройство пищеварительного тракта;
- болевые ощущения в правом подреберье.
Течение болезни характеризуется как тяжелое с высоким процентом смертности. Диагностировать гепатит Е можно с помощью выявления следующих маркеров.
- РНК вируса. Наличие такого антигена – признак активного распространения вируса в организме.
- Ag. Маркер подтверждает наличие гепатита Е в крови пациента.
- Анти-ВГЕ IgM. Антитела этого типа присутствуют во время острого течения болезни.
- Анти-ВГЕ IgG. Если в крови найден такой маркер, значит, человек ранее уже болел гепатитом Е и организм выработал иммунитет к вирусу.
Вирус гепатита D относится к антропонозным инфекциям. Заражение происходит посредством любых жидкостей зараженного человека, однако ему подвержены лишь те, кто болен гепатитом B. Симптомы этих заболеваний во многом похожи, однако вирус типа D часто вызывает асцит и отеки. Анализы назначают в первую очередь пациентам с гепатитом В и тем, кто принимает наркотические средства.
Выявить болезнь можно по антигенам и антителам к ним:
- РНК данного вируса. Этот маркер присутствует в организме в период активного распространения инфекции.
- Анти-ВГД IgM появляется в период острого течения.
- HDAg. Наличие антигена в крови подтверждает заражение.
- Анти-ВГД IgG. Человек уже перенес болезнь в прошлом, и теперь у него есть иммунитет к данному типу вируса.
Вирус гепатита G распространяется половым путем и через многократное использование одноразовых шприцев. Реже передача вируса происходит при иглоукалывании или пирсинге. Как и тип D, этот вид болезни может возникнуть лишь у людей с наличием гепатита C, B или D. Длительное отсутствие симптомов приводит к хроническому течению и повышает риск развития цирроза печени.
Ранняя диагностика возможна путем исследования крови для обнаружения маркеров:
- РНК вируса. В этом случае ставят диагноз острого течения гепатита G.
- Анти-ВГG. Признак того, что пациент перенес гепатит и теперь в организме у него есть иммунитет к этому заболеванию.
Для получения максимально точных результатов исследования пациенту нужно правильно подготовиться к процедуре забора крови:
- За неделю до исследования исключают прием всех противовирусных лекарственных средств.
- За двое суток до сдачи крови желательно отказаться от тяжелых физических нагрузок. Важно также перейти на диетическое питание. Для этого исключают из рациона острые, копченые, жирные, жареные блюда.
- В день сдачи анализов с утра не завтракают – кровь нужно сдавать натощак.
После процедуры остается лишь ждать результаты.
источник
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
В ирусные гепатиты — группа острых инфекционных заболеваний человека, которые вызываются различными гепатотропными вирусами, имеют разнообразные механизмы передачи и разные исходы. Эти заболевания объединяет то, что все они протекают циклически и центральное место в клинической картине занимает поражение печени. В настоящее время известно 7 вирусов, являющихся причиной их развития. Гепатиты А и Е относятся к энтеральным гепатитам с фекально-оральным механизмом передачи инфекции. Гепатиты В, С и D образуют группу парентеральных гепатитов. В последние годы идентифицированы вирусы G и TTV, передающиеся парентеральным путем, которые также способны вызывать поражение печени. Кроме того, существует группа неуточненных вирусных гепатитов, при которых пока не удается идентифицировать ни один из известных вирусов. Термин “вирусный гепатит” имеет самостоятельное нозологическое значение и не должен смешиваться с гепатитами, вызываемыми вирусами желтой лихорадки, инфекционного мононуклеоза, цитомегалии, герпеса и др.
Вирусные гепатиты являются одной из сложнейших общемедицинских проблем, поскольку имеют широкое распространение и серьезные исходы. Так, часто после перенесенной острой формы болезни формируется хронический гепатит (особенно при гепатите С), в последующем возможно развитие цирроза печени; доказана также этиологическая связь между первичной гепатоцеллюлярной карциномой и вирусами гепатитов В и С. Кроме того, несмотря на использование современных методов лечения, практически не удается предотвратить летальные исходы при развитии острой дистрофии печени. Учитывая это, а также значительный рост заболеваемости парентеральными вирусными гепатитами в последние годы в России, проблема вирусных гепатитов выступает на первый план.
Вирус гепатита А (ГА) относится к семейству Picornaviridae, содержит РНК, имеет 7 генотипов. Вирус распространен повсеместно, устойчив во внешней среде, поэтому может длительно сохраняться в воде, пищевых продуктах, сточных водах и др.
Эпидемиология и патогенез
ГА является антропонозом, единственный источник инфекции — человек. Механизм передачи инфекции — фекально-оральный. Пути передачи — алиментарный и контактно-бытовой. Возбудитель выделяется из организма человека с фекалиями, при этом экскреция вируса и соответственно риска заражения максимальны в преджелтушном периоде. Факторами передачи являются вода, термически не обработанные пищевые продукты, грязные руки. При ГА присутствие вируса в крови непродолжительно, поэтому передача вируса с кровью и половым путем происходит крайне редко. Чаще ГА болеют дети (около 80% заболевших). После перенесенного заболевания остается пожизненный иммунитет.
Развитие болезни начинается после попадания вируса через рот в желудочно-кишечный тракт, оттуда через кровеносную систему возбудитель попадает в печень, где происходит репликация вируса. В дальнейшем через желчевыделительную систему вирус оказывается в просвете кишечника и выводится с фекалиями. Гепатоциты повреждаются не за счет прямого цитопатического действия вируса, а в результате иммунопатологических механизмов, им запускаемых. Активация всех звеньев иммунной системы приводит к быстрому накоплению противовирусных антител, которые способствуют прекращению репликации вируса, что в конечном итоге приводит к очищению организма от вируса. Адекватный иммунный ответ обеспечивает сравнительно легкое течение болезни и полное выздоровление в подавляющем большинстве случаев.
ГА обычно имеет острое циклическое течение. Инкубационный период составляет от 7 до 50 дней (чаще 15—30 дней).
Преджелтушный период начинается остро, характерно повышение температуры тела до 38—39°С, головная боль, общее недомогание, слабость, ломота в мышцах и костях. Снижается аппетит, появляется тошнота, рвота, горечь во рту, чувство тяжести в правом подреберье и эпигастрии. Стул может быть учащенным, но чаще отмечается запор. Через несколько дней от начала болезни увеличивается печень, иногда селезенка. В сыворотке крови повышается активность аминотрансфераз (АЛТ и ACT). К концу преджелтушного периода, продолжительность которого обычно составляет 5—7 дней (с колебаниями от 2 до 14 дней), моча становится темной, в ней повышается количество уробилина и появляются желчные пигменты; кал нередко обесцвечивается.
Присоединяется желтушность склер, свидетельствуя о наступлении следующего — желтушного — периода. В 2—5% случаев желтуха является первым симптомом ГА. Обычно с появлением желтухи самочувствие больных улучшается, нормализуется температура тела. Интенсивность желтухи нарастает в течение 2—5 дней, в последующие 5—10 дней сохраняется на том же уровне, а затем уменьшается. Средняя продолжительность желтушного периода составляет около 2 нед. На высоте желтухи характерна брадикардия. В сыворотке крови определяется гипербилирубинемия за счет преобладания прямой фракции билирубина, гиперферментемия, характерно значительное повышение показателя тимоловой пробы. В фазу обратного развития желтухи светлеет моча, кал приобретает нормальную окраску, исчезает желтушное окрашивание кожи.
В подавляющем большинстве случаев выздоровление наступает через 1—1,5 мес от начала клинических проявлений заболевания. Желтушный вариант ГА чаще всего протекает в легкой или среднетяжелой форме. Тяжелая форма встречается не более чем у 1% больных, преимущественно у лиц старше 40 лет, у пациентов с хронической инфекцией вирусами гепатита В и/или С. Развитие острой печеночной недостаточности с энцефалопатией при ГА встречается очень редко, в этом случае диагноз формулируется, как гепатит А с печеночной комой. Изредка ГА протекает с холестатическим синдромом.
Безжелтушный вариант ГА характеризуется теми же клиническими (кроме желтухи) и биохимическими (кроме гипербилирубинемии) признаками, что и желтушный, однако выраженность их обычно меньше. Субклинический (инаппарантный) вариант в отличие от безжелтушного не сопровождается ни нарушением самочувствия, ни увеличением печени, ни появлением желтухи. Выявляется в эпидемических очагах по повышению активности АЛТ и ACT и наличию специфических маркеров ГА в сыворотке крови.
| Инкубационный период ОГВ без d-агента составляет от 6 нед до 6 мес (обычно 2-4 мес). |
Диагноз ГА устанавливается на основании эпидемиологических, клинических и лабораторных данных. Специфическим маркером ГА являются антитела к вирусу гепатита А класса М (анти-ВГА IgM), выявляемые с помощью иммуноферментного анализа (ИФА) в сыворотке крови с первых дней болезни и далее в течение 3—6 мес. Анти-ВГА IgM вырабатываются у всех больных ГА независимо от клинического варианта и формы тяжести. Обнаружение их — ранний надежный тест, позволяющий не только подтвердить клинический диагноз, но и выявить безжелтушный и субклинический варианты ГА, диагностировать ГА в преджелтушном периоде. Благодаря бурному развитию молекулярно-биологических методов исследования стало возможным определение специфических вирусных нуклеиновых кислот, в частности, РНК ВГА (см. таблицу).
Диагноз ГА устанавливается на основании эпидемиологических, клинических и лабораторных данных. Специфическим маркером ГА являются антитела к вирусу гепатита А класса М (анти-ВГА IgM), выявляемые с помощью иммуноферментного анализа (ИФА) в сыворотке крови с первых дней болезни и далее в течение 3—6 мес. Анти-ВГА IgM вырабатываются у всех больных ГА независимо от клинического варианта и формы тяжести. Обнаружение их — ранний надежный тест, позволяющий не только подтвердить клинический диагноз, но и выявить безжелтушный и субклинический варианты ГА, диагностировать ГА в преджелтушном периоде. Благодаря бурному развитию молекулярно-биологических методов исследования стало возможным определение специфических вирусных нуклеиновых кислот, в частности, РНК ВГА (см. таблицу).
Лечение ГА осуществляется с применением базисной терапии, включающей диету (стол № 5) и щадящий режим. Противовирусные препараты не используются. Самостоятельно вирус гепатита А не вызывает хронического гепатита. В некоторых случаях в периоде реконвалесценции ГА наблюдается манифестация синдрома Жильбера. После перенесенного ГА возможно поражение желчевыводящих путей дискинетического или воспалительного характера.
Профилактика ГА состоит прежде всего в улучшении санитарно-гигиенических условий жизни населения. В качестве пассивной иммунизации используется иммуноглобулин, однако он не способен предотвратить развитие субклинической инфекции. Для создания стойкого активного иммунитета применяют инактивированные вакцины.
Вирус гепатита Е (ГЕ) относится к семейству Caliciviridae, по последним данным, вирус является прототипом для нового семейства вместе с вирусом краснухи и некоторыми a-подобными вирусами растений. Геном вируса ГЕ содержит РНК.
ГЕ характеризуется выраженной неравномерностью распространения. Вспышки ГЕ регистрируются в Индии, Непале, Пакистане, Китае, Индонезии, ряде стран Африки и Латинской Америки. На территории бывших среднеазиатских республик СССР существуют стойкие очаги ГЕ. В Москве ГЕ встречается редко, в виде завозных случаев (около 3% всех заболевших вирусными гепатитами – приезжие из Средней Азии).
ГЕ так же, как и ГА, относится к группе кишечных инфекций. ГЕ имеет фекально-оральный механизм передачи инфекции, отличается от ГА водным путем распространения и тяжелым течением у беременных (преимущественно во второй половине беременности или в раннем послеродовом периоде). Летальность в целом от ГЕ составляет около 0,4%, среди беременных женщин достигает 20—40%.
Клинические и биохимические признаки ГЕ сходны с таковыми при ГА. Специфическим маркером, подтверждающим диагноз ГЕ, являются антитела к вирусу ГЕ класса Ig М (анти-ВГЕ IgM), выявляемые с помощью ИФА в сыворотке крови в остром периоде заболевания. Интересен факт обнаружения анти-ВГЕ IgG у некоторых здоровых субъектов и у лиц, получающих частые гемотрансфузии или находящихся на гемодиализе, у наркоманов, использующих внутривенное введение наркотиков.
Лечение противовирусными препаратами не проводится. Выздоровление при ГЕ наступает у подавляющего большинства больных (кроме беременных женщин) в течение 1—1,5 мес. Хронизации инфекционного процесса не бывает. Профилактика ГЕ, как и при других кишечных инфекциях. Разрабатывается генно-инженерная вакцина.
Острый гепатит В (ОГВ) может протекать в виде моноинфекции или коинфекции (если к ОГВ присоединяется дельта(d)-агент). Согласно десятому пересмотру Международной статистической классификация болезней и проблем, связанных со здоровьем (МКБ-10), принятой ВОЗ в 1995 г., в первом случае диагноз формулируется, как острый гепатит В без d-агента, во втором — острый гепатит В с d-агентом.
Острый гепатит В без d-агента
ОГВ без d-агента вызывается вирусом из семейства гепаднавирусов. Это ДНК-содержащий вирус, имеющий несколько антигенов. Наиболее изученными антигенами являются: HBsAg — поверхностный антиген, образующий наружную оболочку, прежде называемый “австралийским” антигеном; HBcAg — сердцевидный антиген; HBeAg — антиген инфекциозности.
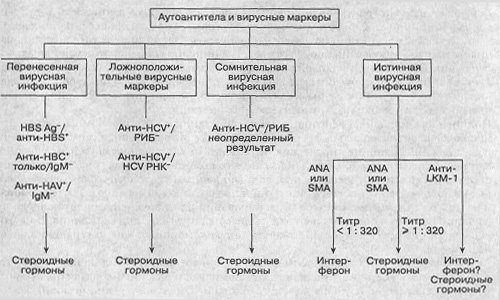
Все антигены вируса гепатита В (ВГВ) и образующиеся к ним антитела являются маркерами инфекционного процесса, и различные сочетания этих маркеров характеризуют определенную стадию течения болезни. Так, маркерами активно текущей инфекции являются HBsAg, HBeAg, анти-HBcIgM, специфическая вирусная ДНК и ДНК-полимераза. При завершившейся инфекции в крови определяются анти-HBs и анти-HBsIgG. Длительная персистенция HBsAg и HBeAg в организме больного свидетельствует о возможном развитии хронического процесса.
Существуют мутанты ВГВ — его генетические варианты, отличающиеся по нуклеотидным последовательностям ДНК. У больных, инфицированных мутантным штаммом ВГВ, наблюдаются более высокие темпы прогрессирования болезни, чаще, чем в случаях заражения “диким” ВГВ, формируется цирроз печени. Кроме того, эти пациенты хуже поддаются лечению препаратами интерферона.
ВГВ отличается очень высокой устойчивостью к различным физическим и химическим факторам, не погибает под действием практически всех дезинфицирующих средств и консервантов крови. Инактивация его наступает при автоклавировании (30 мин), сухожаровой стерилизации, прогревании (60°С в течение 10 ч) или кипячении не менее 30 мин.
Основным источником ОГВ являются носители HBsAg, больные хроническим и, значительно реже, острым вирусным гепатитом В. HBsAg обнаруживается в крови, моче, слюне, желчи, слезах, фекалиях, грудном молоке, вагинальном секрете, сперме, спинномозговой жидкости, крови пуповины. Однако реальную эпидемиологическую опасность представляют кровь, сперма и слюна, так как в других жидкостях концентрация вируса невелика. ОГВ — антропонозная инфекция с кровоконтактным механизмом передачи вируса. Распространение вируса возможно естественными путями (перинатально от беременной женщины, больной ОГВ или носительницы HBsAg, к плоду или новорожденному; при половых контактах; при реализации кровяных контактов в быту).
Искусственные пути передачи инфекции создаются при лечебно-диагностических манипуляциях, проводимых в лечебно-профилактических учреждениях и сопровождающихся нарушением целостности кожных покровов и слизистых (инъекции, стоматологические процедуры, гинекологические и гастроэнтерологические обследования и т.д.), если медицинский инструментарий недостаточно хорошо обработан; при переливаниях крови и ее компонентов, если они содержат ВГВ; при иглоукалывании, татуировке, выполнении ритуальных обрядов, проколе мочки уха, маникюре, косметических процедурах, выполняемых общими инструментами. Однако эпидемия парентеральных гепатитов (прежде всего В и С) в России в последние годы обусловлена катастрофическим увеличением числа лиц, использующих внутривенное введение наркотических средств.
Восприимчивость людей всех возрастов к гепатиту В (ГВ) высокая. Иммунитет после перенесенного ГВ длительный, возможно пожизненный. Патогенез ГВ сложен, заболевание относят к разряду иммунологически опосредованных инфекций, при которых происходит активация Т- и В-клеточной систем иммунитета, формирование аутоиммунных процессов. Повреждающее действие могут оказывать циркулирующие иммунные комплексы (ЦИК), состоящие из антигенов ВГВ и антител к ним. С ЦИК связывают внепеченочные поражения при ГВ (узелковый периартериит, гломерулонефрит и др.). Кроме того, характер течения заболевания и его исходы определяются в большей степени системой HLA макроорганизма.
Инкубационный период ОГВ без d-агента составляет от 6 нед до 6 мес (обычно 2—4 мес).
Преджелтушный период характеризуется постепенным началом, отсутствием высокой температуры тела (возможен субфебрилитет), длительностью (1—4 нед), артралгиями (у 20—30% больных появляются боли в суставах, преимущественно по ночам), экзантемой типа крапивницы. Характерны недомогание, слабость, быстрая утомляемость, снижение аппетита, тошнота, рвота, чувство тяжести или тупые боли в правом подреберье. При пальпации отмечается увеличение размеров печени, реже — селезенки. Уже в преджелтушном периоде в сыворотке крови повышена активность индикаторных ферментов (АЛТ, ACT) и можно обнаружить специфические маркеры ГВ-вирусной инфекции (HBsAg, анти-НВс IgM, HBeAg). У отдельных больных продромальные явления могут полностью отсутствовать, и потемнение мочи или желтушность склер являются первыми симптомами болезни.
В желтушном периоде наблюдаются выраженные и стойкие клинические симптомы болезни: увеличивается слабость, тошнота, снижение аппетита достигает полной анорексии, учащается рвота, возможна головная боль и головокружение. Зуд кожи встречается чаще, чем в преджелтушном периоде (у 20% больных). Печень еще более увеличивается, несколько уплотнена, умеренно чувствительна при пальпации. Желтуха достигает своего максимума на 2—3-й неделе. Моча остается темной, кал обесцвечен. Продолжительность желтушной стадии при ОГВ без d-агента колеблется в широких пределах — от 1 нед до 2—3 мес и более. Наблюдается гипербилирубинемия и закономерное повышение активности аминотрансфераз (АЛТ и ACT) в сыворотке крови. Показатель тимоловой пробы обычно в пределах нормы. Белково-синтетическая функция печени часто нарушена, особенно при тяжелом течении болезни, что проявляется прежде всего существенным снижением протромбинового индекса.
ОГВ без d-агента протекает преимущественно в среднетяжелой форме, реже наблюдается легкая форма болезни. Возможно развитие тяжелых и фульминантных форм, осложняющихся печеночной комой (0,5—1%). В случае развития печеночной недостаточности с явлениями печеночной энцефалопатии диагноз формулируют, как острый гепатит В без d-агента с печеночной комой. В периоде реконвалесценции наблюдается медленное исчезновение клинико-биохимических симптомов заболевания. При ОГВ без d-агента возможно развитие безжелтушного и субклинического вариантов болезни, нередко приводящих к формированию хронического ГВ.
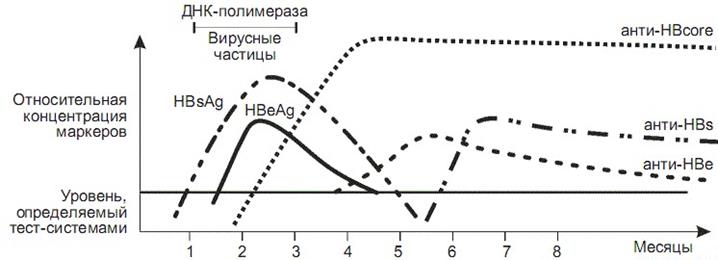
Для диагностики ОГВ без d-агента особое значение имеет определение в сыворотке крови больных специфических маркеров ГВ-вирусной инфекции методом ИФА. Основным маркером является HBsAg, который появляется в крови еще в инкубационном периоде болезни и постоянно определяется в желтушном периоде. В случае острого течения гепатита HBsAg обычно исчезает из крови в течение первого месяца от начала желтухи. Антитела к HBsAg (анти-HBs) появляются обычно в периоде реконвалесценции, через 3—4 мес от начала заболевания, поэтому не играют существенной роли при постановке диагноза ОГВ, а лишь ретроспективно свидетельствуют о ранее перенесенном ОГВ. Следует, однако, помнить о том, что при тяжелых формах ОГВ возможно появление анти-HBs с первых дней желтухи. Наиболее специфическим подтверждением диагноза ОГВ является обнаружение в крови анти-НВс IgM, которые выявляются параллельно с HBsAg еще в конце инкубационного периода и сохраняются в течение всего периода клинических проявлений. Наличие анти-НВс IgM в сочетании с HBeAg свидетельствует об активно текущей инфекции. В стадии реконвалесценции ОГВ без d-агента анти-НВс IgM исчезают, что рассматривается как признак очищения организма от вируса. В острой фазе болезни могут определяться и анти-НВс IgG, сохраняющиеся пожизненно.
В конце инкубационного периода параллельно с HBsAg обнаруживается также HBeAg, который характеризует высокую репликативную активность ВГВ. Через несколько дней после начала желтухи HBeAg исчезает из крови и появляются анти-НВе. Обнаружение этой сероконверсии говорит о резком снижении активности инфекционного процесса, свидетельствует о благоприятном течении ОГВ. Однако и после появления анти-НВе репликация ВГВ полностью не прекращается. Длительная персистенция HBeAg в сыворотке крови свидетельствует об угрозе хронизации ОГВ, поэтому при среднетяжелой и легкой формах болезни в случаях сохранения в крови HBsAg более 30 дней от начала желтухи целесообразно, кроме базисной терапии, применение альфа-интерферонов.
Следует учитывать, что отрицательный результат исследования крови на HBsAg не исключает диагноза вирусного ГВ. Подтверждением диагноза в этих случаях может служить обнаружение анти-НВе IgM. Для отграничения состояния персистирующего HBsAg-носительства от активной инфекции необходимым является исследование в сыворотке крови анти-НВs IgM; отсутствие таких антител характерно для носительства HBsAg, а их наличие — для активного процесса.
Кроме ИФА, используется метод полимеразной цепной реакции (ПЦР) для обнаружения в крови больного ДНК вируса гепатита В (ДНК HBV). Этот метод применяют для подтверждения возможного инфицирования мутантными штаммами ВГВ (в этом случае отсутствует HBeAg при наличии HBsAg, анти-НВе и ДНК HBV) и в качестве критерия эффективности проводимой терапии.
Наиболее частым исходом ОГВ без d-агента является выздоровление (90%). Если ОГВ не разрешился на протяжении 6 мес и более, заболевание переходит в стадию хронического гепатита В (ХГВ). Частота формирования ХГВ составляет от 5 до 10%. ХГВ чаще формируется после легких (в том числе безжелтушных) форм болезни. У части больных ХГВ в последующем может развиться цирроз печени (2%) и первичный рак печени. Возможно также формирование бессимптомного носительства HBsAg. Иногда после перенесенного ОГВ отмечаются поздние осложнения со стороны желчевыводящей системы и манифестация синдрома Жильбера.
Специфическая профилактика ГВ
Специфическая профилактика ГВ осуществляется с помощью рекомбинантных вакцин “Комбиотех ЛТД” (Россия), H-B-VaxII (“Мерк Шарп и Доум”, США), Энджерикс В (“Смит Кляйн Бичем”, Бельгия), Rec-HBs Ag (Куба). Вакцинация против гепатита В внесена в календарь профилактических прививок.
В качестве экстренной профилактики у непривитых медицинских работников (при порезах, уколах) используется гипериммунный специфический иммуноглобулин с наличием высокого титра антител к HBsAg и вакцинация против ГВ по укороченной схеме: 0—1—2 мес и затем спустя 12 мес после первого введения вакцины.
Острый гепатит В с d-агентом
Острый гепатит с d-агентом (коинфекция) развивается в случаях одновременного инфицирования ВГВ и d-вирусом. Вирус гепатита дельта (ВГД) — мелкий сферический агент, состоящий из генома (РНК ВГД) и белка, кодирующего синтез специфического дельта-антигена (dAg). Уникальность ВГД состоит в том, что он дефектен и его репликация зависит от вируса-помощника — ВГВ. Репродукция ВГД и реализация его патогенных свойств осуществляется лишь в организме, инфицированном ВГВ. Внешняя оболочка d-вируса представлена поверхностным антигеном ВГВ — HBsAg. В связи с этим носители HBsAg и больные ХГВ имеют повышенный риск инфицирования d-вирусом. ВГД обладает, вероятно, прямым цитопатическим действием.
Клинические проявления гепатита, развивающегося в результате коинфекции, сходны с таковыми при ОГВ без d-агента, однако течение болезни, как правило, более тяжелое. Длительность инкубационного периода составляет от 6 нед до 6 мес.
Преджелтушный период начинается более остро, с ухудшения общего самочувствия. Одновременно появляются диспепсические явления. Чаще возникают мигрирующие боли в крупных суставах. Почти у половины пациентов в преджелтушном периоде появляется боль в правом подреберье, что нехарактерно для больных ОГВ без d-агента. Другим отличием является лихорадка, часто выше 38°С. Продолжительность преджелтушного периода короче, чем при ОГВ без d-агента, и составляет в среднем около 5 дней.
В желтушном периоде сохраняется или возникает субфебрильная температура, продолжается нарастание интоксикации, усиливаются боли в правом подреберье. Чаще, чем при ОГВ без d-агента, появляются уртикарные высыпания, спленомегалия. Существенной особенностью коинфекции является двухфазное течение болезни с клинико-ферментативным обострением. Предполагают, что первый подъем уровня аминотрансфераз связан с репликацией ВГВ, а повторный — с ВГД. Нередко активность ACT выше АЛТ и коэффициент де Ритиса больше 1. Биохимические исследования свидетельствуют о выраженном цитолитическом синдроме: в сыворотке крови значительно повышено содержание билирубина за счет связанной фракции, активность трансфераз намного выше, чем при ОГВ. Выявляемые изменения связаны с глубиной повреждения гепатоцитов, вовлечением ядерных и митохондриальных структур, что обусловлено цитопатическим действием ВГД. Значительно повышается показатель тимоловой пробы, что несвойственно ГВ.
Специфическая диагностика основана на обнаружении маркеров активной репликации ГВ-вирусной и дельта-вирусной инфекции (см. таблицу).
Период реконвалесценции более продолжителен, чем при ОГВ без d-агента. При нормализации клинико-биохимических показателей и элиминации HBsAg из крови ОГВ с d-агентом завершается выздоровлением. Применение интерферонов в остром периоде болезни целесообразно лишь в случаях длительной персистенции HBeAg, свидетельствующей о возможной хронизации инфекционного процесса.
ОГВ с d-агентом протекает преимущественно в среднетяжелой форме, однако возможно развитие легкой и тяжелой форм. Не исключено также развитие фульминантного гепатита, заканчивающегося смертью. В случае развития печеночной недостаточности с явлениями печеночной энцефалопатии диагноз формулируют, как острый гепатит В с d-агентом (коинфекция) и печеночной комой. Наиболее частым исходом является выздоровление. Угроза хронизации возникает приблизительно с такой же частотой, как и при ОГВ без d-агента. Лица, имеющие антитела к HBsAg в результате перенесенного заболевания или вакцинации, не заболевают дельта-гепатитом. Поэтому вакцину против ГВ можно считать средством профилактики против дельта-инфекции в случаях коинфицирования.
Второй вариант существования d-инфекции — суперинфекция, при которой происходит заражение вирусом гепатита d-носителя поверхностного антигена вируса гепатита В.
Острая d-суперинфекция вирусоносителя гепатита В
Преджелтушный период при этой форме заболевания составляет 3—5 дней. Заболевание начинается остро с появления астеновегетативных и диспепсических симптомов, интенсивных болей в правом подреберье, рвоты, артралгий. Появляется лихорадка. В преджелтушном периоде могут наблюдаться различные проявления отечно-асцитического синдрома.
Желтушный период характеризуется наличием лихорадки в течение 3—5 дней, выраженными явлениями интоксикации, чувством тяжести в правом подреберье. Увеличиваются отеки на голенях, определяется асцит. Характерная для данного варианта острой дельта-инфекции гепатоспленомегалия отмечается практически у всех больных. Размеры селезенки увеличиваются значительно, в некоторых случаях — больше, чем размеры печени, что не свойственно ОГВ без d-агента.
Острая дельта-инфекция характеризуется ранними признаками хронизации гепатита. Нарушается белково-синтетическая функция печени, что проявляется снижением сулемового теста и содержания альбуминов сыворотки крови при значительном увеличении гамма-глобулиновой фракции белкового спектра в ранние сроки желтушного периода. Существенно повышается тимоловый тест. Активность ACT и АЛТ остается высокой дольше, чем при ОГВ без d-агента.
В сыворотке крови отсутствуют маркеры острой НВ-вирусной инфекции (анти-HBsIgM, HBeAg), определяются лишь HBsAg, анти-HBcIgG и анти-НВе, при этом выявляются DAg и/или анти-DIgM, затем — анти-DIgG. Существенной особенностью острой дельта-инфекции вирусоносителя ГВ является многоволновый характер болезни с повторными клинико-ферментативными обострениями, сопровождающимися лихорадкой в течение 1—2 дней, отечно-асцитическим синдромом и желтухой, появлением эфемерной сыпи на коже. У части больных выраженность клинических симптомов уменьшается при каждой новой волне, у других пациентов заболевание принимает прогрессирующий характер, возможно развитие подострой дистрофии печени и наступление летального исхода.
В любом случае выздоровление при этой форме дельта-инфекции наступает крайне редко, исходы ее почти всегда неблагоприятны: либо смерть (20%), либо формирование хронического гепатита D (70—80%) с высокой активностью процесса и быстрым переходом в цирроз печени. Применение препаратов интерферонового ряда замедляет скорость прогрессирования заболевания в цирроз печени, при этом курс проводимой терапии должен составлять не менее 12 мес. Вирус гепатита D нередко вызывает наиболее тяжелый и прогностически неблагоприятный гепатит.
Вакцины, защищающей носителей HBsAg от суперинфицирования d-вирусом, не создано, поэтому на первый план выступают профилактические мероприятия общего характера, направленные на предотвращение парентеральной передачи вируса.
Вирус гепатита С (ВГС) принадлежит к семейству Flaviviridae. Существует 6 генотипов и более 100 субтипов ВГС. Геном вируса представлен одноцепочечной линейной РНК, отличительной особенностью его является генетическая неоднородность, обусловленная быстрой замещаемостью нуклеотидов. В результате изменчивости генома ВГС внутри одного генотипа образуется большое число мутантных, генетически отличающихся друг от друга вариантов вируса — “квазивидов” ВГС, которые циркулируют в организме хозяина. С наличием “квазивидов” связывают ускользание вируса от иммунного ответа, длительную персистенцию ВГС в организме человека и формирование хронического гепатита, а также устойчивость к интерферонотерапии.
Острый гепатит С (ОГС) — антропонозная вирусная инфекция, по эпидемиологическим характеристикам близкая к ОГВ. Наблюдаемая в последние годы эпидемия гепатита С (ГС) в России обусловлена резким ростом числа лиц, практикующих внутривенное введение наркотических препаратов. Распространение ГС естественными путями (от матери к плоду, половым путем) происходит гораздо менее интенсивно, чем ГВ, так как концентрация вируса в крови, сперме и других биологических субстратах существенно ниже.
| Отрицательный результат исследования крови на HBsAg не исключает диагноза вирусного ГВ. |
Инкубационный период ОГС составляет в среднем 6—8 нед (от 2 до 26 нед). Для ОГС характерен высокий удельный вес безжелтушных форм (более 80%), протекающих, как правило, бессимптомно. Клинические симптомы ОГС принципиально не отличаются от таковых при других парентеральных гепатитах. В целом ОГС протекает значительно легче, чем другие острые вирусные гепатиты.
ОГС составляет в среднем 6—8 нед (от 2 до 26 нед). Для ОГС характерен высокий удельный вес безжелтушных форм (более 80%), протекающих, как правило, бессимптомно. Клинические симптомы ОГС принципиально не отличаются от таковых при других парентеральных гепатитах. В целом .
Заболевание начинается постепенно. Основными симптомами преджелтушного периода являются слабость, снижение аппетита, дискомфорт в эпигастральной области и правом подреберье. Реже появляются такие симптомы, как кожный зуд, боль в суставах, головная боль, головокружение, расстройство стула, повышение температуры тела. Длительность преджелтушного периода составляет в среднем 10 дней.
При появлении желтухи больных беспокоит слабость, снижение аппетита и дискомфорт в животе. Практически у всех пациентов определяется увеличение размеров печени, у 20% больных увеличивается селезенка. При биохимическом исследовании выявляется гипербилирубинемия и повышение уровня АЛТ и ACT. ОГС протекает преимущественно в среднетяжелой форме, летальные исходы встречаются редко.
Специфическими маркерами, подтверждающими наличие ОГС, являются антитела к ВГС (анти-HCV), которые обнаруживаются в ИФА современными тест-системами, начиная со 2—3-й недели болезни. Для выявления ложноположительных образцов целесообразно использование иммуноблота в качестве подтверждающего теста. Большое значение имеет определение РНК ВГС с помощью ПЦР в различных биологических субстратах (в сыворотке крови, лимфоцитах, ткани печени и др.) для определения активности репликативного процесса и оценки результатов интерферонотерапии. После перенесенного ОГС анти-HCV в сыворотке крови сохраняются длительно, однако не обладают защитными свойствами.
Несмотря на кажущуюся легкость течения, ОГС имеет серьезный прогноз, поскольку исходом заболевания у 80% переболевших является развитие хронического гепатита. Морфологическое исследование материалов пункционной биопсии печени позволяет выявить хронический гепатит у многих из тех пациентов, у которых после острой фазы болезни нормализовались показатели АЛТ и ACT, но в крови определялись анти-HCV и РНК ВГС. Серьезный прогноз ГС связан также с возможностью развития первичной гепатоцеллюлярной карциномы у части инфицированных лиц. При ОГС с целью снижения риска хронизации целесообразно, помимо базисной терапии, использование препаратов интерферонового ряда по 3 млн ME трижды в неделю на протяжении 3 мес. Специфическая профилактика невозможная из-за отсутствия вакцины, разработка которой затруднена из-за высокой изменчивости ВГС.
Вирус гепатита G (ВГG) относится, так же как и ВГС, к семейству Flaviviridae. Это — РНК-содержащий вирус, характеризующийся значительно меньшей изменчивостью генома, чем ВГС. Гепатит G (ГG) распространен в мире повсеместно и неравномерно. В России частота выявления вируса — от 2% в Москве до 8% в Якутии. ГG относится к инфекции с парентеральным механизмом передачи возбудителя.
Клинические проявления этого заболевания описаны неполно, что обусловлено редким выявлением моноинфекции ГG. Описаны случаи острого и хронического ГG, однако количество их невелико. Среди больных острым вирусным гепатитом неуточненной этиологии (гепатит ни А, ни Е) выявление РНК ВГG составляет 3—4%. Чаще этот возбудитель встречается в сочетании с гепатитами В, С и D — при ОГВ и ОГС вирус ГG удается определить в 24-37% соответственно, при этом присутствие ВГG не отягощает течения ГВ или ГС.
Методы специфической диагностики основаны на выявлении РНК ВГG, характеризующие присутствие вируса и его репликацию, и анти-ВГG, появляющиеся после освобождения организма от вируса и свидетельствующие об иммунитете. Однако, несмотря на то что ВГG связывают с поражением печени, более чем у половины инфицированных не отмечается изменений аминотрансфераз в сыворотке крови, в связи с чем высказывается предположение о том, что внедрение вируса в организм не всегда сопровождается заболеванием печени, т.е. отсутствует первичная гепатотропность ВГG. Предполагают, что ВГG сопутствует еще не распознанному вирусу ни А, ни G.
Исходом перенесенной инфекции является выздоровление с элиминацией вируса, при этом в крови выявляются анти-ВГG. Возможно формирование хронического ГG и длительное носительство РНК ВГG.
Несколько лет назад было описано 5 случаев посттрансфузионного гепатита, (развившегося у пациентов через 8—11 нед после переливания крови), при которых удалось выявить ДНК нового возбудителя, ассоциированного с поражением печени и обозначенного TTV (transfusion transmitted virus). В настоящее время известно 3 генотипа и 9 субтипов этого вируса, который отнесли к инфекциям с кровоконтактным механизмом передачи возбудителя. Однако заслуживает внимания факт обнаружения ДНК TTV в сыворотке крови и фекалиях больных в острой фазе гепатита, в связи с чем высказано предположение о том, что TTV может быть очередным представителем группы энтерально передающихся гепатитов. Дальнейшие исследования в этой области позволят определить гепатотропность этого возбудителя, уточнить эпидемиологические и клинические характеристики, а также выработать эффективные методы диагностики и профилактики этого заболевания.
1. Соринсон С.Н. Вирусные гепатиты. СПб.: Теза, 1997; 325.
2. Лекции по инфекционным болезням / Под ред. акад. РАМН проф. Н.Д. Ющука, М.: ВУНМЦ, 1999; 2: 3—59.
3. Балаян М.С., Михайлов М.И. Энциклопедический словарь — вирусные гепатиты. М., Амипресс, 1999; 302.
источник
Таблица 2. Диагностические маркеры ВГ
антитела класса М к вирусу гепатита А
указывают на острую инфекцию
антитела класса G к вирусу гепатита А
свидетельствуют о перенесенной инфекции или HAV-пастинфекции, сохраняются в крови пожизненно
антитела класса М к вирусу гепатита E
указывают на острую инфекцию
антитела класса G к вирусу гепатита E
свидетельствуют о перенесенной инфекции или HEV-пастинфекции
поверхностный антиген HBV
маркирует инфицированность HBV
указывает на репликацию HBV в гепатоцитах, высокую инфекционность крови и высокий риск перинатальной передачи вируса
маркирует репликацию HBV в гепатоцитах, обнаруживается только при морфологическом исследовании биоптатов печени и на аутопсии, в крови в свободном виде не выявляется
суммарные антитела к HBcAg
важный диагностический маркер, особенно при отрицательных результатах индикации HBsAg, используется для ретроспективной диагностики ГВ и при неверифицированных гепатитах, определяют HBcAb без разделения на классы
антитела класса M к ядерному антигену
один из наиболее ранних сывороточных маркеров ГВ, наличие его в крови указывает на острую инфекцию (фазу болезни), при хроническом ГВ маркирует репликацию HBV и активность процесса в печени
может указывать на начало стадии реконвалесценции (исключение — мутантная форма HBV)
протективные антитела к поверхностному антигену HBV
указывают на перенесенную инфекцию или наличие поствакцинальных антител (их защитный титр от HBV-инфекции 10МЕ/л); обнаружение же антител в первые недели ГВ прогнозирует развитие гипериммунного варианта фульминантного ГВ
маркер наличия и репликации HBV
антитела класса М к вирусу гепатита D
маркируют репликацию HDV в организме
антитела класса G к вирусу гепатита D
свидетельствуют о возможной инфицированности HDV или перенесенной инфекции
маркер наличия HDV в организме
маркер наличия и репликации HDV
антитела класса G к вирусу гепатита C
свидетельствуют о возможной инфицированности HCV или перенесенной инфекции (определяются в скрининговых иследованиях)
антитела класса М к ядерным белкам HCV
указывают на текущую инфекцию (острая или хроническая в фазе реактивации
антитела класса G к ядерным белкам HCV
свидетельствуют об инфицированности HCV или перенесенной инфекции
антитела к неструктурным белкам HCV
обычно обнаруживаются в хронической стадии ГС
маркер наличия и репликации HCV
маркер наличия и репликации HGV
Расшифровка маркеров вирусного гепатита
антитела класса М к вирусу гепатита А
указывают на острую инфекцию
антитела класса G к вирусу гепатита А
свидетельствуют о перенесенной инфекции или HAV-пастинфекции, сохраняются в крови пожизненно
антитела класса М к вирусу гепатита E
указывают на острую инфекцию
«антитела класса G к вирусу гепатита Е
свидетельствуют о перенесенной инфекции или HEV-пастинфекции
поверхностный антиген HBV
маркирует инфицированность HBV
указывает на репликацию HBV в гепатоцитах, высокую инфекционность крови и высокий риск перинатальной передачи вируса
маркирует репликацию HBV в гепатоцитах, обнаруживается только при морфологическом исследовании биоптатов печени и на аутопсии, в крови в свободном виде не выявляется
суммарные антитела к HBcAg
важный диагностический маркер, особенно при отрицательных результатах индикации HBsAg, используется для ретроспективной диагностики ГВ и при неверифицированных гепатитах, определяют НВсАg без разделения на классы
антитела класса М к ядерному антигену
один из наиболее ранних сывороточных маркеров ГВ, наличие его в крови указывает на острую инфекцию (фазу болезни), при хроническом ГВ маркирует репликацию HBV и активность процесса в печени
может указывать на начало стадии реконвалесценции (исключение — мутантная форма HBV)
протективные антитела к поверхностному антигену HBV
указывают на перенесенную инфекцию или наличие поствакцинальных антител (их защитный титр от HBV-инфекции «10 МЕ/л); обнаружение же антител в первые недели ГВ прогнозирует развитие гипериммунного варианта фульминантного ГВ
маркер наличия и репликации HBV
антитела класса М к вирусу гепатита D
маркируют репликацию HDV в организме
антитела класса G к вирусу гепатита
свидетельствуют о возможной инфицированности HDV или перенесенной инфекции
маркер наличия HDV в организме
маркер наличия и репликации HDV
антитела класса G к вирусу гепатита С
свидетельствуют о возможной инфицированности HCV или перенесенной инфекции (определяются в скрининговых исследованиях)
антитела класса М к ядерным белкам HCV
указывают на текущую инфекцию (острая или хроническая в фазе реактивации)
антитела класса G к ядерным белкам HCV
свидетельствуют об инфицированности HCV или перенесенной инфекции
антитела к неструктурным белкам HCV
обычно обнаруживаются в хронической стадии ГС
маркер наличия и репликации HCV
маркер наличия и репликации HGV
Ориентировочная интерпретация диагностических данных при выявлении маркеров вирусных гепатитов
Вирусный гепатит А. Сопутств.: «носительство HBsAg».
При типичных признаках острого ГА. Необходимо тщательное клинико-лабораторное исследование для исключения ОГВ и ХГВ.
IgM анти-HAV, HBsAg, анти-НВс (total), IgG анти-НВс
Вирусный гепатит А. Сопутств.: хронический гепатит В (нерепликативная фаза).
При выявлении признаков хронического гепатита у больных острым ГА и отсутствии маркеров репликации (HBV-DNA, HBeAg, IgM анти-НВс).
IgM анти-HAV, HBsAg, анти-НВс (total), IgG анти-НВс, IgM анти-НВс, HBeAg, HBV-DNA
Вирусный гепатит А. Сопутств.: хронический гепатит В (репликативная фаза).
При выявлении признаков хронического гепатита у больных острым ГА.
HBsAg, HBeAg, IgM анти-НВс, IgM анти-HDV
Острая коинфекция ВГВ и ВГD.
При отсутствии IgG анти-НВс и клинико-анамнестических признаков обострения ХГВ
При отрицательных результатах обследования на IgM анти-HBV (или низких титрах этих антител).
Реконвалесцент ВГС (или ВГС-пастинфекция) — при отрицательных результатах исследования на: IgM анти-HCV и HCV-RNA.
Только у практически здоровых при отсутствии эпидемиологических данных и клинико-лабораторных признаков поражения печени.
При невозможности подобного исследования
Диспансерное наблюдение такое же, как при диагнозе «носительство HBsAg»
Анти-HCV (total), анти — HCV core IgM, HCV-RNA
Острый вирусный гепатит С.
При наличии эпидемиологических и клинико-лабораторных признаков острого гепатита и отсутствии маркеров других ВГ. Диспансерное наблюдение такое же, как и при ОГВ.
Анти-HCV IgG, анти — HCV core IgM, анти — HCV core IgG, анти — HCV NS, HCV-RNA
Хронический вирусный гепатит С (фаза реактивации).
При наличии клинико-биохимических признаков хронического поражения печени. Диспансерное наблюдение такое же, как при ХГВ.
Анти-HCV IgG анти-HCV core IgG, анти — HCV NS
Хронический вирусный гепатит С (латентная фаза).
При отсутствии в крови HCV-RNA, анти — HCV core IgM и клинико-биохимических признаков обострения ХГС.
HBsAg, IgM анти-НВс, HBeAg, анти — HCV IgG, анти-HCV core IgM, анти — HCV core IgG, анти — HCV NS, HCV-RNA
Острый вирусный гепатит В Сопутств.: хронический вирусный гепатит С (фаза деактивации)
При наличии клинико-лабораторных признаков ОГВ. Сопутствующий диагноз является следствием детального клинико-лабораторного обследования на ГС.
HBsAg, IgM анти-НВс, HBeAg, анти — HCV IgG, анти-HCV core IgG, анти — HCV NS
Острый вирусный гепатит В Сопутств.: хронический вирусный гепатит С (латентная фаза)
При наличии клинико-лабораторных признаков ОГВ. Сопутствующий диагноз является следствием детального клинико-лабораторного обследования на ГС.
HBsAg, IgM анти-НВс, HBeAg, анти — HCV (total), анти-HCV core IgM, HCV-RNA
При наличии лишь клинико-лабораторных и эпидемиологических признаков, характерных для острых вирусных гепатитов.
Анти-HCV (total), анти — HCV core IgM, HCV-RNA, HBsAg, анти-НВс (total), IgG анти-НВс
Острый вирусный гепатит С. Сопутств.: хронический гепатит В (нерепликативная фаза).
При наличии эпидемиологических и клинико-лабораторных признаков острого ГС.
Анти-HCV (total), анти — HCV core IgM, HCV-RNA, HBsAg, анти-НВс (total), IgG анти-НВс, IgM анти-НВс, HBeAg, HBV-DNA
Острый вирусный гепатит С. Сопутств.: хронический гепатит В (репликативная фаза).
При наличии эпидемиологических и клинико-лабораторных признаков острого ГС и хронического ГВ.
источник
Вирусные гепатиты
Вирусные гепатиты (hepatites virosae) – группа вызываемых облигатно гепатотропными вирусами антропонозных болезней с разнообразными механизмами заражения, характеризующихся преимущественным поражением печени с развитием общетоксического синдрома, гепатоспленомегалии, нарушениями функции печени и нередко с желтухой. В данную группу не включаются поражения печени факультативно гепатотропными вирусами – Эпштейна—Барр (возбудитель инфекционного мононуклеоза), цитомегаловирусом, вирусом желтой лихорадки и др.
Исторические сведения. Предположение об инфекционной природе желтух, известных со времен Гиппократа (V в. до н.э.), принадлежит выдающемуся русскому клиницисту С.П.Боткину, который в 1888 г. сформулировал представление о гепатите («катаральной желтухе») как об общем инфекционном заболевании и указал на связь болезни с циррозом и «острой желтой атрофией» печени. Клинико-эпидемиологические доказательства вирусной природы заболевания получены в 1937 г. в США Дж.Финдлеем и Ф.Маккаллюмом и в 40-х годах П.П.Сергиевым и Е.М.Тареевым в России в процессе вакцинации от желтой и флеботомной лихорадок соответственно. При этом стали различать эпидемический (инфекционный) и сывороточный типы гепатита.
В 1962—1964 гг. Б.Бламбергом был открыт «австралийский антиген», связь которого с сывороточным гепатитом установлена А.Принсом и др. в 1968 г. В 1970 г. Д.Дейн и соавт. обнаружили в сыворотке крови и в ткани печени возбудитель сывороточного гепатита – вирус В. В 1973 г. в США С.Фейнстоун открыл возбудитель инфекционного гепатита – вирус А. В 1975 г. в США была разработана вакцина против гепатита В. В 1977 г. М.Ризетто и соавт. открыли дельта-антиген – возбудитель вирусного гепатита ^.
Сероэпидемиологические исследования 70-х годов установили факт существования группы гепатотропных вирусов, не относящихся к ранее известным возбудителям (гепатиты ни А ни В) и вызывающих как посттрансфузионный гепатит, так и водные вспышки болезни. В 1989—1990 гг. эти возбудители были идентифицированы соответственно как вирус С и вирус Е. Наряду с этим имеются случаи вирусных гепатитов, при которых известные вирусные маркеры не выявляются.
В настоящее время наиболее изучены вирусные гепатиты типов А, В, С, D и Е.
Син.: болезнь Боткина, эпидемический гепатит
Гепатит А (ГА, hepatitis А) – острая энтеровирусная инфекция с фекально-оральной передачей возбудителей, характеризующаяся воспалительными и некробиотическими изменениями в печеночной ткани и проявляющаяся синдромом интоксикации, гепатоспленомегалией, клинико-лабораторными признаками нарушения функции печени и иногда желтухой.
Этиология. Возбудитель – вирус гепатита А (ВГА, НАV) – энтеровирус тип 72, относится к роду Enterovirus, семейству Picornaviridae, имеет диаметр около 28 нм (от 28 до 30 нм). Геном вируса представлен однонитчатой РНК.
ВГА выявляется в сыворотке крови, желчи, фекалиях и цитоплазме гепатоцитов у зараженных лиц в конце инкубации, продромальном и начальной фазе периода разгара болезни и крайне редко в более поздние сроки.
ВГА устойчив во внешней среде: при комнатной температуре может сохраняться в течение нескольких недель или месяцев, а при 4 °С – несколько месяцев или лет. ВГА инактивируется при кипячении в течение 5 мин, чувствителен к формалину и ультрафиолетовому облучению, относительно устойчив к хлору (хлорамин в концентрации 1 г/л вызывает полную инактивацию вируса при комнатной температуре через 15 мин).
Эпидемиология. ГА – антропонозная кишечная инфекция. Источником возбудителей являются больные, находящиеся в конце периода инкубации, продроме и в начальной фазе периода разгара болезни, в фекалиях которых обнаруживают ВГА или его антигены. Наибольшее эпидемиологическое значение имеют лица с инаппарантной формой ГА, число которых может значительно превышать численность больных манифестными формами болезни.
Ведущий механизм заражения ГА – фекально-оральный, реализуемый водным, алиментарным и контактно-бытовым путями передачи возбудителя. Особое значение имеет водный путь передачи ВГА, обеспечивающий возникновение эпидемических вспышек заболевания. Не исключается теоретически и парентеральный путь инфицирования, но это встречается крайне редко.
ГА свойственно сезонное повышение заболеваемости в летне-осенний период. Восприимчивость к болезни всеобщая, но наиболее часто болеют дети в возрасте старше 1 года (особенно в 3—12 лет, находящиеся в организованных коллективах) и молодые люди. Дети до 1 года малочувствительнык заражению вследствие пассивного иммунитета. У большинства людей к 35—40 годам вырабатывается активный иммунитет, подтверждаемый обнаружением в их сыворотке крови антител к ВГА (IgG – анти-ВГА), которые имеют протективное значение.
Патогенез и патологоанатомическая картина. Вирусный ГА – доброкачественная циклическая инфекция, протекающая со сменой фаз и периодов болезни.
После заражения и первичной репликации вирус ГА из кишечника проникает в кровь. Возникшая вирусемия обусловливает развитие общетоксического синдрома в начальный период болезни и гематогенную (и лимфогенную) диссеминацию возбудителя в печень. Интимные механизмы поражения вирусами гепатоцитов изучены не достаточно полно. Основное значение в повреждении гепатоцитов и развитии воспалительных изменений в печеночной ткани при ГА придают прямому цитопатогенному действию вируса и иммунным механизмам. Нарушение клеточного метаболизма, усиление процессов переокисного окисления липидов с нарушением антиоксидантной защиты сопровождается повышением проницаемости клеточных мембран гепатоцитов. Вследствие этого происходит перераспределение биологически активных веществ: выход из клетки ферментов и ионов калия и, наоборот, приток в клетку из внеклеточной жидкости ионов натрия, кальция, что способствует гипергидратации и снижению биологического потенциала клетки.
Процесс дезинтеграции мембран гепатоцитов распространяется и на внутриклеточные органеллы. Повышение проницаемости лизосомальных мембран и массивный выход активных гидролаз приводят к аутолизу клеток, что в значительной мере определяет развитие цитолиза и некробиоза гепатоцитов.
Воспалительные и некробиотические процессы развиваются преимущественно в перипортальной зоне печеночной дольки и в портальных трактах, приводят к возникновению цитолитического, мезенхимально-воспалительного и холестатического клинико-биохимических синдромов. Ведущим синдромом при гепатитах является цитолитический, лабораторными критериями которого служат повышение активности АсАТ и в большей степени АлАТ, увеличение содержания железа в сыворотке крови, а при массивном цитолизе с явлениями гепатоцеллюлярной недостаточности – падение синтеза протромбина, других факторов свертывания и альбумина, эфиров холестерина. Мезенхимально-воспалительный синдром проявляется повышением уровня ?2 –, ?– и g-глобулинов, иммуноглобулинов всех классов, изменением коллоидных проб (снижением сулемового титра и повышением тимолвероналовой пробы). При холестатическом синдроме в крови повышаются уровни связанного билирубина, желчных кислот, холестерина, меди, активности щелочной фосфатазы, 5-нуклеотидазы (5-НУК), гаммаглютамилтранспептидазы (ГГТП); отмечается билирубинурия.
Структурно-функциональные изменения в печеночной ткани при ГА носят обратимый характер.
В результате развития иммунного ответа наступают элиминация ВГА и выздоровление с формированием стойкого видоспецифического иммунитета. ГА не свойственно развитие прогрессирующих и хронических форм болезни, в том числе вирусоносительства. Однако течение заболевания может быть существенно модифицировано в случаях микст-инфекции с другими гепатотропными вирусами (ВГВ, ВГС и др.).
Клиническая картина. ГА характеризуется полиморфизмом клинических проявлений. Различают следующие формы болезни:
• по «степени выраженности симптомов – субклиническая (инаппарантная), стертая, безжелтушная, желтушная;
• по течению – острая, затяжная;
• по степени тяжести – легкая, средней тяжести, тяжелая.
При заражении ВГА часто развивается субклинический инфекционный процесс (инаппарантная инфекция).
В манифестных случаях болезни выделяют следующие периоды: инкубационный, продромальный (преджелтушный), разгара болезни (желтушный) и реконвалесценции.
Инкубационный период ГА составляет в среднем 21—28 дней (1—7 нед).
Продромальный период ГА продолжается в среднем 5—7 дней (с 1—2-го до 14—21-го дня) и характеризуется общетоксическим синдромом, который может проявляться гриппоподобным (лихорадочным), астеновегетативным, диспепсическим и смешанными вариантами. Наиболее часто развивается «лихорадочно-диспепсический» (по Е.М.Тарееву) вариант, для которого характерны острое начало болезни и повышение температуры тела до 38—40 °С в течение 1—3 дней, появление легких катаральных изменений в носоглотке, головная боль, снижение аппетита, тошнота и изредка рвота, ощущение дискомфорта в эпигастральной области. Спустя 2—4 дня моча приобретает цвет пива или чая (уробилин– и холурия). В конце продромального периода кал становится ахоличным, часто жидкой консистенции.
В этот период наряду с признаками «респираторного заболевания» у больных обычно выявляется увеличение печени и иногда селезенки, пальпация которых чувствительна. При биохимическом исследовании, как правило, отмечается повышение активности АлАТ, может быть повышен показатель тимоловой пробы, а при серологическом – определяются антитела к ВГА IgМ-анти-ВГА).
Период разгара продолжается в среднем 2—3 нед (с колебаниями от 1 нед до 1,5—2 мес). Наиболее полно картина болезни представлена при форме средней тяжести, протекающей обычно с желтухой. Возникновение желтухи наблюдается после снижения температуры тела до нормального и реже субфебильного уровня, сопровождается уменьшением головной боли и других общетоксических проявлений, улучшением самочувствия больных, что может служить важным дифференциально-диагностическим признакомГА. Как правило, в желтушном периоде сохраняются диспепсические симптомы, а при тяжелой форме они могут усиливаться. Больные жалуются на снижение аппетита, тошноту, редко на рвоту, ощущения тяжести и распирания в эпигастральной области и правом подреберье. Дискомфорт в области живота обычно усиливается после приема пищи.
В развитии желтухи выделяют фазы нарастания, максимального развития и угасания. Раньше всего желтуха выявляется на слизистой оболочке рта (уздечка языка и небо) и склерах, в дальнейшем – на коже; при этом степень желтушности часто соответствует тяжести болезни.
Наряду с желтухой у больных имеются признаки астении – общая слабость, вялость, утомляемость. При объективном осмотре обращают на себя внимание тенденция к брадикардии и гипотензии, глухость сердечных тонов, обложенность языка, увеличение печени, край которой закруглен и болезнен при пальпации. В 1/3 случаев наблюдается увеличение селезенки. В этот период наиболее выражены потемнение мочи и ахолия кала. При лабораторных исследованиях выявляются характерные признаки цитолитического мезенхимально-воспалительного и разной степени холестатический синдром. В периферической крови – лейкопения и относительный лимфоцитоз, замедленная СОЭ. В крови имеются антитела к ВГА (IgМ-анти-ВГА и IgА-анти-ВГА).
Фаза угасания желтухи протекает медленнее, чем фаза нарастания, и характеризуется постепенным ослаблением признаков заболевания.
Исчезновение желтухи обычно указывает на развитие периода реконвалесценции ГА, продолжительность которого весьма вариабельна (от 1—2 до 6 мес и более). В этот период у больных нормализуются аппетит, размеры печени и селезенки, угасают астеновегетативные нарушения, постепенно нормализуются функциональные печеночные тесты.
В определении формы тяжести заболевания наиболее существенное значение имеют наличие и выраженность синдрома интоксикации. В качестве дополнительного критерия тяжести используется такой показатель, как уровень гипербилирубинемии. В подавляющем большинстве случаев ГА протекает в легкой и средней тяжести формах.
У 5—10 % больных наблюдается затяжная форма ГА продолжительностью до нескольких месяцев, характеризующаяся монотонной динамикой клинико-лабораторных показателей и проявляющаяся преимущественно гепатомегалией и гиперферментемией. Как правило, затяжные формы ГА заканчиваются выздоровлением.
Осложнения. У ряда больных могут развиться различные осложнения. В период угасания симптомов иногда наблюдается обострение заболевания с ухудшением клинических и(или) лабораторных показателей. Рецидивы ГА могут возникать в период реконвалесценции спустя 1—6 мес после клинического выздоровления и нормализации лабораторных тестов.
Затяжные формы ГА, обострения и рецидивы болезни требуют пристального внимания и тщательного лабораторно-морфологического обследования для исключения возможной микст-инфекции (ВГВ, ВГС и др.) и в связи с этим хронизации заболевания.
Помимо указанных осложнений, у некоторых больных могут наблюдаться признаки поражения желчных путей (дискинезии, воспалительные процессы), вторичные бактериальные инфекции с поражением легких и других органов. Описаны случаи агранулоцитоза, панцитопении, тромбоцитопении, миокардита, ухудшающих прогноз заболевания.
У некоторых больных ГА отмечаются остаточные явления в виде гепатофиброза, постгепатитного астеновегетативного синдрома, поражения билиарной системы при неизмененных функциональных печеночных пробах. Возможна манифестация синдрома Жильбера с повышением в сыворотке крови уровня свободного билирубина при нормальных остальных биохимических показателях.
Прогноз. Обычно благоприятный. У 90 % больных наблюдается полное выздоровление, у остальных – выздоровление с остаточными явлениями. Летальность при ГА не превышает 0,04 %.
Диагностика. Диагноз ГА устанавливается с учетом комплекса эпидемиологических (возникновение болезни через 7—50 дней после контакта с больными ГА или пребывания в неблагоприятном районе), клинических данных (циклическое течение болезни с закономерной сменой симптомокомплекса продромального периода появлением кардинального признака – желтухи) и результатов лабораторного обследования больных. Одним из важных объективных признаков ГА является гепатомегалия, обнаруживаемая уже в преджелтушном периоде.
Диагноз гепатита основывается на комплексе биохимических показателей, отражающих важнейшие функции печени. Одним из ранних и чувствительных показателей нарушения пигментного обмена является повышенный уровень уробилиногена в моче. Увеличение содержания билирубина в сыворотке крови происходит преимущественно за счет связанной его фракции. В клинической практике наибольшее значение приобрело определение активности АлАТ в крови, причем диагностическое значение имеет активность фермента, в 10 раз и более превышающая нормальные показатели (0,3-0,6 нмоль/ ч * л). Гиперферментемия может служить одним из основных показателей при безжелтушной форме ГА. Широкое применение в практике имеет определение коллоидных проб – повышение показателя тимоловой пробы и снижение сулемового титра.
Вирусологические исследования (иммунная электронная микроскопия фильтрата фекалий) для обнаружения ВГА и иммуноферментный метод для выявления ВГА-Аg эффективны лишь в ранние периоды болезни (инкубационный и продромальный) и поэтому не имеют практического значения.
Достоверная верификация диагноза ГА достигается серологическими методами (РИА, ИФА и др.) с обнаружением в нарастающем титре IgМ-анти-ВГА в продроме и в разгаре болезни. IgG-анти-ВГА имеют анамнестическое значение.
Дифференциальная диагностика. В продромальном периоде ГА дифференцируют от гриппа и других ОРЗ, энтеровирусной инфекции, тифопаратифозных заболеваний, некоторых острых кишечных инфекций. В желтушный период необходима дифференциальная диагностика с желтушными формами инфекционного мононуклеоза, лептоспироза, псевдотуберкулеза, желтухами гемолитического, токсического и обтурационного генеза.
Лечение. ГА чаще всего завершается спонтанным выздоровлением, и в основном больные не нуждаются в активных лечебных мероприятиях. Необходимо создать условия для нормализации функциональной деятельности печени и самоизлечения. Это достигается комплексом мероприятий, включающих щадящий режим, рациональную диету и витаминотерапию.
Постельный режим назначают больным на период разгара заболевания. Физическая нагрузка под контролем за клинико-биохимическими показателями разрешается реконвалесцентам спустя 3—6 мес после выписки из стационара.
Пища должна быть достаточно калорийной (соответственно физиологической норме), содержать полноценные белки, углеводы и жиры (исключая лишь трудноперевариваемые жиры – говяжий, бараний, свиной). Этому соответствует стол № 5 (по Певзнеру). Показан частый (5—6 раз в сутки) прием пищи. Объем жидкости (щелочные минеральные воды, чай, соки, кисели) составляет 2—3 л в сутки. Рацион максимально обогащается естественными витаминами за счет включения в него фруктов, овощей, соков. Диетические ограничения рекомендуют реконвалесцентам в течение 6 мес после выписки из стационара.
При синдроме интоксикации больным средней тяжести и при тяжелой форме ГА назначают дезинтоксикационные средства – энтеральные (полифепан, энтеродез и др.) и парентеральные (растворы Рингера, глюкозы, коллоидов и др.).
Для стимулирующего воздействия на метаболические процессы проводят сбалансированную витаминотерапию, включающую витамины группы В, С, жирорастворимые. С этой же целью в период ранней реконвалесценции применяют метилурацил, гепатопротекторы (легален, или карсил, силибор). По показаниям используют желчегонные препараты и спазмолитические средства.
Реконвалесценты ГА подлежат диспансерному клинико-лабораторному наблюдению в течение 3 мес (при остаточных явлениях и более).
Профилактика. Проводят комплекс санитарно-гигиенических мероприятий. Инфицированные лица изолируются на 28 дней от начала болезни. Лица, контактировавшие с больными, подлежат наблюдению и биохимическому обследованию на протяжении 35 дней после изоляции больного. В очагах проводится дезинфекция хлорсодержащими препаратами, вещи больных подвергаются камерной дезинфекции.
Иммунопрофилактика ГА достигается применением донорского иммуноглобулина, который вводят внутримышечно в виде 10 % раствора (детям до 10 лет по 1 мл, старше 10 лет и взрослым по 1,5 мл).
Для вакцинопрофилактики ГА предложен ряд препаратов, например инактивированная вакцина «Хаврикс 720» для детей (0,5 мл) и «Хаврикс 1440» (1 мл) – для взрослых («Нavriх 720», «Нavriх 1440», Smith Claim Bichem), инактивированная адсорбированная вакцина «Аваксим» (0,5 мл) («Аvaxim», Pasteur Merieux Connaught). Создаваемый этими вакцинами иммунитет усиливается после ревакцинации и сохраняется до 20 лет.
Гепатит В (ГВ, hepatitis В) – вирусная антропонозная инфекция с перкутанным механизмом заражения; характеризуется преимущественным поражением печени и протекает в различных клинико-патогенетических вариантах – от вирусоносительства до прогрессирующих форм с развитием острой печеночной недостаточности, цирроза печени и гепатомы.
Этиология. Возбудитель – вирус гепатита В (ВГВ, НВv) – относится к нетаксономической группе Hepadnaviridae. Вирионы ВГВ («частицы Дейна») – сферические, диаметром 42 нм (до 45 нм), имеют наружную липопротеидную оболочку и нуклеокапсид, содержащий двунитчатую циркулярную ДНК, одна нить которой короче другой почти на 1/3 и ДНК-зависимую ДНК-полимеразу; с активностью последней связывают различия в репликативности и инфекционности различных («полных» и «пустых») штаммов вируса. В структуре ВГВ выделяют ряд антигенных систем: 1) поверхностный («австралийский», surface) антиген, НВsАg, находящийся в составе липопротеидной оболочки ВГВ и представленный несколькими антигенными подтипами, из которых в нашей стране распространены подтипы ауw и аdw. Он обнаруживается в виде сферических или тубулярных частиц диаметром 22 нм в крови, гепатоцитах, сперме, влагалищном секрете, цереброспинальной жидкости, синовиальной жидкости, грудном молоке, слюне и моче больных за 1,5—2 мес до первичных проявлений заболевания, на протяжении всего продромального и первых 2—3 нед периода разгара. Персистирование НВsАg в крови более 7—8 нед периода клинической манифестации ГВ указывает на вероятность хронизации процесса;
2) сердцевидный (соrе), НВсАg, выявляется в составе нуклеокапсида вирионов, в ядрах и иногда в перинуклеарной зоне инфицированных гепатоцитов;
3) НВеАg, связанный с НВсАg и представленный тремя подтипами, отражает активность ДНК-полимеразы ВГВ. Его обнаружение в крови указывает на репликативную активность вируса, в связи с чем НВеАg-позитивные лица наиболее опасны в качестве источника инфекции. Персистирование НВеАg более 3—4 нед от начала болезни может свидетельствовать о развитии хронической формы инфекции;
4) НВхАg, расположенный вблизи оболочки вириона; его роль в генезе инфекции изучается. НВхАg и антитела к нему чаще и в более высоком титре обнаруживаются у больных хроническим гепатитом В.
В поверхностных слоях оболочки ВГВ расположены рецепторы для человеческого полимеризированного альбумина, определяющие тропность вируса к гепатоцитам человека, многие инфекционные и репликативные свойства возбудителя.
ВГВ отличается высокой устойчивостью к низким и высоким температурам, многим дезинфектантам. Так, температуру 20 °С он выдерживает в течение 10 лет и более. Вирус устойчив к длительному (18 ч) воздействию кислой среды (рН 2,3), сохраняет антигенную активность в течение 7 дней при воздействии 1,5 % раствора формалина, 24 ч при воздействии 2 % раствора фенола и 5 ч – эфира и хлороформа. Инактивируется при автоклавировании в течение 30 мин, при воздействии ?-пропиолактона.
В последние годы установлено наличие мутантных вирионов НВV, имеющих большие размеры, чем «частицы Дейна», с отсутствием НВеАg и не вызывающих перекрестного иммунитета к HВV, что может иметь значение для диагностики и лечения больных.
Эпидемиология. Вирусный гепатит В – антропонозная инфекция с перкутанным механизмом заражения.
Основным резервуаром и источником ВГВ являются лица с субклинической формой инфекционного процесса, так называемые вирусоносители, общее число которых (по данным ВОЗ) превышает 350 млн человек. Частота «здорового носительства» НВsАg среди доноров колеблется в значительных пределах: от 0,5—1 % в странах Северной
Европы и Америки до 20 % и более в тропических регионах Азии и Африки.
В распространении возбудителей весьма велика роль наркоманов, гомосексуалистов и проституток, большая часть которых инфицирована ВГВ. Источниками инфекции являются также больные острыми и хроническими формами ГВ.
Ведущий механизм передачи ВГВ – перкутанный, который вследствие чрезвычайно малой инфицирующей дозы вируса (для заражения ВГВ достаточно 10 -7 мл инфицированной крови) реализуется преимущественно естественными путями – половым и вертикальным. ГВ занимает ведущее место среди болезней, передаваемых половым путем, в связи с чем он наиболее часто обнаруживается у гомосексуалистов, у людей с половыми перверсиями и большим числом половых партнеров, у проституток. Вертикальная, как правило, интранатальная, передача ВГВ наиболее часто осуществляется в случаях выявления у беременных НВеАg.
Наряду с естественными путями ВГВ распространяется искусственными (артифициальными) путями – при гемотрансфузиях инфицированной крови, в ходе операций, при стоматологических, гинекологических, инструментальных лечебно-диагностических манипуляциях, разнообразных парентеральных процедурах, производимых недостаточно тщательно обеззараженными инструментами многоразового пользования (ятрогенная инфекция). В связи с этим контингентами высокого риска заражения ВГВ становятся реципиенты донорской крови и ее препаратов, в особенности больные гемофилией, гематологическими заболеваниями; пациенты центров хронического гемодиализа; лица, подвергающиеся многократным лечебно-диагностическим и инструментальным процедурам с повреждением кожи и слизистых оболочек, а также медицинский персонал, имеющий профессиональный контакт с кровью больных (трансфузиологи, хирурги, акушеры, стоматологи, лаборанты и т.д.). Высокий риск заражения артифициальным путем имеется у наркоманов и у лиц, подвергающихся татуировкам и обрядовым процедурам.
Возникновение случаев ГВ в семейных и иных очагах инфекции при исключении половых или парентеральных контактов с больными в данных очагах или за их пределами делает вероятным существование так называемого гемоконтактного пути заражения ВГВ и требует проведения в очагах соответствующих профилактических мероприятий.
Восприимчивость людей к ВГВ высокая. Наиболее часто заболевания регистрируются среди детей 1-го года жизни, как правило, с сопутствующей патологией или от ВГВ-инфицированных матерей, среди людей зрелого и пожилого возраста, обычно при наличии у них сопутствующих болезней. В последние годы наблюдается увеличение заболеваемости среди молодых лиц в связи с расширением среди них инъекционных методов введения наркотических средств. НВsАg чаще обнаруживается у мужчин. Сезонных колебаний заболеваемости не наблюдается.
У реконвалесцентов острого ГВ развивается стойкий, возможно, пожизненный иммунитет.
Патогенез и патологоанатомическая картина. После проникновения ВГВ через кожу или слизистые оболочки и его первичной репликации, локализация которой достоверно не установлена, происходят гематогенная диссеминация возбудителя, его внедрение в гепатоциты. Эта фаза соответствует инкубационному периоду болезни.
Последующая репликация вируса в гепатоцитах обусловливает вторичную вирусемию, индуцирует возникновение структурно-функциональных нарушений печени, проявляющихся различными клинико-патогенетическими вариантами болезни, генез которых изучается.
Большинством исследователей установлено, что ВГВ не дает прямого цитопатического эффекта, хотя это свойство допускается для некоторых («полных», с высокой активностью ДНК-полимеразы) штаммов вируса.
Согласно наиболее распространенной вирусоиммуногенетической концепции ГВ [Дадли Ф.Дж., 1972; Блюгер А.Ф. и др., 1978, и др.], повреждение печеночной ткани обусловлено характером и силой иммунного ответа на вирусные антигены и клеточные аутоантигены, степенью вирулентности штамма ВГВ и инфицирующей дозой возбудителя. Вариабельность указанных факторов определяет чрезвычайное разнообразие спектра клинико-патогенетических вариантов болезни.
Адекватный иммунный ответ на экспрессию вирусных антигенов на цитоплазматических мембранах гепатоцитов сопровождается специфической сенсибилизацией Т-лимфоцитов, формированием клона киллерных клеток, синтезом антигеноспецифических иммуноглобулинов, образованием иммунных комплексов, повышением макрофагальной активности и другими эффектами, обеспечивающими в конечном итоге элиминацию возбудителя и развитие стойкого иммунитета. При этом наблюдается циклическое течение заболевания с различной степенью выраженности цитолитического, мезенхимально-воспалительного и холестатического синдрома, маркеры которых аналогичны таковым при ГА.
Генетически обусловленное или приобретенное нарушение иммунного гомеостаза организма человека и особенности антигенной структуры фенотипов ВГВ способствуют возникновению ациклических вариантов патологического процесса в виде хронического вирусоносительства. быстро (например, при фульминантном гепатите) или медленно (при хронических формах болезни) прогрессирующих заболеваний с развитием печеночной недостаточности, цирроза печени, гепатомы. Последнее нередко наблюдается при интеграции вирусной ДНК в геном гепатоцита (в случаях интегративного типа вирусоносительства) и воздействии неблагоприятных экологических или токсических (например, алкоголь) факторов.
В генезе прогрессирующих форм ГВ большая роль отводится аутоиммунным реакциям лимфоцитов, сенсибилизированных к липопротеиду печеночных мембран, митохондриальным и иным аутоантигенам, а также суперинфицированию другими гепатотропными вирусами (ВГА, ВГД, ВГС и др.) или иными фенотипами ВГВ.
Морфологические изменения в печени при ГВ характеризуются более выраженными, чем при ГА, некробиотическими процессами, локализованными преимущественно в центролобулярной и перипортальной зонах печеночной дольки. Наблюдается гидропическая («баллонная») дистрофия гепатоцитов, фокальные, ступенчатые, а при тяжелом течении болезни – субмассивные и массивные некрозы. Характерны активация и пролиферация звездчатых эндотелиоцитов (клеток Купфера), перемещающихся к зонам некроза, где вместе с лимфоцитами, плазмоцитами, гистиоцитами и фибробластами они образуют мононуклеарно-гистиоцитарные инфильтраты.
Холестатические формы ГВ характеризуются вовлечением в патологический процесс внутрипеченочных желчных ходов с образованием в них «желчных тромбов», накоплением билирубина в гепатоцитах. При молниеносном гепатите преобладают распространенные «мостовидные» и мультилобулярные некрозы.
Хроническому ГВ с минимальной (0) степенью активности свойственно преимущественно портальное воспаление без признаков фиброза, а активному (I—IV) – распространение воспалительного инфильтрата внутрь дольки за пределы терминальной пластинки гепатоцитов, флебиты центральных вен и капилляризация синусоидов, развитие слабовыраженного перипортального фиброза (I стадия ХГ), умеренного фиброза с перипортальными септами (II стадия ХГ), выраженного фиброза с портоцентральными септами (III стадия ХГ) и цирроза печени (IV стадия ХГ) – по классификации международной группы экспертов по изучению болезней печени, 1994, Лос-Анджелес, США.
Клиническая картина. В зависимости от характера течения, выраженности проявлений болезни, фазы вирусной инфекции, глубины морфофункциональных нарушений, осложнений и исходов заболевания различают несколько клинико-морфологических вариантов и форм ГВ.
I. По цикличности течения
А – циклические (самолимитирующиеся), острые формы
острый вирусный ГВ с преобладанием цитолитического компонента
острый вирусный ГВ с преобладанием холестатического синдрома
затяжная форма вирусного ГВ
холестатический вирусный ГВ
1) молниеносный (фульминантный) ГВ;
– с минимальной активностью (так называемое хроническое вирусоносительство и хронический персистирующий ГВ);
– со слабо выраженной активностью;
– с умеренно выраженной активностью;
– с высокой активностью процесса фазы вирусной инфекции (репликативная, интегративная)
Ведущие синдромы: цитолитический, холестатический.
II. По степени выраженности симптомов (субклиническая, стертая, безжултушная, желтушная)
III. Постепени тяжести заболевания (легкая, средней тяжести, тяжелая)
IV. По осложнениям:
специфические осложнения (острая печеночная недостаточность, геморрагический синдром, портальная гипертензия, отечно-асцитический синдром, обострения и рецидивы ГВ);
неспецифические осложнения – суперинфекция (вирусная, бактериальная);
активизация эндогенной инфекции (вирусно-бактериально-фибковая ассоциация); обострение сопутствующих заболеваний.
V. По исходам: выздоровление (полное, с остаточными явлениями); смерть (причина – острая печеночная недостаточность, цирроз печени, гепатоцеллюлярный рак).
Острая (циклическая) форма. Наиболее частая среди манифестных форм болезни. В ее течении выделяют четыре периода: инкубационный, продромальный (преджелтушный), разгара (желтушный) и реконвалесценции.
Продолжительность инкубационного периода при ГВ колеблется от 50 до 180 дней и составляет в среднем 2—4 мес.
Продромальный период длится в среднем 4—10 дней, иногда укорачивается или удлиняется до 1 мес. Для него характерны астеновегетативный, диспепсический, артралгический и смешанные синдромы. В последние дни этого периода увеличиваются размеры печени и часто селезенки, появляются первые признаки нарушения пигментного обмена в виде холурии, обесцвечивания кала и иногда кожного зуда. У некоторых больных отмечаются уртикарный дерматит, васкулит, у детей описан папулезный акродерматит.
При лабораторном обследовании больных в моче обнаруживаются уробилиноген, а иногда и билирубиновые тела. В крови повышается активность АлАТ, выявляется НВsАg.
Продолжительность периода разгара, протекающего часто в желтушной форме, составляет 2—6 нед с колебаниями от нескольких дней до нескольких месяцев при затяжном течении болезни. Клинические проявления безжелтушной формы совпадают с таковыми в продромальном периоде. В желтушном периоде различают фазы нарастания, максимального развития и угасания симптомов.
Желтушность, как и при ГА, вначале выявляется на слизистых оболочках полости рта (небо, уздечка языка) и склерах, а затем быстро распространяется на лицо, туловище и конечности. Интенсивность желтухи нередко соответствует степени тяжести болезни, при тяжелых формах она может приобретать «шафранный» оттенок.
В этот период наблюдаются и обычно прогрессируют симптомы интоксикации в виде слабости, раздражительности, нарушения глубины сна и его продолжительности, снижения аппетита, тошноты и рвоты. Беспокоят чувства тяжести или распирания в эпигастральной области и в правом подреберье, особенно после еды, обусловленные растяжением капсулы печени. Реже наблюдаются острые приступообразные боли, возникновение которых связано с поражением желчных путей, перигепатитом, иногда кровоизлияниями в капсулу или развивающейся гепатодистрофией.
У 1/3 больных отмечается зуд, интенсивность которого не всегда коррелирует с интенсивностью гипербилирубинемии. Язык длительное время обложен серым или желтоватым налетом, суховат. При пальпации живота отмечается чувствительность или болезненность в области печени и селезенки.
У большинства больных развивается гепатомегалия, степень которой обычно соответствует тяжести болезни и выраженности холестаза. Поверхность печени гладкая, консистенция плотноэластическая. Нередко значительнее увеличивается левая доля печени.
Уменьшение размеров печени при одновременном нарастании желтухи и интоксикации может указывать на развитие острой печеночной недостаточности и является прогностически неблагоприятным симптомом. Плотная консистенция печени, сохраняющаяся после угасания основных симптомов болезни, может свидетельствовать о хроническом течении заболевания.
Увеличение селезенки наблюдается в первой декаде желтушного периода у 25—30 % больных.
В этот период выявляются артериальная гипотензия, наклонность к брадикардии, приглушенность сердечных тонов, систолический шум на верхушке, обусловленные ваготоническим эффектом желчных кислот.
Поражение нервной системы характеризуется головной болью, сонливостью в дневное время и бессонницей по ночам, раздражительностью или эйфорией.
Период угасания желтухи сопровождается уменьшением проявлений интоксикации при сохранении астеновегетативного синдрома.
В период реконвалесценции, продолжающийся 2—12 мес, иногда и более, симптомы болезни постепенно угасают, но довольно долго могут сохраняться незначительные отклонения функциональных печеночных тестов, астения, вегетативные расстройства, ощущение дискомфорта в правом подреберье.
Степень выраженности клинико-функциональных нарушений обычно соответствует форме тяжести болезни.
Стертые и безжелтушные формы ГВ обычно выявляются в ходе эпидемиологического и лабораторного обследования.
При легкой форме ГВ явления интоксикации непродолжительны и минимальны, желтуха кратковременна (1—2 нед) и мало выражена (билирубинемия до 85—100 мкмоль/л), активность АлАТ умеренно повышена, диспротеинемия незначительна.
Для формы средней тяжести характерны умеренная выраженность признаков интоксикации, яркая и более продолжительная желтуха (билирубинемия до 200—250 мкмоль/л), иногда геморрагии в виде петехий и кровоизлияний в местах инъекций, более значительное отклонение других функциональных проб печени, но зависимость активности АлАТ от тяжести болезни выявляется непостоянно.
Тяжелая форма болезни характеризуется резко выраженными симптомами интоксикации в виде недомогания, адинамии и вялости больных, отсутствия аппетита или полного отвращения к пище и даже к ее запаху. У многих больных отмечаются постоянная тошнота и повторная рвота, наблюдается инсомния, иногда эйфория. Часто при тяжелой форме ВГ развивается геморрагический синдром в виде носового кровотечения, петехий на коже и геморрагии в местах инъекций, может наблюдаться желудочно-кишечное кровотечение, у женщин – метроррагии.
Функциональные пробы печени значительно изменены (высокая степень билирубинемии, диспротеинемии и ферментемии), нередко снижается уровень факторов свертывания крови.
Осложнения острого Г В: острая печеночная недостаточность («ОПН в 0,8—1 % случаев), массивный геморрагический синдром, обострения и рецидивы болезни (в 1—1,5 % случаев), поражение желчных путей, вторичная бактериальная инфекция (пневмония, холангит, холецистит и др.).
Острая печеночная недостаточность, возникающая при тяжелом диффузном поражении печени с преобладанием альтеративных процессов, характеризуется накоплением в крови токсичных субстанций, обусловливающих развитие психоневрологической симптоматики (острая печеночная энцефалопатия – ОПЭ), и развитием массивного геморрагического синдрома. Обычно наблюдаются усиление желтухи, «печеночный» запах изо рта, нередко – сокращение размеров печени, артериальная гипотензия, иногда гипертермия, тахикардия, выраженная кровоточивость.
В зависимости от степени выраженности неврологических расстройств выделяют 4 стадии печеночной энцефалопатии: прекома I; прекома II (развивающаяся кома); неглубокая кома; глубокая кома (клиническая децеребрация).
Стадии прекомы I свойственны нарушения сна (сонливость днем и бессонница ночью, тревожный сон с яркими, часто устрашающими сновидениями), эмоциональная неустойчивость, головокружения, чувство «провала» (тягостное ощущение падения «в бездонную пропасть» при закрывании глаз), повторная рвота, замедленное мышление, нарушение ориентации во времени и пространстве, легкий тремор кончиков пальцев, нарушение координации.
В стадии прекомы II выявляется спутанность сознания, психомоторное возбуждение, сменяющееся заторможенностью, адинамией; усиливается тремор рук, языка и век.
Неглубокая кома характеризуется бессознательным состоянием с сохранением реакции на сильные раздражители, появлением патологических рефлексов, непроизвольными мочеиспусканием и дефекацией.
При глубокой коме отмечается арефлексия, утрачивается реакция на любые раздражители.
Электроэнцефалографическое исследование в стадии прекомы I выявляет нарушение пространственного расположения, дезорганизацию и нерегулярность альфа-ритма; в стадии прекомы II – эпизодические вспышки тета-волн; в стадии неглубокой комы альфа-ритм не определяется, регистрируются медленные дельта– и тета-волны. При наступлении глубокой комы определяются дельта-волны, сменяющиеся изоэлектрической линией («клиническая децеребрация»).
При развитии ОПН выявляются нейтрофильный лейкоцитоз, тромбоцитопения, резкое снижение уровня факторов свертывания крови (протромбин, проконвертин, проакцелерин и др.) и ингибиторов протеаз (?-антитрипсин). Степень изменения этих показателей, в частности прогрессирующая гипербилирубинемия с высоким содержанием свободного билирубина при резком падении активности АлАТ (билирубино-аминотрансферазная диссоциация), снижение протромбинового индекса (ниже 50 %), нарастающая диспротеинемия, имеют важное прогностическое значение. НВsАg в крови часто не обнаруживают.
Печеночная кома нередко является клиническим признаком молниеносного, фульминантного Г В, который характеризуется бурным развитием ОПЭ, геморрагического синдрома с летальным исходом в первые 2—4 нед болезни у 90 % и чаще. Заболевание нередко отмечается у пациентов молодого возраста, в особенности у женщин. В крови таких больных наряду с НВsАg часто встречается и анти-НВs, что может свидетельствовать о чрезмерном иммунном ответе (гипериммунный вариант гепатита В); нередко выявляются и маркеры других гепатотропных вирусов (ВГД, ВГС, ВГА и др.).
Холестатическая форма Г В наблюдается у 5—15 % больных, преимущественно у лиц старшего возраста, и характеризуется развитием стойкого синдрома внутрипеченочного холестаза при слабой выраженности синдрома цитолиза. Клинически эта форма проявляется интенсивной и продолжительной желтухой, нередко приобретающей застойный, зеленоватый оттенок, кожным зудом, длительной ахолией стула и холурией, значительным увеличением печени; при этом у части больных увеличен желчный пузырь (как при симптоме Курвуазье). Общетоксический синдром, как правило, выражен умеренно, не соответствует степени гипербилирубинемии. Развитию этой формы может способствовать прием алкоголя, особенно в продромальном периоде, некоторых лекарственных средств (противотуберкулезные препараты, «большие транквилизаторы», тетрациклиновые производные, гестагены и т.д.), сопутствующие хронические заболевания (например, сахарный диабет и др.).
В ряде случаев (15—20 %) ГВ приобретает затяжное течение. Несмотря на длительную желтушную фазу болезни (в течение нескольких месяцев), по клинико-лабораторным и морфологическим параметрам затяжной гепатит мало отличается от типичной острой, циклической формы болезни (морфологически нередко выявляется «лобулярный гепатит»).
У беременных ГВ нередко протекает более тяжело, особенно во второй половине беременности, осложняясь ОПН или нарушением беременности (отслойка плаценты, гибель плода и др.). Тяжелое течение ГВ часто наблюдается у детей раннего возраста.
Прогноз циклических форм ГВ в большинстве случаев благоприятный. У 80—95 % больных наблюдается выздоровление, которое часто сопровождается остаточными явлениями в виде гепатофиброза, дискинезии или воспаления желчевыводящих путей, постгепатитного астеновегетативного синдрома. У некоторых больных, обычно у молодых мужчин, отмечается манифестация синдрома Жильбера. Клиническое выздоровление значительно опережает «морфологическое выздоровление», поэтому реконвалесценты ГВ подлежат диспансерному наблюдению в течение 12 мес, а при наличии клинико-лабораторных нарушений – дольше. У 10—15 % больных возможно развитие хронических форм болезни.
Летальные исходы острого вирусного ГВ наблюдаются редко (около 1 %), развиваются вследствие ОПН, массивных кровотечений, иногда при ассоциированной инфекции.
Подострый Г В. Изучен недостаточно полно, характеризуется длительным преджелтушным периодом смешанного типа, волнообразно-прогрессирующим течением болезни без заметных ремиссий, развитием отечно-асцитического, геморрагического синдромов, выраженной диспротеинемией и малой эффективностью базисной терапии.
Прогноз подострого Г В неблагоприятный. Исходом этой формы часто является смерть больных в течение 8—12 мес от начала болезни.
Хронический гепатит В (X Г В) развивается у 10—15 % больных.
Выделение клинической формы болезни основывается на анализе клинико-лабораторных и морфологических данных и результатов определения маркеров ВГВ.
ХГВ с минимальной или слабо выраженной активностью отражает, как правило, интегративную фазу вирусной инфекции; обычно наблюдается у мужчин и протекает бессимптомно или со скудной симптоматикой в виде астенодиспепсического синдрома, преходящей холурии, умеренно выраженной гепатомегалии, незначительно нарушенными функциональными печеночными пробами.
Структурные изменения минимальны, ограничиваются портальной и/или перипортальной инфильтрацией и обычно без признаков фиброза. В крови больных обнаруживается НВsАg и часто анти-НВс (суммарные). Вирусная ДНК в ПЦР не определяется. Прогноз в большинстве случаев благоприятный.
ХГВ с умеренно выраженной активностью развивается на фоне репликативной фазы вирусной инфекции и чаще наблюдается у мужчин. Заболевание характеризуется волнообразным течением с развитием продолжительных ремиссий, в течение которых работоспособность пациентов может оставаться удовлетворительной. В период обострений, нередко спровоцированных приемом алкоголя или других токсических веществ, в том числе гепатотоксичных медикаментов, физической нагрузкой, инсоляцией, интеркуррентными заболеваниями и суперинфекцией, отмечаются симптомы интоксикации по астенодиспепсическому типу, субфебрилитет, признаки холестаза, увеличение размеров печени и селезенки, геморрагические высыпания, преходящий отечно-асцитический синдром.
При биохимических исследованиях выявляются стойкие нарушения всех функциональных печеночных проб с преобладанием маркеров мезенхимального воспаления, степень выраженности которых увеличивается в период обострения болезни. В крови обнаруживаются НВsАg (обычно более 100 нг/мл), нередко НВеАg или анти-НВе, IgМ-анти-НВс, обычно выявляется ДНК ВГВ.
В последующем более выраженными и постоянными становятся признаки портальной гипертензии и печеночной недостаточности, свидетельствующие о прогрессировании портопортального и портоцентрального фиброза, что подтверждается результатами морфологического исследования биоптатов печени. Прогноз у большинства больных неблагоприятный.
источник