Для определения вируса гепатита, получения информации о происхождении болезни, условиях и причинах возникновения проводится серодиагностика гепатита с, b, a. Выявление серологических маркеров позволяет поставить диагноз и предпринять правильное лечение. К маркерам относятся вирусные белки, специфичные антитела, которые вырабатывает организм как ответ на инфекцию и нуклеиновые кислоты вируса.
ВАЖНО ЗНАТЬ! Даже «запущенная» печень или желчный пузырь лечатся дома, без операций и уколов. Просто прочитайте что сделала Ольга Кричевская читать далее.
Серодиагностика — распознавание этиологии заболеваний способом выявления антител в крови. Серологические маркеры относятся к поздней диагностике, так как реакции возможны на 10−12 дней от начала болезни. Серодиагностические исследования проводят, чтобы:
- диагностировать заболевание — определить наличие антител в крови, используя стандартные антигены;
- определить возбудитель — выявить неизвестные антигены.
Для проведения серодиагностики используют: бактериальные клетки; плазмоциты и лимфоциты, опухолевые и пораженные клетки; растворимые компоненты. Выделяют 6 групп серологических реакций:
- Реакции, которые происходят с укрупнением частиц Ag.
- Реакции связывания комплемента и иммунный гемолиз.
- Реакция иммунофлюоресценции.
- Реакции нейтрализации Anti.
- Реакция с фагоцитозом.
- Реакции иммуносорбентного анализа с применением антигенов и антител.
Вернуться к оглавлению
Проведение серодиагностики назначают больным, если по каким-то причинам нет возможности провести диагностику, исключающую заболевание. Анализ выявляет тип возбудителя инфекции и помогает поставить диагноз. Также серодиагностика позволяет подобрать наилучший вариант лечения. Симптомы для сдачи анализа: необоснованные приступы слабости, плохой аппетит, тошнота, изменение цвета каловых масс и урины, желтизна кожи. Своевременная серодиагностика подтверждает или опровергает инфицирование и определяет стадию заболевания.
Оболочка каждого вируса имеет собственный набор белков. А аминокислоты, которые составляют белок, считаются своеобразным кодовым набором. Этот код и является маркером при серодиагностике. Маркерами гепатита А являются anti-НАV IgM и IgG. Маркерами гепатит В — HBcAg, HBsAg, HBeAg. Маркерами вируса С — HBCAg. Для проведения серодиагностики на вирус А применяют: ИЭМ (иммуноэлектронную микроскопию), РСК (связывания комплемента), РИА (применение меченых Anti и Ag), РЭМА (реакцию энзим антител). Серодиагностика на вирус В использует РИА, РЭМА, РПГ (преципитация в геле) и РИГА (непрямая гемагглютинация). При реакции РИГА используют эритроциты, которые нагружены HBsAg. Для серодиагностики гепатита С применяют иммуноферментный анализ.
Исследование при гепатите А нацелено на определение IgM и IgG. Данные показатели появляются в крови как только уровень сывороточных ферментов в организме увеличивается. Anti-НАV IgМ — является показателем уровня антител М к вирусу гепатита. После инфицирования показатель вырастает и пока не появятся первые симптомы, анализ крови будет показывать положительный результат. Аnti-НАV IgG — данный класс определяется через 10 недель после попадания инфекции в организм. Показатель чаще всего остается высоким и после выздоровления, он свидетельствует о том, что начинается процесс формирования иммунитета к вирусу типа А.
С помощью маркера HBsAg можно выявить гепатит B на самом раннем этапе, антиген проявляется на 27−41 день после попадания инфекции в организм.
Исследование нацелено на выявление антигенов и антител. Серодиагностика позволяет поставить диагноз и спрогнозировать исход болезни. Для каждой стадии, обнаруживается разный маркер HBV. На протяжении инкубационного периода антиген сохраняется в крови от 2 до 5 месяцев. Показателем инфицирования является одновременное определение HBs и НВс. В начале восстановления из крови исчезают HBc и HBe, образуется anti-НВс, позже в крови определяются антитела ко всем типам антигена. Наличие HbsAg говорит о заражении, если антиген есть в крови больше полугода, значит, заболевание находится в хронической стадии. Anti-HbsAg — показывает, что в организме образовались антитела и иммунная система активно борется с вирусом. HbsAg выявляется еще некоторое время после выздоровления. Anti-HbcAg выявляется с проявления симптомов и продолжается на протяжении всего периода.
Вирус гепатита С размножается неактивно, поэтому возникают трудности в диагностике инфицирования. Единственный способ выявления вируса С — определение РНК. Его определение проводят способом иммуноферментного анализа, выявляя количество Anti-HCV. Антитела определяются через 4−6 недель после попадания вируса в кровь. В этот период начинается формирование и циркуляция IgM. Через 3 месяца начинается синтез IgG. Длительное обнаружение IgM говорит об активности вируса и хронической стадии болезни. При хронической форме выявление IgM свидетельствует о поражении печени. Результат иммуноферментного анализа не является основанием для постановки диагноза, метод используется как скрининговый тест для выявления хронической формы. Обнаружив антитела к HCV и при подозрении на гепатит С необходимо пройти комплексное лабораторное обследование.
Иммуноферментный анализ серодиагностики позволяет обнаружить антитела к гепатиту С в 95% случаев хронической формы, при острой форме — точность метода 50−70%.
Серодиагностика не имеет 100% специфичности и чувствительности при диагностике вирусных гепатитов. Поэтому при оценке результатов необходимо учитывать симптоматику и использовать для диагностики несколько тестов, подтверждающих полученный результат. При оценке результатов серологических исследований следует учитывать анамнез заболевания, сведения о перенесенных заболеваниях и вакцинации, а также возможный контакт с источником инфекции.
Судя по тому, что вы сейчас читаете эти строки — победа в борьбе с заболеваниями печени пока не на вашей стороне.
И вы уже думали о хирургическом вмешательстве? Оно и понятно, ведь печень — очень важный орган, а его правильное функционирование — залог здоровья и хорошего самочувствия. Тошнота и рвота, желтоватый или сероватый оттенок кожи, горечь во рту, потемнение цвета мочи и диарея. Все эти симптомы знакомы вам не понаслышке.
Но возможно правильнее лечить не следствие, а причину? Рекомендуем прочитать историю Ольги Кричевской, как она вылечила печень и очистила желчный пузырь. Читать статью >>
источник
В основе всех серологических реакций лежит взаимодействие антигена и антитела.
Метод обнаружения с диагностической целью антител в сыворотке крови обследуемого .
В этом случае из двух компонентов реакции (антитело, антиген) неизвестным является сыворотка крови, так как постановка реакции проводится с заведомо известными антигенами. Положительный результат реакции свидетельствует о наличии в крови антител, соответствующих применяемому антигену; отрицательный результат указывает на отсутствие таковых.
Достоверные результаты получают при исследовании «парных» сывороток крови больного, взятой вначале заболевания (3-7 день) и через 10-12 дней. В этом случае удается наблюдать динамику нарастания антител. При вирусных инфекциях лишь четырехкратное и более повышение титра антител во второй сыворотке имеет диагностическое значение.
С внедрением в практику лабораторий метода иммуноферментного анализа (ИФА) стало возможным определять в крови больных антитела, относящиеся к различным классам иммуноглобулинов (JgM и JgG), что существенным образом повысило информативность серологических методов диагностики.
При первичном иммунном ответе, когда иммунная система человека взаимодействует с инфекционным агентом в первый раз, синтезируются преимущественно антитела, относящиеся к иммуноглобулинам класса М ( JgM ) . Лишь позднее, на 8-12-й день после попадания антигена в организм, в крови начинают накапливаться антитела иммуноглобулинов класса G ( JgG ) . При иммунном ответе на инфекционные агенты вырабатываются также и антитела класса А ( JgA ), которые играют важную роль в защите от инфекционных агентов кожи и слизистых оболочек.
Полимеразная цепная реакция (ПЦР), являющаяся одним из методов ДНК-диагностики, позволяет увеличить число копий детектируемого участка генома (ДНК) бактерий или вирусов в миллионы раз с использованием фермента ДНК-полимеразы. Тестируемый специфический для данного генома отрезок нуклеиновой кислоты многократно умножается (амплифицируется), что позволяет его идентифицировать. Сначала молекула ДНК бактерий или вирусов нагреванием разделяется на 2 цепи, затем в присутствии синтезированных ДНК-праймеров (последовательность нуклеинов специфична для определяемого генома) происходит связывание их с комплементарными участками ДНК, синтезируется вторая цепь нуклеиновой кислоты вслед за каждым праймером в присутствии термостабильной ДНК-полимеразы. Получается две молекулы ДНК. Процесс многократно повторяется.
Для диагностики достаточно одной молекулы ДНК, т. е. одной бактерии или вирусной частицы. Введение в реакцию дополнительного этапа — синтеза ДНК на молекуле РНК при помощи фермента обратной транскриптазы — позволило тестировать РНК-вирусы, например вирус гепатита С.
ПЦР — это трехступенчатый процесс , повторяющийся циклично: денатурация, отжиг праймеров, синтез ДНК (полимеризация). Синтезированное количество ДНК идентифицируют методом иммуноферментного анализа или электрофореза.
- Преимущество ПЦР в диагностике инфекционных заболеваний перед другими методами исследований заключается в следующем:
- возбудитель инфекции может быть обнаружен в любой биологической среде организма, в том числе и в материале, получаемом при биопсии;
- возможна диагностика инфекционных болезней на самых разных стадиях заболевания;
- возможность количественной оценки результатов исследований ( сколько вирусов или бактерий содержится в исследуемом материале);
- высокая чувствительность метода.
В настоящее время выделяют следующие формы вирусных гепатитов: гепатит А, гепатит В, гепатит С, гепатит D, гепатит Е, гепатит G и гепатит ТТ. Для диагностики каждой из перечисленных форм вирусных гепатитов используется определенный перечень маркеров.
Гепатит А — острая энтеровирусная инфекция. Возбудитель — вирус гепатита А (ВГА,HAV) — энтеровирус типа 72. Геном вируса представлен однонитчатой РНК. Вирус гепатита А содержит единственный антиген (HA-Ag). Удельный вес гепатита А в суммарной заболеваемости вирусными гепатитами составляет 70-80%. В структуре заболеваемости гепатитом А дети составляют до 80%, причем основная масса — дошкольники и школьники начальных классов.
Гепатит В – вирусная антропонозная инфекция. Возбудитель вирус гепатита В (ВГВ, HBV) – относится к семейству гепаднавирусов, ДНК-содержащих вирусов, поражающих клетки печени. Вирионы ВГВ имеют наружную липопротеидную оболочку и нуклеокапсид, содержащий двунитчатую ДНК и ДНК-зависимую ДНК-полимеразу.
- В структуре ВГВ (HBV) выделяют следующие антигенные системы:
- поверхностный («австралийский») антиген, HBsAg, находящийся в составе липопротеидной оболочки ВГВ, является маркером ВГВ, указывая на инфицированность вирусом;
- ядерный (core), HBcAg – обнаруживается в составе нуклеокапсида вирионов, свидетельствует об активной репродукции вируса;
- HBeAg – входит в состав ядра ВГВ, указывая на активность вируса и, кроме того, на его высокую вирулентность и инфицированность;
- HBxAg – расположен вблизи оболочки вириона, его роль в генезе инфекции изучается.
В диагностике вирусного гепатита В ведущее значение имеет определение комплекса маркеров гепатита. Свыше 5% населения планеты охвачено этой инфекцией, а частота безжелтушных форм ВГВ составляет, по данным разных авторов, от 60 до 82%.
Гепатит С (ВГС) – вирусное заболевание, наиболее часто протекающее в виде посттрансфузионного гепатита с преобладанием безжелтушных и легких форм и склонное к хронизации процесса.
Возбудитель — вирус гепатита С – имеет сходство с флавовирусами, содержит РНК. На основе филогенетического анализа выделено 6 генотипов ВГС и более 80 субтипов.
Генотип 1 — наиболее распространенный генотип во всем мире (от 40 до 80%). Генотип 1а является доминирующим для США, а 1b преобладает в Западной Европе и Южной Азии.
Генотип 2 распространен во всем мире, однако встречается с меньшей частотой, чем генотип 1 (от 10 до 40%).
ВГС тип 3 характерен для Индии, Пакистана, Австралии и Шотландии. Генотип 4 распространен преимущественно в Средней Азии и Египте, генотип 5 – в Южной Африке, а генотип 6 – в Гонконге и Мокао.
Примерно 90% всех случаев посттрансфузионных гепатитов связано с ВГС. Среди доноров антитела к вирусу гепатита С (анти-ВГС) обнаруживают в 0,2-5% случаев.
У 40-75% пациентов регистрируется бессимптомная форма болезни, у 50-75% больных острым ВГС формируется хронический гепатит, у 20% из них развивается цирроз печени. Важная роль ВГС отводится и в этиологии гепатоклеточной карциномы.
Геном вируса гепатита С представлен одноцепочечной положительно заряженной РНК, которая кодирует 3 структурных и 5 неструктурных белков. К каждому из этих белков вырабатываются антитела, обнаруживаемые в крови больных гепатитом С.
Отличительной чертой ВГС является волнообразное течение заболевания, в котором разграничивают 3 фазы: острую, латентную и фазу реактивации.
Для острой фазы характерно повышение активности печеночных ферментов в сыворотке крови, уровня антител класса IgM и IgG к ВГС с нарастанием титров, а также РНК ВГС.
Латентная фаза характеризуется отсутствием клинических проявлений, наличием в крови антител класса IgG к ВГС в высоких титрах, отсутствием антител класса IgM и РНК ВГС либо их присутствием в низких концентрациях на фоне незначительного повышения активности печеночных ферментов в периоды обострения.
Для фазы реактивации характерно появление клинических признаков, повышение активности печеночных ферментов, наличие антител класса IgG (к нуклеокапсидному белку core и неструктурным белкам NS) в высоких титрах, присутствие РНК ВГС и нарастание титров антител класса IgM к ВГС в динамике.
Гепатит D – вирусная инфекция, вследствие биологических особенностей вируса протекающая исключительно в виде ко- или суперифекции при гепатите В, характеризующаяся тяжелым течением,
часто неблагоприятным исходом.
Самостоятельно, без вируса В, вирус гепатита D не может попасть в организм человека
Возбудитель – вирус гепатита D (ВГD), по своим биологическим свойствам приближается к вироидам – обнаруженным молекулам нуклеиновых кислот. Печень человека – единственное место размножения (репликации) ВГD.
Известно существование двух вариантов инфекции: коинфекция (одновременное заражение ВГВ и ВГD) и суперинфекция (заражение HBsAg-позитивных пациентов). Сочетание ВГВ и ВГD сопровождается развитием более тяжелых форм патологического процесса, что определяется главным образом действием ВГD.
Летальность при суперинфекции достигает 15-20%. Инфицирование дельта-вирусом может вызывать острое заболевание, заканчивающееся выздоровлением, или формировать хроническое носительство ВГD.
При гепатите D могут отсутствовать в крови маркеры гепатита В – анти НВс и НВs-антиген – и наблюдается угнетение ДНК-полимеразной активности, так как ВГD ингибирует репликацию вируса гепатита В.
источник
Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
Ульяновский государственный университет
Институт медицины, экологии и физической культуры
Кафедра инфекционных и кожно-венерических болезней
По дисциплине « Инфекционные болезни»
МАРКЕРНАЯ ДИАГНОСТИКА ОСТРЫХ И ХРОНИЧЕСКИХ ГЕПАТИТОВ В И С.
Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
Ульяновский государственный университет
Институт медицины, экологии и физической культуры
Кафедра инфекционных и кожно-венерических болезней
Выявление серологических маркеров вирусных гепатитов …. 3 стр
Серодиагностика вирусного гепатита В…………………………. 4 стр
Серодиагностика вирусного гепатита С………………………….10 стр
Список использованной литературы. ………………………….. 19 стр
Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
Ульяновский государственный университет
Институт медицины, экологии и физической культуры
Кафедра инфекционных и кожно-венерических болезней
Выявление серологических маркеров вирусных гепатитов
Установить вирусную природу гепатита и получить информацию об его этиологии возможно только путем выявления серологических маркеров вирусов гепатита. К таким маркерам относят вирусные белки (антигены), специфичные антитела, вырабатываемые организмом в ответ на инфекцию, и нуклеиновые кислоты вируса (ДНК или РНК), представляющие его геном. Совокупность методов, позволяющих выявлять в биологических тканях и жидкостях специфические вирусные или бактериальные белки (антигены) или антитела, вырабатываемые в организме хозяина в присутствии того или иного возбудителя, относят к иммунологическим методам лабораторного анализа. За последние несколько десятилетий иммунологические методы исследования получили повсеместное распространение. Причиной этого явилось тесное слияние иммунологии и биотехнологии, которое позволило разработать и внедрить в практику широкий спектр тест-систем, основанных на взаимодействии антиген — антитело. Применительно к вирусным гепатитам, иммуноферментный анализ относится к непрямым методам обнаружения возбудителя, позволяющим установить этиологию болезни. Сравнительно недавно в практику клинико-диагностических лабораторий вошли методы генодиагностики, позволяющие обнаруживать и характеризовать гены или несмысловые последовательности ДНК и/или РНК. Своим развитием эти методы обязаны разработкой в 1983 г принципа полимеразной цепной реакции (ПЦР). Первые сообщения по практическому применению ПЦР появились в 1985 г и с тех пор количество публикаций, где ПЦР используется в качестве одного из методов исследования, занимает одно из первых мест в мировой научной литературе. Эти подходы приложимы для обнаружения и исследования геномов инфекционных
Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
Ульяновский государственный университет
Институт медицины, экологии и физической культуры
Кафедра инфекционных и кожно-венерических болезней
агентов, обнаружения маркеров онкологических заболеваний, выявления генетических изменений в геноме человека, связанных с теми или иными функциональными нарушениями. В отличие от ИФА, ПЦР-анализ относится к прямым методам обнаружения возбудителя в клиническом материале, что позволяет оценить активность вирусного процесса и проследить процессы распространения возбудителя в различных органах и тканях.
Серодиагностика вирусного гепатита В.
Вирус гепатита В (hepatitis B virus, HBV) относится к семейству Hepadnoviridae. Геном вируса представлен частично сдвоенной кольцевой молекулой ДНК размером 3200 п.н. При световой микроскопии HBV выглядит сферической частицей диаметром 42 нм (частица Дейна), состоящей из ядра — нуклеоида, имеющего форму икосаэдра диаметром 28 нм, внутри которого находится двуцепочечная ДНК, концевой белок и фермент ДНК-полимераза. В состав нуклеоидного белка входят HBcAg и HBeAg. Внешняя оболочка (толщиной 7 нм) образована поверхностным антигеном HBV — HBsAg . Вирус гепатита В является псевдоретровирусом, т. е. его ДНК может частично встраиваться в геном гепатоцитов.
При ОВГ и обострении ХГ вирусные частицы можно обнаружить в гепатоцитах и сыворотке крови больного. При интегративной форме ХГ В и в стадии ремиссии HBV в сыворотке крови не выявляется. Основой лабораторной диагностики инфекции HBV является определение серологических маркеров инфицирования вирусом: HBsAg, HВeAg, анти-НВс класса IgM и IgG, анти-НВе и анти-HBs, HBV ДНК и активности вирусной ДНК — полимеразы. В зависимости от течения вирусного гепатита В спектр изменения серологических маркеров выглядит по-разному.
Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
Ульяновский государственный университет
Институт медицины, экологии и физической культуры
Кафедра инфекционных и кожно-венерических болезней
HBsAg — основной маркер инфицирования HBV. При остром вирусном В в большинстве случаев (90-80 %) HBsAg удается выявить в инкубационном периоде, начиная с 3-5-й недели заражения. Средняя продолжительность циркуляции антигена — 70-80 дней. Быстрое исчезновение HBsAg (в первые дни желтухи) с появлением антиНВs — плохой прогностический признак. При хроническом гепатите В HBsAg может циркулировать в крови больного на протяжении многих лет. Следует отметить, что применяющиеся в настоящее время методы определения HBsAg, в том числе ИФА, имеют порог чувствительности. Поэтому при наличии клинических признаков гепатита и отсутствиии HBsAg в сыворотке крови необходимо исследовать другие маркеры инфекции HBV. Наличие HBsAg в крови свидетельствует о присутствии вируса в печени и с большой долей вероятности в крови. Не всякая сыворотка, содержащая HВsAg, содержит вирус гепатита В. В ряде случаев ДНК вируса встраивается в ДНК гепатоцита не полностью, а частично, только тем участком, который кодирует синтез HBsAg. В этих случаях синтезируются HBsAg без других компонентов вириона, (то есть без других антигенов). Считают, что такая ситуация возникает при «здоровом» носительстве HBsAg. HBeAg вируса гепатита В характеризует высокую инфекционность крови, являясь показателем активной репликации HBV. HBeAg циркулирует в крови больного только в присутствии HBsAg. В первую неделю желтушного периода он выявляется у 85-95 % больных. Выявление HBeAg в течение двух и более месяцев служит прогностическим признаком развития хронического гепатита. У большинства больных хроническим гепатитом с высокой активностью процесса HBeAg сохраняется на длительный срок (до нескольких лет). Антитела к ядерному антигену вируса гепатита В класса M (анти-НВc IgM) — маркер активной репликации НВV и острой инфекции. Выявляются через 1-2 недели после обнаружения HBsAg и сохраняются на протяжении 2-18 месяцев. У 4-20 % больных острым гепатитом В анти-HBc IgM являются единственным маркером инфекции. При
Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
Ульяновский государственный университет
Институт медицины, экологии и физической культуры
Кафедра инфекционных и кожно-венерических болезней
ХГ В анти-НВс IgM могут быть выявлены у некоторых больных в меньших титрах, чем при острой инфекции, причем титр антител отражает тяжесть гепатита. Антитела к HBcAg класса G (анти-НВс IgG) появляются практически одновременно с анти-НВс IgM. Как првило, они остаются у всех лиц, переболевших гепатитом В, пожизненно. У 95 % носителей HBsAg наряду с HBsAg циркулируют и анти-НВс IgG. Антитела к HBsAg (анти-НВs) свидетельствуют о ранее перенесенной инфекции или о наличии поствакцинального иммунитета (защитный уровень — 10 МЕ/мл). Они появляются в период выздоровления, через 4 недели после исчезновения HBsAg, достигая максимальной концентрации через 1-2 года, с последующим постепенным снижением уровня, недоступного выявлению современными методами диагностики. В некоторых случаях анти-HВs могут циркулировать пожизненно. Появление анти-HBs на фоне клинического улучшения у больного гепатитом В является хорошим прогностическим признаком. Важно отметить, что в динамике острой инфекции HBV имеется «окно», когда HBsAg уже не определяется, а анти-HBs еще не появились. При этом выявляются анти-HBc IgM и IgG. Из этого следует вывод о необходимости обследования больных ОВГ на анти-HBc IgM даже при отрицательных результатах исследования HBsAg и анти-НВs. Антитела к HBeAg (анти-НВе) появляются в крови после элиминации HBeAg и завершения репликации вируса. К концу 9-й недели острого периода гепатита В более 90 % больных имеют анти-НВе. В период выздоровления анти-НВе могут исчезать. Однако, наличие анти-НВе не является показателем отсутствия инфекционности конкретной сыворотки крови. Показано, что у ряда больных в ходе развития гепатита В (около 10%) под влиянием «иммунного давления» на вирус возникают мутантные формы, которые «избегают» иммунного надзора и не элиминируются. У носителей анти-HBe был выделен мутант, неспособный продуцировать HBeAg из-за дефектов в области precore и получивший обозначение HBeAg-отрицательного. Появление HBeAg-отрицательного мутанта приводит к прогрессированию поражения печени при
Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
Ульяновский государственный университет
Институт медицины, экологии и физической культуры
Кафедра инфекционных и кожно-венерических болезней
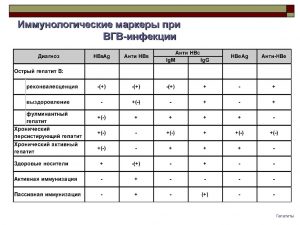
продолжающейся репликации вируса (наличие ДНК HBV в сыворотке крови). При первичном инфицировании HBeAg-отрицательным мутантом существенно возрастает риск развития фульминантного гепатита. Описанные маркеры гепатита В исследуются методом ИФА. Спектр антител (анти-НВе, анти-НВs, анти-НВc IgM, анти-НВc IgG) и антигенов (HBsAg, HBeAg) позволяет установить диагноз гепатита В и определить стадию заболевания (таблица 3). Недостатком данного метода является невозможность его использования при заражении мутантными формами вируса, при иммуносупрессии (больные онкологическими заболеваниями, наркоманы и т.д.) и для количественной оценки присутствующего в организме возбудителя. Решение этих задач стало возможным в результате внедрения молекулярно-биологических методов в практику клинико-диагностических лабораторий.
Таблица 3. Различные сочетания серологических маркеров инфицирования вирусом гепатита В и их интерпретация
источник
You are using an outdated browser. Please upgrade your browser or «>activate Google Chrome Frame to improve your experience.
022 944 944 069 944 944 069 944 949
Пн — Пт с 7.30 до 19.00, Сб 8.00 — 16.00
Если нет достаточных клинических и эпидемиологических данных для предварительного предположения этиологии гепатита, на первом этапе исследуются следующие серологические маркеры:
- HAVAb, IgM (острая форма гепатита А)
- HEVAb, IgM (острая форма гепатита Е)
- HBsAg, HBcAb (гепатит В)
- HCVAb (гепатит С)
При положительной реакции на HВsAg и (или) суммарные НВсorAb необходима дальнейшая уточняющая диагностика стадии инфекционного процесса, тестирование:
Длительная персистенция НВсorAb, при отрицательных тестах HВsAg и НВsAb может являться единственным маркером хронической инфекции мутантным штаммом вируса гепатита В.
Диагностика ко-инфекции или суперинфекции вирусом гепатита Дельта:
При положительной реакции на HCVAb, необходимо дополнительное исследование:
- HCVAb, IgM
- HCVAb белковый спектр в ИФА или иммуноблоте
- HCV, RNA
Для оценки прогноза развития гепатита С и ответа на интерферонотерапию рекомендуем проводить типирование HCV .
Диагностические маркеры вирусных гепатитов и клиническая интерпретация полученных результатов
Определение
Клиническая интерпретация
Маркеры гепатита А
вирусом гепатита А
Маркеры гепатита E
вирусом гепатита Е
Маркеры гепатита В
Один из важных показателей для назначения терапии препаратами интерферона
Антитела к HBeAg не являются защитными
Маркеры гепатита D (дельта)
Маркеры гепатита С
белков вируса гепатита C
+
типирование РНК вируса
определение методом ПЦР или реакции молекулярной гибридизации
Маркеры гепатита G
Рекомендуемый объем предвакцинального обследования:
Перед проведением вакцинации к вирусу гепатиту В необходимо провести исследование:
Выявление высокого титра защитных антител: HВsAb свидетельствуют об уже перенесенной инфекции, наличии устойчивого иммунитета и об отсутствии необходимости в вакцинации. Положительные реакции на HВsAg, и НВсAb свидетельствующие о наличии инфекции требуют индивидуального решения о целесообразности введения вакцины.
Источник: USAID, Ministerul Sanatatii al Republicii Moldova. Diagnosticul de laborator al Hepatitelor virale B, C si D. Instructiuni metodice, 2007
В случае отрицательных реакций при выявлении маркеров вирусных гепатитов А, В, С и D следует исключить гепатиты, вызванные вирусами Эпштейна-Барр и цитомегалии:
- CMV, IgG
- CMV, IgM
- EBV Early Antigen, IgG
- EBV Nuclear Antigen, IgG
- EBV VCA (капсидный антиген), IgG
- Epstein Barr Virus VCA (капсидный антиген), IgM
источник
Диагностика острых и хронических гепатитов обязательно должна носить комплексный характер.
Прежде всего она направлена на определение возбудителя данного заболевания. Также врач обязательно должен оценить степень нарушения работы печени и выявить сопутствующие осложнения. Начальной стадией диагностики является изучения анамнеза и осмотр пациента. После этого специалист назначает другие методы диагностики вирусных гепатитов – лабораторные и инструментальные.
В процессе ПЦР-диагностики заболевания определяют маркеры острых и хронических гепатитов. К ним относят следующее:
- Маркеры гепатита А. Анти-НАV IgM появляются в крови к окончанию инкубационного периода. В этот момент у человека возникают первые симптомы гепатита. Антитела присутствуют в сыворотке около полугода. Благодаря выявлению данных веществ методом ПЦР можно говорить о текущей или недавно возникшей инфекции.
Анти-НАV-total возникают в сыворотке позже. Они говорят о присутствии HAV-инфекции и последующем формировании иммунитета. Данный показатель, полученный в процессе исследований методом ПЦР, может использоваться для определения эффективности профилактики с помощью вакцин. - Маркеры гепатита В. В эту категорию входит НВsAg, который является поверхностным антигеном гепатита В и появляется в завершающей стадии инкубационного периода. Его не удается выявить в 10 % острых случаев заболевания и большинстве хронических.
Антитела анти-НВs возникают спустя 3-12 месяцев после начала развития патологии. Они присутствуют в организме примерно 5 лет. Ангиген НbcorA не удается определить в сыворотке крови. Его удается выявить лишь в гепатоцитах.
Анти-Нвcor IgM представляет собой антитела к ядерному антигену, которые характерны для завершения инкубационного периода и начала развития болезни. Определение данных веществ является значимым критерием при проведении ПЦР-диагностики.
Анти-Нвcor IgG характерны для парентеральных гепатитов во время развернутой клинической картины. Они сохраняются на всю жизнь и свидетельствуют о том, что человек перенес инфекцию. В завершение инкубационного периода можно обнаружить НвeAg. Он сохраняется в течение 10-12 недель и говорит о репликации парентеральных вирусов.
Анти-Нве представляют собой антитела к HbeAg и возникают во время развернутых проявлений. Данные вещества сохраняются на 5 лет после заболевания. При хронических парентеральных гепатитах их выявляют и по истечении указанного времени.
Помимо ПЦР-диагностики, очень важно оценить количество ферментов печени. Поражение тканей органа сопровождается попаданием в кровь ферментов, что влечет их увеличение в составе плазмы. В нормальном состоянии количество АСАТ составляет 5-35 Ед./л, а АЛАТ – 5-40 Ед./л.
Лабораторная диагностика вирусных гепатитов должна включать определение плазматической активности щелочной фосфатазы. В случае развития гепатита она увеличивается. В норме данный показатель составляет 30-115 Ед./л.
Немаловажное значение имеет оценка фракций билирубина – свободного и связанного. Его повышение обусловлено неспособностью клеток печени выводить из организма данный пигмент. В норме концентрация связанного билирубина составляет 0,1-0,3 мг/дл, а свободного – 0,2-0,7 мг/дл.
Наши постоянная читательница

Чтобы обследовать органы брюшной полости, обычно применяют ультразвуковое исследование. Это достаточно простой метод, который помогает визуализировать увеличение печени и других органов, а также оценить происходящие в них изменения. Также с помощью УЗИ оценивается состояние сосудов. Если же врач планирует сделать пункционную биопсию, данный метод поможет выбрать оптимальное место для прокола.
С помощью данного аппарата удается увидеть на мониторе определенные сечения внутренних органов. В результате можно визуализировать локальные изменения в них – камни, опухолевые образования и т.д.
Неправильные результаты можно получить исключительно в том случае, если работа органа нарушается на клеточном уровне. Вследствие этого весь орган поражен. К примеру, при изменении клеток печени удастся обнаружить нарушение оттенка тканей. Однако информацию относительно характера и тяжести болезни получить не удастся.
В такой ситуации проводится пункционная биопсия. Это наиболее точная методика, которая позволяет получить максимальное количество информации. С помощью данного способа оценивается структура тканей печени, что позволяет наиболее точно диагностировать гепатит.
Гепатит у беременных – очень опасная патология, поскольку она практически всегда провоцирует нарушения в развитии плода. При поражении вирусом типа В практически всегда заражается и ребенок. Наличие гепатита С у беременных провоцирует несколько иную картину. Тем не менее, нельзя сказать, развитие данного заболевания у беременных спровоцирует инфицирование малыша.
Чтобы провести правильную диагностику, прежде всего нужно сдать анализ крови и провести ПЦР-диагностику. При гепатите В у беременных имеет значение наличие HBsAg и НВеАg. Если они присутствуют, риск заражения ребенка повышается. В такой ситуации также уменьшается эффективность вакцины для беременных.
Если же будущая мама заболевает гепатитом С, инфицирование ребенка происходишь лишь в 5 % случаев. При этом данный вид заболевания передается от беременных к плоду лишь при условии активного протекания недуга. В большинстве случае ребенок заражается от матери при родах.
При выявлении вирусного гепатита у беременных обязательно требуется стационарная терапия. Если у женщин развивается цирроз печени, нужно принимать все меры, чтобы беременность и вовсе не наступила. Дополнительные нагрузки на организм, которые возникают у беременных, спровоцируют сильное обострение болезни.
При хронизации процесса беременность не оказывает влияния на клиническую картину патологии. Иногда у беременных женщин воспаления в печени и вовсе прекращаются. Однако нужно быть готовой к тому, что после родов гепатит резко обострится. Потому так важно держать данный процесс под контролем.
Дифференциальная диагностика проводится для того, чтобы отличить вирусный гепатит от острых поражений печени, связанных с воздействием химических веществ. Особенно важно провести диф диагностику алкогольной формы заболевания. На начальном этапе развития этого недуга часто ставят ошибочный диагноз, принимая его за вирусный гепатит. Это происходит в 50 % случаев.
Чтобы провести диф диагностику этих процессов, нужно учитывать, что алкогольный гепатит развивается исключительно на фоне постоянного употребления большого количества спиртного. Важными критериями диф диагностики в данном случае является следующее:
источник
Диагностика начинается с обследование больного. Для правильной и своевременной постановки диагноза «вирусный гепатит» врачи сначала обследуют пациента, направляют его на сдачу анализов крови и мочи.
В первую очередь они обращают внимание на такие характерные для начального периода этого заболевания симптомы, как вялость, общая мышечная слабость, снижение аппетита, тошнота, неприятные ощущения в животе, потемнение цвета мочи, увеличение и уплотнение печени, повышение болевой чувствительности ее нижнего края. В общем анализе крови врачи обращают внимание на содержание лейкоцитов, лимфоцитов, СОЭ.
Прибегают к проведению биохимических анализов крови и мочи для того, чтобы оценить степень поражения печени и подтвердить, связана ли желтуха с воспалением печени. Наиболее показательным является уровень желчного пигмента — билирубина, образующегося в печени в результате распада эритроцитов.
В норме билирубин связывается белками крови и не оказывает токсического действия на ткани организма. При гепатитах концентрация свободного и связанного билирубина в крови резко повышается. Когда она превышает 200–400 мг/л, желтуха становится видимой на глаз.
Говорит о повреждении гепатоцитов возрастающий уровень активности трансаминаз — АлАТ и АсАТ, которые попадают в кровь из клеток печени сквозь поврежденные оболочки. Существуют также специальные тесты на состояние системы свертывания крови, в которой участвуют белки, синтезируемые в печени. Диагностическое значение имеет положительная реакция мочи на уробилин.
Свидетельствующим о нарушении функции печени, является показателем — тимоловая проба. Изменение протромбинового индекса характеризует тяжесть течения вирусного гепатита, а повышение активности щелочной фосфатазы, общего билирубина свидетельствуют о нарушении секреторной функции печени. Реакция мочи на желчные пигменты в начале болезни бывает положительной значительно реже.
В диагностике немаловажное значение, как острых, так и хронических форм вирусных гепатитов отводится ультразвуковому обследованию органов брюшной полости. С помощью этого метода врачи могут определить такие изменения, которые не обнаруживаются при внешнем обследовании: увеличение печени, сужение печеночных вен, уплотнение и утолщение их стенок, признаки воспаления желчного пузыря и поджелудочной железы, расширение воротной и селезеночной вен, увеличение селезенки, увеличение лимфатических узлов. Важнейшим методом диагностики, в особенности хронических гепатитов, является биопсия печени.
Методы обнаружения антител и антигенов в крови и других жидкостях организма включает в себя серологическая диагностика. Для ранней диагностики вирусных гепатитов, в том числе безжелтушных, бессимптомных форм, в сыворотке крови определяют наличие вирусных белков (антигенов, которые еще называют маркерами вирусных гепатитов) или антител к ним с помощью иммупоферментного анализа (ИФА). Кроме того, ИФА по возможности дополняется полимеразной цепной реакцией (ПЦР), позволяющей определить наличие в сыворотке крови вирусных нуклеиновых кислот — ДНК вируса гепатита В, РНК вирусов других гепатитов, что особенно важно для начала своевременного лечения.
Иммуноферментный анализ (ИФА) — является универсальным методом иммунологической диагностики, который широко используется на практике. Он предназначен для выявления вирусных белков (антигенов) или антител, которые вырабатываются иммунной системой в ответ на проникновение вирусов в организм человека. Эти белки являются своеобразными маркерами (метками) или признаками, наличие которых позволяет поставить точный диагноз, оценить характер заболевания, помочь лечащему врачу выбрать правильное лечение. Этот метод основан на известном взаимодействии «антиген-антитело».
Для определения антигенов различные коммерческие фирмы выпускают тест-системы, которые представляют собой 96-луночные полистироловые планшеты. На дно лунок заранее сорбируют («пришивают») антитела к тому или иному антигену возбудителя, например, к поверхностному антигену вируса гепатита В — HBs-антигену.
На первом этапе в каждую лунку добавляют образец, например, сыворотку крови больного в разных разведениях, содержащую пока не определенный вирусный белок (антиген). Если этот белок (антиген) «узнал» свое антитело, то происходит их связывание. Это означает, что сыворотка больного содержит тот антиген, антитела к которому сорбированы на дне планшетки.
Для того чтобы увидеть результаты этой реакции, существует следующая стадия, на которой к комплексу «антиген-антитело» добавляют соединение, которое связывается с антителом. Это соединение содержит фермент, например, пероксидазу хрена. При добавлении к нему субстрата происходит расщепление последнего с последующим окрашиванием раствора в желто-коричневый цвет.
На следующей стадии проводят тщательную промывку каждой лунки от непрореагированных компонентов. В тех лунках, где антиген, как в нашем случае, полностью связан с антителом, он уже не может взаимодействовать с добавляемым соединением.
Поэтому оно удаляется из лунки при отмывании. По мере разведения сыворотки содержание в ней антител снижается, и они уже не в состоянии полностью связать антиген. В этих лунках соединение, содержащее фермент, связывается с антигеном и остается в лунке после промывания. На следующей стадии добавляют субстрат и смотрят результаты реакции, которые оценивают визуально или с помощью спектрофотометра.
Таким образом, мы выявили, что в образце сыворотки от больного содержится HBs-антиген. Можно также выяснить его количество или титр, определив то последнее разведение сыворотки, где появилось желтое окрашивание. Чем больше степень разведения, тем больше вируса содержится в крови больного.
Подобным образом можно определить наличие антител к тому или иному возбудителю вирусного гепатита. Только в этих случаях используют диагностические тест-системы с «пришитыми» на дно лунок не антителами, а известными антигенами. Достоинствами этого метода являются высокая чувствительность и специфичность, простота постановки реакции, возможность обследования одновременно большого количества пациентов. Среди недостатков метода можно отметить необходимость специального дорогостоящего оборудования и соответствующей квалификации персонала.
В современной лабораторной диагностике ПЦР занимает особое место. Метод ПЦР поднял клиническую лабораторную диагностику па принципиально иную высоту — уровень определения нуклеиновых кислот (ДНК и РНК), что позволяет провести прямое обнаружение инфекционного агента или генетической мутации в любой биологической среде.
При этом способом ПЦР теоретически может быть обнаружена одна искомая молекула нуклеиновой кислоты среди миллионов других. С точки зрения клинической медицины определение нуклеиновой кислоты равнозначно обнаружению возбудителя в объекте исследования.
Из биологии известно, что нуклеиновые кислоты (ДНК или РНК) обладают свойством к саморепродукции (воспроизводству). Этот принцип и лежит в основе метода ПЦР, когда этот процесс осуществляется искусственно в лабораторных условиях. Для этого из полученного от больного образца ткани (например, в случае подозрения на вирусный гепатит) выделяют сначала нуклеиновую кислоту.
Она выполняет роль своеобразной «матрицы», на которой осуществляется синтез. Нуклеиновая кислота имеет свой «отпечаток» — уникальную последовательность нуклеотидов, из которых она состоит. Для каждого возбудителя такая последовательность изучена, составлена своеобразная «карта».
Самый главный элемент в ПЦР — это праймер (короткие участки ДНК, комплементарные (соответствующие) участкам выделенной из образца нуклеиновой кислоты). Праймеры обеспечивают запуск и специфичность реакции.
Таким образом, тест-система для ПЦР состоит из смеси нуклеиновых кислот испытуемого образца, праймера и специальных ферментов (полимераз)) с помощью которых эта реакция невозможна. ПЦР-анализ включает несколько циклов (этапов), в результате которых получаются точные копии распознаваемого участка матричной нуклеиновой кислоты. Эти циклы повторяются 30–50 раз в соответствии с заданной программой. Конечный продукт этой реакции распознается с помощью метода электрофореза в геле.
Одним из важнейших критериев диагностической эффективности любого лабораторного анализа является показатель «чувствительности». При этом следует различать аналитическую и диагностическую чувствительность. Аналитическая чувствительность, применительно к ПЦР, представляет собой то минимальное количество копий ДНК или РНК в 1 мл раствора образца, которое может быть определено данной тест-системой.
Большинство коммерческих тест-систем позволяет обнаружить в биологической пробе искомую нуклеиновую кислоту, даже если ее концентрация составляет несколько сот копий в 1 мл образца. С этим связано общее положение, определяющее клиническую пригодность любых лабораторных способов диагностики или тест-систем — диагностическая чувствительность метода не должна быть ниже 95–98 %.
Второй универсальный критерий лабораторной эффективности — «специфичность», которая определяется процентом здоровых людей, имеющих истинно отрицательные результаты анализа. Метод ПЦР обладает высочайшей специфичностью, которая достигает 99-100 %.
Диагностическая чувствительность и специфичность ПЦР сопоставимы, а зачастую и превосходят показатели, обеспечиваемые другими методами, которые являются «золотым стандартом» в диагностике инфекционных заболеваний.
Результаты ПЦР-анализа можно получить в течение одного рабочего дня, при этом отобранные для анализа пробы могут храниться (накапливаться) в течение даже нескольких недель при соблюдении соответствующих температурных норм. Проведенная недавно в нескольких зарубежных исследовательских центрах суммированная оценка чувствительности различных методов диагностики показала, что ИФА имеет чувствительность 50–70 %, а ПЦР — от 90 до 100 %.
ПЦР, по сравнению с ИФА и другими способами, обладает двумя важными преимуществами: высокой чувствительностью и непродолжительностью анализа по времени, то есть «актуальностью» получения результата исследования врачом и пациентом.
— метод позволяет обнаруживать любые ДНК и РНК даже в тех случаях, когда с помощью других способов это сделать невозможно;
— метод обладает высокой специфичностью (до 100 %). Она обусловлена тем, что в исследуемом «материале определяется уникальный фрагмент нуклеиновой кислоты, характерный только для данного возбудителя или гена;
— возможность проведения не только качественной (наличие), но и количественной (концентрация) оценки содержания нуклеиновой кислоты. В настоящее время с помощью коммерческих тест-систем можно определять несколько сот копий в исследуемом образце;
— высокая технологичность и автоматизация метода позволяют врачу получить результаты исследования и ознакомить с ними пациента в день проведения анализа;
— ПЦР позволяет выявить возбудителя в организме еще до развития заболевания, например, в инкубационном периоде;
— для проведения ПЦР—анализа достаточен минимальный объем пробы (до нескольких микролитров);
— ПЦР-анализ позволяет одновременно диагностировать несколько возбудителей заболеваний в одной пробе без ущерба для чувствительности или специфичности результата;
— полученные результаты ПЦР можно вносить в компьютерные информационные носители или фотографировать для дальнейшей оценки независимыми экспертами.
Несмотря на вышеуказанные достоинства метод ПЦР все же не лишен некоторых недостатков, которые следует учитывать при оценке результатов исследований:
— высочайшие требования к оснащению лаборатории, качеству тест-систем и строжайшее соблюдение регламента исследования во избежание получения ложных результатов. Решение проблемы качества анализов возможно при соответствующей квалификации персонала и обязательной сертификации лаборатории;
— неоднозначная оценка положительного результата ПЦР. Именно этот факт зачастую является необоснованным аргументом врачей-практиков для сомнения в полученном результате и эффективности метода ПЦР. Например, у лиц с обнаруженной в крови методом ПЦР ДНК возбудителя клинически заболевание может развиться не всегда.
В данной ситуации при оценке ПЦР-анализа следует говорить об инфицированное больного, а не о развитии инфекционной болезни. Метод ПЦР — анализа позволяет определять наличие или отсутствие возбудителя, в значительной мере отвечает на вопрос «лечить не лечить», а также дает возможность оценить качество лечения путем контроля наличия или отсутствия возбудителя. Врач, оценивая итог ПЦР-анализа, осознает, что этот результат является не единственным аргументом в принятии решения о начале лечения или отказе от него.
Для каждого вида возбудителя вирусных гепатитов разработаны тест-системы, но наиболее ценным метод ПЦР оказался в диагностике вирусов гепатитов В, С, D, G. Метод ПЦР является крайне важным для диагностики гепатита В. Это связано с тем, что среди множества разновидностей этого вируса встречаются мутантные (с измененными признаками), которые не определяются обычными серологическими тестами.
Метод ПЦР-анализа позволяет выявить, и какой форме находится вирус гепатита 15, способен ли он к самостоятельному размножению или интегрировался (встроился) в ДНК клетки-хозяина. Это имеет крайне важное клиническое значение, так как при интегративной форме этой инфекции человек не заразен для окружающих (безопасность для полового партнера, профессиональная пригодность, отсутствует риск вертикальной передачи вируса от матери к плоду и т. п.).
Кроме того, таким пациентам не показана противовирусная терапия, более того — она даже опасна. Вместе с тем, при интегративной форме инфекции резко возрастает (более чем в 200 раз) вероятность развития рака печени. Таким людям необходимо не менее одного раза в год проходить комплексное клинико-лабораторное и инструментальное обследование.
Метод ПЦР может выступать в качестве арбитра для определения необходимости начала лечения и контроля его эффективности. Быстрое исчезновение из крови ДНК вируса гепатита В является прямым и надежным тестом успешного исхода противовирусного лечения.
Таким образом, определение ДНК вируса гепатита В в плазме крови является важнейшим анализом, который в совокупности с другими лабораторными исследованиями позволяет объективно диагностировать инфекцию, определять характер инфекционного процесса, выступать в качестве критерия в проведении терапии и оценки ее эффективности.
Метод ПЦР—анализа не имеет себе равных и в диагностике, оценке прогноза и успеха противовирусной терапии инфекции, вызванной вирусом гепатита С. Применение ПЦР позволяет выявлять вирус гепатита С на самом раннем этапе инфекционного процесса, поскольку РНК вируса гепатита С может обнаруживаться в сыворотке крови уже через неделю после инфицирования. С помощью этого метода определяют генетические разновидности этого вируса, которые позволяют врачу назначить правильное лечение.
В случае вирусного гепатита D метод ПЦР-анализа позволяет определить вирусную РНК в сыворотке крови пациента, а также смешанную гепатит В и D инфекцию. Поэтому данный метод исследования может использоваться для контроля эффективности лечения, прогноза течения и исхода болезни. Врачу важно определить, имеется ли смешанная инфекция, так как гепатит D усиливает некротический эффект при гепатите В, а, стало быть, повышает риск его развития.
Метод ПЦР-анализа в настоящее время остается единственным способом доказать наличие заражения вирусом гепатита С.
Гепатит Е. Основными диагностическими признаками вируса гепатита Е являются: предположение о водном механизме передачи, возраст больного от 20 до 40 лет, распространение в регионах преимущественно тропического и субтропического пояса, клинические проявления подобно гепатиту А с преобладанием легких форм, регистрация тяжелых форм с угрозой летального исхода у беременных женщин во второй половине беременности, реже — в раннем послеродовом периоде и у кормящих матерей (протекают с интенсивным гемолизом, гемоглобинурией, острой почечной недостаточностью и тяжелым тромбогеморрагическим синдромом). Подтверждает диагноз выявление антител в крови.
Гепатит В. Вирусный гепатит В врачи подозревают в случае, если заболевшему за 45-180 дней до начала болезни переливали кровь или ее компоненты (эритроцитарную, лейкоцитарную, тромбоцитарную массу), проводили оперативные вмешательства, исследования внутренних органов, многочисленные инъекции (в том числе наркотиков), или, что случается гораздо реже, если больной имел половой или тесный контакт с больным гепатитом В. Критерием раннего подтверждения диагноза служит обнаружение в крови HBs, НВе и НВс-антигенов, а также вирусной ДНК.
Гепатит С. В отличие от гепатита В, в диагностике которого учитываются антигенные и антительные маркеры, при гепатите С методом ИФА улавливаются только антитела, что связано с низкой концентрацией вируса в крови. Антигены вируса гепатита С могут быть обнаружены в биоптатах печени.
Лабораторная диагностика включает в себя три основных вида анализов.
Определение антител. Несмотря на высокую специфичность, современные диагностические иммуноферментные системы не застрахованы от гипердиагностики, то есть отложноположительных результатов. Для их исключения также требуется оценка на основе результатов анализов, полученных через разные промежутки времени. Возможны и ложноотрицательные результаты, когда антивирусные антитела не удается обнаружить, несмотря на присутствие вируса в организме. Это бывает в следующих случаях:
— начальный период заболевания;
— во время приема больными иммунодепрессантов — препаратов, подавляющих иммунную систему;
— при заражении некоторыми генотипами (прежде всего 3 и 4).
В настоящее время выпускаются коммерческие тест-системы для выявления антител к вирусу гепатита С 1-го генотипа. Однако такие тесты могут быть недостаточно эффективны для надежного определения антител при инфицировании вирусом иного генотипа. Это имеет огромное значение для регионов, где превалируют вирусы других типов. Таким образом, для эффективной диагностики гепатита С необходим высокочувствительный тест, способный реагировать с антителами к вирусу гепатита С любого генотипа.
Определение вирусной РНК. С диагностической целью производится обнаружение РНК вируса гепатита С. На сегодняшний день этот тест считается «золотым стандартом» в диагностике гепатита С. Для этого наиболее широко используется классический вариант полимеразной цепной реакции (ПЦР). С ее помощью удается следить за размножением вируса, а также судить о присутствии его в печени и других тканях. Определение РНК наиболее часто применяют для подтверждения результатом выявления антител, постановки раннего диагноза острою гепатита (вирусную РНК удается обнаружить уже на 7-21-й день после инфицирования, то есть задолго до появления первых антител), для наблюдения за беременными в перинатальный период заражения и контроля за эффективностью антивирусной терапии.
Данные этих двух анализов хорошо дополняют друг друга. Положительные результаты ПЦР-анализа в сочетании с отрицательными результатами на антивирусные антитела характерны для некоторых периодов острого гепатита. Негативные показатели ПЦР-анализов на фоне положительных антительных тестов могут быть следствием низкой (не улавливаемой в ПЦР) концентрации вируса в крови. Повторные положительные ПЦР-анализы крови отражают активацию вируса в клетках печени или других органов.
Также ПЦР применяется для обнаружения вируса в тканях печени, взятых при биопсии. Это дает более полную информацию о развитии инфекционного процесса, так как вирус способен длительное время находиться в гепатоцитах, не выходя в кровь или присутствуя в ней в низких концентрациях. Это чаще происходит на ранних этапах инфекции, но наблюдается и при хроническом гепатите.
Определение белков (антигенов) вируса гепатита С. Принципиальная возможность выявления белков вируса гепатита С была установлена вскоре после открытия вируса при иммунофлюоресцентном изучении тканей, взятых из печени больных хроническим гепатитом С людей и шимпанзе, зараженных этим вирусом.
Определение вирусных белков (антигенов) в сыворотке крови из-за их низкого содержания долго не удавалось. Лишь недавно были разработаны методические подходы для иммуноферментного выявления внутреннего С-белка в крови и организовано производство первых коммерческих тест-систем. Их внедрение в практику позволит решать спорные вопросы диагностики на более экономичной основе, чем определение вирусной РНК. Определение уровней АлАТ является наиболее дешевым методом оценки активности течения гепатита С. Однако однократно полученные данные могут быть недостаточными для определения тяжести заболевания.
Более важную информацию относительно поражения печени может дать определение концентрации АлАТ в течение нескольких месяцев. Получить информацию о степени поражения печени, недоступную при других методах исследования, может дать врачу биопсия печени. Данные, полученные в результате этой процедуры, позволяют принять решение в пользу начала или отмены противовирусного лечения.
В статье использованы материалы из открытых источников: Автор: Трофимов С. — Книга: «Болезни печени»
А. А. Асратян Институт эпидемиологии и микробиологии им. Н.Ф.Гамалеи РАМН,
Московская медицинская академия им. И.М.Сеченова
Основой лабораторной диагностики вирусных гепатитов служат:
— знания об их возбудителях и репликации
— информация о появлении и исчезновении маркеров инфицирования
— современные иммунохимические и молекулярно- биологические методы детекции антигенов, антител и нуклеиновых кислот/
Лабораторная диагностика гепатита В (ГВ) Строение вириона см. рис. 1.
Лабораторная диагностика ГВ — основана на выявлении специфических для ГВ антигенов и соответствующих антител в крови, а также вирусных нуклеиновых кислот, основными из которых являются:
анти-НВс класса Ig М и IgG
Наиболее широко в диагностике ГВ используется определение НВsAg. Данный антиген выявляется как при остром, так и при хроническом заболевании (однако острая инфекция обычно подтверждается наличием высоких титров анти-НВс IgМ). При остром ГВ поверхностный антиген вируса обнаруживается через 3-5 недель от момента инфицирования, то есть задолго до появления клинических признаков болезни и в этих случаях является единственным серологическим маркером. НВsAg постоянно выявляется в преджелтушном и желтушном периодах болезни. Персистирование НВsAg в течение 6 месяцев и более указывает на затяжное или хроническое течение болезни, и позволяет предположить хроническое носительство вируса. Элиминация НВsAg и появление антител к нему является непременным условием выздоровления. Серологическими маркерами репликации ВГВ являются — анти-НВс класса IgМ, НВеAg, ДНК и ДНК-полимераза, которые обнаруживаются при остром ГВ с первых дней клинических проявлений и могут обнаруживаться при обострении хронического ГВ. Серологические маркеры репликации ВГВ определяют как в целях общей диагностики, так и для оценки эффективности применяемой терапии. НВсAg выявляется в ткани печени и не определяется в сыворотке крови. Опосредовано его присутствие в организме отражают циркулирующие антитела – анти-НВс класса IgМ и IgG. В острый период ГВ наличие анти-НВс класса IgМ является дополнительным маркером этого заболевания. Однако необходимо учитывать, что около 50% больных хроническим ГВ также могут иметь эти антитела в периоде обострения, но чаще в низких концентрациях. Наличие в сыворотке крови только анти-НВс класса IgG наблюдается в период между исчезновением НВsAg и образованием анти-НВs. Сочетанное выявление анти-НВс класса IgG в низком титре с анти-НВs указывает на перенесенную ГВ-инфекцию и наличие иммунитета. Тестирование НВеAg проводят в сыворотках крови только с наличием НВsAg и позитивный результат данного маркера свидетельствует об активном процессе – либо подтверждает диагноз острого ГВ, либо свидетельствует об обострении хронического ГВ. Длительность циркуляции НВеAg имеет важное прогностическое значение: выявление НВеAg через 2 и более месяца после начала заболевания служит признаком возможного развития хронического гепатита. Выявление НВеAg без присутствия НВsAg в сыворотке крови в подавляющем большинстве случаев указывает на ложный результат анализа. Однако больные, инфицированные мутантным вирусом могут оставаться серонегативными по НВеAg, несмотря на сохраняющуюся инфекционность и наличие анти-НВе Наличие ДНК-ВГВ (наиболее чувствительный маркер продолжающейся репликации ВГВ) в сыворотке крови указывает на высокую инфекционность данного образца и активное размножение вируса в организме. Позитивный результат удается зарегистрировать практически у всех больных острым ГВ в разгар заболевания. Снижение его концентрации в процессе лечения хронического гепатита является хорошим прогностическим признаком, указывающим на эффективность применяемой терапии. Высокая активность аминотрансфераз сыворотки отражает воспалительное повреждение ткани печени, вызываемое преимущественно реакциями иммунной системы организма против инфицированных вирусом гепатоцитов, а не прямым цитопатическим действием вируса. Высокий уровень ДНК-ВГВ в сочетании с низким уровнем аминотрансфераз свидетельствует о недостаточном иммунном ответе организма. Выявление анти-НВе при отсутствии НВеAg и ДНК-ВГВ свидетельствует о закончившейся активной репликации инфекции. Сероконверсия НВsAg в анти-НВs происходит у 90-95% больных с острым ГВ в стадии разрешения инфекционного процесса и, является показателем иммунитета к вирусу ГВ, то есть наличие анти-НВs свидетельствует о перенесенной инфекции и наличие иммунитете к этой инфекции. Лица, имеющие эти антитела в защитной концентрации (10 МЕ и более) не болеют ГВ и не нуждаются в вакцинации. Все применяемые методы исследования для определения специфических маркеров ГВ можно разделить на 2 группы – иммунохимический и молекулярно-биологические. Иммунохимические – основное место принадлежит иммуноферментному анализу (ИФА) с его высокой чувствительностью и специфичностью, простотой проведения и стабильностью реактивов. Молекулярно-биологические – точечная и жидкостная гибридизация, а также цепная полимеразная реакция (ПЦР) – позволяет выявлять наличие ДНК-ВГВ непосредственно, либо с помощью определения вирусоспецифического фермента – ДНК- полимеразы. НВ sAg /анти-НВ s Для выявления основного маркера ВГВ, разработаны разнообразные методы, позволяющие определить антиген в концентрации до 0,05 нг/мл, которые подразделяются на так называемые «поколения» (табл. 1). В настоящее время основным методом обнаружения НВsAg является ИФА Важным этапом в развитии лабораторной диагностики вирусных гепатитов в России стали проведение (с 1998 г.) сравнительных испытаний диагностических препаратов для оценки их качества под эгидой МЗ РФ. Современные диагностические препараты обладают высокой специфичностью, но возможны и ложноположительные результаты. Для разграничения ложноположительных от истинно положительных результатов применяется тест нейтрализации НВsAg – специфической сывороткой. Принципиально новым для системы выявления НВsAg стало требование к отечественным производителям диагностических препаратов – обязательное включение в тест-систему слабоположительного контрольного образца, содержащего НВsAg в концентрации 1 нг/мл. Для определения анти- НВsAg был испытан весь спектр иммунохимических методов, основной из которых сейчас – ИФА (для качественного и количественного анализа). Анти-НВс класса Ig М и IgG , НВе Ag – анти-НВе (рис. 2 и табл. 2) Для тестирования этих маркеров могут быть использованы различные варианты твердофазного иммуноанализа: иммуноферментный, радиоиммунный, химиолюминисцентный и их различные варианты. ДНК ВГВ — определяют при помощи проведения ПЦР– анализа. В настоящее время наиболее широкое распространение получили амплификационные методы детекции ДНК ВГВ. Появилась возможность определять ДНК ВГВ в качественном и количественном варианте.
Лабораторная диагностика гепатита Д (ГД) Вирус гепатита Д (ВГД) – это дефектный вирус, содержащий одно-спиральную РНК, которому для репликации необходимо помощь вируса ГВ для синтеза оболочечных белков, состоящих из HBsAg, который используется для инкапсуляции генома ВГД. ВГД не принадлежит ни к одному из известных семейств вирусов животных, по своим свойствам ВГД наиболее близок к вироидам и сателлитным вирусам растений. Лабораторная диагностика осуществляется путем обнаружения серологических маркеров ВГД, включая наличие антигена, антител к нему и РНК ВГД. Обнаружение антигена ВГД и РНК ВГД в сыворотке крови или ткани печени свидетельствует о наличии активной ГД-инфекции, однако, следует отметить, что эти маркеры могут не обнаруживаться в сыворотке больных фульминантным ГД. Маркером активной репликации ВГД также является анти-ВГД класса IgМ. Серологические маркеры инфекции ГД зависят от того, как был приобретен вирус – в виде коинфекции с ВГВ (у большинства больных заболевание имеет острое течение и заканчивается выздоровлением) или суперинфекции у больных с хронической ГВ-инфекцией (протекает тяжелее, чем коинфекция — в 10% развивается фульминантный гепатит). При коинфекции в большинстве случаев антитела — анти-ВГД класса IgМ и IgG — обнаруживаются в течение заболевания. Титр анти-ВГД обычно снижается до практически неопределяемых уровней после выздоровления, и не сохраняется никаких серологических маркеров того, что человек был когда-либо инфицирован ВГД. Антиген ВГД определяется только у 25% больных и обычно исчезает вместе с исчезновением HВsAg. При суперинфекции у больных с хронической ГВ-инфекцией серологическая картина имеет следующие характерные особенности: – титр HBsAg снижается к моменту появления антигена ВГД в сыворотке; — антиген ВГД и РНК-ВГД продолжают определяться в сыворотке, так как обычно у большинства пациентов с суперинфекцией ГД (70-80%) развивается хроническая инфекция, в отличие от случаев коинфекции; — определяются высокие титры антител (анти-ВГД) как класса IgМ, так и IgG, которые сохраняются неопределенное время. Серологические маркеры вируса ГД определяют методом иммуноферментного и радиоиммунного анализа, а РНК-ВГД — методом полимеразной цепной реакции. Отечественными и зарубежными промышленными биотехнологическими предприятиями выпускаются диагностические наборы, включающие все необходимые компоненты и реактивы для постановки теста. В диагностических препаратах используют дельта-антиген, полученный из печени сурков, экспериментально зараженных ГД; антиген, выделенный из печени погибших носителей ВГД; дельта-антиген, полученный генно-инженерным способом.
Лабораторная диагностика гепатита С (ГС) Открытие возбудителя ГС стало возможным благодаря методам молекулярной биологии в 1989-1991 гг. Сначала путем клонирования был получен из сыворотки больных с гепатитом “ни-А, ни-В” вирусный геном, а затем был установлена и структура самого вируса. Физико-химическая характеристика вируса позволили отнести ВГС к семейству флавовирусов. Геном вируса ГС (ВГС) представлен однонитчатой позитивной РНК, состоящих из 10 000 нуклеотидных оснований, образующих регионы, которые кодируют три структурных белка (С, Е1, Е2) и пять неструктурных (NS2, NS3, NS4, NS5). Особенностью ВГС является чрезвычайно высокая гетерогенность его генома. Анализ нуклеиновых кислот РНК-ВГС различных изолятов выявил существенные отличия в их первичной структуре. На основании этих данных была построена классификация ВГС, разделяющая их на варианты ( их 6-9) и субтипы- генотипы, одни из которых присутствуют во всех регионах мира, а другие только в отдельных странах. Лабораторная диагностика ГС была решена при помощи современных методов молекулярной биологии, учитывая, что при ГС вирус находится в крайне низкой концентрации и его антигены не доступны выявлению с помощью современных методов индикации, усилия исследователей сосредоточены на выявлении антител к различным антигенным компонентам вируса, обнаружение которых может служить индикатором наличия вируса. В качестве антигенов использовали белки, кодированные структурной и неструктурной зоной РНК-ВГС, полученные при помощи рекомбинантной технологиии или синтеза (полипептиды, используемые в современных иммунологических методах – С22-3; С33с, С100-3, С200, NS5, S-1-1). Лабораторная диагностика ГС основывается на обнаружении серологических маркерв ВГС: антител к вирусу ГС (анти-ВГС, анти-ВГС класса IgМ, IgG) методом ИФА и РНК-ВГС методом ПЦР. К настоящему времени разработаны 4 поколения тест-систем для выявления анти-ВГС в иммуноферментном методе, но ИФА первого поколения сейчас не используется из-за низкой чувствительности. РНК-ВГС является показателем активной репликации ВГС и самым ранним маркером инфекции, и может быть обнаружена методом полимеразной цепной реакции уже через 1- 2 недели после инфицирования, незадолго до повышения уровня сывороточных трансаминаз. Анти-ВГС обнаруживаются к 5-6 неделе после начала гепатита в 80% случаев и к 12 неделе у 90% лиц методом иммуноферментного анализа. При определении анти-ВГС в некоторых случаях регистрируется ложноположительная реакция. Для разграничения ложноположительных образцов от образцов действительно содержащих антитела к ВГС, разработаны дополнительные тесты – рекомбинантный иммуноблотинг, определение спектра белков анти-ВГС. Иммуноблотинговые диагностикумы позволяют исключить неспецифический результат, полученный методом ИФА, однако визуальная оценка иммуноблотинговых полос может быть неоднозначной в разных диагностических центрах. В нашей стране более широкое распространение получили отечественные подтверждающие твердофазные иммуноферментные тест-системы (так называемы системы «Спектр»), основанные на определении антител к отдельным вирусным антигенам: core, NS3, NS4ab, NS5a. Выявление РНК ВГС считается «золотым» стандартом в диагностике ГС и подтверждением положительных результатов обнаружения анти-ВГС. В настоящее время для индикации РНК ВГС используется ПЦР в качественном и количественном варианте. Чувствительность методов определения РНК ВГС повышается с каждым годом, достигая в настоящее время 10-50 копий РНК в 1 мл крови. Диагноз хронического ГС у лиц с наличием анти-ВГС обычно ставится на основании повышенных печеночных проб в течение более 6 месяцев.
Лабораторная диагностика гепатита А (ГА) Вирус ГА (рис. 3) — это РНК- содержащий вирус, размером 27 нм, классифицированный как пикорнавирус. Во всех изолятах собранных в разных частях мира, наблюдается только один серотип ВГА. ВГА не имеет наружной оболочки, но состоит из наружной белковой капсулы, или капсида, содержащего внутри положительную одноцепочную РНК, который действует в качестве матрицы для выработки вирусных белков внутри клетки-хозяина. Лабораторная диагностика ГА основана на выявлении маркеров вируса ГА – антигена ВГА, антител (анти-ВГА класса IgМ и IgG ), а также РНК ВГА. Окончательным доказательством о текущей или недавней инфекции служит наличие в сыворотке крови (даже в одной пробе сыворотки) антител к ВГА класса IgM (анти-ВГА IgM) и наличие ВГА в фекалиях. На перенесенную инфекцию ГА, а также на длительный иммунитет, указывает наличие антител к ВГА класса IgG (анти-ВГА IgG). Диагноз острого ГА подтверждается в острой или ранней стадии выздоровления при наличии анти-ВГА класса IgM, которые появляются в последние 5-10 дней инкубационного периода и продолжают выявляться на протяжении 6-7 месяцев от начала заболевания. Кроме того, эти антитела могут быть выявлены в первые месяцы у лиц (20-30%), вакцинированных инактивированной вакциной против ГА. Их образование связано с первичным иммунным ответом на введение антигена, а не на инфекцию, вызванную вакциной. РНК ВГА может быть выявлена за несколько дней до повышения активности АлАТ и в течение 5 — 59 дней заболевания при типичном течении ГА; при затяжных случаях — РНК ВГА в среднем может определяться до 95 дней. Антиген вируса ГА (ВГА-Ag) обнаруживается в фекалиях больных за 7-10 дней до проявления клинических симптомов и в первые дни заболевания, что используется также для ранней диагностики и выявления источников возбудителя инфекции. Концентрация ВГА в фекалиях является наивысшей на протяжении 2-х нед. перед появлением желтухи. У взрослых выделение вируса с фекалиями продолжается обычно менее одной недели после появления желтухи. Вирус, однако, был обнаружен также через 2 мес. от начало заболевания (во время обострения). Дети могут выделять вирус более длительно, чем взрослые, возможно в течение нескольких недель после клинического проявления заболевания. Хроническое выделения ВГА из фекалий не отмечается. Определение антигена ВГА нашло также применение в санитарной вирусологии при исследовании воды на наличие вируса. Анти-ВГА класса IgG (рис. 4) также появляются рано в начале заболевания (с 3-4 недели), сохраняются на протяжении всей жизни и обеспечивают пожизненную защиту от этого заболевания. Определение анти-ВГА IgG используется для изучения иммуноструктуры населения, динамики специфического гуморального иммунитета. Определение анти-ВГА класса IgG важно также для пред- и поствакцинального скрининга (минимальная протективная концентрация анти-ВГА соответствует 20 МЕ/л). Для их определения отечественными производителями выпускаются коммерческие диагностические препараты иммуноферментного анализа. Лабораторная диагностика основана на выявлении маркеров вируса ГА с помощью специфических иммунодиагностических методов — методы ИФА, РИА. Отечественными и зарубежными промышленными биотехнологическими предприятиями выпускаются диагностические наборы, включающие все необходимые компоненты и реактивы для постановки теста. Кроме твердофазных ИФА и РИА с успехом применяется и метод иммуноэлектронной микроскопии, метод ПЦР. Все вышеупомянутые методы иммунодиагностики с равной вероятностью выявляют инаппарантные, бессмиптомные или клинически выраженные формы ГА. Особое место в лабораторной диагностике ГА занимают молекулярно-генетические методы тестирования РНК ВГА. ПЦР диагностика позволяет обнаружить РНК ВГА в концентрации 40 копий/мл. В настоящее время происходит накопление данных о месте ПЦР в системе лабораторной диагностики ГА.
Лабораторная диагностика гепатита Е (ГЕ) Этиологический агент гепатита Е (ГЕ) — это сферический вирус, лишенный внешней оболочки, это односпиральный РНК-вирус размером около 32-34 нм в диаметре. При постановке диагноза ГЕ в каждом отдельном случае необходимо принять во внимание несколько диагностических аргументов: — наличие у больного симптомокомплекса острого, и предположительно инфекционного гепатита, — надежное исключение этиологического участия вирусов ГА и ГВ, основанное на отрицательных результатах серологических тестов — анти-ВГА класса IgM и анти-НВс класса IgM, — тщательный анализ данных эпидемиологического анамнеза, включая указания на недавние выезды в эндемичные регионы, — исследование (по возможности) фекалий больного на присутствие частиц вируса ГЕ методом иммуноэлектронной микроскопии, ПЦР. Существуют диагностические методы, основанные на применении иммунофлюоресцирующих антител (МФА) для определения антигена ВГЕ в фекалиях и иммуноферментного анализа (ИФА) для определения антител к ВГЕ — анти-ВГЕ класса IgM и IgG. Наличие анти-ВГЕ класса IgM с высокой частотой определяются в сыворотках больных ГЕ в острой стадии заболевания и в период ранней реконвалесценции; выявление анти-ВГЕ класса IgG свидетельствуют о перенесенной в прошлом ГЕ — инфекции. Для диагностики ГЕ определяют также РНК ВГЕ. Отечественные фирмы производители диагностических тест-систем для выявления маркеров вирусных гепатитов:
МОСКВА и область — НИАРМЕДИК — ЭКОлаб — БИОСЕРВИС
НОВОСИБИРСК — ВЕКТОР БЕСТ — ВЕКТОР МБС ( МЕДИКОБИОЛ.СОЮЗ) — ВЕКТОР БИАЛЬГАМ
НИЖНИЙ НОВГОРОД — МИКРОГЕН (бывший ИМБИО) — ДИАГНОСТИЧЕСКИЕ СИСТЕМЫ САНКТ-ПЕТЕРБУРГ — АВИЦЕННА — АКВАПАСТ
Когда необходима лабораторная диагностика вирусного гепатита С, то врач обязательно учитывает следующие факторы, которые являются важными:
- наличие или отсутствие в крови маркеров инфицирования вирусом гепатита С, а также других типов;
- показатели активности ферментов печени;
- результаты клинического осмотра больного;
- данные эпидемиологического анамнеза.
Диагностировать гепатит С с высокой степенью надежности позволяет только комплексный учет всех данных (нужно отметить, что диагностика гепатита В проводится также). Для полной диагностики вирусного проводится ряд анализов крови:
- общий анализ крови;
- биохимический анализ крови;
- ПЦР на определение РНК вируса (ПЦР – полимеразная цепная реакция);
- коагулограмма (определение свертываемости крови).
Также проводится УЗИ органов брюшной полости. Может назначаться пункционная биопсия печени. Только имея на руках все результаты, врач сделает точную диагностику. Также будет определен уровень развития вирусного процесса в организме, сделана оценка состояния печени и степень ее повреждения. Доктор подберет безопасное и эффективное лечение.
Задача врача при определении предрасположенности к вирусному гепатиту С существенно упрощается, если он располагает информацией о ранее имеющихся у человека заболеваниях и проведенных обследованиях.
Для проверки функционирования печени ее необходимо обследовать. Для выявления дисфункции в ее работе помогут исследования крови. При предположении наличия гепатита С врач назначает специальные исследования для обнаружения антител, которые вырабатываются для борьбы с этим тяжелым недугом.
При исследовании крови вирус гепатита С в крови подтверждается прямым или косвенным путем, на основании РНК – наследственной информации вируса (определяется с помощью ПЦР) либо при обнаружении антител в крови. Если посредством ПЦР подтверждается наличие в крови РНК вируса, то это говорит об остром течении заболевания.
При наличии антител против вируса гепатита С существует два варианта – либо хроническое течение заболевания, либо инфекция была излечена ранее. Дело в том, что даже после полного излечения антитела обнаруживаются в крови человека еще продолжительное время.
То есть лабораторная диагностика подразумевает сдачу анализа на определение наличия антител к вирусу гепатита С (если проводится диагностика гепатита В, то определяются антитела к этому типу вируса). При положительном результате назначается прямое исследование на нахождение в крови вируса. Для этого применяется метод ПЦР – полимеразная цепная реакция. Тест ПЦР является особо чувствительным, он используется именно для подтверждения наличия в крови человека вируса гепатита С.
В связи с тем, что у людей с хронической формой гепатит С очень высока вероятность возникновения рака печени, у них систематически, через определенные промежутки времени (от полугода до года) берут анализ крови для определения наличия онкомаркера рака печени или альфа-фетопротеина. Точно с такими же временными интервалами проводится и ультразвуковое исследование печени.
При положительных результатах анализов, то есть если анализ ПЦР подтвердил наличие вируса в организме, врачом может быть назначена биопсия печени. Эта процедура позволяет увидеть, насколько вирус распространен в печени, и определить степень ее повреждения.
При проведении биопсии производится забор участка ткани печени. Для анализа материал забирают с помощью специальной иглы. Далее полученный образец ткани подвергают исследованию, которое проводится под микроскопом.
Для диагностики назначаются и другие процедуры, такие как КТГ, УЗИ. Они применяются для того, чтобы исключить рак печени.
Анализ крови сдается также для определения типа вируса гепатита С или его генотипа, который поразил организм больного человека. Если есть данные о генотипе вируса и области поражения им печени, лечащему доктору будет проще подобрать необходимые методы лечения.
Необходимо провериться и сдать анализы крови на наличие гепатита С, в том числе сделать исследование методом ПЦР, если:
- присутствуют симптомы каких-либо заболеваний печени, например, плохой анализ крови;
- были использованы нестерильные шприцы, даже если это произошло много лет назад;
- половой партнер имеет такое заболевание, как гепатит С;
- проводился гемодиализ;
- при лечении применялись донорские органы или кровь, которые были получены до 1992 года (после этого года все донорские материалы подвергаются проверке на гепатит С).
Обязательно сдают анализ крови на гепатит С работники медицинских учреждений, которые по роду своей работы контактируют со шприцами, кровью и другими биологическими жидкостями пациентов.Нужно отметить, что в настоящее время существует возможность обследоваться в домашних условиях. Для этого применяется специальный тест, который продается в аптеке. При получении положительного результата необходимо сразу же обратиться к врачу и пройти обследование, которое определит наличие или отсутствие вируса в организме.
При постановке диагноза гепатит С врач назначит лечение и даст рекомендации для того, чтобы предотвратить дальнейшее распространение вируса.
двунитчатая ДНК с однонитчатым участком
в среднем 60-90 дней, может быть до 6 месяцев
преимущественно дети до 1 5 лет
Переход в хроническую форму
I. Гепатит А (гА). Лабораторная диагностика гА основывается либо на выявлении самого возбудителя (метод иммунной электронной микроскопии — ИЭМ), его антигенов (радиоиммунный, иммуноферментный, иммунофлюорес-центный метод — РИА, ИФА, ИФ) или антител к вирусу гА (РИА, ИФА).
Для ранней диагностики заболевания, а также выявления источников инфекции используется определение антигена вируса гА в фекалиях больных, где он появляется за 7-10 дней до клинических симптомов и в первые дни заболевания.
Из определяемых в настоящее время специфических маркёров гА важнейшими являются антитела класса Ig M к вирусу гА, которые появляются в сыворотке крови и слюне уже в начале заболевания и сохраняются в течение 3-6 месяцев. Обнаружение антител класса Ig M к вирусу гА однозначно свидетельствует о гепатите А и используется для диагностики заболевания, в том числе и бессимптомных случаев инфекции,и выявления источников инфекции в очагах.
Антитела к вирусу гА класса Ig G выявляются с 3-4-й недели заболевания и сохраняются длительно, что позволяет оценить состояние иммунитета населения, динамику специфического гуморального иммунитета.
Вирус гепатита А в материале от больного можно выявить методом иммунной электронной микроскопии. В основе метода лежит смешивание суспензии вируса с антисывороткой, отделение иммунных комплексов и исследование их в электронном микроскопе.
II. Гепатит В (гВ). В организме людей, заражённых вирусом гВ, с разной частотой и на разных этапах могут выявляться серологические маркёры: поверхностный HBs Ag и сердцевинный НВе Ag, а также антитела к ним (anti-НВс, anti-HBe, anti-HBs). Динамика их появления и интерпретация результатов представлены в табл. 4 и 5.
источник







