Исследование РНК вируса гепатита С является наиважнейшей процедурой, которая позволяет с большой точностью устанавливать длительность и методы лечения больных.
Диагностика заболевания состоит из нескольких различных исследований крови, таких как:
- маркеры гепатита С (анти-HCV);
- определение РНК вируса гепатита С (РНК HCV).
Первое исследование делается при первом подозрении на гепатит. Второй вариант является наиболее значимым при лечении HCV РНК, поэтому рассмотрим его более подробно.
Вирусный гепатит C, или HCV, это инфекционная болезнь, поражающая печень. Заражение вирусом происходит через кровь. Заразиться можно, делая переливание крови, когда не соблюдаются правила по стерилизации медицинских инструментов. Реже встречаются случаи, когда заболевание получается половым путем или от беременной матери к плоду. Гепатит С бывает 2-х типов.

Важнейшая опасность гепатита С состоит в том, что он протекает скрытно, без желтушных признаков. При этом чаще всего жалуются на поднятие температуры, тошноту и рвоту, физическую слабость, повышенную утомляемость, потерю аппетита и веса. При этом на фоне небольшого уплотнения тканей печени достаточно часто происходит ее злокачественное перерождение. По этой причине вирусный гепатит С зачастую называют «бомбой замедленного действия» или «ласковым убийцей».
Другая особенность болезни заключается в очень медленном ее развитии, исчисляемом десятками лет.
Как правило, заразившиеся не ощущают никаких симптомов и не подозревают о своем истинном состоянии. Часто заболевание можно выявить только при обращении к врачу по другому вопросу.
- дети, получившие вирус гепатита С от матерей;
- наркоманы;
- люди, прокалывавшие части тела или сделавшие татуировки нестерильными инструментами;
- получившие донорскую кровь либо органы (до 1992 года, когда гемодиализ не проводился);
- лица, инфицированные ВИЧ;
- медицинские работники, контактирующие с инфицированными пациентами.
Основной метод проведения теста — ПЦР, или метод полимеразно-цепной реакции.
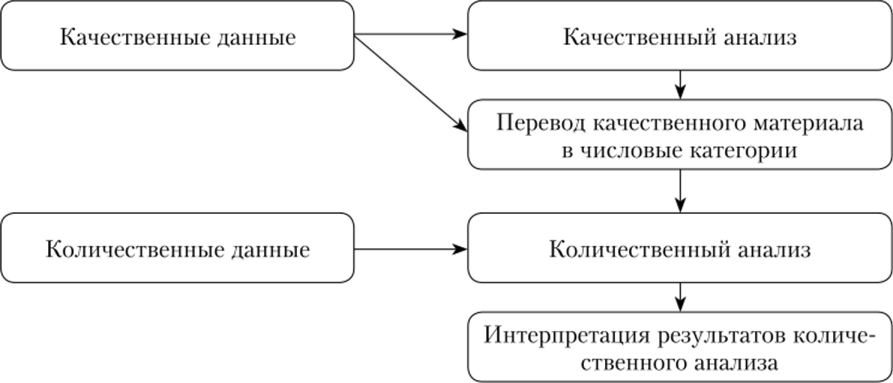
Существуют два вида тестов крови на определение РНК HCV:
Проведение качественного анализа дает возможность определить, находится ли вирус в составе крови. Все пациенты, у которых найдены антитела С-гепатита, должны пройти данный тест. По его результатам можно получить 2 ответа: «присутствует» либо «отсутствует» вирус. По положительному результату теста (обнаружено) можно судить об активном размножении вируса, который заражает здоровые клетки в печени.
Тест, проводимый на качественный ПЦР, настроен на конкретную чувствительность, от 10 до 500 МЕ/мл. Если обнаруженный в составе крови вирус гепатита при удельном содержании меньше 10 МЕ/мл, то обнаружение вируса может стать невозможным. Очень низкое значение удельного содержания вируса наблюдается среди пациентов, для которых назначена противовирусная терапия. Поэтому важным является тот факт, насколько высока чувствительность медицинской системы для диагностирования и постановки качественного результата при полимеразной цепной реакции.
Зачастую полимеразная цепная реакция C-гепатита проводится сразу же после нахождения соответствующих антител. Последующие тесты, при прохождении противовирусной терапии, проводятся на 4-ю, 12-ю и 24-ю недели. И еще один анализ после прекращения ПВТ делается через 24 недели. Затем — один раз в год.
Количественный анализ ПЦР РНК, иногда называемый вирусной нагрузкой, определяет концентрацию (удельное содержание) вируса в составе крови. Другими словами, под вирусной нагрузкой понимается определенное количество вирусной РНК, которое может находиться в конкретном количестве крови (принято использовать 1 мл, равный 1 см в кубе).
Единицы измерения для результатов теста — международные (стандартные) единицы, разделенные на один миллилитр (МЕ/мл). Содержание вируса иногда представляется по-разному, это зависит от лабораторий, где проводятся исследования. Для гепатита С количественное определение иногда использует такие значения, как копии/мл.
Необходимо понимать, что нет никакой конкретной зависимости в степени тяжести гепатита С от концентрации данного штамма в составе крови.
Проверка «вирусной нагруженности» позволяет определить степень инфекционности заболевания. Так риск заразить вирусом другого человека повышается при повышении концентрации гепатита в составе крови. К тому же высокое содержание вируса снижает эффект от проводимого лечения. Поэтому малая вирусная нагрузка является очень благоприятным фактором для успешного лечения.
К тому же тест гепатита С и его определение методом ПЦР играют большую роль при применении терапии от болезни и определения успешности лечения. На основании результатов теста осуществляется планирование курса реабилитации. Например, при слишком медлительном уменьшении удельной концентрации вируса гепатита, противовирусная терапия продлевается, и наоборот.
В современной медицине считается, что нагрузка больше 800000 ME/мл является высокой. Нагрузка же сверх 10000000 ME/мл считается критической. Но у специалистов из разных стран и по сей день не появилось одинакового мнения о пределах вирусной нагрузки.
В общих случаях количественный анализ на гепатит HCV-RNA делается перед проведением противовирусной терапии и через 3 месяца по окончании лечебных процедур для определения качества проведенной терапии.
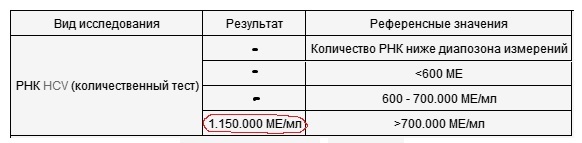
В качестве результата для количественного теста станет считаться количественная оценка результатов по образцу, указанному выше. В результате будет вынесен вердикт «ниже измеряемого диапазона» или «в крови не обнаружено» — это является нормой для здорового человека.
Параметр чувствительности качественного теста обычно ниже, чем чувствительность количественного анализа. Расшифровка «Отсутствующий» показывает, что оба вида анализов не нашли РНК вируса. При показателе теста «ниже измеренного диапазона» анализ количественного типа, скорее всего, не нашел РНК гепатита, хотя это подтверждает наличие вируса с очень маленьким удельным содержанием.
Генотипирование РНК вируса гепатита C диагностирует присутствие разных генетических типов гепатита С. Науке известно более 10 типов генома вируса, но для медицинской практики достаточно выделить несколько генотипов, имеющих наибольший удельный вес в регионе. Определение генетического типа играет ключевую роль при выборе сроков лечения, что очень необходимо, если принять во внимание обширный спектр побочных эффектов лекарств от гепатита.
Единственным действенным способом вылечить вирус гепатита С, как правило, оказывается сочетание 2-х медпрепаратов:
По отдельности эти лекарства не так эффективны. Рекомендуемые дозировки лекарств и сроки применения должны назначаться только врачом и индивидуально каждому пациенту. Лечение этими лекарствами может растянуться на срок от 6 до 12 месяцев по первой схеме и от 3 до 6 месяцев по второй и третьей схеме.
Сегодня не изобретено препаратов, гарантирующих стопроцентное выздоровление от вируса. Однако при верно подобранном лечении исцеление пациентов может достигать до 98% от числа заболевших.
источник
Вирус гепатита С – возбудитель инфекционного заболевания, сопровождающегося постоянным прогрессированием некротических изменений тканей печени, вплоть до злокачественного перерождения и формирования метастатических опухолей.
РНК вируса обнаруживается в крови лабораторными методиками уже спустя 7–14 дней после инфицирования. Но выделение патогена в отдельной культуре и его искусственная репликация до недавнего времени представляли серьезную проблему.
И только в середине 2000-х годов удалось выделить главные структурные протеины и неструктурные белки вируса, механизмы его репликации в гепатоцитах.
Основные случаи инфицирования вирусом HCV связаны с непосредственным попаданием патогена в кровь при гемотрансфузии, с засохших частиц контаминированного материала на медицинских, диагностических и косметологических инструментах.
Гораздо реже возбудитель HCV передается при половом акте. Вероятность внутриутробного инфицирования не превышает 3–5%. При этом окончательно не установлено, происходит передача вируса через плаценту либо во время родов.
Впервые о гепатите «ни А ни В» заговорили в 1970-х годах. Но клонировать патоген удалось только в начале 1990-х годов. История болезни связана с разнообразными теориями, впоследствии не получившими подтверждения.
Изначально большинство специалистов склонялось к мнению, что заболевание является асимптоматическим расстройством функциональной активности печени. При этом утверждалось, в отличие от других известных на тот момент инфекционных болезней органа, гепатит С не способен вызвать значимых осложнений (за исключением неспецифического увеличения концентрации аминотрансфераз).
Но последующее наблюдение за пациентами с HCV продемонстрировало, что у каждого пятого без лечения спустя 10–11 лет развивался цирроз.
С появлением лабораторных методик, позволяющих подробно изучить, как выглядит вирус под микроскопом, выделить из сыворотки крови специфические антитела стали возможными долговременные клинические исследования. Провели культивирование и анализ образцов биологического материала, ранее полученных от пациентов, инфицированных HCV (до 5–10 –15 и более лет назад). Таким образом появились убедительные данные относительно эволюции HCV-инфекции.
Одним из главных выводов стало подтверждение возможности самостоятельной эрадикации вируса на острой стадии течения заболевания. Причем чаще это происходит у больных младше 12 лет.
Риск развития цирроза установили на уровне 15%, и подобные нарушения печени формировались спустя 20–25 лет. Позже, по мере накопления клинического и практического опыта, данные были скорректированы.
Сформировалось четкое представление о прогрессировании вирусной инфекции. Установлена взаимосвязь между HCV и разнообразными внепеченочными проявлениями. Изучение иммунологического ответа на антигены вируса позволило предположить вероятность формирования аутоиммунных нарушений, которые затрагивают щитовидную железу, сосудистую систему, опорно-двигательный аппарат.
Причем если доктора могут с уверенностью сказать, как HCV повлияет на работу печени через 5–20 и более лет после заражения, то прогнозировать внепеченочные проявления инфекции невозможно.
Только недавно частицы вируса были обнаружены в различных структурах нервной системы, в частности, головном мозге. Это позволило предположить прямую связь первых симптомов инфекции (усталости, слабости, психоэмоциональных расстройств и т.д.) с особенностями патогенеза заболевания.
Постоянно появляются новые тест-системы. Причем каждое последующее поколение диагностических наборов отличается большей специфичностью, точностью и чувствительностью.
Общее количество инфицированных колеблется в пределах 3–5% населения земного шара. Но медицинская статистика учитывает только официальные данные, на практике эта цифра гораздо выше. Патология преимущественно распространена в странах, расположенных на севере Африканского континента, в Европе – на юге Италии.
Недавно появились данные относительно увеличения количества заболевших в Китае, Пакистане и некоторых других азиатских странах. Минимальное число пациентов (менее 0,1%) зарегистрировано в Великобритании и странах Скандинавии.
Эпидемиология гепатита С на территории России изучена недостаточно. Полагают, что количество заболевших составляет 2,0–2,9%.
Передача инфекционного гепатита С возможна при:
- переливании крови и ее продуктов;
- трансплантации органов, изъятых у инфицированных доноров;
- инъекциях и другие инвазивных процедурах, выполняемых контаминированным инструментарием.
С появлением высокочувствительных тест-систем вероятность инфицирования при гемотрансфузии практически сведена к нулю. А большая часть случаев заболевания связана с заражением при использовании общих игл (например, в США эта цифра достигает 60% от общего количество заболевших).
По сравнению с парентеральным путем передачи, вероятность заразиться при половом контакте либо внутриутробно низка. Так, при случайном, единоразовом повреждении кожи контаминированным инструментом риск заражения оценивают в 7–10%, перинатально – не более 5–6%.
Данные относительно полового пути передачи HCV противоречивы. Известны случаи длительных постоянных отношений, когда один из партнеров инфицирован, при этом другой оставался совершенно здоровым. Точный источник заражения вирусом установить чаще всего затруднительно.
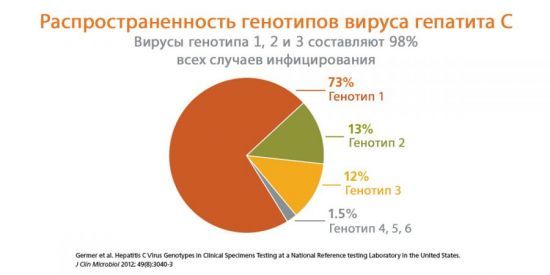
К настоящему моменту идентифицировано 6 основных генотипов инфекционного гепатита С, которые отличаются специфической географической привязанностью. Определение конкретной разновидности заболевание имеет огромное значение в подборе схемы терапии патологии. Установлено, что если выявлен 1 генотип, вероятность положительного эффекта лечения ниже.
HCV относится к семейству Flaviviridae. Как и другие представители этого класса, представляет собой заключенный в оболочку нуклеокапсид, который проникает в клетки печени из кровотока. После попадания в гепатоциты внешняя мембрана патогена разрушается, и высвобождаются частицы вируса, размер которых не превышает 70 нм.
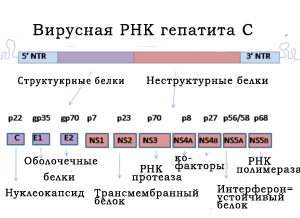
РНК вируса гепатита С – это значит геном патогена, состоит из одной цепи и включает короткие некодируемые участки, каждый из которых заканчивается кодируемой последовательностью полипротеинов. На 341 «звене» находится 5 нетранслируемый участок, который формирует сложную вторичную структуру, необходимую для репликации вируса.
N-участок полипротеинов кодирует структурные белки, включая основной элемент нуклеокапсида core и гликопротеины оболочки Е1 и Е2, которые в сочетании с неструктурными протеинами NS2–NS5B формируют вирусные частицы (NS3, NS4A, NS4B, NS5A и NS5B также играют огромную роль в репликации HCV).
С-конечный участок core и протеины оболочки при помощи специфических пептидаз обеспечивают проникновение вируса в клетку печени и последующее взаимодействие с эндоплазматическим ретикулумом и другими органеллами гепатоцита.
Core и фактически каждый из неструктурных протеинов являются антигенами, провоцирующими выработку антител (АТ). Установление их титра лежит в основе иммуноферментного анализа – одного из основных диагностических тестов для подтверждения болезни. При позитивном результате обследование пациентов продолжают при помощи полимеразной цепной реакции, основная цель которой – определение РНК HCV.
Если РНК не обнаружена, лечение не назначают, даже при позитивном ИФА. Но наличие РНК, подтвержденное результатами ПЦР, свидетельствует об инфицировании. При минимальной виремии (без роста показателей) человек долгое время может оставаться носителем болезни. Но в любой момент распространение процесса может ускориться.
После постановки диагноза у пациента возникает вопросы:
- HCV является вирусом или бактерией?
Возбудитель заболевания – РНК-содержащий вирус, поэтому прием антибиотиков не только нецелесообразен, но и опасен из-за гепатотоксичности подавляющего большинства антибактериальных средств. - Когда лучше делать анализ на HCV?
Антитела к патогену выделяются сразу же после проникновения вируса в организм. Но в количестве, достаточном для определения лабораторным путем, иммуноглобулины накапливаются в среднем через 2 месяца. Что касается ПЦР, сроки выявления зависят от аналитической чувствительности РНК. При использовании современных тестов анализ можно делать уже через 10–14 суток.
Изучение под микроскопом и при помощи других технологий строение вируса позволило создать высокоэффективные препараты, необратимо останавливающие процессы деления РНК.
Распространенность HCV и существующий риск заражения при различных манипуляциях, включая эстетические процедуры, обуславливает устойчивость вируса гепатита С во внешней среде. Перечень биологических жидкостей, где содержится возбудитель в концентрациях, достаточных для заражения, ограничен.
В первую очередь, это кровь (как в «свежем», так и в засохшем состоянии). В сперме, выделениях из влагалища, менструальной крови HCV присутствует в минимальной концентрации. Как правило, ее недостаточно для заражения человека с полноценно работающей иммунной системой. Но при снижении резистентности организма, вероятность инфицирования многократно возрастает.
В слюне вирус практически не обнаруживается. Это связывают с находящимися в ротовой полости ферментами, которые разрушают белки, составляющие структуру HCV. Поэтому вероятность передачи патогена при поцелуях минимальна.
Жизненный цикл вируса таков, что он сохраняет активность и контагиозность продолжительное время в засохшей крови. При благоприятных температурных условиях (от 6 до 20 градусов выше нуля) этот срок длится до 4–6 недель. При повышении температуры данный период сокращается до 5–6 суток. При заморозке (в том числе донорского материала) HCV остается жизнеспособным на протяжении неопределенного времени и является заразным и после размораживания.
Основной «мишенью» для HCV являются клетки печени. Однако при хроническом течении инфекции (по данным клинических экспериментов, проведенных с участием шимпанзе) частицы вируса обнаруживаются в лимфоидной ткани и дендритных клетках.
Но применительно к течению патологии у человека эта информация требует подтверждения. Достоверно известно, что HCV отличается тропностью именно к тканям печени.
Выявить возбудителя гепатита С в крови можно при помощи ряда диагностических тестов:
- иммуноглобулины к HCV определяют иммуноферментным анализом;
- установить наличие РНК можно методом качественной или количественной ПЦР.
Косвенно на вирусное поражение печени могут указывать результаты печеночных проб и биохимического анализа крови. Если антитела или РНК патогена в крови не обнаружены, но риск заражения слишком велик (например, после случайного пореза, незащищенного полового акта и т.д.) исследования повторяют через 2–3 месяца.
Разница в структуре между разновидностями патогена составляет порядка 30–35%. Внутри одного генотипа выделяют субтипы, различия между ними не превышают 25%. У каждого пациента Hepatitis C Virus может мутировать с формированием так называемых квази-типов.
Генотипирование вируса гепатита С – один из основных анализов, назначается только один раз и обязательно проводится перед началом курса противовирусной терапии.
Для определения разновидности патогена РНК HCV должна содержаться в крови в достаточно высокой концентрации. Поэтому, если не определяется генотип патогена, исследование повторяют через 1–2 недели.
Тип возбудителя гепатита С в целом влияет как на медикаменты, составляющие схему лечения, так и на прогноз. При 3 генотипе обязательны инструментальные исследования печени из-за высокого риска осложнений. Первый тип крайне сложно поддается терапии.
Эффективность противовирусной терапии напрямую зависит от стадии болезни, когда был поставлен диагноз. Софосбувир, Даклатасвир, Велпатасвир и другие медикаменты прямого действия позволяют вывести вирус из организма практически у всех пациентов вне зависимости от генотипа.
Поэтому при подозрении на заражение следует сдать кровь на ИФА или ПЦР. Для постановки диагноза на ранней стадии эти исследования повторяют ежегодно.
Специфической профилактики (вакцины) от гепатита С не существует.
Для обработки медицинских инструментов и рабочей поверхности используют химические растворы и соединения, способные убить вирус, т. е. содержащие хлористоводородную, фосфорную кислоту, пропанол, этанол.
Когда пациенты интересуются, убивает ли спирт вирус, доктора дают положительный ответ. Но объясняя, погибает ли от спирта возбудитель гепатита С, врач подчеркивает, что концентрация этанола должна быть не менее 70%.
Также патоген уничтожается при термической обработке. При какой температуре убивается возбудитель HCV? При 60°для этого требуется 20–30 минут, при температуре кипячения – до 5 минут, при дезинфекции в автоклаве – около 1,5–2 минут. Подобные режимы обработки подходят для стерилизации медицинского и косметического инструментария, стирки белья, загрязненного контаминированным материалом.
источник



Вирус гепатита С (HCV или иногда HVC) – это маленький (размером 55–65 нм) позитивный однонитевой РНК-вирус в оболочке из семейства Flaviviridae. Вирус гепатита C – это причина гепатита C у людей.
Вирус гепатита C принадлежит к роду гепацивируса, члена семейства Flaviviridae. До недавних пор он считался единственным членом этого рода. Однако у собак был открыт другой член этого рода – canine hepacivirus. Также есть, по крайней мере, один вирус в этом роде, который инфицирует лошадей.
Частица вируса гепатита C состоит из ядра генетического материала (РНК), окруженного икосаэдрической защитной оболочкой из белка и далее погруженного в жировую оболочку клеточного происхождения. Два гликопротеина вирусной оболочки, Е1 и Е2, встроены в жировую оболочку.
Вирус гепатита C имеет геном позитивной однонитевой РНК. Геном состоит из единой открытой рамки считывания длиной 9600 нуклеотидных основ. Эта единая открытая рамка считывания транслируется для образования единого белкового продукта, который далее обрабатывается для образования меньших активных белков.
На 5′ и 3′ концах РНК находятся участки UTR, которые не транслируются в белки, но важны для трансляции и репликации вирусной РНК. Участок 5′ UTR имеет место связывания рибосомы (IRES – участок внутренней посадки рибосомы), который начинает трансляцию очень длинного белка, содержащего около 3000 аминокислот. Домен ядра IRES вируса гепатита C (HCV) содержит четырехстороннее спиральное соединение, объединенное в прогнозированном псевдоузле. Конформация этого домена ядра сдерживает направление открытой рамки считывания для позиционирования на рибосомальной субъединице 40S. Большой первичный белок затем разрезается клеточными и вирусными протеазами на 10 меньших белков, которые позволяют репликацию вируса в клетке носителя или собираются в зрелые вирусные частицы.
Структурные белки, образованные вирусом гепатита С, включают капсидный белок, E1 и E2; неструктурные белки включают NS2, NS3,NS4, NS4A, NS4B, NS5, NS5A и NS5B.
Белки этого вируса упорядочены вдоль генома в следующем порядке: N конец-ядро-оболочка (E1)-E2-p7-неструктурный белок 2 (NS2)-NS3-NS4A-NS4B-NS5A-NS5B-C-конец. Поколение зрелых неструктурных белков (от NS2 до NS5B) полагается на активность вирусной протеиназы. Соединение NS2/NS3 расщепляется металл-зависимой автокаталитической протеиназой, закодированной в NS2 и в N-конце NS3. Оставшееся расщепление ниже от этого участка катализируется сериновой протеиназой, также содержащейся в N-концевом участке NS3.
Капсидный белок имеет 191 аминокислоту и может быть разделен на три домена на основе гидрофобности: домен 1 (остатки 1-117) содержит главным образом основные остатки с двумя короткими гидрофобными участками; домен 2 (остатки 118-174) менее основной и более гидрофобный, и его С-конец находится в конце p21; домен 3 (остатки 175-191) высоко гидрофобный и действует, как сигнальная последовательность для белка оболочки Е1.
Оба белка оболочки (E1 и E2) высоко гликозилированны и важны в проникновении клетки. E1 служит в качестве сливающей субъединицы, а Е2 служит, как белок связывания рецепторов. Е1 имеет 4-5 N-связанных гликанов и E2 имеет 11 участков N-гликозилации.
Белок p7 необязателен для репликации вирусного генома, но играет важную роль в вирусном морфогенезе. Этот белок – это трансмембранный белок из 63 аминокислот, который располагается в эндоплазматической сети. Расщепление p7 опосредовано сигнальными пептидазами эндоплазматической сети. Два трансмембранных домена р7 соединены цитоплазматической петлей и направлены к просвету эндоплазматической сети.
Белок NS2 – это трансмембранный белок 21-23 килодальтон (кДа) с активностью протеаз.
NS3 – это белок 67 кДа, чей N-конец имеет активность сериновой протеазы и С-конец имеет активность NTP-азы/геликазы. Он расположен в эндоплазматической сети и формирует гетеродимерный комплекс NS4A – мембранный белок из 54 аминокислот, который выступает, как кофактор протеиназы.
NS4B — это маленький (27 кДа) гидрофобный цельный мембранный белок с 4 трансмембранными доменами. Он расположен в пределах эндоплазматической сети и играет важную роль для рекрутинга других вирусных белков. Он стимулирует морфологические изменения в эндоплазматической сети, образуя структуру под названием «мембранная сеть».
NS5A – это гидрофобный фосфопротеин, играющий важную роль в вирусной репликации, модуляции сигнальных путей клеток и реакции интерферона. Он связывается с васкулоадгезивными белками человека, закрепленными на эндоплазматической сети.
Белок NS5B (65 кДа) – вирусная РНК-зависимая РНК-полимераза. NS5B имеет ключевую функцию репликации вирусной РНК вируса гепатита С, используя положительно полярную нить РНК вируса в качестве матрицы, и катализирует полимеризацию рибонуклеозид—трифосфатов (rNTP) во время репликации РНК. Несколько структур кристаллов полимеразы NS5B в нескольких кристаллических формах были определены на основе той же консенсусной последовательности BK (HCV-BK, генотип 1). Структура может быть представлена в форме правой руки с пальцами, ладонью и большим пальцем. Охваченный по окружности активный участок, уникальный для NS5B, содержится в структуре ладони белка. Недавние исследования структуры нити J4 (HC-J4) генотипа 1b белка NS5B указали на присутствие активного участка, где возникает возможный контроль связывания нуклеотидов и инициация синтеза РНК заново. Процесс заново добавляет необходимые праймеры для инициации репликации РНК. Текущее исследование пытается связать структуры с этим активным участком для изменения его функциональности, чтобы предотвратить дальнейшую репликацию вирусной РНК.
Также был описан 11-й участок. Этот белок кодируется +1 сдвигом рамки считывания в капсидном гене. Он кажется антигенным, но его функция не известна.

Попав внутрь печеночной клетки, вирус гепатита C овладевает частями внутриклеточной механики для репликации. Геном вируса гепатита C транслируется для образования одного белка из приблизительно 3011 аминокислот. Затем полипротеин проходит протеолитическую обработку вирусными и клеточными протеазами для образования трех структурных (вирион-ассоциированных) и семи неструктурных (NS) белков. Альтернативно сдвиг рамки может возникнуть в области ядра для образования белка альтернативной рамки считывания (ARFP). Вирус гепатита C кодирует две протеазы, аутопротеазу цистеина NS2 и сериновую протеазу NS3-4A. NS белки затем вербуют вирусный геном в комплекс репликации РНК, который связан с перегруппированными цитоплазматическими мембранами. Репликация РНК происходит через РНК-зависимую РНК-полимеразу NS5B, которая производит промежуточную форму отрицательно полярной нити РНК. Отрицательно полярная нить РНК затем выступает в качестве матрицы для новых вирусных геномов с положительной полярностью. Появляющиеся геномы затем могут быть транслированы, далее воспроизведены или упакованы в новых вирусных частицах. Новые вирусные частицы, как считается, пускают ростки в выделительные пути и выпускаются на поверхности клетки.
Вирус воспроизводится на внутриклеточных липидных мембранах. В частности, эндоплазматическая сеть деформируется в мембранные структуры уникальных форм под названием «мембранные сети». Эти структуры могут быть вызваны единой экспрессией вирусного белка NS4B. Белок ядра соединяется с липидными капельками и использует микротрубочки и динеины для изменения их местоположения в перинуклеарном распределении.
Выпуск из печеночной клетки может вовлекать выделительные пути липопротеинов очень низкой плотности.
Вернуться к содержанию
На основе генетических различий между изолятами вируса гепатита C его виды классифицируются на семь генотипов (1-7) с несколькими подвидами в каждом генотипе (в названиях представлены строчными буквами). Подвиды далее подразделяются на квазивиды на основе их генетического разнообразия. Генотипы различаются на 30-35% нуклеотидных участков по всему геному. Разница в геномном составе подвидов генотипа составляет обычно около 20-25%. Подвиды 1a и 1b обнаружены по всему миру и вызывают 60% всех случаев.
Генотип имеет клиническую важность в определении потенциальной реакции на терапию на основе интерферона и требуемой длительности такого лечения. Генотипы 1 и 4 менее восприимчивы к лечению на основе интерферона, чем другие генотипы (2, 3, 5 и 6). Длительность стандартной терапии на основе интерферона для генотипов 1 и 4 составляет 48 недель, в то время как лечение для генотипов 2 и 3 длится 24 недели. Устойчивые вирусологические реакции возникают в 70% случаев генотипа 1, около 90% случаев генотипов 2 и 3, 65% — генотипа 4 и 80% — генотипа 6.
Инфицирование одним генотипом не дает иммунитета против других, и возможно сопутствующее инфицирование двумя штаммами. В большинстве этих случаев один из штаммов удаляет другой из хозяина в короткий период времени. Эта находка открывает дверь для замещения штаммов, не реагирующих на медикаменты, другими штаммами, которые легче поддаются лечению.
Определение происхождения этого вируса было трудным, но генотипы 1 и 4 кажутся имеющими общее происхождение. Байсовский анализ предполагает, что главные генотипы разошлись около 300-400 лет назад от вируса-предка. Второстепенные генотипы разошлись около 200 лет назад от главных генотипов. Считается, что все сохранившиеся до наших дней генотипы возникли от подтипа 1b генотипа 1.
Исследование штаммов генотипа 6 предполагает более раннюю дату эволюции: около 1100-1350 лет назад (95% вероятная область, от 600 до >2500 лет назад). Оцененная скорость мутации была 1,8 × 10−4 (95% вероятная область: 0,9 × 10−4 to 2.9 × 10−4). Этот генотип может быть предком других генотипов.
Исследование изолятов из Европы, США и Японии предполагает, что датой происхождения генотипа 1b является приблизительно 1925 г. Оцененные даты происхождения типов 2a и 3a – 1917 и 1943 гг., соответственно. Время расхождения типов 1a и 1b было оценено приблизительно в 200-300 лет назад.
Исследование генотипа 1a и 1b оценило следующие даты происхождения: 1914-1930 (95% вероятный интервал: 1802-1957 гг.), для типа 1a – 1911-1944 гг. (95% вероятный интервал: 1806-1965 гг.), для типа 1b. Оба вида 1a и 1b перенесли массовую экспансию в размере эффективной популяции между 1940 и 1960 гг. Экспансия подвида 1b вируса гепатита C предшествовала экспансии подвида 1а минимум на 16 лет (95% вероятный интервал: 15–17 лет). Оба вида, как кажется, распространились из развитых стран в развивающиеся страны.
Штаммы генотипа 2 из Африки можно разделить на четыре клада, которые связаны со страной своего происхождения:
- Камерун и Центральная Африканская Республика;
- Бенин, Гана и Буркина-Фасо;
- Гамбия, Гвинея, Гвинея-Биссау и Сенегал;
- Мадагаскар.
- Считается, что генотип 3 происходит из Юго-Восточной Азии.

В отличие от гепатита A и B в настоящий момент не существует вакцины для предотвращения инфекции гепатита C.
Исследованию вируса гепатита C помешал узкий диапазон хозяев вируса гепатита С. Использование репликонов было успешным, но они были открыты только недавно. Вирус гепатита C, как и большинство РНК-вирусов, существует в качестве вирусных квазивидов, что делает очень трудным выделение одной нити или типа рецептора для исследования. В настоящий момент исследование сфокусировано на ингибиторах вирусной протеазы с низким молекулярным весом, полимеразы РНК и других неструктурных генов. Два вещества, ингибиторы протеазы NS3, – боцепревир компании «Merck» и телапревир от «Vertex Pharmaceuticals Inc» — были одобрены для применения 13 мая 2011 г. и 23 мая 2011 г., соответственно.
Сообщалось о возможной связи между низкими уровнями витамина D и плохой реакцией на лечение. В работе в лабораторных условиях было показано, что витамин D может быть способен уменьшить репликацию вируса. Хотя эта работа выглядит многообещающей, все еще не получены результаты клинических исследований.
Другие исследуемые вещества включают аналог-игибиторы нуклеозида/нуклеотида и ненуклеозидные ингибиторы РНК-зависимой РНК-полимеразы, ингибиторы неструктурного белка 5А и нацеленные на хозяина соединения, такие как ингибиторы циклофилина и силибинин.
Как множество вирусов, вирус гепатита C постепенно инактивируется снаружи тела носителя. Присутствие тепла может оказать сильное влияние на продолжительность жизни вируса за пределами тела. Вирус может оставаться заразным снаружи носителя в течение приблизительно 16 дней при 25°C и двух дней при 37°C, хотя он может оставаться активным в течение более 6 недель при температуре менее или равной 4°C. При нагреве до температур 60°C и 65°C, однако, вирус гепатита C может быть инактивирован за 8 и 4 минуты, соответственно.
источник
Когда необходимо определить наличие вируса гепатита С в организме, следует провести анализ РНК, расшифровка которого и даст нужную информацию.
С помощью этого анализа можно выяснить, есть ли у пациента следы заболевания, а также определить, как далеко оно зашло, о каком именно типе патологии идет речь. После выяснения этой информации можно назначать терапию наиболее подходящего вида.
РНК вируса гепатита С представляет собой генетическую структуру заболевания, которое поражает, в первую очередь, печень.
Процесс заражения происходит, как правило, через кровь, поэтому наиболее часто заражение этим заболеванием происходит во время операций, проведенных плохо стерилизованными инструментами, или при переливаниях, если не были проведены все необходимые анализы.
Выясняя, что такое РНК гепатита и как можно заразиться этим заболеванием, нужно также отметить, что опасны все биологические жидкости. Поэтому при плотном контакте с больным нужно соблюдать большую осторожность.
Случаются и ситуации, когда анализ выявляет следы такой патологии у новорождённых детей, если их матери страдали этим заболеванием.
Для печени опасность вируса зависит от того, какой формой патологии страдает пациент.
- Острая форма. Характеризуется болями в печени, резкими изменениями цвета кожи на желтоватый, рвотой, повышением температуры, часто приступ начинается после употребления алкогольных напитков или вредной пищи, особенно жирной и острой.
- Хроническая форма. На начальном этапе эта форма заболевания никак не проявляется и потому считается гораздо более опасной, чем острая. Именно пациенты, страдающие от хронического гепатита С, чаще всего сталкиваются с раком или циррозом печени.
При этом около 70% людей, столкнувшихся с острой формой болезни, рано или поздно приобретают и хроническую. Это зачастую характеризуется злокачественными изменениями структуры печени.
Основным анализом, определяющим содержание в крови РНК гепатита С, является HCV. Для него берётся кровь из вены, и такой метод называется также ПЦР. Определение методом ПЦР обнаруживает нуклеиновые элементы в крови, принадлежащие С-вирусу.
Существует два вида исследований РНК заболевания:
- Качественное исследование. Позволяет определить, заражен ли пациент вообще инфекцией. Определение РНК этого заболевания почти всегда возможно, если болезнь зашла достаточно далеко. Ошибки могут возникнуть только на самом начальном этапе развития патологии, когда содержание её частиц в крови ещё слишком мало, чтобы быть обнаруженным и определенным.
- Количественное HCV-исследование. Это второй этап анализа, когда качественное исследование уже показало, что у пациента возникли проблемы. Количественный анализ позволяет определить, как сильно развилась болезнь.
Кроме того, после количественного проводится генотипическое исследование, с помощью которого можно также выяснить, каким именно видом болезни страдает пациент. В России активно распространены всего три, и схемы лечения различаются.
Когда анализируется РНК, результаты HCV, необходимые для правильного лечения, включают в себя три основных пункта:
- Положительный или отрицательный результат дал качественный анализ на гепатит РНК. В этом случае, что значит получение положительного результата: в первую очередь, вероятность заражения для окружающих. При этом положительный HCV может указывать также на недавно перенесённый острый приступ заболевания, при котором в организме ещё остались следы. Однако, если результаты показывают, что не обнаружено следов этой патологии, это почти всегда значит, что пациент здоров. Иногда на начальном этапе болезнь может быть не выявлена. Это происходит из-за того, что тест может демонстрировать результат «РНК гепатита не обнаружено», если его содержание в крови крайне мало.
- Количество рибонуклеиновых кислот, когда тест все же дал положительный результат. Он позволяет определить то, насколько сильно успело развиться заболевание.
- Конкретный вид заболевания. Если расшифровываются тесты на гепатит, определение его вида — одно из важнейших условий для правильного лечения. Даже существующие в России типы этой болезни требуют разницы в подходе, и терапия в каждом отдельном случае будет выглядеть по-разному. Особенно сложной ситуация станет, если пациент болен каким-либо экзотическим видом. В результатах это часто отмечается прочерком в графе определения типа и требует дополнительного осмотра.
Для получения точных результатов, соответствующих ситуации, необходимо перед началом осмотра и передачи материалов на исследование соблюдать некоторые правила:
- за трое суток до сдачи отказаться от вредной пищи, алкоголя, приёма лекарств,
- отказаться от ультразвука, рентгена и прохождения других видов осмотра за две недели до сдачи,
- сдавать кровь натощак, желательно утром.
Только в этом случае полученные результаты будут достаточно точными для того, чтобы поставить по ним правильный диагноз.
Определение РНК гепатита С с помощью качественного теста требуется в каждом случае, когда в организме пациента есть антитела к этому заболеванию.
При этом результат может быть представлен только в крайне простой форме: «вирус гепатита С обнаружен» или «не обнаружен». Если результат положителен, то это означает, что болезнь активно развивается или, как минимум, находится в хронической стадии.
Выявление вируса происходит при помощи теста, который настроен на определённый уровень восприятия частиц. Он способен уловить только РНК болезни в диапазоне от 10 МЕ/мл до 500. Если его содержание в крови ниже этого уровня, то тест покажет отрицательный результат.
Кроме того, вероятность искажения результатов как в случае качественного, так и в случае количественного тестов увеличивают следующие факторы:
- плохо взятая для теста кровь (например, в недостаточно очищенной пробирке или с неправильной техникой забора крови),
- использование средств, содержащих гепарин и другие вещества, способствующих свертываемости крови (они уменьшают эффективность теста),
- неправильная перевозка материалов до лаборатории.
Важно соблюдать и обычные правила сдачи крови для анализа, перечисленные выше.
Когда анализируется гепатит С и его РНК, и получен положительный ответ на результаты качественного теста, следующим будет проведен количественный ВГС. Его расшифровка указывает на то, какова концентрация заболевания в организме.
Норма при количественном исследовании выглядит следующим образом:
Количество вируса в организме пациента, МЕ/мл Расшифровка результата Вирус не обнаружен Обычное состояние человека, не больного гепатитом, или того, у которого содержание вируса в крови минимально и не может быть определено качественным тестом
| Уровень не превышает 1.8*102 | Низкий уровень заражения (количество содержания гепатита проходит по минимальной границе) | Уровень не превышает 8*105 | Уровень заражения все ещё достаточно низок, и допустимо быстрое и эффективное излечение пациента |
| Уровень превышает 8*105 | Уровень заражения высок | Уровень превышает 2,4*107 | Уровень заражения существенно превышает норму, допускающую лёгкое излечение |
Резкие изменения уровня вируса в крови могут указывать на обострение и стремительное развитие заболевания.
После количественного теста проводится генотипический, определяющий, каким именно вирусом болен пациент.
Тест обладает высокой чувствительностью к РНК вируса гепатита С. Он может выявить даже самый минимальный уровень содержания болезни в крови. При этом количественный анализ способен точно описать, сколько генетической информации об этой проблеме содержится в организме.
Тест проводится несколько раз в течение болезни:
- Перед началом терапии для правильного определения состояния организма в целом и молекулярной структуры отдельного вида заболевания. Это позволяет назначить правильное лечение.
- В ходе терапии, на 4 неделе, а потом и на 24. Изменение уровня болезни в нужном участке молекулы ДНК является сигналом того, насколько правильно построено лечение.
- После терапии, когда подводится итог, и лечащему специалисту необходимо убедиться, что все гены пациента больше не содержат следов патологии.
Иногда приходится также повторять тест через три месяца, полгода и год. Избегать этих проверок не следует — это значит подвергать опасности окружающих.
Репликация вируса гепатита C.
источник

Сегодня в разработке препаратов для лечения вирусного гепатита С достигнуты приемлемые результаты. Современные лекарственные средства позволяют получить устойчивый вирусологический ответ (УВО) в 98% случаев даже при вирусе 1 и 4 типов.

Для гепатита С это могут быть клетки печени (гепатоциты), а также клетки иммунной системы (лимфоциты), причем не любого живого существа, а только человека. Гепатиты — это исключительно антропонозные вирусы.
Что же такое РНК вируса гепатита С? Макромолекула рибонуклеиновой кислоты (РНК) находится внутри вириона (вирусной частицы). Она представляет собой нить сцепленных друг с другом нуклеотидов, последовательность которых кодирует генетическую информацию вируса.
Такое огромное количество нуклеотидов кодирует всего 10 вирусных белков — 3 структурных протеина и 7 не структурных.
Макромолекула РНК компактно свернута и «запакована» в предохраняющую ее капсулу (оболочку). Вторгаясь в гепатоцит или лимфоцит, вирион «распаковывается»: РНК вируса гепатита С освобождается от оболочки и встраивается в процесс биосинтеза клетки для воспроизводства тех самых 10 белков, закодированных в ее геноме. Для лучшего понимания рассмотрим, что такое фаза репликации гепатита С.

По этой причине в большинстве случаев заболевание протекает бессимптомно и даже такие общие признаки, как интоксикация, повышение температуры, не свойственны течению этого заболевания. Заболевший чувствует себя хорошо, к врачу не обращается. Тем не менее количество вирусных частиц в организме растет, увеличивается вирусная нагрузка. Все большее количество гепатоцитов переключается со своих естественных функций на копирование чужеродных белков.
Фаза репликации при гепатите С может длиться сколько угодно долго. Несмотря на то, что иммунная система распознает вторжение вируса сразу после попадания его в кровь, лишь в редких случаях, которые могут быть отнесены к исключительным, ей удается подавить инфекционный процесс. В большинстве же случаев вялотекущая репликативная фаза продолжается, переводя заболевание в хроническую форму.
Почему же, несмотря на все усилия, иммунная система не в состоянии справиться с вирусом?
До 30% генома подвергается мутации. Это означает, что выходящая из гепатоцита «свежая» вирусная частица имеет поверхностный антиген, отличный от того, который был у изначальной частицы. Этот факт имеет следующие последствия:
- Для иммунной системы, которая узнает вирусы по белкам их оболочки (поверхностным антигенам), вышедший вирион будет уже не тем вирусом, антитела к которым она выработала.
- Так как новых антител (которые узнают антигены) еще не выработано, то новые вирионы ускользают от иммунной системы.
- Для того чтобы иммунитет «познакомился» и начал вырабатывать антитела к новым вариантам вируса («квазивидам»), должно пройти определенное время, за которое вирус, опять же, успевает мутировать.
- Считается, что в течение 1 недели вирус успевает полностью изменить свою антигенную структуру.
В большинстве случаев иммунная система никогда не успевает за появлением новых квазивидов вируса, что и является причиной хронического вирусного гепатита С.
Гепатит С передается через кожный покров, целостность которого нарушена. Это может происходить:
- при инъекциях и других медицинских манипуляциях;
- при нанесении татуировок, при маникюре и других манипуляциях немедицинского характера;
- при незащищенном половом акте (крайне редко);
- от матери — к ребенку при родах.
Тем же способом, при тех же ситуациях передается и хронический вирусный гепатит С.
По степени заразности гепатит С значительно уступает гепатиту В. То есть при прочих равных условиях заразиться первым видом © сложнее, чем вторым (В).
Вирусные частицы, находящиеся в окружающей среде, проявляют достаточно высокую степень устойчивости. Вирус сохраняет свои патогенные свойства:
- при комнатной температуре — до нескольких месяцев;
- при отрицательных температурах — в течение лет.
Вирус сохраняется, в том числе в высохших пятнах крови, на бритвенных лезвиях, на иглах от шприцов, от тату-машинок и прочих инструментах и предметах, проконтактировавших с кровью человека.
Возникает закономерный вопрос: можно ли убить вирус гепатита С? Безусловно, можно. Оболочка вириона не абсолютно устойчива и разрушается под действием химических веществ и экстремальных условий окружающей среды.
Таблица. Чего боится вирус гепатита С
| Что убивает вирус гепатита С | Время воздействия |
|---|---|
| Антисептические препараты (спирт, хлоргексидин, мирамистин, перекись водорода) | мгновенно |
| Кипячение | 5 минут |
| Воздействие ультрафиолетом (вирус должен быть доступен для ультрафиолетовых лучей) | 1 час |
Таким образом, термическая стерилизация инструментов и обработка их антисептиками способна убить вирус достаточно быстро.

Вирусные протеазы — это ферменты, расщепляющие вирусные белки NS3 и NS4A. Расщепление является одной из фаз репликации, без которой невозможно построение копий вирусов. Полимеразы — другой вид ферментов, связанных с вирусными белками NS5A и NS5B, которые участвует в построении вирусной РНК.
К ингибиторам протеазы неструктурных белков NS3/NS4A относятся:
К ингибиторам полимеразы неструктурных белков NS5A/NS5B относятся:
Схемы лечения вирусного гепатита С могут включать:
- комплекс из двух ингибиторов полимеразы (напр., софосбувир + даклатасвир);
- ингибитор протеазы + ингибитор полимеразы (напр., симепревир + софосбувир);
- ингибитор протеазы/полимеразы + пегинтерферон альфа + рибавирин;
- ингибитор полимеразы + рибавирин.
Разработка и внедрение в терапевтическую практику ингибиторов вирусной протеазы и полимеразы позволили сделать гепатит С, даже 1 типа, излечимым в 90 и более процентах случаев.

Единственно возможная профилактика вирусного гепатита С заключается в соблюдении мер предосторожности:
- все медицинские и немедицинские манипуляции, связанные с нарушением целостности кожного покрова должны проводиться стерильными (желательно одноразовыми) инструментами;
- нестерильные инструменты необходимо подвергать термической стерилизации и/или обрабатывать антисептиками;
- при любом виде полового контакта необходимо пользоваться презервативом;
- предметы личной гигиены (бритвы, зубные щетки) должны быть строго индивидуального использования.
В следующем видео вы можете получить дополнительную информацию о том, что такое вирусный гепатит С:
источник
Гепатит С следует отнести к разряду коварных заболеваний, которые могут протекать бессимптомно, но угроза жизни пациента от этого не уменьшается. Для окружающих такой человек превращается в источник инфекции.
Чтобы добиться снижения темпов роста заболеваемости и улучшения здоровья людей, важно периодически контролировать состояние печени. Метод исследования крови на наличие РНК вируса гепатита С признан наиболее достоверным для диагностики и лечения заболевания.
Среди воспалительных заболеваний, поражающих печень, особую угрозу для жизни человека представляет гепатит С. Причиной заражения может стать нарушение правил стерильности во время процедуры переливания крови. Намного реже инфицирование происходит в результате полового контакта, а также во время родов, когда болеющая мать заражает новорожденного.
Течение гепатита С, наличие которого выявляют анализом на HCV, может быть острым или хроническим. Именно острая форма часто не сигнализирует явными симптомами, а обнаруживают патологию по результатам диагностики других заболеваний.
С переходом острого гепатита в стадию хронической патологии, возможны следующие варианты развития болезни:
- каждый пятый пациент выздоравливает после вовремя назначенного лечения;
- часть больных переходит в группу носителей вируса (неактивная форма хронического заболевания);
- у остальных заболевших прогресс хронической фазы подтверждают признаки поражения печени.
Момент перехода острого этапа в хроническую форму зафиксировать сложно. Причина в постепенном нарастании симптомов медленного поражения печени с отсутствием признаков желтухи.
Популяция вируса скрытно поражает клеточную структуру крови, страдает также печень. Обнаружить фрагменты РНК возбудителя удается только при помощи ПЦР тестирования образцов крови на гепатит С.
Основной способ инфицирования гепатитом – через кровь. Вирусные агенты, оказавшись в здоровой клетке, вместе с кровотоком достигают печени, где активно размножаются.
Накопление вирионов в зараженных гепатоцитах приводит к разрушению печеночных клеток. Процесс стимулирует выработку антител, которые вступают в борьбу с неповрежденными гепатоцитами, утяжеляя последствия болезни.
Самым надежным способом, позволяющим обнаружить в крови следы вируса, специалисты называют ПЦР анализ. Суть революционного метода полимеразной цепной реакции состоит в обнаружении цепочек вирусных РНК при создании определенной среды, куда помещают взятую на анализ пробу крови. Этапы диагностического процесса:
- После получения отобранного биоматериала в нем тиражируют множество копий РНК, принадлежащих вирусу гепатита С.
- Использованием многофункциональных тестовых систем с нагреванием и очисткой раствора добиваются необходимого количества копий.
- При помощи тестовой диагностики определяют концентрацию в анализируемом образце сформировавшихся генов.
В процессе нескольких этапов диагностики происходит трансформация нуклеотидных цепочек с формированием РНК вируса гепатита С, если порция крови пациента содержала фрагменты возбудителя.
Безоговорочная достоверность ПЦР тестирования объясняется высоким уровнем чувствительности полимеразной реакции, обладающей следующими преимуществами:
- Для обнаружения HCV достаточно одного генома вируса на весь объем биоптата;
- Высокая способность к генотипированию для выявления определенного возбудителя;
- Возможность за одно тестирование обнаружить РНК различных типов вирусов.
ПЦР-диагностика показана пациентам:
- при подозрении на воспаление печени без проявления симптомов патологии;
- для проведения скрининга во время профилактических мероприятий;
- в ходе обследования людей после контакта с инфицированным человеком;
- при хроническом гепатите для оценки активности размножающегося вируса;
- для выяснения степени эффективности проведенной терапии.
Сдавать анализ на выявление вирусного РНК обязательно должны пациенты, болеющие циррозом. Диагностика ПЦР показана людям, имеющим инфицированных гепатитом С родственников или половых партнеров.
Хроническую стадию заболевания печени сопровождают признаки фиброза с разрастанием соединительных тканей, что со временем нарушает структуру органа. Если вовремя начать лечение, повышается вероятность обратимости фиброза. Именно для выбора адекватной терапии важен учет результатов диагностики HCV, выполняемой поэтапно:
- Сначала методом качественного тестирования пытаются обнаружить следы вируса.
- Результаты количественного теста уточняют концентрацию в пробе вирусной РНК.
- Методом генотипирования устанавливают, к какому генотипу принадлежит возбудитель.
Ряд медиков считает диагностику на РНК вирусного гепатита обязательной для большинства пациентов, даже не имеющих характерных для патологии симптомов. Появление определенных жалоб уже свидетельствует о запущенном процессе с поражением печени циррозом, некрозом, онкологией.
В домашних условиях можно самостоятельно выполнить несложную диагностику гепатита, пользуясь экспресс-тестом ИФА. Тестовый комплект позволяет определить наличие антител к РНК вируса всего за 15 минут по капле крови. При выявлении антител потребуется дальнейшее обследование.
Задача начального этапа исследования – подтвердить наличие в тестируемом объеме генетических фрагментов HCV, если анализ крови показал наличие у пациента антител, готовых атаковать вирус гепатита С. Интерпретация результатов качественной диагностики имеет две позиции, с их особенностями важно ознакомиться:
- «РНК обнаружено». Положительный вариант результата указывает, что биологическая жидкость содержит фрагменты РНК возбудителя гепатита. Интерпретация показателя является подтверждением факта инфицирования: вирус размножается в крови носителя, печень подвергается разрушению.
- «РНК не обнаружено». При отрицательном варианте результата сохраняется вероятность малой концентрации вирусной РНК даже при явном отсутствии ее фрагментов. Тест не сможет выявить ничтожную концентрацию вирионов при недавнем заражении либо предшествовавшей противовирусной терапии.
Обнаружения РНК возбудителя по методике качественного тестирования, обеспечивающего 95% точности, достаточно для подтверждения гепатита С. Достоверность качественного этапа анализа ПЦР обеспечивает система с определенным порогом чувствительности (до 500 МЕ/мл).
При низкой виремии (концентрация вируса) потребуется помощь диагностической системы с показателем минимум 50 МЕ/мл. По результатам следующей части анализа определяют концентрацию вирионов в объеме исследуемого биоматериала.
Следующая ступень тестирования биологического материала заключается в определении количественного состава популяции возбудителя. Тестирование вирусной нагрузки на единицу фиксированного объема крови способствует выяснению степени виремии, а также тяжести заболевания.
Таблица расшифровки числовых обозначений (норма) инфицирования по тесту HCV
| Спектр вирусной нагрузки, измеряемый в МЕ/мл | Интерпретация показателей, полученных методом полимеразной цепной реакции |
| Следы РНК вируса гепатита не обнаружены | Нулевой показатель признают нормой, а человека – здоровым |
| Значение 180 | РНК отсутствует или концентрация вируса ниже порогового диапазона |
| Меньше 800 тысяч | Обнаружена низкая степень виремии |
| Больше 800 тысяч | Обнаружена виремия высокого уровня |
| Значение выше 25 млн. | Виремия превышает допустимый диапазон измерений |
Если результаты качественного анализа с отсутствием следов РНК вируса гепатита подтверждаются количественно на следующем этапе тестирования, то человека действительно можно считать здоровым. В крови полностью отсутствует вирус опасной патологии.
Показатель количественной диагностики, не превышающий 400 тысяч МЕ/мл, указывает на минимальную концентрацию РНК опасного вируса, но не на отсутствие патологии. Нагрузку, превышающую значение 800 тысяч, считают высокой. Но среди медиков нет единого мнения в вопросе жестких рамок, ограничивающих минимальную и максимальную виремию.
Даже людям, не сталкивавшимся с гепатитом С, необходимо знать, что возбудитель смертельно опасного заболевания имеет несколько генотипов. Благодаря прогрессивным методикам исследований удалось обнаружить 11 генотипов вируса гепатита С, но наиболее распространенных всего 6 видов.
Каждому типу генома, имеющему определенные характеристики, дали буквенное наименование и присвоили статус квазивирусов.
Из-за постоянных мутаций, обеспечивающих способность вируса к выживанию в окружающей среде, иммунная система человека не успевает быстро распознать очередного мутанта, чтобы вырабатывать к нему антитела. Это объясняет высокую опасность заболеть гепатитом С, а вакцинация против печеночной патологии сегодня только на стадии разработки.
Современные методики лечения новейшими препаратами позволяют не только вылечить патологию, но также избавить организм от вируса. Для этого необходимо установить его генотип и уровень концентрации в организме пациента.
Тест-системы некоторых лабораторий не оснащены соответствующими реагентами. Отсутствие возможности детерминирования субтипов генома приводит к выдаче результатов о невозможности типирования РНК.
В этом случае необходимо подтверждение диагноза методами дополнительных исследований с использованием основных маркеров гепатита. Обнаружение в крови человека иммуноглобулинов М и G сигнализирует о развитии в организме процесса, не характерного для здорового состояния.
Обозначенную ситуацию можно назвать первичным диагнозом, предупреждающим о необходимости комплексного обследования для получения объективной картины развивающегося процесса.
источник