Вирус гепатита С (HCV) является основной причиной заболевания печени во всем мире: им инфицированы 170 млн человек. Около 4,1 млн американцев (1,6% всего населения США) имеют хроническую HCV-инфекцию. Вирус гепатита С (HCV) — самая частая хроническая, передающаяся парентеральным путем инфекция, которую выявляют у 50% американцев с хроническими заболеваниями печени.
Стоит отметить, что с середины 1980-х гг. инфицирование HCV достигло своего пика и составило более 230 тыс. новых случаев. В настоящее время отмечается снижение инфицирования до 19 тыс. новых случаев в год. Такое снижение прежде всего является результатом значительного уменьшения случаев заражения при переливании крови благодаря широкому распространению скрининга донорской крови на HCV.
Тем не менее количество пациентов с хронической HCV-инфекцией продолжает увеличиваться вследствие пожизненной персистенции вируса. В отличие от HBV-инфекции заболевание прогрессирует в хроническое у большинства HCV-инфицированных лиц, а цирроз печени развивается у 20-30% пациентов с хронической HCV-инфекцией. HCV — основная причина хронических заболеваний печени в США и наиболее частое показание к трансплантации печени.
Согласно данным USA Centers for Disease Control за 2008 г., наиболее частыми установленными факторами риска инфицирования HCV являются:
— внутривенное введение наркотиков (54%);
— многочисленные половые партнеры (36%);
— хирургические вмешательства в течение последних 6 мес (16%);
— повреждения острыми предметами (иглами и т.д.) (10%);
— неоднократные контакты с HCV-инфицированными лицами (10%);
— трудовая деятельность в сфере медицины и стоматологии (1,5%).
В 32% случаев факторы риска инфицирования не были установлены.
В настоящее время в США число случаев передачи HCV при переливании крови приближается к нулю, но риск инфицирования HCV при уколе иглой в 6 раз выше, чем для ВИЧ (1,8% vs 0,3%). У детей основным путем инфицирования является перинатальный, однако частота его ниже, чем при HBV (6% vs 20%). Следует отметить, что у одного пациента может быть несколько факторов риска, тогда суммарный риск инфицирования для него будет превышать 100%.
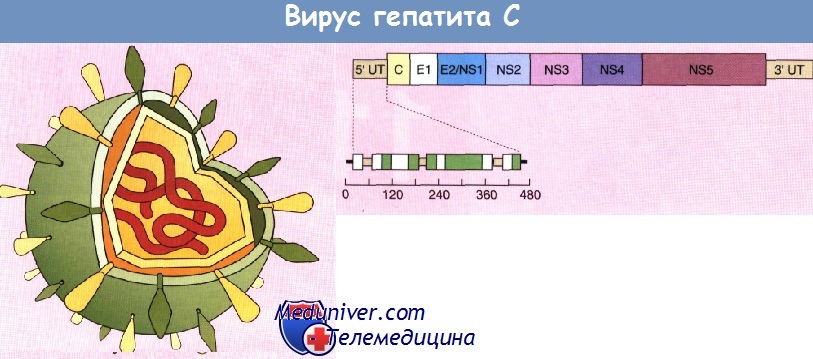
Вирус гепатита С (HCV), открытый в 1989 г., является членом семейства Flaviviridae. Это небольшой, состоящий из одноцепочечной РНК оболочечный вирус с геномом размером 9,6 кб, который кодирует один полипротеин с одной открытой рамкой считывания, впоследствии превращающийся в функциональные белки. Далее кратко опишем структуру генома HCV, т.к. ее знание является основой понимания патогенеза гепатита С.
5′-концевой участок генома кодирует высококонсервативный нуклеокапсидный коровый белок, за которым следуют белки оболочки E1 и Е2. В последовательности Е2 есть 2 гипервариабельных региона — HVR1 и HVR2. Следующий за ними белок р7, вероятно, функционирует как ионный канал. По направлению к З’-концевому участку расположены 6 менее консервативных неструктурных белков: NS2, NS3, NS4A, NS4B, NS5A и NS5B.
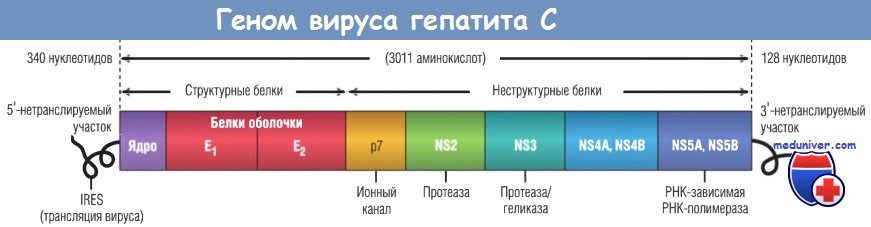
HCV является вирусом с положительной цепочкой РНК, содержащей два нетранслируемых участка на 5′- и 3′-концах.
Вирус кодирует один полипептид, который дает начало множеству вирусных белков.
IRES — Internal Ribosome Entry Site; РНК — рибонуклеиновая кислота.
NS5B является вирусной РНК-зависимой РНК-полимеразой. 3′-концевая последовательность обеих (положительной и отрицательной) цепочек РНК функционирует в цис-положении, что необходимо для репликации вируса. Вторичная структура и протеинсвязывающие свойства этих высококонсервативных нетранслируемых участков способствуют синтезу РНК HCV и обеспечивают стабильность генома путем связывания различных белков организма-хозяина и вируса.
Вследствие низкой точности транскрипции NS5B HCV является внутренне нестабильным, что приводит к появлению множества его генотипов и подтипов. Действительно, в организме инфицированного HCV человека циркулирует популяция дивергентных, но близкородственных вариантов вируса (квазитипы).
Со временем у одного пациента можно определить множество квазитипов, являющихся производными оригинального штамма HCV, который инфицировал человека изначально. Белок оболочки Е2 представляет собой мишень для большинства анти-HCV антител, но также является производным самого вариабельного участка вирусного генома, что приводит к образованию штаммов вируса, на которые не действуют нейтрализующие антитела. Такая нестабильность генома и антигенная вариабельность — серьезные препятствия для разработки вакцины против HCV.
Высокие титры анти-HCV IgG, определяемые после перенесения активной инфекции, не свидетельствуют о наличии эффективного иммунитета. Именно поэтому характерным признаком HCV-инфекции служат вторичные повреждения печени в результате реактивации предшествующей инфекции или появления нового эндогенного мутантного штамма.
Инкубационный период вирусного гепатита С варьирует от 2 до 26 нед, в среднем составляя 6-12 нед. Практически у 85% пациентов острая инфекция протекает бессимптомно и часто не диагностируется. РНК HCV определяется в крови на 1-3-й неделе заболевания, что совпадает с периодом повышения уровня трансаминаз в сыворотке крови. При симптомной острой HCV-инфекции анти-HCV антитела определяются только у 50-70% пациентов, у остальных анти-HCV антитела появляются через 3-6 нед после инфицирования. Клиническое течение острого вирусного гепатита С более мягкое, чем гепатита В.
Изредка наблюдается тяжелое течение, неотличимое от такового при вирусных гепатитах А и В. Выраженный иммунный ответ с вовлечением Т-лимфоцитов CD4+ и CD8+ наблюдается при самокупировании HCV-инфекции, однако до сих пор неизвестно, почему только у небольшого количества лиц происходит полная элиминация HCV.
Персистирующая инфекция и хронический гепатит — типичные признаки хронической HCV-инфекции (острая инфекция обычно протекает бессимптомно). Персистенция вируса и хроническая форма заболевания отмечаются в 80-85% наблюдений. Цирроз печени может развиться через 5-20 лет после острой инфекции у 20-30% пациентов с персистирующей инфекцией.
Механизмы, лежащие в основе хронической HCV-инфекции, до конца не ясны, но очевидно, что вирус обладает множеством механизмов «ускользания» от антивирусного иммунитета организма-хозяина. HCV может активно подавлять IFN-опосредованный антивирусный клеточный ответ на различных этапах, включая сигнальный путь с участием TLR в ответ на распознавание вирусной РНК и ингибирование рецепторов IFN, опосредующих антивирусный клеточный ответ.
При хронической HCV-инфекции РНК HCV в течение длительного времени циркулирует в крови у многих пациентов (более 90% пациентов с хроническим заболеванием), несмотря на наличие у них нейтрализующих антител. В связи с этим для оценки репликации вируса и для подтверждения диагноза «HCV-инфекция» у лиц с хроническим гепатитом следует выполнить тест на РНК HCV.
Характерным клиническим признаком хронической HCV-инфекции является периодическое повышение уровня трансаминаз в сыворотке крови, чередующееся с периодами снижения их концентрации до нормы. Молниеносная печеночная недостаточность развивается при HCV-инфекции достаточно редко.
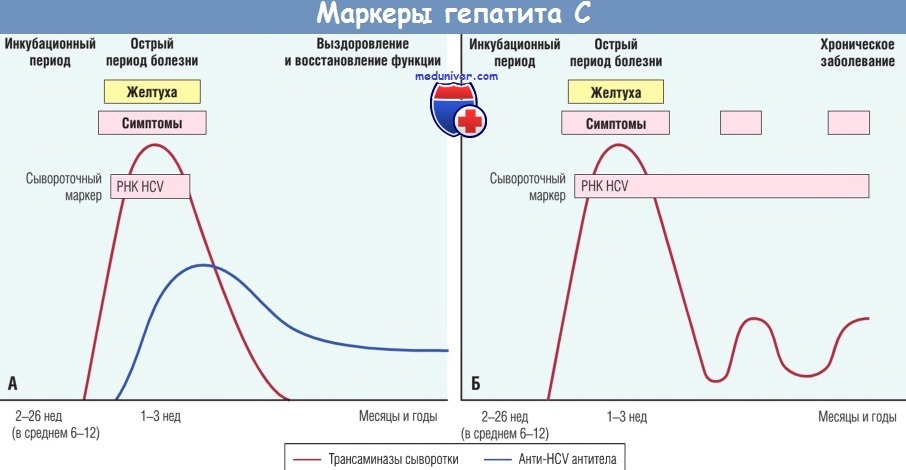
(А) Острая инфекция с выздоровлением.
(Б) Прогрессирование в хроническое заболевание.
РНК — рибонуклеиновая кислота.
источник
Клинико-анатомические формы вирусного гепатита:
1. острые: а) острая циклическая б) безжелтушная в) некротическая (молниеносная) г) холестатическая
2. хронический вирусный гепатит
Хронические вирусные гепатиты — заболевания, обусловленные гепатотропными вирусами с парентеральным путём инфицирования, сопровождающиеся гепатолиенальным синдромом, повышением активности печёночных ферментов и длительной персистенцией вирусов-возбудителей.
Прямые маркеры — этиологические агенты или их компоненты, выявляемые в тканях: частицы вируса (ЭМ), АГ вируса (ЭМ, иммуногистохимия).
Непрямые маркеры — клеточные изменения, характерные для заболевания определенной этиологии:
1. изменения гепатоцитов: а) матово-стекловидные гепатоциты (HBs-АГ) б) песочные ядра (HBc-АГ) в) тельца Каунсильмана (гепатоциты в состоянии коагуляционного некроза)
2. киллерный эффект Т-л в отношении гепатоцитов
3. белковая дистрофия гепатоцитов
4. очаги колликвационного некроза
5. воспалительный инфильтрат из макрофагов и лимфоцитов
6. перестройка структуры печени с образованием ложных преимущественно мультилобулярных долек
ЭПИДЕМИОЛОГИЯ.
Источник инфицирования при хроническом вирусном гепатите — человек, переносящий острую форму гепатита В, С или страдающий хроническим вирусным гепатитом указанной этиологии, а также носители, в основном это люди, у которых отсутствует желтуха и наблюдается бессимптомное или малосимптомное течение заболевания. Передаются вирусы гепатитов В, С через парентеральные манипуляции, при трансфузиях крови и препаратов крови, оперативных вмешательствах, внутривенном употреблении психотропных веществ, в анте- и перинатальном периодах, а также половым путём. Чаще всего инфицируются молодые люди, преимущественно мужчины в возрасте около 20 лет, примерно 40% из них заражаются при внутривенном введении наркотиков. Во всех странах, в том числе в Российской Федерации, постоянно регистрируют десятки тысяч новых случаев хронических вирусных гепатитов. В России наиболее распространены гепатиты В и С;
Приблизительно у половины больных путь инфицирования HCV установить не удается.
В настоящее время благодаря повсеместной вакцинопрофилактике гепатита резко уменьшается число вновь заразившихся данным заболеванием. Согласно статистике Госсанэпиднадзора, в РФ за 2005-й год было обнаружено 68 333 впервые заболевших хроническими вирусными гепатитами, в том числе 1063 ребёнка; 2/3 случаев пришлось на хронический гепатит С. Возрастает количество так называемых носителей. За вышеуказанный период в качестве носителей вируса гепатита В было зарегистрировано 72 678 человек, из них 1877 детей, а носителей вируса гепатита С — 151452 человек, из них детей 6447. Именно носители составляют основной резервуар инфекции.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ ГЕПАТИТА В.
Возбудитель — ДНК-содержащий вирус диаметром 42 нм из семейства Hepadnaviridae. Липопротеидная оболочка содержит поверхностный антиген вируса гепатита В (HВsAg), в структуру нуклеокапсида входят ДНК, ДНК-полимераза, протеинкиназа, ядерный антиген (HВcAg) и его секретируемая субъединица HВeAg. Описано 8 генотипов HBV (A, B, C, D, E, F, G, H). Особенностью вируса является способность формирования при репликации ковалентно замкнутой кольцевой ДНК (сссДНК), служащей матрицей для синтеза мРНК. Образование сссДНК выступает в роли механизма персисти-рования HBV и определяет трудности полной элиминации вируса.
HBV не оказывает прямого цитопатического действия на гепатоциты. Ведущая роль в патогенезе повреждения печени принадлежит Т-клеточным иммунным реакциям, обусловливающим Fas-зависимый апоптоз гепатоцитов. HBV обладает способностью к репликации в мононуклеарных фагоцитах. Нечасто наблюдающиеся внепеченочные проявления инфекции (гломерулонефрит, миокардит, узелковый периартериит и др.) представляют собой преимущественно иммунокомплексные синдромы.
В случае хронизации острого гепатита В наблюдается слабый как гуморальный, так и клеточный иммунный ответ. Первый характеризуется низкой продукцией анти-HBs, ведущей к персистенции внеклеточного пула HBV; второй — дефицитом образования сенсибилизированных к HBcAg Т-хелперов и цитотоксических Т-лимфоцитов, обусловливающим внутриклеточную персистенцию вируса
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ ГЕПАТИТА С
Вирус гепатита С относится к семейству флавивирусов. Геном вируса представлен однонитевой РНК протяженностью около 10 000 нуклеотидов. Вирус гепатита С вызывает заболевание только у человека. В экспериментальных условиях воспроизвести инфекцию можно у высших обезьян.
Популяция вируса неоднородна. Идентифицированы 6 генотипов (классификация по Simmonds), более 90 субтипов и множество вариантов вируса, обозначаемых как квазивиды. Зарегистрирована территориальная неравномерность циркуляции генотипов вируса гепатита С. В России чаще всего выявляются генотипы 1b и 3а этого вируса.
Определение генотипов вируса гепатита С имеет большое значение для практической медицины. Хотя до сих пор не установлено четкой корреляции между генотипами и уровнем виремии, характеристиками пациента, тяжестью течения заболевания, большинство исследователей
Вакцину против гепатита С создать пока не удалось из-за высокой изменчивости вируса гепатита С (ВГС).
В качестве основного механизма поражения печени при HCV-инфекции соглашаются с выводами о значении генотипов вируса как важного фактора, влияющего на эффективность противовирусной терапии. Рассматривается иммуноопосредованное повреждение гепатоцитов. Вирус обладает способностью к внепеченочной репликации, что может приводить у отдельных пациентов к развитию системных проявлений. Наиболее хорошо изучена связь длительно персистирующей HCV-инфекции со смешанной криоглобулинемией.
При хронизации HCV-инфекции в ее острую фазу не наблюдается активный вирус-специфический CD4 + Т-клеточный ответ, отмечается преобладание Т-хелперов 2-го типа и продуцируемых ими цитокинов. Считается, что вирус способен влиять на процессы активации Т-хелперов, нарушая их взаимодействие с цитотоксическими лимфоцитами. Предполагается возможность процессинга неиммуногенных фрагментов вирусных белков, нарушающих их распознавание и, следовательно, активацию Т-хелперов.
Гуморальный иммунный ответ при HCV-инфекции, характеризующийся продукцией антител, направленных против структурных и неструктурных антигенов HCV, не защищает от повторного инфицирования даже гомологичными штаммами вируса. Тем не менее в экспериментальных исследованиях установлено образование специфических антител к белкам вирусной оболочки Е1 и Е2 (преимущественно к гипервариабельному региону HVR1), обладающих способностью к нейтрализации вируса. Этот факт в определенной степени объясняет возможность реактивации HCV-инфекции у лиц, получающих иммуносупрессивную терапию. Высокая гетерогенность HVR1 в совокупности с чрезвычайной изменчивостью в процессе инфекции обусловливает неэффективность гуморального ответа, т. к. нейтрализующее действие постоянно продуцируемых антител оказывается ограниченным во времени.
КЛАССИФИКАЦИЯ.
1994 г., Лос-Анджелес: три категории оценки 1. этиология 2. степень активности ХГ 3. стадия ХГ
а) хронический аутоиммунный гепатит
б) хронический вирусный гепатит В
в) хронический вирусный гепатит С
г) хронический вирусный гепатит В и D
д) хронический лекарственный гепатит
е) хронический криптогенный (не вирусный, не аутоимунный) гепатит
ж) хронический наследственный гепатит (а) болезнь Вильсона-Коновалова б) недостаточность альфа-1-антитрипсина)
2. По степени активности: а) минимальной б) слабой в) умеренной г) тяжелой
3. По стадии ХГ: I-IV стадии
2) Патоморфологические признаки активности ХГ:
| Признак | Минимальная степень активности | Слабая степень активности | Умеренная степень активности | Тяжелая степень активности |
| Наличие балонной и/или жировой дистрофии + внутридольковые фокальные некрозы | ||||
| Слабо выраженная дистрофия | + | |||
| Умеренно выраженная дистрофия + мелкофокусные некрозы | + | |||
| Выраженная дистрофия + крупнофокусные некрозы | + | |||
| Тотальная дистрофия + сливные крупнофокусные некрозы | + | |||
| Перипортальные некрозы | ||||
| Отсутствуют | + | |||
| Мелкие | + | |||
| Ступенчатые | + | |||
| Мостовидные | + | |||
| Локализация воспалительного инфильтрата | ||||
| Только в портальных трактах | + | |||
| В отдельных портальных трактах проникает через пограничну | + | |||
| ю пластинку | ||||
| Сопровождает ступенатые некрозы | + | |||
| Сопровождает мостовидные некрозы | + |
3) Морфологическая характеристика стадии ХГ определяется степенью фиброза — единственный дифференциальный признак между острым и хроническим процессами:
| Фиброз | I стадия | II стадия | III стадия | IV стадия |
| Малозаметен и только в портальных трактах | + | |||
| Портальный + начальный перипортальный | + | |||
| Порто-портальный | + | |||
| Порто-портальный и неполный порто-центральный (предцирроз) | + |
4) Патоморфология хронических вирусных гепатитов: 2 формы — 1. хронический активный ВГ и 2. хронический персистирующий ВГ
Для двух форм характерны прямые и непрямые маркеры ВГ +:
а) хронический активный ВГ: дистрофия и различной степени некрозы + перестройка печени с прогрессией в цирроз
б) хронический персистирующий ВГ: практически в цирроз не происходит
источник
Вирусный гепатит А-острая циклическая инфекция, характеризующаяся четкой сменой периодов.После заражения ВГА из кишечника проникает в кровь и далее в печень, где после фиксации к рецепторам гепатоцитов проникает внутрь клеток. На стадии первичной репликации отчетливых повреждений гепатоцитов не обнаруживается. Новые поколения вируса выделяются в желчные канальцы, далее поступают в кишечник и выделяются с фекалиями во внешнюю среду. Часть вирусных частиц проникает в кровь, обусловливая развитие интоксикационной симптоматики продромального периода. Повреждения гепатоцитов, возникающие в ходе дальнейшего течения ГА, обусловлены не репликацией вируса, а иммуноопосредованным цитолизом. В периоде разгара ГА морфологическое исследование позволяет выявить воспалительные и некробиотические процессы, происходящие преимущественно в перипортальной зоне печеночных долек и портальных трактах. Эти процессы лежат в основе развития трех основных клинико-биохимических синдромов: цитолитического, мезенхимально-воспалительного и холестатического. К лабораторным признакам цитолитического синдрома относятся: повышение активности ферментов АлАТ и АсАТ (аланинамино- и аспартатаминотрансферазы), уровня железа в сыворотке крови, снижение синтеза альбумина, протромбина и других факторов свертывания крови, эфиров холестерина. Начальным этапом цитолитического синдрома является повышение проницаемости мембраны гепатоцитов. Это обусловливает выход в кровь, прежде всего АлАТ — фермента, находящегося в цитоплазме печеночной клетки. Повышение активности АлАТ — ранний и надежный индикатор повреждения гепатоцита. Мезенхимально-воспалительный синдром характеризуется повышением уровня бета- и гаммаглобулинов, изменением коллоидных проб (снижение сулемового титра и повышение тимоловой пробы). Холестатический синдром проявляется повышением в крови уровня связанного билирубина, желчных кислот, холестерина, меди, активности щелочной фосфатазы, а также билирубинурией, уменьшением (исчезновением) уробилиновых тел в моче. Вследствие комплексных иммунных механизмов (усиление интерферонопродукции, активизации естественных киллеров, антителопродукции и активности антителозависимых киллеров) репликация вируса прекращается, и происходит его элиминация из организма человека. Для ГА не характерны ни длительное присутствие вируса в организме, ни развитие хронической формы болезни. Однако иногда течение заболевания может быть модифицировано в случаях ко-инфекции или суперинфекции другими гепатотропными вирусами. У лиц же с генетической предрасположенностью возможно развитие хронического активного аутоиммунного гепатита 1-го типа
Вирусный гепатит В Из места внедрения ВГВ гематогенно достигает печени, где в гепатоцитах происходит репликация вирионов. ВГВ не обладает цитотоксичностью. Сам вирус гепатита В проникнув в клетку, оставляет свой антиген на поверхности гепатоцита. Эти клетки опознаются Т-лимфоцитами как чужеродные и подвергаются агрессии. Таким образом, поражение клеток печени при гепатите В является иммуннообусловленными. Кроме этого при хроническом гепатите В в процесс вовлекаются Т-супрессоры. Они находятся в подавленном состоянии и поэтому формируются условия для развития аутоиммунных реакций, направленных против собственных клеточных антигенов.Следствием этого является развитие некробиотических и воспалительных изменений в паренхиме печени. В результате патологических изменений в печеночной ткани возникают цитолитический, мезенхимально-воспалительный и холестатический синдромы с определенными клиническими и лабораторными проявлениями .
При морфологическом исследовании обнаруживают дистрофические изменения гепатоцитов, зональные некрозы, активизацию и пролиферацию звездчатых эндотелиоцитов (клеток Купфера); в более тяжелых случаях — субмассивные и массивные некрозы печени, которые, как и распространенные «мостовидные» и мультилобулярные некрозы, являются нередко патологоанатомическим субстратом печеночной комы. Холестатические варианты ГВ сопровождаются вовлечением в патологический процесс внутрипеченочных желчных ходов с образованием в них «желчных тромбов», увеличением содержания билирубина в гепатоцитах.
В патогенезе ГВ, кроме репликативной, выделяют также интегративную форму течения инфекции. При этом происходит встраивание всего генома вируса в геном клетки хозяина или его фрагмента, отвечающего, например, за синтез HBsAg. Последнее приводит к присутствию в крови лишь HBsAg.Интеграция генома ВГВ в геном гепатоцита является одним из механизмов, обусловливающих развитие персистирующих (ациклических) форм течения ГВ и первичной гепатоцеллюлярной карциномы.
Вирусный гепатит С После проникновения в организм человека ВГС, обладая гепатотропностью, реплицируется преимущественно в гепатоцитах. ВГС обладает слабой иммуногенностью, что определяет замедленный, неинтенсивный Т-клеточный и гуморальный ответ иммунной системы на инфекцию. Так, в острой стадии ГС сероконверсия возникает на 1-2 мес. позже появления признаков цитолиза гепатоцитов (повышения активности АлАТ). Лишь через 2-10 нед. от начала заболевания в крови больных начинают определяться антитела к ядерному антигену классов M, затем G. Однако они обладают слабым вируснейтрализующим действием. Антитела же к неструктурным белкам ВГС в острой фазе инфекции обычно не выявляются. Зато в крови в течение острой стадии болезни (и при реактивации — в хронической) определяется присутствие РНК вируса. Устойчивость ВГС к специфическим факторам иммунитета обусловлена его высокой способностью к «ускользанию» из-под иммунологического надзора. Таким образом, слабость иммунного реагирования и мутационная изменчивость вируса во многом обусловливают высокий хрониогенный потенциал данного заболевания.
Вирусный гепатит D Этот вирус является дефектным, так как он на своей поверхности не имеет рецепторов для гепатоцитов. Поэтому он не может проникнуть в клетку и реплицироваться в ней. Для репродукции данного вируса необходимо участие «вируса-помощника». Роль этого помощника играет вирус гепатита В. таким образом, заболевание может возникнуть при одновременном заражении обоими вирусами или при инфицировании лиц уже имеющих вирус гепатита В (суперинфекция). Сочетанное действие обоих вирусов приводит к развитию более тяжелых форм заболевания с выраженными явлениями печеночно-клеточной недостаточности. В большинстве случаев заболевание приобретает прогрессирующее течение с быстрым переходом в цирроз печени и смертью.
Вирусный гепатит Е изучен недостаточно. Большинство исследователей полагают, что центральным звеном патогенеза является цитопатическое действие вируса. Не исключается и участие иммунных механизмов в некробиотических изменениях печеночной ткани.
источник
Любая договоренность, достигнутая посредством и/или связанная с нашим сайтом («medtour.md»), обращается ли заявитель через сайт по телефону, номер которого появляется на сайте, через чат или форум, доступные на сайте, или мы связываемся с заявителем по просьбе заявителя («Пациент»), должна регулироваться в соответствии со следующими условиями:
- Материалы, доступные на этом сайте или через него предоставлены по принципу «как есть». Компания отказывается от каких-либо подразумеваемых гарантий или условий какого-либо вида, включая гарантии коммерческой выгоды, пригодности для конкретной цели или соблюдения прав.
- Несмотря на то, что Компания старается предоставить точную информацию на этом сайте в качестве услуги для своих пользователей, Компания не несет ответственности за точность или полноту информации, размещеннной на сайте или за какие либо результаты использования или получения доступа к этой нформации, а также не делает никаких заявлений в отношении этой информации.
- Информация, содержащаяся в данном сайте не является профессиональной медицинской консультацией, или рекомендацией по диагностике или лечению, и не должна использоваться для диагностики или лечения проблем со здоровьем или болезни, а так же она не являет собой замену любого профессионального ухода, если таковой предоставляется не через посредство Компании. В то время как Компания прилагает все возможные усилия, чтобы обеспечить точную и актуальную информацию, Компания и/или кто-либо от ее имени, является исключительно посредником между поставщиками услуг и пациентами.
- Пациент признает, что все медицинские процедуры несут определенные риски, и соглашается нести ответственность за любой риск или результаты лечения. Компания не несет никакой ответственности за результаты лечения.
- Любые рекомендации предоставленные Компанией или любым физическим или юридическим лицом от ее имени, если таковые имеются, не заменяют профессиональное мнение медицинского персонала больницы или клиники, а так же ни в коей мере не обязывают Компанию или физическое или юридическое лицо, предоставляющее такие рекомендации фактически предоставить эти Услуги. Кроме того, Компания не гарантирует того, что, за исключением услуг, которые были непосредственно согласованы между Компанией и пациентом, какие-либо услуги, упомянутые в данном сайте будут доступны, или будут доступны в той форме, в которой они описаны на сайте.
- Пациент осознает и обязуется обеспечить и продолжить страхование от всех рисков, охватывающие все соответствующие медицинские процедуры, до его взаимодействия с Компанией.
- Пациент признает и соглашается, что его платежные обязательства по отношению к Компании не обусловлены каким-либо образом, в том числе выполнением или результатами или успехом Услуг.
- Компания не несет никакой ответственности за само лечение, его проведение или результаты, и, в частности, не несет ответственности за какие-либо задержки, незапланированные расходы и другие факторы, не находящиеся под контролем Компании (например, стихийных бедствий, отмены полетов, форс-мажорные обстоятельства и т.д.).
- Ни при каких обстоятельствах Компания не несет ответственности за любой ущерб, включая, без ограничения, специальные, непрямые, прямые или косвенные убытки, связанные с Услугами или в других случаях. Не умаляя вышесказанное, общий объем ответственности компании в любом случае не должен превышать суммы, фактически уплаченной Компании Пациентом в связи с соответствующим лечением.
- Пациент обязуется обеспечить все необходимые страховые покрытия и разрешения в связи с его пребыванием в Молдове за свой счет. Компания не предоставляет страховое покрытие для пациентов.
- Компания не несет никакой ответственности по отношению к любому сопровождающему лицу Пациента. В связи с этим настоятельно рекомендуется, чтобы таковые сопровождающие лица или другие третьи лица получили необходимые страховые покрытия и разрешения на пребывание в Молдове. Ни одна из Услуг не предоставляется и недоступна для таких третьих лиц.
- Взаимодействия между Компанией и пациентом осуществляются исключительно для предоставления Услуг. Компания не несет ответственности в какой-либо форме по любому другому виду деятельности пациента или кого-либо от его имени в Республике Молдова. Взаимодействуя с Компанией, пациент осознает и принимает, что он или кто-либо от его имени не будет заниматься какой-либо противозаконной или неблагочестивой деятельностью во время его пребывания в Молдове. В случае, если Пациент остается в Молдове для других целей, кроме получения медицинской помощи, он несет полную ответственность за любою такую деятельность и Услуги не распространяется на такие виды деятельности в любой форме.
- Данные Условия отменяют другие условия, заверения или гарантии, выраженные или подразумеваемые в любом месте сайта и/или в устной форме нашими представителями.
- Эти Условия должны регулироваться законами Республики Молдова, и любые споры между Компанией и Пациентом будут разрешаться исключительно компетентным судом в Молдове.
- Личная информация, предоставленная Пациентом и/или оставленная на сайте, строго конфиденциальна и не передается третьим лицам.
Единственным возбудителем гепатита С у людей разных возрастных категорий выступает один и тот же вирус. На сегодняшний день, патогенез гепатита С изучен не в полной мере, однако все-таки составлены некоторые наработки научных деятелей относительно деятельности печени и ее разрушения. Стоит отметить тот факт, что гепатит С стал отдельным заболеванием относительно недавно, порядка 20-ти лет назад, в то время, как остальные разновидности болезни, среди которых А и В, зафиксированы в медицине более 50 -ти лет назад.
Что послужило причиной возникновения столь опасного штамма, пока неизвестно. Однако, принимая во внимание, что он пока не успел окончательно сформироваться, поэтому имеет потенциал к мутации РНК, благодаря чему он устойчив к применению медикаментов и имеет защиту к воздействию иммунитета человека.
Этиология вирусного гепатита С заключается в инфицировании инфекцией, относящейся к семейству Flaviviridae. Ранее считалось, что рассматриваемый вирус выступает лишь одним адептом подсемейства, однако не так давно была раскрыта еще одна разновидность вируса С, преимущественно поражающего животных. Специфика его распространения полностью пока не установлена, ведутся исследования. Структура вируса гепатита С довольно проста. Диаметр тела вируса, покрытого липидным слоем, равен 50-55 нм. Рассматриваемый вирус содержит нуклеокапсид, в составе которого имеется однонитная линейная РНК. Проведение многочисленных исследований позволило установить, что генотип вируса содержит более 9500 нуклеотидов.
Преимущественно вирус разрушает гепатоциты — это клетки печени, имеющие строение, существенно отличающееся от клеток остальных органов
Некоторые моменты, касающиеся патогенеза гепатита С, по-прежнему для научных деятелей остаются загадкой. Допустим, патогенез гепатита В имеет конкретные принципы формирования и распространения, которые с легкостью можно отследить при проведении лабораторных исследований. Ситуация с гепатитом С абсолютно другая, поскольку входящая в его состав РНК непрерывно мутирует, что усложняет формирование стойкого иммунитета. Кроме того, осуществляется циркуляция квазивидов в организме. Специалистами установлено несколько основных стадий распространения вируса в организме:
- дифференциально-диагностическое гепатитовпроникновение в организм;
- разрушение гепатоцита;
- синтез белков;
- упаковка РНК;
- распространение вируса из клетки печени.
Структура гепатита В в патогенезе имеет определенные сходства с гепатитом С. Однако главным различием выступает способ инфицирования. Если инфицирование вирусом гепатита С происходит сугубо через кровь, гепатитом А и В можно заразиться вследствие незащищенной половой связи.
Известно, что гепатит С является вирусным заболеванием, симптомы которого выявляются не сразу, а через некоторое время. Если были определены первые признаки поражения болезнью, нужно сдать анализы, пройти исследование.
Важно устранить причины появления патологии, поддерживать ослабевшую печень. Может произойти ее воспаление, когда соединительной тканью будут замещаться поврежденные структуры. Перед тем, как поддерживать гепатит С, следует определиться с его влиянием на печень. В действительности, вирус становится причиной серьезной патологии, приводя к развитию цирроза и онкологическими осложнениями. Не всегда получается полностью избавиться от болезни. Поэтому часто пациентам приходится поддерживать свой организм медикаментозными средствами и придерживаться диетического питания. Такие меры исключают рецидив и прохождение вторичной терапии.
Обычно первые симптомы определяются через четыре года, а именно:
- желтушность кожных покровов;
- чувство слабости и усталости;
- апатия, подавленность;
- внезапная субфебрильная температура;
- сниженный иммунитет и частые заболевания.
После определения патологии начинается восстановление печени с усилением иммунитета. Рекомендуется применение противовирусных препаратов. Симптомы гепатита могут быть схожи с другими патологиями. Около 20% пациентов с хронической патологией болеют фиброзом, после чего у них проявляется рак, цирроз.
Если у человека гепатит С, как поддержать печень существует много способов. При поражении печени нельзя переедать. Основным критерием правильного лечения становится щадящая и сбалансированная диета, способствующая улучшению самочувствия и снижающая нагрузку на пораженный орган. Из рациона исключаются консервы, маринады с соленьями, жирная и жареная пища, острые приправы и блюда. Также нельзя потреблять бобовые, крепкие чаи и кофе, пищевые добавки, консервированные соки, газированные напитки, сырой лук и чеснок, сдобные изделия и торты, алкоголь, копченые колбасы, сыры высокой жирности. В процессе приготовления продукты можно тушить, запекать или варить.
Также уменьшается объем соленых и белковых продуктов, суточная калорийность не должна быть больше 3000 килокалорий. Обязательно следует придерживаться строгого графика, разделить питание на 5-6 раз в сутки по небольшим объемам. Организм не желательно перегружать трудно перевариваемой пищей. Рекомендуется есть продукты, насыщенные клетчаткой. Например, тыквенную кашу, чаи из трав, напиток цикория, отваренные семена расторопши, растительное и оливковое масла, несдобную выпечку, нежирные кисломолочные продукты, овощные и фруктовые салаты, диетическое мясо в отварном виде, супы без зажарки, сухофрукты, зеленый горошек и молодую фасоль. Также следует есть витамины С, Е, А. Аскорбиновая кислота способствует регенерации тканей, снижает восприимчивость к вирусу. Витамин Е поддерживает целостность клеток, быстро восстанавливает. Токоферол имеет антиоксидантные качества, синтезирует гормоны.
Заболеваемость и смертность, вызванные инфекцией вируса гепатита С (ВГC), на сегодняшний день стали проблемой международного уровня. Ежегодно от различных ВГC осложнений, в том числе цирроз печени и гепатоцеллюлярная карцинома (ГЦК), погибает порядка 700 тысяч человек. Основными препаратами для борьбы с инфекцией ВГC являются противовирусные средства; однако ввиду того, что в большинстве случаев заболевание протекает практически бессимптомно, основная масса зараженных людей даже не догадывается о наличии такой патологии. Более того, для многих, кому поставлен диагноз, доступ к проведению необходимых терапевтических мер остается ограниченным. Всемирной организацией здравоохранения (ВОЗ) в 2014 году было разработано первое Руководство по скринингу, оказанию необходимой медицинской помощи и лечению людей с диагнозом гепатит С.
Основной задачей Руководства ВОЗ является составление научно аргументированных рекомендаций для эффективного лечения инфекции гепатита С с применением, по возможности, пероральных комбинаций современных противовирусных препаратов прямого действия (ПППД), позволяющих излечить вирусный гепатит С. Рекомендации
сопутствуются пояснениями об уровне доказательности каждого момента.
Основными достоинствами лечения на основе ПППД являются простота и относительно короткий курс терапии заболевания. Однако при этом, рассматриваемое лечение отличается высокой эффективностью (частота стабильного вирусологического ответа [УВО] не менее 90%).
Лечение острого (вирусного) заболевания имеет некоторые характерные черты. Главное не допустить того, чтобы болезнь переросла в хроническую форму. Важно понимать, что гепатит С, рекомендации к лечению которого, обновляются ВОЗ систематически, все чаще перерастает в хроническую форму, и это выступает основной проблемой. Дело в том, что хронический HCV-вирус требует продолжительного медикаментозного курса лечения, который составляется только после проведения непростых обследований. При проведении диагностики больного в большинстве случаев используются следующие лабораторные мероприятия:
- серологический метод, при котором устанавливается наличие антител;
- молекулярный, позволяющий установить РНК-вирус;
- метод генотипирования вируса, для конкретного планирования терапевтических мер, подбора требуемых препаратов и дозировки;
- определение генотипа обследуемого пациента.
Проведение правильных лабораторных обследований имеет большое значение при диагностике гепатита С и его генотипа. Полученные данные помогают специалисту назначить наиболее подходящую методику лечения.
Многих, кто перенес гепатит С, интересует вопрос: «Может ли гепатит С вернуться после лечения?». Врачи говорят о том, что такое происходит из-за того, что пациенты пренебрегали профилактикой и не соблюдали личную гигиену. Рецидив заболевания после выздоровления может произойти потому, что антитела одного вида находятся в крови. Поэтому произошедший рецидив говорит о том, что заражение уже другого вида. Это связано с тем, что у заболевания существует около 6 генотипов. Стоит отметить, что вирус может выработать устойчивость к лекарственным препаратам. Симптомы рецидива точно такие же, как и у начальной стадии гепатита С. Причины возвращения гепатита различны. Среди наиболее популярных выделяют:
- Разновидность генотипов.
- Очень сильное повреждение печени, которое обусловлено различными патологиями или другими причинами.
- Неправильное лечение в связи с несоблюдением дозировки препарата.
- Несоблюдение профилактики после выздоровления.
- Ослабленный иммунитет в связи с лечением гепатита.
- Инфекционные и вирусные заболевания.
- Хронические заболевания, связанные с желудочно-кишечным трактом.
- Сахарный диабет 2 типа. 2 тип диабета оказывает отрицательное влияние на работу печени. Если происходит сочетание двух заболеваний, то следствием будет рецидив гепатита С в более тяжелой форме.
Больше всего риску получить рецидив подвержены те, кто болел гепатитом первого генотипа. Также врачи говорят о том, что вирус может быть подвержен мутациям, что также ведет к рецидиву. Чаще всего рецидив происходит в первый год после первого лечения. Если после года анализ, который определяет наличие вируса, продолжает быть отрицательным, то можно говорить о том, что достигнута устойчивость. А значит, гепатит был побежден навсегда. В случае, когда инфекция вернулась, пациент попадает в группу риска. Поэтому ему требуется повторная терапия с измененной дозировкой или полностью сменой препарата. Повторное лечение после рецидива дает положительные результаты. Суть терапии в этом случае заключается в том, что прием лекарств продлевается. Для лечения используются препараты Интерферон-А и Рибавирин. Также повторное лечение включает в себя витамины и вещества, которые способны выводить токсины. Схема лечения точно такая же, как и при первичном заражении. Чтобы исключить возможность повторного заражения, необходимо сделать акцент на восстановлении иммунитета после того, как происходит выздоровление. Весь последующий период жизни будет состоять в реабилитации, так как если не соблюдать рекомендации, данные врачом, то вирус может перерасти в хроническое заболевание. Больной должен соблюдать диету, чтобы восстановить работу всех внутренних органов. По статистике около 30% зараженных, прошедших полную терапию лечения гепатита С могут быть снова подвержены заболеванию. Однако врачи уверены в том, что снизить риски рецидива возможно благодаря более длительным и интенсивным курсам лечения. Также не стоит забывать о профилактических мерах.
источник
В настоящее время проблемой хронической HCV-инфекции интересуются как врачи-специалисты, так и люди, никак не связанные с медициной. От гепатита С во всем мире страдают по меньшей мере 200 млн человек.
В настоящее время проблемой хронической HCV-инфекции интересуются как врачи-специалисты, так и люди, никак не связанные с медициной.
От гепатита С во всем мире страдают по меньшей мере 200 млн человек. Последствиями перенесенного заболевания могут быть хронический гепатит, цирроз и первичный рак печени.
Распространенность хронической HCV-инфекции на земном шаре варьирует от 0,5 до 2%. Существуют регионы, для которых характерна более высокая распространенность этого заболевания: 6% в Заире и Саудовской Аравии, 16% в изолированных поселениях в Японии. В России наблюдается рост заболеваемости гепатитом С (3,2 на 100 тыс. населения в 1994 году и 19,3 в 1999 году). Источниками заражения вирусным гепатитом C служат больные острыми и хроническими формами HCV-инфекции, причем в основном это люди, у которых отсутствует желтуха и наблюдается бессимптомное или малосимптомное течение заболевания.
В настоящее время HCV чаще всего инфицируются молодые люди, преимущественно мужчины в возрасте около 20 лет, примерно 40% из них заражаются при внутривенном введении наркотиков. Основным путем инфицирования HCV является парентеральный. Так, у 6,1% больных, которым производилось переливание крови и ее компонентов во время кардиохирургических операций, развивался острый вирусный гепатит C, у 60% из них гепатит принимал хроническую форму.
Существует и риск заражения гепатитом C половым путем, однако он невелик (5-8%). Возможна передача HCV от матерей с острой или хронической формой инфекции; это также редкое явление, встречается не чаще чем в 5-6% случаев. Риск заражения вышеуказанными путями уступает таковому при гепатите В.
Приблизительно у половины больных путь инфицирования HCV установить не удается.
Вирус гепатита С относится к семейству флавивирусов. Геном вируса представлен однонитевой РНК протяженностью около 10 000 нуклеотидов. Вирус гепатита С вызывает заболевание только у человека. В экспериментальных условиях воспроизвести инфекцию можно у высших обезьян.
Популяция вируса неоднородна. Идентифицированы 6 генотипов (классификация по Simmonds), более 90 субтипов и множество вариантов вируса, обозначаемых как квазивиды. Зарегистрирована территориальная неравномерность циркуляции генотипов вируса гепатита С. В России чаще всего выявляются генотипы 1b и 3а этого вируса.
Определение генотипов вируса гепатита С имеет большое значение для практической медицины. Хотя до сих пор не установлено четкой корреляции между генотипами и уровнем виремии, характеристиками пациента, тяжестью течения заболевания, большинство исследователей соглашаются с выводами о значении генотипов вируса как важного фактора, влияющего на эффективность противовирусной терапии.
Вакцину против гепатита С создать пока не удалось из-за высокой изменчивости вируса гепатита С (ВГС).
Считают, что вирус оказывает прямое цитопатическое действие и вызывает иммуноопосредованное повреждение гепатоцитов. Высокая степень хронизации вирусного гепатита С обусловлена некоторыми особенностями действия вируса:
- возможностью внепеченочной репликации вируса, включая иммунокомпетентные клетки (клетки, предшественники гемопоэза, лимфоциты и моноциты периферической крови, миофибробласты);
- гетерогенностью генотипов и частыми мутациями генома вируса;
- индукцией каскада иммунопатологических реакций;
- активизацией процессов перекисного окисления липидов в печени.
В течении хронической HCV-инфекции может происходить нейтрализация мажорного варианта вируса, но тогда генерируются минорные варианты. Квазивиды HCV представляют собой движущуюся мишень, которую ограничивает иммунная система хозяина. Появление нового мажорного квазивида сопровождается повышением виремии и увеличением титра Ig M антител к вирусным белкам. Постепенно и этот новый мажорный вариант заменяется. Такой процесс приводит к периодической волнообразной виремии, сопровождающейся обострением хронического гепатита С (ХГС) и повышением уровня антител.
Возможно, антивирусному Т-клеточному ответу отведена центральная роль в элиминации ВГC, так как нейтрализующие антитела, по-видимому, очень часто оказываются неэффективными. Т-хелперные (Th) лимфоциты распознают вирусные антигенные пептиды, представленные HLA-комплексом II класса на поверхностной мембране антиген-презентирующих клеток. В зависимости от типа цитокинового профиля Th-клетки делятся на две группы: Th1 и Th2. Первые продуцируют IFNg и IL2, стимулируя Т-клеточный ответ и цитотоксическую Т-лимфоцитную активность, а вторые продуцируют IL4 и IL10, стимулируя В-клеточный ответ. Таким образом, Тh-лимфоциты играют существенную роль в регуляции иммунного ответа. У пациентов, у которых болезнь перешла в хроническую стадию, в острой фазе вирус-специфический Th ответ был ниже и преобладали цитокины типа Th2.
У хронически ВГC-инфицированных пациентов значительно увеличено содержание вирусоспецифических Th2-клеток и их цитокинов. Нарушение баланса Th1/Th2 цитокиновой продукции может играть важную роль в иммунопатогенезе хронической ВГC-инфекции. Показано снижение уровня IFNg и IL12 при ХГС. Этот дефицит является следствием повышенного уровня IL10, предполагаемого отрицательного регулятора для IFNg. Повышенное содержание Th2-клеток при ХГС может снижаться при комбинированной терапии рибавирином и IFNa. Обнаружено, что у пациентов с клинико-биохимическим улучшением после лечения IFNa произошло увеличение уровня Th1-цитокинов.
Цитотоксические лимфоциты (CTL) играют, по-видимому, некоторую роль в ограничении репликации ВГС. Этот ответ недостаточен для полной элиминации вируса при хронической инфекции и, кроме того, может вызывать повреждение печени. Известно, что CTL способны быстро опознавать и направленно лизировать клетки, несущие ВГC-антигены, не провоцируя значительного воспаления, с помощью перфоринового, FasL- и TNFα-базируемых механизмов.
ТNF, как предполагается, индуцируют апоптоз клеток, опосредуя высвобождение свободных радикалов из митохондриальных электронно-транспортных путей и модуляцию синтеза некоторых белков. Взаимодействие нуклеокапсидного белка ВГC с внутрицитоплазматической частью рецептора TNFb, вероятно, представляет собой эволюционно-отобранный механизм, с помощью которого вирус препятствует преждевременному апоптозу клетки-хозяина. В отсутствие доступных модельных клеточных культур прямая цитопатичность вируса гепатита С не может быть исследована в полном объеме.
В подавляющем большинстве случаев острого гепатита С иммунной системе не удается элиминировать вирус. До сих пор нет ясного представления о том, почему это происходит. Очевидно, ВГС обладает эволюционно-закрепленными способностями, обеспечивающими ему персистенцию.
Однако иммунная система может оказывать существенное влияние на ВГC-инфекцию. В 15% случаев острого гепатита С она эффективно уничтожает вирус, а у хронически ВГC-инфицированных обеспечивает умеренное ограничение инфекции в течение почти 20 лет. Возможно, ослабление какого-либо звена антивирусных иммунных механизмов позволяет вирусу активно воздействовать на иммунную систему. Длительная ВГC-персистенция может привести к развитию В-клеточных лимфопролиферативных нарушений, таких, как смешанная криоглобулинемия, злокачественная не-Ходжкинская лимфома и появление органоспецифических и неспецифических аутоантител. Таким образом, хроническую ВГC-инфекцию следует рассматривать как мультисистемное заболевание.
Лабораторная диагностика гепатита С основана на выявлении специфических маркеров инфицирования ВГС (анти-ВГС-IgM/G, РНК ВГС) и должна проводиться разрешенными МЗ РФ к применению диагностическими препаратами отечественного или зарубежного производства в лабораториях, имеющих лицензию на проведение данного вида лабораторных исследований.
HCV RNA — самый ранний маркер репликации вируса, определяемый с помощью полимеразной цепной реакции (ПЦР) спустя несколько недель после заражения. Для выявления анти-ВГС применяют иммуноферментный анализ (ИФА). В настоящее время используют тест-системы третьего поколения ELISA-3. Подтверждающим методом является рекомбинантный иммуноблотинг (RIBA). У 60% больных анти-ВГС определяются в острой фазе, у 35% они появляются спустя 3-6 месяцев после инфицирования, у 5% инфицированных лиц анти-ВГС не определяются.
Болезнь может протекать бессимптомно. Наиболее распространенным симптомом является слабость. Целенаправленный опрос больных часто помогает выявить такие факторы риска, как переливание крови, внутривенное введение наркотиков, хронический гемодиализ и др. Кроме слабости больной может жаловаться на быструю утомляемость, тяжесть в правом подреберье, боли в правом верхнем квадранте живота, диспепсические явления.
Критериями постановки диагноза являются увеличение печени и селезенки, гиперферментемия и анти-ВГС в крови в течение не менее 6 месяцев.
Гепатоспленомегалия выявляется не более чем у 50% обратившихся за помощью больных, активность сывороточных трансаминаз редко превышает верхнюю границу нормы в 6 раз. Следует обратить внимание на то, что активность сывороточных трасаминаз не отражает степени изменений в печени: она может быть нормальной, несмотря на значительные морфологические изменения. Концентрация РНК ВГС в сыворотке имеет существенное значение для определения контагиозности и для мониторинга результатов лечения. При наличии в крови HCV-РНК биопсия печени, как правило, выявляет ряд изменений. Концентрация HCV-РНК в сыворотке, превышающая 105 молекулярных эквивалентов (копий) в 1 мл, наблюдается в активной фазе заболевания и совпадает с пиками активности трансаминаз.
Наличие или отсутствие РНК ВГС, как правило, не является диагностическим критерием хронического гепатита С и определяет фазу процесса (активный, неактивный).
Для раннего выявления ГЦК у больных циррозом печени, особенно у мужчин старше 40 лет, каждые 6 месяцев определяют уровень сывороточного α-фетопротеина и выполняют УЗИ печени.
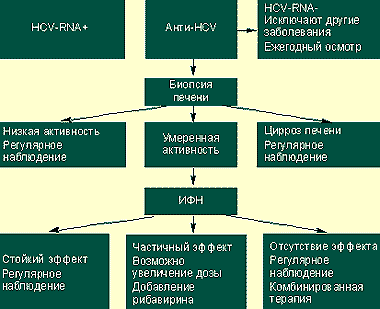 |
| Алгоритм ведения HCV-положительных больных |
Инфицирование ВГС приводит к развитию острого гепатита С, протекающего в манифестной (желтушной) или чаще в латентной (безжелтушной) формах, которые развиваются в соотношении 1:6. Около 17-25% больных острым гепатитом С выздоравливают спонтанно, у остальных 75-83% развивается хронический гепатит С. Большинство больных с биохимическими и иммунологическими признаками хронического гепатита имеют слабовыраженную или умеренную степень воспалительно-некротического поражения печени и минимально выраженный фиброз. Примерно у 26-35% больных хроническим гепатитом С в течение 10-40 лет развивается фиброз печени и может наступить смерть от цирроза печени и его осложнений. У 30-40% больных с циррозом печени высок риск заболевания раком печени.
Считается, что не более чем у 30% больных ВГС с минимальной морфологической активностью через 20 лет возможно развитие цирроза печени. Таким образом, больные, у которых при гистологическом исследовании биоптата печени выявляется наличие минимального воспаления и минимального фиброза, нуждаются в динамическом наблюдении.
Если персистенция РНК ВГС сохраняется более 6 месяцев, то спонтанное разрешение хронической HCV-инфекции маловероятно.
У большинства больных с хроническим гепатитом С заболевание протекает бессимптомно. Если жалобы существуют, то это чаще всего слабость, тупые боли в правом подреберье, тошнота, снижение аппетита, кожный зуд, артралгии и миалгии. Физикальный осмотр пациента помогает установить диагноз зачастую только на стадии цирроза печени.
Ассоциация хронического гепатита С с различными внепеченочными проявлениями — хорошо известный врачам факт. Наиболее вероятным для большинства заболеваний и синдромов, наблюдаемых при HCV-инфекции, представляется иммунный патогенез, хотя конкретные механизмы во многом еще не выяснены. Доказанные и предполагаемые иммунные механизмы включают:
- моно- или поликлональную пролиферацию лимфоцитов;
- образование аутоантител;
- отложение иммунных комплексов;
- секрецию цитокинов.
Частота иммуноопосредованных заболеваний и синдромов у больных хроническим гепатитом С достигает 23%. Наиболее характерны аутоиммунные проявления для больных с гаплотипом HLA DR4, который ассоциируется с внепеченочными проявлениями при аутоиммунном гепатите. Этот факт подтверждает гипотезу о триггерной роли вируса в инициации аутоиммунных процессов у генетически предрасположенного индивидуума.
Ассоциированные с продукцией или отложением иммуноглобулинов:
- Криоглобулинемия
- Лейкоцитокластерный васкулит
- Мембранозно-пролиферативный гломерулонефрит
- В-клеточная лимфома
- Плазмоцитома
- MALTома
- Тиреоидит
- Синдром Шегрена
- Гемолитическая анемия
- Тромбоцитопения
- Красный плоский лишай
Ассоциированные с неизвестным механизмом:
Выявление сывороточных аутоантител отражает наиболее частый феномен аутоиммунизации при HCV-инфекции, который диагностируют у 40-65% больных. Спектр аутоантител достаточно широк и включает ANA (до 28%), SMA (до 11%), анти-LKM-1 (до 7%), антифосфолипидные (до 25%), антитиреоидные (до 12,5%), ревматоидный фактор, анти-ASGP-R и др. Чаще всего титры этих антител не достигают диагностических значений, показательных для той или иной аутоиммунной патологии.
Анти-GOR являются антителами, специфичными для HCV-инфекции, и их выявляют не менее чем у 80% больных. Эпитоп, распознаваемый анти-GOR, локализуется на пока неидентифицированном ядерном белке, гиперэкспрессию которого наблюдают при гепатоцеллюлярной карциноме. Выработка анти-GOR ассоциирована только с HCV-инфекцией, но не с АИГ.
Аутоиммунные расстройства наблюдаются в среднем у 23% больных хроническим гепатитом С. Наиболее часто встречаются патология щитовидной железы.
Гистологическая картина не является патогномоничной, при этом достаточно часто выявляются характерные изменения. Отличительная особенность ее — лимфоидные агрегаты или фолликулы в портальных трактах, которые могут быть как изолированными, так и частью воспалительных изменений портальных трактов. По клеточному составу эти агрегаты напоминают первичные лимфоидные фолликулы в лимфатических узлах. Жировая дистрофия обнаруживается в 75% случаев. Кроме того, выявляются следующие характерные изменения: негнойный холангит с лимфоидной и плазмоклеточной инфильтрацией стенок протоков; лимфогистиоцитарная инфильтрация перипортальной зоны; слабовыраженные ступенчатые некрозы; мостовидные некрозы (обнаруживаются редко), пролиферация и активация сателлитных клеток печени, пролиферация эпителия желчных канальцев.
Отмечено, что индекс гистологической активности (ИГА) и индекс фиброза (ИФ) у больных хроническим гепатитом С с наличием жировой дистрофии достоверно выше, чем у пациентов без сопутствующей жировой дистрофии. У 93% больных с жировой дистрофией в гепатоцитах обнаруживался Core-протеин ВГС, при отсутствии жировой дистрофии — лишь у 39%. Этим фактом подчеркивается роль Core-протеина в развитии жировой дистрофии гепатоцитов.
Биопсия печени играет существенную роль в уточнении диагноза и оценке активности и стадии заболевания.
РНК ВГС можно определить в ткани печени методом ПЦР.
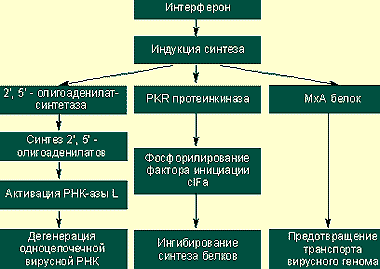 |
| Предотвращение вирусной транскрипции и трансляции |
Основная цель лечения — предотвратить прогрессирование заболевания.
Режим отдыха, диета и прием витаминов не оказывают лечебного действия.
Отбор пациентов для лечения. Показанием к назначению терапии интерфероном служит умеренное (но не минимальное) либо тяжелое воспаление и/или фиброз. Решение о лечении пациентов с циррозом печени принимают индивидуально в каждом конкретном случае. Больные, у которых гистологическая активность минимальна, должны находиться под динамическим наблюдением, так как они имеют хороший жизненный прогноз без лечения и очень низкий риск развития цирроза печени через 10-20 лет.
Факторы, связанные с благоприятным эффектом противовирусной терапии при хронической HCV-инфекции:
- Возраст моложе 45 лет
- Женский пол
- Отсутствие ожирения
- Срок инфицирования менее 5 лет
- Отсутствие коинфекции HBV
- Отсутствие иммунодепрессии
- Отсутствие алкоголизма
- Умеренное повышение АЛТ
- Отсутствие цирроза
- Низкое содержание железа в печени
- Низкий уровень HCV RNA в сыворотке
- Генотип 2 или 3
- Однородность популяции вируса
Больным с нормальным уровнем АЛТ и положительным тестом на HCV RNA без результатов гистологического исследования противовирусное лечение проводить не рекомендуется.
Основной препарат, эффективность которого в лечении гепатита С доказана, — это интерферон альфа (ИФα).
В настоящее время принята оптимальная схема монотерапии ИФ: разовая доза составляет 3 млн МЕ, ее вводят подкожно или внутримышечно 3 раза в неделю в течение 3 месяцев. Через 3 месяца необходимо исследовать РНК ВГС. Если результаты ПЦР положительные схему лечения меняют. Если же РНК не выявляется, лечение продолжают до 12 месяцев. Стойкий положительный ответ в этом случае регистрируется у 15-20% больных.
Оптимальная схема лечения хронического гепатита С в настоящее время — это комбинация ИФa и рибавирина.
Согласно рекомендации согласительной конференции Европейской ассоциации по изучению печени (1999), больным с впервые установленным диагнозом «хронический гепатит С» и показаниями к лечению необходимо назначать ИФa в комбинации с рибавирином следующими курсами:
- в течение 6 месяцев — при генотипах 2 и 3;
- в течение 6 месяцев — при генотипе 1 и низком уровне виремии;
- в течение 12 месяцев — при генотипе 1 и высоком уровне виремии.
Стойкий положительный ответ при комбинированном лечении ИФa с рибавирином наблюдается в 40-60% случаев.
Суточная масса рибавирина составляет 1000-1200 мг в зависимости от массы тела.
В последние годы для повышения эффективности интерферона применяют пегилирование, которое заключается в присоединении к молекуле интерферона полиэтиленгликоля. В итоге образуется ПЭГ-интерферон, имеющий более длительный период полураспада. Предварительные данные свидетельствуют о большей эффективности такого лечения по сравнению с терапией интерфероном альфа.
Одним из наиболее перспективных пегилированных интерферонов является пегасис — ПЭГ-интерферон альфа-2а, соединенный с разветвленной молекулой полиэтиленгликоля, молекулярная масса которого составляет 40 kDa, общий вес молекулы — около 60 kDa. Особенности химической структуры данного препарата определяют его фармакокинетические свойства и клиническую эффективность. Молекула полиэтиленгликоля присоединена к альфа-интерферону посредством самой стабильной амидной связи, это делает молекулу пегасиса чрезвычайно устойчивой к действию петидаз и позволяет выпускать препарат в виде растворенной и готовой к употреблению лекарственной формы. Особенностью молекулы полиэтиленгликоля является способность активно связывать несколько молекул воды, что создает вокруг химически структурной единицы пегасиса эффект «водного облака», делая ее устойчивой во внутренней среде и сообщая препарату относительно небольшой объем распределения. Это, в свою очередь, способствует тому, что отпадает необходимость в коррекции дозы препарата в зависимости от массы тела пациента: пегасис вводится один раз в неделю в дозе 180 мкг. Существенными преимуществами препарата пегасис являются значительно лучшая переносимость и меньшая частота побочных реакций, ассоциированных с системным действием альфа-интерферона, что значительно улучшает качество жизни пациентов, получающих лечение по поводу хронического гепатита С. Кроме того, в отличие от других пегилированных интерферонов пегасис не требует существенной коррекции дозы в зависимости от функционального состояния почек, что делает препарат незаменимым у пациентов с сопутствующей хронической почечной недостаточностью.
Клиническая эффективность пегасиса оценена солидными широкомасштабными многоцентровыми рандомизированными исследованиями. Было показано, что частота доказанного ответа на лечение значительно превышает таковую по сравнению с «короткими» интерферонами как в схемах монотерапии, так и в сочетании с рибавирином. Особенно впечатляющими в этой связи являются результаты этиопатогенетической терапии с использованием пегасиса в сочетании с рибавирином у так называемой «трудной» категории пациентов, имеющих морфологические проявления цирроза печени, 1b-генотип вируса, высокую виремию: частота доказанного ответа на лечение у данной категории пациентов при использовании пегасиса в сочетании с рибавирином может составлять около 40%, у иных категорий пациентов этот показатель может превышать 75%, что ранее было практически немыслимым результатом.
Имеются данные, свидетельствующие о положительном действии таких препаратов, как ремантадин, урсодеоксихолевая кислота, пегилированные интерфероны, препараты глициризиновой кислоты, однако эта информация нуждается в дальнейшей проверке.
По вопросам литературы обращаться в редакцию
источник