Для лечения печени наши читатели успешно используют Leviron Duo. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
Цирроз печени при гепатите С представляет собой диффузный фиброз с нарушением структуры печеночной ткани, в частности печеночной дольки. Нарушается структура и расположение ее сосудов. Образуются аномальные соединительнотканные рубцы и узлы. Структура печени изменяется необратимо.
Гепатит С занимает уверенное второе место среди прочих причин циррозов печени (19,1-25,1%). Его называют «ласковым убийцей». Он может протекать почти бессимптомно даже тогда, когда начинает формироваться вирусный цирроз печени. И только при его прогрессировании и осложнениях пациент обращается к врачу. Но уже может быть слишком поздно. Цирроз печени имеет постоянно прогрессирующее течение.
Хронические гепатиты и циррозы печени характерны постепенным изменением и перерождением клеток печени. Они не могут уже выполнять свои жизненно необходимые для организма функции и заменяются соединительной тканью. Она образует разной величины узлы. В зависимости от этого различают мелко узловой (до 3 мм) и крупно узловой (более 3 мм) вид цирротического изменения печени. Возможен и смешанный цирроз.
Из-за перерождения структуры печени и разрастания узлов нарушается кровоснабжение печени. Узлы смещают и сдавливают сосуды. При этом уменьшается или совсем исчезает их просвет. Сама же соединительная ткань прорастает сосудистыми коллатералями крайне скудно. В результате даже оставшиеся вполне жизнеспособными гепатоциты не могут принять нормальный объем крови и выполнять свои функции.
По сосудам, которые еще способны выполнить свои функции, ток крови идет под значительным давлением. Внутри печени формируются шунты, которые соединяют портальную вену с печеночными. В итоге повышается давление крови в воротной вене. Из-за переполнения и замедления кровотока воротной вены развивается обходное (коллатеральное) кровообращение. Происходит перераспределение крови в вены пищевода и верхней трети желудка. И уже в этих венах возрастает давление крови.
Постепенно в результате перерастяжения кровью, они варикозно изменяются, истончается их сосудистая стенка. Это опасно тяжелым и даже летальным осложнением — их разрывом и кровотечением.
Длительно вирусный цирроз печени может себя ярко не проявлять. Ощущение постоянной усталости и дискомфорта в подреберье справа и метеоризм люди списывают на утомительный ритм жизни и неправильное питание.
Степень выраженности проявлений цирроза зависит от его активности, стадии и общего состояния организма.
Возможно, но не обязательно, пожелтение кожных покровов и склер. Со временем деформируются концевые фаланги пальцев на руках по типу «барабанных палочек» и ногти по типу «часовых стекол».
Характерно похудание. Оно объясняется снижением массы жировой ткани и атрофическими изменениями мышц.
Цирроз печени проходит в три этапа:
- В течение фазы компенсации у пациента появляется варикозное расширение вен пищевода, изменяются показатели печеночных проб крови.
- В субкомпенсированной фазе больные жалуются на слабость и ощущение усталости без видимой на то причины. В животе постоянно присутствует метеоризм.
- В последней, декомпенсированной фазе, присоединяются осложнения цирроза. Эта фаза наиболее тяжелая. К большому сожалению, ее переживают не более 40% пациентов.
Все осложнения цирроза относятся к крайне тяжелым состояниям.
В результате снижения количества функционирующих клеток печени обезвреживание токсических веществ из кишечника, в том числе аммиака, уменьшается, и они попадают в кровь, а оттуда в другие органы и головной мозг. Присоединяется печеночная энцефалопатия.
Больные становятся тревожны, раздражительны, нарушается сон. Со временем присоединяется дезориентация в пространстве и времени, а также в собственном состоянии. Возможен переход в печеночную кому. Летальный исход при этом высоко вероятен.
Асцит характеризуется скоплением асцитической жидкости в брюшной полости. Физиологический объем ее около 150 мл. У больных с декомпенсированной стадией цирроза печени ее количество может достигать 10 и более литров. Эта жидкость начинает подпирать снизу грудную полость. В результате прогрессирует дыхательная и сердечная недостаточность. При асците длительность жизни больного составляет около 5 лет.
Она проявляется варикозными расширенными венами желудка и пищевода, увеличением селезенки. Переполняются и расширяются вены на коже живота («голова медузы»).
Присоединяются кровотечения из варикозных вен пищевода и желудка.
Кровотечение из пищеводных и желудочных вен является тяжелым, угрожающим жизни осложнением. Вены истончены, объем их велик, поэтому такой сосуд не спадается и затромбироваться ему крайне сложно.
Кроме того, в результате нарушения функции печени снижается и способность вырабатывать факторы свертывания крови. После первого случая кровотечения летальный исход происходит в 30-50% случаев. Из них больше чем у половины кровотечения повторяются.
Инфекционные осложнения. Ввиду снижения иммунитета больные, имеющие гепатит С и цирроз, склонны к развитию инфекционных осложнений. Возможно развитие спонтанного бактериального перитонита. Повышается температура, болит живот, нарастает ощущение вздутия живота. У 70 % больных, перенесших уже однажды такой перитонит, в течение года он повторяется. При лапаротомии причины перитонита, как правило находят.
У больных с вирусным циррозом печени определяется больший процент рака печени.
Полиорганная недостаточность — крайне тяжелое осложнение. В этом случае наблюдается недостаточность нескольких систем.
Лечение больных с диагнозом хронический гепатит и цирроз печени направлено то, чтобы замедлить развитие вирусного цирроза и симптоматическое уменьшение клинических проявлений.
Противовирусное лечение направлено на уменьшение титра гепатита С.
Для уменьшения портальной гипертензии, особенно при расширенных варикозных венах пищевода, рекомендуется снижение давления в воротной вене. Для этого используют б-адреноблокаторы или вазодилататоры. При рецидиве кровотечения из вен пищевода возможна эндоскопическая операция со склерозированием вен пищевода.
Для уменьшения асцита назначается диета без соли, мочегонные препараты.
При выраженном асците для выведения жидкости из брюшной полости проводится парацентез.
При варикозном кровотечении проводится гемостатическая (останавливающая кровь) терапия, восполняются недостающие факторы свертывания.
При неостанавливающемся кровотечении проводится баллонная тампонада пищеводных вен.
Показанием к хирургической операции является продолжающееся кровотечение при неэффективных прочих методах. Проводится заместительное переливание крови. При правильном лечении и ответственном отношении к нему больному удается симптоматически улучшить качество жизни и замедлить течение цирроза.
При циррозе печени здоровые клетки органа повреждаются и заменяются рубцовой тканью. Необратимые изменения в структуре печени при циррозе препятствуют нормальному потоку крови через печень. Это приводит к неспособности печени выполнять свои жизненно важные функции, такие как:
- производство белков и ферментов;
- регуляция уровня холестерина;
- хранение энергии;
- нейтрализация токсинов.
Цирроз является причиной серьезных осложнений: внутреннего кровотечения, почечной недостаточности, спутанности сознания, комы, накопления жидкости в организме, частых инфекций.
- Каковы основные причины цирроза печени?
- Всегда ли гепатит приводит к циррозу?
- Гепатит С – предвестник цирроза
- Гепатит В и риск развития цирроза
- Как диагностировать и лечить цирроз печени?
- Признаки заболевания:
- Как вылечить цирроз?
- Сколько живут с циррозом печени?
Множество различных факторов могут послужить толчком к развитию заболевания:
- самая распространенная причина цирроза — злоупотребление алкоголем.Клинически доказано, что потребление 100-300 мл крепких алкогольных напитков в день в течение 15 и более лет в 30 % случаев приводит к развитию цирроза;
- гепатит В и С — вирусные заболевания печени, которые чаще всего связывают с циррозом печени;
- многие наследственные расстройства приводят к накоплению токсичных веществ в печени, которые впоследствии повреждают ткани органа и вызывают цирроз. Например, гемохроматоз —наследственная патология, вызывающая избыточное накопление железа, или болезнь Вильсона — вызывает накопление меди.
- аномальные изменения иммунной системы. По неизвестным причинам, организм настраивает иммунную систему против своей собственной печени;
- осложнения язвенного колита, в результате которого большие желчные протоки вне печени воспаляются, и закупорка желчи приводят к частым инфекциям, а в конечном итоге — к циррозу;
- травмы желчных протоков могут привести к непроходимости и циррозу печени;
- врожденная желчная атрезия (отсутствие желчных протоков) – приводит к развитию заболевания;
- негативное воздействие лекарственных средств и токсинов, а также хроническая сердечная недостаточность (сердечный цирроз);
- паразитическое поражение печени — шистосомоз.
Не у всех пациентов с хроническим вирусным гепатитом развивается цирроз печени. Есть пять известных типов вирусных гепатитов, каждый из которых вызывается присущим только ему вирусом:
- острый гепатит А и острый гепатит Е не приводят к развитию хронического гепатита;
- острый гепатит B приводит к хронической форме заболевания примерно у 5 % взрослых пациентов. У некоторых из пациентов хронический гепатит данного типа прогрессирует в цирроз;
- острый гепатит D поражает людей, которые уже инфицированы вирусом гепатита B;
острый гепатит С переходит в хроническую форму примерно у 80 % взрослого населения.
У небольшой части этих пациентов (20-30 %) болезнь будет прогрессировать до цирроза печени, как правило, в течение многих лет.
Вирусный гепатит С также известен как «молчаливый убийца». Можно болеть гепатитом С много лет и не знать об этом. Возбудитель заболевания — вирус гепатита С – в первую очередь передается при применении внутривенных препаратов или переливании крови.
Гепатит С является основной причиной пересадки печени.
В целом около 300 миллионов населения мира страдают от вирусного гепатита С в настоящее время. Этот вирус является причиной почти половины случаев цирроза, которые заканчиваются смертью пациента, и более 70 процентов людей, страдающих от хронического гепатита, заражены им.
Симптомы всех заболеваний печени сходны между собой. Течение хронического заболевания характеризуется такими признаками, как:
- потеря аппетита;
- тошнота и рвота;
- потеря веса;
- увеличение печени;
- желтуха белков глаз и кожи;
- зуд;
- асцит – вздутие живота из-за скопления жидкости;
- рвота кровью;
- повышенная чувствительность к лекарственным средствам из-за неспособности печени нейтрализовать их;
- энцефалопатия (надвигающаяся кома) — психические изменения, дошедшие до глубокой растерянности и комы.
У четверти пациентов, инфицированных вирусом, впоследствии могут диагностировать цирроз печени. Некоторая часть пациентов более подвержена переходу к тяжелейшему заболеванию:
- употребление алкоголя влияет на развитие заболевания;
- инфицирование помимо вируса гепатита другими видами вирусов (например, ВИЧ) может увеличить риск цирроза печени;
- высокий уровень железа в крови влияет на появление осложнений;
- развитию цирроза подвержены люди старше 45 лет.
Своевременное и адекватное лечение предотвращает прогрессирование вирусного гепатита в цирроз.
Хронический вирусный гепатит B имеет длительную латентную (клинически бессимптомную) фазу, в течение которой симптомы не проявляются.
Это усложняет диагностику заболевания до развития симптомов поздней стадии, которые могут проявиться много лет спустя после начала болезни. Около 5 процентов инфицированных людей в конечном итоге получают осложнения в виде цирроза печени.
Хорошая новость заключается в том, что при своевременной диагностике заболевания оно успешно лечится. После полного выздоровления повторное заражение вирусом невозможно.
Исследования показали, что использование иммуностимулирующих препаратов позволяет достигать устойчивого вирусологического ответа, то есть снижения или полного прекращения вирусной нагрузки. Чтобы добиться стойкого регресса заболевания, важно проводить регулярный контроль показателей вирусной нагрузки для корректировки медикаментозного лечения.
Для лечения печени наши читатели успешно используют Leviron Duo. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
Диагноз цирроз печени можно поставить на основе физического осмотра и лабораторных исследований.
- увеличение и изменение структуры печени (видно при УЗИ);
- наличие маленьких красных паукообразных маркировок (телеангиэктазии) могут быть видны на коже, особенно в области груди;
- желтушность кожи и белков глаз;
- анализы крови часто показывают снижение белка в крови, повышенный уровень билирубина, патологический уровень ферментов печени, а также снижение свертываемости крови;
- специальные тесты на наличие вируса показывают положительный результат;
- повышенный уровень железа в крови свидетельствует о возможности гемохроматоза;
- сниженные показатели церулоплазмина в крови говорят о нарушении усвоения меди, и, следовательно, о болезни Вильсона;
- наличие аномальных антител (антинуклеарных антител) в крови предполагает аутоиммунный гепатит;
- подтверждение диагноза можно получить путем биопсии образца печени.
Лечение заболевания зависит от типа и стадии цирроза печени. Оно направлено на прекращение развития заболевания, устранение последствий поражения клеток органа и предотвращение развития осложнений.
При циррозе, вызванном вирусным гепатитом, назначают следующее лечение:
- воздержание от алкоголя;
- адекватная, здоровая диета;
- использование Интерферона и Рибавирина для повышения иммунного ответа на вирусные инфекции;
- прием дополнительных жирорастворимых витаминов;
- трансплантация печени с заменой пораженного органа.
Своевременно начатое лечение способствует переходу заболевания в стадию устойчивой ремиссии. Пациенту требуется длительное и систематическое лечение. Об исходе заболевания можно судить на основании регулярных лабораторных исследований.
Согласно опубликованным данным, регресс цирроза возможен в 53 % случаев заболевания даже при достижении ранее устойчивого вирусологического ответа.
Если заболевание вовремя диагностировано, цирроз может иметь благоприятный прогноз. Грамотное лечение способно замедлить прогрессирование цирроза печени. В запущенном случае единственным эффективным методом лечения является пересадка печени.
На продолжительность жизни пациента напрямую влияет своевременно начатое лечение. Сколько проживет пациент, зависит от тяжести заболевания, возраста и общего состояния организма.
Печень является одним из самых сложных органов. Печень может не только продолжать работать даже при частичном удалении органа, но и повторно восстановить те части, которые были удалены хирургическим путем.
Чрезмерное потребление алкоголя, гепатиты или другие заболевания могут разрушать клетки печени, лишая их способности к регенерации и выполнению важных жизнеобеспечивающих функций. Если вовремя диагностировать цирроз, течение заболевания можно остановить.
В нашем организме есть главные и вспомогательные органы: печень является главным. Она выполняет важные функции, без которых невозможно прожить. Печень — мощный паренхиматозный орган, она впитывает разные вещества и служит в качестве пищеварительной железы. Болезни печени часто связаны с нагрузкой на ее ткани. Этот орган имеет сложную структуру, и, несмотря на защитные оболочки, является крайне уязвимым.
Причин для заболевания печени достаточно много. Многие из них вызваны скорее неправильным образом жизни, чем внешними факторами.
- Патологии могут возникать при воздействии вирусов. Вирусы гепатита вызывают воспаление печеночной ткани. Наиболее благоприятный прогноз у гепатита А; самый опасный — гепатит В, который переходит в хроническую форму. Гепатит С часто выявляется при циррозе.
- Говоря о причинах печеночных патологий, нам стоит обозначить токсическое воздействие. Если организм получает определенную долю токсинов, внутренние органы страдают. Печень чувствительна к токсинам, поэтому заболевания, связанные с ней, могут возникать вследствие токсического воздействия. На печень плохо влияют промышленные пары, соединения металлов, химикаты. При воздействии раздражающих веществ этот орган увеличивается, но признаков болезни может не быть. Функциональные расстройства у каждого проявляются по-разному.
- Лекарства нагружают печень, однако не каждое из них обладает гепатотоксическим эффектом. Печень не любит средства с гормонами, антибиотики, лекарства для химиотерапии. Если человек периодически употребляет алкоголь, это отражается на функционировании печени. Спиртные напитки разрушают ее клетки, что приводит к развитию болезней. Злоупотребление алкоголем становится причиной цирроза.
- Патологии печени возникают на фоне паразитарных, инфекционных недугов (они часто связаны с другими органами). Такие болезни приводят к острым печеночным патологиям. У некоторых людей появляется кистозная деформация, чаще всего это обусловлено хроническим заболеванием.
- Во избежание патологий печени надо правильно питаться. Если человек переходит на жирные, соленые острые блюда, он рискует заболеть: помимо патологий печени, может развиться гастрит, язва двенадцатиперстной кишки. Даже при таких недугах печень будет нагружаться. При употреблении вредных продуктов желчь не отходит должным образом, она застаивается: такая проблема приводит к холангиту, желчекаменной болезни.
- Важную роль играет наследственная склонность. Если у ближних родственников были болезни печени, вероятна наследственная передача. У новорожденных малышей могут быть пороки развития печени: это тоже предрасполагающий фактор.
- Патологии, связанные с паренхиматозным органом, возникают из-за поражения печеночных артерий. Если острое заболевание сопровождается нагноением, гной проникает в воротную вену, в результате развивается тромбоз.
- Травмы живота приводят к печеночным патологиям, в связи с этим, их нужно вовремя лечить. Воспаление при травме может возникнуть из-за того, что в паренхиме скапливается вода.
- Патологии печени возникают на фоне ионизирующего излучения.
Нужно рассмотреть кожу при дневном свете: при патологиях печени она начинает желтеть. Помимо кожи, желтеют глазные яблоки. Подмышечные впадины могут обретать светло-коричневый окрас: такой недуг появляется из-за скопления меланина (бывает при билиарном циррозе). В зависимости от заболевания, паховая область может посинеть. Печеночные патологии сопровождаются зудом: он связан с застоем желчи. Желтушность кожи является основным признаком болезни, но помимо него, у человека возникает много неприятных симптомов:
- Кожная сыпь, появляющаяся на фоне, аутоиммунных процессов.
- Сосудистые звездочки — проявление цирроза.
- Сухость кожи.
- Трещинки в уголках рта.
- Синдром лакированного языка (указывает на дефицит витаминов).
- Синяки, трещины.
- Побеление ногтей (бывает при циррозе).
- Набухшие вены.
Кожные поражения, появляющиеся в результате поражения печени могут быть разнообразными. Какими они могут быть и почему, читайте подробно в этой статье.
Печень является важным пищеварительным органом, в ее отделах производится желчь. Соответственно, если у человека имеются болезни, связанные с печенью, нарушается функционирование ЖКТ. Возникают боли в зоне правого подреберья, в животе ощущается тяжесть. При патологиях печени появляется ощущение переполненности желудка. Сбои со стороны ЖКТ проявляются потемнением мочи. При циррозе печени талия увеличивается: многие люди думают, что это связано с газообразованием. На самом деле, органы брюшной стенки накапливают жидкость. При асците отекают ноги. У мужчин, употребляющих алкоголь, наблюдаются признаки феминизации: например, появление округлости груди (симптом также появляется при вирусном циррозе).
В этом видео вам расскажут об общих симптомах заболевания печени.
Для мужчин алкоголь особенно вреден, потому что преобразует мужские гормоны в женские. У мужчин меняется тип оволосения, увеличивается грудь, атрофируются яички. Постепенно развивается импотенция. Повышение уровня гормонов влияет на скелет: у человека часто случаются переломы. Вдобавок к этому, происходят нарушения со стороны ЦНС. Диабет может возникнуть на фоне патологий печени. При болезнях этого органа нарушается обезвреживание аммиака, в результате возникают неврологические расстройства.
Больные женщины с патологиями печени гораздо сильнее чувствуют хроническую усталость. У женщин нарушается аппетит, появляется бессонница. Если сонливость сменяется бессонницей, возможно, развивается печеночная энцефалопатия — смертельно-опасное заболевание. У некоторых больных дрожат пальцы, появляются судороги, нарушается память. В отдельных случаях проявляются эпилептические припадки. Проблемы со свертывающей способностью крови тоже могут быть. Помимо кровоизлияний, у пациентов возникают спонтанные или вызванные травмой кровотечения. Вышеперечисленные симптомы указывают на разные болезни. Для постановки диагноза нужно обратиться к терапевту, гастроэнтерологу и гепатологу. Судить о конкретном заболевании можно на основании анализов и с учетом клинической картины.
Мы выбрали самые распространенные болезни и расскажем вам об их симптомах.
Симптомы этого заболевания невозможно не заметить:
- у человека ухудшается общее самочувствие, наблюдается потеря в весе.
- если рак печени развивается у маленького ребенка, он заболевает анорексией.
- болезнь характеризуется потерей аппетита, поскольку у некоторых людей появляется отвращение к еде;
- люди с раком печени утомляются, у них присутствуют пищеварительные расстройства: понос, рвота, метеоризм.
- у некоторых больных возникают неприятные ощущения в желудке.
- появляются боли, которые часто появляются под ребрами, а при ходьбе усиливаются. С развитием рака боли появляются в подреберной области, причем, даже в спокойном состоянии;
- когда опухоль растет, живот увеличивается в объемах (при подозрении на рак нужно обратить внимание на этот признак);
- при онкологии повышается температура тела: она держится в пределах 38-ми градусов.
Подробнее о раке печени вы можете узнать в статье «Рак печени», посвященной этой теме.
В зависимости от формы цирроза, симптомы возникают на ранней или поздней стадии недуга. Большинство людей, обратившихся к врачу, не связывают тревожные симптомы с болезнями печени:
- недуг проявляется болями в правом подреберье: при физических нагрузках они нарастают;
- во избежание этого симптома надо соблюдать диету. Не следует употреблять, жирные, жареные, острые продукты. Алкоголь категорически запрещен;
- во рту появляется горечь.
- расстройство стула, повышенное газообразование;
- человек может становиться очень нервным.
Гепатит С часто проявляется внепеченочные симптомами. При таком заболевании нарушается работа сердца, возможно поражение разных органов: болевые ощущения могут локализоваться в почках, мочевом пузыре, поэтому этот вид гепатита обнаруживается при комплексной диагностике, однако общие признаки все же есть:
- отличительная черта заболевания — отсутствие желтушной кожи (симптом может появиться позже);
- гепатит С сопровождается слабостью, повышенной утомляемостью, снижением аппетита;
- человека начинают беспокоить боли в правом подреберье. Они связаны с застоем желчи и воспалительным процессом в желчном пузыре. Однако если поражается паренхима печени, человек не чувствует неприятных ощущений;
- при надавливании можно заметить, что печень и селезенка увеличены в размере;
- у человека может появляться распирающая боль в правом подреберье.
Как известно, этот недуг связан с отравлением рыбой и паразитами, находящиеся в ней, поэтому признаки довольно специфические:
- при описторхозе повышается температура, появляется ломота в мышцах и суставах, возникают боли в правом подреберье и напоминают колику;
- описторхоз сопровождается болями в эпигастральной (подложечной) области;
- периодически появляется рвота, тошнота, изжога, понос;
- на фоне этого недуга снижается аппетит, нарушается функционирование желудка, двенадцатиперстной кишки;
- если описторхоз переходит в хроническую форму, он становится похожим на холецистит, гастродуоденит и панкреатит;
- при надавливании ощущаются боли в желчном пузыре.
Болезнь не выявляется при визуальном осмотре: чтобы установить диагноз, нужно провести УЗИ и КТ, но если есть риск появления кисты, важно обратиться к врачу даже при малейших симптомах:
- боли в правом боку (если кисты крупные);
- в этой же области появляется чувство давления;
- киста печени сопровождается тошнотой, рвотой, расстройством со стороны пищеварительной системы;
- у человека пропадает аппетит, появляется слабость, одышка.
В зависимости от недуга, у человека могут возникнуть неинтенсивные распирающие боли: они будут располагаться в области правого подреберья. Такие боли указывают на то, что болезнь протекает вяло. Причины неприятных ощущений кроются в токсическом поражении. В этом случае боли появляются на фоне увеличения печени, деформации печеночной капсулы.
Сильные боли могут указывать на желчекаменную болезнь они локализуются на обширном участке правого подреберья. Помимо желчекаменной болезни, причиной сильных болей может быть травма печени.
Боль, которая можно охарактеризовать как «неприятные ощущения» могут быть вызваны проблемами с желчным пузырем. Печеночная ткань вынослива: она защищает орган от пагубного воздействия, но есть вирусы, которые нарушают ее целостность, в результате развивается заболевание. Симптомы патологии могут быть скрытыми. Она может прогрессировать, а человек не будет догадываться об этом (типичный пример — рак печени). Если больной поздно обратится к врачу, заболевания даст осложнения, а онкология закончится летальным исходом.
При болях в печени нужно принять медикаменты: спазмолитики. К их числу относятся Но-шпа и Дротаверин; есть фито-лекарства: Карсил и Эссенциале. При печоночной колике можно принимать народные средства, но у вас не должно быть аллергии!
При постоянных болях в печени нужно обратиться к гастроэнтерологу! Народные средства эффективны в совокупности с лекарствами, которые назначит врач. Среди народных средств выделяют следующие:
- Следует взять 50 мл растительного масла (лучше оливкового), развести со свежим грейпфрутовым соком в количестве 20 мл. Средство принимается за 2 часа до сна: перед приемом рекомендуется прочистить кишечник: можно сделать клизму. Если боли не отступили, надо выпить это же лекарство через 5 дней. Храниться оно в холодильнике.
- Моно сделать травяной отвар. Следует взять по маленькой ложке чистотела, мяты, корневищ пырея и листьев крапивы. Должно получиться 2,5 больших ложки сбора. Он заливается водой в количестве 500 мл. Выдерживается 12 часов. Утром нужно прогреть эту смесь и пить в течение дня.
- Следующее средство состоит из ромашки, зверобоя, тысячелистника, фиалки и мяты. Возьмите по 20 г каждого растения, залейте 200 мл кипятка, оставьте на пару часов. Лекарство принимается теплым: его можно пить утром и вечером.
- Для профилактики болезней печени принимается расторопша в таблетках. После принятия таблетки запиваются 2 ст. воды.
- Чтобы устранить боли в печени, можно съесть мед с маточным молочком. Следует взять мёд в количестве 60 гр и соединить с ложкой маточного молочка. Средство принимается после еды 1 раз в день.
- При болях в печени помогает яблочный сок с медом. Его нужно пить 2 раза в течение 30-ти дней. Благодаря витаминам в составе напитка, печень справляется с нагрузкой.
- Чтобы приготовить отвар с одуванчиком, нужно измельчить корни растения: 1 ч. л. заливается 200 мл воды. Такой отвар принимается за 25 минут до еды. Терапия длится месяц.
При необходимости врач назначает вибромассаж: он способствует оттоку желчи. Лечение болезней печени проходит по-разному: все зависит от стадии недуга и выраженности его симптомов. В большинстве случаев требуется стационарное лечение.
источник
Хронический вирусный гепатит С с исходом в цирроз и гепатоцеллюлярную карциному (клиническое наблюдение)
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
В статье представлен клинический случай пациента с диагнозом «цирроз печени, класс В по Чайлд — Пью» в исходе хронического гепатита С, пролеченного препаратами интерферона и рибавирина в течение 18 мес. На фоне противовирусной терапии РНК вируса гепатита С стала отрицательной через 8 нед. и оставалась стойко отрицательной на протяжении 2-х лет. В последующем на фоне стресса, через 3 мес. после окончания лечения возник рецидив хронического гепатита С с умеренной биохимической и вирусологической активностью. Через 6 мес. после рецидива при ультразвуковом исследовании был заподозрен рак печени, было получено гистологическое подтверждение. Через несколько месяцев у пациента развилось кровотечение из варикозно расширенных вен пищевода (ВРВП), а еще через 1 мес. возникло повторное кровотечение из ВРВП. Пациент наблюдался и лечился в реанимационном отделении. Появились асцит, двусторонняя пневмония, лихорадка, лейкоцитоз. Состояние больного прогрессивно ухудшалось, и при нарастающем психомоторном возбуждении, прогрессирующей дыхательной и сердечно-сосудистой недостаточности была зафиксирована биологическая смерть.
Имело место расхождение диагнозов, категория II. Причиной летального исхода стала гнойная интоксикация в результате перфорации язв пищевода, гнойного медиастинита с эмпиемой плевры слева.
Ключевые слова: хронический гепатит С, цирроз печени, гепатоцеллюлярная карцинома.
Для цитирования: Макашова В.В., Омарова Х.Г., Хохлова О.Н., Лукашенко Т.Н. Хронический вирусный гепатит С с исходом в цирроз и гепатоцеллюлярную карциному (клиническое наблюдение) // РМЖ. Медицинское обозрение. 2018. №8(II). С. 92-96
Chronic hepatitis C virus with the outcome of cirrhosis and hepatocellular carcinoma (clinical observation)
V.V. Makashova 1,2 , H.G. Omarova 1 , O.N. Hohlova 1 , T.N. Lukashenko 3
1 Central Research Institute of Epidemiology, Moscow
2 Clinical Hospital for the Infectious Diseases, Moscow
3 Outpatient Clinic № 5, Moscow
The article presents a clinical case of a patient with a diagnosis of liver cirrhosis of Child-Pugh class B in the outcome of chronic hepatitis C, treated with interferon and ribavirin for 18 months. In the course of antiviral therapy, RNA of the hepatitis C virus became negative after 8 weeks and remained steadily negative for 2 years. Subsequently, on the background of stress, 3 months after the end of treatment, a relapse of chronic hepatitis C appeared with moderate biochemical and virological activity. 6 months after the relapse, a liver cancer was suspected during an ultrasound examination and histological confirmation was obtained. After a few months, hemorrhage from esophageal varicose veins dilatation (EVVD) occurred in the patient, and after another 1 month, there was repeated hemorrhage from EVVD. The patient was monitored and treated in the intensive care department. Ascites, bilateral pneumonia, fever, leukocytosis appeared. The patient’s condition progressively worsened and with increasing psychomotor agitation, progressive respiratory and cardiovascular insufficiency, biological death was recorded.
There was a divergence of diagnoses, category II. The cause of the fatal outcome was purulent intoxication, as a result of ulcers perforation of the esophagus, purulent mediastinitis with pleural empyema on the left.
Key words: chronic hepatitis C, cirrhosis, hepatocellular carcinoma.
For citation: Makashova V.V., Omarova H.G., Hohlova O.N., Lukashenko T.N. Chronic hepatitis C virus with the outcome of cirrhosis and hepatocellular carcinoma (clinical observation) // RMJ. Medical Review. 2018. № 8(II). P. 92–96.
В статье представлен клинический случай пациента с диагнозом «цирроз печени, класс В по Чайлд — Пью» в исходе хронического гепатита С с развитием гепатоцеллюлярной карциномы
Пациент Т., 1948 г. р., 22.01.2009 г. обратился в поликлинику к инфекционисту в связи с лейкопенией (до 3,2×10 9 /л), тромбоцитопенией (60–120×10 9 ). Со слов пациента, антитела к HCV впервые выявлены в 1998 г. Не обследовался, не лечился. Впервые обследовался в поликлинике ФСБ № 5 в 2009 г., выявлена РНК HCV+, 1в генотип, вирусная нагрузка — 1,3×10 6 коп/мл.
Жалобы на периодически возникающую слабость и утомляемость.
Перенесенные заболевания: 1972 г. — аппендэктомия, 1992 г. — острый вирусный гепатит А, 1995 г. — оперирован по поводу синдрома Меллори — Вейса. В это же время были гемотрансфузии. 1996 г. — грыжесечение, 1997 г. — повторное грыжесечение, 2004 г. — язвенная болезнь 12-перстной кишки, 2005 г. — правостороннее воспаление легких, хронический бронхит, 2007 г. — повторная пневмония, 2007 г. — сильное кровотечение при удалении зубов, гипертоническая болезнь, сахарный диабет 2-го типа.
Аллергоанамнез — не отягощен.
Наследственность: у отца — цирроз печени алкогольного генеза, у матери — инсульт, у брата — хронический вирусный гепатит В.
Вредные привычки: не курит, алкоголь употреблял часто, но немного (со слов), крепкие напитки (виски, коньяк).
Объективно при осмотре: сосудистые звездочки в области грудной клетки, умеренная пальмарная эритема, иктеричность склер. Печень пальпаторно и перкуторно увеличена — выступает на 4–5 см ниже реберной дуги, селезенка не пальпируется.
Рост — 173 см, вес — 80 кг.
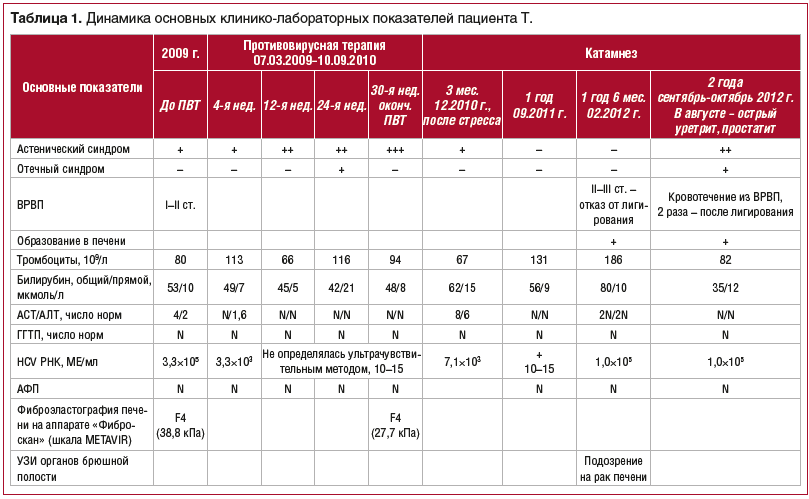
Динамика основных показателей общего и биохимического анализов крови, данные ПЦР-диагностики представлены в таблице 1.
02.02.2009 г. проведено ультразвуковое исследование (УЗИ), выявлены диффузные изменения в печени, увеличение левой доли печени (8,4 см, норма — до 7,0 см), хронический бескаменный холецистит, желчный пузырь деформирован с перегибом в теле; умеренное увеличение селезенки (13,8×6,9 см), киста правой почки.
11.03.2009 г. Фиброэластография печени: F4 по шкале METAVIR (кПа — 38,8).
Эзофагогастродуоденоскопия (ЭГДС) 20.03.2009 г. — варикозно расширенные вены пищевода (ВРВП) 1–2 ст., эрозивный бульбит.
С 07.03.2009 г. по 10.09.2010 г. проводилось противовирусное лечение препаратами интерферон альфа-2b 1 млн через день и рибавирин 800 мг/сут (по весу); постоянно получал урсодезоксихолевую кислоту 750 мг/сут.
Через 8 нед. противовирусной терапии РНК HCV не определялась (менее 500 МЕ/мл), аланинаминотрансфераза (АЛТ) и аспартатаминотрансфераза (ACT) — в норме, билирубин общий — до 42 мкм/л.
Через 6 мес. после начала противовирусной терапии состояние ухудшилось, в связи с чем был госпитализирован в ГБУЗ ИКБ № 2 ДЗМ, где находился с 08.09.2009 г. по 27.09.2009 г. Впервые выявлен асцит, по данным УЗИ увеличены печень (15 см — правая доля), селезенка (143×67 мм), Vena portae — 15 мм, селезеночная вена — 10 мм. Проведено лечение: альбумин 100 мл № 3, адеметионин, мочегонные препараты (спиронолактон, фуросемид), пропранолол 20 мг. Самочувствие и состояние значительно улучшились. В последующий период наблюдения асцит не отмечался.
Через 1,5 года стандартной противовирусной терапии (интерферон короткого действия и рибавирин) пациент жалоб не предъявлял, достигнута положительная динамика по данным УЗИ, фиброэластографии печени (эластичность печени снизилась с 38,8 до 27,7 кПа), печеночные трансаминазы и количество тромбоцитов нормализовались. РНК HCV стойко не определялась.
У пациента через 2 мес. после окончания противовирусной терапии был стресс, а через 3 мес. однократно была обнаружена РНК HCV (7,1×10 3 МЕ/мл) от 02.12.2010 г., повысилась активность ферментов (8 N).
Назначен гепатопротектор (расторопши пятнистой плодов экстракт 140 мг/сут). Через 1 мес. активность трансаминаз стала нормальной, РНК HCV не определялась ультрачувствительным методом в течение 1 года 3 мес. В марте 2012 г. при повышении активности ферментов в 2,5 раза вновь была обнаружена РНК вируса гепатита С — 1,0×10 5 МЕ/мл.
Были проанализированы показатели иммунного статуса в динамике — на фоне противовирусного лечения при декомпенсации ЦП, при окончании противовирусной терапии и в катамнезе. Выявлено, что на фоне противовирусной терапии в период декомпенсации ЦП отмечалось увеличение Т-хелперной активности при снижении цитотоксических Т-лимфоцитов, при этом иммунорегуляторный индекс оставался выше нормы. Одновременно отмечалось снижение показателей В-лимфоцитов, натуральных киллеров (NK-клеток) и TNK-клеток (Т-клетки с функциями NK-клеток), что говорит о нарушении не только гуморального, но и клеточного звена иммунного ответа и может свидетельствовать о формировании иммунодефицита. На фоне длительной противовирусной терапии пациент был обследован повторно через 1 год 3 мес. Обнаружено, что показатели всех субпопуляций Т-лимфоцитов нормализовались. Кроме этого, отмечалось выраженное увеличение показателей В-лимфоцитов (до 30%) и антител класса IgG (увеличены в 2 раза по сравнению с показателями после 6-месячного лечения). Однако клеточное (NK-клетки) звено иммунитета оставалось несостоятельным. Показатели катамнестического третьего иммунологического статуса не отличались от таковых при предыдущем исследовании. Такое медленное восстановление иммунной системы можно объяснить вновь обнаруженной репликацией HCV и ухудшением биохимических показателей.
Планировался курс повторной противовирусной терапии ХГС.
Однако 28.02.2011 г. возникла клиническая картина кровотечения из ВРВП (на фоне астенических явлений: резкое снижение уровня гемоглобина — до 92 г/л, эритроцитов — до 3,6×10 12 /л). Пациент отказался от консультации и госпитализации в отделение портальной гипертензии, необходимой для склерозирования ВРВП.
При ЭГДС от 04.03.2011 г. — ВРВП 2–3 ст., на момент осмотра — без признаков состоявшегося кровотечения или картины нестабильного местного гемостаза. Поверхностный гастродуоденит, очаговый эрозивный гастрит выходного отдела без геморрагического компонента.
Пациент постоянно получал урсодезоксихолевую кислоту 750 мг, карведилол 125 мг.
На УЗИ от 10.04.2012 г. (предыдущее — от 06.09.2011 г.)
впервые выявлено образование в правой доле печени до 3 см, смешанной эхогенности, с нечеткими контурами.
13.04.2012 г. Компьютерная томография (КТ): при и после в/в болюсного контрастирования: в артериальную фазу контрастирования на границе 7–8 сегмента и в 6 сегменте печени определяются 3 округлой формы зоны активного и равномерного накопления контрастного препарата: 1,2×0,9 см, 1,9×1,7 см и 0,8×0,7 см соответственно. Заключение: основное заболевание — ЦП в исходе ХГС. КТ-признаки 3 образований правой доли печени на фоне жирового гепатоза (дифференцировать между узлами регенерации и бластоматозным процессом); умеренно выраженная портальная гипертензия (спленомегалия, умеренное расширение воротной вены (1,4 см), вен желудка и селезенки), аномалия развития почек (подковообразная почка), псевдокисты поджелудочной железы.
24.04.2012 г. Магнитно-резонансная томография органов брюшной полости. Контрастное усиление: гадобутрол. Заключение: косвенные признаки ЦП, портальная гипертензия, спленомегалия. Зоны измененного MP-сигнала в правой доле печени, вероятно, узлы-регенераты. Образование тела поджелудочной железы, вероятно, серозная цистаденома.
В период обследования пациент жалоб не предъявлял, осмотр — без динамики.
Для исключения бластоматозных образований печени на фоне ЦП в исходе ХГС (стадия репликации вируса) и решения вопроса о возможности продолжения противовирусной терапии пациент был направлен на биопсию печени.
С 23.05.2012 г. по 28.05.2012 г. находился в хирургическом отделении ГКБ им. С.П. Боткина для проведения биопсии образования печени под УЗ-наведением.
Макроскопическое описание материала от 24.05.2012 г.:
дифференциальный диагноз между гепатоцеллюлярной аденомой и высокодифференцированным гепатоцеллюлярным раком (ГЦР). Микроскопическое описание материала от 07.06.2012 г.: фрагмент ткани печени с признаками цирротической трансформации и микроскопическая фрагментированная частица, крайне подозрительная по высокодифференцированной ГЦК с очагами некроза (проконсультировано профессором Г.А. Франком).
Для определения тактики дальнейшего ведения пациент направлен на консультацию в НИИ скорой помощи им. Склифосовского.
В июле пациент уехал в отпуск, в Крым. 18.07.2012 г. отметил подъем температуры до 39 °С, озноб, боли и увеличение правого яичка, рези и боли при мочеиспускании, кровь в конце акта мочеиспускания. Обратился к урологу. Диагноз: острый уретрит, острый простатит. Получал амоксициллин и клавулановую кислоту в течение 5 дней. Состояние улучшилось — уменьшились боли при мочеиспускании и отек яичка.
При возвращении госпитализирован в урологическое отделение ЦВКГ, где находился с 14.08.2012 г. по 31.08.2012 г. с диагнозом «острый простатит, уретрит». В урологическом отделении было кровотечение из ВРВП, остановленное консервативно. После выписки кровотечение из ВРВП повторилось. Был повторно госпитализирован в хирургическое отделение ЦКВГ, где находился с 31.08.2012 г. по 17.09.2012 г. В отделении состояние стабильное, проводилась консервативная терапия: гемостатики (этамзилат, менадиона натрия бисульфит), октреотид, противоязвенная терапия, гепатопротекторы, препараты железа. Рецидива кровотечения не отмечалось. Состояние улучшилось, стул — без признаков мелены, сохранялась анемия, уровень гемоглобина — в пределах 83–92 г/л.
Больной выписан на амбулаторное наблюдение с диагнозом «ЦП, класс В по Чайлд — Пью в исходе ХГС. Портальная гипертензия: ВРВП 4 ст., гепатомегалия. Подозрение на ГЦК в 5 сегменте печени. Состоявшееся кровотечение из ВРВП от 31.08.2012 г. Хроническая анемия смешанного генеза. Гастропатия. Доброкачественная гиперплазия предстательной железы. Аномалия развития верхних мочевых путей: подковообразная почка, без нарушения уродинамики ВМП».
В начале октября 2012 г. в ГКБ № 57 проведено эндоскопическое лигирование вен пищевода по поводу ВРВП.
12.10.2012 г. у больного появилась клиническая картина желудочно-кишечного кровотечения, в связи с чем в экстренном порядке был госпитализирован в ЦКВГ ФСБ РФ.
При поступлении — состояние средней тяжести. Кожные покровы бледные, сухие, теплые. Тошноты, рвоты нет. Температура — 36,5 °С. В сознании, адекватен, ориентирован в пространстве и времени. ЧСС — 90 уд/мин. АД — 120/70 мм рт. ст. ЧДД — 17/мин. Дыхание проводится во все отделы. Язык влажный, обложен белым налетом. Живот мягкий, не вздут, не увеличен, симметричный, участвует в акте дыхания. При пальпации — безболезненный во всех отделах. Перистальтика ослаблена. Дизурии нет. Газы отходят.
Вечером этого же дня пациент отметил рвоту кровью, установлен зонд Блэкмора. В связи с тяжестью состояния больной был переведен в реанимационное отделение. Проводилась инфузионная, спазмолитическая, гемостатическая, антисекреторная терапия. После стабилизации состояния больной переведен в хирургическое отделение. Зонд Блэкмора удален. Состояние пациента оставалось стабильным. Но 19.10.2012 г. появились боли в животе. Проведено УЗИ органов брюшной полости, отмечалось расширение общего печеночного протока, панкреатического протока. При рентгенографии органов брюшной полости патологии не выявлено. На фоне проводимой инфузионно-спазмолитической терапии боли в животе были купированы. Однако 21.10.2012 г. у пациента возник рецидив кровотечения из ВРВП. Переведен повторно в реанимационное отделение, установлен зонд Блэкмора. При динамическом УЗИ органов брюшной полости выявлено большое количество свободной жидкости. Выполнена КТ органов брюшной полости: Заключение: асцит, киста поджелудочной железы, гемангиома 4 сегмента правой доли печени. Двусторонний гидроторакс. Нижнедолевая пневмония. Инфильтрации парапанкреатической клетчатки поджелудочной железы не выявлено. Отмечалось большое количество свободной жидкости в брюшной полости.
В анализе крови — лейкоцитоз до 27×10 9 /л. Для исключения острого панкреатита с ферментативным перитонитом, воспалительных заболеваний органов брюшной полости, пареза кишечника 23.10.2012 г. проведена диагностическая лапароскопия. Интраоперационно выявлен асцит. Другой патологии не выявлено. Выполнены санация и дренирование брюшной полости. На фоне проводимого лечения у пациента отмечались эпизоды рецидива кровотечения из ВРВП. Проводились плазмо- и гемотрансфузии. Несмотря на последующую интенсивную терапию, направленную на коррекцию волемических нарушений, состояние больного прогрессивно ухудшалось. Отмечались психомоторное возбуждение, прогрессирующая дыхательная недостаточность, гипотония. 26.10.2012 г. в 18:30 пациент переведен на ИВЛ, к лечению добавлены вазопрессоры. На фоне прогрессирующей сердечно-сосудистой недостаточности в 19:00 зафиксирована асистолия. Начаты реанимационные мероприятия в полном объеме, интенсивная терапия. Все мероприятия в течение 45 мин были неэффек-
тивны. В 19:45 зафиксирована биологическая смерть.
В отделении причиной смерти указана острая сердечно-сосудистая недостаточность, развившаяся на фоне прогрессирующей полиорганной, сердечно-сосудистой недостаточности.
Основной диагноз: ЦП, класс С по Чайлд — Пью.
Осложнение основного диагноза: портальная гипертензия: ВРВП 4 ст., гепатомегалия. Состоявшееся кровотечение из варикозно расширенных вен пищевода от 12.10.2012 г., 21.10.2012 г., 25.10.2012 г. Постгеморрагическая анемия тяжелой степени. Гастропатия. Асцит. Печеночная недостаточность.
Сопутствующие заболевания: двусторонняя нижнедолевая пневмония. Двусторонний гидроторакс. ИБС: атеросклеротический кардиосклероз, гипертоническая болезнь 2 ст. Язвенная болезнь 12-перстной кишки. Киста поджелудочной железы. Гемангиома 4 сегмента печени.
Патологоанатомический диагноз (после гистологического исследования).
Основное комбинированное заболевание:
Мелкоузловой ЦП.
Операция диагностической лапароскопии 23.10.2012 г.
по поводу подозрения на острый панкреатит с санацией и дренированием брюшной полости.
Фоновые заболевания:
Сахарный диабет (по клиническим данным).
ХГС (по клиническим данным).
Осложнения: варикозное изменение вен пищевода. Эрозивно-язвенный эзофагит нижней трети пищевода с перфорацией в ткани заднего средостения. Гнойный
медиастинит заднего средостения. Эмпиема плевры слева — 3,3 л гнойного экссудата (по данным посмертного бактериологического исследования от 31.10.2012 г.). — Klebsiella pneumoniae, Enterococcus faecalis, Staphylococcus epidermidis. Ателектаз левого легкого. Правосторонний гидроторакс — 0,5 л. Мелкоочаговая бронхопневмония в нижней доле правого легкого. Малокровие оболочек головного мозга и внутренних органов. Асцит (0,4 л). Гепато- и спленомегалия (1375 и 355 г). Мелкоочаговые инфаркты в печени и предстательной железе. Отек правого легкого. Отек головного мозга. Паренхиматозная дистрофия миокарда, почек.
Сопутствующие заболевания: атеросклероз аорты (IV стадия, 3 степень). Мелкоочаговый кардиосклероз миокарда стенок левого желудочка, атеросклероз венечных артерий (IV стадия, 3 степень). Гипертоническая болезнь: эксцентрическая гипертрофия миокарда, стенок левого желудочка (стенка левого желудочка — 1,3 см, масса сердца — 395 г), артерио-артериоло-нефросклероз. Мелкоузловая гиперплазия коркового слоя надпочечников. Железистый тип нодозной гиперплазии предстательной железы. Киста поджелудочной железы. Сахарный диабет 2-го типа (по клиническим данным). Давние операции: аппендэктомия (1972 г.), верхнесрединная лапаротомия (по поводу синдрома Меллори — Вейса, 1995 г.).
Таким образом, при аутопсийном исследовании подтвердился диагноз ЦП и обнаружены: гнойный медиастинит, левосторонняя эмпиема плевры, развившиеся в исходе эрозивно-язвенного эзофагита на фоне сахарного диабета.
Непосредственной причиной смерти больного явилась гнойная интоксикация.
Сличение диагнозов: расхождение диагнозов. Категория II. Причина субъективная — не учтена роль сахарного диабета в развитии гнойных осложнений. Не диагностированы смертельные осложнения: перфорация язв пищевода, гнойный медиастинит с эмпиемой плевры слева. Эндоскопическое исследование проводилось однократно в день поступления, рентгенологически не выявлены тяжелые гнойно-деструктивные изменения в левой плевральной полости и заднем средостении. Причина объективная — тяжесть состояния больного.
источник
Ретроспективное изучение хронического гепатита С (ХГ С) позволяет говорить, что в среднем у 20% больных в течение 20–30 лет развивается цирроз печени (ЦП). Скорость формирования цирроза зависит от ряда факторов.
Ретроспективное изучение хронического гепатита С (ХГ С) позволяет говорить, что в среднем у 20% больных в течение 20–30 лет развивается цирроз печени (ЦП). Скорость формирования цирроза зависит от ряда факторов. Медленное нарастание фиброза при ХГ С наблюдается у женщин молодого возраста в отсутствие таких факторов, как стеатоз печени, синдром перегрузки железом, злоупотребление алкоголем. Ряд причин обусловливает быстрое формирование ЦП: пожилой возраст при инфицировании, мужской пол, систематическое употребление алкоголя более 50 г/сут, наличие коинфекции вирусов гепатита В и/или ВИЧ, избыточная масса тела (> 28 кг/мІ), гетерогенность по гену гемохроматоза, полиморфизм генов ряда цитокинов, играющих ключевую роль в фиброгенезе. Среднее время развития ЦП у лиц, инфицированных в возрасте после 40 лет и злоупотребляющих алкоголем, составляет 13 лет, а у молодых женщин в отсутствие приема алкоголя ЦП формируется через 42 года. У 32% больных ХГ С протекает стабильно и не сопровождается прогрессированием болезни.
Важным фактором фиброгенеза является сохраняющаяся активность ХГ С по лабораторным данным и морфологическим признакам. У больных со стойко нормальным уровнем трансаминаз сыворотки риск развития ЦП С составляет 5%, в то время как наличие 3–5-кратного повышения АЛТ сыворотки ассоциируется с быстрым формированием ЦП С у 50% больных. Показано также, что факторами риска прогрессирования фиброза являются: наличие фиброза в ткани печени при первой биопсии, стеатоз печени и возраст больных. Быстрота прогрессирования фиброза определяется предшествующим фиброзом, стеатозом и лобулярным гепатитом [1]. При ХГ С низкой степени активности (ИГА по Knodell 4–8 баллов) риску развития ЦП С подвержены 7–10% больных, при ХГ С высокой степени активности (ИГА — более 13 баллов) у 71% больных цирроз может развиться уже через 7 лет. Проспективное изучение 404 больных компенсированным ЦП С показало, что за 85,7±36 мес наблюдения у 28% больных развивается хотя бы одно осложнение ЦП С, в том числе гепатоцеллюлярная карцинома (ГЦК) — у 19%, асцит — у 17%, кровотечение из варикозно расширенных вен пищевода (ВРВП) — у 5%, декомпенсация ЦП С (Чайлд В/С) — у 17%, энцефалопатия — у 2% [2].
Высокая частота развития ЦП С при хронической HCV-инфекции и риск серьезных осложнений в этой группе больных определяют задачи противовирусной терапии (ПВТ). Основная задача лечения — эрадикация вируса гепатита С и достижение стойкой ремиссии ХГ С, однако возможности достижения устойчивого вирусологического ответа (УВО) у больных ЦП С значительно ниже, чем при ХГ С. Исследования последних лет показали, что ПВТ способствует уменьшению выраженности фиброза, поэтому у больных ЦП С без вирусологического ответа целью противовирусного лечения является замедление прогрессирования болезни, снижение риска декомпенсации ЦП и развития его осложнений, в том числе ГЦК, В-клеточной лимфомы, криоглобулинемии, внепеченочных проявлений, портальной гипертензии и печеночно-клеточной недостаточности.
Представляют интерес исследования M. Curry и соавторов (2005), изучивших влияние длительной терапии пегинтерфероном α-2b в малых дозах на динамику портальной гипертензии у больных ХГ С со стадией фиброза F3 и ЦП С (F4). В исследование COPILOT были включены 267 больных, получавших колхицин 0,6 мг 2 раза в день, и 270 больных, которым проводится лечение пегинтроном 0,5 мкг/кг 1 раз в неделю в течение 4 лет. Обе группы были представлены больными, не ответившими на комбинированную терапию интерфероном и рибавирином. 83% больных в каждой группе имели ЦП С, у 40% из них имелись признаки портальной гипертензии, выявленные при эндоскопии (ВРВП или портальная гастропатия). ЭГДС проводилась с интервалом в 2 года. Опубликованы предварительные результаты исследования.
У 5 больных ЦП С, не получавших β-блокаторы с целью коррекции портальной гипертензии, до лечения пегинтроном провели измерение портального давления. Спустя 2 года лечения при повторной ЭГДС новые ВРВП появились у 11 из 66 больных, получавших колхицин, и сохранялись у 5 из 66 больных, получавших монотерапию пегинтроном. У всех 5 больных первоначальное портальное давление составляло 15 мм рт. ст., через 24 нед лечения составило в среднем 6 мм рт. ст. Кровотечение из ВРВП через 2 года отмечено у 11 (9%) больных, получавших колхицин, и у одного (1%) больного, получавшего пегинтрон. Асцит и печеночно-клеточная недостаточность также чаще выявлялись при лечении колхицином (20 больных), чем пегинтроном (13 больных). Таким образом, длительное лечение малыми дозами пегинтрона больных ЦП С может замедлить формирование ВРВП, снизить портальное давление, предотвратить кровотечение из ВРВП и другие осложнения портальной гипертензии у больных ЦП С, не достигших УВО на предшествующую комбинированную терапию интерфероном и рибавирином [3].
В последние годы ПВТ претерпела существенные изменения: с 2000 г. комбинированная терапия пегилированными интерферонами α-2a и 2b и рибавирином заняла ведущие позиции в лечении ХГ С и компенсированного ЦП С. Изучены прогностические факторы ответа на лечение, появились возможности коррекции ряда побочных эффектов ПВТ, что позволило достичь УВО у 56–63% больных ХГ С, включенных в лечение. Приверженность больных к лечению, адекватные дозы препаратов и длительность ПВТ позволяют повысить УВО до 72–75% [4, 5]. Наибольший эффект комбинированной терапии ХГ С отмечается у больных с генотипами 2 или 3 HCV: непродолжительный курс лечения (24 нед) при высокой приверженности к лечению пегилированными ИФН α и рибавирином позволяет достичь успеха в 84–94% случаев.
Повышению эффективности ПВТ способствуют обязательное назначение комбинированной ПВТ (ИФН α и рибавирин) первичным больным, выбор оптимальных доз препаратов и длительности лечения в зависимости от генотипа HCV и вирусной нагрузки. Кроме того, необходима коррекция факторов неблагоприятного ответа на лечение (стеатоз, холестаз, синдром перегрузки железом) и побочных эффектов ПВТ (депрессия, гемолитическая анемия при применении рибавирина, лейко- и тромбоцитопения при лечении ИФН α, дисфункция щитовидной железы). Субоптимальные дозы препаратов, используемых при проведении ПВТ, и недостаточная продолжительность лечения способствуют формированию группы резистентных к противовирусной терапии больных ХГ С, что делает необходимым проведение повторных курсов ПВТ. Так, было показано, что при 48-недельной комбинированной ПВТ УВО достигалось у 72% больных с генотипом 1b HCV и низкой вирусной нагрузкой. Последующее обострение ХГ С отмечалось у 3% пациентов. В то же время при 24-недельной ПВТ УВО отмечался только у 51% больных указанной категории, причем обострение ХГ С и возобновление виремии через 6–18 мес после окончания ПВТ наблюдались у 40% пациентов.
Несмотря на достижения последних лет, остаются категории трудных для лечения больных ХГ С, к которым относятся пациенты с генотипом 1 HCV и высокой вирусной нагрузкой и больные ЦП С.
Генотип 1 HCV и высокая вирусная нагрузка оказались независимыми прогностическими факторами слабого ответа на лечение. Причины этого до конца не ясны. Изучается значение мутаций в E2 и NS5A генах HCV (неструктурный регион NS5A определяет чувствительность к интерферону). Элиминация гепатоцитов, инфицированных генотипом 1 HCV, в процессе ПВТ происходит медленнее, чем при других генотипах. В первые 1–2 нед терапии вирусная нагрузка снижается на 1,6 log копий/мл при генотипе 1 HCV и на 2,9 log копий/мл при генотипе 2. Скорость гибели инфицированных гепатоцитов составляет 0,1 в день у больных с генотипом 1 и 0,26 в день при генотипе 2, что объясняется различиями в иммунном ответе у больных и дает основание для обсуждения необходимости более агрессивной и, возможно, более длительной ПВТ при генотипе 1 HCV [5].
Стратегия лечения больных ЦП и ХГ С, инфицированных генотипом 1 HCV и имеющих высокую вирусную нагрузку, тесно связана. УВО при лечении ИФН α в стандартном режиме больных ХГ С с генотипом 1 HCV не превышает 10% независимо от сроков лечения — 24 или 48 нед. При использовании комбинированной терапии (ИФН α/рибавирин) в течение 48 нед УВО у таких больных возрастает до 28–36%, оставаясь значительно ниже УВО при генотипах 2 и 3 HCV (64–79%). Лечение ХГ С с генотипом 1 HCV в течение 48 нед дает более высокие результаты (46–52%), чем 24 нед (29–42%). Таким образом, генотип вируса HCV определяет стратегию ПВТ ХГ С и ЦП С.
Уровень вирусной нагрузки, как и генотип вируса, не влияет на вариант и тяжесть течения ХГ C. Высокая вирусная нагрузка (более 2х10 6 копий/мл или более 800 000 МЕ/мл) может быть выявлена при хроническом гепатите низкой, умеренной, высокой степени активности, при минимальных изменениях в печени или при ЦП С. Однако уровень виремии отчетливо влияет на частоту достижения УВО: пегилированный ИФН α-2b 1,5 мкг/кг 1 раз в неделю в комбинации с рибавирином в дозе 800 мг/сут при высокой вирусной нагрузке обеспечивает УВО в 42% случаев, а при низкой — в 78%.
В последние годы разработан метод оценки успеха терапии на основании изучения вирусной кинетики на ранней стадии ПВТ. Ранний вирусологический ответ позволяет прогнозировать УВО. Высокая приверженность больных ХГ C к лечению и оценка прогноза ПВТ на основании данных раннего вирусологического ответа на 4-й или 12-й неделе позволили повысить результативность терапии в группе всех леченных больных ХГ С до 90%. Отказ от стандартных схем лечения ИФН α (3 млн МЕ 3 раза в нед) с переходом на комбинированную ПВТ также способствует повышению количества больных с ранним вирусологическим ответом.
Изучение раннего вирусологического ответа на основании количественного анализа HCV-РНК с помощью высокочувствительной ПЦР позволяет идентифицировать больных, которые не ответят на ПВТ. Если после 12-недельной ПВТ пегилированными ИФН α и рибавирином уровень HCV-РНК снизился на два и более десятичных логарифмов, но РНК вируса по-прежнему выявляется в крови, то целесообразно продолжить ПВТ еще в течение 12 нед, а затем провести повторное исследование HCV-РНК. При его отрицательном результате УВО колеблется от 42 до 78% в зависимости от вирусной нагрузки. Представляется целесообразным 72-недельный курс ПВТ, т. е. продление лечения до 1,5 лет, что позволяет значительно улучшить результаты лечения. При сохраняющейся виремии с падением ее уровня на 12-й неделе менее чем на два десятичных логарифма УВО составляет от 0 до 5%, что позволяет уже на ранних этапах либо отказаться от бесперспективной терапии при генотипе 1 HCV, либо модифицировать ее, либо перейти на поддерживающую терапию пегилированным ИФН α-2а (90 мкг) или ИФН α-2b (0,5 мкг/кг) с целью замедления прогрессирования ЦП С и профилактики развития ГЦК и лимфомы.
Таким образом, генотип 1b и высокая вирусная нагрузка определяют категорию «трудных» для лечения больных ХГ C. В отношении этой группы пациентов необходимо строго следовать правилу применения максимально эффективных доз пегилированных ИФН α-2b (1,5 мкг/кг) или ИФН α-2a (180 мкг) в сочетании с рибавирином в дозе выше 13 мг/кг при продолжительности лечения 48–52 нед. Известно, что пегилированные ИФН α-2a и 2b отличаются друг от друга по фармакокинетике и фармакодинамике. Была проведена независимая сравнительная оценка кинетики вирусологического ответа на пегилированные ИФН α-2a в дозе 180 мкг/нед и ИФН α-2b в дозе 1,5 мкг/кг/нед при их сочетании с рибавирином в дозе 15 мг/кг/сут у первичных больных ХГ C. В конце курса лечения вирусологический ответ на комбинированную терапию пегИФН α-2a/рибавирином и пегИФН α-2b/рибавирином у пациентов с генотипом 1 HCV составил 55% и 76% соответственно, что позволяет рекомендовать применение пегИФН α-2b в составе комбинированной ПВТ у данной категории больных [6]. В настоящее время ряд авторов предлагают оценивать ранний вирусологический ответ на 4-й неделе и при отсутствии вирусологического ответа модифицировать лечение. Используется индукционная терапия пегилированным ИФН α-2b в дозе 3 мкг/кг/нед в течение 4 неделе или 2 мкг/кг/нед в течение 8 нед с последующим применением препарата в дозе 1,5–1,0 мкг/кг/нед.
Тройная схема комбинированной ПВТ с включением помимо пегилированного ИФН α и рибавирина 200 мг амантадина не имеет преимуществ перед обычной схемой в лечении ХГ C генотипа 1b с высокой вирусной нагрузкой.
В 2004 г. опубликованы предварительные результаты лечения больных с генотипом 1 HCV и высокой вирусной нагрузкой, не ответивших на первый курс ПВТ ИФН α и рибавирином, комбинацией α-тимозина-1 (1,6 мг 2 раза в неделю подкожно), пегилированного ИФН α-2a (180 мкг в неделю) и рибавирина (1000–1200 мг/сут) в течение 24 недель. Ранний вирусологический ответ на 12-й неделе лечения достигнут у 47,8% больных, вирусологический ответ после 24 нед терапии сохранялся у 39,1% пациентов ХГ C, представляющих «трудную» для лечения группу. Дополнительный препарат (α-тимозин-1) не добавлял новых побочных эффектов и хорошо переносился больными.
Новые стратегии в лечении «трудных» больных с генотипом 1 HCV и высокой вирусной нагрузкой включают продление сроков комбинированной ПВТ до 72 нед у пациентов, не достигших раннего вирусологического ответа на 4-й неделе, что позволяет повысить УВО с 22% (при 48-недельной терапии) до 51% и снизить частоту обострений [7].
Обоснованием для лечения ХГ C с продвинутой стадией фиброза или сформировавшимся ЦП С стали данные о снижении риска декомпенсации ЦП и развития ГЦК, а также регрессе фиброза у 60% больных, получающих ПВТ. Наличие портального фиброза или ЦП С считается независимым фактором низкой частоты УВО у HCV-инфицированных больных. Пациенты с ЦП C обычно плохо отвечают на стандартную монотерапию ИФН α: УВО составляет от 5 до 20%. Эффективность комбинированной терапии ИФН α и рибавирином составила в этой группе 5–29%. Применение пегилированных ИФН α в составе комбинированной терапии компенсированного ЦП C или ХГ С с мостовидным фиброзом позволило повысить УВО до 44–50%.
Следует отметить, что даже при монотерапии пегилированным ИФН α можно достигнуть гистологического улучшения у 54% больных компенсированным ЦП С. В сравнительном исследовании эффективности пегилированных ИФН α-2a и 2b у больных ЦП C наличие мостовидного фиброза являлось отрицательным прогностическим фактором достижения раннего вирусологического ответа. В конце 24-недельной ПВТ вирусологический ответ в 1-й группе больных ЦП C составил 83%, во 2-й — 60%. Таким образом, пегилированный ИФН α-2a может быть препаратом выбора в комбинированной терапии ЦП C [8]. Даже при отсутствии вирусологического ответа на комбинированную ПВТ при ЦП C отмечается улучшение гистологической картины в печени (снижение ИГА и ГИС).
Наиболее значимое улучшение морфологических данных имеет место при достижении УВО, что сопровождается улучшением качества жизни больных ЦП С, несмотря на наличие продвинутой стадии болезни. Интерес представляют данные Poynard и соавторов (2000), наблюдавших 3010 больных ХГ С с повторной биопсией печени (до начала ПВТ и спустя 6–12 мес после ее окончания) при использовании различных режимов лечения: монотерапии ИФН α-2b, комбинированной ПВТ ИФН α или пегилированным ИФН α-2b и рибавирином в течение 48 нед. Более чем у трети больных, у которых был достигнут УВО, улучшилась гистологическая картина (ГИС и ИГА) в печени, морфологическая динамика отмечена также у трети больных без вирусологического ответа [9]. Анализ биопсий печени у больных ХГ С, участвовавших в четырех многоцентровых исследованиях, показал, что у 75 (49%) из 153 пациентов ЦП С после окончания терапии ГИС (уровень фиброза) снизился на 1–3 балла, что позволяет говорить о возможности регресса фиброза при ЦП С под влиянием настойчивой целенаправленной ПВТ [10].
В последние годы предпринимаются попытки противовирусного лечения декомпенсированного ЦП С (Чайлд В и С). Известно, что 40% всех ортотопических трансплантаций печени проводится в связи с ЦП С. Больные с сохраняющейся виремией имеют высокий риск реакций отторжения трансплантата и инфицирования донорской печени вирусом гепатита С с быстрым развитием (в течение 5–7 лет) ЦП С и/или ГЦК в пересаженной печени. В 2003–2004 гг. появились первые публикации использования ПВТ малыми дозами интерферона и рибавирина при декомпенсированном ЦП С у кандидатов на трансплантацию печени. Предлагается начинать лечение ИФН α 3 млн МЕ ежедневно и рибавирином 800 мг/сут за 4 мес до предполагаемой операции. Режим ежедневного введения интерферона позволяет уменьшить частоту гриппоподобного синдрома, лечение в течение 4 мес позволяет добиться максимального снижения виремии (до операции). У 9 (30%) из 30 больных декомпенсированным ЦП С (Чайлд В или С) удалось достичь вирусологического ответа на 12-й неделе, у 6 из них (20%) авиремия сохранялась после трансплантации печени [11]. Аналогичные данные о возможности развития УВО в 18–20% случаев декомпенсированного ЦП С опубликованы рядом авторов, длительность наблюдения за такими больными продолжается более 3,9 лет.
Известно, что употребление алкоголя значительно повышает смертность при вирусных ЦП: пятилетняя выживаемость больных достигает лишь 43%, значительно отличаясь в группах ЦП Чайлд А (66%), Чайлд В (50%) и Чайлд С (25%). При продолжающемся приеме алкоголя риск смерти у больных ЦП С повышается в случае наличия таких факторов, как пожилой возраст, печеночно-клеточная дисфункция (Чайлд В или С), желудочно-кишечное кровотечение, коинфекция (HBV, HCV), курение и отсутствие признаков острого алкогольного гепатита при биопсии печени. Среди механизмов влияния алкоголя на прогрессирование HCV-инфекции отмечают активацию репликации, повышение разнообразия квазивидов и мутаций вируса, усиление апоптоза гепатоцитов, подавление иммунного ответа хозяина, нарастание стеатоза и уровня железа в печени. Все это ведет к быстрому развитию болезни, высокой частоте формирования ЦП С и ГЦК и низкой эффективности интерферонотерапии. Эффективность ПВТ при ХГ С у лиц, употребляющих алкоголь, в 3 раза ниже стандартных показателей УВО: при монотерапии ИФН УВО снижается до 7–8% по сравнению с 25% у больных, не употребляющих алкоголь; при комбинированной терапии — до 12–4% по сравнению с 41%. Не существует безопасных доз алкоголя для больных ХГ С. Рекомендуется полный отказ от его приема за 6 мес до предполагаемой ПВТ, что улучшает результаты противовирусного лечения, однако УВО не достигает показателей, свойственных больным, не употреблявшим алкоголь в прошлом. Возврат к приему алкоголя после окончания ПВТ повышает риск обострения ХГ С и возврата виремии.
У больных ХГ С на стадии цирроза или при наличии мостовидного фиброза (F3) риск развития побочных эффектов интерферонотерапии выше, чем при менее продвинутых стадиях фиброза. Показано, однако, что частота их выявления и необходимость прекращения ПВТ существенно не отличаются в группах больных, леченных пегилированным ИФН α или ИФН α в стандартном режиме. Пегилированный ИФН α-2а обладает более выраженным миелосупрессивным действием, чем ИФН α-2b. Гематологическая токсичность при применении пегилированных ИФН α проявляется в первые 4 нед лечения, затем достигается устойчивый уровень лейкоцитов и тромбоцитов. Особенно быстро их число снижается после первой дозы препаратов. ПВТ назначают больным компенсированным ЦП С с уровнем лейкоцитов 3000/ммЁ и тромбоцитов 50 000/ммЁ. При снижении уровня нейтрофилов до 600/ммЁ, а уровня тромбоцитов до 20 000/ммЁ ИФН α отменяют.
Модификация дозы пегилированного ИФН α или рибавирина (снижение дозы или отмена препарата) в связи с побочными эффектами отмечена у 50% больных ЦП С. В зависимости от достижения раннего вирусологического ответа на 12-й неделе лечения предложены различные варианты лечения ЦП С: продолжение комбинированной терапии в максимально эффективных дозах в течение 36 нед при достижении раннего вирусологического ответа; лечение небольшими дозами пегилированного ИФН α-2b (0,5 мкг/кг) в течение 5 лет при отсутствии такого ответа на 4-й нед (EPIC3) или малыми дозами пегилированного ИФН α-2а (90 мкг) в течение 4 лет (HALT-С).
Определены показания к повторным курсам ПВТ: наличие генотипов 2 или 3 НСV; частичный ответ при предшествующем курсе ПВТ, F3- и F4-стадии фиброза. Противопоказаниями к повторным курсам лечения являются: пожилой возраст, генотип 1, ЦП С с гипербилирубинемией, высокая вирусная нагрузка, высокий индекс массы тела, минимальные изменения в печени при биопсии (ИГА менее 4 баллов) и продолжающееся употребление алкоголя или наркотиков.
Таким образом, ПВТ компенсированного и декомпенсированного ЦП при ХГ С решает ряд следующих задач: замедление декомпенсации цирроза, снижение смертности от его осложнений (кровотечение из варикозно расширенных вен, печеночно-клеточная недостаточность и т. д.), предотвращение развития ГЦК и профилактику реактивации инфекции после трансплантации печени, а также улучшение качества жизни больных и обеспечение их социальной реабилитации. Несомненно, что на ранних стадиях HCV-инфекции ПВТ дает лучшие результаты: частота УВО при лечении острого гепатита С достигает 90%, ХГ С — 60–70%, что превышает эффективность лечения ЦП С пегилированными ИФН α и рибавирином (30–50%). Наш опыт ПВТ ХГ С низкой степени активности позволяет говорить о высокой эффективности лечения данной категории больных. Используя пегилированный ИФН α-2b (1,5 мкг/кг) и рибаверин (более 10,6 мг/кг) при лечении первичных больных с небольшим сроком заболевания (5,9±5,7 лет), преимущественно низкой степени активности и слабым фиброзом (F1), а также низкой вирусной нагрузкой, мы получили устойчивый вирусологический ответ в 86 % случаев, в том числе у 77% пациентов с генотипом 1 HCV, включая 5 больных на стадии ЦП С [12].
- Collier J. D., Woodall T., Wight D. G. D. et al. Predictiv of progressive hepatic fibrosis stage on sabsequent liver biopsy in chronic hepatitis C virus infection. J. Viral Hepatitis, 2005; 12: 74-80.
- Niederau C., Lange S., Heintgest T. et al. Prognosis of chronic Hepatitis C: Results of a Large, Prospective Cohort Study. Hepatology, 1998; 28: 1687-1695.
- Curry M., Cardenas A., Afdhal N. H. Effect of maintenance Peg-Intron therapy on portal hypertension and its complications: results from the COPILOT study. J. Hepatol., 2005; 42 (2): 95.
- Fried M. W., Shiffman M., Reddy R. et al. Peginterferon alfa-2a plus ribavirin for chronic hepatitis C virus infection. N Engl J. Med., 2002; 347: 975-982.
- Manns M., McHutchison J., Gordon S. et al. Peginterferon alfa-2b plus ribavirin compared with interferon alfa-2b plus ribavirin for initial treatment of chronic hepatitis C: a randomized trial. Lancet, 2001; 358: 958-965.
- Luise S., Bernardinello E., Cavalletto L. et al. Kinetic of Virolological Response Duning Peg-IFNS in Chronic Hepatitis C. J. Hepatol 2004; 40 (1): A 490.
- Berg T., von Wagner M., Hinrichsen H. et al. Comparison of 48 or 72 weeks of treatment with pegiterferon alfa-2a (40 KD) (Pegasys) plus ribavirin (Copegus) in treatment-naive patients with chronic hepatitis C infected with HCV genotype 1 [Abstract]. Hepatology 2003; 38 (1): 317A.
- Hadziyannis S. J., Papatheodoridis G. V. Peginterferon-(2a (40 kDa) for chronic hepatitis C. Expert Opin. Pharmacother. 2003; 4:541-551.
- Poynard T., Marcellin P., Lee S. S. et al. Randomised trial of interferon alpha 2b plus ribavirin for 48 weeks or for 24 weeks versus interferon alpha 2b plus placebo for 48 weeks for treatment of chronic infection with hepatitis C virus. Lancet 1998; 352:1426-1432.
- Poynard T., McHutchison J., Manns M. et al. Impact of Pegylated Interferon Alpha-2b and Ribavirin on Liver Fibrosis in Patients with Chronic Hepatitis C. Gastroenterol. 2002; 122: 1303-1313.
- Forns X., Navasa M., Rodes J. Treatment of HCV Infection in Patients With Advanced Cirrhosis. Hepatology, 2004; 40: 498.
- Никулкина Е. Н., Крель П. Е., Лопаткина Т. Н. и др. Комбинированная терапия пегинтерфероном альфа-2b (пегинтроном) и рибавирином (Ребетолом) у первичных больных хроническим гепатитом C // Клиническая фармакология и терапия. — 2004. — № 13 (2). — С. 48-52.
Т. Н. Лопаткина, кандидат медицинских наук, доцент
источник