Семейство Poxviridae включает несколько родов, имеющих разнообразных хозяев. Патогенным для человека является вирус натуральной оспы.
Заболевание оспой известно с незапамятных времен (около 3000 лет до н. э.) и распространено оно было во всех странах мира.
Один из древних историков писал: «Никакой народ, никакая раса, ни звание, ни возраст, ни пол не щадились оспой. Все трепетало перед ней». Оспа страшна своей контагиозностью. В Германии в XVIII веке от оспы погибло 80 тыс. человек. От оспы умерли русский царь Петр II, австрийский император Иосиф, французский король Людовик XIV, английская королева Анна, знаменитая русская актриса Комиссаржевская и др.
Нам сейчас трудно представить себе ту сокрушительную силу, с которой орудовал вирус оспы. Но этот бич человечества был сломлен наукой. Прекратились эпидемии оспы.
И за последние несколько лет не было зарегистрировано ни одного случая оспы во всем мире.
Этиология оспы была установлена к концу XIX века. В 1892 г. Гварниери в гистологических срезах, сделанных и роговицы глаз кролика, зараженного оспенным материалом, обнаружил шаровидные и серповидные включения величиной от 3-4 до 10 мкм, окрашивающиеся по Романовскому — Гимзе в красный цвет. Эти включения были названы тельцами Гварниери. А в 1906 г. в содержимом оспенных пустул Пашен обнаружил оспенные корпускулы, в препаратах, обработанных методом серебрения по Морозову. Эти корпускулы были названы тельцами Пашена — Морозова.
Морфологическая структура. Вирус оспы крупный, размером 300-350 нм, кубоидальной формы. На ультрасрезах оспенных вирионов обнаружена липопротеидная оболочка, под ней вироплазма, в которой содержится нуклеокапсид. ДНК у вируса оспы — двунитчатая. Из нуклеокапсида вириона выделены некоторые ферменты.
Культивирование. Вирус натуральной оспы хорошо развивается в куриных эмбрионах на хорион-аллантоисной оболочке. Репродукция его характеризуется образованием на оболочке белых, плотных точечных бляшек с блестящей поверхностью, величиной около 1 мм.
Вирус можно также культивировать на первичных и перевиваемых клеточных культурах человека и животных. Здесь рост характеризуется цитопатическим действием (дегенерацией клеток через 48-72 ч).
Антигенная структура. У вируса оспы обнаружено несколько антигенов: растворимые (L-термолабильный и S-термостабильный), нуклеопротеидный NP-антиген. Вирусы оспы имеют общие антигены с вирусом оспенной вакцины и эритроцитами человека группы А и АВ.
Устойчивость к факторам окружающей среды. При температуре 100° С вирусы погибают моментально. Температура 60° С губит их через час. Низкие температуры и высушивание вирусы натуральной оспы переносят хорошо — в оспенных корочках сохраняются длительно. Дезинфицирующие растворы (30% хлорамин, лизол) инактивируют вирусы оспы через 30 мин. К фенолу и эфиру они более устойчивы, а в 50% глицерине вирусы оспы сохраняются месяцами.
Восприимчивость животных. К вирусу оспы чувствителен мелкий и крупный рогатый скот. В экспериментальных условиях легко заражаются обезьяны, морские свинки, кролики и др. Однако воспроизвести заболевание, сходное по клинике с болезнью человека, можно только у обезьян.
У новорожденных белых мышей вирус вызывает оспенный энцефалит.
Источники инфекции. Больные люди.
Пути передачи. Воздушно-капельный и воздушно-пылевой (вирус передается при кашле, разговоре, через посуду, а также через пылевые частицы, находящиеся на одежде).
Патогенез. Вирус оспы проникает через слизистую оболочку дыхательных путей и через кожные покровы. Проникнув в организм, вирусы локализуются в регионарных лимфатических узлах. Размножившись там, они попадают в кровь, обусловливая вирусемию. Вторичная репродукция (размножение) происходит в лимфоидной ткани и сопровождается клиническими проявлениями заболевания: высокой температурой, головной болью, потерей сознания и т. д. Обладая дермотропными свойствами, вирусы попадают в эпидермис. На коже и слизистых оболочках образуются папулы, везикулы и пустулы. Оспенные папулы характеризуются прозрачным содержимым и имеют вид жемчужин с перламутровым блеском. На месте появления пустул образуется некроз, после заживления которого остаются рубцы. Образование рубцов на слизистой глаз приводит к слепоте (в 25% случаев). Процент смертности при оспе велик, при геморрагической форме — 100%. При этой форме пустулы наполняются кровью — черная оспа.
Встречаются легкие формы оспы, когда заболевание протекает без температуры и сыпи.
Иммунитет. У переболевших людей иммунитет пожизненный. Обусловливается он вируснейтрализующими, гемагглютинирующимися и комплементсвязывающими антителами. Искусственная иммунизация с последующей ревакцинацией дает стойкий иммунитет. Считают, что интерферон также является фактором защиты.
Профилактика. Ранняя диагностика, изоляция, дезинфекция, предупреждение завоза оспы из других стран, карантин и т. д.
Специфическая профилактика. В борьбе с натуральной оспой большое значение имеет специфическая профилактика. За много лет до нашей эры на востоке существовали разные методы борьбы с оспой. В Индии, Иране — растертые корочки из пустул больных легкой формой втирали в кожу здоровых, а в Китае наносили на слизистые оболочки носа.
В 1796 г. английский врач Э. Дженнер после длительных наблюдений использовал содержимое пустул коровьей оспы для вакцинации людей. Отсюда название — вакцина (от лат. vacca — корова).
Вакциной, приготовленной таким методом, пользовались длительное время. Затем был разработан метод получения ововакцины (вирус накапливали в курином эмбрионе). Этот метод удобнее для изготовления и экономнее.
В настоящее время вакцину готовят из вируса, выращенного в культуре клеток.
В марте 1919 г. В. И. Лениным был подписан декрет об обязательном оспопрививании. После проведения массовой иммунизации оспа в СССР была ликвидирована.
В 1958 г. по инициативе СССР на XI Ассамблее ВОЗ было принято решение о ликвидации оспы во всем мире путем массовой вакцинации. В результате за последние годы не было зарегистрировано ни одного случая заболевания оспой в мире и в 1981 г. по рекомендации ВОЗ обязательная прививка против оспы была отменена.
Цель исследования: выявление возбудителя оспы. Работа с вирусом оспы проводится в строго режимных условиях (см. «Особо опасные инфекции»).
1. Содержимое папул, везикул, пустул.
2. Отделяемое слизистой оболочки носоглотки.
3. Кровь (с 5-го дня болезни) берут для выявления специфических антител.
Способы сбора материала
1. Метод иммунофлюоресценции (экспресс-диагностика) (см. главу 12).
2. Реакция РСК, РТГА и РНГА (см. главу 12).
3. Выделение вируса в куриных эмбрионах и культуре клеток Hela, Нер-2.
4. Обнаружение телец Гварниери в зараженных клетках.
5. Обнаружение телец Пашена в содержимом везикул (окраска по Морозову).
1. Какова величина и структура вириона оспы?
2. Каковы основные методы культивирования вируса оспы?
3. Патогенез натуральной оспы.
4. Иммунитет и специфическая профилактика? Кем и когда был подписан первый декрет об обязательной прививке против оспы?
5. Каковы основные методы диагностики оспы?
источник
Вирусы— мельчайшие микробы, не имеющие клеточного строения, белоксинтезирующей системы, содержащие только ДНК или РНК. Относятся к царству Vira. Являясь облигатными внутриклеточными паразитами, вирусы размножаются в цитоплазме или ядре клетки. Они — автономные генетические структуры. Отличаются особым — разобщенным (дизъюнктивным) способом размножения (репродукции): в клетке отдельно синтезируются нуклеиновые кислоты вирусов и их белки, затем происходит их сборка в вирусные частицы. Сформированная вирусная частица называется вирионом.
Морфологию и структурувирусов изучают с помощью электронного микроскопа, так как их размеры малы и сравнимы с толщиной оболочки бактерий.
Формавирионов может быть различной: палочковидной (вирус табачной мозаики), пулевидной (вирус бешенства), сферической (вирусы полиомиелита, ВИЧ), в виде сперматозоида (многие бактериофаги). Различают просто устроенные и сложно устроенные вирусы.
Простые, или безоболочечные, вирусы состоят из нуклеиновой кислоты и белковой оболочки, называемой капсидом. Капсид состоит из повторяющихся морфологических субъединиц — капсомеров. Нуклеиновая кислота и капсид взаимодействуют друг с другом, образуя нуклеокапсид.
Сложные, или оболочечные, вирусы снаружи капсида окружены липопротеиновой оболочкой (суперкапсидом, или пеплосом). Эта оболочка является производной структурой от мембран вирус-инфицированной клетки. На оболочке вируса расположены гликопротеиновые шипы, или шипики (пепломеры). Под оболочкой некоторых вирусов находится матриксный М-белок.
Фенотипическое смешивание довольно широко распространено среди близкородственных безоболочечных вирусов, таких, например, как вирусы полиомиелита типов 1 и 2, вирусов ЭКХО и Коксаки, других пикорнавирусов. Таким образом, немутационные вирусы-гибриды — полноценные вирионы. Подобно вирусам-мутантам, возникают путем комплементации, а не вследствие скрещивания геномов, как рекомбинанты. Состояния гетерозиготности и транскапсидизации вирусов неустойчивы и быстро исчезают при пассажах. Биологическое значение гетерозигот не выяснено. Транскапсидизация же может обеспечить вирусам-гибридам широкий круг хозяев и преодоление межвидовых барьеров.
Капсид и суперкапсидзащищают вирионы от влияния окружающей среды, обусловливают избирательное взаимодействие (адсорбцию) с клетками, определяют антигенные и иммуногенные свойства вирионов. Внутренние структуры вирусов называются сердцевиной.
Тип симметрии. Капсид или нуклеокапсид могут иметь спиральный, икосаэдрический (кубический) или сложный тип симметрии.Икосаэдрическийтип симметрии обусловлен образованием изометрически полого тела из капсида, содержащего вирусную нуклеиновую кислоту (например, у вирусов гепатита А, герпеса, полиомиелита).Спиральныйтип симметрии обусловлен винтообразной структурой нуклеокапсида (например, у вируса гриппа).
Включения— скопление вирионов или отдельных их компонентов в цитоплазме или ядре клеток, выявляемые под микроскопом при специальном окрашивании. Вирус натуральной оспы образует цитоплазматические включения — тельца Гварниери; вирусы герпеса и аденовирусы — внутриядерные включения.
Размеры вирусов определяют с помощью электронной микроскопии, методом ультрафильтрации через фильтры с известным диаметром пор, методом ультрацентрифугирования. Одним из самых мелких вирусов является вирус полиомиелита (около 20 нм), наиболее крупным — натуральной оспы (около 350 нм).
Вирусы имеют уникальный геном, так как содержат либо ДНК, либо РНК. Поэтому различают ДНК-содержащие и РНК-содержащие вирусы. Они обычно гаплоидны, т.е. имеют один набор генов. Геном вирусов представлен различными видами нуклеиновых кислот: двунитчатыми, однонитчатыми, линейными, кольцевыми, фрагментированными. Среди РНК-содержащих вирусов различают вирусы с положительным (плюс-нить РНК) геномом. Плюс-нить РНК этих вирусов выполняет наследственную функцию и функцию информационной РНК (иРНК). Имеются также РНК-содержащие вирусы с отрицательным (минус-нить РНК) геномом. Минус-нить РНК этих вирусов выполняет только наследственную функцию.
Геномвирусов способен включаться в состав генетического аппарата клетки в виде провируса, проявляя себя генетическим паразитом клетки. Нуклеиновые кислоты некоторых вирусов (вирусы герпеса и др.) могут находиться в цитоплазме инфицированных клеток, напоминая плазмиды.
Внутримолекулярные рекомбинации у вирусов, как и других микроорганизмов, реализуются механизмом разрыв — воссоединение, а у РНК-вирусов с сегментированным геномом — перемешиванием генов. В общем, у вирусов различают две группы рекомбинаций -рекомбинация у ДНК-вирусов и рекомбинация-пересортировка у РНК-вирусов с сегментированным геномом.
Среди генетических рекомбинаций ДНК-вирусов выделяют рекомбинации:
1) между двумя дикими типами вирусов с интактными (лат intactus — нетронутый), т. е. полными, геномами;
2) между диким типом и его мутантным вариантом;
3) между вариантами мутантов дикого типа вируса.
источник
Вирусы [от лат. virus, яд] — наименьшие по размерам агенты, имеющие геном, окружённый белковой оболочкой. Вирусы не воспроизводятся самостоятельно, они — облигатные внутриклеточные паразиты, репродуцирующиеся только в живых клетках. Все вирусы существуют в двух формах. В настоящее время известны вирусы бактерий (бактериофаги), грибов, растений и животных.
Внеклеточная форма — вирион — включает в себя все составные элементы (капсид, нуклеиновую кислоту, структурные белки, ферменты и др.). Внутриклеточная форма — вирус — может быть представлена лишь одной молекулой нуклеиновой кислоты, так как, попадая в клетку, вирион распадается на составные элементы.
Несмотря на внутриклеточный паразитизм, среди вирусов имеются крупные виды, соизмеримые по размерам с микоплазмами и хламидиями. Например, вирус натуральной оспы достигает 400 нм и вполне сравним с риккетсиями (300-500 нм) и хламидиями (300-400 нм). По морфологии выделяют вирусы палочковидные (например, возбудитель лихорадки Эбола), пуле-видные (вирус бешенства), сферические (герпесвирусы), овальные (вирус оспы), а также бактериофаги, имеющие сложную форму (рис. 2-1). При всём разнообразии конфигураций, размеров и функциональных характеристик вирусам присущи некоторые общие признаки. В общем виде зрелая вирусная частица (вирион) состоит из нуклеиновой кислоты, белков и липидов, либо в его состав входят только нуклеиновые кислоты и белки.
Вирусы содержат только один тип нуклеиновой кислоты, ДИК или РНК, но не оба типа одновременно. Например, вирусы оспы, простого герпеса, Эпстайна-Барр — ДНК-содержащие, а тогавирусы, пикорнавирусы — РНК-содержащие. Геном вирусной частицы гаплоидный. Наиболее простой вирусный геном кодирует 3-4 белка, наиболее сложный — более 50 полипептидов. Нуклеиновые кислоты представлены однонитевыми молекулами РНК (исключая реовиру-сы, у которых геном образован двумя нитями РНК) или двухнитевыми молекулами ДНК (исключая парвовирусы, у которых геном образован одной нитью ДНК). У вируса гепатита В нити двухнитевой молекулы ДНК неодинаковы по длине.
Вирусные ДНК образуют циркулярные, ковалентно-сцёпленные суперспирализованные (например, у паповавирусов) или линейные двухнитевые структуры (например, у герпес- и аденовирусов). Их молекулярная масса в 10-100 раз меньше массы бактериальных ДНК. Транскрипция вирусной ДНК (синтез мРНК) осуществляется в ядре заражённой вирусом клетки. В вирусной ДНК на концах молекулы имеются прямые или инвертированные (развёрнутые на 180″) повторяющиеся нуклеотидные последовательности. Их наличие обеспечивает способность молекулы ДНК замыкаться в кольцо. Эти последовательности, присутствующие в одно- и двух-нитевых молекулах ДНК, — своеобразные маркёры вирусной ДНК.
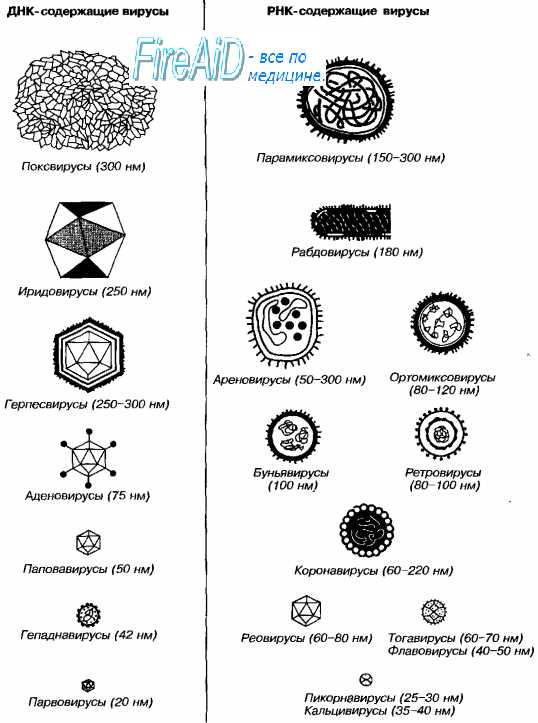
Вирусные РНК представлены одно- или двухнитевыми молекулами. Однонитевые молекулы могут быть сегментированными — от 2 сегментов у ареновирусов до 11 — у ротавирусов. Наличие сегментов ведёт к увеличению кодирующей ёмкости генома. Вирусные РНК подразделяют на следующие группы: плюс-нити РНК (+РНК), минус-нити РНК (-РНК). У различных вирусов геном могут образовывать нити +РНК либо -РНК, а также двойные нити, одна из которых -РНК, другая (комплементарная ей) — +РНК.
Плюс-нити РНК представлены одиночными цепочками, имеющими характерные окончания («шапочки») для распознавания рибосом. К этой группе относят РНК, способные непосредственно транслировать генетическую информацию на рибосомах заражённой вирусом клетки, то есть выполнять функции мРНК. Плюс-нити выполняют следующие функции: служат мРНК для синтеза структурных белков, матрицей для репликации РНК, упаковываются в капсид с образованием дочерней популяции. Минус-нити РНК не способны транслировать генетическую информацию непосредственно на рибосомах, то есть они не могут функционировать как мРНК. Однако такие РНК служат матрицей для синтеза мРНК.
Многие вирусные нуклеиновые кислоты инфекционны сами по себе, так как содержат всю генетическую информацию, необходимую для синтеза новых вирусных частиц. Эта информация реализуется после проникновения вириона в чувствительную клетку. Инфекционные свойства проявляют нуклеиновые кислоты большинства +РНК- и ДНК-содержащих вирусов. Двухнитевые РНК и большинство -РНК не проявляют инфекционных свойств.
источник
История открытия вируса оспы, изучение его этимологии, строения. Подвиды вируса натуральной оспы по вирулентности для людей. Изучение патогенеза вируса и его жизненного цикла. Физиология развития болезни. Практическое применение вируса в настоящее время.
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Министерство здравоохранения Российской Федерации
Государственное бюджетное образовательное учреждение высшего профессионального образования
«Санкт-Петербургская государственная химико-фармацевтическая академия»
Выполнил (а): студентка 3 курса 222 группы
Андреева Екатерина Алексеевна
Научный руководитель: Ольга Михайловна
- Введение
- 1. История открытия вируса
- 2. Этимология и особенности строения
- 3. Жизненный цикл
- 4. Механизм зарождения и развития болезни
- 4.1 Преодоление барьеров
- 4.2 Физиология развития болезни
- 4.3 Иммунные реакции организма на ВНО
- 5. Практическое применение
- Список используемой литературы
Несмотря на победу над болезнью, которая стала возможна благодаря сотрудничеству всех стран мира, вирус натуральной оспы все еще жив и активно используется во многих научных исследованиях.
— узнать историю открытия вируса, его этимологию и особенности строения;
— исследовать практическое применение вируса в настоящее время.
Эпидемия чёрной оспы впервые прокатилась по Китаю в IV веке, а в середине VI века — поразила Корею. В 737 году от оспы вымерло более 30 % населения Японии. В VI веке оспа уже хозяйничала в Византии, будучи занесённой в последнюю из Африки. Арабы-мусульмане, приступив к завоеваниям, в VII — VIII веках разнесли оспу от Испании до Индии: история засвидетельствовала появление оспы в Сирии, Палестине и Персии в VII веке, в Сицилии, Италии, Испании и Франции в следующем, VIII столетии.
С VI века оспа фигурирует под сохранившимся до сих пор её латинским названием variola, впервые употреблённым епископом Марием из Аванша в 570 году. С этого времени оспа, под своим несменяемым именем, уносила ежегодно множество жизней в Европе.
Из Европы оспа перешла в Америку, где она похитила много миллионов жизней, вымерли без остатка многие племена.
Начиная с XVII столетия, имеется уже много фактических данных об оспе, зарегистрированных современниками. В общей сумме было вычислено, что в Европе ежегодно умирало от оспы более 1,5 миллионов человек.
Возбудитель оспы относится к вирусам семейства Poxviridae, подсемейства Chordopoxviridae, рода Orthopoxvirus.
По вирулентности для людей ВНО делится на два подвида: Variola major (летальность среди заболевших людей колеблется в пределах от 5 до 40 %); и Variola minor или алястрим (летальность 0,1-2 %).
Вирусы оспы — наиболее крупные из всех вирусов животных. Под электронным микроскопом они выглядят как большие овальные частицы размером около 250-350×200-270 нм.
В структуре вирусов оспы различают три основных компонента: двояковогнутую сердцевину, овальные боковые тела и оболочку вириона. Сердцевину вириона составляют ДНК и связанные с нею белки. Сердцевина окружена гладкой мембраной (толщиной около 5 нм), снаружи покрытой слоем вертикально уложенных и плотно прилегающих друг к другу цилиндрических субъединиц (5×10 нм). Вогнутость сердцевины с обеих сторон занята овальными образованиями (неизвестной природы), называемыми боковыми телами. Они как бы сдавливают сердцевину, придавая ей форму двояковогнутого диска, имеющего на разрезе вид гантели.
Вирионы заключены в липопротеиновую супероболочку, которая имеет толщину 20 — 30 нм и содержит липиды клетки и вирусспецифические белки.
Вирионы большинства вирусов оспы окружены слоем беспорядочно расположенных трубчатых структур, придающих им характерный вид. Эти структуры состоят из сферических субъединиц диаметром около 5 нм. Субъединицы построены из молекул протеина или гликопротеина. В состав ворсинок длиной 20 нм покрывающих поверхность вируса осповакцины (ВОВ), входит белок с молекулярной массой 58 кД, относящийся к главным полипептидам вириона.
Вирус осповакцины содержит белки, липиды и ДНК, которые соответственно составляют 90, 5 и 3,2% массы вириона (5х10
15 г). В вирусе оспы птиц около 1/3 массы составляют липиды.
Вирионы, содержащие двухцепочечную геномную ДНК, ферменты, факторы транскрипции, адсорбируются на клетке (1) и сливаются с плазматической мембраной клетки, высвобождая сердцевины в цитоплазму (2). Сердцевины синтезируют ранние мРНК, с которых транслируются различные белки, включая факторы роста, молекулы защиты от иммунной системы, ферменты и факторы для репликации ДНК и транскрипции промежуточных генов (3). Происходит раздевание сердцевины (4) и вирусная ДНК реплицируется, формируя конкатемерные молекулы (5). Промежуточные гены транскрибируются на дочерних молекулах ДНК и с этих мРНК транслируются факторы поздней транскрипции (6). Затем транскрибируются поздние гены. С их мРНК транслируются вирионные структурные белки, ферменты и факторы ранней транскрипции (7). Сборка вирионов начинается с образования дискретных мембранных структур (8). Конкатемерные промежуточные формы вирусной ДНК разделяются на единичные геномы и упаковываются в незрелые вирионы (9). Созревание приводит к образованию внутриклеточных зрелых вирионов (10). Эти вирионы покрываются модифицированными мембранами аппарата Гольджи и перемещаются к периферии клетки (11). Слияние таких вирионов с плазматической мембраной завершается высвобождением внеклеточных вирионов. Хотя размножение вируса происходит полностью в цитоплазме, ядерные факторы могут быть вовлечены в процессы транскрипции генов и сборки вирионов.
РНК-вирусы имеют определенный лимит генетической сложности, обусловленный небольшими размерами их геномов — от 3 до 30 кб. Однако они более эффективно, чем ДНК-вирусы используют мутационный процесс для изменения своей антигенной структуры и тропизма в организме хозяина, а также для уклонения от антител и цитотоксических лимфоцитов. Высокую частоту мутаций у РНК-вирусов обычно объясняют отсутствием механизмов корректировок в синтезе РНК. Все молекулы вирусной РНК обычно реплицируют через ассиметричную транскрипцию от одной цепи, исключающую большинство корректирующих механизмов, характерных для репликации молекул ДНК. S. Holland и соавт. (1982) экспериментально доказали, что вероятность ошибки во время копирования РНК-молекулы будет в 105 — 107 раз больше, чем при копировании ДНК-молекулы. Ими также была установлена средняя частота мутаций для РНК-вирусов, составляющая приблизительно 10-4,5. Это означает, что до 10% всех молекул РНК в популяции вируса, могут содержать мутации.
Инфекционные частицы поксвирусов содержат в своем составе полную ферментативную систему транскрипции, способную синтезировать функциональную мРНК в полиаденилированной, кэпированной и метилированной форме. Это позволяет ВНО:
1) самостоятельно осуществлять эффективную защиту от ранних специфических реакций на инфекцию и противодействовать развивающимся позже специфическим реакциям;
ВНО variola maior обуславливает генерализованную инфекцию, которая в высоком проценте случаев завершается летальным исходом. Для этого вирус располагает беспрецедентным, по сравнению с вирусами других семейств, набором генов, белковые продукты которых эффективно изменяют многочисленные защитные реакции организма.
Рис.4. Общая схема синтеза ВНО молекулярных факторов, обеспечивающих вирусу преодоление защитных барьеров человека
Первым неспецифическим и, возможно, самым древним барьером, который вынужден преодолевать ВНО, является программированная гибель клеток (апоптоз). Инфицирование клетки запускает механизм ее самоубийства, благодаря чему предотвращается размножение вируса и его распространение среди соседних клеток. ВНО располагает, по крайней мере, четырьмя генами, белковые продукты которых ингибируют апоптоз по альтернативным и дублирующим механизмам.
Вторым неспецифическим барьером являются местные воспалительные процессы. Они быстро индуцируются для ограничения распространения вируса в первые часы и дни после инфицирования, пока формируется полноценный иммунный ответ. ВНО несет гены не менее чем пяти белков, блокирующих различные этапы развития воспаления в участках размножения вируса (SPI-2, G3R, растворимых аналогов рецепторов фактора некроза опухолей — TNF и гамма-интерферона — гаммаlFN) и предотвращающих развитие системных реакций (растворимый рецептор интерлейкина-1бета — IL-1 бета). Как правило, все эти белки обладают одновременно несколькими активностями. Например, TNF-связывающий белок необходим еще и для развития генерализованной инфекции, столь характерной для ВНО. Поэтому эти белки считаются факторами вирулентности.
Система блокирования интерферона у ВНО также мультигенна (не менее 5 белков), поэтому он очень устойчив к его действию. Синтезируемые вирусом аналоги растворимых рецепторов IFN обоих типов, интерферируют с IFN, связывая его клеточные рецепторы. Это приводит к блокированию антивирусного состояния клетки и предотвращает лейкоцитарную инфильтрацию в участки вирусной репликации.
Для облегчения распространения ВНО по тканям организма хозяина, в его геноме содержится ген C11R VAC-COP, кодирующий белок VGF, отнесенный к семейству эпидермального фактора роста. Он стимулирует рост и / или метаболическую активность неинфицированных клеток, обеспечивая тем самым распространение ВНО по организму. На эффективность диссеминации ВНО в организме человека также влияют белки оболочки внеклеточных вирионов (прежде всего, гемагглютинин) и анкиринподобные белки (определяют круг хозяев вируса). Пока не идентифицированы вирусные белки, подавляющие созревание гликопротеидов главного комплекса гастосовместимости класса I и тем самым снижающих эффективность представления на поверхности инфицированной клетки вирусных антигенов специфическим цитотоксическим Т-лимфоцитам.
Однако большое количество синтезируемых ВНО белковых структур неизбежно обнаруживаются иммунной системой хозяина. Поэтому, патогенез ВНО построен на компромиссе между скоростью развития иммунного ответа хозяина (индуцируется полный спектр клеточно-опосредованных и гуморальных иммунных ответных реакций) и скоростью размножения вируса до количеств, достаточных для его передачи другому реципиенту.
У переболевших оспа оставляет длительный, стойкий и стерильный иммунитет, что исключает возможность повторного использования вирусом для своего размножения того же хозяина. Эта та цена, которую вирус платит за сложность своего генома иммунной системе человека. Однако заболевший успевает инфицировать от 5 (в среднем) до 38 человек, из них не менее трети погибнет — это уже цена, которую платим мы за то же самое.
ВНО среди людей распространяется воздушно-капельным путем. В организме человека он предварительно накапливается в альвеолярных макрофагах, затем по лимфатическим путям проникает в лимфатические узлы, где происходит его репликация. Ортопоксвирусы в отношении фагоцитирующих клеток ведут себя как паразитические организмы и используют их для своего размножения. Разрушившиеся фагоцитирующие клетки становятся источником вируса, а через 2 — 3 суток его обнаруживают уже в крови (первичная виремия), костном мозге, печени и селезенке.
В пробах крови больного натуральной оспой в этот период инфекционного процесса можно обнаружить как инфицированные, так и не инфицированные лейкоциты, но в основном репликация ВНО происходит в моноцитах / макрофагах. Лимфоциты остаются неинфицированными, они сохраняют свою функцию, хотя при этом и наблюдается выраженная лимфопения. Вирус распространяется из лимфатических узлов фагоцитирующими клетками крови по внутренним органам через выносящие (эфферентные) лимфатические сосуды. Затем вирус проникает в эпителий кожи и слизистых, где начинается его репликация. Появляются энантемы и экзантемы, инфицирование которых вторичной микрофлорой определяет эволюцию кожных элементов из везикул в пустулы. Количество вируса через 4 — 5 суток уже превышает емкость ретикуло-эндотелиальной системы, и он вновь проникает в кровяное русло.
Вторичная виремия обычно соответствует началу клинической манифестации болезни. Специфические антитела выявляются в крови на седьмые сутки после инфицирования, и их максимальный уровень достигается на 14 сутки. Уже на 10-е сутки болезни заразность больного для окружающих резко снижается. Через 4 недели от начала болезни вирус невозможно выделить из отделяемого носоглотки и из мочи реконвалесцента. У выживших людей развивается стерильный иммунитет.
Интенсивная репликация ВНО в макрофагах сопровождается явлением, которое из-за его неблагоприятного исхода, назвали «цитокиновым штормом» («cytokine storm»). Оно проявляется каскадной активацией и выбросом инфицированными макрофагами значительных количеств различных лимфокинов (monocyte chemoattractant protein 1, macrophage inflammatory protein 1бета, IFN-гамма, IL-6 и др.) и развитием клиники токсемии и шока, приводящих больного к смерти.
Для освобождения организма от ортопоксвирусов, необходимо участие в иммунных ответах CD4 + T-клеток — субпопуляция Т-клеток, оказывающая помощь В-клеткам в продукции специфических антител; и MHC класса II — эти молекулы локализованы на поверхности макрофагов и обеспечивают включение в иммунный ответ CD4 T-клеток. В ответах на острую инфекцию, вирусоспецифические антитела наиболее эффективно освобождают организм от вируса. Вирус разрушается по различным механизмам, предполагающим участие таких антител. Во-первых, антитела могут непосредственно связывать вирус, вызывая его агрегацию и препятствуя адсорбции и интернализации в клетках. Во-вторых, они могут связывать вирус, вызывая его разрушение с помощью комплемента или опсонизации, а затем посредством фагоцитоза. Антитела могут связывать инфицированные клетки хозяина, вызывая цитотоксические реакции со стороны клеток-киллеров и др.
Геморрагическая форма натуральной оспы с летальным исходом развивалась у людей с врожденными дефектами иммунной системы, проявившимися отсутствием антител в ответ на вакцинацию против натуральной оспы. При инфицировании таких больных ВНО, у них развивалась выраженная виремия, вирус в высоких титрах обнаруживали в фарингеальном тракте.
ВНО и другие ортопоксвирусы представляют собой очень благодарный для иммунолога объект исследования, так как реакции иммунной системы человека на них всегда укладываются в представления об иммунитете и инфекции, сложившиеся еще в начале ХХ столетия. В таких исследованиях открывается обширное поле деятельности по детализации прописных истин из старых учебников, поэтому они всегда «глубоко научны».
Основной антигеной детерминантой поксвирусов и мишенью для протективных антител является консервативный белок L1 (другое название L1R). У вируса вакцины (так называют ортопоксвирус, используемый в настоящее время для вакцинации людей против ВНО), вируса оспы обезьян и ВНО этот белок различается отдельными аминокислотами. Антитела к L1 способны блокировать инвазию ортопоквирусов в клетки. Поэтому он рассматривается учеными в качестве кандидата на включение в перспективные противооспенные вакцины.
Вакцинация обычно предупреждает заражение ВНО в течение, по меньшей мере, 5-10 лет. При развитии болезни ее симптомы у вакцинированных лиц менее выражены, чем у невакцинированных. Так как специфические антитела считаются «первой линией обороны» против вторжения возбудителей инфекционных болезней, их обычно выявляют для оценки иммунной защиты индивидуума. По данным Gallwitz S. et al. (2003), использовавших ферментативный иммуноанализ для поиска антител к вирусу вакцины у лиц, вакцинированных 30-60 лет назад, их можно обнаружить у 65% обследуемых, вакцинированных однократно; и у 80 % обследуемых, вакцинированных два раза и более. Crotty S. et al. (2003) продемонстрировали присутствие у лиц, вакцинированных более 50 лет назад, В-клеток памяти, специфических к вирусу вакцины. Количество таких клеток после вакцинации снижается в течение нескольких лет до уровня, представляющего примерно десятую часть от достигнутого максимума. Далее количество противооспенных антител (0,1% от общего количества IgG + B-клеток) не меняется практически на протяжении всей оставшейся жизни вакцинированного. Этим объясняется выраженная антительная реакция на противооспенную ревакцинацию. В опытах Frey S.E. et al. (2003) вакцинация ранее вакцинированных лиц давала очень хороший результат даже при десятикратном разведении вакцины.
1. Научный обзор исследований вируса натуральной оспы, 1999-2010 гг. Antonio Alcami, Inger Damon, David Evans, John W. Huggins, Christine Hughes, Peter B. Jahrling, Grant McFadden, Hermann Meyer, Bernard Moss, Sergei Shchelkunov, Evgeni Stavskiy, Nina Tikunova. Всемирная организация здравоохранения, 2011 г.
2. Консультативный комитет ВОЗ по исследованию вируса натуральной оспы. Всемирная организация здравоохранения. Доклад пятнадцатого совещания, Женева, Швейцария, 24-25 сентября 2013 г.
3. Супотницкий М.В. Эволюционная патология. К вопросу о месте ВИЧ-инфекции и ВИЧ/СПИД-пандемии среди других инфекционных, эпидемических и пандемических процессов — М., 2009. — 400 с.: ил.
4. Супотницкий М.В. Натуральная оспа, оспа обезьян. В кн.: Супотницкий МВ. Биологическая война. Введение в эпидемиологию искусственных эпидемических процессов и биологических поражений. М.: «Кафедра», «Русская панорама»; 2013.
5. Супотницкий М.В. Микроорганизмы, токсины и эпидемии. Глава 1.6. Патогенность вирусов.
6. http://www.who.int/ru/ Всемирная организация здравоохранения, 2015 г.
Исследование понятия и основных особенностей ДНК-геномных вирусов. Изучение жизненного цикла вируса. Характеристика вируса папилломы человека. Описание болезней, вызываемых вирусом папилломы человека. Лабораторная диагностика папилломавирусной инфекции.
реферат [94,2 K], добавлен 17.03.2014
Вирус иммунодефицита человека — ретровирус из рода лентивирусов, вызывающий медленно прогрессирующее заболевание — ВИЧ-инфекцию. Схематическое строение вируса. Проникновение ВИЧ в клетку человека. Транспорт вирусной ДНК в ядро и интеграция в геном.
презентация [20,6 M], добавлен 03.05.2017
Латенция и вирогения как типы взаимодействия вируса с клеткой. Процесс адсорбции вируса и его проникновения в клетку, синтез вирусных белков. Этапы созревания дочерних вирусных частиц, способы их выхода из клетки, общие принципы сборки вирионов.
реферат [18,6 K], добавлен 29.09.2009
Отрицательная роль вирусов в жизни человека как возбудителей ряда опасных заболеваний: оспы, гепатита, энцефалита, краснухи, кори, бешенства, гриппа. «Индикаторы жизни»: происхождение и природа вирусов, их строение. Взаимодействие вируса с клеткой.
реферат [164,7 K], добавлен 01.04.2009
Вирусы как первая форма жизни на Земле и возбудители болезней. Предыстория их открытия. Схема проведения биологического эксперимента. Строение вируса и бактериофага. Виды вирусных заболеваний человека. Жизненный цикл вируса иммунодефицита человека.
презентация [690,1 K], добавлен 27.02.2011
Свойства вирусов, особенности их строения и классификация. Взаимодействие вируса с клеткой. Процессы, связанные с размножением вируса. Описание основных вирусных заболеваний. Эволюция вирусов на современном этапе. Влияние загрязнения внешней среды.
реферат [466,4 K], добавлен 24.03.2011
Организация генома и кодируемые белки вируса иммунодефицита человека. Транскрипция провирусной дезоксирибонуклеиновой кислоты и синтез вирусных веществ. Анализ получения сыворотки и плазмы крови. Характеристика референсных сиквенсов и электрофореграмм.
дипломная работа [1,3 M], добавлен 04.06.2017
Схема строения булавовидного бактериофага. Жизненный цикл вируса на примере ортомиксовирусов, к которым относятся вирусы гриппа А, В и С типов. Описание вирусов иммунодефицита человека (ВИЧ), вызывающего СПИД, табачной мозаики, герпеса 8 типа, гриппа.
презентация [864,8 K], добавлен 07.09.2010
Таксономия вируса и морфология вириона. Антигенная структура и вариабельность. Гемагглютинирующие и гемадсорбирующие свойства вирусов, их культивирование в различных живых системах. Диагностика чумы плотоядных. Способы введения вакцин и схема вакцинации.
реферат [33,6 K], добавлен 25.04.2015
Эволюционное происхождение. Свойства вирусов. Природа вирусов. Строение и классификация вирусов. Взаимодействие вируса с клеткой. Значение вирусов. Вирусные заболевания. Особенности эволюции вирусо на соременном этапе.
реферат [299,2 K], добавлен 22.11.2005
Работы в архивах красиво оформлены согласно требованиям ВУЗов и содержат рисунки, диаграммы, формулы и т.д.
PPT, PPTX и PDF-файлы представлены только в архивах.
Рекомендуем скачать работу.
источник
Вирус вызывает особо опасное высококонтагиозное инфекционное заболевание, характеризующееся общим поражением организма и обильной сыпью на коже и слизистых оболочках. В прошлом отмечались эпидемии и пандемии заболевания, сопровождающиеся высокой летальностью. В 1892 г. Г.Гварниери, исследуя под микроскопом срезы роговицы зараженного кролика, обнаружил специфические включения, впоследствии названные тельцами Гварниери, представляющие собой скопления вирусов натуральной оспы. Возбудитель оспы впервые обнаружен в световом микроскопе Е. Пашеном (1906).
Таксономия. Вирус натуральной оспы – ДНК-содержащий; относится к семейству Poxviridae (от англ, рох – язва), роду Orthopoxvirus.
Морфология, химический состав, антигенная структура. Вирус натуральной оспы является самым крупным вирусом, при электронной микроскопии имеет кирпичеобразную форму с закругленными углами размером 250-400 нм. Вирион состоит из сердцевины, имеющей форму гантели, двух боковых тел, расположенных по обе стороны от сердцевины, трехслойной наружной оболочки. Вирус содержит линейную двунитчатую ДНК, более 30 структурных белков, включая ферменты, а также липиды и углеводы.В составе вируса обнаружено несколько антигенов: нуклео-протеидный, растворимые и гемагглютинин. Вирус натуральной оспы имеет общие антигены с вирусом осповакцины (коровьейоспы).
Культивирование. Вирусы хорошо размножаются в куриных эмбрионах, образуя белые плотные бляшки на хорионаллантоисной оболочке. Репродукция вируса в культуре клеток сопровождается цитопатическим эффектом и образованием характерных цитоплазматических включений (телец Гварниери), имеющих диагностическое значение.
Резистентность. Вирусы оспы обладают довольно высокой устойчивостью к окружающей среде. На различных предметах при комнатной температуре сохраняют инфекционную активность в течение нескольких недель и месяцев; не чувствительны к эфиру и другим жирорастворителям. При температуре 100ºС вирусы погибают моментально, при 60ºС – в течение 15 мин, при обработке дезинфицирующими средствами (фенол, хлорамин) – в течение нескольких часов. Длительно сохраняются в 50 % растворе глицерина, в лиофилизированном состоянии и при низких температурах.
Восприимчивость животных. Заболевание, сходное по клиническим проявлениям с болезнью человека, можно воспроизвести только у обезьян. Для большинства лабораторных животных вирус оспы малопатогенен.
Эпидемиология. Натуральная оспа известна с глубокой древности. В XVII-XVIII вв. в Европе оспой ежегодно болело около 10 млн человек, из них умирало около 1,5 млн. Оспа являлась также главной причиной слепоты. На основании высокой контагиозности, тяжести течения и значительной летальности натуральная оспа относится к особо опасным карантинным инфекциям.
Источником инфекции является больной человек, который заразен в течение всего периода болезни. Вирус передается воздушно-капельным и воздушно-пылевым путями. Возможен контактно-бытовой механизм передачи – через поврежденные кожные покровы.В начале 20-х годов текущего столетия в результате применения оспенной вакцины удалось ликвидировать натуральную оспу в Европе, Северной Америке, а также в СССР (1936). Отечественные ученые В. М. Жданов, М. А. Морозов и др. обосновали возможность осуществления глобальной ликвидации оспы. В 1958 г. по предложению СССР Всемирная организация здравоохранения приняла резолюцию и разработала программу по ликвидации оспы во всем мире, которая была успешно выполнена благодаря глобальной противооспенной вакцинации людей. В 1977 г. в Сомали был зарегистрирован последний случай оспы в мире. Таким образом, оспа исчезла как нозологическая форма.
Патогенез и клиническая картина. Вирус оспы проникает в организм через слизистую оболочку дыхательных путей и реже через поврежденную кожу. Размножившись в регионарных лимфатических узлах, вирусы попадают в кровь, обусловливая кратковременную первичную вирусемию. Дальнейшее размножение вирусов происходит в лимфоидной ткани (селезенка, лимфатические узлы), сопровождается повторным массивным выходом вирусов в кровь и поражением различных систем организма, а также эпидермиса кожи, так как вирус обладает выраженными дерматотропными свойствами. Инкубационный период составляет 8-18 дней. Заболевание начинается остро, характеризуется высокой температурой тела, головной и поясничной болью, появлением сыпи. Для высыпаний характерна последовательность превращения из макулы (пятна) в папулу (узелок), затем в везикулу (пузырек) и пустулу (гнойничок), которые подсыхают с образованием корок. После отпадения корок на коже остаются рубцы (рябины). По тяжести течения различают тяжелую форму («черная» и сливная оспа) со 100% летальностью, среднюю с летальностью 20-40% и легкую с летальностью 1-2%. К числу легких форм натуральной оспы относится вариолоид – оспы у привитых. Вариолоид характеризуется отсутствием лихорадки, малым количеством оспенных элементов, отсутствием пустул или сыпи вообще.
Иммунитет. У переболевших людей формируется стойкий пожизненный иммунитет, обусловленный выработкой антител, интерферона, а также клеточными факторами иммунитета. Прочный иммунитет возникает также в результате вакцинации.
Лабораторная диагностика. Работа с вирусом натуральной оспы проводится в строго режимных условиях по правилам, предусмотренным для особо опасных инфекций. Материалом для исследования служит содержимое элементов сыпи на коже и слизистых оболочках, отделяемое носоглотки, кровь, в летальных случаях – кусочки пораженной кожи, легкого, селезенки, кровь. Экспресс-диагностика натуральной оспы заключается в обнаружении: а) вирусных частиц под электронным микроскопом; б) телец Гварниери в пораженных клетках; в) вирусного антигена с помощью РИФ, РСК, РПГА, ИФА и других специфических реакций. Выделение вируса осуществляют в куриных эмбрионах или клеточных культурах. Идентификацию вируса, выделенного из куриного эмбриона, проводят с помощью РН (на куриных эмбрионах), РСК или РТГА. Вирус, выделенный на культуре клеток, обладает гемадсорбирующей активностью по отношению к эритроцитам кур, поэтому для его идентификации используют реакцию торможения гемадсорбции и РИФ. Серологическую диагностику осуществляют с помощью РТГА, РСК, РН в куриных эмбрионах и на культурах клеток.
Специфическая профилактика и лечение. Живые оспенные вакцины готовят накожным заражением телят или куриных эмбрионов вирусом вакцины (осповакцины). Повсеместная вакцинация населения привела к ликвидации натуральной оспы на земном шаре и отмене с 1980 г. обязательного оспопрививания. Поэтому оспенные вакцины необходимо использовать только по эпидемическим показаниям с целью экстренной массовой профилактики. Методы введения вакцин – накожно или через рот (таб-летированная форма). После вакцинации формируется прочный иммунитет.
Для лечения натуральной оспы, помимо симптоматической терапии, применяли химиотерапевтический препарат – метисазон.
Не нашли то, что искали? Воспользуйтесь поиском:
источник
Вирус натуральной оспы
Вирус натуральной оспы (Variola major) из семейства ортопоксвирусов. Натуральная (черная) оспа — высокозаразное заболевание, передающееся контактным путем и приводящее к смерти в 40-90 процентах случаев. В конце XVIII века от него ежегодно умирало, по оценкам, до 400 тысяч европейцев. В XX веке оспа стала причиной от 300 до 500 миллионов смертей. Однако успешная всемирная прививочная кампания, начавшаяся в XIX веке, привела к полной победе над этим заболеванием в 1979 году. На сегодняшний день оспа считается единственной искорененной инфекцией.
Натуральная оспа – очень заразное заболевание. Заразны почти все выделения больного: мокрота, капельки слизи из зева и полости рта, разбрызгиваемые при кашле, чихании, крике. Заразны моча, кал. Вирус оспы долго сохраняется в постельном белье, домашних вещах, особенно в сухом состоянии. Заражение происходит либо непосредственно от больного, либо через зараженные предметы и вещи.
В 1886 г. Бьюст обнаружил возбудителя оспы. В 1906 г. Пашен предложил окрашивать вирионы специальной краской, позволяющей наблюдать их в световом микроскопе. Вирусы оспы довольно крупные и первыми были рассмотрены под микроскопом. Окрашенные вирионы получили название «тельца Пашена». Вирус оспы содержит двухцепочную линейную ДНК, размножается в цитоплазме клеток, образуя характерные включения.
Возбудитель оспы проникает в организм человека через верхние дыхательные пути (слизистую носоглотки) воздушно-капельным путем, а также через кожу. Затем возбудитель попадает в кровь, с током которой разносится по всему организму. Вирус интенсивно размножается в клетках костного мозга и печени, откуда опять попадает в кровь, затем – в большом количестве в клетки слизистой и кожи. Здесь вирус интенсивно размножается и вызывает типичное поражение, последовательно проходя стадии папулы, везикулы, пустулы, корочки и рубца. Покрытое «оспинами» лицо – типичное последствие перенесенной оспы. Оспенный больной заразен примерно с третьего дня после заражения (инкубационный период – до 12 дней) и до отпадения оспенных корочек.
Оспа известна с древнейших времен. Рукописные памятники Древнего Египта позволяют предполагать, что она возникла на территории Центральной Африки. Так, в египетском папирусе, составленном Аменофисом I за 4 тыс. лет до н.э., описана оспа. На коже мумии, захороненной в Египте за 3 тыс. лет до н.э., сохранились оспенные поражения. В древнейшем китайском трактате «Чеу-Чиуфа» упоминается оспа, которую китайцы называли «ядом из материнской груди» (1120 г. до н.э.). Первое классическое описание оспы сделал арабский врач Аль-Рази (IX–X в. н.э.). Ибн-Сина (980–1037) – первый врач, описавший оспу как заразную болезнь.
В прошлом оспа была самым опасным и распространенным заболеванием. Столетиями она свирепствовала в Азии, откуда в VI в. н.э. сарацины завезли ее в Европу.
В XVI — XVIII вв. произошел наиболее убийственный «расцвет» оспы, тогда от этой болезни умирал каждый третий ребенок. В Европе в отдельные годы оспой заболевало до 12 млн человек, 1,5 млн человек умирало.
Оспа была широко распространена в войсках и, передвигаясь с ними, страшнее войн опустошала целые области.
Древний историк Курциус (I в. до н.э.) писал, что оспа уничтожила воинов Александра Македонского, возвращающихся из завоеванной Индии.
Во время эпидемий оспа поражала молодых и старых, простолюдина и владыку, не щадя никого, проникала в хижину бедняка и во дворцы царей. От оспы умерли русский император Петр II, австрийский император Иосиф, короли Франции – Людовик XIV, Людовик XV, король Нидерландов Вильгельм II Оранский, королева Англии Анна.
Древний историк Тебезиус написал: «Никакой народ, никакая раса, никакое звание, никакой темперамент, ни возраст, ни пол не щадились оспой. Все трепетали перед ней».
Оспа приобретала чудовищную силу на территориях, куда она проникала впервые. В XVI в. конкистадоры завезли оспу в Америку. Возможно, это было первое бактериологическое оружие, использованное против людей: индейцам преднамеренно оставляли одеяла от больных оспой, развешивали на деревьях рубахи, пропитанные оспенным гноем.
В 1520 г., во время завоевания Мексики от оспы погибли 3,5 млн человек. Вымирали целые племена. Из оставленных очевидцами описаний следует, что «несметное количество трупов туземцев валялось в лесах». Страна опустела. В 1576 г. в Перу погибло свыше 2 млн человек.
В Средние века при возникновении оспы основной рецепт гласил: «Быстро, далеко, долго», т.е. предписывалось убираться быстро, далеко и долго не возвращаться.
В Европе даже в XVIII в. от оспы ежегодно погибало 0,5 млн человек. Многие из «благополучно» перенесших оспу слепли, лица их обезображивались.
В 1563 г. оспа была занесена в Бразилию. Во время эпидемии только в провинции Чату погибли 100 тыс. человек.
Методы заражения куриных эмбрионов: а – заражение в полость аллантоиса; б – заражение в амнион закрытым способом; в – заражение в амнион открытым способом; г – заражение на хорионаллантоисную оболочку
Путешествие в невидимый мир
Англичане занесли оспу на Восточное побережье Северной Америки. В 1616–1617 гг. зарегистрирована крупнейшая эпидемия среди индейцев. В частности, почти полностью погибло племя алгонкинов, населявшее леса Массачусетса.
В Европе даже в XVIII в. от оспы ежегодно погибало 0,5 млн человек. Многие из «благополучно» перенесших оспу слепли, лица их обезображивались оспенными знаками.
В Австралию оспу завезли в конце XVIII в.
В Россию оспа впервые попала в XVI в. В 1610 г. инфекция была занесена в Сибирь и унесла жизни около трети населения. Люди бежали в леса, тундру, горы. На лицах идолов выжигали оспенные знаки для обмана злого духа. Но ничто не могло остановить безжалостного убийцу.
В дореволюционной России процент заболеваемости оспой был высок. По дорогам, городам и селам бродили нищие, ослепшие после оспы. В период 1901–1910 гг. только в европейской части России с населением 70–80 млн человек оспа унесла 414 143 жизнь.
В Средние века во время эпидемий оспы основной «рецепт» был таков: «быстро, далеко, долго», т.е. предписывалось убираться быстро, далеко и долго не возвращаться.
Академик Н.Ф. Гамалея писал: «. Не видя пользы от стремления избежать заразы, человечество перешло к противоположной крайности и стало искать ее». Действительно, попытки защититься от оспы так же древни, как и сама оспа.
С течением времени стало ясно, что люди, переболевшие оспой, больше не заболевали. Кроме того, в некоторых случаях оспа протекает очень легко. У многих народов стало применяться искусственное заражение легкой формой оспы, или вариоляция.
В древней Индии за 1000 лет до н.э. брахманы надевали на детей рубашки, смоченные гноем легкобольных оспой. Китайцы через бамбуковые трубочки вдували в нос измельченные оспенные корочки. Арабы давали пить настой оспенных корочек. В Шотландии перевязывали ниткой, смоченной оспенным гноем, слегка оцарапанную ручку ребенка (шотландский метод). Славяне стегали людей прутьями, смоченными оспенным гноем. На Кавказе прививки делали иголками, смоченными выделениями пустул.
В Оттоманской империи в гарем поставляли только девочек со шрамиком на руке или бедре – результатом прививки против оспы. Эта была гарантия от заболевания и, следовательно, сохранения красоты лица.
В Западной Европе со времен Средневековья бытовал особый способ предохранения от оспы – «покупка оспы». Здорового ребенка приводили к больному, и малыш, протягивая монеты больному, говорил: «Я покупаю у тебя оспу». Домой ребенок возвращался с корочками оспы, плотно зажатыми в кулак. В Аравии также «покупали» оспу, расплачиваясь за нее изюмом или винными ягодами. Уличные глашатаи на улицах объявляли о продаже оспы.
В Средние века в Константинополе сложилась своеобразная школа вариоляции. Известная писательница, леди Монтегю (1689–1762), сама перенесшая оспу, в 1717 г., будучи в качестве жены посла в Константинополе, привила оспу сыну, а через четыре года, уже в Лондоне, – дочери. В 1721 г. по ее рекомендации для проверки безопасности и эффективности вариоляции привили оспу заключенным Ньюгетской тюрьмы. Все окончилось благополучно, как и в описанных выше случаях.
В то же время далеко не все прививки заканчивались хорошо. В большинстве случаев вариоляция приводила к трагедиям, поэтому прививки легкой формы оспы в конце XVIII в. практически прекратились.
Несмотря на то, что Екатерине II и ее сыну Павлу в 1768 г. была удачно привита оспа, вариоляцию в России почти не проводили. Правда, надо отметить, что в воспитательных домах для подкидышей прививки делали постоянно. А.Н. Радищев (1749–1802) во время ссылки в Сибирь занимался вариоляцией.
В 1796 г. в Беркли была открыта новая страница истории борьбы с оспой, связанная с именем английского врача Эдварда Дженнера (1749–1823). Свое открытие Дженнер сделал на основании замечательных народных наблюдений: человек, заразившийся от больной оспой коровы, становится невосприимчивым к натуральной оспе. Коровья оспа поражает вымя животного, поэтому чаще заражаются доярки, у которых на кистях рук образуются оспенные пузырьки.
Дженнер в течение долгих 25 лет проверял народное наблюдение. С большим терпением и исключительной добросовестностью врач изучал каждый случай. Наконец он решился на прививку коровьей оспы пастушонку, восьмилетнему Джеймсу Фиппсу. Оспенный материал он взял у Сарры Нельм, заразившейся коровьей оспой. Прививка прошла хорошо. Но этого было мало. Требовалось доказать, что привитой ребенок не заболеет натуральной оспой. После мучительных раздумий Дженнер идет на решительный шаг и заражает Фиппса натуральной оспой. Мальчик не заболел.
Начало оспопрививанию было положено. Однако прошло немало времени, пока это замечательное открытие получило признание. К сожалению, многие ученые не поняли этого метода. Так, Лондонское Королевское общество возвратило Дженнеру его работу «Исследование причин и действие коровьей оспы», сопроводив наставлением «не компрометировать своей научной репутации подобными статьями». Дженнеру пришлось печатать этот труд за свои деньги. Во многих странах, в том числе и на родине ученого, духовенство с негодованием отвергло прививки коровьей оспы.
Первая вакцинация против оспы в России проходила в торжественной обстановке. В 1801 г. профессор Московского университета Ефрем Мухин привил оспу Антону Петрову из воспитательного дома. Мальчику присвоили фамилию Вакцинов, пожаловали дворянство и пенсию. В период 1805–1810 гг. в России вакцинировали около 1 млн человек. В 1824–1847 гг. вакцинировано было примерно 24 млн младенцев. К сожалению в России прививка была передана в руки невежественных «оспенников» – людей, обязанных за мизерную плату проводить оспопрививание, но зачастую имевших лишь смутное представление о его сущности. Результатов прививок никто не проверял.
Со временем во многих странах убедились, что Дженнер предложил безопасный способ борьбы с натуральной оспой. Однако не все в методе английского врача было безупречно. Для прививки использовали так называемую «гуманизированную лимфу», т.е. содержимое оспенных пузырьков человека, зараженного коровьей оспой. Прививку делали с ручки на ручку – от одного привитого ребенка к другому. В этом-то и была слабая сторона метода Дженнера. Кроме того, при оспопрививании существовала возможность заражения кожными болезнями.
Название «вакцина» (от лат. vacca корова) в науку ввел Луи Пастер (1822–1895), указавший: «Я придаю слову «вакцина» более широкое значение в надежде, что наука оставит его, как выражение признательности к заслугам Дженнера».
Были разработаны новые методы получения вакцины против оспы. Для ее производства отбирали здоровых телят определенной масти и заражали их оспой. Перед заражением на боках и животе телят выбривали шерсть, тщательно мыли и дезинфицировали выбритые участки кожи. Через несколько дней созревали оспенные пузырьки, в которых накапливались вирусы. После сбора и специальной обработки оспенного материала получали готовую вакцину в виде прозрачной вязкой жидкости.
Большая заслуга нашего соотечественника М.А. Морозова состояла в разработке метода получения сухой вакцины против оспы. Преимущества ее очевидны: сухая вакцина более стойкая, имеет более длительный срок годности. Позже была создана новая сухая вакцина, получаемая при заражении вирусом оспы куриных эмбрионов.
В 1979 г. Всемирная организация здравоохранения (ВОЗ) констатировала полное исчезновение вируса натуральной оспы в природе (сохранились лишь образцы в Центре контроля и предотвращения болезней в Атланте (США) и Российском научном центре вирусологии и биотехнологии в Кольцово) и рекомендовала прекратить вакцинацию населения. В 1999 г. все вирусы оспы в лабораториях должны были быть уничтожены, но сохранены фрагменты ДНК. Тем не менее, ВОЗ имеет запас в 500 тыс. доз вакцины против оспы и будет его поддерживать.
Вирусы оспы — наиболее крупные из всех вирусов животных. Под электронным микроскопом они выглядят как большие овальные (кирпичеобразные) частицы размером около 250-350×200-270 нм.
В структуре вирусов оспы различают три основных компонента: двояковогнутую сердцевину, овальные боковые тела и оболочку вириона. Сердцевину вириона составляют ДНК и связанные с нею белки. Сердцевина окружена гладкой мембраной (толщиной около 5 нм), снаружи покрытой слоем вертикально уложенных и плотно прилегающих друг к другу цилиндрических субъединиц (5×10 нм). Вогнутость сердцевины с обеих сторон занята овальными образованиями (неизвестной природы), называемыми боковыми телами. Они как бы сдавливают сердцевину, придавая ей форму двояковогнутого диска, имеющего на разрезе вид гантели.
Геном вирусов оспы представлен одной линейной молекулой двуцепочечной ДНК с ковалентно замкнутыми концами размером 130 тпн (парапоксвирусы) — 280 тпн (авипоксвирусы). На обоих концах генома имеются идентичные, но противоположно ориентированные тандемы повторяющихся нуклеотидных последовательностей. Геномы вирусов оспы способны кодировать около 200 белков, из которых не менее 100 входят в структуру вириона. Однако функциональные особенности определены лишь у небольшого количества вирусных белков. Наиболее важными из них являются ферменты, участвующие в синтезе вирусных нуклеиновых кислот и структурных компонентов вирионов. Например, синтез ДНК-полимеразы, ДНК-лигазы, РНК-полимеразы, энзимов, связанных с кэппированием и полиаденилированием мРНК и тимидинкиназы.
Инфекционные вирусные частицы содержат системы транскрипции, которые могут выполнять in vitro синтез РНК, а также способны полиаденилировать, кэппировать и метилировать. В вирусных частицах содержится большое количество кодируемых вирусом энзимов и других биологически активных факторов.
Некоторые гены вирусов оспы кодируют белки, которые секретируются инфицированными клетками и вызывают ответ организма на инфекцию, в том числе и формирование иммунитета.
К таким вирокинам относятся гомологичный эпидермальный фактор роста, белок, снижающий активность комплемента, вирокины, обеспечивающие устойчивость к интерферону, и другие супрессоры иммунного ответа, подавляющие действие некоторых цитокинов организма хозяина.
Вирусы оспы обычно характеризуются узким спектром хозяев. Они передаются чаще респираторным путем и реже через поврежденную кожу. Вирусы оспы овец, свиней, птиц и миксоматоза передаются также через укус членистоногими. Вирусы оспы устойчивы в окружающей среде и могут сохраняться годами в высохших струпьях кожи или других вируссодержащих материалах.
Большинство вирусов оспы хорошо размножаются в культуре клеток. Исключение составляют парапоксвирусы, вирус оспы свиней и вирус контагиозного моллюска. Однако они, так же как и ортопоксвирусы, легко образуют оспины на хориоал-лантоисной оболочке куриных эмбрионов.
Вирусы оспы размножаются в цитоплазме, и, в отличие от других ДНК-вирусов, их размножение происходит независимо от ядра клетки, благодаря кодированию всех ферментов, необходимых для транскрипции и репликации вирусного генома. Некоторые из этих функций выполняются вирионами как таковыми. После слияния оболочки вириона с плазматической мембраной клетки или после эндоцитоза вирусная сердцевина освобождается в цитоплазму. Транскрипция вирусного генома характеризуется каскадностью, когда каждый временной класс генов («ранние», «промежуточные» и «поздние» гены) требует наличия специфических транскрипционных факторов, которые создаются предшествующим временным классом генов. Факторы, обеспечивающие транскрипцию промежуточных генов, кодируются ранними генами, тогда как факторы транскрипции поздних генов кодируются промежуточными генами. Транскрипция начинается вирионной транскриптазой и другими факторами, находящимися в сердцевине вириона, которые способны образовывать мРНК спустя минуты после инфицирования.
Белки, образующиеся в результате трансляции этих мРНК, включая ДНК-полимеразу, тимидинкиназу и несколько других ферментов, необходимы для репликации вирусной ДНК. Репликация ДНК ВО связана с синтезом конкатемерных промежуточных структур, которые затем разрезаются с образованием единиц геномной длины. Детали этого процесса недостаточно изучены. С началом репликации ДНК происходит резкий сдвиг в генной экспрессии. Транскрипция «промежуточных» и «поздних» генов контролируется специфическими вирусными белками. Некоторые продукты транскрипции ранних генов образуются на поздней стадии инфекции, упаковываются в вири-оны и используются в следующем круге инфекции. Так как в состав вирусов оспы входит большое количество белков, не является неожиданным, что сборка вирионов есть комплексный процесс, который длится несколько часов и все еще целиком не выяснен.
Образование вириона связано с вхождением ДНК внутрь незрелой сердцевинной структуры, которое затем завершается включением наружных покрывающих слоев. Репликация и сборка вирионов происходят в разных местах цитоплазмы в так называемых виропластах или вирусных фабриках. Вирионы выходят из клетки почкованием (оболочечные вирионы), или путем экзоцитоза, или при лизисе клеток (вирионы без оболочки). Большинство вирионов освобождаются при цитолизе и не имеют оболочки. Вирионы с оболочкой и без нее обладают инфекционностью, но первые, вероятно, играют более значительную роль в возникновении и распространении заболевания, а также в создании иммунитета.
В очищенном вирусе осповакцины (ВОВ) выявлены белки с молекулярной массой 10-250 кД. Многие из них сосредоточены в сердцевине вириона. Два структурных гликопротеина располагаются между оболочкой и сердцевиной. В оболочке ВОВ содержится около 10 белков, из которых иммунологически наиболее активны крупномолекулярные белки с молекулярной массой 58—32 кД (VP4c, VP6a, VP6b и VP7a). Белок 32 кД определяет круг хозяев и важен для репликации вируса.
В составе очищенного вируса оспы птиц обнаружено 29 полипептидов с молекулярной массой 14-138 кД. Наивысшей антигенной и иммуногенной активностью обладают полипептиды с молекулярной массой 35 и 37 кД. За индукцию вируснейтрализующих антител ВО ответственны антигены, расположенные на поверхности наружной оболочки вириона, и прежде всего белок 58 кД (VP4c), являющийся основным структурным компонентом трубочек (ворсинок). Антисыворотка к этому белку нейтрализовала инфекционность вируса и предотвращала образование синцития в культуре клеток. Этот белок ответственен за выработку иммунитета.
Внеклеточные вирионы покрыты дополнительной наружной оболочкой, отсутствующей у внутриклеточных вирионов. Она играет важную роль в индукции синтеза ВН-антител. Инфекционность ВОВ и ВО крупного рогатого скота, имеющих наружную оболочку, нейтрализовалась антисывороткой к имеющему эту оболочку ВОВ, но не нейтрализовалась антисывороткой к ВОВ, лишенному наружной оболочки.
За гемагглютинирующую активность ортопоксвирусов ответственны полипептид 85 кД и гликопротеид 41 кД. Во внеклеточном оболочечном ВОВ гемагглютинирующие свойства связаны с полипептидом 85 кД. Внутриклеточные вирионы (без дополнительной оболочки) практически не содержали этого полипептида. Неструктурный гемагглютинин формируется на цитоплазматических мембранах. С его образованием инфицированные клетки приобретают способность адсорбировать эритроциты. Вирусспецифические белки с молекулярной массой 32 и 37 кД, экспрессируемые на поверхности клеток, инфицированных ВОВ, делают их мишенями для специфических цитотоксических Т-лимфоцитов. МАТ-реактивные против каждого из пяти (54; 34; 32; 29 и 17—25 кД) белков наружного слоя поверхности вируса осповакцины нейтрализовали его инфекционность. В структуре полипептида 54 кД обнаружено два нейтрализующих эпитопа(Аи В). Анализ антигенных детерминант поверхностных полипептидов, проведенный с помощью МАТ, выявил в составе ортопоксвирусов, наряду с видоспецифическими, группоспецифические эпитопы.
Связывание ВОВ с нейтрализующими МАТ не препятствовало его прикреплению к клеткам-мишеням, но блокировало депротеинизацию вирионов.
Бешенство (лисса, или водобоязнь) – острое инфекционное заболевание теплокровных животных и человека, характеризующееся поражением центральной нервной системы. Чаще всего передается человеку при укусе больного животного (собаки, волка, лисицы и др.) или при попадании слюны больного животного на поврежденную кожу или слизистые оболочки. Без лечения бешенство практически всегда приводит к смерти больного.
В 1903 г. Рамленже доказал вирусную природу бешенства. Вирус бешенства относится к семейству рабдовирусов (возбудители бешенства, везикулярного стоматита у крупного рогатого скота и лошадей, а также других заболеваний у животных, от насекомых до млекопитающих, и растений). Вирион имеет пулевидную форму. Его размеры 180–300ґ65 нм. Вирион окружен белково-липидной оболочкой, содержащей единственный гликопротеин, который является видоспецифичным антигеном, и содержит спиральный нуклеокапсид с единственной РНК, а также собственную РНК-полимеразу.
Дата добавления: 2016-04-14 ; просмотров: 545 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
источник