К серьёзным достижениям XX века следует отнести разработку профилактики ОРЛ. Составной частью превентивных мероприятий при ревматизме является первичная и вторичная профилактика, направленная на предупреждение развития заболевания, возникновение рецидивов и прогрессирование патологического процесса.
Первичная профилактика направлена на предупреждение ревматизма и включает:
Повышение иммунитета (закаливание, чередование нагрузки и отдыха, полноценное питание, др.).
Выявление и лечение острой и хронической стрептококковой инфекции.
Профилактические мероприятия у предрасположенных к развитию ревматизма детей: из семей, в которых имеются случаи ревматизма или других ревматических заболеваний; часто болеющих носоглоточной инфекцией; имеющих хронический тонзиллит или перенесших острую стрептококковую инфекцию.
Вторичная профилактика направлена на предупреждение рецидивов и прогрессирование заболевания у детей с ревматизмом в условиях диспансерного наблюдения.
Системное назначение антибиотиков показано при инфекциях, вызванных β-гемолитическим стрептококком группы А (БСГА), инфицирование которым грозит развитием ревматизма. Признание этиологической роли БСГА в возникновении и развитии острой ревматической лихорадки и его влияния на дальнейшее прогрессирование ревматического процесса лежит в основе лечебно-профилактических мероприятий, направленных на борьбу с этим заболеванием, и определяет важность своевременной диагностики и назначения соответствующей антибиотикотерапии при БСГА инфекции.
Заболевания, связанные с БГСА-инфекцией: ангина, фарингит. Основные клинические признаки БГСА-инфекции: лихорадка, отсутствие кашля, регионарный лимфаденит, гнойный экссудат в области миндалин. Терапия включает применение антибактериальной терапии в течение 10 дней:
Лекарственные средства первого ряда – β-лактамные антибиотики.
1. Бензатина бензилпенициллин в/м однократно: взрослым 2,4 млн ЕД, детям с массой тела 25 кг – 1,2 млн ЕД. Бензатина бензилпенициллин в/м целесообразно назначать при сомнительной комплаентности (исполнительности) пациента в отношении перорального приёма антибиотиков, наличии ОРЛ в анамнезе у больного или ближайших родственников, неблагоприятных социально-бытовых условиях, вспышках БГСА – инфекции в детских дошкольных учреждениях, школах, интернатах и т.д.
2. Феноксиметилпенициллин внутрь за 1 час до еды в течение 10 дней. Взрослым 0,5 г х 3 раза в сутки, детям с массой тела до 25 кг – по 0,125 г х 3 раза в сутки, детям с массой тела > 25 кг – по 0,25 г 3 раза в сутки. Феноксиметилпенициллин, учитывая наличие лекарственной формы в виде суспензии, рекомендуется преимущественно детям раннего возраста;
3.Амоксициллин внутрь в течение 10 дней. Взрослым по 0,5 г х 3 раза в сутки, детям по 0,25 х 3 раза в сутки.
Цефадроксил – внутрь в течение 10 дней: взрослым по 0,5 г х 2 раза в сутки, детям 30 мг/кг/сут в 1 приём.
При непереносимости ß-лактамов:
макролиды (эритромицин, мидекамицин, спирамицин, азитромицин, кларитромицин, рокситромицин): 1) Азитромицин внутрь за 1 час до еды 5 дней: взрослым 0,5 г однократно 1 раз в 1-е сутки, затем по 0,25 в течение 4 дней; детям – 12 мг/кг/сут в 1 приём. 2) Кларитромицин внутрь в течение 10 дней: взрослым 0,25 г 2 раза в сутки; детям – 15 мг/кг/сут в 2 приёма. 3) Рокситромицин внутрь за 1 час до еды 10 дней: взрослым 0,15 г 2 раза в сутки; детям – 5 мг/кг/сут в 2 приёма. 4) Спирамицин — внутрь 10 дней: взрослым 3 млн. МЕ 2 раза в сутки; детям – 1,5 млн. МЕ в 2 приёма
линкозамиды – клиндамицин (2,4–2,7 г в сутки), линкомицин, оказывающие по отношению к БГСА четкое бактерицидное действие.
Препараты резерва (при непереносимости ß-лактамов и макролидов):
Линкомицин внутрь за 1-2 часа до еды 10 дней: взрослым 0,5 г 3 раза в сутки; детям – 30 мг/кг/сут в 3 приёма;
Клиндамицин внутрь (запивать стаканом воды) 10 дней: взрослым 0,15 г 4 раза в сутки; детям – 20 мг/кг/сут в 3 приёма
Альтернативой системной антибиотикотерапии может быть местное назначение антимикробных препаратов. В состав этих препаратов, обычно входят антисептические средства (хлоргексидин, гексетидин, бензидамин, амбазон, тимол и его производные, спирты, препараты йода, природные антисептики и др.), реже — антибиотики, сульфаниламиды, синтезированные факторы неспецифической защиты слизистых оболочек. Однако следует помнить, что при полоскании лекарственный препарат редко проникает глубже, чем передняя поверхность мягкого неба и миндалин, особенно это касается лиц с высоким глоточным рефлексом. Назначение препаратов с местным антисептическим действием в виде леденцов, пастилок и таблеток для рассасывания, безусловно, дает эффект, но ограничено лишь легкими формами инфекции.
Ингаляционный антибиотик фюзафюнжин — препарат, сочетающий в себе антибактериальные свойства с противовоспалительными и выпускаемый в форме дозированного аэрозоля. Помимо антибактериального фюзафюнжин обладает собственным противовоспалительным действием: он усиливает фагоцитоз макрофагов и ингибирует образование медиаторов воспаления.
Антимикробная терапия хронического рецидивирующего БГСА-тонзиллита/фарингита
Лекарственные средства первого ряда:
Амоксициллин/клавулановая кислота внутрь в течение 10 дней, взрослым 0,625 г 3 раза в сутки, детям 40 мг/кг/сут в 3 приёма.
Цефуроксим внутрь (сразу после еды) в течение 10 дней: взрослым по 0,25 г 2 раза в сутки, детям 20 мг/кг/сут в 2 приёма.
Препараты резерва (при непереносимости ß-лактамов и макролидов):
1) Линкомицин внутрь за 1-2 часа до еды 10 дней: взрослым 0,5 г 3 раза в сутки; детям – 30 мг/кг/сут в 3 приёма;
Клиндамицин внутрь (запивать стаканом воды) 10 дней: взрослым 0,15 г 4 раза в сутки; детям – 20 мг/кг/сут в 3 приёма
Вторична профилактика (предупреждение рецидива инфекции) состоит в длительном назначении антибиотиков пациентам, у которых уже была острая ревматическая атака. Одним из оптимальных методов такой профилактики является введение взрослым и подросткам бензатин-пенициллин 2,4 млн ЕД внутримышечно 1 раз в 3 нед.; детям с массой тела 25 кг – 1,2 млн. ЕД.
Длительность вторичной профилактики составляет:
а) для лиц, перенесших острую форму ревматической лихорадки без кардита (артрит, хорея) – не менее 5 лет после атаки или до 18-летнего возраста;
б) для больных с излеченным кардитом без порока сердца — не менее 10 лет после атаки ил до 25-летнего возраста;
б) для больных, перенесших первичную или повторную атаку заболевания с формированием порока сердца (в т.ч. оперированным) – пожизненно.
Наиболее эффективной лекарственной формой бензатина бензилпенициллина является экстенциллин. Из отечественных лекарственных средств рекомендуется бициллин – 1, который назначают 1 раз в 7 дней. Бициллин – 5 не является приемлемым для проведения полноценной вторичной профилактики.
Беременным, перенесшим ревматизм или имеющим активный ревматический процесс назначается бензатин – бензилпенициллин с 8-10 недельного срока беременности на весь период до родов. В послеродовом периоде длительность профилактики зависит от активности ревматизма.
При присоединении острой респираторной инфекции с целью вторичной профилактики рекомендуется введение пенициллина до 2 млн./сутки, или эритромицина или цефалоспоринов в течение 10 дней. Пенициллин также назначается до и после любых оперативных вмешательств.
Если имеются изменённые клапаны обязательна профилактика инфекционного эндокардита. При стоматологических вмешательствах, операциях на органах полости рта, верхних дыхательных путях, манипуляциях на ЖКТ и мочеполовом трактах применяют амоксициллин 2,0 г за 1 час до процедуры, детям до 12 лет внутрь за 1 час до процедуры амоксициллин 50 мг/кг. При аллергических реакциях на пенициллины назначают клиндамицин внутрь за 1 час до процедуры 600 мг, или цефалексин 2 г, или азитромицин 500 мг, или кларитромицин 500 мг. Детям до 12 лет: клиндамицин за 1 час до процедуры 20 мг/кг или цефалексин 50 мг/кг, или азитромицин 15 мг/кг, или кларитромицин 15 мг/кг.
Возможно парентеральное введение препаратов:
ампициллин 2 г в/в или в/м за 30 минут до вмешательства; детям до 12 лет в/в или в/м 50 мг/кг;
клиндамицин за 30 мин до процедуры в/в 600 мг или цефазолин в/м или в/в 1 г, детям до 12 лет – за 30 мин до процедуры – клиндамицин в/в 20 мг/кг или цефазолин в/м или в/в 25 мг/кг.
Антибиотикопрофилактика не является обязательной при выполнении следующих процедур: интубация, бронхоскопия, пломбирование зуба выше линии дёсен, стоматологическое протезирование, не осложнённые роды.
Лечение ревматизма всегда комплексное.
При выраженном кардите показано стационарное лечение с соблюдением постельного режима в первые 2-3 недели болезни. Полноценное белковое питание 1 г/кг, углеводы, с ограничением поваренной соли, жидкости.
Этиотропная терапия ОРЛ осуществляется пенициллином, оказывающим бактерицидное действие на гемолитический стрептококк группы А.
Взрослым назначается бензилпенициллин 500 000 – 1 000 000 МЕ в сутки в/м в течение 14 дней, затем бензатин – бензилпенициллина в дозе 2,4 млн. ЕД в/м каждые 3 недели. При непереносимости пенициллинов возможно использование макролидов или линкозамидов (см. вторичная профилактика). Необходимое условие терапии – достаточная продолжительность.
Патогенетическая терапия. Противовоспалительная, может проводится как нестероидными противовоспалительными, так и кортикостероидами при высокой степени активности процесса. Препаратом выбора в лечении ОРЛ у взрослых считается Диклофенак (150 мг/сутки), до 3-5 мес при необходимости. Применяют индометацин по 100 мг/сутки 1 месяц, затем 75 мг/сутки 2 недели, продолжая по 50 мг/сутки до конца стационарного лечения, вольтарен 100 мг/сутки, ортофен 100 мг/сутки, снижая дозы, как при приёме индометацина. При остром полисиндромном течении ОРЛ или при развитии панкардита показаны глюкокортикостероиды – преднизолон или метилпреднизолон (0,6-0,8 мг/кг/день) в течение 10-14 дней, реже дольше (до 1,5-2 мес). При положительной динамике начинают снижение суточной дозы глюкокортикостероидов на 2,5 мг в неделю, затем переходят на приём нестероидных противовоспалительных препаратов.
Продолжительность стационарного лечения составляет от 6 до 8 недель. После чего необходима длительная терапия в амбулаторных условиях. Продолжается терапия нестероидными противовоспалительными препаратами (Диклофенак, Индометацин) по 0,25-0,5 г/сутки длительно.
Второй этап лечения ревматизма включает пребывание в ревматологических и кардиологических санаториях. Больных целесообразно направлять в местные санатории, однако все методы физиотерапии при этом исключают. Больных без порока сердца либо с недостаточностью митрального или аортального клапана при отсутствии декомпенсации целесообразно направлять в Кисловодск или на Южный берег Крыма, а больных с недостаточностью кровообращения I степени, в том числе с нерезкими митральными стенозами,- только в Кисловодск. Противопоказано курортное лечение при выраженных признаках активности процесса, тяжелых комбинированных или сочетанных пороках сердца, недостаточности кровообращения II или III стадии
Показания к хирургическому лечению: выраженные клинические проявления порока сердца, ограничивающие физическую активность больного.
источник
Острая ревматическая лихорадка (ОРЛ) — это воспалительное заболевание соединительных тканей, которое поражает сердце, суставы, кожу и даже нервную систему. Оно обычно наблюдается у генетически предрасположенных людей, через несколько недель после перенесенной болезни, например ангины, вызванной особым штаммом стрептококков.
Обычно это заболевание называется ревматизм, однако сегодня под ревматизмом понимают состояние, при котором наблюдаются симптомы как ревматической лихорадки, так и хронической ревматической болезни сердца. Ранее считалось, что ревматизм поражает суставы, однако современные исследования доказали, что это повреждение кратковременно и не имеет особенных последствий. Однако заболевание вызывает порок сердца, обычно нарушая работу его клапанов. При этом начальная стадия болезни чаще протекает бессимптомно, и выявляется обычно при профилактическом осмотре при подозрении на аритмии или сердечную недостаточность.
Острая ревматическая лихорадка длительное время была основной причиной пороков сердца, но благодаря использованию антибиотиков при стрептококковой инфекции, число больных значительно снизилось.
В России распространенность острой ревматической лихорадки составляет 0,05%, и обычно оно начинается в подростковом возрасте (до 16 лет). Женщины болеют в три раза чаще, чем мужчины.
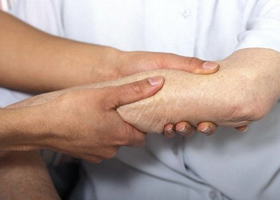
Боль при этом мигрирующая, то есть может передвигаться из одних суставов в другие. Это проявления артрита, который длится не более 10 дней. Через некоторое время признаки артрита исчезают, чаще у детей, а у взрослых иногда артрит может перерасти в синдром Жакку, характеризующийся деформацией костей рук без нарушения функций суставов. В результате повторных атак, артрит поражает большее количество суставов, переходя в хроническую форму.
Одновременно с симптомами артрита развивается и ревмокардит (поражение сердца). Иногда симптомов не наблюдается, но чаще бывает аритмия, одышка, ноющие боли в сердце и отеки. Даже при легком течении ревмокардита затрагиваются сердечные клапаны, они сморщиваются и теряют свою эластичность. Это приводит к тому, что они либо не открываются полностью или неплотно смыкаются, и формируется клапанный порок.
Обычно ревмокардит наблюдается в молодом возрасте от 15 до 25 лет, и ревматическим пороком сердца в результате страдают почти 25% заболевших, особенно при отсутствии адекватного лечения. Кстати, на долю ОРЛ приходится примерно 80% приобретенных пороков сердца.
У многих наблюдается моносимптомное течение ОРЛ, с преобладанием симптоматики артрита или ревмокардита.
На коже симптомы острой ревматической лихорадки проявляются в виде кольцевидных высыпаний (эритема) и подкожных ревматических узелков. Эти узелки обычно имеют размер зернышка, и располагаются в периартикулярных тканях. Они абсолютно безболезненны, кожные покровы не изменены. Ревматические узелки часто образовываются над костными выступами в области суставов. Встречаются они исключительно у детей. Кольцевидная эритема – это заболевание, характерным симптомом которого является появление на теле розовых пятен диаметром примерно 5 сантиметров. Они спонтанно возникают и исчезают, и локализуются на груди, спине и внутренней поверхности конечностей.
Ревматическое поражение нервной системы, вызванное ОРЛ, чаще всего наблюдается у детей в малом возрасте, в результате чего ребенок ставится капризным, он быстро утомляется, изменяется почерк, походка. Малая хорея часто наблюдается у девочек через 1,5-2 месяца после стрептококковой инфекции. Хорея представляет собой непроизвольные подергивания конечностей и мускулатуры, которые исчезают во время сна.
У подростков, перенесших ангину, часто острая ревматическая лихорадка начинается постепенно, температура поднимается до субфебрильной, беспокоят боли в крупных суставах и умеренные признаки кардита. Рецидивы ОРЛ связаны с перенесенной стрептококковой инфекций, и обычно проявляются как ревмокардит.
Причиной возникновения острой ревматической лихорадки является бета-гемолитический стрептококк группы А, который поражает ослабленный организм. Именно после того, как человек переболел ангиной, скарлатиной или тонзиллитом, вызванной стрептококками, у него начинается ОРЛ. Обратите внимание, что острая ревматическая лихорадка — это заболевание неинфекционной природы, т.к. стрептококки не поражают суставы. Просто в результате инфицирования нарушается нормальная работа иммунной системы. Исследования доказывают, что некоторые белки стрептококка имеют много схожего с белками суставов, в результате чего иммунитет, «отвечая» на стрептококковый вызов, начинает атаковать собственные ткани, развивается воспаление.
Велик шанс получить острую ревматическую лихорадку у тех, чьи родственники страдают ревматизмом. Заболеванию подвержены дети от 7 до 16 лет, взрослые болеют гораздо реже. Кроме того, шанс инфицирования стрептококком повышается в плохих условиях жизни, при недостаточном питании и регулярном недоедании.
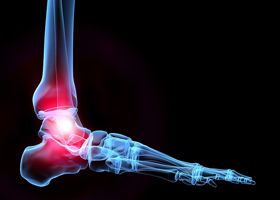
Назначаются общий клинический и иммунологический анализ крови. Лабораторные анализы также помогают правильно установить диагноз. У больных на ревматизм наблюдается развитие нейтрофильного лейкоцитоза и увеличение скорости оседания эритроцитов (выше 40 мм/ч), и сохраняется на длительное время. В моче иногда обнаруживается микрогематурия. При анализе серийных посевов из зева и с миндалин обнаруживают β-гемолитический стрептококк. Могут проводиться биопсия сустава и артроскопия. Ультразвуковое исследование сердца и электрокардиография целесообразны для выявления пороков сердца.
Первые симптомы острой ревматической лихорадки требуют соблюдения постельного режима, и применения лекарственных препаратов, которые помогут справиться с симптомами и предотвратить рецидивы заболевания. Диета при острой ревматической лихорадке — с низким содержанием соли и высоким — витаминов и минералов. Рацион необходимо обогатить фруктами и овощами, яйцами, куриным мясом, гречневой крупой, рыбой, курагой, а также продуктами, богатыми витамином С (цитрусовые, сладкий перец, шиповник), витаминами В1, В6, Р и РР, которые способствуют ускорению метаболических процессов в организме.
Для устранения причины заболевания — микроорганизма стрептококка, используются антибиотики ряда пенициллинов (амоксициллин) или макролиды (рокситромицин, кларитромицин). После завершения курса лечения принимаются антибиотики продолжительного действия.
Кроме того, уменьшить проявления воспаления суставов помогают противовоспалительные препараты (например, ибупрофен и диклофенак), которые назначаются лечащим врачом. При задержке жидкости в организме могут быть назначены мочегонные препараты (фуросемид). Иногда могут назначаться и лекарства, стимулирующие иммунный ответ организма, такие как гамма-глобулин и другие.
При проявлениях ревмокардита принимают препараты для стимуляции сердечной деятельности, например, дигоксин.
Иногда применяют такую схему лечения: назначают преднизолон, постепенно уменьшая дозу (начинать с 20-25 мг в сутки), и ацетилсалициловую кислоту в дозе до 4 г в день.
Сформированные пороки лечатся антиаритмическими препаратами, нитратами и мочегонными. Длительность и особенности лечения зависят от выраженности порока, наличия сердечной недостаточности и т.д. В случае, когда диагностика острой ревматической лихорадки показывает наличие тяжелого порока сердца, обычно есть необходимость операции на сердечных клапанах, пластики или протезирования клапана.
Одновременно с медикаментозными препаратами лечение острой ревматической лихорадки включает также физиотерапевтические процедуры, например, инфракрасное излучение и прогревание УВЧ-лампами. На пораженные суставы полезно накладывать грязевые и парафиновые аппликации, принимать кислородные и радоновые ванны. После окончания лечения необходимо проходить курс лечебного массажа и регулярно заниматься оздоровительной гимнастикой.
источник
Ревматическая лихорадка (PЛ) — это постинфекционное осложнение А-стрептококкового тонзиллита или фарингита у предрасположенных лиц с развитием аутоиммунного ответа на эпитопы стрептококка группы А и перекрестной реактивности со сходными эпитопами тканей человека (сердце, суставы, ЦНС).

Эпидемиология ревматической лихорадки тесно связана с эпидемиологией А-стрептококковых инфекций верхних дыхательных путей. Высокий уровень ревматической лихорадки начал снижаться еще до использования антибиотиков в клинической практике, применение же антибиотиков с 1950 г. стремительно ускорило этот процесс. Так, в развитых странах уровень заболеваемости ревматической лихорадкой понизился со 100-250 до 0,23-1,88 на 100 000 населения. Тем не менее в мире на настоящий момент страдают ревматической лихорадкой и ревматической болезнью сердца около 12 млн человек. Большинство из них проживают в развивающихся странах, где заболеваемость РЛ находится в диапазоне от 1,0 на 100 000 населения в Коста-Рике, 72,2 на 100 000 во Французской Полинезии, 100 на 100 000 в Судане до 150 на 100 000 в Китае, В некоторых районах, таких как Гавана (Куба), Коста-Рика, Каир (Египет), Мартиника и Гваделупа, где были введены профилактические программы, отмечено заметное снижение смертности, распространенности и тяжести РЛ и РБС. Сопиоэкономические показатели и факторы окружающей среды играют косвенную, но важную роль в распространенности и тяжести ревматической лихорадки и РБС. Такие факторы, как недостаток ресурсов для обеспечения качественной охраны здоровья, низкий уровень осведомленности о заболевании в обществе, скученность населения, могут существенно влиять на заболеваемость в популяции. Вместе с тем ревматическая лихорадка не является проблемой только неблагополучных в социальном и экономическом отношениях популяций. Это продемонстрировали локальные вспышки ревматической лихорадки. зафиксированные в 80-90-е гг. XX в. в некоторых районах США, Японии и ряда других развитых стран мира.

Этиологическая связь между инфекциями, вызванными БГСА, и последующим развитием острой ревматической лихорадки (ОРЛ) хорошо известна. Несмотря на отсутствие доказательств прямого вовлечения стрептококков группы А в повреждение тканей пациентов с острой ревматической лихорадкой, существуют значительные эпидемиологические иммунологические доказательства косвенного участия БГСА в инициации заболевания:
- вспышки ревматической лихорадки близко следуют за каждой эпидемией ангины или скарлатины;
- адекватное лечение документированного стрептококкового фарингита заметно уменьшает число последующих атак ревматической лихорадки;
- подобающая антимикробная профилактика предупреждает рецидивы заболевания у пациентов, перенесших ОРЛ;
- наличие у большинства пациентов с ОРЛ повышенных титров хотя бы одного из антистрептококковых антител.
Ревматическая лихорадка и ревматическая болезнь сердца наблюдаются только после инфекций верхних дыхательных путей, вызванных стрептококками группы А. Хотя бета-гемолитические стрептококки серогрупп В, С, О и Р могут вызвать фарингит и быть триггерами иммунного ответа хозяина, они не связаны с этиологией РЛ.
Стрептококковый фарингит/тонзиллит является единственной инфекцией, ассоциированной с ОРЛ. Так, например, существует много описаний вспышек кожных стрептококковых инфекций (импетиго, рожистого воспаления), которые были причиной постстрептококкового гломерулонефрита, но никогда — причиной ревматической лихорадки.
Штаммы стрептококка группы А, колонизирующие кожу, отличались от штаммов, вызывающих ревматическую лихорадку. Бактериальные генетические факторы могут быть важной детерминантой места возникновения группы А стрептококковой инфекции. Структура антигенов, кодирующая М- и М-подобные поверхностные протеины стрептококка, распознана и промаркирована от А до Е. Фарингеальные штаммы имеют структуру А-С, в то время как все кожные штаммы имеют Д и Е структуру.
Другим фактором, влияющим на локализацию в глотке, может быть рецептор СD44, связанный с гиалуроновой кислотой протеин, который служит в качестве фарингеального рецептора для стрептококков группы А. В эксперименте показано, что после интраназального введения стрептококки группы А колонизируют ротоглотку у обычных мышей и не колонизируют у трансгенных мышей, не экспрессирующих СD44.
Многие теории пытаются объяснить, почему острая ревматическая лихорадка ассоциируется только со стрептококковым фарингитом, но точного объяснения до сих пор нет. Группу стрептококков А разделяют на два главных класса, в основе этого деления лежат различия в С-последовательностях М-протеина. Один класс ассоциируется со стрептококковой фарингеальной инфекцией, другой (за некоторыми исключениями) — со штаммами, наиболее часто вызывающими импетиго. Таким образом, особенности стрептококковых штаммов бывают решающими в инициации болезни. Фарингеальная инфекция с ее вовлечением большого количества лимфоидной ткани сама по себе может быть важна для инициации аномального гуморального ответа на микробные антигены с формированием перекрестной реактивности к тканям организма. Кожные штаммы могут колонизировать глотку, но они неспособны вызвать такой сильный иммунологический ответ на М-протеин, как фарингеальные штаммы.
Ревматическая лихорадка происходит в результате неправильного иммунного ответа на фарингит, вызванный стрептококками группы А. Клинические манифестации этого ответа и его выраженность у конкретного индивидуума зависят от вирулентности микроба, генетической восприимчивости хозяина и «подходящих» условий окружающей среды.
Одной из хорошо изученных детерминант бактериальной вирулентности является М-протеин. Стрептококковый М-протеин располагается на поверхности стрептококковой клетки и обладает структурной гомологией с миозином кардиомиоцитов, а также с другими молекулами: тропомиозином, кератином, ламинином. Предполагается, что эта гомология ответственна за гистологические изменения при остром ревматическом кардите. Например, ламинин — протеин внеклеточного матрикса, секретируемый эндотелиальными клетками, выстилающими клапаны сердца, служит важнейшим компонентом структуры клапана. Он также служит мишенью для полиреактивных антител, которые «узнают» М-протеин, миозин и ламинин.
Из более чем 130 идентифицированных типов М-протеина ассоциируются с ревматической лихорадкой такие М-типы, как 1, 3, 5, 6, 14, 18, 19 и 24. Постулируют, что указанные М-типы стрептококков группы А обладают ревматогенным потенциалом. Эти серотипы обычно с трудом инкапсулируются и формируют крупные мукоидные колонии, богатые М-протеином. Данные характеристики усиливают способность бактерий к тканевой адгезии и устойчивость к фагоцитозу в организме хозяина.
Еще один фактор вирулентности — стрептококковые суперантигены. Это уникальная группа гликопротеи нор, которые могут связывать молекулы II класса главного комплекса гистосовместимости с V-рецепторами Т-лимфоцитов, симулируя связывание антигена. Таким образом, Т-клетки становятся подвержены антиген-неспецифичной, и аутореактивной стимуляции. В патогенезе ревматической лихорадки в роли суперантигенов рассматривают некоторые фрагменты М-протеина и стрептококковый эритрогенный экзотоксин. Стрептококковый эритрогенный токсин может вести себя как суперантиген и для В-клеток, приводя к продукции аутореактивных антител.
Для развития ревматической лихорадки необходима также генетическая предрасположенность макроорганизма. Это на настоящий момент единственное объяснение того факта, что ревматическая лихорадка возникает лишь у 0,3-3% индивидуумов с острым А-стрептококковым фарингитом. Концепция о генетической предрасположенности РЛ интригует исследователей более 100 лет. Все это время считали, что ген заболевания имеет аутосомно-доминантный путь передачи, аутосомно-рецессивный с лимитированной пенетрантностью или передача осуществляется геном связанным с секреторным статусом группы крови. Вновь интерес к генетике ОРЛ вырос в связи с открытием у человека комплекса гистосовместимости. Результаты исследований позволяют предположить, что иммунный ответ контролируется генетически и при этом существует высокая реактивность к антигену клеточной стенки стрептококка, экспрессируемая через отдельный рецессивный ген, и низкая реактивность, экспрессируемая через отдельный доминантный ген. Современные данные подтверждают, что генетический контроль низкого ответа на стрептококковый антиген тесно связан с антигенами II класса гистосовместимости. Вместе с тем связь между восприимчивостью к ревматической лихорадке и антигенами II класса НLА сильно различается в зависимости от этнических факторов. Например, DR4 чаше присутствует у пациентов с РЛ — европеоидов; DR2 — у негроидов, DR1 и DRw6 — у пациентов из Южной Африки; DRЗ чаще находят у пациентов с РЛ из Индии (у которых также отмечают низкую частоту встречаемости DR2); DR7 и DW53 — у пациентов из Бразилии; DQW2 — у монголоидов. Вероятнее всего, данные гены расположены рядом с геном предрасположенности к ревматической лихорадке, возможно, в том же локусе, но не идентичны ему.
Несколько позже у больных РЛ были идентифицированы поверхностные аллоантигепы В-лимфоцитов, названные аллоантигенами D8/17 по наименованию клона моноклональных антител, с помощью которых они были выделены. Согласно мировым данным, аллоантиген В-лимфоцитов D8/17 идетнифицируют у 80-100% больных ОРЛ и лишь у 6-17% здоровых индивидуумов. Причастность аллоантигена В-лимфоцитов пациентов к патогенезу ревматической лихорадки продолжают изучать. Наиболее правдоподобно, что предрасположенность к ОРЛ полигенна, и D8/17-антиген может быть ассоциирован с одним из генов, отвечающих за предрасположенность; другим же может быть комплекс гистосовместимости, кодирующий DR-антигены. Хотя точное объяснение отсутствует, повышенное количество D8/17 положительных В-клеток — признак особого риска заболеваемости острой ревматической лихорадкой.

Стрептококковая инфекция начинается со связывания поверхностных лигандов бактерии со специфическими рецепторами клеток организма-хозяина и последующим включением специфических процессов адгезии, колонизации и инвазии. Связывание поверхностных лигандов бактерии с поверхностными рецепторами хозяина — ключевое событие в колонизации организма хозяина, оно инициируется фибронектином и стрептококковыми фибронектин-связывающими протеинами. Стрептококковая липотейхоевая кислота и М-протеин также играют существенную роль в бактериальной адгезии. Организм хозяина отвечает на стрептококковую инфекцию опсонизацией и фагоцитозом. Стрептококковая инфекция в генетически предрасположенном организме при соответствующих условиях окружающей среды приводит к активации Т- и В-лимфоцитов стрептококковыми антигенами и суперантигенами, что, в свою очередь, способствует продукции цитокинов и антител, направленных против стрептококкового N-ацетил-бета-D-глюкозами на (карбогидрата) и миозина.
Считается, что повреждение клапанного эндотелия антикарбогидратными антителами приводит к увеличению выработки молекул адгезии и притоку активированных СD4+ и СD8+ Т-клеток. Нарушение целостности эндотелия клапанов сердца приводит к экспозиции субэндотелиальных структур (виментин, ламинин и клетки клапанного интерстиция), что способствует развитию «цепной реакции» клапанной деструкции. После вовлечения в процесс воспаления створок клапанов, благодаря вновь образовавшимся микрососудам, происходит инфильтрация клапанного эндотелия Т-клетками, поддерживая процесс разрушения клапана. Наличие Т-клеточной инфильтрации даже в старых минерализованных повреждениях служит показателем персистирования заболевания и прогрессирования повреждения клапана. Под влиянием провоспалительных цитокинов клетки клапанного интерстиция и другие клапанные компоненты приводят к «неправильному восстановлению» клапана.
Описанный выше патогенетический механизм наиболее вероятен, однако до настоящего времени нет непосредственных и убедительных доказательств патогенетической роли перекрестнореагирующих антител in vivo и отсутствует подходящая животная модель для изучения ревматической лихорадки.
В 2000-2002 гг. Европейское общество кардиологов опубликовало данные о возможной триггерной роли вирусов и стресс-белков теплового шока (heat stress proteins) в формировании рецидивов ревматической лихорадки и ревмокардита, однако эта теория еще требует дальнейшего изучения.
Таким образом, в основе современных представлений о ревматической лихорадки лежит признание этиологической роли БГСА и наследственной предрасположенности к заболеванию, реализующейся аномалией иммунного ответа организма.
Ревматическая лихорадка протекает в виде атак. У 70% больных ревматическая атака стихает, по клинико-лабораторным данным, в течение 8-12 нед, у 90- 95% — 12-16 нед, и лишь у 5% больных атака продолжается более 6 мес, т.е. принимает затяжное либо хроническое течение. Иными словами, в большинстве случаев ревматический процесс имеет циклическое течение, и атака заканчивается и среднем в течение 16 нед.
Более чем в половине случаев больные жалуются на одышку, перебои в сердце, сердцебиение, которые возникают на фоне общих симптомов ревматической лихорадки: быстрой утомляемости, вялости, потливости, повышения температуры тела. У взрослых могут появляться боли в области сердца неопределенного характера.
Ревмокардит, ревматический артрит, хорея, кольцевидная эритема и подкожные узелки служат большими диагностическими признаками острой ревматической лихорадки.
Подкожные узелки и кольцевидная эритема — редкие проявления ревматической лихорадки, они встречаются менее чем к 10% случаев.
Подкожные узелки — это круглые, плотные, легко смещаемые, безболезненные образования размером от 0,5 до 2 см, чаще локализующиеся на разгибательных поверхностях локтевых, коленных и других суставов, в затылочной области и по ходу сухожильных влагалищ, крайне редко бывают при первой атаке ревматической лихорадки. Число узелков варьирует от одного до нескольких десятков, но обычно их 3-4. Считается, что их легче прощупать, чем увидеть. Они сохраняются от нескольких дней до 1-2 нед, реже — больше месяца. Подкожные узелки почти всегда ассоциируются с вовлечением сердца и обнаруживаются чаще у пациентов с тяжелым кардитом.
Кольцевидная эритема — это преходящие кольцевидные пятна с бледным центром, как правило, возникающие на туловище, шее, проксимальных отделах конечностей. Кольцевидная эритема никогда не локализуется на лице. В связи с мимолетностью изменений и отсутствием ассоциированных симптомов кольцевидная эритема может быть пропущена, если ее специально не искать, особенно у темнокожих пациентов. Отдельные элементы могут возникать и исчезать в течение минут или часов, иногда меняя форму на глазах у специалиста, сливаясь с соседними элементами с формированием сложных структур (поэтому в некоторых источниках они описываются как «кольца сигаретного дыма»). Кольцевидная эритема обычно появляется в начале ревматической атаки, однако она может персистировать или рецидивировать в течение месяцев или даже лет, сохраняясь после того, как другие проявления заболевания стихнут; на нее не влияет противовоспалительное лечение. Этот кожный феномен ассоциируется с кардитом, но, в отличие от подкожных узелков, не обязательно с тяжелым. Узелки и кольцевидная эритема част о сочетаются.
Кольцевидная эритема не является уникальной для ревматической лихорадки, она также описана при сепсисе, аллергических реакциях на лекарственные препараты, гломерулонефрите и у детей без каких-либо диагностированных заболеваний. Ее следует отличать от токсической эритемы у лихорадящих пациентов и сыпи при ювенильном идиопатическом артрите. Кольцевая эритема при болезни Лайма (хроническая мигрирующая эритема) также может напоминать кольцевидную эритему при ревматической лихорадке.
Артралгии и лихорадку обозначают как «малые» клинические проявления ревматической лихорадки в диагностических критериях Т. Джонса не потому, что они встречаются реже, чем пять больших критериев, а потому, что они обладают меньшей диагностической специфичностью. Лихорадка наблюдается и начале почти всех ревматических атак и обычно составляет 38,4-40 С. Как правило, бывают колебания в течение дня, но характерной температурной кривой нет. Дети, у которых есть только легкий кардит без артритов, могут иметь субфебрильную температуру, а пациенты с «чистой» хореей афебрильны. Лихорадка редко сохраняется больше нескольких педель. Артралгия без объективных изменений часто встречается при ревматической лихорадке. Боль обычно возникает в крупных суставах и может быть незначительной и очень сильной (вплоть до невозможности движений), она может сохраняться от нескольких дней до недель, меняясь в интенсивности.
Хотя абдоминальную боль и носовое кровотечение отмечают примерно у 5% пациентов с РЛ, их не рассматривают как часть критериев Т. Джонса из-за отсутствия специфичности этих симптомов. Однако они могут иметь клиническое значение, так как появляются за несколько часов или дней до развития больших проявлений РЛ, абдоминальная боль обычно локализуется в эпигастрии или околопупочной области, может сопровождаться симптомами мышечной защиты и часто симулирует различные острые заболевания органов брюшной полости.

Больная С., 43 года, консультирована в Московском городском ревматологическом центре 20.01.2008, куда направлена из городской поликлиники для уточнения диагноза.
При осмотре предъявляла жалобы на общую слабость, потливость, быструю утомляемость, одышку при физической нагрузке. В декабре 2007 г. перенесла острый фарингит, по поводу которого антибактериального лечения не получала. Через 3-4 нед появились одышка и сердцебиение при небольшой физической нагрузке, боли в прекардиальной области различного характера, повышение температуры тела до 37,2 С, увеличение СОЭ до 30 мм/ч.
Из анамнеза также известно, что с детства наблюдается у кардиолога по поводу первичного пролапса митрального клапана, постоянно выслушивались мезодиастолический щелчок и позднесистолический шум над верхушкой при аускультации сердца. В течение последнего месяца кардиолог отметила усиление систолического шума с приобретением пансистолического звучания, что стало основанием для подозрения ОРЛ и направления на консультацию в ревмоцентр.
Объективно: кожные покровы обычной окраски, нормального питания. Периферических отеков нет. Миндалины гипертрофированы, разрыхлены. В легких везикулярное дыхание, хрипы не выслушивались. Границы относительной тупости сердца не расширены. Ослабление I тона над верхушкой, выслушивается пансистолический шум с иррадиацией в левую подмышечную область и межлопаточную область 5-й градации, а также систолический шум над трехстворчатым клапаном и клапаном легочной артерии 3-й градации. Экстрасистолия. ЧСС — 92 в минуту, АД — 130/70 мм рт.ст. Живот при пальпации мягкий, безболезненный. Перкуторно печень и селезенка не увеличены.
Клинический анализ крови от 16.01.08: Нb
118 г/л, лейкоциты — 9,4х10 9 /л, СОЭ — 30 мм/ч
Общий анализ мочи от 16.01.08 без патологических изменений. В иммунологическом анализе крови от 16.01.08: С-реактивиый белок — 24 мг/л, антистрептолизин-О — 600 ЕД.
На ЭКГ — нормальное положение электрической оси сердца, ритм синусовый, ЧСС — 70 в минуту, единичные предсердные экстрасистолы, РQ — 0,14 с, QRS — 0.09 с.
При допплер-ЭхоКГ от 20.01.08 обе створки митрального клапана пролабируют в полость левого предсердия, краевое уплотнение передней створки, движения их в противофазе. Фиброзное кольцо — 30 мм, размер отверстия 39×27 мм, пиковый градиент — 5,8 мм рт.ст., митральная регургитация 3-й степени. Левое предсердие 44 мм, дилатация левого желудочка: конечно-диастолический размер (КДР) — 59 мм, конечно-систолический размер (КСР) — 38 мм, конечно-диастолический объем (КДО) — 173 мл, конечно-систолический объем (КСО) — 62 мл, ударный объем — 11 мл, фракция выброса (ФБ) — 64%. Аорта 28 мм, не изменена. Аортальный клапан трехстворчатый, небольшое краевое уплотнение створок, фиброзное кольцо — 24 мм, пиковый градиент давления — 4 мм рт.ст. Правое предсердие — 48 мм, правый желудочек — небольшая дилатация (равен левому по объему), расчетное давление — 22 мм.рт.ст. Легочная артерия умеренно расширена, легочный клапан не изменен, фиброзной кольцо — 29 мм, систолический градиент давления на клапане легочной артерии — 3 мм. рт.ст., регургитации нет. Трикуспидальный клапан пролабирует, фиброзное кольцо 30 мм, 1-я степень ригургитации. Заключение: пролапс обеим створок митрального клапана, краевое уплотнение створок митрального и аортального клапанов, митральная регургитация 3-й степени, трикуспидальная регургитация 1-й степени, дилатация полостей сердца.
С учетом связи ухудшения состояния пациентки с перенесенным острым фарингитом и доказательств перенесенной А-стрептококковой инфекции (выявление повышенного титра антистрептолизина-О), усиления имевшегося систолического шума над верхушкой сердца, а также кардиомегалии, обнаруженной с помощью ЭхоКГ, повышения уровня С-реактивного белка и увеличения СОЭ был поставлен диагноз: «Острая ревматическая лихорадка: кардит средней степени (митральный и аортальный вальвулит). Митральная регургитация 3-й степени. Трикуспидальная регургитация 1-й степени. Наджелудочковая зкстрасистолия. НК 1 ст., II ФК».
Больная госпитализирована в ГКБ № 52, где было проведено лечение стрептококковой инфекции амоксициллином в течение 10 дней в дозе 1500 мг/сут, диклофенаком в дозе 100 мг/сут в течение 14 дней, соблюдался строгий постельный режим в течение 2 нед с дальнейшим расширением режима нагрузок. Состояние больной улучшилось, сократились размеры сердца. На момент выписки из стационара на амбулаторное долечивание больная жалоб не предъявляла. В анализах крови СОЭ составляла 7 мм/ч, С-реактивный белок — 5 мг/л, антистрептолизин-О — менее 250 ЕД. Была начата вторичная профилактика ревматической лихорадки бензатина бензилпенициллином в дозе 2,4 млн ЕД внутримышечно 1 раз каждые 4 нед, которую рекомендовано было проводить в течение последующих 10 лет.

В настоящее время в Российской Федерации принята национальная классификация ревматической лихорадки.
Классификация ревматической лихорадки (АРР, 2003)
Стадии недостаточности кровообращения (НК)
Острая ревматическая лихорадка
Повторная ревматическая лихорадка
Ревматическая болезнь сердца
без порока сердца***
порок сердца****
- * По классификации Н.Д, Стражеско и В.Х, Василенко.
- ** Функциональный класс сердечной недостаточности по Нью-Йоркской классификации.
- *** Возможно наличие поствоспалительного краевого фиброза клапанных створок без регургитации, который уточняется с помощью ЭхоКГ.
- **** При наличии «первые обнаруженного порока сердца необходимо по возможности исключить другие причины его формирования (инфекционный эндокардит, первичный антифосфолипидный синдром, кальциноз клапанов дегенеративного генеза и др.).

В анамнезе больных с подозрением на ревмокардит необходимо подробно описать семейно-половой анамнез на предмет наличия ревматической лихорадки у ближайших родственников и документированные подтверждения данного диагноза, а также установить наличие или отсутствие документально подтвержденного тонзиллофарингита, скарлатины, отита, ринита, лимфаденита переднешейных лимфатических узлов в течение последних 2-3 нед. Следует также учитывать наличие факторов риска:
- наследственную предрасположенность (выявление специфического антигена В-лимфоцитов D8/17, а также высокая распространенность II класса антигенов системы НLА);
- «уязвимый» возраст;
- скученность населения;
- неудовлетворительные жилищные и санитарно-гигиенические условия быта (маленькая жилплощадь, многодетные семьи);
- низкий уровень медицинской помощи,
В настоящее время в соответствии с рекомендациями ВОЗ в качестве международных применяют диагностические критерии ревматической лихорадки Т. Джонса, пересмотренные в 2004 г.
Диагностические критерии ревматической лихорадки
| Большие критерии | Малые критерии | ||||||
| Диагностические категории | Критерии |
