Термин лихорадка (от лат. — febris и греч. — pyrexia, что означает жар, горячка, «лихая радость», средство очищаться) — один из древнейших в медицине. Лихорадка, как и воспаление, является типовым патологическим процессом, часто встречающимся при различных заболеваниях (инфекционных, травматических, онкологических и др.) которые сопровождаются повреждением клеточно-тканевых структур организма и характеризуются повышением температуры тела. В древней медицине, вплоть до прошлого века, лихорадкой именовали отдельные нозологические формы с выраженным подъемом температуры тела (лихорадка Папатачи, Ку лихорадка, желтая лихорадка и др.).
В современном понимании, лихорадка — это эволюционно выработанная типическая преимущественно защитно-приспособительная реакция высших гомойотермных животных и человека на пирогены, характеризующаяся повышением температуры тела вследствие временной активной перестройки аппарата теплорегуляции на более высокий уровень функционирования.
Повышение температуры тела характерно и для перегревания организма — гипертермии. Принципиальные отличия лихорадки от гипертермии представлены в таблице 16-1.
Гипертермия, в отличие от лихорадки, вызывается не пирогенами, а повышением температуры окружающей среды, либо нарушением механизмов химической терморегуляции (повышением теплообразования), либо нарушением механизмов физической терморегуляции (ограничением теплоотдачи), либо их сочетанием.
Развитие гипертермии ускоряется и усиливается при:
— низкой скорости движения воздуха;
— длительном нахождении в герметично изолирующей одежде (помещении);
— интенсивной и продолжительной физической работе;
— употреблении большого количества пищи (особенно белковой);
— нарушениях центрального, регионарного и микроциркуляторного крово- и лимфообращения;
— различных видах дисрегуляционной патологии и т.д.
— При гипертермии даже незначительное (на десятые доли градуса, а тем более на 1-2-3 0 С) повышение температуры тела (ядра), несмотря на активизацию процессов теплоотдачи и снижение процессов теплообразования, сопровождается развитием:
— состояния субъективного и объективного дискомфорта, значительно более выраженного, чем при лихорадке;
— нарушений поведения, работоспособности, жизнедеятельности;
— расстройств функционирования регуляторных, исполнительных и метаболических систем;
— дегидратации, сгущения крови, расстройств микроциркуляции, гипоксии, ацидоза и других нарушений.
Таблица 16-1.
Отличия лихорадки от перегревания организма
| п/п | Отличительные признаки | Лихорадка | Перегревание организма |
| 1. | Этиология | Пирогены | Повышение температуры окружающей среды или действие химических веществ (токсинов, ядов), вызывающих в организме эффект «разобщения» окислительного фосфорилирования. |
| 2. | Патогенез | Активная перестройка аппарата теплорегуляции | Нарушение (повреждение) аппарата теплорегуляции |
| 3. | Изменения в организме | Определяются стадией развития | Относительно постоянны |
| 4. | Биологическое значение | Обычно положительное, приспособительное | Отрицательное, повреждающее |
| 5. | Развитие в филогенезе | У высших гомойотермных организмов | У всех организмов |
| 6. | Развитие в онтогенезе у человека | К концу 1-го года жизни (по мере созревания ЦНС) | В любом возрасте |
Этиология лихорадки
Лихорадка вызывается пирогенами (греч. pyrоs, pyretos — огонь, жар; genesis — происхождение), действие которых усиливается неблагоприятными внешними и внутренними условиями.
По происхождению различают экзогенные и эндогенные пирогены.
Экзогенные пирогены (первичные) представлены липополисахаридами, а также белками и различными белково-липидными и белково-углеводными комплексами вирусов, микоплазм, риккетсий, бактерий, грибов, простейших.
Липополисахаридные (ЛПС) мембранные комплексы и, прежде всего, липоид А, входящие в состав оболочек микроорганизмов, (особенно грамотрицательных бактерий), обладают наибольшей пирогенной активностью. Они вызывают лихорадку у человека. в дозе 1 мкг/кг. Кролики более чувствительны ЛПС, которые даже в дозе 0,01-0,001 мкг/кг способны вызвать у них лихорадку. ЛПС термостабильны, не обладают специфической токсичностью и антигенностью. При многократном применении к ним развивается толерантность. Их пирогенная активность, как правило, не зависит от патогенности микроорганизмов. Из ЛПС оболочек микроорганизмов получают стандартные пирогенные препараты (пирогенал, пирексаль, пиромен и др.).
Белки микроорганизмов также обладают пирогенной активностью, но в значительно (1000 раз) меньшей степени.
Пирогены неинфекционной (немикробной) природы (чужеродные белки, их комплексы, органические и другие вещества, способные вызвать воспаление также обладают определенной пирогенной активностью.
Экзогенные пирогены проявляют свою пирогенную активность через образование в организме эндогенных пирогенов (первичных и вторичных).
Первичные эндопирогены образуются под влиянием разнообразных патогенных факторов, способных вызвать повреждение клеточно-тканевых структур, воспаление, аллергию, реакцию иммунной системы и системы фагоцитов (макро- и микрофагов).
Вторичные эндопирогены образуются, главным образом, активированными моноцитами, (как циркулирующими и фиксированными), гистио-макрофагами, а также нейтрофильными гранулоцитами, клетками-киллерами: NK- клетками,Т- и В-лимфоцитами. К эндопирогенам относят высоко активный интерлейкин-1 (ИЛ-1), интерлейкин-6 (ИЛ-6), а также менее активные
интерлейкин-3 (ИЛ-3), a-интерферон (a-ИФ), фактор некроза опухоли альфа (ФНОa), катионные белки, колониестимулирующие факторы и др. Эти пирогены вызывают развитие лихорадочной реакции в дозе нг/кг массы тела.
Вторичные эндопирогены термолабильны, не токсичны, не обладают антигенными свойствами. Они не только вызывают, но и поддерживают лихорадку. Кроме того у них обнаруживается антитоксическое, антибактериальное и антивирусное действие.
Можно утверждать, что любая лихорадка в конечном итоге всегда реализуется с участием вторичных эндопирогенов.
Следует отметить, что кривые температуры тела при введении в организм экзо- и эндопирогенов отчетливо различаются. Это можно проиллюстрировать в опыте на кролике (рис. 16-1). Так, при внутривенном введении ИЛ-1 в дозе 100 нг/кг массы температурная кривая имеет монофазный дозозависимый характер (1) при минимальном латентном периоде, в то время как при введение экзогенного пирогена (очищенного липополисахаридного комплекса — пирогенала, в дозе 1 мкг/кг массы) подъем t o происходит после выраженного латентного периода, температурная кривая не имеет строгой монофазности и длится несколько часов (2).
Рис. 16-1.Характер температурных кривых при введении кролику
интерлейкина (1) и липополисахаридного коплекса (2)
Патогенез лихорадки
Механизм развития лихорадки определяется действием вторичных эндогенных пирогенов (рис. 16-2.). Центральным звеном в патогенезе лихорадки является смещение (изменение) установочной точки (Set point) температурного гомеостазиса на более высокий уровень (например, с 36-37° С на 38-39°С).
Этот механизм реализуется за счет изменения порогов возбудимости термочувствительных («холодовых» и «тепловых») нейронов медиальной преоптической области переднего гипоталамуса к температуре крови и афферентации от холодовых и тепловых терморецепторов организма. Наряду с этим происходят изменения порогов возбудимости и нетермочувствительных нейронов переднего гипоталамуса.
В I стадию лихорадки наблюдаются, сначала повышение возбудимости холодочувствительных нейронов (величина критического уровня деполяризации, КУД, уменьшается), что сопровождается снижением теплоотдачи (ТО); а затем и снижение возбудимости теплочувствительных нейронов (величина КУД увеличивается), что сопровождается повышением теплопродукции (ТП).
Во II стадию лихорадки отмечаются, фазные изменения возбудимости холодочувствительных нейронов (повышенная, нормальная, сниженная), что сопровождается фазными изменениями ТО (сначала снижение, потом нормализация, а затем повышение); а также снижение возбудимости теплочувствительных нейронов, что сопровождается повышением ТП.
В целом устанавливается равновесие между ТО и ТП, но на более высоком их уровне (в связи с повышением Set point).
В III стадию лихорадки обнаруживаются уменьшение возбудимости холодочувствительных нейронов, что сопровождается дальнейшим повышением ТО и увеличение возбудимости теплочувствительных нейронов, что сопровождается снижением ТП.
Механизмы изменения ТО и ТП в разные стадии лихорадки предтсавлены в таблице 16-2.
Классификация лихорадки
В настоящее время лихорадку классифицируют по:
— инфекционная (септическое воспаление);
— неинфекционная (асептическое воспаление).
· не ясной этиологии (продолжающаяся более трех недель без устранения ее причины в условиях стационарного обследования);
уровню повышения температуры тела:
· гиперпиретическая (41 о С и выше );
продолжительности:
характеру температурной кривой:
источник
Краснодар, 2017 год
1.2 Биологическое значение.
- Гипертермия: этиология, отличия от лихорадки
Лихорадка – определение, этиология, биологическое значение
Лихорадка – общая реакция организма на повреждение, важнейшим признаком которой является повышение температуры тела
Лихорадка – типовой патологический процесс, в основе которого лежит активная перестройка функции центра термогегуляции под действием пирогенного фактора
Этиология: 2 (две) группы факторов: 1) инфекционные;
1. Инфекционные факторы: — бактерии;
2. Неинфекционные факторы: экзо- и эндогенные факторы, вызывающих повреждение тканей
Пример неинфекционной лихорадки: на фоне ожогов, травм, инфарктов, внутренних кровоизлияний, аллергического повреждения тканей.
Биологическое значение лихорадки:
1. Лихорадка – это типовой патологический процесс, который носит в себе элементы защиты и повреждения
2. Защитная роль лихорадки (проявляется только при умеренной недлительной лихорадке):
а) стимуляция иммунных реакций;
в) торможение развития аллергических реакций;
г) нарушение размножения бактерий, вирусов, опухолевых клеток;
д) понижение выживаемости микроорганизмов.
3. Лихорадка может негативно влиять на организм (высокая и длительная лихорадка):
а) неблагоприятное действие на ССС;
б) неблагоприятное действие на ЦНС;
в) неблагоприятное действие на пищеварение;
г) неблагоприятное действие на метаболизм;
д) ослабляет физиологические функции;
е) отягощает состояние больного.
4. Лихорадка – одно из проявлений заболеваний. Часто она первый и единственный симптом на протяжении длительного времени.
Пирогенные вещества. Их природа и источники образования
Пирогенные вещества есть непосредственная причина лихорадки. Лихорадка развивается в организме вслед за появлением в нём этих веществ.
Выделяют экзо- и эндогенные пирогенные вещества.
Экзогенные пирогенны сами по себе не вызывают повышения температуры тела. Но они стимулируют образование в организме эндогенных пирогенов.
Эндогенные пирогенны действуют на центр терморегуляции, следовательно изменяют его работу и температура тела возрастает.
Экзогенные пирогенные вещества:
1. Происхождение: являются составной частью эндотоксинов микробной клетки
2. По химическому строению:
— липиполисахариды, содержащие липоид А;
— полисахариды, свободные от белка
3. Токсичность: нетоксичны. Точнее, в больших дозах экзопирогены являются токсичными для организма, но для развития лихорадочной реакции достаточно их малых количеств, когда токсический эффект не успевает наступить.
4. Толерантность. Развитие толерантности к экзопирогенам при повторных введениях
5. Реакция на нагревание. Термостабильны.
6. Видовая специфичность: есть
Эндогенные пирогенные вещества:
1. Химическая природа: полипептиды или белки с м.м. от 1500 до 40000Д.
2.Реакция на нагревание: термолабильны.
3. Толерантность: при повторном введении не возникает.
4. Видовая специфичность: нет.
5. Место образования: образуются в клетках, которые обладают способностью к фагоцитозу:
— клетки РЭС печени et lien.
а) в организм поступает м/о;
б) из мембран м/о освобождается экзопироген;
в) экзопироген фагоцитируется вышеперечисленными клетками;
г) факт фагоцитоза экзопирогена есть стимул для образования в них эндопирогена.
7. Роль лимфоцитов в образовании эндопирогенов: Сами лимфоциты не образуют эндопирогенов, но Тл способны усиливать эндопирогенобразующую функцию моноцитов за счёт синтеза лимфокинов. Лимфокины – группа веществ, которые образуются в лимфоцитах. Лимфокины влияют на различные функции моноцитов, могут их повышать или понижать. Среди эффектов лимфокинов – стимуляция эндопирогенобразующей функции моноцитов.
Образование эндогенных и пирогенных веществ – основное патогенетическое звено лихорадки, независимо от её причины.
Патогенез лихорадки
Температура тела человека обеспечивается 2 механизмами:
Регуляция теплопродукции и теплоотдачи – центр терморегуляции.
Центр терморегуляции
Местонахождение: преотическая зона переднего отдела гипоталамуса (около дна IV желудочка).
Анатомически и функционально в центре терморегуляции выделяют области:
1. Термочувствительная область («термостат»).Роль – определение температуры тела. Механизм:
а) регистрация температуры протекающей через центр терморегуляции крови;
б) регистрация нервных импульсов с кожи и внутренних органов.
2. Термоустановочная область («установочная точка»).Роль:
а) Получает информацию от «термостата» о температуре тела в данный момент;
б) Сравнивает имеющуюся температуру тела с желаемой. Говоря о желаемой температуре тела, чаще употребляют слово «эталонная», т.е. такая, которая должна быть в здоровом организме;
в) Решает вопрос: является ли имеющаяся в данный момент температура эталонной, ниже эталона, выше эталона.
г) Если температура тела выше или ниже эталонной, то «установочная точка»изменяет работу центров теплопродукции и теплоотдачи с целью коррекции температуры тела.
3. Центры теплопродукции и теплоотдачи.Центр теплоотдачи и центр теплопродукции – это анатомически разные образования. Эти центры своё влияние на состояние теплообразования осуществляют через:
А) ВНС: симпатическую и парасимпатическую;
Б) Эндокринную систему: гипофиз, надпочечники, щитовидная железа.
а) Уменьшение теплоотдачи за счет активации симпатической ВНС:
— взъерошивание шерсти у животных;
— характерное изменение позы;
— торможение мочеиспускания и дефеквции.
б) Увеличение теплоотдачи за счет активации парасимпатической ВНС:
а) Увеличение теплопродукции: активация симпатической ВНС.
— увеличение окисления и восстановления в скелетных мышцах, печени и внутренних органах;
— увеличение тонуса мышц и мышечная дрожь. Мышечная дрожь возникает из-за того, что при увеличении температуры тела появляется разница между температурой кожи и окружающей средой.
Механизм появления мышечной дрожи:
а) температура кожи снижается из-за спазма сосудов кожи и замедления кровотока в капиллярах
б) температура окружающей среды становится выше температуры кожи
в) возбуждаются холодовые рецепторы кожи
г) нервные импульсы идут в гипоталамус
д) в результате непроизвольного мышечного подёргивания
е) почему мышечные подёргивания увеличивают образование тепла? Ответ: непроизвольно сокращающиеся мышцы не совершают полезной работы и часть химической энергии АТФ превращается в тепловую энергию.
Итак: При уменьшении теплоотдачи спазмируются сосуды кожи появляется разница между температурой кожи и окружающей среды, возникает мышечная дрожь, часть химической энергии АТФ переходит в тепловую энергию, Образование тепла
Влияние нервной системы на процессы терморегуляции
На терморегуляцию оказывают влияние следующие отделы НС:
А) гипоталамус, где находится центр терморегуляции
Б) спинной мозг, в нём находятся спинно-мозговые центры терморегуляции, но они подчинены гипоталамусу. При перерезке спинного мозга возможно прекращаеие потоотделения и другие нарушения терморегуляции
В) кора больших полушарий, так как увеличение температуры тела можно вызвать условно рефлекторным путём.
В центре терморегуляции работают следующие нейромедиаторы:
а) «термостат» — серотонин, норадреналин
б) «установочная точка» — ацетилхолин
Механизм повышения температуры.
1. поступление в организм экзогенного пирогенна, например, микроорганизмов.
2. Фагоцитоз экзогенного пирогенного фактора
3. Образование экзогенных пирогенов в фагоцитах
5. кровь, содержащая эндогенные пирогенны, омывает центр терморегуляции
6. Действие эндогенных пирогенов на «установочную точку»
а) смена медиатора ацетилхолина на простагландин Е2 за счёт активации фермента простагландинсинтетазы
б) образование нового белка- медиатора, который вообще в норме отсутствует в центре терморегуляции
в) увеличение Na и уменьшение Ca в преоптической зоне гипоталамуса
Эти три нарушения приводят к тому, что нейроны «установочной точки» приобретают повышенную чувствительность, их порог возбудимости снижается и нормальную температуру тела они воспринимают как заниженную.
7. «установочная точка» активирует центры теплопродукции и теплоотдачи
а) Центр теплопродукции возбуждает симпатический отдел ВНС следовательно теплопродукция усиливается
-увеличивается распад гликогена в hepar
-увеличивается о/в в hepar и внутренних органах
-появляется мышечная дрожь
б) Центр теплоотдачи возбуждает симпатический отдел ВНС и угнетает парасимпатический отдел ВНС, следовательно теплоотдача уменьшается
-взъерошивание шерсти у животных
8. температура тела возрастает
1. стадия повышения температуры (= st. Incrementum)
температура тела повышается до момента, пока не достигнет нового «эталона» установочной точки
при повышении температура тела никогда не превысит 42,2 0 С
варианты повышения температуры тела:
а) резкое уменьшение теплоотдачи и умеренное повышение теплопродукции. Температура тела увеличивается очень быстро. Может быть при гриппе, крупозной пневмонии
б) значительное увеличение теплопродукции и умеренное снижение теплоотдачи. Температура тела повышается медленно. Может быть при бронхопневмонии, бр. тифе.
2. Стадия высокого стояния температуры (= st. fascigium)
температура тела соответствует новому «эталонному» уровню установочной точки.
Кожа гиперемирована и горячая. Озноб прекращается.
3. Стадия снижения температуры (st. descrementum)
увеличение теплоотдачи и снижение теплопродукции.
Снижение температуры тела может быть
А) критическое – т.е. стремительное. Осложнение – резкое падение АД в результате выраженное расширение сосудов
Б) литическое – постепенное
Типы лихорадки
А. По степени подъёма температуры
Субфебрильная – от 37,1 до 37,9 0 С
Умеренная — от 38,0 до 39,5 0 С
Высокая — от 39,6 до 40,9 0 С
Гиперпиретическая – от 41, 0 и выше
Б. По характеру колебаний суточной температуры
1. Перемежающаяся лихорадка размах колебаний большой, утром – норма, вечером – максимум.
Может быть при: гнойной инфекции, туберкулёзе и т.д.
2. Послабляющая лихорадка суточные колебания превышают 1 0 С, но снижение температуры до нормы не бывает. Может быть при: вирусных и бактериальных инфекциях.
3. Изнуряющая лихорадка суточные колебания температуры 3 – 5 0 С
Может быть при: сепсисе, гнойной инфекции
4. Постоянная лихорадка температура высокая (39,6 – 40,9 0 С)
Суточные колебания не более 1 0 С
Может быть при: крупозной пневмонии, сыпном и брюшном тифе
5. Возвратная лихорадка чередование лихорадочных и безлихорадочных периодов. Приступ лихорадки может длиться от 1 до нескольких суток
Может быть при: возвратном тифе, малярии, лимфогрануломатозе
6. Атипичная лихорадка в этом случае обычно утренная температура выше вечерней
Изменение обмена веществ и физиологических функций при лихорадке
Набор нарушений включает следующее: 1. Активация окислительных процессов
3. Углеводный обмен – усиливается распад гликогена в hepar
— снижается (гликогена) в гепатоцитах
— в моче глюкозурия (не всегда)
Причина: активация симпатического отдела ВНС
4. Жировой обмен: — увеличивается мобилизация жира из депо
— обмен ж/кислот идёт не до конца
— увеличивается образование кетоновых тел
5. Белковый обмен – распад белка преобладает над синтезом (+ опер. азотистый баланс)
а) стадия стояния температуры: задержка в тканях воды и хлоридов
Причины: увеличение содержания в крови альдостерона
б) стадия снижения температуры: увеличение выведения воды и хлоридов с мочой и потом.
— нарушение условно-рефлекторной деятельности коры
— угнетение процессов торможения
Эти нарушения дают клинически
— головная Большое спасибо,- бред
8. Сердечно-сосудистая система
— увеличение ЧСС (на 1 0 С тепературы приходится 8 – 10 ударов)
— увеличение МОК примерно на 27%
— АД изменяется постадийно: I ст. лихорадки- немного выше
III ст. лихорадки- может резко снизиться при критическом падении температуры до развития острой сосудистой недостаточности S. Коллапса
9. Система дыхания – наблюдается изменение ЧД, причём по-разному в зависимости от стадии лихорадки.
10. Со стороны почек – наблюдается изменение диуреза в зависимости от стадии лихорадки.
I стадия – увеличение диуреза. Причина6 увеличение притока крови, ко внутренним органам, в том числе к почкам
II стадия – снижение диуреза. Причина: испарение воды с кожи и слизистых.
– угнетение секреции пищеварительных соков:
слюны, желудочного сока, кишечного сока, сока панкреаз
отсюда резкое нарушение пищеварения. Следовательно при лихорадке должна быть легкоусвояемая, но высококалорийная диета
— угнетение моторики желудка приводит к задержке пищи в желудке и развиваются запоры
— сочетание угнетения секреции и моторики приводит к усилению гниения, брожения, аутоинтоксикации и образованию токсинов
— образование токсинов в кишечнике: интоксикация
а) снижение АД во II стадию лихорадки
б) ослабляют функцию миокарда
в) приводят к головной боли
д) действие на периферический отдел НС
Весь этот комплекс по сути и есть комплекс ИНТОКСИКАЦИ. Другими словами, при лихорадке интоксикация связана с нарушением пищеварения.
Гипертермия: этиология, отличия от лихорадки
Дополнения: два вида экзогенные
Экзогенные гипертермии: при снижении теплоотдачи за счёт внешних факторов
Эндогенные гипертермии: увеличение теплообразования без действия эндогенных пирогенов.
Как увеличенное теплообразование при эндогенной гипертермии за счёт разобщения тканевого дыхания и окислительного фосфорилирования
Механизм разобщения т.к. дыхания и окисления фосфорилирования
А) непосредственная стимуляция симпатического отдела ВНС
Б) прямое воздействие на клетки периферических тканей
— действии некоторых гормонов
— действии некоторых лекарств
— введении в кровь гипертонических растворов NaCl
— механической травме мозга («тепловой укол»)
Лихорадка и гипертермия (различия)
Лихорадка: работа центра терморегуляции перестраивается для активной задержки тепла независимо от температуры окружающей среды
Гипертермия: организм стремится освободиться от излишнего тепла путём максимального напряжения процессов теплоотдачи.
1. Быков К.М., Владимиров Г.Е., Делов В.Е., Конради Г.П., Слоним А.Д. / Учебник физиологии Под ред. Акад. К.М. Быкова Гос. Изд-во мед. Литературы.
2. Патофизиология: практикум / Под ред. В.Ю. Шанина. СПб: Питер, 2002.
3. Руководство по внутренним болезням / Под ред. L. Krehl‘я. Т 1, русское издание четвертое.
источник
1.Определение понятия лихорадка и гипертермия.
2.Патогенез клинических проявлений лихорадки.
4.Патогенез лихорадочной реакции.
Лихорадка (febris, pyrexia) — типовое изменение терморегуляции высших гомойотермных животных и человека на воздействие пирогенных раздражителей, выражающееся перестройкой терморегуляторного гомеостаза организма на поддержание более высокого уровня теплосодержания и температуры тела.
В отличие от лихорадки — гипертермия (hyperthermia — перегревание) — состояние организма, характеризующееся нарушением теплового баланса и повышением теплосодержания организма.
Лихорадка и гипертермия -это типические патологические процессы,общим признаком которых является повышение температуры тела. Главным их отличием является то, что при лихорадке уровень температуры тела не зависит от температуры окружающей среды. При гипертермии имеется прямая зависимость.
По своему биологическому значению лихорадка — это защитно-приспособительная реакция, а гипертермия — это полом, нарушение терморегуляции, отсюда разный подход к ведению больных.
Принято выделять ядро организма и его оболочку. Ядро составляют мозг, грудная, брюшная и тазовая полости. В ядре организма температура жестко фиксирована в пределах 37 градусов — т.е. ядро гомойотермно. А температура оболочки зависит от температуры окружающей среды. Таким образом, оболочка — пойкилотермна.
Какие же механизмы так тонко регулируют теплопродукцию и теплоотдачу? Это осуществляет центр терморегуляции гипоталамуса. Он состоит из трех различных морфологических образований.
1. термочуствительная часть,
2. термоустановочная часть, определяет уровень температуры тела,
3. два эфферентныхобразования:
Стадии лихорадки:
1) Stadium incrementi — стадия подъема температуры тела,
2) Stadium fastigii — стадия стояния высокой температуры,
3) Stadium decrementi — стадия снижения температуры и возврат ее к норме.
Клиническая характеристика стадий:
1-я стадия — повышение температуры — характеризуется ознобом, сопровождающимся ощущением холода. Патогенез озноба — происходит спазм сосудов кожи и понижение температуры кожи на 10-12 градусов (кроме подмышечной и паховой области). Это вызывает раздражение холодовых рецепторов (ощущение холода) и ответную реакцию на холод — мышечную дрожь. Субъективно все это воспринимается, как озноб. Подъем температуры тела может быть быстрым, а озноб очень сильным и наоборот, медленным, постепенным, с незначительным ознобом или даже без него.
Во второй стадии (патогенез ощущения жара) больной говорит, что он горит от жара. Это ощущение обусловлено расширением сосудов кожи при высокой температуре тела. По особенностям температурной кривой (высоты подъема) в зависимости от характера ее колебаний в течение суток различают следующие виды лихорадки:
1) субфебрильную — до 38 градусов,
2) умеренную — 38-39 градусов,
3) высокую — 39-40 градусов и
4) чрезмерную — гиперпиретическую (41 градус и выше). Во время лихорадки температура тела может доходить до 42 градусов. При превышении этой границы возникают глубокие нарушения функции ЦНС и может возникнуть угроза для жизни больного.
Степень повышения температуры при различных заболеваниях зависит:
1) от реактивности организма (например у холериков температура тела выше),
2) от введения возбуждающих ЦНС веществ: кофеин, фенамин (а наркоз и бромиды снижают реакцию),
3) от пирогенной активности микробов,
4) от интенсивности выработки эндогенных пирогенов, то определяется количеством лейкоцитов,
5) от функционального состояния центров терморегуляции и образования медиаторов.
Типы лихорадочных (температурных) кривых:
1) постоянная температурная кривая (febris continua) — колебания в пределах не более 1 градуса,
2) ремиттирующая — febris remittens — или послабляющая (колебания температуры в пределах 1,5 — 2 градусов),
3) перемежающаяся или интермиттирующая — febris intermittens- это правильное чередование нормальной температуры с периодами подъема,
4) возвратная — febris recurrens -5-7 дней лихорадка и 3-4 дня норма, т.е. промежутки между лихорадочным периодом и периодами нормы, как правило, не одинаковые.
5) изнуряющая или гектическая — febris hectica колебания температуры в течение суток доходят до 3-5 градусов (утром норма, вечером 40 градусов). При этом лихорадка может быть атипичной, когда утром температура выше, чем вечером.
Патогенез 3 стадии (снижения температуры) проявляется клинически потоотделением. Потоотделение является основным видом отдачи тепла в период снижения температуры и возврата ее к норме. Температура тела может падать быстро (критически) и медленно (литически). Быстрое падение температуры может быть опасным, особенно у лиц пожилого возраста, перенесших инфаркт миокарда или имеющих кардиосклероз. Кризис может привести к коллапсу от острой сердечной недостаточности.
Этиологические факторы лихорадки. Они делятся на инфекционные и неинфекционные: это липополисахариды микробов, их экзо- и эндотоксины, вирусы, риккетсии, клетки чужеродного трансплантата, продукты распада собственных тканей, лимфокины, хемотаксины, комплекс аллерген-антитело, аллергены.
Лихорадка вызывается особыми веществами — пирогенами. Они по происхождению делятся на:
1. Экзопирогены (из эндотоксинов микробов — бактериальные).
2. Эндопирогены (клеточные).
Характеристика экзопирогенов: по химическому строению — это высокомолекулярные липополисахариды.
1) экзопирогены вызывают лихорадку опосредованно через образование эндопирогенов, поэтому лихорадка развивается через 45-60 минут и максимум ее через 3-4 часа,
3) термоустойчивы (для разрушения надо автоклавировать в течение 1-2 часов при температуре 200 градусов),
6) но несут на себе антигенную химическую специфичность — т.е. являются гаптенами. Для приобретения антигенных свойств они должны соединиться с белками клеток и тканей,
7) при ежедневном введении 5-6 раз к экзопирогенам возникает толерантность и лихорадка не развивается,
8) экзопирогены вызывают ряд защитных эффектов.
Эндогенные пирогены: их источником являются нейтрофилы, макрофаги и лимфоциты крови — это лейкоцитарные пирогены или интерлейкин-1.
Свойства лейкопирогенов:
1) вырабатываются только живыми лейкоцитами, по строению — это белок типа альбумина,
2) неустойчивы к нагреванию — разрушаются при температуре, вызывающей коагуляцию белка (60-70 градусов),
3) температурная реакция на эндопироген развивается через 10-15 мин. Максимум подъема температуры после введения эндопирогена через 1-2 часа (экзопирогена 3-4).
1) он вырабатывается в микро- и макрофагах, не вызывает толерантности, нетоксичен, действует на все основные регулирующие системы организма и прежде всего те, которые определяют реактивность и резистентность — нервную и эндокринную,
2) действует на клетки гипоталамуса и усиливает выработку CRF, которые запускают стресс-реакцию, мобилизуют энергетические ресурсы, развиваются гипергликемия, липемия.
Эндопирогены дают такой же биологический эффект, как и экзопирогены, повышая защитные свойства организма:
2) усиливают выработку глюкокортикоидов,
3) усиливают регенерацию тканей, которая ведет к образованию нежных рубцов (применяется при повреждении ЦНС для предотвращения осложнений (эпилепсии, парезов, параличей),
4) усиливают дезинтоксикационную функцию печени,
5) улучшают процессы микроциркуляции — вот почему пирогены применяются при вялом течении заболеваний,при хронической язве желудка для ускорения заживления и рубцевания язв, при почечной гипертонии для улучшения процессов микроциркуляции в почках(в нефроне, клубочках) и уменьшения выработки ренина.
Лейкопироген вырабатывается при раздражении лейкоцитов:
3) под влиянием шероховатости стенки сосудов, при контакте лейкоцитов с микробами даже в кровеносном русле,
4) при изменении pH в кислую сторону (ацидоз).
Характеристика лимфоцитарных и макрофагальных пирогенов. Макрофаги крови альвеол и брюшины в процессе фагоцитоза вырабатывают такое же вещество, как нейтрофилы — интерлейкин-1. Лимфоцитарный пироген вырабатывается сенсибилизированными лимфоцитами при аллергии при контакте с аллергеном.
Патогенез лихорадочной реакции(механизмы накопления тепла в организме). Измерение количества тепла в организме методом прямой калориметрии показало, что увеличение образования тепла не превышает 25 %. Лишь в стадии стояния температуры на высоких цифрах увеличение образования тепла достигает 40 %. Каковы же особенности теплообмена при лихорадке? Почему повышается температура тела?
2) усиление теплопродукции. Исследования влияния пирогенов показало, что организм сам активно формирует лихорадку. Подъем температуры в начальной стадии связан с уменьшением теплоотдачи — это главное звено патогенеза. Усиление теплопродукции помогает быстрее повысить температуру (быстрее разогреться).
Цепь патогенеза лихорадки:
1) внедрение экзогенных пирогенов в организм,
2) взаимодействие экзопирогенов с фагоцитами организма,
4) выделение активированными фагоцитами эндопирогенов — интерлейкина-1,
5) воздействие интерлейкин-1 на центр терморегуляции (в 1-ю очередь на термоустановочную точку),
6) повышение возбудимости холодочувствительных нейронов и снижение возбудимости теплочувствительных нейронов,
7) индукция усиленного синтеза простагландина Е2 в нервных клетках гипоталамуса и возбуждение симпатоадреналовых структур,
8) ограничение теплоотдачи (за счет спазма поверхностных сосудов) и повышение теплопродукции,
9) повышение температуры тела до нового уровня регулирования.
Влияние на лихорадку физической работы и температуры окружающей среды. Установлено, что: 1) физическая работа, 2) умеренное согревание или 3) умеренное охлаждение при лихорадке температуру тела не меняют. Увеличение теплообразования даже более чем на 200 % не меняет температуры. Т.е. при лихорадке механизмы терморегуляции находятся в активном состоянии, лихорадящий организм удерживает температуру на высоких цифрах, сохраняя температурный гомеостаз.
Доказательства прямого действия эндопирогенов на центры терморегуляции:
1) наркоз подавляет лихорадку,
2) введение возбуждающих средств — усиливает ее,
3) у больных с психическими заболеваниями в стадии возбуждения пирогены вызывают более высокую лихорадку, чем в состоянии депрессии,
4) после введения пирогенов возникает повышение биоэлектрической активности центров теплорегуляции на электроэнцефалограмме,
5) у истощенных, ослабленных людей, у стариков с пониженной реактивностью ЦНС лихорадочная реакция резко ослаблена,
6) применение жаропонижающих средств, которые оказывают специфическое тормозящее влияние на центры терморегуляции и вызывают понижение температуры тела. Вызывая расширение сосудов, они увеличивают теплоотдачу и за счет этого снижение температуры.
Состояние центров теплорегуляции находит отражение в характере температурной кривой:
● лихорадка постоянного типа свидетельствует об устойчивом — оптимальном возбуждения центра терморегуляции,
● ремиттирующая кривая свидетельствует о неустойчивости возбуждения центра терморегуляции,
● интермиттирующая лихорадка характерна для септического состояния.
● неблагоприятно протекает гектическая — она свидетельствует о том, что периоды возбуждения центра терморегуляции сменяются периодами запредельного торможения. Характер температурной кривой отражает состояние реактивности еще ряда центров: ДЦ и ВМЦ.
Вот почему эти кривые имеют диагностическое и прогностическое значение. Особенно неблагоприятным является извращенный характер лихорадки — что говорит о быстром истощения центра терморегуляции.
Биологическое значение лихорадки — в основном создание более высокого температурного фона для обменных процессов, что ведет к повышению уровня защитных реакций:
1) активирование ферментов,
Известно, что биохимические процессы протекают значительно быстрее при температуре 39 градусов, чем при 36. Это одна из приспособительных реакций организма.
1. Виды, причины и патогенез гипертермий.
2. Отличие лихорадки от гипертермий.
3. Тактика врача при повышении температуры тела.
4. Особенности перегревания у детей.
Дата добавления: 2015-06-27 ; Просмотров: 2726 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
источник
| Показатели | Лихорадка | Гипертермия |
| Этиология | Пирогенны | Без воздействия пирогенов, а за счет ¯ ТО при T° |
| Патогенез | Активная перестройка ЦТР ® работа на новом более высоком уровне | Нарушение функции ЦТР, перегревание организма |
| Терморегуляция | Активное Т° | Противодействие Т° |
| Участие организма | Создается организмом | Возникает вопреки организму |
| Биологическое значение | Преимущественно адаптационное | Дезадаптация |
| Повреждение организма | Редко | Всегда |
| Течение | Стадийное | Нет стадийности, возрастание Т° и симптоматики |
| Филогенез | Только у гомойотермных животных | У гомо- и пойкилотермных животных |
| Онтогенез | Развивается к концу первого года жизни | Имеется и у новорожденных |
Гипертермический синдром возникает при острых и хронических заболеваниях головного мозга, характеризуется периодическими подьёмами температуры тела до высоких значений. При этом самочувствие не страдает. Механизмы гипертермического синдрома во многом неясны.
Температурный гомеостаз обеспечивает оптимальные условия для метаболических процессов при изменениях температуры внешней и внутренней среды (табл.6.2.). При патологии увеличение температуры тела – лихорадка способствует повышению резистентности организма к действию повреждающих факторов. Однако, неконтролируемое повышение температуры тела, обусловленное неспособностью организма вывести избыток тепла – перегревание является всегда патологическим, угрожающим жизни состоянием.
Глава 7. Инфекционный процесс
Инфекционные заболевания являются одной из основных причин смертности. Возбудители особо опасных инфекционных заболеваний, таких как чума, оспа, сибирская язва до недавнего времени рассматривались в качестве биологического оружия. В последние десятилетия человечество сталкивалось как с открытием новых опасных возбудителей, так и с мутацией известных. Открыт вирус, вызывающий синдром приобретенного иммунодефицита (СПИД), а также бактерия (Helicobacter pylori), способствующая поражению слизистой оболочки желудка и развитию язвенной болезни. В настоящее время представления о роли инфекции в качестве причины развития заболеваний значительно расширились. Доказано её существенное влияние на развитие некоторых онкологических заболеваний, в частности, рака шейки матки и печени. Нередко инфекция провоцирует развитие аутоиммунных заболеваний, например вирус Коксаки может быть фактором развития сахарного диабета 1 типа, а стрептококковая инфекция — провоцировать аутоиммунное поражение сердца и почек. Имеются экспериментальные и клинические данные об участии инфекции в развитии таких неинфекционных заболеваний как атеросклероз, синдром хронической усталости и многих других видов патологии.
Инфекционный процесс – типовой патологический процесс, возникающий под действием внедрившихся в организм патогенных микроорганизмов и характеризующийся комплексом реакций, направленных на уничтожение возбудителя и восстановление гомеостаза. Инфекционный процесс составляет основу инфекционных заболеваний.
Основными видами инфекционного процесса являются: сепсис — генерализованный инфекционный процесс, обусловленный размножением микроорганизмов в крови и, нередко, в других биологических жидкостях организма; септикопиемия — характеризуется вторичным развитием гнойных очагов в различных тканях и органах у пациентов с сепсисом.
Инфекционный процесс, вызванный одновременно двумя или более возбудителями называется микстинфекцией. Под реинфекцией понимают повторное (после выздоровления) возникновение инфекционного процесса, вызванное тем же микроорганизмом; суперинфекция – повторное инфицирование организма (до выздоровления) тем же возбудителем; вторичная инфекция — инфекционный процесс, развивающийся на фоне инфекционной болезни, вызванной другим микроорганизмом.
Инфекционный процесс вызывается патогенными микроорганизмами, основными из которых являются бактерии, вирусы и грибы (табл.7.1).
Основные микроорганизмы, вызывающие инфекционный процесс
| Группа (семейство) | Размер | Характер повреждения |
| Вирусы | 20-300 нм | Внутриклеточное |
| Хламидии | 200-1000 нм | Внутриклеточное |
| Риккетсии | 300-1200 нм | Внутриклеточное |
| Микоплазмы | 100-300 нм | Внеклеточное |
| Бактерии | 1-15 mм | Внеклеточное, внутриклеточное |
| Грибы | 2-200 mм | Внеклеточное, внутриклеточное |
| Простейшие | 1-50 mм | Внеклеточное, внутриклеточное |
Патогенность (способность вызывать заболевание) определяет: проникновение микроорганизма в макроорганизм (инфективность), размножение в нём, развитие болезни с характерным для данного возбудителя патогенезом. Выделяют непатогенные, условно патогенные и патогенные микроорганизмы. Условно патогенные микроорганизмы могут вызвать заболевание только при иммунодефицитных состояниях или при наличии особых условий. Мерой патогенности микроорганизмов является вирулентность. Под вирулентностью понимают свойство, характеризующее степень болезнетворности микроорганизма. Она зависит от характеристик микроорганизма, а также от резистентности макроорганизма.
Факторы распространения инфекционного процесса обеспечивают или облегчают проникновение возбудителя в организм и распространение в нём. К ним относятся: ферменты (гиалуронидаза, коллагеназа, нейраминидаза); специальные органы-жгутики (имеются у холерного вибриона, кишечной палочки, протея); ундулирующая мембрана (есть у спирохет и некоторых простейших).
Однако даже при высокой степени патогенности и вирулентности микроорганизма для развития инфекционного процесса необходимы определенные условия: 1) взаимодействие патогенного микроорганизма со своими «входными воротами», т.е. контакт с теми клетками, с которыми он может связаться, взаимодействуя со структурами клеточной мембраны; 2) нарушение барьерных систем, препятствующих внедрению микроорганизмов (кожа и слизистые оболочки, мукоцилиарный клиренс, бактерицидное действие компонентов слюны, желудочного и кишечного соков, выведение микроорганизмов из организма – мочеиспускание и дефекация); 3) Недостаточность систем неспецифического или специфического иммунитета; 4) Высокая индивидуальная восприимчивость к инфекции зависит от пола, возраста, конституции и наследственности. Основными являются возраст и наследственный фактор.
Развитие инфекционного процесса обусловлено индивидуальной чувствительностью организма к возбудителю, определяющейся наследственным фактором. Состояние здоровья, характер питания, наличие сопутствующих заболеваний также влияют на развитие инфекционного процесса.
Патогенез инфекционного процесса зависит от множества факторов, в первую очередь от вида и свойств возбудителя, определяющих его повреждающую способность, а также от реактивности организма.
Повреждающее воздействие микроорганизмов обусловлено их следующими свойствами: способностью внедряться в клетку; образованием токсинов, особенно экзотоксинов, вызывающих повреждение клеток (например, токсин возбудителя газовой гангрены) или резкое нарушение их функции (например, токсин возбудителя холеры); способностью изменять антигенную структуру клетки, что приводит к повреждению клетки иммунной системой (например, вирус гепатита В при попадании в клетки печени не вызывает их повреждения, но вызывает реакцию иммунной системы и повреждение гепатоцитов происходит Т-лимфоцитами и тканевыми макрофагами – клетками Купфера.
Вторым важнейшим фактором, определяющим развитие инфекционного процесса, является активация защитных реакций организма, направленных на обнаружение, уничтожение и/или удаление возбудителя, а также на восстановление структурно-функциональных нарушений.
Механизмы, препятствующие проникновению возбудителя в организм и развитию инфекционного процесса, подразделяют на две группы: неспецифические (играющие роль при контакте со всеми или многими возбудителями) и специфические (направленные против конкретного микроорганизма).
Инфекционный процесса развивается стадийно: происходит проникновение возбудителя в организм, размножение микроорганизма и выделение продуктов его жизнедеятельности (инкубационный период), а также возникает неспецифический ответ организма (повышение активности нервной, эндокринной, иммунной систем) на последствия жизнедеятельности микроорганизма (продромальный период).
В зависимости от вида возбудителя продромальный период может быть различной длительности и выраженности (может даже отсутствовать). Наиболее тяжело протекает период разгара заболевания, то есть максимального патогенного воздействия микроорганизмов и максимальной ответной реакции организма.
Исходы инфекционного процесса зависят от типа возбудителя, реактивности и резистентности организма, а также от качества лечения. Инфекционный процесс может завершиться: 1) полным выздоровлением; 2) выздоровлением с последствиями (дефект ткани, формирование рубца, уменьшение количества функционирующих клеток органа с развитием его недостаточности, например, сердечной недостаточности вследствие миокардита); 3) переходом инфекционного процесса в хроническую форму (специфические инфекции — туберкулез, неспецифические инфекции, например, при гнойных заболеваниях, когда вокруг гнойного очага формируется соединительнотканная капсула) и 4) генерализацией инфекции – наиболее опасный для жизни вариант развития процесса.
Инфицирование сопровождается воспалением — защитной реакцией организма. Локализация (нераспространение) инфекции обеспечивается в основном с помощью системы неспецифического иммунитета и в меньшей степени — специфического иммунитета. При несостоятельности системы иммунитета происходит распространение инфекции (генерализация инфекционного процесса) по кровеносным и лимфатическим сосудам, вдоль нервных стволов.
Клинически генерализация инфекции проявляется в виде следующих состояний (по мере их утяжеления): синдром системного воспалительного ответа (ССВО), сепсис, септический шок, полиорганная недостаточность.
Дата добавления: 2018-10-26 ; просмотров: 85 ; ЗАКАЗАТЬ РАБОТУ
источник
Опубликовано в журнале:
«Русский медицинский журнал», 2011, ТОМ №19, № 18, с. 1-7
Профессор Л.И. Дворецкий
1 МГМУ имени И.М. Сеченова
Лихорадка – один из древнейших защитно–приспособительных механизмов организма в ответ на действие патогенных раздражителей, главным образом инфекционных агентов.
Издавна у постели лихорадящего больного перед врачами всех времен возникало две проблемы, требующие по возможности быстрого принятия решения – диагностическая и терапевтическая. Основная проблема, разумеется, заключалась в распознавании причины лихорадки, а следовательно, в выборе адекватного лечения (этиотропная, патогенетическая, симптоматическая терапия). Другая задача касалась воздействия на лихорадку как на симптом (симптоматическая терапия), влияющий на состояние больного, на различные органы и системы. По мере прогресса медицинской науки обе проблемы и поныне сохраняют актуальность и клиническое значение во врачебной практике.
В данной статье предполагается рассмотреть современное состояние проблемы симптоматического лечения лихорадки с использованием жаропонижающих средств, независимо от ее причины, а также с позиций современного понимания механизмов лихорадочной реакции организма.
Патофизиология лихорадки
Повышение температуры тела является одной из приспособительных реакций живого организма в ответ на воздействие разнообразных патогенных факторов (инфекции, эндотоксины, опухоли, конфликты в иммунной системе, травмы и повреждения, отравления, физические факторы и др.). Показано, что у млекопитающих при повышении температуры тела повышается фагоцитоз, продукция антител, выработка интерферона, стероидных гормонов и альдостерона, что позволяет рассматривать лихорадку как биологически целесообразную реакцию [1].
Терморегуляция представляет собой процесс, в котором участвует целый континиум нервных структур и соединительных нервных волокон, исходящих из гипоталамуса и лимбической системы и идущих через нижние отделы ствола головного мозга и ретикулярную формацию в спинной мозг и симпатические ганглии. Главную роль в процессе терморегуляции играет участок головного мозга, расположенный в переднем гипоталамусе и в преоптической области, более известный, еще со студенческой скамьи как центр терморегуляции, предназначенный для регулирования температуры тела в норме и патологии [2].
Следует различать понятия «лихорадка» и «гипертермия», которые иногда употребляются как синонимы при обозначении одного и того же состояния. В основе повышения температуры тела при лихорадке и гипертермии лежат разные механизмы. Лихорадка представляет собой сложный патофизиологический ответ организма на различные патогенные воздействия в виде повышения температуры тела, опосредуемого цитокинами, наряду с образованием реактантов острой фазы и активацией многих систем (иммунной, эндокринной и др.). В отличие от лихорадки, гипертермия – нерегулируемое повышение температуры тела, в котором пирогенные цитокины непосредственного участия не принимают, а жаропонижающие средства при этом оказываются неэффективными. Иными словами, гипертермия представляет собой сбой терморегуляторного гомеостаза, при котором происходит неконтролируемая выработка тепла, недостаточная теплоотдача или нарушение терморегуляции на уровне гипоталамуса [3]. Теплопродукция может повышаться при тиреотоксикозе и феохромоцитоме. Причиной гипертермий могут быть лекарственные препараты (ингибиторы моноаминоксидазы (МАО), трициклические атидепрессанты, нейролептики, М–холиноблокаторы, антипаркинсонические препараты). Особое место среди гипертермий занимает так называемая злокачественная гипертермия – наследственное заболевание, характеризующееся избыточным накоплением ионов кальция в миоплазме, что вызывает длительную контрактуру мышц. Длительное мышечное сокращение вызывает значительное повышение температуры тела под влиянием анестетиков и мышечных релаксантов (триггерные агенты). Гипертермия развивается обычно во время или после анестезии. В таблице 1 представлены основные признаки лихорадки и гипертермии.
Таблица 1. Основные признаки лихорадки и гипертермии
| Основные признаки | Лихорадка | Гипертермия |
| Величина температуры тела | Обычно до 40°С | Часто выше 40°С |
| Патофизиологический механизм | Высвобождение пирогенных цитокинов под влиянием экзогенных пирогенов | Повышенное высвобождение тепла |
| Механизмы терморегуляции | Сохранены | Нарушены |
| Основные причины | Инфекции, опухоли, системные васкулиты, медикаменты | Перегревание, лекарства, нарушение ЦНС, тиреотоксикоз, феохромоцитома, злокачественная гипертермия |
| Эффект жаропонижающих препаратов | Обычно эффективны | Отсутствует |
| Прогноз | Зависит от основного заболевания | Летальность до 20% при злокачественной гипертермии |
Схема лихорадочной реакции у человека в ответ на воздействие различных патогенных факторов представлена на рисунке 1. Данная схема заимствована из статьи А.И. Воробьева и М.Д. Бриллиант [1], одной из первых, посвященных проблеме лихорадок неясного генеза в клинической практике.
| Рис. 1. Схема развития лихорадочной реакции [1] | Рис. 2. Гипотетическая модель лихорадочной реакции [3] Повышение температуры тела происходит при участии экзогенных и эндогенных пирогенов и их взаимодействии друг с другом. Экзогенные пирогены представлены микроорганизмами, токсинами и другими продуктами микробного происхождения (липополисахариды), а также неинфекционными антигенами, иммунными комплексами. Эндогенные пирогены – это клеточные цитокины, являющиеся главным медиатором лихорадки. Под воздействием экзогенных пирогенов происходит стимуляция клеток, главным образом нейтрофилов, моноцитов, макрофагов, вырабатывающих эндогенный пироген (пирогенные цитокины). Способностью к выработке эндогенного пирогена обладают опухолевые клетки (лимфопролиферативные опухоли, рак почки, печени и др.). Этим, по–видимому, и объясняется наличие лихорадки у данной категории пациентов, причем нередко опережающей другие симптомы болезни [4]. В настоящее время известно 11 цитокинов, обладающих пирогенной активностью. К наиболее важным пирогенным цитокинам относятся: интерлейкин–1 (ИЛ–1), интерлейкин–6 (ИЛ–6), фактор некроза опухоли–α (ФНО–α), γ–интерферон [5]. Указанные цитокины находятся в тесном взаимодействии друг с другом: некоторые из них в одних условиях усиливают экспрессию других цитокинов или их рецепторов, а в других – снижают ее. Согласно одной из гипотез, предполагается, что при взаимодействии между пирогенными цитокинами и их рецепторами в преоптической области происходит активация фосфолипазы А2, с высвобождением арахидоновой кислоты в качестве субстрата для циклооксигеназного пути. Некоторые цитокины могут вызывать такой эффект посредством прямого увеличения экспрессии циклооксигеназы, в результате чего образуются метаболиты арахидоновой кислоты – простагландина (ПГ) Е2 и ПГF2a [3,6]. Последний легко проникает через гематоэнцефалический барьер и может служить медиатором, активирующим термочувствительные нейроны с последующим повышением температуры тела (рис. 2). Негативные эффекты лихорадки Будучи биологически целесообразной реакцией организма, свидетельствующей о неблагополучии и направленной на борьбу с патогенами, в частности инфекцией, лихорадка в то же время может вызывать целый ряд негативных последствий у пациентов всех возрастных групп. Такие ситуации могут возникать у больных при наличии тяжелой сопутствующей патологии и риске ее декомпенсации на фоне лихорадки, а также в случаях индивидуальной плохой переносимости высокой температуры. Негативные последствия повышения температуры тела до фебрильных цифр сводятся к следующим:
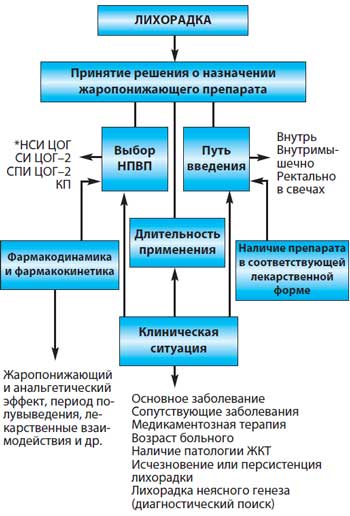
Вышеуказанные негативные последствия лихорадки могут оказывать особенно неблагоприятное воздействие на больных, страдающих различными сердечно–сосудистыми, неврологическими и другими заболеваниями. С учетом этого лихорадка у данной категории пациентов требует купирования или ослабления ее проявлений, т.е. симптоматического лечения. Медикаментозные способы купирования лихорадки основаны на знаниях и понимании механизмов повышения температуры тела при различных патологических процессах. Жаропонижающий эффект препаратов осуществляется на уровне центра терморегуляции при их взаимодействии с так называемыми медиаторами повышения температуры – «посредниками» между эндогенным пирогеном (пирогенными цитокинами) и температурными рецепторами преоптической области гипоталамуса. Одним из таких «посредников» является ПГ Е2, производное арахидоновой кислоты. Так, например, салицилаты необратимо связываются с синтетазой простагландина, а глюкокортикоиды подавляют синтез ПГ Е2, ингибируя фосфолипазу А2. Таким образом, мишенью всех антипиретиков является ПГ Е2, а возможно, и другие метаболиты арахидоновой кислоты. Вместе с тем жаропонижающие препараты не оказывают антипиретического действия при повышении температуры, не связанной с пирогенными цитокинами, например при гипертермиях, обусловленных уменьшением теплоотдачи (атропиновая гипертермия, злокачественная гипертермия, тепловой удар при перегревании и др.) История жаропонижающих средств Усилия врачей всех эпох медицины сводились к уменьшению выраженности лихорадки, снижению температуры тела и облегчению состояния больного даже при невозможности воздействовать на основную причину лихорадки. Способы купирования лихорадки были многообразны и диктовались исключительно клиническим опытом медиков, а также самих пациентов и их окружающих. Достаточно указать на воздействие низких температур непосредственно на тело больного (холодные компрессы, обертывания, пузыри со льдом и др.), использование некоторых химических веществ. Иногда эмпирически применяемые у лихорадящих больных «лекарства» оказывались в последующем именно этиотропными препаратами. Об этом свидетельствует опыт использования коры хинного дерева, которая веками применялась индейцами как жаропонижающее средство. С 1632 г. иезуитский миссионер Бернабе Кобо дал первое описание «иезуитской коры» и привез ее в Европу, где кору стали с успехом применять у лихорадящих больных. Оказалось, что эффект наблюдался только при лихорадках у больных малярией. Это происходило задолго до того, как в 1880 г. французский военный врач Шарль Лаверан предположил, что малярия вызывается простейшими, за что был удостоен впоследствии Нобелевской премии. В 1763 г. было сделано первое научное сообщение о жаропонижающем действии препарата, полученного из ивовой коры. Позже было установлено, что активным началом этого препарата является салицин, на основе которого в лабораториях немецкой компании Bayer, ранее производившей лишь анилиновые красители и учрежденной в 1863 г. коммерсантом Фридрихом Байером и владельцем небольшой красильни Иоганном Вескоттом, была создана ацетилсалициловая кислота (АСК), появившаяся в немецких аптеках в 1899 г. под торговым названием «аспирин». Однако задолго до появления на фармацевтическом рынке аспирина компанией Bayer был разработан препарат с жаропонижающими свойствами. Принятый в 1884 г. на службу в компанию 23–летний Карл Дуйсберг, вставший в последующем у руля корпорации, поручил одному из научных сотрудников разработать лекарство на базе паранитрофенола – побочного продукта производства красок, лежавшего на складе мертвым грузом. Так в 1887 г. на свет появился жаропонижающий препарат, для которого Дуйсберг придумал фирменное имя – фенацетин. Это лекарство широко использовалось в качестве жаропонижающего и анальгетического средства несколько десятков лет и лишь в 60–70–е гг. ХХ в. из–за негативных побочных эффектов было полностью изъято из употребления. К тому времени на фармацевтическом рынке появился новый препарат – парацетамол, который позиционировался как жаропонижающее и болеутоляющее средство, более безопасное по сравнению с АСК для детей и лиц с «язвенным анамнезом» [10]. В 1955 г. начались продажи парацетамола в США («Тайленол»), а в 1956 году – в Великобритании («Панадол»). Небезынтересно отметить, что это оказалось вторым рождением парацетамола, который является метаболитом фенацетина и был синтезирован в 1877 г. Однако только в 1887 г. (время внедрения в клиническую практику фенацетина) он был применен у больных Джозефом фон Мерингом. В 1893 г. автор опубликовал результаты клинического применения парацетамола и фенацетина (ацетанилида), утверждая, что парацетамол, в отличие от фенацетина, обладает способностью вызывать метгемоглобинемию. Это и открыло дорогу фенацетину, а парацетамол оказался забытым на десятилетия. В 1949 г. удалось установить, что фенацетин действительно метаболизируется в парацетамол, а метгемоглобинемия возникает у людей в основном под действием другого метаболита – фенилгидроксиламина. Было также высказано предположение, что загрязнение парацетамола 4–аминофенолом (веществом, из которого он был синтезирован фон Мерингом) могло стать причиной ложных выводов [7]. Это и привело к «повторному открытию» парацетамола [6]. Наконец фенацетин уступил место парацетамолу, который относительно широко стали применять после изъятия из оборота амидопирина и фенацетина. Появилось множество парацетамолсодержащих комбинированных лекарственных форм, в том числе в сочетаниях с ацетилсалициловой кислотой, метамизолом, кодеином, кофеином и другими препаратами. Лекарственные препараты с жаропонижающим эффектом Первые попытки воздействовать на лихорадку с помощью лекарственных средств связаны с применением ацетилсалициловой кислоты, уже с момента легализации ее в качестве лекарственного препарата. Однако с учетом ставших впоследствии известными фармакологических свойств АСК жаропонижающий эффект препарата в ряде случаев мог быть обусловлен не только и не столько его антипиретическими свойствами, но и воздействием на механизмы воспаления, одним из проявлений которого оказывалась лихорадка. АСК до сих пор служит препаратом номер один при лечении многих заболеваний, в том числе используется как жаропонижающее средство. Правда, показания к ее применению при лихорадке в последнее время были серьезно пересмотрены, особенно в педиатрической практике в связи с риском возникновения у детей синдрома Рея. В настоящее время АСК вытесняют другие жаропонижающие препараты, в первую очередь парацетамол. Парацетамол ингибирует синтез простагландинов, блокируя обе формы фермента циклооксигеназы (ЦОГ–1 и ЦОГ–2), причем действует преимущественно в ЦНС, воздействуя на центры боли и терморегуляции. Предполагается также, что препарат селективно блокирует ЦОГ–3, которая находится только в ЦНС, не влияя на ЦОГ–1 и ЦОГ–2, расположенные в других тканях. Этим объясняется выраженный анальгетический и жаропонижающий эффекты и низкий противовоспалительный [8]. Отсутствие блокирующего влияния на синтез простагландинов в таких тканях обусловливает отсутствие у него отрицательного влияния на слизистую оболочку желудочно–кишечного тракта (ЖКТ) и водно–солевой обмен (задержка ионов Na+ и воды). В отличие от АСК и других нестероидных противовоспалительных препаратов (НПВП), парацетамол не вызывает существенных побочных эффектов, прежде всего эрозивно–язвенных процессов в желудке, и поэтому остается предпочтительным для купирования лихорадки. Вместе с тем жаропонижающий эффект парацетамола был менее выраженным по сравнении с НПВП. Однако у АСК есть преимущества перед ним, когда речь идет о лихорадке у пациента с тяжелым поражением печени (в частности, при хроническом алкоголизме) и некоторых других состояниях. Вслед за АСК и парацетамолом арсенал жаропонижающих средств пополнялся новыми препаратами из группы НПВП, в частности производными индолуксусной кислоты (индометацин), фенилускусной кислоты (диклофенак), пропионовой кислоты (ибупрофен, кетопрофен, напроксен), оксикамы (пироксикам, мелоксикам), производные гетероарилуксусной кислоты (кеторолак) и др. Ибупрофен синтезирован и зарегистрирован в 1962 г., а с 1974 г. стал применяться в США в качестве болеутоляющего и жаропонижающего препарата. Самым ярким моментом в истории ибупрофена было получение в 1985 г. Королевской награды в знак признания научно–технических достижений в разработке этого препарата. В 1966 г. арсенал НПВП пополнился диклофенаком, а в дальнейшем были синтезированы пироксикам, напроксен. Комбинированное использование двух препаратов из группы НПВП обычно не считается рациональным, так как возможны нежелательные реакции со стороны желудочно–кишечного тракта. Вместе с тем, поскольку жаропонижающий эффект парацетамола был менее выраженным по сравнению с НПВП, с клинической точки зрения казалось логичным использовать комбинацию парацетамола с одним из НПВП (ибупрофеном), когда при суммировании обезболивающего эффекта побочные явления не усиливаются. Таким образом, ибупрофен является НПВП, обладающим противовоспалительным, жаропонижающим и обезболивающим действием, а парацетамол оказывает обезболивающее и жаропонижающее действие. Эффективность комбинации этих препаратов выше, чем отдельных компонентов. Парацетамол и ибупрофен, входящие в состав комбинированного препарата Ибуклин ® , полностью отвечают критериям высокой эффективности и безопасности и официально рекомендуются ВОЗ и национальными программами в качестве жаропонижающих средств [WHO, 1993; S. M. Lesko et al., 1997; Практические рекомендации для врачей Российской ассоциации педиатрических центров, 2000]. Ибуклин ® имеет существенные преимущества перед монопрепаратами – парацетамолом и ибупрофеном, т.к. в комбинированном препарате сочетается быстрое начало действия и длительный жаропонижающий эффект [13]. Ибуклин ® содержит 400 мг ибупрофена и 325 мг парацетамола. Препарат оказывает жаропонижающее, противовоспалительное, анальгезирующее действие, обусловленное неселективным ингибированием ЦОГ–1 и ЦОГ–2 и подавлением синтеза ПГ. Ибуклин ® применяется внутрь по 1 таблетке 3 раза/сут. (не более 6 таблеток в сутки). Длительность лечения – не более 3 дней в качестве жаропонижающего средства. Помимо купирования лихорадочного синдрома, препарат может быть использован в лечении болевого синдрома средней интенсивности. Препарат отпускается по рецепту врача. Кроме того, зарегистрирована детская форма препарата Ибуклин юниор, содержащая 100 мг ибупрофена и 125 мг парацетамола. Ибуклин юниор отпускается по рецепту врача. Возможность комбинированного применения ибупрофена и парацетамола в педиатрической практике оценивалась в рандомизированном исследовании у 146 детей в возрасте от 6 мес. до 6 лет [9]. За 24 ч комбинация ибупрофена и парацетамола снизила продолжительность лихорадочного периода на 4,4 ч по сравнению с парацетамолом и на 2,5 ч по сравнению с ибупрофеном. Побочные эффекты при всех вариантах терапии существенно не различались. Тактика применения жаропонижающих препаратов При принятии решения о назначении антипиретиков с целью купирования лихорадки врач должен отдавать себе отчет в том, что подобная терапия в данной ситуации носит исключительно симптоматический характер (если назначение НПВП не имеет целью достижение противовоспалительного эффекта, например, при артритах различного происхождения). При легкой или умеренной лихорадке жаропонижающие препараты назначают только детям с фебрильными припадками, беременным, а также больным с сердечной и дыхательной недостаточностью или сосудистым поражением головного мозга. Необоснованное применение жаропонижающих препаратов не дает возможности проследить за динамикой температуры, а противовоспалительное действие НПВП может маскировать проявления местной инфекции, затрудняя своевременную диагностику, а также способствует ее распространению. Следует помнить о биологической целесообразности лихорадочной реакции, а также о том, что отсутствие повышения температуры при инфекции свидетельствует о вероятности иммунодефицита и является неблагоприятным прогностическим фактором. Поэтому показаниями к назначению жаропонижающих средств являются не столько высокие цифры температуры тела, сколько ее плохая переносимость и риск возможного негативного влияния высокой температуры на различные органы и системы у больных с сопутствующей патологией и факторами риска. Принятие решения о назначении жаропонижающего средства требует ответа на следующие вопросы:
При выборе препарата среди НПВП следует учитывать не только жаропонижающие свойства, но также и анальгетический эффект, поскольку болевые ощущения (головные боли, миалгии, артралгии и др.) нередко сопутствуют лихорадке. В таблице 2 представлены основные характеристики наиболее часто используемых НПВП, оцениваемые в порядке убывания того или иного свойства. Таблица 2. Сравнительная характеристика основных НПВП [10]
Большой выбор НПВП, обладающих жаропонижающими свойствами, ставит перед врачом проблему выбора препарата не только с точки зрения его антипиретического эффекта, но и минимального побочного действия. При выборе НПВП необходимо учитывать безопасность препарата, в том числе риск ульцерогенного эффекта, гепатотоксичность, цитопеническое действие, нефротоксичность, возможность взаимодействия с другими медикаментами, фармакокинетику препарата (длительность полувыведения, связь с белками, биодоступность и др.). При этом потенциальный риск развития побочных эффектов даже при кратковременном приеме препаратов может превышать их жаропонижающий эффект. Поэтому принятие решения о назначении антипиретиков должно быть взвешенным с учетом конкретной клинической ситуации, знаний особенностей фармакодинамики и фармакокинетики препаратов, имеющихся в распоряжении врача. Путь введения НПВП должен обеспечивать оптимальную терапевтическую концентрацию препарата в крови, минимизировать риск побочных эффектов со стороны ЖКТ, быть удобным для применения и комфортным для пациента. С целью жаропонижающего эффекта используется прием препаратов внутрь, внутримышечные инъекции, внутривенные вливания и введение ректальных суппозиториев. Пероральный прием НПВП является наиболее распространенным, но влечет за собой наибольший риск побочных эффектов со стороны ЖКТ (до 15%) [11]. Это зависит от продолжительности печеночной рециркуляции, определяющей длительность контакта со слизистой ЖКТ, что и приводит к гастроэнтерологической токсичности НПВП. С учетом этого при выборе перорального пути назначения НПВП предпочтение следует отдавать препаратам с коротким периодом полувыведения, быстрым всасыванием и быстрой элиминацией (ибупрофен, кетопрофен, диклофенак). Быстрая абсорбция способствует скорому наступлению жаропонижающего эффекта, а короткий период полувыведения снижает риск аккумуляции НПВП. Внутримышечное (или внутривенное) введение НПВП с целью купирования или ослабления лихорадки широко практикуется врачами из–за более быстрого достижения жаропонижающего эффекта, а также в расчете на меньший риск гастроэнтерологической токсичности. Следует отметить, что различные побочные эффекты НПВП, в том числе и со стороны желудка, обусловлены не местным воздействием препарата, а ингибицией ЦОГ–1 независимо от способов введения их больному. Вместе с тем при внутримышечном введении часто назначаемого диклофенака возможно развитие мышечных некрозов в местах инъекций, а при длительном внутримышечном введении увеличивается риск возникновения инфильтратов и абсцессов мягких тканей. Кроме того, применение инъекционных форм является экономически более затратным. Лекарственные формы НПВП в виде ректальных суппозиториев, применяемые в качестве жаропонижающих средств, имеют целый ряд преимуществ, в частности абсорбция лекарственного препарата через кровеносную и лимфатическую систему, отсутствие влияния пищи и других медикаментов на биодоступность НПВП, уменьшение риска побочных эффектов со стороны ЖКТ, особенно при патологии желудка, двенадцатиперстной кишки, высокая биодоступность, сравнимая с таковой при внутримышечном введении. Не следует назначать АСК детям при вирусных инфекциях из–за опасности развития синдрома Рейе (обычно он развивается при гриппе и ветряной оспе, реже – при энтеровирусных инфекциях). Кроме того, АСК обладает антиагрегантным и антифагоцитарным действием, поэтому лучше применять парацетамол. Он почти не угнетает циклооксигеназу в периферических тканях и поэтому не обладает противовоспалительным действием; при окислении парацетамола в ЦНС образуется мощный ингибитор циклооксигеназы, который и отвечает за жаропонижающее действие препарата. В плане быстроты начала действия и длительности жаропонижающего эффекта комбинация ибупрофена (400 мг) + парацетамола (325 мг) (Ибуклин ® ) более эффективна в сравнении с монопрепаратами [13]. Продолжительность применения жаропонижающих средств определяется главным образом клинической ситуацией. В большинстве случаев, например при ОРВИ, инфекциях ЛОР–органов, длительность назначения НПВП для купирования лихорадки не превышает нескольких дней. В то же время у больных с различными бактериальными инфекциями при сохраняющейся лихорадке на фоне неэффективной антибактериальной терапии потребность в назначении НПВП может быть более длительной. Особое место занимают так называемые лихорадки неясного генеза, причина которых нередко остается нерасшифрованной в течение длительного времени, а сохраняющаяся лихорадка требует более продолжительного использования НПВП. В подобных ситуациях важное значение приобретает эффективность жаропонижающего действия, удобство применения и главное – безопасность используемого препарата. Необходимость более длительного применения должна определяться клинической ситуацией (переносимость препарата, риск развития побочных эффектов, наличие и тяжесть сердечно–сосудистой, психоневрологической патологии и др.). Алгоритм принятия решений при назначении НПВП у больных с лихорадкой представлен на рисунке 3. Рис. 3. Алгоритм принятия решений при назначении НПВП у больных с лихорадкой [12]
источник |