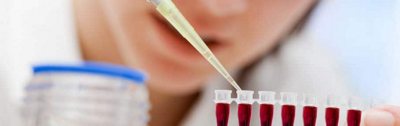
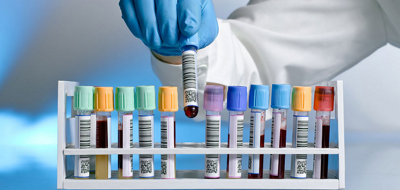
С 8-го дня заболевания в крови у больных брюшным тифом можно обнаружить агглютинины. Для постановки реакции агглютинации необходимо иметь сыворотку больного и диагностикумы – взвеси убитых бактерий брюшного тифа, паратифы А и В (реакция Видаля). У больного из вены берут в пробирку 1-2 мл крови. Для ускорения свертывания крови пробирку ставят на 30 минут в термостат. Затем свернувшуюся кровь некоторое время дают отстояться на холоде, далее осторожно отделяют сгусток обожженной петлей от стенок пробирки, после чего сыворотку отсасывают. Кровь для» получения сыворотки можно взять и посредством укола мякоти безымянного пальца. Из сыворотки с помощью физиологического раствора готовят три ряда разведений: 1:100, 1:200, 1:400, 1:600 каждое в объеме 1 мл. Затем в пробирки с разведенной сывороткой добавляют по 1-2 капле диагностикумов тифа и паратифа А и В. Для контроля реакции в конце каждого ряда помещают пробирку, в которой смешивают по 1 мл физиологического раствора и по 1-2 капле соответствующих диагностикумов. Пробирки ставят на 2 часа в термостат, после чего учитывают предварительный результат реакции. Окончательный результат отмечают на второй день после стояния пробирок в условиях комнатной температуры. Реакция считается положительной при наличии агглютинации в разведении сыворотки не менее чем 1:200.
Реакция Видаля может дать положительный результат не только у больных, но и у лиц, до того перенесших брюшной тиф («анамнестический Видаль»). Кроме того, положительная реакция иногда является результатом проведенных ранее прививок («прививочный Видаль»). «Анамнестический» и «прививочный Видаль» отличают от инфекционного следующим образом. Реакцию Видаля ставят повторно на протяжении болезни. В случае заболевания брюшным тифом с каждым днем происходит нарастание титра антител, то есть положительная реакция отмечается все в больших разведениях сыворотки. Этого не наблюдается при «анамнестическом» или «прививочном Видале».
Для этиотропного лечения используют антибиотики или другие химиотерапевтические препараты.
Специфическая профилактика тифо-паратифозного заболевания проводится убитыми и химическими вакцинами по эпидемическим показаниям, контактным лицам — экстренная фагопрофилактика сальмонеллезными поливалентными бактериофагами.
Вопросы для обсуждения
1. Классификация и общая характеристика семейства энтеробактерий.
2. Патогенез брюшного тифа и паратифа А и В.
3. Методы лабораторной диагностики брюшного тифа и паратифа А и В в
различные сроки заболевания.
4. Бактериологический метод исследования брюшного тифа и
паратифа А и В в разные стадии патогенеза заболевания.
5. Выявление бактерионосительства при брюшном тифе.
6. Серологический метод диагностики брюшного тифа и паратифа А и В.
7. Лечение и профилактика брюшного тифа и паратифа А и В.
Самостоятельная работа
Бактериологическое исследование крови брюшнотифозного больного на гемокультуру:
1. Произвести посев исследуемого материала на среду Рапопорт.
2. Изучить изменение цвета среды (помутнение; наличие пузырьков газа в поплавке).
3. Пересеять на среду Эндо.
4. Занести полученные данные в протокол.
5. Изучить различия колоний на среде Эндо. Отобрать подозрительные колонии и произвести посев для накопления чистой культуры. Описать культуральные свойства.
6. Исследовать чистую культуру по морфологическим, тинкториальным, биохимическим, антигенным свойствам. Полученные данные занести в протокол.
7. Идентифицировать чистую культуру возбудителя.
Серологическая диагностика брюшного тифа
1. Учесть результаты реакции Видаля.
2. Полученные данные занести в протокол.
Протокол бактериологического исследования
Материал для исследования:
| Этапы исследования | Ход исследования | Результаты исследования с предварительными выводами |
Дата добавления: 2015-10-19 ; просмотров: 4369 . Нарушение авторских прав
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Брюшной тиф диагностируют на основании длительной лихорадки, головной боли, нарастающей интоксикации с развитием тифозного статуса, типичных изменений языка, появления метеоризма, розеолёзной сыпи, гепатоспленомегалии и изменений периферической крови.
Лабораторная диагностика брюшного тифа основана на обнаружении возбудителя в биоматериале и специфических антител в крови больного. Решающее значение имеет обнаружение возбудителя в крови (гемокультура), моче (уринокультура), испражнениях (копрокультура), жёлчи (биликультура), а также в костном мозге, спинномозговой жидкости, розеолах, гное или экссудате.
В практической работе для ранней диагностики брюшного тифа наибольшее значение имеет гемокультура, которую следует проводить на протяжении всего лихорадочного периода. Кровь из вены в количестве 5-10 мл засевают во флакон с 50-100 мл 10-20% жёлчного бульона (лучшие результаты даёт посев в трипсин-соевый бульон). Положительные результаты гемокультуры чаще получают при посевах крови на первой неделе заболевания, когда бактериемия наиболее выражена. Со второй недели болезни брюшнотифозные палочки можно обнаружить в посевах кала, мочи и дуоденального содержимого. Наиболее высокий процент выделения палочек брюшного тифа получают при посевах костного мозга. В целом бактериологическое подтверждение диагноза брюшного тифа удаётся получить у 80-90% больных.
Серологические методы позволяют обнаружить специфические антитела в крови или антигены в биосубстрате. В практической работе чаще всего применяют реакцию Видаля и РНГА (реакция непрямой гемагглютинации) с использованием эритроцитарных О-, Н- и Vi-антигенов. Реакция Видаля основана на обнаружении специфических О- и Н-антител-агглютининов в крови больного с помощью соответствующих антигенов. Положительные результаты можно получить с 8-9 сут болезни. Реакция Видаля может быть положительной у привитых и перенёсших брюшной тиф, поэтому решающее значение имеет нарастание титра антител в динамике заболевания. Для более точного выявления специфических иммунных сдвигов в крови больного реакцию Видаля следует повторять с О- (IX и XII) и Н-монодиагностикумами для исключения перекрёстных реакций с сальмонеллами других групп.
Более специфичны и чувствительны РНГА с эритроцитарными О- и Vi-антигенами и реакция Vi-гемагглютинации. Эти реакции используют для ранней диагностики брюшного тифа. В РНГА концентрация О-антител нарастает в динамике заболевания, а титры Vi-антител существенно не меняются. Реакция Vi-гемагглютинации имеет наибольшее значение при обследовании лиц, подозрительных на брюшнотифозное носительство.
Серологические реакции на обнаружение специфических антител в крови больного следует ставить с 4-5-го дня болезни, а затем на 2-3-й нед и позднее. Диагноз брюшного тифа считают серологически подтверждённым при титре антител 1:200 и выше или при нарастании титра антител в 2-3 раза в динамике заболевания. При оценке серологических реакций важно учитывать, что нарастание титров специфических О-антител свидетельствует об остром инфекционном процессе, а наличие только Н- или Vi-антител — о перенесённом ранее брюшном тифе или бактерионосительстве.
Для серологической диагностики бактерионосительства и вакцинальных реакций предложено раздельное определение специфических антител, относящихся к IgM и IgG в ИФА. Выявление специфических брюшнотифозных IgM указывает на текущий инфекционный процесс, а изолированное обнаружение специфических антител, относящихся к классу IgG, — о вакцинальной природе антител или перенесённом ранее брюшном тифе.
Дифференциальная диагностика брюшного тифа
В практической работе брюшной тиф у детей чаще приходится дифференцировать с тифоподобной формой сальмонеллёза, паратифами, инфекционным мононуклеозом, лимфогранулематозом, иерсиниозом, малярией, а в начальном периоде — с гриппом, энтеровирусной инфекцией и острой кишечной инфекцией другой этиологии.

источник
Лабораторная диагностика брюшного тифа включает общеклинические методы исследования и специфические реакции. В результате комплексного обследования специалист сможет сделать заключение о тяжести заболевания, свойствах возбудителя (в том числе и чувствительности к антибиотикам), степени опасности пациента для окружающих (его заразности). Все необходимые исследования проводятся в начале болезни (при поступлении пациента в стационар) и перед выпиской. При необходимости анализ на брюшной тиф повторяется несколько раз.
Ваш ребенок постоянно болеет?
Неделю в садике (школе), две недели дома на больничном?
В этом виновато много факторов. От плохой экологии, до ослабления иммунитета ПРОТИВОВИРУСНЫМИ ПРЕПАРАТАМИ!
Да-да, вы не ослышались! Пичкая своего ребенка мощными синтетическими препаратами вы, порой, наносите больше вреда маленькому организму.
Чтобы в корне изменить ситуацию, необходимо не губить иммунитет, а ПОМОГАТЬ ЕМУ.
Есть еще один важный нюанс: дифференциальная диагностика брюшного тифа и паратифов возможна только на основании специфического лабораторного обследования. Ни клинические детали, ни общеклинические методы диагностики не позволяют отличить возбудитель брюшного тифа от возбудителей паратифов А, С или В. Эта информация может иметь существенное значение с точки зрения возможного заражения окружающих, а также формирования только типоспецифического иммунитета.
Где сдать анализ с целью диагностики брюшного тифа? Этот вопрос не должен беспокоить пациента, так как современные медицинские протоколы подразумевают обязательную госпитализацию больных с таким предварительным диагнозом. В крупных медицинских учреждениях (или в пределах одного города) функционирует многопрофильная лаборатория, сотрудники которой смогут сделать все необходимые специфические и неспецифические исследования для полноценной диагностики брюшного тифа и паратифов.
Универсального ответа на вопрос, через сколько дней пациент будет знать точный диагноз, не существует. Для проведения неспецифических исследований требуется только один день, результат специфических реакций придет только на 4-5 сутки или даже больше.
Выявление возбудителя брюшного тифа и паратифов является главным направлением комплексного обследования не только больного, но потенциальных носителей (здоровых людей, выделяющих возбудитель и заражающих окружающих). Результаты такого обследования заносятся в санитарную (медицинскую) книжку человека (декретированная специализированная группа), работающего в пищевой отрасли, в детских учреждениях и некоторых других предприятиях.
Для проведения различных диагностических тестов у больного (носителя) берут следующие биологические жидкости:
Необходимость взятия той или иной биологической среды пациента определяется лечащим доктором. С другой стороны, действовать нужно достаточно быстро, так как назначенные антибиотики снижают эффективность микробиологической диагностики брюшного тифа – биологические жидкости нужно брать до начала лечения.
Стандартные процедуры, такие как общеклинический анализ крови и мочи, в данном случае действительно имеют диагностическую ценность, так как выявленные изменения очень характерны.
В общем анализе крови при тифо-паратифозных заболеваниях выявляются:
- лейкоцитоз в первые 1-2 дня, который сменяется лейкопенией;
- нехарактерные для бактериальной инфекции лимфоцитоз, тромбоцитопению, анэозинофилию;
- в тяжелых случаях может наблюдаться панцитопения (угнетение функции всех кровяных ростков);
- выявление эозинофилов в период выздоровления пациента является прогностически благоприятным признаком в течении болезни.
Многим знакомы эти ситуации:
- Как только начинается сезон простуд — ваш ребенок обязательно заболевает, а потом и вся семья.
- Вроде бы покупаете дорогие препараты, но они действуют только пока их пьешь, а через неделю-две малыш заболевает по-новой.
- Вы переживаете, что иммунитет вашего ребенка слабый, очень часто болезни берут верх над здоровьем.
- Боитесь каждого чиха или покашливания.
Необходимо укреплять ИММУНИТЕТ ВАШЕГО РЕБЕНКА!
В общеклиническом анализе мочи выявляются традиционные изменения (повышение уровня лейкоцитов, эритроцитов), типичные для выраженной интоксикации.
При проведении общеклинического исследования кала (копрограмма) могут быть выявлены эритроциты, что свидетельствует о наличии незначительного кишечного кровотечения. Наряду с копрограммой принято назначать еще исследование кала на скрытую кровь, чтобы исключить диагностическую ошибку и своевременно диагностировать кровотечение.
В случае тифо-паратифозных заболеваний биохимические показатели исследуются только с целью выявления выраженных нарушений функций внутренних органов, например, при развитии специфического гепатита или пиелонефрита.
Микробиологическая диагностика брюшного тифа является основанием для постановки окончательного диагноза и дальнейших противоэпидемических действий. При обследовании особых групп населения (декретированная группа) отметка об отрицательном результате исследования крови на брюшной тиф для санкнижки является допуском к рабочему месту. Специфический анализ на брюшной тиф включает бактериологическое и серологическое исследования.
Предполагает взятие биологического материала от больного и последующий посев на специальные питательные среды (чаще всего – желчный бульон). Изучение морфологических, биохимических и многих других свойств микроорганизма позволяют со 100% точностью идентифицировать его. Кроме того, современная микробиология предусматривает такой обязательный этап как антибиотикочувствительность, без которой существенно затрудняется процесс эффективной противомикробной терапии.
Кровь на брюшной тиф лучше сдавать в первую неделю болезни. Положительный анализ крови на брюшной тиф, то есть положительная гемокультура – это абсолютное подтверждение диагноза. Обнаружение тифозной сальмонеллы в моче и каловых массах может наблюдаться в одинаковой степени у больного человека и носителя, то есть требуются другие дополнительный исследования.
Основой множества реакций, реализующих серологический метод исследования, является соединение известного антигена (брюшнотифозного) и антител, которые синтезируются в крови больного. Серологическая диагностика брюшного тифа — это реакция Видаля, реакция непрямой гемагглютинации (РНГА), при необходимости – реакция с Vi – антигеном.
Реакция Видаля – это модификация реакции агглютинации, диагностическая ценность заключается в нарастании титра антител по мере течения заболевания. Эта реакция может быть ложноположительной при других сальмонеллезах, поэтому требуется и другая серодиагностика брюшного тифа. Например, более специфична РНГА с различными антигенами. Некоторые лаборатории проводят РПГА – реакцию пассивной агглютинации антител известными антигенами.
При подозрении на брюшной тиф диагностика специфическая позволяет подтвердить или опровергнуть диагноз этого инфекционного заболевания, а также, возможно, выяснить, откуда появилась эта инфекция.
источник
Возбудителями брюшного тифа и паратифов (А, В) являются бактерии рода Salmonella, в состав которого входят два вида: Salmonella enterica с 6 подвидами (включая возбудители брюшного тифа, паратифов, сальмонеллезов – всего более 2400 сероваров) и Salmonellabongori(редко встречающиеся сальмонеллы).Возбудитель брюшного тифа обозначается как Salmonellaсеровара Typhi (Salmonella entericaspp. enterica ser. typhi, прежнее название Salmonella typhi), паратифа А — Salmonellaсеровара ParatyphiA, паратифа В — Salmonellaсеровара Paratyphi В.
Методы микробиологической диагностики брюшного тифа и паратифов представлены в схеме 9.
Выбор материала и метода микробиологической диагностики этих заболеваний зависит от стадии патогенеза. На первой неделе заболевания и в течение всего лихорадочного периода возбудитель можно выделить из крови (гемокультура), с конца второй и на третьей неделе — из мочи (уринокультура) и испражнений (копрокультура). Высокий процент высеваемости возбудителя отмечается при исследовании костного мозга (выделение миелокультуры). Удается обнаружить сальмонеллы в скарификате розеол (розеоло-культура), ликворе, содержимом двенадцатиперстной кишки, секционном материале. У реконвалесцентов исследуют испражнения и желчь (выделение биликультуры). Начиная со второй недели заболевания проводят серологическое исследование. Микроскопическое исследование материала от больного не проводится, т.к. все энтеробактерии (как патогенные, так и непатогенные, например, E.coli) по морфологическим свойствам идентичны (рис. 14).
Бактериологическое исследованиеявляется основным лабораторным методом диагностики брюшного тифа и паратифов.
Ранним и надежным методом бактериологической диагностики является выделение возбудителей из крови (гемокультура).Взятую в асептических условиях кровь (15-20 мл) засевают на 10% желчный бульон или среду Рапопорт (10% желчный бульон, 1 % маннита или 2 % глюкозы, 1 % индикатора Андреде; в среду помещен поплавок для улавливания газа) в соотношении крови и среды 1:10 для накопления сальмонелл. Посевы инкубируют при 37 0 С 18 —24 ч. При наличии сальмонелл маннит или глюкоза расщепляется с образованием кислоты и среда приобретает красный цвет; появление в поплавке газа свидетельствует о газообразовании — характерном признаке паратифозных бактерий.
Схема 9.Микробиологическая диагностика брюшного тифа и паратифов.
Рис. 14. а — кишечная палочка(E.coli ув. Х1350), б— возбудитель брюшного тифа(S.typhi, ув. Х630) в мазках из чистой культуры. Окраска по Граму. Грамотрицательные беспорядочно расположенные палочки средних размеров.
Копрокультуру выделяют путем посева фекалий на среду Плоскирева, Эндо, висмут-сульфит агар и среды накопления (селенитовую, магниевую, тетратионатную, Кауфмана, Мюллера) с последующей 18 —24-часовой инкубацией при 37 °С.
На 2-й день на средах Плоскирева, МакКонки или Эндо вырастают бесцветные (лактозоотрицательные) колонии, а на висмут-сульфит-агаре – черные. Колонии сальмонелл паратифа А окрашены взеленый цвет, так как не образуют сероводород. Из типичных колоний готовят мазок, окрашивают по Граму и после микроскопии остаток колонии пересевают на среду Ресселя или Олькеницкого. При отсутствии типичных колоний на те же среды засевают материал со среды обогащения.
На 3-й день исследования учитывают характер роста на среде Ресселя или Олькеницкого (окрашивание столбика среды Ресселя в синий цвет, среды Олькеницкого в желтый в результате ферментации глюкозы в анаэробных условиях; скошенная часть среды не изменена – отсутствие ферментации лактозы), готовят мазок для проверки чистоты выделенной культуры, выполняют пересев в среды «пестрого» ряда для изучения биохимических свойств (см. табл. 10), после чего
ставят ориентировочную, а потом развернутую РА. Ориентировочную РА ставят со смесью О-сывороток, включающей агглютинины к О-антигенам 2, 4, 7, 8, 9, 3-10. При отсутствии РА с этой смесью используют смесь монорецепторных О-сывороток к редким группам сальмонелл (антитела к антигенам 11, 13, 15, 19, 23 и т.д.) При получении положительных результатов культуру испытывают отдельно с каждой из О-сывороток, входящих в состав смеси. После этого культуру агглютинируют с Н-сыворотками 1 фазы (a, b, i, c, d, g, m) а потом 2 фазы (1,2; 1,5), устанавливая антигенную формулу выделенной сальмонеллы в соответствии со схемой Кауфмана-Уайта (таблица 9). Эта схема разработана на основании изучения у сальмонелл О и Н антигенов и применяется с целью антигенной идентификации патогенных сальмонелл.
Таблица 9. Антигенная структура сальмонелл (сокращенная схема Кауфмана-Уайта)
| Группа | Серовар | О-антиген | Н-антиген | |
| Фаза 1 | Фаза 2 | |||
| А | Paratyphi A | 1, 2, 12 | a | — |
| B | Paratyphi B Typhi murium | 1, 4, 5, 12 1, 4, 5, 12 | b i | 1, 2 1, 2 |
| C | Paratyphi C Cholerae suis | 6, 7, Vi 6, 7 | c c | 1, 5 1, 5 |
| D | Typhi Enteritidis | 9, 12, Vi 1, 9, 12. | d g, m | — — |
На 4-й день от начала исследования учитывают изменения сред «пестрого» ряда (см. табл. 10), результаты развернутой РА и выдают ответ. Выделенные культуры подвергают фаготипированию, что позволяет установить источник и пути заражения.
Мочу, дуоденальное содержимое, соскоб розеол, секционный материал с целью выделения тифо-паратифозных бактерий засевают на плотные среды (Эндо, Мак-Конки и т.п. в чашке Петри), а также в среды накопления. При наличии характерного роста идентификация проводится по вышеописанной схеме.
Таблица 10. Биохимические свойства возбудителей брюшного тифа и паратифов
| Биовар S.enterica | Ферментация | Продукция | ||||||
| Лакто- Зы | Глю- козы | Маль- тозы | Саха- розы | Ман- нита | Н2S | NH3 | индо- ла | |
| Typhi | — | К | К | — | К | + | — | — |
| Paratyphi A | — | КГ | КГ | — | КГ | — | — | — |
| Paratyphi В | — | КГ | КГ | — | КГ | + | + | — |
Обозначения: (+) — наличие свойства, (-) — отсутствие свойства, К – образование кислоты, КГ – образование кислоты и газа.
Аналогично проводится исследование испражнений упереболевших брюшным тифом и паратифом лиц, а также у работников детских учреждений, питания и водоснабжения с целью выявления бактерионосителей.
Серологическое исследование.Для серологической диагностики брюшного тифа и паратифов ставят реакцию Видаля (развернутая РА) с целью определения соответствующих антител в крови больного. Антитела к возбудителям брюшного тифа, паратифов А и В обнаруживаются в сыворотке крови больных с 8— 10-го дня заболевания. Исследуемую сыворотку крови разводят двукратно в 6 параллельных рядах пробирок от 1:100 до 1: 1600 в объеме 1 мл, куда вносят по 2 капли ОН— и О- брюшнотифозного, паратифозного Аи паратифозного В диагностикумов. О-диагностикумы получают кипячением или обработкой спиртом взвеси соответствующих культур, ОН—диагностикумы — обработкой формалином. Для контроля антигена диагностикумы вносятся в той же дозе в 1 мл физиологического раствора, а для контроля сыворотки используют сыворотку в разведении 1:100 без добавления диагностикумов.
О-антитела имеют диагностическое значение, они появляются в крови на второй неделе заболевания и исчезают к его концу, а Н-агглютинины нарастают к концу заболевания. и диагностической ценности не имеют. Н-антитела могут обнаруживаться также у переболевших и вакцинированных. Ряд брюшнотифозных вакцин вызывает также выработку Vi – и О антител. Диагностический титр О-антител в реакции Видаля у неиммунизированных лиц 1 :100, а при отсутствии типичной клинической картины — 1 :200. Однако титр антител у больных может быть ниже диагностического в связи с ранним назначением антибиотиков или наличием у больного вторичного иммунодефицита. Таким образом, отрицательная реакция Видаля не исключает тифопаратифозное заболевание. С другой стороны, повышенные титры О-антител могут быть обусловлены прививками. Поэтому при подозрении на брюшной тиф или паратифы целесообразно исследовать сыворотку крови как можно раньше (до появления антител), а затем в динамике (с интервалом 7-12 дней) для выявления нарастания титра антител более чем в 4 раза. Если сыворотка крови больного агглютинирует одновременно два или три вида диагностикумов, учитывают титр агглютинации: специфическая агглютинация происходит обычно с более высокими, а групповая — с более низкими разведениями сыворотки.
Более чувствительны РНГА с эритроцитарными групповыми (А, В, С, Д, Е)и монорецепторными диагностикумами, а также ИФА, которые ставят с парными сыворотками в динамике заболевания.
Vi-антитела чаще обнаруживаются у бактерионосителей сальмонелл брюшного тифа, т.к. Vi-антиген способствует длительной персистенции возбудителя в организме. При обследовании лиц, подозрительных на носительство брюшнотифозных палочек, применяется РНГА с эритроцитарным Vi-диагностикумом для определения соответствующих антител и их принадлежности к классу IgG.
Не нашли то, что искали? Воспользуйтесь поиском:
источник
Цель. Провести бактериологический и серологический методы диагностики дизентерии. Оценить их диагностическую ценность. Ознакомиться с ИБМП для лабораторной диагностики дизентерии.
Задача. В инфекционной больнице в течение 6 дней лечиться больной с диагнозом: «Острая дизентерия». Жалобы при поступлении на высокую температуру, частый жидкий стул со слизью и кровью, боли в животе. Для подтверждения диагноза проведено бактериологическое исследование парными сыворотками на 3-й и 6-й дни болезни. Учтите результаты бактериологического и серологические исследования.
Бактериологический метод диагностики: выделение и идентификация чистой культуры.
1-й этап. Посев нативного материала. Или взятого с помощью петли из прямой кишки. Материал засевают на среду Плокирева или Левина или висмут-сульфит агар и помещается в термостат при температуре 37°С и инкубируется в течение 24-48 часов, петлю заливаем средой накопления ( селенитовый или желчный бульоны).
2-й этап. Выделение чистой культуры. Через 24 часа инкубации в термостате с помощью петли отвить типичную для дизентерийных бактерий бесцветную колонию на скошенный МПА или среду Олькеницкого для выделения чистой культуры и поместить в термостат на сутки. Из сред накопления произвести высев на среды Плоскирева, Левина или висмут-сульфит агар.
3-й этап. Идентификация выделенной культуры: а) морфология; б) биохимические свойства; в) антигенная структура;
4-й этап: учесть чувствительность выделенной культуры к антибиотикам и бактериофагу.
Серологический метод диагностики.
Для серологического исследования при постановке РПГА берется: а) сыворотка больного; б) эритроцитарный диагностикум; в) физиологический раствор.
| Исследуемый материал | Среда для посева | Характеристика колоний по цвету | Идентификация цистой культуры | |
| Морфология | Биохимические свойства | агглютинации | Чувствительность к антибиотикам и бактериофагу | |
| лактоза | глюкоза | маннит | С сывороткой Флекснера | С сывороткой зонне и ньюкастл |
| Срок исследования | Разведение сыворотки больного | ||
| 1/100 | 1/200 | 1/400 | Контроль |
| 3-й день 6-й день |
Цель. Изучить специфические препараты для диагностики дизентерии.
Используя аннотации к диагностическим препаратам по теме «микробиология дизентерии», изучите препараты, применяемые при диагностике этой инфекции.
| Название препарата | Состав | К какой группе диагностических препаратов относится | Практическое использование (метод диагностики) |
Аннотация лечебно-профилактических и диагностическим препаратов по теме «Микробиология дизентерии»
Бактериофаг дизентерийный поливалентный жидкий или в таблетках – стерильный фильтрат фаголизатов возбудителей бактериальной дизентерии: шигелл Флекснера 1,2,3,4,6- типов и шигелл Зонне
Интести-бактериофаг жидки – смесь стерильных фильтратов фаголизатов шигелл Флекснера 1,2,3,4,6-го серовариантов, шигелл Зоне; сальмонелл паратифа А, паратифа В, тифимуриум, инфантис, холерасуис, ораниенбург, энтеритидис; наиболее распространенных серовариантов кишечной палочки, протеус вульгарис и мирабилис, энтерококков, стафилококков, псевдомонас аеругиноза. Применяется для лечения кишечных инфекций.
Адсорбированные агглютинирующие сыворотки для идентификации шигелл. Получены из крови животных, иммунизированных определенными видами шигелл. Используются в бактериологическом методе для идентификации чистых культур.
Дизентерийный диагностикум. Состоит из взвеси убитых бактерий Флекснера и Зоне. Используется в серологическом методе.
Дизентерийный эритроцитарный диагностикум состоит из взвеси эритроцитов, нагруженных антигенами Флекснера, Зоне и др. используются для постановки РПГА в серологическом методе.
Цель. Изучить этиологию, эпидемиологию и патогенез брюшного тифа, паратифов и ПТИ. Овладеть основными методами лабораторной диагностики брюшного тифа, паратифов, и оценки результатов исследований. Научиться практически решать вопросы по специфической профилактике брюшного тифа.
По последней классификации отмечают два вида сальмонелл: 1)Salmonella bogori содержит 10 очень редких сероваров; 2)Salmonella choleraesuis включает 2500 сероваров. Диагностическим лабораториям рекомендовано внутри рода Salmonella использовать названия сероваров, например: Salmonella typhi или Salmonella typhimurium. Природный резервуар сальмонелл – человек, животные и птицы. Основной путь передачи – водный и пищевой. Сальмонеллы высокоустойчивы в окружающей среде: в питьевой воде – до 120 суток, в комнатной пыли – до 560 суток, в замороженном мясе – до 13 месяцев. Сальмонеллы имеют сложную антигеннюую структуру: в соответствии с содержанием тех или иных О-АГ сальмонеллы разделяют на серологические группы, обозначаемые арабскими цифрами. По Н-АГ микроорганизмы делят на серовары, Vi-АГ – фактор вирулентности. При идентификации сальмонелл принимают во внимание 3 антигена: О, Н и Vi. Этот принцип положен в основу диагностической антигенной схемы Кауфмана-Уайта. Типичную клиническую картину брюшного тифа и характерные патологоанатомические изменения вызывают как брюшнотифозные бактерии, так и бактерии паратифа А и В. Остальные сальмонеллы вызывают заболевания с синдромом гастроэнтероколита.
Для лабораторной диагностики сальмонеллезов используют оба принципа:
1) обнаружение возбудителя – метод бактериологический;
2) обнаружение специфических изменений – метод серологический;
Самостоятельная практическая работа
Цель. Провести бактериологический и серологический методы диагностики брюшного тифа, паратифов.
Задача. В инфекционную больницу поступила женщина на 6-й день болезни. для подтверждения диагноза был сделан посев крови, мочи, испражнений больной для выделения чистой культуры. Поставлена серологическая реакция с сывороткой больной. Учтите результаты исследований, оформите протокол.
Бактериологический метод диагностики
Выделение и идентификация чистой культуры.
1-й этап. Посев материала. Материал для исследования в зависимости от условий задачи может быть различным: кровь, испражнения, моча. Кровь больного берется на первой неделе болезни в количестве 5-10 мл стерильно из локтевой вены и засевается у постели больного во флаконы с 50-100 мл 10-20% желчного бульона. Испражнения и мочу засевают на среду Плоскирева, висмут-сульфит агар и залить средами обогащения: магниевую среду и селенитовый бульон.
2-й этап. Выделение чистой культуры. Через сутки делается посев петлей с желчного бульона на среды Плоскирева и висмут-сульфит агар для выделения чистой культуры. Из чашки со средой Плоскирева петлей откалывают типичную для сальмонеллезных палочек бесцветную колонию на трехсахарный (Олькеницкого, Клиглера) агар. Посевы помещают в термостат при температуре 37°С на сутки.
3-й этап идентификация чистой культуры:
а) морфологические свойства;
Положительная реакция агглютинации с одной из О-сывороток позволит определить групповую принадлежность выделенной культуры сальмонелл по таблице Кауфмана, после чего с соответствующими данной группе Н-монорецепторными сыворотками определяется серовар культуры.
Исследование выделенной культуры заканчивается определением фаготипа микроорганизмов. С этой целью выделенную культуру сеют на питательную среду и наносят петлей на засеянную поверхность брюшнотифозные фаги различных типов. Лизис культуры вызывается определенным фагом, что соответствует фаготипу культуры.
Серологический метод диагностики брюшного тифа. РНГА.
Ставиться по стандартной схеме в плашках или пробирках.
Выделение чистой культуры и её идентификация
| Исследуемый материал | Среда для посева | Характеристика колоний по цвету | Идентификация чистой культуры | |
| Морфология | Подвижность | Биохимические свойства | Антигенные свойства | Вид культуры и фаготип |
| Лактоза | Глюкоза | Сероводород | О-сыворотки | Н-сыворотки |
| Диагностикум | Разведение сыворотки | |||
| 1/100 | 1/200 | 1/400 | 1/800 | К |
| Брюшнотифозный Паратифозный А S.typhimirium |
Цель. Провести исследования для диагностики брюшнотифозного бактерионосительства.
Задача. Больной перенес брюшной тиф. Перед выпиской из стационара он был обследован для выявления бактерионосительства: возбудитель обнаружен в испражнениях, из мочи и желчи микроорганизмы не выделены. Проведен серологический метод диагностики: поставлена реакция Vi-гемагглютинации. Учтите результат. Оформите протокол.
Для серологического метода использованы ингредиенты: сыворотка больного, эритроцитарный Vi-диагностикум, физиологический раствор.
| Диагностикум | Разведение сыворотки | ||
| 1/20 | 1/40 | 1/80 | К |
| Vi-эритроци тарный |
Цель. Изучить специфические препараты для диагностики сальмонеллезных инфекций.
Из аннотации по теме «Микробиология брюшного тифа » внести в протокол перечень специфических диагностических препаратов.
| Название препарата | Состав | К какой группе диагностических препаратов относится | Практическое использование | Максимальное и минимальное разведение сывороток |
Аннотация К лечебно-профилактическим и диагностическим препаратам по теме «Микробиология брюшного тифа».
Вакцина брюшнотифозная спиртовая, обогащенная Vi-антигеном.
Вакцина брюшнотифозная Vi-полисахаридная.
Интести бактериофаг жидкий.
Люминисцирующаю брюшнотифозная сыворотка.
Адсорбированные агглютинирующие сыворотки.
Эритроцитарный сальмонеллезный диагностикум
Тема:Микробиологическая диагностика пищевых токсикоинфекций.
Цель. Изучить этиологию, эпидемиологию и патогенез пищевых токсикоинфекций (далее ПТИ). Овладеть основными методами лабораторной диагностики ПТИ и оценки результатов исследований.
Теоретическая справка. К пищевым отравлениям микробной природы относятся острые системные заболевания, возникающие в результате употребления пищевых продуктов, массивно обсемененных некоторыми микроорганизмами или зараженных микробными экзотоксинами. Это определение позволило подразделить все пищевые отравления, связанные с микроорганизмами, на пищевые токсикоинфекции и интоксикации. Первые вызывают преимущественно грамотрицательные бактерии, среди которых энтеробактерии занимают первое место. При этом название токсикоинфекции определяется поступлением в кровь бактериального эндотоксина (ЛПС), освобождающегося в большом количестве после массивного разрушения бактерий. Пищевые продукты, содержащие экзотоксины бактерий, вызывают пищевые интоксикации, а токсины грибов микотоксикозы.
Наиболее распространенными возбудителями пищевых токсикоинфекций являются сальмонеллы, реже E.coli, P.vulgaris, P.morganii, Bacillus cereus.
Патогенез и клиническая картина ПТИ определяются проникновением в желудочно-кишечный тракт большого количества соответствующих бактерий с зараженными пищевыми продуктами (мясо, рыба), подвергшимися недостаточной термической обработке. При этом сохранившие жизнеспособность бактериальные клетки быстро размножаются в благоприятных условиях. Одновременное проникновение в кишечник человека массивной дозы возбудителя, его последующее размножение и разрушение бактериальных клеток приводит к освобождению большого количества эндотоксина, оказывающего воздействие на интрамуральный нейрорецепторный аппарат тонкой кишки, периферические сосуды брюшной полости. Это сопровождается нейродистрофическими изменениями в стенке тонкой кишки и поражением клеток других органов. При ПТИ освобождение желудочно-кишечного тракта от возбудителей во многих случаях происходит достаточно быстро, иногда через несколько часов после начала заболевания. Бактериемия при этих заболеваниях как правило не наступает..
Лабораторная диагностика проводится бактериологическим методом, Материалом для исследования являются испражнения, рвотные массы, промывные воды желудка больных людей и остатки пищи и продуктов, из которых лона была приготовлена.
Пищевые интоксикации бактериальной природы возникают также при попадании с пищей в желудочно-кишечный тракт бактериальных токсинов, из которых наибольшую опасность представляют энтеротоксины Staphylococcus aureus, Clostridium perfringens и особенно ботулонейротоксин C. Botulinum. Для возникновения пищевой интоксикации не обязательно присутствие в продукте живых возбудителей.
Микробиологическая диагностика пищевых отравлений проводится методом выявления токсинов, а также выделения чистых культур возбудителя – продуцентов токсинов в остатках пищи и в материале, взятом от больного.
Бактериологическая диагностика токсикоинфекций, вызванных сальмонеллами, эшерихиями и протеем.
Материалом для исследования являются испражнения, рвотные массы, промывные воды желудка, остатки пищевых продуктов – возможные факторы передачи инфекции.
1этап Производится посев материала на дифференциально-диагностические среды (Эндо, Плоскирева, Левина, висмут-сульфит агар) для выделения чистой культуры сальмонелл или эшерихий, а также в конденсационную воду в пробирке со скошенным агаром.
2 этап. После инкубации посевов при температуре 37°С в течение 20 – 24 ч. отмечают цвет колоний на чашках с дифференциальной средой и наличие «ползучего» роста, характерного для протея, в пробирке со скошенным агаром. Подозрительные колонии пересевают на трехсахарный агар для получения чистой культуры и одновременно ставят с ними реакцию агглютинации на стекле, используя смесь диагностических сывороток к разным сероварам сальмонелл.
3 этап. С выросшей культуры на трехсахарном агаре делают мазок и определяют чистоту выделенной культуры, ставят реакции агглютинации с групповыми О сыворотками и монорецепторными Н- сыворотками и делают посев на среды «пестрого» ряда. При выделении одного и того же серовара сальмонелл из организма больного и пищевого продукта делают окончательное заключение об этиологии пищевой токсикоинфекции- факторе передачи инфекции.
На условно-патогенную микрофлоруфлору
2этап При наличии «ползучего» роста на скошенном питательном агаре из конденсационной воды петлей берут материал для приготовления препарата «висячая» капля с целью установления подвижности и для мазка, который окрашивают по Граму и микроскопируют.
3 этап Производят пересев на трехсахарный агар (Клиглера, Олькеницкого) и выделяют чистую культуру протея,
4 этап определяют биохимические и другие признаки и устанавливают вид: P. vulgaris, P. mirabilis.
Оценка роли условно-патогенных микроорганизмов в этиологии пищевых токсикоинфекций должна быть строго аргументирована:
а) бактериологическим, серологическим, эпидемиологическим и клиническим исключением сальмонеллезов, дизентерии, холеры;
б) выделением идентичных штаммов условно-патогенных бактерий из рвотных масс, промывных вод желудка, испражнений, продуктов;
в) нарастанием титров реакции агглютинации с аутоштаммами возбудителей в динамике заболевания.
Лабораторная диагностика пищевых интоксикаций бактериальной природы
1. Материалом для определения стафилококкового энтеротоксина являются рвотные массы, промывные воды желудка больных, остатки пищи (чаще кремы, сметана, мороженое, а также мясные продукты, в которых хорошо размножаются стафилококки).
С целью выделения чистой культуры стафилококка исследуемые материалы, которые могут содержать жизнеспособные бактерии, засевают в чашки с ЖСА.
Для эпидемиологического анализа массовых стафилококковых интоксикаций проводят фаготипирование выделенных культур с помощью набора стафилококковых фагов.
2. Материалом для выявления энтеротоксина клостридий С. perfringens являются мясные, рыбные консервы и другие продукты, из которых экстрагируют токсин изотоническим раствором хлорида натрия. Экстракт центрифугируют и надосадочную жидкость вводят внутрибрюшинно белым мышам или внутрикожном морским свинкам. Гибель животных в течение первых 3-4 дней появление некроза на месте внутрикожных инъекций свидетельствует о наличии токсина. Для его идентификации ставят реакцию нейтрализации с антитоксическими сыворотками С. perfringens.
Выделение чистой культуры С. perfringens и С. botulinum производят, используя методы выделения анаэробных бактерий.
3. Материалом для выявления ботулотоксина служат сыворотка крови, моча, испражнения, промывные воды желудка больного, остатки пищи или подозреваемые продукты (колбасы, мясные, рыбные, фруктовые, овощные консервы и др.). Для обнаружения ботулотоксина в сыворотке крови больного ставят реакцию нейтрализации таксина антитоскической сывороткой в биопробе на белых мышах. (с , моновалентными антитоксическими противоботулиническими сыворотками типов А, В, Е. F,C В качестве контроля берут нормальную сыворотку крови. При нейтрализации токсина гомологичной антитоксической сывороткой мыши остаются живыми.
Дата добавления: 2013-12-13 ; Просмотров: 2658 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
источник
Тема: Серодиагностика брюшного тифа, паратифов А и В. Сальмонеллы – возбудители острых гастроэнтеритов.
Цель: Освоение методов микробиологической диагностики сальмонеллезов и серологической диагностики брюшного тифа и паратифов А и В.
Модуль 2. Специальная, клиническая и экологическая микробиология.
Содержательный модуль 10. Патогенные прокариоты и эукариоты.
Тема занятия 25. Серодиагностика брюшного тифа, паратифов А и В. Сальмонеллы – возбудители острых гастроэнтеритов.
Сальмонеллез – острая кишечная инфекция. характеризующаяся преимущественным поражением желедочно-кишечного тракта, возбудителями которой являются многочисленные бактерии рода Salmonella (кроме S. typhi, S, paratyphi A, S. schottmuelleri).
Таксономическое положение и свойства. см. в методичке 26.
Морфология и тинкториальные свойства.
Эпидемиология. Основной источник заболевания – животные, преимущественно домашние и птицы. Реже источниками заболевания являются люди – больные и носители. Механизм заражения – фекально-оральный. Основной путь передачи инфекции – пищевой. Факторами передачи могут быть не только мясо животных и птиц, инфицированное при жизни животного либо при его обработке, но и яйца. Наиболее восприимчивы к заболеванию люди со сниженным иммунным статусом (в том числе грудные дети) и больные, получающие антибиотики. Подъем заболеваемости наблюдается летом.
Патогенез. Сальмонеллы проникают в организм через рот, достигают тонкого кишечника, где и развертывается патологический процесс. Бактерии благодаря факторам адгезии прикрепляются к слизистой оболочке, проникают в ее глубокие слои, где захватываются макрофагами. Сальмонеллы размножаются и погибают с освобождением эндотоксина, который, помимо общей интоксикации, вызывает диарею и нарушение вводно-солевого обмена. Находящаяся в нормальном состоянии микрофлора кишечника в значительной мере препятствует накоплению сальмонелл. В некоторых случаях (при снижении иммунного статуса и высокой вирулентности возбудителя) возможно развитие бактериемии и поражение костей, суставов, мозговых оболочек и других органов.
Клиническая картина. Инкубационный период равен в среднем 12-24 часа. Заболевание характеризуется повышением температуры, тошнотой, рвотой, поносом, болью в животе. Как правило, продолжительность болезни составляет 7 дней. но в некоторых случаях наблюдается молниеносная токсическая форма, приводящая к смерти больного.
Иммунитет после перенесенного заболевания сохраняется менее года.
Микробиологическая диагностика. Основной материал для исследования — рвотные массы, испражнения, промывные воды желудка. Применяют бактериологический и серологический (РА, РПГА) методы диагностики.
Лечение сальмонеллеза заключается в промывании желудка, диете, введении жидкостей для нормализации вводно-солевого обмена. Антибиотики при формах средней тяжести и легких не назначают, т.к. их применение приводит к дисбактериозу и в результате более длительному течению болезни; кроме того, очень велико число антибиотикорезистентных сальмонелл.
Профилактика неспецифическая — санитарно-гигиенические мероприятия, заключающиеся, в частности, в правильной кулинарной обработке мяса и яиц.
Серологическая диагностика брюшного тифа и паратифов А и В.
Для постановки диагноза применяется реакция агглютинации Видаля, основанная на обнаружении в сыворотке крови людей агглютининов, которые появляются в конце 1-й — начале 2-й недели заболевания. Особенности реакции заключаются в том, что реакция ставится одновременно с 4 разными диагностикумами (антигенами): ОН-диагностикум брюшного тифа, О-диагностикум брюшного тифа, ОН-диагностикум паратифа А и ОН-диагностикум паратифа В. Брюшнотифозные монодиагностикумы применяются для установления стадии болезни, т.к. содержание О- и Н-антител в разные ее периоды неодинаково. О-антитела накапливаются в разгвр заболевания и исчезают к моменту выздоровления. Н-антитела появляются к концу заболевания и сохраняются у переболевших в течение длительного времени.
Это помогает дифференцировать острую стадию заболевания и «прививочную» или анамнестическую реакции.
У больных брюшным тифом в сыворотке крови определяются О- и Н-антитела, а в сыворотке крови людей, перенесших брюшной тиф или вакцинированных против него, сохраняются только Н-антитела.
Для серологического исследования реконвалесцентов и выявления бактерионосителей широко используют реакцию пассивной Vi-гемагглютинации (РПГА), с помощью которой определяют Vi-антитела в сыворотке крови людей, появляющиеся только к концу заболевания, но постоянно обнаруживающиеся у носителей брюшного тифа.
Ознакомиться с биологическими свойствами и классификацией представителей семейства Salmonella.
Описывать патогенез сальмонеллезов.
Изучить методы микробиологической диагностики сальмонеллезов.
Ознакомиться с методами серологической реакции брюшного тифа, паратифов А и В.
Ознакомиться с методами профилактики и специфической терапии брюшного тифа, паратифов А и В.
Трактовать результаты бактериологического и серологического исследования.
Проводить дифференциацию сальмонелл – возбудителей сальмонеллезов.
Забирать материал для исследования от больных сальмонеллезами.
Выделять чистые культуры сальмонелл.
Трактовать результаты бактериологического и серологического исследования.
Сальмонеллы – возбудители пищевых токсикоинфекций.
Антигенная структура, факторы патогенности.
Патогенез и иммуногенез заболеваний. Бактерионосительство.
Методы микробиологической диагностики сальмонеллезов.
Специфическая профилактика и лечение сальмонеллезов.
Практические задания, выполняемые на занятии:
Выделение чистой культуры S. typhi :
Изучение посевов «фекалий» больного брюшным тифом на среде Ресселя.
Проверка чистоты культур: приготовление мазков, окраска по Грамму, микроскопия и зарисовывание.
Пересев чистой культуры на среду Гиса и МПБ для выявления индола и сероводорода.
Постановка реакции агглютинации на стекле с диагностическими сыворотками для идентификации выделенной чистой культуры.
Микроскопия демонстрационных микропрепаратов чистых культур S. typhimurium, S. choleraesuis, S. enteritidis.
Зарисовывание демонстрационных микропрепаратов в протокол.
Пяткин К.Д., Кривошеин Ю.С. Микробиология с вирусологией и иммунологией.– Киев: Высшая школа, 1992.- 431с.
Воробьев А.В., Быков А.С., Пашков Е.П., Рыбакова А.М. Микробиология.- М.: Медицина, 1998.- 336с.
Медицинская микробиология /Под редакцией В.П. Покровского.– М.: ГЕОТАР-МЕД, 2001.– 768с.
Коротяев А.И., Бабичев С.А. Медицинская микробиология, иммунология и вирусология /Учебник для медицинских ВУЗов, С-Пб.: «Специальная литература», 1998.- 592с.
Тимаков В.Д., Левашев В.С., Борисов Л.Б. Микробиология /Учебник.- 2-е изд., перераб. и доп.– М.: Медицина, 1983.- 512с.
Титов М.В. Инфекционные болезни.- К., 1995.– 321с.
Шувалова Е.П. Инфекционные болезни.– М.: Медицина, 1990.- 559с.
Краткие методические указания для работы на практическом занятии.
В начале занятия проводится проверка уровня подготовки студентов к занятию.
Самостоятельная работа состоит из изучения методов микробиологической диагностики сальмонеллезов и серологической диагностики брюшного тифа, паратифов А и В. Далее студенты знакомятся с правилами забора материала от больных сальмонеллезами для бактериологического и серологического исследования. Потом продолжают выделение чистой культуры S. typhi :
Изучение посевов «фекалий» больного брюшным тифом на среде Ресселя.
Проверка чистоты культур: приготовление мазков, окраска по Грамму, микроскопия и зарисовывание.
Пересев чистой культуры на среду Гиса и МПБ для выявления индола и сероводорода.
Постановка реакции агглютинации на стекле с диагностическими сыворотками для идентификации выделенной чистой культуры.
В состав самостоятельной работы входит также микроскопия демонстрационных микропрепаратов чистых культур S. typhimurium, S. choleraesuis, S. enteritidis и зарисовывают их в протокол.
В конце занятия проводится оформление протокола, тестовый контроль и анализ результатов самостоятельной работы каждого студента.
источник
Реакция Видаля. Со второй недели заболевания в крови больных накапливаются антитела против возбудителя инфекции. Для их выявления исследуют сыворотку крови больного в реакции агглютинации. В качестве антигена используют убитые культуры сальмонелл — диагностикумы.
Для постановки реакции Видаля используют сыворотку больного, набор диагностикумов, изотонический раствор натрия хлорида.
Кровь (2-3 мл) из мякоти пальца или локтевой вены собирают в стерильную пробирку и доставляют в лабораторию. В лаборатории пробирку ставят в термостат на 20-30 мин для образования сгустка, затем пастеровской пипеткой обводят сгусток, чтобы отделить от стенки пробирки, и ставят на 30-40 мин на холод. Отделившуюся сыворотку отсасывают и используют для постановки реакции агглютинации с диагностикумами из сальмонелл тифа и паратифов. Для получения сыворотки кровь можно отцентрифугировать.
При возникновении инфекционного процесса — брюшного тифа или паратифов — в организме вырабатываются О- и Н-антитела к одноименным антигенам возбудителя.
О-антитела появляются первыми и исчезают довольно быстро. Н-антитела сохраняются долго. То же самое происходит и при вакцинации, поэтому положительная реакция Видаля с О- и Н-антигенами свидетельствует о наличии заболевания, а реакция только с Н-антигенами может быть и у переболевших (анамнестическая реакция), и у привитых (прививочная). Исходя из этого, реакцию Видаля ставят раздельно с О- и Н-антигенами (диагностикумы).
Так как клинически брюшной тиф и паратифы А и В сходны, то для выявления природы заболевания сыворотку больного испытывают одновременно с диагностикумами из сальмонелл тифа и паратифа А и В.
Реакцию Видаля широко используют, так как она проста и не требует специальных условий.
Поставить реакцию можно двумя способами: капельным и объемным (см. главу 12). В практике чаще используют объемный метод. При постановке линейной реакции агглютинации количество рядов должно соответствовать количеству антигенов (диагностикумы). Возбудителем заболевания считают микроорганизм, диагностикум из которого агглютинировался сывороткой больного. Иногда отмечают групповую агглютинацию, так как возбудители тифа и паратифов обладают общими групповыми антигенами. В этом случае положительным считают результат реакции в ряду, в котором агглютинацию отмечают в большем разведении сыворотки (табл. 36).
Таблица 36. Возможный результат реакции агглютинации
Примечание. В практике реакцию Видаля ставят с четырьмя диагностикумами: брюшного тифа «О» и «Н», а паратифов А и В — с диагностикумами «ОН».
Если агглютинация возникает только в небольших разведениях сыворотки — 1:100, 1:200, то для отличия реакции при заболевании от прививочной или анамнестической прибегают к повторной постановке реакции агглютинации через 5-7 дней. У больного титр антител повышается, а у привитого или переболевшего не изменяется. Таким образом, нарастание титра антител в сыворотке крови служит показателем заболевания.
В ответ на внедрение в организм возбудителей брюшного тифа, обладающих Vi-антигеном, в крови больного появляются Vi-агглютинины. Их определяют со 2-й недели болезни, но титр их обычно не превышает 1:10. Обнаружение Vi-антител связывают с наличием в организме возбудителей брюшного тифа, поэтому определение этих антител имеет большое эпидемиологическое значение, так как позволяет выявить бактерионосителей.
Реакция Vi-гемагглютинации. Это наиболее чувствительная реакция для выявления антител.
Принцип реакции заключается в том, что эритроциты человека (I группы) или барана после специальной обработки могут адсорбировать на своей поверхности Vi-антиген и приобретают при этом способность агглютиниповаться соответствующими Vi-антителами.
Эритроциты с адсорбированными на поверхности антигенами называют эритроцитарными диагностикумами.
Для постановки реакции Vi-гемагглютинации берут:
1) сыворотку крови больного (1-2 мл); 2) эритроцитарный сальмонеллезный Vi-диагностикум; З) Vi-сыворотку; 4) О-сыворотку; 5) изотонический раствор натрия хлорида.
Реакцию ставят в агглютинационных пробирках или в пластмассовых пластинах с лунками.
Кровь у больного берут так же, как для реакции Видаля. Получают сыворотку. Из сыворотки готовят двукратные серийные разведения, начиная с 1:10 до 1:160.
По 0,5 мл каждого разведения вносят в лунку и прибавляют по 0,25 мл эритроцитарного диагностикума. Реакцию ставят в объеме 0,75 мл.
Контролем служат: 1) стандартная агглютинирующая монорецепторная сыворотка + диагностикум — реакция должна быть положительной до титра сыворотки; 2) диагностикум в изотоническом растворе натрия хлорида (контроль) — реакция должна быть отрицательной.
Содержимое лунок тщательно перемешивают, ставят в термостат на 2 ч и оставляют при комнатной температуре до следующего дня (на 18-24 ч).
Учет начинают с контроля. Реакцию оценивают в зависимости от степени агглютинации диагностикума.
Результаты учитывают по четырехкрестной системе:
++++ эритроциты полностью агглютинированы — осадок на дне лунки в виде «зонтика»;
+++ «зонтик» меньше, не все эритроциты агглютинировались;
++ «зонтик» маленький, на дне лунки имеется осадок из неагглютинированных эритроцитов;
— реакция отрицательная; эритроциты не агглютинировались и осели на дно лунки в виде пуговки.
1. В какой период заболевания ставят реакцию Видаля?
2. Какие ингредиенты необходимы для постановки реакции Видаля?
3. С какими диагностикумами ставят реакцию Видаля?
4. Какая из серологических реакций является самой чувствительной при диагностике тифопаратифозных инфекций?
5. Каким диагностикумом пользуются при постановке реакции Vi-гемагглютинации?
6. Какой сывороткой определяют наличие Vi-антигена у исследуемой культуры?
7. Какое значение имеет определение Vi-фаготипа?
Возьмите у преподавателя О- и Н-диагностикумы из сальмонелл тифа, паратифа А и паратифа В и сыворотку больного. Поставьте реакцию Видаля.
Питательные среды
Среды ЭМС, Плоскирева, висмут-сульфитный агар выпускаются медицинской промышленностью в виде сухого порошка. Их готовят согласно указаниям на этикетке: отвешивают определенное количество порошка, наливают соответствующее количество воды, кипятят и разливают в стерильные чашки Петри.
Среда Рассела. В 950 мл дистиллированной воды добавляют 40 г сухой питательной среды и прибавляют 5 г питательного агара. Нагревают до кипения и растворения порошков. В 50 мл дистиллированной воды растворяют 1 г х. ч. глюкозы и добавляют к приготовленной смеси. Среду разливают в стерильные пробирки по 5-7 мл, стерилизуют текучим паром (2 дня по 2 мин) и скашивают так, чтобы оставался столбик. Среду Рассела с маннитом и сахарозой готовят так же.
Среда Олькеницкого из сухого агара. 2,5 г сухого питательного агара расплавляют в 100 мл дистиллированной воды. В остуженный до 50° С агар прибавляют все ингредиенты, указанные в рецептуре (этикетке). Среду, разлитую в пробирки, стерилизуют текучим паром (3 дня по 20 мин) и затем скашивают. Готовая среда должна быть бледно-розового цвета.
Дата добавления: 2016-11-22 ; просмотров: 498 | Нарушение авторских прав
источник