Теобальду Смиту, бактериологу из Министерства сельского хозяйства США, было поручено найти микроб, вызывающий свиную холеру. Болезнь представляла серьезную угрозу для промышленного животноводства.
Теобальд Смит и его руководитель Дэниел Салмон смогли выделить и изолировать бактерии, вызывающие заболевание, а вскоре сделали еще одно важнейшее открытие: если убить микробы с помощью высокой температуры и ввести полученный материал голубям, те становятся невосприимчивы к смертельной форме бактерии.
Эта находка, опубликованная в 1886 г. и вскоре подтвержденная другими исследователями, отметила новый этап в истории вакцинации.
Ученые выяснили, что вакцины можно создавать из убитой, а не просто ослабленной болезнетворной культуры.
Концепция использования «убитых» (инактивированных) вакцин стала огромным шагом вперед в области безопасности, особенно для тех, кто выступал против вакцин на основе живых или ослабленных микроорганизмов.
Другие ученые вскоре начали пытаться создавать инактивированные вакцины от других болезней, и всего через 15 лет плодами их трудов смогли воспользоваться не только голуби, но и люди, страдавшие от трех серьезнейших заболеваний: холеры, чумы и брюшного тифа.
В конце XIX века холера оставалась серьезной проблемой во всем мире, несмотря на передовые открытия Джона Сноу, в конце 1840-х установившего, что она распространяется через загрязненную воду, и открытые Робертом Кохом в 1883 г. бактерии Vibrio cholerae.
Ранние попытки создать вакцину на основе живого или ослабленного вируса имели некоторый успех, но от них вскоре отказались, отчасти из-за бурного протеста общественности.
В 1896 г. Вильгельм Колле сделал очередное эпохальное открытие, разработав первую инактивированную вакцину против холеры на основе культуры, убитой с помощью высокой температуры.
Еще одной серьезной угрозой жизни был брюшной тиф. Его вызывали бактерии Salmonella typhi, передающиеся через загрязненную пищу и воду. Хотя сегодня по-прежнему неясно, кто первым ввел человеку вакцину, приготовленную на основе убитых тифозных бактерий, известно, что в 1896 г. британский бактериолог Алмрот Райт опубликовал статью, в которой объявил, что человек, получивший инъекцию мертвыми сальмонеллами, обладает эффективной защитой против заболевания.
Инактивированная противотифозная вакцина Райта позднее была с огромным успехом испытана в полевых условиях на 4000 британских солдат, служивших в Индии. Позже вакциной Райта прививали британских солдат в Южной Африке во время Англо-бурской войны.
К сожалению, противники вакцинации лишили этой возможности многих других военнослужащих. Некоторые протестующие заходили так далеко, что даже выбрасывали за борт грузовых кораблей ящики, в которых переправляли вакцину.
Результат? Более 58 тыс. случаев брюшного тифа в британской армии, из которых 9000 стали смертельными.
Чума, уничтожившая миллионы жителей Европы в Средние века, обычно передается через укусы блох, которых, в свою очередь, разносят крысы. Вредоносные бактерии Pasteurella pestis (позже получившие новое название Yersinia pestis) были открыты в 1894 г.
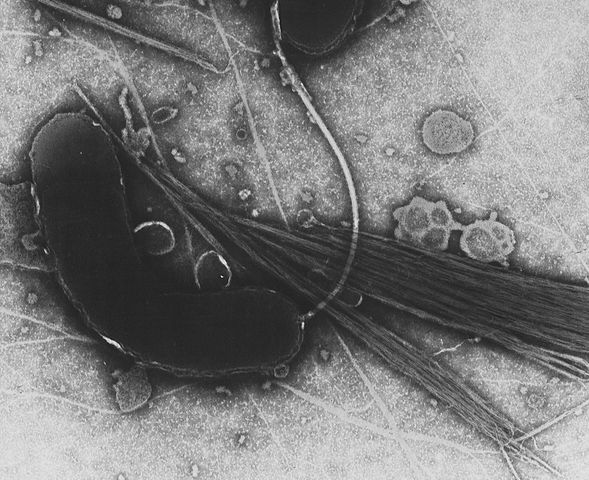
Через два года после этого, когда русский ученый Владимир Хавкин (см. фото) работал в Индии над вакциной против холеры, в Бомбее разразилась эпидемия чумы. Хавкин переключился на более злободневную задачу и вскоре создал инактивированную вакцину против чумы.
В 1897 г., чтобы проверить безопасность вакцины, он опробовал ее на себе. Риск себя оправдал, и через несколько недель вакцину получили 8000 человек.
К началу ХХ века, всего через 100 лет после самого первого открытия Дженнера , семья вакцин значительно увеличилась. Теперь в нее входили одна живая вакцина (против натуральной оспы), три аттенуированных (от бешенства, птичьей холеры и сибирской язвы) и три инактивированных (от брюшного тифа, холеры и чумы).
Джон Кейжу. Открытия, которые изменили мир.
источник
Наиболее массовую смертность пандемия чумы принесла в средине XIV века, прокатившись по всей Евразии и унеся по самым скромным подсчетам историков жизни 60 млн. человек. Если учесть, что в это время население земли составляло всего 450 млн., то можно представить себе катастрофические масштабы «черной смерти», как назвали эту болезнь. В Европе население уменьшилось примерно на треть, и недостаток рабочей силы здесь чувствовался еще не менее 100 лет, хозяйства стояли заброшенными, экономика была в ужасном состоянии. Во все последующие века также наблюдались крупные вспышки чумы, последняя из которых была отмечена в 1910-1911 годах в северо-восточной части Китая.
Названия происходит с арабского языка. Арабы называли чуму «джумма», что в переводе означает «шарик», или «боб». Причиной этому послужил внешний вид воспаленного лимфоузла чумного больного – бубон.
Выделяют три формы чумы: бубонная, легочная и септическая. Всех их вызывает одна бактерия Yersinia pestis, или, проще говоря, чумная палочка. Носителями ее выступают грызуны, обладающие противочумным иммунитетом. А блохи, покусавшие этих крыс, также через укус, передают ее человеку. Бактерия поражает пищевод блохи, в результате чего он блокируется, и насекомое становится вечно голодным, кусает всех подряд и сразу же заражает через образовавшеюся ранку.
В средневековые времена чумные воспаленные лимфоузлы (бубоны) вырезали или прижигали, вскрыв их. Чуму считали разновидностью отравления, при котором в организм человека попали некие ядовитые миазмами, поэтому лечение заключалось в приеме известных тогда противоядий, например, измельченных драгоценностей. В наше время чуму успешно одолевают с помощью распространенных антибиотиков.
Каждый год чумой заражаются около 2,5 тыс. человек, но это уже не в виде массовой эпидемии, а случаи по всему миру. Но чумная палочка постоянно эволюционирует, и старые лекарства оказываются не эффективными. Поэтому, хотя все, можно сказать, находится под контролем врачей, но угроза катастрофы существует и ныне. Примером этому может послужить смерть человека, зарегистрированная на Мадагаскаре в 2007 г., от штамма чумной палочки, при котором не помогли 8 видов антибиотиков.
Во времена средневековья женщины, у которых не было следов поражений оспой на лице (оспин), было не так уж много, а остальным приходилось скрывать рубцы под толстым слоем косметики. Это повлияло на моду чрезмерного увлечения косметикой, которая сохранилась до нашего времени. По мнению ученых-филологов, у всех женщин ныне с буквосочетаниями в фамилиях «ряб» (Рябко, Рябинина, и т.д.), шадр и часто щедр (Щедрины, Шадрины), Коряв (Корявко, Коряева, Корячко) предки щеголяли оспинами (рябинами, щедрами и т.д., зависимо от диалекта). Приблизительная статистика существует за XVII-XVIII века и говорит о том, что только в Европе появлялось 10 млн. новых больных оспой, а для 1,5 млн. человек из них это имело летальный исход. Благодаря именно этой инфекции белый человек колонизировал обе Америки. Например, на территорию Мексики в XVI веке испанцы завезли оспу, из-за которой умерло около 3 млн. местного населения – захватчикам не осталось с кем воевать.
У «оспы» и «сыпи» один корень. На английском языке оспа называется «малой сыпью» (smallpox). А сифилис называют при этом большой сыпью (great pox).
После попадания в человеческий организм, оспенные варионы (Variola major и Variola) приводят к появлению на коже пузырьков-пустул, места образования которых, потом рубцуются, если человек выжил, разумеется. Распространяется болезнь воздушно-капельным путем, также вирус остается активным в чешуйках с кожи заболевшего человека.
Индусы приносили богатые дары богине оспы Мариателе, чтобы задобрить ее. Жители Японии, Европы и Африки верили в страх демона оспы перед красным цветом: больным нужно было одеть красную одежду и находится в комнате с красными стенами. В ХХ веке оспу начали уже лечить противовирусными препаратами.
В 1979 г. ВОЗ официально сообщила о том, что натуральная оспа полностью искоренена, благодаря вакцинации населения. Но в таких странах, как США и Россия и поныне хранятся возбудители. Это делается «для научных исследований», и все время переносится вопрос полного уничтожения этих запасов. Возможно, что тайно хранят вирионы оспы Северная Корея и Иран. Любой международный конфликт может послужить поводом для использования этих вирусов в качестве оружия. Так что лучше привиться от оспы.
Данная кишечная инфекция до конца XVIII в основном обходила Европу стороной и бушевала в дельте Ганга. Но потом произошли перемены в климате, вторжения европейских колонизаторов в Азию, наладились перевозки товаров и людей, и это все изменило ситуацию: в 1817-1961 годах в Европе произошло шесть пандемий холеры. Самая массовая (третья) забрала жизни 2,5 млн. человек.
Слова «холера» походит от греческого «желчь» и «теку» (из больного в реальности вытекала вся жидкость изнутри). Второе название холеры из-за характерного посиневшего цвета кожи больных – «синяя смерть».
Вибрионом холеры является бактерия Vibrio choleare, обитающая в водоемах. Когда она попадает в тонкую кишку к человеку, то выделяет энтеротоксин, который приводит к обильному поносу, а потом и рвоту. В случае тяжелого течения болезни организм обезвоживается настолько быстро, что заболевший умирает через несколько часов после проявления первых симптомов.
К стопам больных прикладывали самовары или утюги для согревания, давали пить настои цикория и солода, натирали тело камфорным маслом. Во время эпидемии верили, что можно отпугнуть болезнь поясом изготовлеым из красной фланели или шерстяным. В наше время заболевших холерой эффективно лечат антибиотиками, а от обезвоживания дают пить вовнутрь или вводят внутривенно специальные растворы солей.
ВОЗ утверждает, что сейчас в мире седьмая пандемия холеры, началом которой называют 1961 год. Пока болеют в основном жители бедных стран, в первую очередь в Южной Азии и Африке, где каждый год заболевают 3-5 млн. человек и 100-120 тыс. из них не выживают. Еще, по мнению специалистов, из-за глобальных негативных изменений в окружающей среде скоро возникнут серьезные проблемы с чистой водой и в развитых странах. Кроме того глобальное потепление повлияет на то, что в природе очаги холеры появятся в более северных регионах планеты. При этом прививки от холеры, к сожалению, не существует.
До второй половины XIX века так именовали полностью все болезни, при которых наблюдались сильная лихорадка и путаность в сознании. Среди них самые опасные были сыпной, брюшной и возвратный тиф. Сыпной, например в 1812 году почти переполовинил 600-тысячную армию Наполеона, которая вторглась на территорию России, что послужило одной с причин его поражения. А через столетие в 1917-1921 годах умерло от тифа 3 млн. граждан Российской империи. Возвратный тиф в основном доставлял горя жителям Африки и Азии, в 1917-1918 годах лишь жителей Индии от него погибло около полумиллиона.
Название болезни происходит от греческого «тифос», что означает «туман», «спутанное сознание».
При сыпном тифе на коже образуются мелкие розовые высыпания на коже. При возвратном после первого приступа больному будто бы становится лучше на 4-8 дней, но потом болезнь вновь сваливает с ног. Брюшной тиф – это кишечная инфекция, которая сопровождается поносом.
Бактерии-возбудители сыпного и возвратного тифа переносят вши, и по этой причине вспышки эти инфекции вспыхивают в местах скопления людей во время гуманитарных катастроф. При укусе одной из этих тварей важно не чесаться – именно через расчесанные ранки инфекция попадает в кровь. Брюшной тиф вызывается палочкой Salmonella typhi, которая попав в организм с пищей и водой, приводит к поражению кишечника, печени и селезенки.
Во времена средневековья считали, что источником заразы выступает зловоние, которое исходит от больного. Судьи в Британии, которым приходилось иметь дело с преступниками больными тифом, как средство защиты носили бутоньерки из сильно пахнущих цветов, а также раздавали их пришедшим на суд. Польза от этого была разве что эстетическая. С XVII осуществлялись попытки борьбы с тифом с помощью коры хинного дерева, завезенной из Южной Америки. Так тогда лечили все болезни, при которых повышалась температура. В наши дни вполне успешно с тифом справляются антибиотики.
Список особо опасных болезней ВОЗ возвратный и сыпной тиф покинули в 1970 году. Случилось это благодаря активной борьбе с педикулезом (вшивостью), которая осуществлялась по всей планете. А вот брюшной тиф и дальше продолжает причинять беды людям. Самыми подходящими условиями для развития эпидемии являются жара, недостаточное количество питьевой воды и наличие проблем с гигиеной. Поэтому основными претендентами на вспыхивание эпидемий брюшного тифа являются Африка, Южная Азия и Латинская Америка. За оценками специалистов МОЗ каждый год брюшным тифом заражаются 20 млн. человек и для 800 тыс. из них это имеет летальный исход.
Лепра, еще именуемая проказой, – «медленная болезнь». Она, в отличии от чумы, например, не распространялась в виде пандемий, а тихо и постепенно покоряла пространства. В начале XIII на территории Европы находилось 19 тысяч лепрозориев (учреждение, для изоляции прокаженных и борьбы з болезнью) и жертва были миллионы. Уже к началу XIV века уровень смертности от лепры резко упал, но вряд ли из-за того что научились лечить больных. Просто инкубационный период у этой хвори составляет 2-20 лет. Бушевавшие в Европе инфекции вроде чумы и холеры убивали многих людей еще до того, как его относили к прокаженным. Благодаря развитию медицины и гигиены прокаженных сейчас в мире не более 200 тыс. Они в основном проживают в странах Азии, Африки и Латинской Америки.
Название походит от греческого слова «лепра», что в переводе «болезнь, которая делает кожу чешуйчатой». Проказой называли на Руси – от слова «казить», т.е. приводить к искажению, обезображиванию. В этой болезни также существует ряд других имен, например, финикийская болезнь, «ленивая смерть», болезнь Хансена и др.
Заразится лепрой возможно лишь долго контактируя с кожей носителя инфекции, а также при попадании во внутрь его жидких выделений (слюны или из носа). Потом проходит довольно длительное время (зафиксированный рекорд составляет 40 лет), после которого бацилла Хансена (Mucobacterium leprae) сначала изуродует человека, покрыв пятнами и наростами на коже, а потом сделает гниющим заживо инвалидом. Также при этом повреждается периферическая нервная система и заболевший теряет возможность чувствовать боль. Можно взять и отрезать себе часть тела, не поняв куда она делась.
Во времена средневековья прокаженных еще при их жизни объявляли умершими и помещали в лепрозории – подобие концлагерей, где больные были обречены на медленную смерть. Лечить зараженных пытались при помощи растворов, в которые входило золото, кровопусканием и ваннами с кровью гигантских черепах. В наши дни от этой болезни можно полностью избавиться с помощью антибиотиков.
С уверенностью можно сказать, что эпидемия нам не грозит. Лепрозории существуют и ныне, но их количество далеко не то что было когда-то, хотя условия нахождения и сейчас там, мягко говоря, не очень в большинстве. В России, например, их действует 4, а в Украине – всего 1, а в развитых странах их помещение больных в подобные учреждения не практикуется.
источник
Иллюстрация 1866 года. Источник
Холера вызывается подвижными бактериями — холерным вибрионом, Vibrio cholerae. Вибрионы размножаются в планктоне в солёной и пресной воде. Механизм заражения холерой — фекально-оральный. Возбудитель выводится из организма с фекалиями, мочой или рвотой, а проникает в новый организм через рот — с грязной водой или через не немытые руки. К эпидемиям приводит смешение сточных вод с питьевой водой и отсутствие обеззараживания.
Бактерии выделяют экзотоксин, который в организме человека приводит к выходу ионов и воды из кишечника, что приводит к диарее и обезвоживанию. Некоторые разновидности бактерии вызывают холеру, другие — холероподобную дизентерию.
Болезнь приводит к гиповолемическому шоку — это состояние, обусловленное быстрым уменьшением объёма крови из-за потери воды, и к смерти.
Холера известна человечеству ещё со времён «отца медицины» Гиппократа, умершего между 377 и 356 годами до нашей эры. Он описывал болезнь задолго до первой пандемии, начавшейся в 1816 году. Все пандемии распространялись из долины Ганга. Распространению способствовали жара, загрязнение вод и массовое скопление людей у рек.
Возбудитель холеры был выделен Робертом Кохом в 1883 году. Родоначальник микробиологии в период вспышек холеры в Египте и Индии из испражнений больных и кишечного содержимого трупов погибших, а также из воды выращивал микробы на покрытых желатином стеклянных пластинах. Он сумел выделить микробы, имевшие вид изогнутых палочек, похожих на запятую. Вибрионы назвали «Запятой Коха».
Учёные выделяют семь пандемий холеры:
- Первая пандемия, 1816—1824 гг.
- Вторая пандемия, 1829—1851 гг.
- Третья пандемия, 1852—1860 гг.
- Четвертая пандемия, 1863—1875 гг.
- Пятая пандемия, 1881—1896 гг.
- Шестая пандемия, 1899—1923 гг.
- Седьмая пандемия, 1961—1975 гг.
Возможной причиной первой эпидемии холеры была аномальная погода, вызвавшая мутацию холерного вибриона. В апреле 1815 года произошло извержение вулкана Тамбора на территории нынешней Индонезии, катастрофа в 7 баллов унесла жизни десяти тысяч жителей острова. Затем погибли до 50 000 человек от последствия, включая голод.
Одним из последствий извержения стал «год без лета». В марте 1816 года в Европе была зима, в апреле и мае было много дождей и града, в июне и июле в Америке были заморозки. Германию терзали бури, в Швейцарии каждый месяц выпадал снег. Мутация холерного вибриона, возможно, вкупе с голодом из-за холодной погоды, способствовала распространению холеры в 1817 году во всех странах Азии. От Ганга болезнь дошла до Астрахани. В Бангкоке погибли от 30 000 человек.
Остановить пандемию смог тот же фактор, что послужил её началом: аномальный холод 1823-1824 года. Всего первая пандемия продлилась восемь лет, с 1816 по 1824 года.
Спокойствие было недолгим. Всего через пять лет, в 1829 году, на берегах Ганга вспыхнула вторая пандемия. Она продлилась уже 20 лет — до 1851 года. Колониальная торговля, усовершенствованная транспортная инфраструктура, передвижения армий помогали болезни распространяться по миру. Холера дошла до Европы, США и Японии. И, конечно, она пришла в Россию. Пик в нашей стране пришёлся 1830-1831 годы. По России прокатились холерные бунты. Крестьяне, рабочие и солдаты отказывались терпеть карантин и высокие цены на продукты и потому убивали офицеров, купцов и врачей.
В России в период второй эпидемии холеры заболели 466 457 человек, из которых умерли 197 069 человек. Распространению способствовало возвращение из Азии русской армии после войн с персами и турками.
Император Николай I своим присутствием усмиряет холерный бунт в Санкт-Петербурге в 1831 году. Литография из французского периодического издания Album Cosmopolite. Датирована 1839 годом. Источник
Третью пандемию относят к периоду с 1852 по 1860 год. На этот раз только в России умерли более миллиона человек.
В 1854 году в Лондоне от холеры умерли 616 человек. С канализацией и водоснабжением в этом городе было много проблем, и эпидемия привела к тому, что над ними начали задумываться. До конца XVI века лондонцы брали воду из колодцев и Темзы, а также за деньги из специальных цистерн. Затем в течение двухсот лет вдоль Темзы установили насосы, которые стали качать воду в несколько районов города. Но в 1815 году в ту же Темзу разрешили вывести канализацию. Люди умывались, пили, готовили пищу на воде, которая затем наполнялась их же отходами жизнедеятельности — в течение целых семи лет. Сточные ямы, которых в то время в Лондоне было около 200 тысяч, не чистились, что привело к «Великому зловонию» 1858 года.
Лондонский врач Джон Сноу в 1854 году установил, что болезнь передаётся через загрязнённую воду. Общество на эту новость не обратило особого внимания. Сноу пришлось доказывать свою точку зрения властям. Сначала он убедил снять ручку водозаборной колонки на Брод-Стрит, где был очаг эпидемии. Затем он составил карту случаев холеры, которая показала связь между местами заболевания и его источниками. Наибольшее число умерших было зафиксировано на окрестности именно этой водозаборной колонки. Было одно исключение: никто не умер в монастыре. Ответ был прост — монахи пили исключительно пиво собственного производства. Через пять лет была принята новая схема канализационной системы.
Объявление в Лондоне, распространяемое в 1854 году, предписывало употреблять только кипячёную воду
Седьмая, последняя на сегодня пандемия холеры, началась в 1961 году. Она была вызвана более стойким в окружающей среде холерным вибрионом, получившим название Эль-Тор — по названию карантинной станции, на которой мутировавший вибрион обнаружил в 1905 году.
К 1970 году холера Эль-Тор охватила 39 стран. К 1975 она наблюдалась в 30 странах мира. На данный момент опасность завоза холеры из некоторых стран не ушла.
Высочайшую скорость распространения инфекции показывает тот факт, что в 1977 году вспышка холеры на Ближнем Востоке всего за месяц распространилась на одиннадцать сопредельных стран, включая Сирию, Иордан, Ливан и Иран.
Обложка журнала начала XX века
В 2016 году холера не так страшна, как сто и двести лет назад. Гораздо большему количеству людей доступна чистая вода, канализация редко выводится в те же водоёмы, из которых люди пьют. Очистные сооружения и водопровод находятся на абсолютно другом уровне, с несколькими степенями очистки.
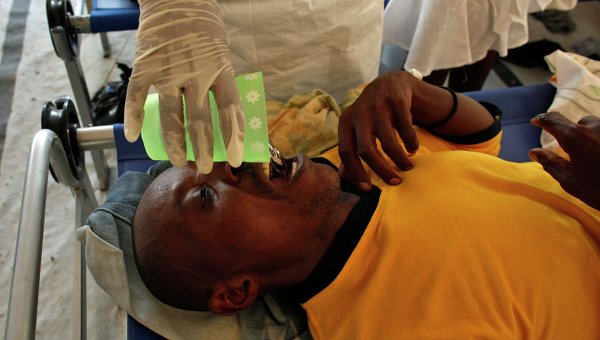
Хотя в некоторых странах вспышки холеры происходят до сих пор. Один из последних на данный момент случаев эпидемии холеры начался (и продолжается) на Гаити в 2010 году. Всего были заражены более 800 000 человек. В пиковые периоды за день заболевали до 200 человек. В стране живут 9,8 миллиона человек, то есть холера затронула почти 10% населения. Считают, что начало эпидемии положили непальские миротворцы, которые занесли холеру в одну из главных рек страны.
8 ноября 2016 года в стране объявили о массовой вакцинации. В течение нескольких недель планируют вакцинировать 800 000 человек.
Холера на Гаити. Фото: РИА Новости
В октябре 2016 года сообщалось, что в Адене, втором по величине городе Йемена, зафиксировали двести случаев заболевания холерой, при этом девять человек умерли. Болезнь распространилась через питьевую воду. Проблема усугубляется голодом и войной. По последним данным, во всём Йемене холеру подозревают у 4 116 человек.
Под названием «тиф», что в переводе с древнегреческого означает «помрачнение сознания», скрываются сразу несколько инфекционных заболеваний. У них есть один общий знаменатель — они сопровождаются нарушениями психики на фоне лихорадки и интоксикации. Брюшной тиф был выделен в отдельное заболевание в 1829 году, возвратный — в 1843 году. До этого у всех подобных болезней было одно название.

В США эта лихорадка распространена и сейчас, ежегодно регистрируется до 650 случаев болезни. О распространении говорит тот факт что в период с 1981 по 1996 годы лихорадка встречалась в каждом штате США, кроме Гавайи, Вермонт, Мэн и Аляска. Даже сегодня, когда медицина находится на гораздо более высоком уровне, смертность составляет 5-8%. До изобретения антибиотиков количество летальных исходов доходило до 30%.
В 1908 году Николай Фёдорович Гамалея доказал, что бактерии, вызывающие сыпной тиф, передаются вшами. Чаще всего — платяными, что подтверждают вспышки в холодное время года, периоды «завшивленности». Гамалея обосновал значение дезинсекции в целях борьбы с тифом.
Бактерии проникают в организм через начёсы или другие повреждения кожи.
После того, как вошь укусила человека, болезнь может не наступить. Но как только человек начинает чесаться, он втирает выделения кишечника вши, в которых содержатся риккетсии. Через 10-14 дней, после инкубационного периода, начинается озноб, лихорадка, головная боль. Через несколько дней появляется розовая сыпь. У больных наблюдается дезориентация, нарушения речи, температура до 40 °C. Смертность во время эпидемии может составить до 50%.
В 1942 году Алексей Васильевич Пшеничнов, советский учёный в области микробиологии и эпидемиологии, внёс огромный вклад методологию профилактики и лечения сыпного тифа и разработал вакцину против него. Сложность в создании вакцины была в том, что риккетсии нельзя культивировать обычными методами — бактериям необходимы живые клетки животного или человека. Советский учёный разработал оригинальный метод заражения кровососущих насекомых. Благодаря быстрому запуску в нескольких институтах производства этой вакцины во время Великой Отечественной войны СССР удалось избежать эпидемии.
Время первой эпидемии тифа определили в 2006 году, когда исследовали останки людей, найденных в братской могиле под Афинским акрополем. «Чума Фукидида» за один год в 430 году до нашей эры болезнь убила более трети населения Афин. Современные молекулярно-генетические методы позволили обнаружить ДНК возбудителя сыпного тифа.
Тиф иногда поражал армии эффективнее, чем живой противник. Вторая крупная эпидемия этой болезни датируется 1505-1530 годами. Итальянский врач Фракастор наблюдал за ней во французских войсках, осаждавших Неаполь. Тогда отмечали высокую смертность и заболеваемость до 50%.
В Отечественной войне 1812 года Наполеон потерял треть войска от сыпного тифа. Армия Кутузова потеряла от этой болезни до 50% солдат. Следующая эпидемия в России была в 1917-1921 годах, на этот раз погибли около трёх миллионов человек.
Сейчас для лечения сыпного тифа используют антибиотики тетрациклиновой группы и левомицетин. Для профилактики заболевания используются две вакцины: Vi-полисахаридная вакцина и вакцина Ту21а, разработанная в 1970-х.
Брюшной тиф характеризуется лихорадкой, интоксикацией, высыпаниями на коже и поражением лимфатической системы нижнего отдела тонкой кишки. Его вызывает бактерия Salmonella typhi. Бактерии передаются так же, как и в случае сыпного тифа — алиментарным, или фекально-оральным, способом. За 2000 год брюшным тифом во всём мире переболели 21,6 миллиона человек. Смертность составила 1%. Один из эффективных способов профилактики брюшного тифа — мытьё рук и посуды. А также внимательное отношение к питьевой воде.
У больных наблюдается сыпь — розеолы, брахикардия и гипотония, запор, увеличение объёмов печени и селезёнки и, что характерно для всех видов тифа, заторможенность, бред и галлюцинации. Больных госпитализируют, дают левомицетин и бисептол. В самых тяжёлых случаях используют ампициллин и гентамицин. При этом необходимо обильное питьё, возможно добавление глюкозно-солевых растворов. Все больные принимают стимуляторы выработки лейкоцитов и ангиопротекторы.
После укуса клеща или вши, переносчика бактерии, у человека начинается первый приступ, который характеризуется ознобом, сменяемым жаром и головной болью с тошнотой. У больного поднимается температура, кожа высыхает, пульс учащается. Увеличивается печень и селезёнка, может развиться желтуха. Также отмечают признаки поражения сердца, бронхит и пневмонию.
От двух до шести дней продолжается приступ, который повторяется через 4-8 суток. Если для болезни после укуса вши характерны один-два приступа, то клещевой возвратный тиф вызывает четыре и более приступов, хотя они легче по клиническим проявлениям. Осложнения после болезни — миокардит, поражения глаз, абсцессы селезёнка, инфаркты, пневмония, временные параличи.
Для лечения используют антибиотики — пенициллин, левомицетин, хлортетрациклин, а также мышьяковистые препараты — новарсенол.
Летальный исход при возвратном тифе случается редко, за исключением случае в Центральной Африке. Как и остальные виды тифа, заболевание зависит от социально-экономических факторов — в частности, от питания. Эпидемии среди групп населения, которым недоступна квалифицированная медицинская помощь, могут приводить к смертности до 80%.
Во время Первой мировой в Судане от возвратного тифа погибли 100 000 человек, это 10% населения страны.
Эдвард Мунк. «У смертного одра (Лихорадка)». 1893 год
Чуму и оспу человечество сумело загнать в пробирку благодаря высокому уровню современной медицины, но даже эти болезни иногда прорываются к людям. А угроза холеры и тифа существует даже в развитых странах, что уж говорить о развивающихся, в которых в любой момент может вспыхнуть очередная эпидемия.
4 ноября 2016 года сообщалось, что эпидемия брюшного тифа угрожает Дагестану. В Махачкале госпитализировали около 500 человек с острой кишечной инфекцией после отравления водой. Два человека попали в реанимацию. Для предотвращения эпидемии Минздрав России планировал передать лекарственные препараты «Альгавак М»,«Вианвак», «Шигеллвак» и «Интести-бактериофаг».
Причиной заражения в Махачкале была водопроводная вода. Директор местного водоканала арестован, ещё двадцать три человека — под следствием. Сейчас того же опасаются жители Ростова.
источник
Острое кишечное инфекционное заболевание из широкой группы сальмонеллезов, вызванное S.typhi abdominalis, и протекающая с преимущественным поражением подвздошной кишки; типичный антропоноз. Общая заболеваемость брюшным тифом в мире низкая и она неуклонно снижается. Однако ввиду участившихся в настоящее время военных конфликтов, приводящих к массовым исходам беженцев с из последующим скучиванием в концентрационных лагерях, нередки вспышки брюшного тифа из-за нехватки качественной питьевой воды и отсутствия надлежащих санитарно-гигиенических условий. После перенесенного заболевания формируется стойкий пожизненный иммунитет, повторные заболевания очень редки. Заражение здорового человека происходит алиментарным путем. Инкубационный период длится 10-14 дней. Попав в подвздошную кишку, возбудители поселяются в солитарных фолликулах и пейеровых бляшках подслизистого слоя, где находят для себя удобные условия для размножения. Оттуда они через в конце первой недели проникают в кровь, а по лимфатическим путям в брыжеечные лимфоузлы; с этого момента начинается формирование клеточного и гуморального иммунитета против бактерий. На 2-й неделе начинается выработка специфических антител, приводящая к постепенной элиминации микробов через потовые и молочные железы, с мочой, калом и что особенно важно — через печень с желчью. В этот период больной наиболее опасен для окружающих как источник инфекции. Бактериемия, развивающаяся на 2-1 неделе заболевания, сопровождается появлением на коже живота бледной необильной розеолезной сыпи. Выделяющиеся с желчью возбудители опять попадают в просвет кишечника, однако встретившись там вновь с лимфоидным аппаратом, где уже сформировался к ним клеточный иммунитет, микробы индуцируют развитие в нем реакции гиперчувствительности замедленного типа. Она проявляется в характерных морфологических изменениях солитарных фолликулов и пейеровых бляшек.
Патологическая анатомия кишечных изменений при брюшном тифе. Наиболее выраженные изменения лимфоидного аппарата отмечаются в подвздошной кишке (илеотиф), менее выраженные в толстом кишечнике (колотиф). Морфологические изменения лимфоидного аппарата подслизистой кишки проходят 5 стадий, каждая из которых занимает примерно 1 неделю. Стадия мозговидного набухания — в лимфоидных фолликулах происходит выраженная пролиферация ретикулярных и макрофагальных клеток, в которых находятся живые возбудители (незавершенный фагоцитоз); пролиферирующие ретикулярно-макрофагальные клетки формируют очаговые скопления в виде гранулем с нечеткими очертаниями (брюшнотифозные гранулемы). В результате клеточной пролиферации лимфоидные фолликулы и особенно пейеровы бляшки значительно увеличиваются в размерах, на их поверхности образуются борозды и извилины, так что бляшки становятся похожими на кору головного мозга.
Стадия некроза — реакции ГЗТ обусловливают гибель макрофагальных и ретикулярных клеток, что проявляется некрозом пейеровых бляшек. Некроз начинается в поверхностных отделах бляшек и постепенно углубляется, иногда поражая всю толщу стенки кишки. Стадия образования язв — некротические массы отторгаются и образуются язвы. Именно в эту стадию высока опасность кишечных кровотечений, в то время как опасность перфорации язв еще невелика. Стадия чистых язв — во время полного очищения дна и стенок язв от некротических масс резко повышается риск перфорации стенки кишки с развитием перитонита. Кишечные кровотечения и перфорации с развитием перитонита — типичные и классические осложнения брюшного тифа. Летальность при брюшнотифозном перитоните высокая — до 50 %. Стадия заживления язв — завершается образованием на их месте нежных рубчиков, лимфоидная ткань частично или полностью восстанавливается. В лимфоузлах брыжейки (в первую очередь в области илеоцекального угла) отмечаются сходные изменения — гиперплазия с образованием брюшнотифозных гранулем, некротические изменения, микроперфорации капсулы; в дальнейшем происходит организация поражений с рубцеванием и петрификацией лимфоузлов. Гиперпластические изменения происходят и в селезенке, которая увеличивается в 3-4 раза, гистологически в ее пульпе находят те же брюшнотифозные гранулемы. По ходу брюшного тифа при его тяжелом течении возможны внекишечные осложнения со стороны верхних дыхательных путей и легких: вторичные бактериальные (пневмококковые или стафилококковые) пневмонии, гнойный перихондрит гортани. В доантибиотическую эру брюшной тиф мог протекать как генерализованная инфекция с развитием гнойных остеомиелитов, артритов, циститов, простатитов или же в форме сепсиса.
Острое кишечное инфекционное заболевание с преимущественным поражением толстой кишки. Вызывается группой родственных бактерий — шигелл, ввиду чего дизентерию называют также ш и г е л л е з о м. Как и брюшной тиф, дизентерия — строгий антропоноз. Распространена гораздо более широко, чем брюшной тиф; путь передачи — алиментарный. После перенесенного заболевания формируется нестойкий иммунитет (от 3 мес до 1 года). Инкубационный период 1-7 дней (обычно 3 дня). Шигеллы поселяются непосредственно в цитоплазме эпителиальных клетках толстой кишки (эндоцитобиоз), чаще поражая при этом прямую и сигмовидную кишки. Микробы выделяют экзо- и эндотоксины с мощным энтеротоксическим действием. В результате происходит гибель и десквамация эпителия кишки, развиваются тяжелые расстройства кровообращения в слизистой оболочке (гиперемия со стазами, кровоизлияния), резко усиливается продукция слизи, повреждаются интрамуральные нервные ганглии, наблюдается весьма болезненное спазмирование кишки.
Стадийность морфологических изменений толстого кишечника.
1) Стадия катарально-геморрагического колита — продолжается 2-3 дня, характеризуется гиперемией и набуханием слизистой оболочки кишки, гиперпродукцией слизи бокаловидными клетками. Клинически это проявляется характерным видом каловых масс — «слизистый плевок с кровью».
2) Стадия фибринозного колита — продолжается 5-10 дней, морфологически проявляется некрозом слизистой оболочки кишки с образованием на ее поверхности фибринозно-гнойного экссудата в виде желтовато-зеленоватой пленки.
3) Стадия образования язв (10-12 сутки) — при отторжении фибринозных пленок открываются обширные эрозивно-язвенные дефекты, нередко циркулярные, которые являются источниками кишечных кровотечений и могут перфорировать (обычно микроперфорации, в противоположность брюшному тифу, где развиваются «макроперфорации»). В результате перфораций развиваются местные перитониты или парапроктиты.
4) Стадия заживления отмечается на 3-4-й неделях: язвенные дефекты замещаются грануляционной тканью, эпителизируются. Возможны рубцовые стенозы просвета толстой кишки (отсутствующие при брюшном тифе).
Осложнения и причины смерти.
Кишечные кровотечения, перфорации с развитием местного перитонита или парапроктита, у маленьких детей — тяжелая жировая дистрофия печени с печеночной недостаточностью, при иммунодефицитах — развитие токсико-инфекционного шока.
В настоящее время ввиду раннего применения эффективных антибиотиков дизентерия обычно протекает по типу катарально-геморрагического колита с минимумом осложнений (терапевтический патоморфоз).
Острейшее инфекционное заболевание с преимущественным поражением желудка и тонкого кишечника по типу катарально-серозного гастроэнтерита. Возбудителем является грамотрицательный холерный вибрион Коха (открыт в 1883 г) и вибрион Эль-Тор (открыт в 1906 г). Последний вид вибриона более устойчив во внешней среде, но вызывает несколько более легкое течение заболевания и атипичные его формы, с ним связано более частое вибриононосительство. Источником инфекции является вибриононоситель, резервуаром хранения инфекции — водоемы. Путь заражения — фекально-оральный. Антропоноз. Относится к карантинным инфекциям (вместе с чумой и натуральной оспой). Восприимчивость к инфекции составляет 80-95% (но не 100%), что связано с разрушительным действием на вибрионы соляной кислоты желудка. Пройдя желудочный барьер, микробы попадают в 12-перстную кишку, где начинают размножаться и выделять мощный экзотоксин — холероген. Под действием холерогена повышается проницаемость капилляров ворсинок тонкого кишечника, после чего они начинают выделять большое количество изотонической жидкости плазменного происхождения. Одновременно холероген нарушает всасывание натрия, что приводит к развитию не прекращающихся рвоты и поноса. В результате развивается обезвоживание и обессоливание организма (теряются не только ионы натрия, но и калия, а также гидрокарбонаты и хлор). Кровь сгущается, развиваются тяжелые генерализованные расстройства микроциркуляции с картиной гиповолемического шока.
Клинико-морфологические стадии холеры:
1) Холерный энтерит — слизистая тонкого кишечника отечна, полнокровна, отмечается гиперсекреция бокаловидных клеток. Клинически отмечается понос. При своевременном лечении процесс может оборваться на этой стадии.
2) Холерный гастроэнтерит — явления энтерита нарастают, начинается гибель покровного эпителия, который слущивается в просвет кишки с образованием беловатых комочков, видимых глазом в испражнениях (стул типа рисового отвара). Присоединяется гастрит, что клинически проявляется рвотой, в результате чего расстройства водно-электролитного баланса прогрессируют. Черты лица заостряются, глаза западают, кожа на руках сморщивается («рука прачки»), падает температура тела, появляетсярезкая жажда.
3) Алгидный период — к явлениям дегидратации присоединяется падение артериального давления, отмечается олиго- или анурия с развитием клинической картины гиповолемического шока с тоническими судорогами и смертельным исходом. Во внутренних органах обнаруживаются тяжелые дистрофические и некротические изменения. У выживших может развиться из-за перенесенного шока острая почечная недостаточность (постхолерная уремия). Возможны вторичные пневмонии. В качестве осложнения холеры описывается холерный тифоид — фибринозный колит, схожий с дизентерийным. При правильном лечении холеры не встречается.
Острейшее инфекционное заболевание из группы карантинных болезней. Вызывается палочкой чумы (Yersinia pestis), которая является аэробом и факультативным анаэробом. Антигены микроба близки к антигенам тканей человека. Типичный антропозооноз. Человек заражается от животных — (суслики, табарганы, тушканчики, белые крысы и др. грызуны), а также кошек и верблюдов. Переносчиком микробов от животных являются блохи, реже заражение происходит от больного человека воздушно-капельным путем. Инкубационный период длится от нескольких часов до 6 суток. Инфицирующая доза равна 1 микробной палочке. Для чумы характерны эпидемии пандемии с огромной летальностью. После перенесенного заболевания формируется ограниченный и нестойкий иммунитет, повторные заболевания не редки.
Различают бубонную и кожно-бубонную формы (возбудитель передается с укусами блох), первично-легочную и первично-септическую формы (преимущественно аэрогенный путь передачи от больных людей). На микроб развивается тяжелое серозно-геморрагическое или гнойно-некротическое воспаление с очень низкой барьерноиксирующей функцией. Бубонная чума характеризуется резким увеличением лимфоузлов по отношению к воротам инфекции, при этом первичного инфекционного очага нет. Обычно поражаются паховые, реже подмышечные и шейные лимфоузлы. Они резко увеличиваются в размерах (до кулака), спаяны между собой и с окружающими тканями (перилимфаденит), на разрезе темно-красного цвета, в них развивается гнойно-некротическое воспаление с выраженным геморрагическим компонентом. При затянувшемся течении болезни образуются свищи, язвы, которые в дальнейшем рубцуются. Если инфекция начинает распространяться лимфогенно, то могут поражаться и отдаленные лимфоузлы. При гематогенном распространении инфекции возникает вторично-септическая чума. Кожно-бубонная чума (кожная чума) — в отличие от предыдущей формы в месте входных ворот развивается серозно-геморрагическое воспаление (первичный чумной аффект) в виде пузырька с серозно-геморрагическим содержимым или чумного карбункула. В дальнейшем карбункул изъязвляется. Возможна трансформация во вторично-септическую форму. Первично-легочная чума — очень контагиозна и протекает гораздо тяжелее предыдущих форм. Развивается серозно-геморрагическая и гнойно-некротическая лобарная плевропневмония. Выражены явления общей интоксикации с развитием распространенных расстройств микроциркуляции и дистрофических изменений внутренних органов.
Острое инфекционное заболевание из группы бактериальных антропозоонозов. Заболевание вызывается спороносной и устойчивой во внешней среде палочкой (Bac. anthracis). Кроме человека болеют домашние и дикие животные, от которых и происходит заражение человека. В мирное время сибирской язвой заболевают преимущественно люди, постоянно контактирующие с сельскохозяйственными животными: скотники, мясники, переработчики шкур КРС. После перенесенного заболевания возникает стойкий иммунитет, повторные заболевания редки. Микробы могут попадать в организм человека через кожу, желудочно-кишечный тракт и легкие. Соответственно путям проникновения возбудителей выделяют кожную (в т.ч. конъюнктивальную), кишечную, первично-легочную и первично-септическую формы сибирской язвы. Кожная форма сибирской язвы: втречается наиболее часто, на месте внедрения возбудителя на коже лица, шеи, конечностей, туловища образуется небольшое красное пятно, в центре которого образуется пузырек с серозно-геморрагической жидкостью. Вскоре центральная его часть некротизируется и образуется сибиреязвенный карбункул, в основе которого лежит острейшее серозно-геморрагическое воспаление. По периферии очага воспаления в отечных тканях обнаруживается огромное количество сибиреязвенных палочек, которые практически не подвергаются фагоцитозу ПМЯЛ (незавершенный фагоцитоз из-за чрезвычайной патогенности сибиреязвенного токсина). Почти одновременно развивается регионарный лимфаденит,
при этом лимфоузлы резко увеличиваются в размерах, на разрезе темнокрасного цвета.
Конъюнктивальная форма (разновидность кожной формы) развивается при попадании спор в конъюнктиву глаз, при этом развивается тяжелый серозно-геморрагический офтальмит с отеком периорбитальной жировой клетчатки.
Кишечная форма: наибольшие изменения отмечаются в подвздошной кишке, где появляются обширные участки геморрагической инфильтрации (геморрагически-некротический энтерит) с язвообразованием. В полости брюшины
накапливается серозно-геморрагический выпот, в брыжеечных лимфоузлах возникает картина серозно-геморрагического лимфаденита. Первично-легочная форма характеризуется развитием геморрагического трахеобронхита с серозно-геморрагической очаговой или сливной пневмонией. Как правило, осложняется вторичным сепсисом. Первично-септическая форма — в отличие от вторичной септической формы характеризуется отсутствием первичного аффекта, однако развиваются септическая гиперплазия селезенки и геморрагический менингоэнцефалит («шапка кардинала»). Смерть больных сибирской язвой обычно наступает от сепсиса.
Не нашли то, что искали? Воспользуйтесь поиском:
источник
Фармацевтика, медицина, биология
Брюшной тиф (лат. Typhus abdominalis) — острая антропонозная инфекционная болезнь с фекально-оральным механизмом передачи, которую вызывает сальмонелла брюшного тифа, характеризуется лихорадкой преимущественно постоянного типа, общей интоксикацией с развитием заторможенности нервной деятельности до тифозного статуса, кожной сыпью, увеличением печени, селезенки и поражением лимфатического аппарата тонкой кишки.
Со времен Гиппократа до XIX века тифом (от греч. Τυφος — дым, туман, мгла) называли те болезни, которые сопровождались лихорадкой, затемнением сознания и бредом. Таким образом, очень долгое время под совокупным названием «тиф» проходили такие заболевания, как брюшной тиф и паратиф, эпидемический сыпной, возвратный и другие тифы, чума, сепсис и др. Только в начале XIX в. были накоплены данные, как клинические, так и морфологические, позволившие выявить особенности течения различных форм «тифов». В течение многих лет врачи разных стран отмечали особенности течения брюшного тифа, однако достоверное комплексное описание клинических проявлений его были сделаны выдающимися французскими врачами: Пьером Бретонне в 1826, а затем Пьером Луи в 1829, когда последний и предложил современную название болезни.
Возбудитель брюшного тифа обнаружен в 1880 году немецким микробиологом Карлом Эбертом в мезентериальных лимфатических узлах В чистой культуре возбудителя получил немецкий бактериолог Георгом Гаффки в 1884 г. Но не смог установить его родовую принадлежность. Но его совместные исследования вместе с выдающимся патологом Вирхов позволили утверждать, что эта болезнь передается водным путем, а не через воздух. Через год после выделения возбудителя Г. Гаффки американские ученые — ветеринарный хирург Даниель Сальмон и выдающийся эпидемиолог, патолог Теобальд Смит обнаружили, исследуя выделенного ими микроба «свиной холеры» (лат. Cholera sius), что существует целая группа возбудителей одного рода, которые получили в дальнейшем название «сальмонеллы». В дальнейшем быстро было доказано, что «палочка Эберта-Гаффки» принадлежит к роду сальмонелл. Из крови больного (гемокультура) впервые возбудителя выделил российский ученый, врач А. И. Вильчур в 1887, а В. Колеман и Б. Бакстон в 1907 году предложили для выделения возбудителя брюшного тифа искусственные живильни среды, содержащие желчь, которая используется и по сей день. Широко применяют до сих пор диагностическую реакцию агглютинации (так называемая реакция Видаля), которая была предложена французским врачом Георгом-Фердинандом Видалем в 1896
ВОЗ считает, что каждый год происходит в мире в 22-30 млн случаев брюшного тифа. Он вызывает до 1-3 млн смертей. Как полагают, из-за некачественного характер статистического учета в большинстве развивающихся стран, истинная заболеваемость и смертность большая зарегистрированной минимум втрое. Брюшной тиф и паратиф, возникая в виде эпидемических вспышек или спорадических случаев, обуславливают значительные экономические потери. Последняя на сегодня эпидемия произошла в Уганде в начале 2015 года, когда, по состоянию на 5 марта, было обнаружено 1940 случаев заболевания. В Украине сейчас преобладает спорадическая заболеваемость регистрируют отдельные небольшие вспышки с преимущественно пищевым заражением.
Возбудитель брюшного тифа (Salmonella typhi, или как ее на данный момент называют согласно существующей международной микробиологической классификации — вида Salmonella enterica, подвида enterica, серовар typhi) относят к роду Salmonella, семейства Enterobacteriaceae. По схеме Кауфмана-Уайта с дополнением Попофф / Ле Минор (международная классификация рода сальмонелл согласно разницей в О-и Н-антигенам) тифозная бактерия отнесена к серологической группы D1 В: 9.
Тифозные бактерии — это грамотрицательные палочки, имеют жгутики, со слабой биохимической активностью в отличие от других сальмонелл. Все они растут на обычных питательных средах, но особенно хорошо на содержащих желчь. Оптимум роста + 37 ° С, рН — 7,2-7,4.
Во внешней среде тифо-паратифозные сальмонеллы относительно устойчивые, хорошо переносят низкие температуры в течение нескольких месяцев. Выживание этих возбудителей в воде зависит от условий — в проточной они хранятся несколько дней, в водопроводной — до 3 мес., В иле колодцев — до 6 месяцев. Очень хорошо они сохраняются в пищевых продуктах, особенно в молоке, сыре, сметане, мясном фарше, в овощных салатах. Под действием высокой температуры быстро погибают (при t + 50 ° С — через час, + 60 ° С — через 20-30 мин., При кипячении — мгновенно). Прямые солнечные лучи действуют на них губительно. Под действием обычных дезинфектантов они погибают через несколько минут.
Брюшнотифозные палочки содержат:
- 2-3 соматические О-антигены,
- Базальное Н-антиген,
- особый антиген вирулентности — Vi-антиген.
Ведущий фактор патогенности тифо-паратифозных микробов — эндотоксина (липидно-полицукридний комплекс), который выделяется при разрушении бактерии. Именно он является ведущим в формировании многих основных клинических проявлений брюшного тифа. Общее токсическое действие эндотоксина тифозной бактерии выражена сильнее, чем в других сальмонелл.
Возбудители имеют достаточно большой набор ферментов, повышают их агрессивность:
- гиалуронидаза,
- фибринолизин,
- лецитиназа,
- гемолизинов т.
Многие атрибуты тифозных палочек — вирулентность, аглютинабильнисть, лизабельнисть не является постоянной степени, неизменными, они могут изменяться под влиянием антибиотиков, бактериофагов и других неблагоприятных для бактерий факторов. Даже в процессе заболевания у одного больного свойства возбудителя меняются.
Брюшной тиф относится к антропонозам. Источником инфекции является больной или носитель этих микробов. Больной выделяет возбудителей во внешнюю среду клинически значимое с испражнениями и мочой. 1 г фекалий больного в разгаре болезни (на 2-3 недели) содержит сотни миллионов микробов, а 1 мл мочи — до 180 млн. Если учесть, что в среднем человек выделяет в сутки около двух литров мочи, то самыми опасными считают так называемых «мочевых »носителей. Кроме того, акт мочеиспускания часто не сопровождается достаточным соблюдение навыков гигиене. При попадании в организм 1 000 микробных тел заболевает 25% инфицированных, 10000 — 50%, 10000000 — 100%. Так как больных с тяжелым течением брюшного тифа в большинстве случаев проявляют и госпитализируют, они реже становятся источником инфекции, как правило, только для тех, кто ими занимается или их непосредственно окружает. Интенсивно рассеивают возбудителей во внешней среде больные с легкими, атипичными формами. Эпидемиологическая опасность больного любую клиническую форму значительно уменьшается в периоде реконвалесценции.
Особую опасность в широком распространении этих микробов составляют хронические бактерионосители, а особенно те, которые по роду своей деятельности связаны с пищевыми продуктами, источниками водоснабжения. В мировой медицинской практике в настоящее время известно много таких случаев. Первым установленным медицинскими работниками хроническим фекальным носителем была американка Мэри Меллон, более известная, как «Тифозная Мэри», которая, работая кухаркой в различных семействах и учреждениях Нью-Йорка в начале XX века, заразила по официальным данным 53 человека, из которых 4 умерли от брюшного тифа.
Механизм передачи инфекции — фекально-оральный. Передача возбудителей происходит контактным, водным, пищевым путями, определенную роль играют механические переносчики — мухи. Факторами передачи служат зараженная вода, пищевые продукты.
Возникают в результате фекальных загрязнений источников водоснабжения, для них характерно поражение ограниченного контингента населения, территориально связанного с инфицированным водным источником. Водные вспышки брюшного тифа могут быть кратковременными или длительными. Возможно возникновение случаев среди купающихся в загрязненных водоемах, при случайном заглатывании инфицированной воды. Водные вспышки чаще носят взрывной характер. Кривая заболеваемости в случае одномоментного массового заражения имеет крутой подъем и быстрый спад после принятия соответствующих мер на водопроводе, а «эпидемический хвост» обусловлен контактными случаями заражения.
Характеризуются быстрым нарастанием количества заболевших и возникают преимущественно при употреблении инфицированного молока, молочных продуктов, преимущественно в горячую пору года. Можно заразиться при употреблении в пищу инфицированного мороженого, сливочного масла. Инфицирования пищевых продуктов, в том числе готовых блюд происходит при нарушении санитарных норм и правил переработки сырья, хранения, транспортировки, реализации готовой пищевой продукции. При пищевых вспышках источником инфекции чаще всего является носитель, этим объясняется необходимость строгого контроля за работниками предприятий общественного питания. На овощах, фруктах, хлебе и других продуктах, принимаемых без термической обработки, могут откладывать возбудителей мухи, которые являются механическим переносчиком, из-за чего возможно передачи инфекции именно таким образом. Жизнеспособных тифозных возбудителей находили в кишечнике и на лапках мух.
Происходит через загрязненные руки (прямой путь передачи), посуда, белье, дверные ручки (непрямой путь). При этом заболеваемость невысокая, но в случае выявления источника заражения заболевания могут регистрировать длительное время. Этот путь передачи способствует возникновению спорадических случаев, а источник инфекции выявить не удается только в 10-15% случаев.
Заболевания брюшным тифом в Украине характеризуются преимущественно летне-осенней сезонностью, на этот период приходится до 75% всех случаев. Считают, что сезонный подъем заболеваемости обусловлен не только упрощенным механизмом передачи инфекции, но и снижением реактивности организма под влиянием чрезмерной инсоляции, а также купанием в открытых водоемах, употреблением в пищу в большом количестве углеводов, нарушением водного обмена, снижением барьерной функции желудка, бактерицидных свойств крови. Определенное значение в распространении инфекции имеет также усиление миграции населения в летнее время (туризм, отдых у моря и др.), Купание в загрязненных водоемах, употребление некипяченого молока, немытых ягод, фруктов, овощей. В субтропических и тропических регионах заболеваемость сезонности отсутствует, случаи и вспышки встречаются равномерно в течение года. Риск заболевания брюшным тифом в Южной Азии (Индия, Пакистан, Бангладеш) в 30 раз больше, чем при поездках в другие географические регионы распространения брюшного тифа. В частности, больше всего случаев его регистрируют в Индии (980 на 100 тыс. Населения) и в дельте Меконга — Вьетнам, Камбоджа (200 на 100 тыс. Населения).
Восприимчивость к брюшного тифа всеобщая. Невосприимчивость определенной части населения обусловлена наличием специфического иммунитета в результате перенесенного в легкой форме заболевания (бытовая иммунизация). Наиболее резистентны к брюшного тифа лица с O (I) группой крови, у них и реже формируется носительство. Более склонны к этому заболеванию люди с АВ (IV) группой крови. Большое число носителей среди лиц с A (II) группой крови является генетически детерминированным. Перенесенное заболевание, если не сформировалось носительство, приводит к длительному стерильного иммунитета. На данный момент существует также мнение, что хроническое носительство, которое сформировалось после перенесенной острой формы брюшного тифа нужно рассматривать как своеобразную хроническую форму клинического течения, потому что у этих лиц происходят в течение жизни кратковременные подъемы температуры тела с непродолжительной появлением возбудителя в крови. В хронических бактерионосителей наиболее частая локализация возбудителя — желчный пузырь, почки, костный мозг. Способствуют этому желчнокаменная или мочекаменная болезни, наличие мочеполового шистосомоза и тому подобное. Такие лица составляют 3-6% от всех заболевших. После удаления желчного пузыря в «желчных» носителей нередко происходит элиминация сальмонелл из организма.
Через рот тифозные бактерии попадают в пищеварительный тракт, через их большую устойчивость к кислой среде желудка, они спокойно проходят внутрь барьерных к другим инфекционным агентам лимфатических образований: пейеровых бляшек и солитарных фолликулов тонкого кишечника. Способствуют такому глубокому их проникновению операции на желудке, алкоголизм с образованием устойчивой ахлоргидрии, прием антацидов, блокаторов Н2-гистаминорецепторов или ингибиторы протонного насоса. Иногда микробы способны попасть даже в лимфатические образования ротоглотки. Тифозные палочки способны спокойно проникать в лимфоидные клетки неиммунный человека и размножаться там, в то время как в цитоплазму иммунных лимфоцитов из периферической крови привитых людей и хронических носителей, бактерии не проникают, а располагаются вокруг лимфоцитов. Микроорганизмы размножаются в этих лимфатических образованиях, накапливаются в достаточном количестве и лимфогенно поступают в следующий защитный барьер — мезентериальные лимфатические узлы. В результате происходит гиперплазия, образование гранулем с крупными «тифозными» клетками со светлой цитоплазмой в этих лимфоузлах.
С момента прорыва лимфатического барьера и попадания первых тифозных сальмонелл к кровтотоку появляются клинические признаки заболевания. Эндотоксина, который выделяют первые тифозные бактерии, попавшие в кровь и гибнут в результате действия иммунной защиты, вызывает постепенное возбуждения терморегуляционные центра с повышением в типичных случаях температуры тела до фебрильных цифр в течение первых 3-5 дней болезни, загальноинтоксикацийни проявления, подавляет отдельные составляющие симпатической иннервации вегетативной нервной системы (кровеносных сосудов, сердца, слюнных желез и т.д.), приводя к соответствующему росту там парасимпатического влияния, что приводит, в первую очередь, перераспределение крови — скопление ее в кровеносных сосудах внутренних органов с возникновением некоторого отека их, вместе с тем уменьшение кровотока в кровеносных сосудах кожи. Происходит уменьшение слюноотделения, что в дальнейшем приводит к проблемам в полости рта. Однако общего угнетения симпатического влияния на все составляющие вегетативной нервной системы не происходит. Так при снижении активности симпатического отдела вегетативной нервной системы и повышении активности парасимпатической должны проходить повышение перистальтики кишечника, расслабление мочевого пузыря, расширение бронхов и зрачков. Этого при брюшном тифе не происходит, что означает избирательность действия эндотоксина на симпатичную иннервацию. Более того, задержка стула, мочеиспускания может быть обусловлена возбуждающие действием эндотоксина именно на симпатичную иннервацию на уровне автономных узлов брюшной полости. Уменьшение перистальтики кишечника также обусловлено и выразительностью мезаденита. Эндотоксина подавляет работу костного мозга, вызывая уменьшение уровня лейкоцитов и нейтрофилов, тромбоцитов. Именно ендотоксинемия приводит на раннем этапе всю клиническую симптоматику.
Практически одновременно идет так называемая паренхиматозная диффузия — возбудители разносятся в разные паренхиматозные органы и ткани, там образуются вторичные очаги воспаления и гранулемы. В результате возникают те или иные проявления поражения тех или иных органов, может искажать типичную клиническую картину (пневмония, нефрит, менингит и т.д.). Есть предположение, что преобладание того или иного поражения внутренних органов при брюшном тифе связано с преморбидным фоном — наличием слабых мест в организме, иногда некоторые из них даже клинически проявлялись к возникновению брюшного тифа. Из этих очагов, образовавшихся и с мест первичной локализации периодически возбудители поступают в кровь, таким образом, поддерживая бактериемию, который может длиться до 5-6 недель при отсутствии антибактериального лечения. Именно наличие Vi-антигена обеспечивает возбудителю брюшного тифа большую вирулентность, агрессивность, из-за чего лихорадочно-интоксикационные проявления при этой болезни поддерживаются продолжалось.
Начинается примерно со 2 недели клинических проявлений. Тифозная сальмонелла выделяется через почки в мочевые пути, через желчь. В кишечник возбудители поступают в большом количестве именно из желчного пузыря, где могут размножаться и накапливаться. При этом пик выделения тифозной сальмонеллы из желчного пузыря и соответственно из кишечника приходится на 2-3 неделе болезни. К этому вследствие попадания возбудителей тифа в лимфатического аппарата тонкого кишечника в инкубационном периоде произошла сенсибилизация к антигенам тифозных сальмонелл. Повторное попадание антигенов приводит к реакциям, описанных как феномен Артюса. Процесс повторного «прохождение» тифозных возбудителей через кишечник сопровождается рядом последовательно возникающих морфологических изменений:
- I неделя болезни — «мозгоподобных набухание» лимфатических образований кишечника, как гистиомоноцитарна реакция на повторное попадание тифозных сальмонелл;
- II неделя — образование местных некрозов в участке фолликулов; некрозы могут распространяться вглубь, достигая иногда мышечного слоя и даже брюшины;
- III неделя — происходит отторжение некротических масс и образование язв. Если при этом повреждается стенка кровеносного сосуда, возможно кровотечение, при образовании глубоких язв могут возникать перфорации кишечника;
- IV неделя — происходит полное очищение язв, также еще возможны кишечные кровотечения и перфорации;
- V неделю — заживление язв. В отличие от язв других отделов пищеварительной системы они не оставляют после себя ни рубцов, ни стриктур. На месте язв образуется пигментация, которая сохраняется много лет и носит название «пятна Петена».
Уже со второй недели болезни можно обнаружить антитела, агглютинируются тифозные сальмонеллы, а также антитела против O, H, и Vi-антигена. Они способствуют более быстрому «очищения» крови от возбудителей, но не играют решающей роли в процессе выздоровления, потому что не могут подействовать на расположенные внутриклеточно микроорганизмы. Главным фактором освобождения организма от возбудителей тифо-паратифозных инфекций являются клеточные защитные реакции, обеспечивающие уничтожение этих микробов и клеток, содержащих их в инфицированных тканях. Выделенная на высоте болезни тифозная сальмонелла более вирулентная, чем обнаружена в период угасания болезни, потому что пребывание в иммунном организме ведет к уменьшению содержания в микробной клетке Vi-антигена. Штаммы от острых носителей обычно имеют большую вирулентность, чем те, которые выделены от хронических носителей. В период высокой эпидемической заболеваемости непрерывный пассаж тифозной сальмонеллы с одной чувствительного организма в другой ведет к росту вирулентности и патогенности тифозных микроорганизмов. Напротив, повышение коллективного иммунитета населения способствует снижению его вирулентных свойств.
Согласно МКБ-10 выделят подкласс «Тиф и паратиф А01», а в этом подклассе выделяют отдельно «Брюшной тиф А01.0».
Длится от 7 до 30 дней, в среднем — 10-14 дней. Продолжительность инкубационного периода определяется многими факторами, но прежде всего количеством тифозных сальмонелл, попавшие в организм, их вирулентностью, по состоянию макроорганизма. Кратчайший период встречается при массивном заражении, водном пути передачи, при наличии тяжелых фоновых заболеваний.
В ходе заболеваний выделяют несколько периодов:
В большинстве случаев заболевание начинается постепенно: повышается температура тела, появляется слабость, повышенная утомляемость, чувство разбитости, ухудшается аппетит, нарушается сон. Практически все симптомы на этом этапе обусловлены действием эндотоксина. Именно поэтому отмечают нарастающую бледность кожи, особенно лица, хотя при повышении температуры тела должно происходить обратное. Спазм поверхностных кровеносных сосудов и расширения их во внутренних органах приводит к постепенному увеличению печени и селезенки. Происходит снижение АД, брадикардия. Нарушается правило Либермейстера — на каждый градус выше 37 ° С частота сердечных сокращений увеличивается не на 10-12, как при большинстве случаев лихорадки, а лишь на 2-4 сокращения. Иногда может быть покашливание, особенно при перемене положения тела из горизонтального в вертикальное, что связано с переполнении кровеносных сосудов легких. Вследствие медленного кровотока и расширения кровеносных сосудов ЦНС происходит определенный отек мозга (токсическая энцефалопатия), через который головная боль становится постоянной, упорным, разлитым, что растет во второй половине дня. Появляется нарушение формулы сна: сонливость днем и бессонница ночью. Как правило, при этом менингеальные признаки не выражены. На раннем этапе перистальтика кишечника еще не возбуждено, но к концу этого периода происходит задержка стула, ухудшение перистальтики, видимо вздутие живота. Сильная слабость заставляет больного оставаться в постели. Больной постепенно теряет интерес к окружающему, неохотно отвечает на вопросы, реакция его замедленная, четко видно заторможенность больного, особенно при попытке установить с ним словесный контакт. Начальный период заканчивается, когда температура тела достигает максимума, длится 4-7 дней.
Без лечения длится 2-3 недели. Лихорадка приобретает устойчивый постоянный характер на уровне 39-40 ° С без озноба. Однако при приеме жаропонижающих средств может будет ремитирующий с несвойственным типичном течении небольшим ознобом. Интоксикация нарастает до максимума, бывает иногда выражена до тифозного статуса. При тяжелом течении у больного появляется спутанность сознания («нечеткость»), он нечетко ориентируется в окружающем, бредит, у него может даже возникнуть психоз. Лицо амимичне. В этих случаях больной беспокоен, полностью дезориентирован в окружающем, иногда у него появляются галлюцинации, агрессивность — но все это происходит в пределах кровати (в отличие от других тифов — сыпного, возвратного!). Иногда это называют «бред бормотание» или «лат. Coma vigile — кома бодрствования». Все признаки, появившиеся в течение предыдущего периода, получают своего наибольшего развития. АО может быть ощутимо снижен. Если до этого была только относительная брадикардия, то она может перейти в абсолютную. Тоны сердца приглушены, может появиться систолический шум на верхушке. У небольшого числа физически развитых людей может появиться дикротия пульса (пальпаторные ощущение дополнительного пульсового удара сразу же после основного). При других инфекционных болезнях такой феномен не встречается. Над легкими прослушивают ослабленное дыхание, единичные сухие хрипы. Кожа и лица бледные. Кожа сухая на ощупь за высокой температуры тела. Язык утолщен, в начале он покрыт белым налетом, но края его и кончик от наслоения свободны, поэтому четко видны отпечатки зубов по краям. Со 2-й недели при отсутствии ухода за полостью рта он покрывается черным налетом («фулигинозный язык»). Закономерный метеоризм, увеличение печени и селезенки. Типичные запоры. При перкуссии правой илеоцекальной участка отмечается ощутимое укорочение перкуторного звука — положительный симптом Падалки. Этот симптом связан со значительным правосторонним мезентериальным лимфаденитом. Возможны дизурические проблемы.
На кожи начиная с 8 дня болезни у половины больных может появляться розеолы с типичной локализацией: боковые поверхности живота, нижняя часть грудной клетки; изредка на предплечьях, верхней части грудной клетки, шеи, коже на пояснице. Представляют они собой розово-красные или бледно-розовые пятна с четкими контурами, до 1 см в диаметре, исчезают при надавливании, но сразу же появляются вновь. Элементов немного, элемент существует 3-5 дней. Новые розеолы могут подсыпать в течение лихорадки. Высыпания с геморрагическим компонентом — признак очень тяжелого течения болезни.
Появляются органные поражения в зависимости от преморбидного фона (легкие, миокард, почки, мозговые оболони и т.д.), что может приводить через выразительность этих проявлений к диагностическим ошибкам.
При этом температура тела может падать как политически, так и критически, симптомы постепенно исчезают в течение 1-2 недель. Длительный субфебрилитет в периоде реконвалесценции — часто предвестник обострение заболевания. Далеко не всегда все описанные выше периоды четко прослеживают. Клиническое течение брюшного тифа за последние десятилетия пережил определенные изменения, объясняют кардинальными переменами условий жизни людей и большим использованием антибиотиков. Чаще регистрируют острое начало болезни с быстрым повышением температуры тела и критическим ее падением, короче лихорадочный период, проявления интоксикации выражены слабо. Тифоидной изменения ЦНС смутные или вообще отсутствуют. Скорее появляется сыпь, розеол очень мало, чаще встречаются легкие формы болезни. Раннее применение антибиотиков в большинстве случаев значительно сокращает продолжительность брюшного тифа, иногда буквально «обрывает» его течение.
Кроме типичного течения клинически выделяют еще атипичные формы брюшного тифа. К ним относят:
- Абортивный тиф, при котором начинается заболевание и в дальнейшем протекает согласно всеми характерными для него закономерностями, а затем внезапно наступает перелом в ходе болезни и больной быстро выздоравливает. Чаще это бывает при раннем назначении антибактериальной терапии, хотя описывали подобные ситуации и в доантибиотичну эру;
- Легкий тиф (стертая форма), носивший в прошлом название «амбулаторный». Для него характерны субфебрильная кратковременная (несколько дней) лихорадка, незначительная интоксикация, при которой больные даже сохраняют работоспособность. Такие проявления, как сыпь, гепатоспленомегалия у них практически не проявляют. Эти случаи обычно своевременно не распознают, диагноз устанавливают или ретроспективно (серологические исследования), либо на основании случайно сделанных бактериологических исследований, а также при появлении таких осложнений, как кишечное кровотечение или перфорация кишечника.
Кроме типичного циклического течения брюшной тиф может протекать с обострениями или с рецидивами.
Четко очерченные обострения — это такие случаи, когда после снижения температуры тела на несколько дней до субфебрильных цифр и существенного улучшения самочувствия больного, снова поднимается температура тела до высоких цифр с последующим проявлением всех ведущих клинических симптомов. В настоящее время причиной обострений чаще всего является раннее отмены антибиотика или уменьшения его дозы.
Рецидивы могут наступить в любые сроки после нормализации температуры тела, но чаще на 2-3 недели, то есть вскоре после отмены антибиотика. Однако, описаны и более поздние рецидивы — через 1-2 месяца после нормализации температуры. При рецидивах также с первых дней вырисовывается типичная клиническая картина брюшного тифа.
У пожилых людей брюшной тиф, как правило, начинается постепенно (очень медленное разогрева), характерно длительное течение, реже бывают сыпь, диарея, но нередко вместо брадикардии обнаруживают тахикардию. В них редко происходит перфорация кишечника через инволюцию лимфоидной ткани, но чаще формируется бактерионосительство.
Специфическими осложнениями брюшного тифа являются кишечное кровотечение и перфорация кишечника, возникающие в течение 2-5 недели болезни, чаще на 3-м.
Считают, что кишечное кровотечение происходит в четверти заболевших брюшным тифом. Однако степень потери крови разный. В большинстве происходит клинически незначительное кровотечение, определяющие только с помощью исследования испражнений на скрытую кровь (реакция Грегерсена). Как правило, из-за отсутствия кровеносных сосудов крупного калибра в тифозных язвах, молотый появляется редко. Однако в определенном количестве случаев кровотечение сопровождается значительным молотой, приводит к выразительным гемодинамических изменений (тахикардия, еще большее снижение АД), внезапного снижения температуры тела, иногда ниже 37 ° С, что на температурном листке может быть замечено в виде так называемого «чертова креста» (пульс, температура тела ↓). Чаще такая массивное кровотечение бывает при возникновении большого количества язв в кишечнике.
Перфорация возникает часто как небольшая по размерам, часто прикрыта брюшиной, через что в отличие от прободения язв желудка и двенадцатиперстной кишки, сопровождающееся «кинжальным» болью, болевые ощущения при тифозных перфорациях нередко отсутствуют и появляются только при развитии разлитого перитонита, когда делать что-то поздно. Поэтому больной и медицинский персонал должны быть постоянно настороже. При появлении у больного каких-либо необычных ощущений в правой илеоцекальной области, выявлении там резистентности брюшной стенки, положительных симптомов раздражения брюшины, потенциально эти признаки нужно расценивать как подозрительные на перфорацию кишечника. Редко перитонит может быть вследствие некроза мезентериального лимфатического узла.
К другим осложнениям следует относить любые клинически явные признаки поражений тех или иных органов (пневмотиф, менинготиф, миокардит, нефротиф, остеомиелит и т.д.).
В большинстве случаев заболевание заканчивается полным выздоровлением с формированием длительного стойкого иммунитета. Повторные заболевания крайне редки. Основными причинами смерти являются осложнения — массивное кишечное кровотечение, перитонит, миокардит, тяжелое поражение ЦНС.
При наличии опорных клинических симптомов и эпидемиологических признаков нужно проводить диагностику брюшного тифа и паратифа. Однако из-за отсутствия високоимовирних (патогномоничных) симптомов главным в клинической диагностике алгоритм: «Если горячку продолжительностью более 5-ти суток клинически ничем нельзя объяснить, то в комплексе обследования больного нужно не забыть соответствующие исследования на брюшной тиф и паратиф»
В общем анализе крови в разгар типичного течения выявляют лейкопению (уменьшение количества лейкоцитов), сдвиг в лейкоцитарной формуле крови вправо — отсутствие эозинофилов (анэозинофилия), уменьшение количества нейтрофилов, увеличение лимфоцитов, в тяжелых случаях — еще и анемия, тромбоцитопения. При появлении осложнений возможно изменение лейкопении на лейкоцитоз с увеличением числа нейтрофилов и, соответственно, уменьшением — лимфоцитов. В общем анализе мочи обычная альбуминурия. При значительном поражении внутренних органов могут наблюдать рентгенологические проявления пневмонии, ультразвуковые изменения в почках, увеличение печени и селезенки. При возникновении менинготифу есть изменения в спинномозговой жидкости как это характерно для гнойного менингита.
Остается и сегодня ведущим для специфической диагностики брюшного тифа, а также паратифа. В первую очередь главным исследованием является посев крови («гемокультура») с целью выделения сальмонелл брюшного тифа. Наличие устойчивой бактериемии, о чем при брюшном тифе свидетельствует любое повышение температуры тела, обусловливает возможность выделения тифозных сальмонелл. Наиболее часто можно выделить тифозных возбудителей на первой неделе болезни, в дальнейшем вероятность обнаружения этих сальмонелл в крови уменьшается, поэтому для посева берут все большее количество крови. Для выделения используют питательные среды, содержащие желчь, так как именно она не дает возможности роста других микробов, а для сальмонелл является селективным. Положительная гемокультура — наиболее надежное подтверждение диагноза. Посев проводят на 10% желчный бульон. Соотношение объема взятой крови и питательной среды — 1:10. На 1-й неделе для исследования достаточно взять 10 мл крови из вены, на 2-м — 20 мл, на 3-м — 30 мл и т. Д.
Хотя ВОЗ считает, что выделение тифозных возбудителей из костного мозга более уловистым — таким образом тифозных сальмонелл можно выделить до 5-го дня после назначения антибактериальных средств, однако технические условия этого исследования и болезненность процедуры уменьшают процент применения методики костно-мозговой культуры. Неплохой результат дает бакпосев с розеол, но эта методика также достаточно болезненной, и поэтому практически ее в Украине на сегодня не используют. Также могут быть выделены тифозные возбудители при развитии осложнений со спинномозговой и перитонеальной жидкости, мезентериальных лимфатических узлов, резецированои кишки, из полости абсцесса и тому подобное. Положительный бактериологический посев кала, мочи, желчи не является подтверждением остроты процесса, а его нужно рассматривать, прежде всего, как возможно носительство. Посев желчи можно проводить через дуоденальное зондирование только в периоде реконвалесценции, потому что его проведение в разгар болезни может привести к нежелательным осложнениям — кишечного кровотечения, особенно перфорации кишечника.
Можно применять для подтверждения диагноза с 2-й недели болезни, исследования обязательно проводят в динамике с интервалом 5-7 дней. Применяют:
- Реакция агглютинации (реакция Видаля), ее диагностический титр не менее 1: 200, в дальнейшем возможен рост титра;
- Реакция непрямой гемагглютинации (РНГА) более специфическая, становится положительной на 6-7 сутки.
- Vi-гемагглютинацию используют для диагностики бактерионосительства;
- Иммуноферментный анализ (ИФА) более чувствителен других серологические методы, позволяет определять антитела разных классов (G, M) и прогнозировать вероятность последствий, в том числе и формирование носительства.
В мире широко используют полимеразной цепной реакции (ПЦР), которая позволяет определить в крови больного ДНК брюшнотифозной сальмонеллы.
При брюшном тифе этот вид терапии является ведущим. В этих случаях этиотропную терапию назначают сразу, как только была высказана подозрение. Но в мире в последние годы существует проблема мультирезистентности тифо-паратифозных сальмонелл в гиперэндемичных районах, поэтому при назначении ведущей в этой ситуации этиотропной терапии необходимо тщательное изучение эпидемиологического анамнеза.
ВОЗ для Украины, других стран Восточной Европы (а также субсахарской Африки, Южной Америки, Ближнего Востока) рекомендует данный момент начинать с фторхинолонов (препаратов первой звена): ципрофлоксацин офлоксацин per os 0,2-0,4 г 2 раза в сутки 7-14 суток, или пефлоксацин 0,4 г 2 раза в сутки 7-14 дней. При возникновении определенных осложнений, тифозного статуса эти препараты назначат можно и парентерально. Как препараты второго звена (т.е. при устойчивости или непереносимости препаратов первого звена) в неосложненных случаях нужно применять азитромицин 0,5 г 1 раз в 1-й день, 0,25 г 1 раз 2-5-й день, или цефиксим 0,2 г 2 раза в день 14 дней, или амоксициллин 0,75-1,0 г 3 раза в сутки 7-10 дней перорально. В осложненных случаях, при тифозной статусе препаратами второго звена для этих регионов ВОЗ рекомендует цефтриаксон 1-2 г 2 раза в день, или цефотаксим 2 г 4 раза в день, или ампициллин 1,0-2,0 г каждые 4-6 часов парентерально.
Для лечения больного, заразился в регионе с мультирезистентнистю тифо-паратифозных сальмонелл (Южная и Восточная Азия), ВОЗ считает необходимым как первая звено в неосложненных случаях использования цефиксиму 0,2 г 2 раза в день 14 дней вместе с ципрофлоксацином или офлоксацина 0,2-0,4 г 2 раза в сутки до 7-14 суток, а как 2-й звена — азитромицин 0,5 г 1 раз в день до 10 суток per os. В осложненных ситуациях в первую звено в этих регионах включают цефтриаксон 1-2 г 2 раза в день, или цефотаксим 2 г 4 раза в день обязательно вместе с ципрофлоксацином или офлоксацина 0,2-0,4 г 2 раза в сутки до 7-14 суток парентерально. Как препараты второго звена в этом регионе предлагаются азтреонам 1-2 г 3-4 раза в день (в Украине на сегодняшний день не зарегистрирован) или имипенем (в Украине он только в комбинации с циластином) по 0,5-1 г каждые 6:00 обязательно вместе с ципрофлоксацином или офлоксацина 0,2-0,4 г 2 раза в сутки до 14 суток, или гатифлоксацином 0,4 г в сутки в течение 7-14 суток, или левофлоксацином 0,5 г в сутки в течение 7 -14 суток — все препараты парентерально.
Нужно динамично оценить эффективность препарата. При подозрении на нечувствительность нужна быстрая смена антибактериального средства. ВОЗ считает, что появление обострения или рецидива тифо-паратифозной инфекции не требует изменения антибактериального препарата, который до этого оказував эффект, а побуждает провести поиск других причин, которые привели к несоответствующего течения болезни. Эксперты ВОЗ считают, что при терапии брюшного тифа в процессе самого лечения в антибактериального препарата выработаться устойчивость не может, а это происходит за этим процессом через плазмидную передачу нечувствительности, свойственную всем кишечным бактериям. Длительное применение антибиотиков может служить причиной развития кандидоза, дисбиоза кишечника. Поэтому в течение всего курса антибиотикотерапии больные должны получать флуконазол или другие противогрибковые препараты, средства, корректирующие микрофлору кишечника.
Патогенетические мероприятия очень важны при брюшном тифе. Всем больным назначают строгий постельный режим в течение всего лихорадочного периода и еще 5 дней после нормализации температуры тела. В случае неосторожного расширение режима к этому сроку существует очень серьезная вероятность возникновения таких осложнений как коллапс, кишечное кровотечение, перфорация кишечника. За больным осуществляют постоянное наблюдение, уход (регулярная обработка полости рта, кожи), при запорах — препараты лактулозы, очистительные клизмы. Диету N1 по Певзнеру назначают с 1-го дня, постепенное расширение ее возможно только после нормализации температуры тела, но не раньше 5-й недели болезни (заживление язв). Пища должна содержать достаточное количество витаминов, солей калия. Не назначают газированные минеральные воды, настой шиповника, желчегонные травы. Учитывая наличие у больных интоксикации, которая в первые дни может даже усиливаться на фоне приема антибиотиков, существенное внимание следует уделять дезинтоксикационная терапия. Если необходимое количество жидкости (до 40 мл / кг массы в сутки) не удается обеспечить перорально, в том числе с пищей, можно назначить в / в сбалансированы полийонни растворы, которые позволят компенсировать водно-электролитные сдвиги, глюкозо-солевые смеси, смеси солей и других углеводов, 5-10% раствор глюкозы, реополиглюкин.
При появлении кишечного кровотечения назначают срочно холод на живот, специальные диеты, Антигеморрагические средства, при необходимости — переливание эритроцитарной массы, тромбомасы, криопреципитата. Если в течение 2-х суток консервативная борьба с кишечным кровотечением к успеху не приводит — необходимо ставить вопрос о хирургическом вмешательстве с починкой кровоточащих язв. Как правило, ревизии подлежат последние 70 см тонкого кишечника, где сосредоточенные такие язвы. При наличии перфорации только немедленная операция по полноценной ревизии перитонеуму может спасти жизнь больному. Весь этот период продолжают антибактериальной терапии.
Согласно существующим в Украине нормативными документами по стационара реконвалесцентов выписывают на 21-й день нормальной температуры тела. Обязательным является контрольное обследование перед выпиской: через 2 дня после отмены антибиотика назначают 3 дня подряд бактериологические посевы кала и мочи (так называемая копроуринокультура — КУК) и однократно — посев желчи (биликультура). При отрицательных результатах Кук и биликультуры больного выписывают. Если в одном из посевов снова обнаруживают тифозных возбудителей, проводят повторный курс лечения антибиотиком, к которому возбудитель чувствителен (10-14 дней) с последующим обследованием перед выпиской, как указано выше. Реконвалесценты подлежат диспансерному наблюдению в течение 2-х лет, но реконвалесценты из числа работников предприятий общественного питания, пищевой промышленности, системы водопровода, детских дошкольных учреждений (так называемых декретированных групп) — пожизненно. Порядок обследования различных категорий реконвалесцентов, допуска их на работу регламентируют специальные подробные инструкции Министерства здравоохранения. Носителей к работе на предприятиях общественного питания, в детских учреждениях не допускают. Санация носителей — сложное, до конца не решен вопрос. При остром носительстве показано назначение антибактериальной терапии, хотя хорошие результаты скорее исключение, чем правило. При хроническом носительстве нужно лечить фоновые болезни, если их удается ликвидировать, то может наступить и элиминация тифозных возбудителей.
Важнейшим условием профилактики брюшного тифа является соблюдение личной гигиены (прежде всего, чистоты рук), защиты от инфицирования продуктов, воды, предметов быта, соблюдения условий приготовления и хранения пищи, выявление бактерионосителей путем регулярных обследований всех, кого относят к декретированных групп, кого нанимают на работу к специальностям этих групп.
После госпитализации больного в очаге проводят заключительную дезинфекцию. Осуществляют активный врачебное наблюдение за теми, кто был в контакте с заболевшим. Профилактическая санация контактных не показано. С целью активного выявления бактерионосителей обследуют всех, кто поступает на работу на декретированы специальности, а также лиц, которые общались с больным в эпидемическом очаге. Обследованию подлежат также лица с впервые установленным хроническим заболеванием печени, желче- и мочевыводящих путей.
По показаниям (чаще всего, это вспышка тифо-паратифозной заболевания отдельной территории, поездка в местности, где существует угроза заболеть этими инфекциями) проводятся вакцинацию. Комплексную тривакциной ТАБ (против тифа и паратифа А и В) в дозе 0,5 мл вводят подкожно, троекратно с интервалами между приемами в 10 дней вводят при поездках на гиперэндемичных территории, где распространены эти инфекции вместе, особым категориям граждан (военнослужащие, работники системы ликвидации чрезвычайных ситуаций, лабораторные работники, работающие с культурами этих возбудителей и т.д.). После вакцинации иммунитет сохраняется до 10 лет. На территории, где регистрируют повышение заболеваемости, ревакцинация проводится каждые 3 года. Проводят также вакцинацию против одного брюшного тифа, существуют как пероральные, так и парентеральные такие вакцины.
Путешественники в эндемичные страны должны избегать сырых неочищенных фруктов или овощей, так как они, возможно, были промыты загрязненной водой. Кроме того, путешественники должны пить только в соответствии подготовленную чистую или обеззараженную, иногда и кипяченую воду, как это описано для профилактики диареи путешественников. Путешественники должны быть вакцинированы по крайней мере за неделю до отъезда в эндемичный район. Поскольку эти вакцины создают искусственный иммунитет лишь на несколько лет, консультацию со специалистом по медицине путешествий настоятельно рекомендуют, если человек едет в эндемичные по брюшному тифа страны через несколько лет после вакцинации.
Находка останков Миртиды позволила ученым установить, что первая в истории человечества эпидемия, чей факт был научно доказан, вспыхнула 430 до н. е. в Древних Афинах после массового заболевания брюшным тифом. Эта эпидемия протяжении 4 лет уничтожила около трех населения города и стала одной из причин поражения государства в Пелопоннесской войне. В остатках костей методом суицидальные полимеразной цепной реакции было найдено ДНК тифозной сальмонеллы. 2010 года в Интернете стартовал проект «Myrtis», на котором размещено обращение Миртиды 15 языках, в котором она призывает мир объединить усилия в борьбе с брюшным тифом и не допустить новые смерти, которые можно и нужно предотвратить.
Вместе с тем определенные описания проявлений тогдашней болезни в записях ее выдающегося современника Фукидида противоречат известным симптомам брюшного тифа, особенностям его эпидемиологического распространения, что сохраняет среди ученых мнение, что так называемая «Пелопоннесская / Афинская чума V в. до н. э. »была вызвана другой болезнью. Возможно сама Миртида и умерла от брюшного тифа, тогда как другие сограждане — от другой болезни. Ведь в период древних эпидемий встречались случаи смерти и от других заболеваний. А может Миртида была просто хроническим носителем брюшнотифозной сальмонеллы, а погибла вообще от совсем второй причины. Поэтому интерпретировать результаты исследования в Миртиды как имеющие автоматически распространиться на всю эпидемию, пока рано. Результаты были получены при исследовании всего лишь трех зубов, поэтому безоговорочно считать, что тайна «чумы Фукидида» раскрыта, пока преждевременно.
источник