Возбудители брюшного тифа, паратифов
Возбудителя брюшного тифа (S. typhi) выявил впервые немецкий гистолог Эберт в 1880 г., увидевший его при микроскопии гистологических препаратов – срезов селезенки, периферических лимфоузлов и пейеровых бляшек, взятых у умерших от тифа больных. В 1884 г. Гаффки получил чистую культуру возбудителя. В этом же году А. Брион и Х. Кайзер описали возбудителя паратифа А (S. paratyphi A), а Г. Шоттмюллер – возбудителя паратифа В (S. paratyphi В). Этих сальмонелл выделили в чистой культуре и изучили Ашар и Бедсон в 1896 г.
Родовое название связано с именем американского ветеринарного врача Д. Сальмона, который в 1885 г. выделил возбудителя сальмонеллезов (S. choleraesuis) от больных свиней. В 1888 г. Гертнер выделил S. enteritidis из мяса и селезенки коров, погибших от острой пищевой инфекции. В 1890 г. Леффлер, 1893 г. С.С. Мережковский и 1900 г. Даниш обнаружили другого возбудителя S. typhimurium, вызвавшего аналогичные заболевания у человека и у мышей.
В 1934 г. Ф. Кауфман и П. Уайт разработали классификацию сальмонелл по антигенной структуре.
(вызывают заболевания у человека и животных)
S. typhi (палочка Эберта-Гаффки)
S. paratyphi A (палочка Бриона-Кайзера)
S. paratyphi В (палочка Шоттмюллера)
Однако в большинстве учебных пособий и справочников для удобства используется исторически сложившаяся таксономия, рассматривающая серовары, как виды (например, S . typhi , вместо S . enterica подвид enterica серовар Typhi )
Морфология и тинкториальные свойства.
Мелкие грамотрицательные палочки с закругленными концами размером 0,7-1,5?2-5 мкм, в мазках располагаются беспорядочно, подвижны (перетрихи), имеют пили I и II типов, S . typhi – микрокапсулу, спор не образуют.
Факультативные анаэробы, хемоорганогетеротрофы. Не требовательны к условиям культивирования: оптимальная температура роста 370С, значение рН 6,8-7,2, длительность культивирования – 24-48 часа. Хорошо растут на простых питательных средах (МПБ, МПА). В МПБ наблюдается рост в виде диффузного помутнения с последующим образованием осадка. На МПА образуют колонии в S — (средних размеров, гладкие, блестящие, полупрозрачные с голубоватым оттенком) и R -форме, S . paratyphi В и S . enteritidis по краю колоний формируют слизистый валик. В качестве накопительных сред используют желчный и селенитовый бульон. На дифференциально- диагностических средах Эндо, Левина и Плоскирева образуют бесцветные колонии (не ферментируют лактозу). На висмут-сульфитном агаре – колонии черного цвета с металлическим блеском, окруженные черным ободком прокрашенной среды.
Сальмонеллы обладают выраженной ферментативной активностью. Оксидазоотрицательны и каталазоположительны. Реакция Фогеса-Проскауэра отрицательная. Сахаролитическая активность: не расщепляют лактозу и сахарозу; глюкозу, маннит, мальтозу и другие сахара разлагают до кислоты и газа (исключение, S . typhi – до кислоты), по способности разлагать ксилозу и арабинозу различают 4 типа: К+А+; К-А-; К+А-; К-А+. Протеолитические свойства: не образуют индол, желатин не разжижают, образуют H 2 S (исключение, S . paratyphi A ).
Антигенная структура сальмонелл – сложная, имеются О-, Н-, Vi -, М-антигены.
* О – соматический антиген, липополисахарид клеточной стенки, термостабильный, (выдерживает кипячение в течение 2,5 часов, автоклавирование при 1200 С – 30 мин.), чувствительны к формальдегиду, но устойчив к спирту, групповой – согласно классификации Кауфмана-Уайта, семейство делится на 67 серогрупп (А, В, С, Д…). О-АГ состоит из R -ядра и боковой S -цепи, к которой присоединяются сахара – рецепторы (обозначаются цифрами). Общность конечного сахара (по химической природе является 3,6-дидезоксигексозой) является основанием для объединения в серогруппу. Некоторые группы имеют общие О-АГ, но каждая группа содержит один основной антиген: в группе А – 2, в группе В – 4, в группе С – 7, Д – 9…
* Н – жгутиковый антиген, белок флагеллин, термолабильный (разрушается при нагревании до 75-100С, а также под действием соляной кислоты, спирта, протеолитических ферментов), типовой (более 250 сероваров, расположены в алфавитном порядке в таблице Кауфмана-Уайта). У Н-АГ сальмонелл различают 2 фазы: I (специфическая) – различна у серотипов, входящих в одну группу, обозначается строчными латинскими буквами; II (неспецифическая) – содержат в своем составе общие для всей группы компоненты, обозначается арабскими цифрами. Если у серовара присутствуют обе фазы Н-АГ, то его называют двухфазным, если одна – монофазным.
* Vi -АГ – поверхностный полисахаридный антиген S . typhi , являющийся разновидностью К-АГ, термолабильный (разрушается при кипячении за 10 минут), чувствительный к соляной кислоте и спирту, встречается только у вирулентных сальмонелл, препятствует агглютинации О-антисыворотками, является рецептором для бактериофагов.
* М-АГ – слизистый, водонерастворимый, разрушается под действием кислот и спиртов.
* эндотоксин – липополисахарид клеточной стенки, высвобождается при массовой гибели возбудителей, играет основную роль в патогенезе брюшного тифа, оказывая пирогенное и токсическое действие;
* возбудители сальмонеллезов выделят экзотоксины – термолабильный белковый энтеротоксин, сходный с холерогеном и LT -токсином E . coli (увеличивают в клетках эпителия тонкого кишечника содержание цАМФ, что приводит к повышенному выходу воды из клеток и развитию диареи) + цитотоксическое действие, вызывая гибель энтероцитов.
2. Ферменты патогенности: гиалуронидаза, фибринолизин, лецитиназа, муциназа, протеаза, супероксиддисмутаза (инактивирует суперактивные радикалы О2, что придает устойчивость к фагоцитозу).
3. Структурные и химические компоненты клетки:
* белки наружной мембраны – инвазины (обеспечивающие инвазию слизистой и резистентность к фагоцитозу, позволяющую сальмонеллам сохраняться и размножаться внутри фагоцитов);
Резистентность у сальмонелл – достаточно высокая. Выдерживают рН в диапозоне 4-9, в водоемах, сточных водах, почве сохраняют жизнеспособность до 3 месяца, в комнатной пыли – от 80 до 550 дней. Хорошо переносят низкие температуры: во льду сохраняются более 60 дней, в замороженном мясе – 6-13 месяцев (в толще мяса могут сохраняться и после тепловой обработки), размножается в мясном фарше при +50С, в яйцах – до 13 месяцев (при хранении яиц в холодильнике могут проникать через неповрежденную скорлупу и размножаться в желтке), в колбасе – 2-4 месяца, в хлебе – до 3-х месяцев, на овощах и фруктах – 5-10 дней. Хуже выдерживают высокую температуру: при 560 С выдерживают 40-60 минут, при 700 С погибают через 10 минут, при 1000 С – моментально. Чувствительны к дезрастворам в рабочей концентрации (5% фенол, 3% хлорамин, 3% лизол вызывают гибель бактерий через 2-3 минуты) и антибиотикам.
Брюшной тиф (название болезни дал Гиппократ, происходит от греч. typos – туман, спутанное сознание) – острое антропонозное инфекционное заболевание, характеризующееся поражением лимфоидного аппарата тонкого кишечника, бактериемией, выраженной лихорадкой, интоксикацией и розеолезной сыпью. Паратифы А и В сходны по характеру и клиническим проявлениям с брюшным тифом, но протекают более легко.
Сальмонеллезы – группа полиэтиологичных острых зооантропонозных кишечных инфекций, протекающих по типу гастроэнтеритов у взрослых и токсико-септических инфекций у детей.
Источник инфекции: больные и бактерионосители.
Механизм передачи: фекально-оральный (пути: пищевой, водный, контактно-бытовой). Брюшной тиф и паратиф А распространяются чаще водным путем (употребление воды из неглубоких загрязненных водоемов, технических водопроводов, в случаях прорыва канализационных вод). При паратифе В преобладает пищевой путь (заражение чаще происходит через молоко, молочные продукты, кремы, овощные салаты). Бытовой путь реализуется, как правило, через бактерионосителей.
Патогенез и клинические особенности брюшного тифа и паратифов А и В .
1. Стадия внедрения возбудителя: сальмонеллы попадают в организм через рот и преодолев барьеры неспецифической защиты организма, проникают в тонкий кишечник, где происходит их адгезия к энтероцитам за счет пилей I типа.
2. Стадия поражения лимфоидной ткани: поражают пейеровы бляшки тонкого кишечника, в лимфатических фолликулах тонкой кишки сальмонеллы фагоцитируются макрофагами, с которыми проникают сначала в лимфоузлы, затем через грудной проток и в кровь.
3. Бактериемия (конец инкубационного периода): с током крови макрофаги вместе с поглощенными сальмонеллами циркулируют по организму (микроорганизмы могут даже в них размножаться).
4. Интоксикация: под воздействием бактерицидных факторов крови сальмонеллы погибают и при этом высвобождается эндотоксин, обусловливая лихорадку и сильнейшую интоксикацию, которая сохраняется на протяжение всего заболевания. (соответствует периоду выраженных клинических проявлений заболевания, температура тела достигает 39-400С и держится от 4 до 8 недель).
5. Стадия паренхиматозной диффузии: макрофаги с сальмонеллами циркулируют по организму и после гибели фагоцитов микробы могут попасть в различные органы: костный мозг, селезенку, печень, желчный пузырь, кожа и т.д. (воспаление, образование гранулем).
6. Выделительно-аллергическая стадия: вместе с желчью возбудители снова попадают в тонкий кишечник, при повторном контакте с сенсибилизированной лимфоидной тканью развивается гиперчувствительность немедленного типа (феномен Артюса), что приводит к некрозу пейеровых бляшек и образованию язв (кишечные кровотечения, прободение кишечника). По мере накопления антител организм постепенно освобождается от возбудителя – они выделяются со слюной, потом, испражнениями, желчью и мочой.
Инкубационный период – 10-14 дней. Клиника брюшного тифа, паратифов А и В характеризуется циклическим течением и проявляется лихорадкой (повышение температуры тела до 39-400С), интоксикацией, появлением розеолезной сыпи, гепатолиенальным синдромом,нарушениями со стороны нервной (бред, галлюцинации) и сердечно-сосудистой (падение АД, коллапс…) систем. Выздоровление не всегда совпадает с освобождением организма от возбудителей, этот процесс затягивается; 5 % переболевших становятся бактерионосителями.
Патогенез и клинические особенности сальмонеллезов .
Возбудители попадают в организм человека с обсемененными пищевыми продуктами. В желудке происходит частичная гибель сальмонелл. Воротами инфекции являются клетки слизистой тонкого кишечника. Здесь сальмонеллы внедряются между ворсинками, колонизируют и повреждают их. Это вызывает умеренное воспаление слизистой оболочки. Эндотоксин, выделяющийся при разрушении сальмонелл, обуславливает интоксикацию. Вырабатываемый сальмонеллами экзотоксин (энтеротоксин) вызывает диарею и рвоту, нарушение водно-солевого обмена и обезвоживание организма. Он обладает также цитотоксическим действием, вызывая гибель энтероцитов. Сальмонеллы проникают в подлежащие ткани слизистой оболочки, транспортируются через нее в макрофаги и могут поступать в лимфу и кровь, вызывая бактериемию и генерализацию инфекционного процесса.
Короткий инкубационный период – 12-24 часа. Начала заболевания – острое: озноб, повышение температуры до 390С, интоксикация (головная боль, слабость, тошнота), боли в животе, диспептические расстройства (рвота, понос), признаки обезвоживания организма, падение АД. Заболевание протекает обычно в течение 3-5 дней и заканчивается выздоровлением. При генерализованных формах сальмонеллез протекает более тяжело и длительно. Как субклиническую форму сальмонеллеза рассматривают бактерионосительство (острое – до 3 месяцев, хроническое – более 3 месяцев).
Постинфекционный иммунитет при брюшном тифе и паратифах – гуморальный, напряженный, длительный (не менее 15-20 лет, часто пожизненный). Образуются антитела к О-, Н-, Vi-антигенам:
* Первыми к концу 1-й недели заболевания появляются антитела к О-АГ, достигая максимума к периоду разгара (14-15 дней), а затем исчезают.
* Антитела к Н-АГ появляются к концу 2-й недели, достигая максимума в период реконвалесценции и длительно сохраняясь в организме после перенесенного заболевания.
* Антитела к Vi-АГ обнаруживаются у бактерионосителей брюшного тифа.
Постинфекционный иммунитет при сальмонеллезах – гуморальный и клеточный, типоспецифический, ненапряженный и недлительный, опосредован SIgA.
Микробиологические исследования при брюшном тифе и паратифе
Исследуемый материал: выбор материала для исследования при брюшном тифе и паратифах определяется стадией заболевания (инкубационный период – испражнения, продромальный период, 1-я неделя заболевания – кровь на посев, разгар заболевания и период реконвалесценции, с конца 2-ой недели – моча, испражнения, желчь, соскоб из розеол, костный мозг…, кровь на серодиагностику), при сальмонеллезах – испражнения, рвотные массы, промывные воды желудка, пищевые продукты, кровь.
1. Бактериоскопический метод.
2. Бактериологичекий метод (основной).
* Реакция Видаля (развернутая РА с О- и Н-антигенами);
* РНГА с эритроцитарными О-, Н-, Vi-диагностикумами;
4. Молекулярно-биологический метод (ПЦР, ДНК-зонды).
5. Аллергологический метод (кожно-аллергическая проба с эбертином).
Специфическая профилактика проводится по эпидпоказаниям:
— Вакцина ТАБТе – химическая сорбированная вакцина (содержит полные антигены брюшнотифозные, паратифозные А и В, столбнячный анатоксин);
— Брюшнотифозная спиртовая вакцина, обогащенная Vi- антигеном;
Неспецифическая профилактика : ранняя диагностика и изоляция больных, дезинфекция в очаге инфекции, выявление бактерионосителей, соблюдение санитарного режима в детских учреждениях, предприятиях питания, санитарно-бактериологический контроль за работой систем централизованного и нецентрализованного водоснабжения.
Лечение : ХТП и антибиотики; при сальмонеллезах применяется, в основном, патогенетическая терапия, направленная на нормализацию ВЭБ (антибиотики назначают только при генерализованных формах); спецефическое лечение – брюшнотифозные и сальмонеллезные бактериофаги.
источник
Сальмонеллы (род Salmonella)
Брюшной тиф как самостоятельную нозологическую единицу впервые попытался выделить русский врач А. Г. Пятницкий еще в 1804 г. Род получил название в честь Д. Сальмона, который в 1885 г описал микроб, выделенный из свиньи и известный в настоящее время под названием S. Choleraesuis.
Возбудители брюшного тифа и паратифов (S. Typhi, S. Paratyphi В, S. Paratyphi A) Род включает лишь один вид — Salmonella enterica (S. enteritidis) и семь подвидов – патогенен для теплокровных лишь — S. Cholerae-suis. Для удобства будет использоваться не совсем корректная таксономия, раасматривающая серовары как виды (например – S. Typhi вместо Salmonella enterica, подвид Cholerae-suis серовар Typhi)
Брюшной тиф представляет собой острую антропонозную системную инфекцию, характеризующуюся циклическим течением, поражением лимфатического аппарата тонкого кишечника, бактериемией, лихорадкой, сыпью и интоксикацией организма.
Возбудителем брюшного тифа является S. Typhi, впервые обнаруженный К. Эбертом в 1880 г. в срезах селезенки, лимфатических узлов и пейеровых бляшек людей, умерших от брюшного тифа. В 1884 г. Т. Гаффки выделил возбудитель в чистой культуре. S. Paratyphi А, описанный А. Брионом и X. Кайзером, и S. Paratyphi В, описанный Г. Шоттмюллером, являются возбудителями паратифов, которые схожи с брюшным тифом по патогенезу, клиническим проявлениям и эпидемиологии заболевания. Брюшной тиф и паратифы являются антропонозами, т. е. S. Typhi, S. Paratyphi A, S. Paratyphi В вызывают заболевание только у человека.
Морфологические и Культуральные свойства. Подвижные грамотрицательные палочки, размером 0,7×1,5×2—5 мкм. Капсулу не образуют. Хорошо растут на простых питательных и желчесодержащих средах. На плотных средах могут образовывать колонии в R- и S-формах, на жидких — S-диффузное помутнение, R-осадок. Колонии в S-форме средних размеров, гладкие, блестящие, полупрозрачные, с голубоватым оттенком, R-сухие шероховатые. Серовар S. Schottmuelleri (S. Paratyphi В) при росте на плотных средах образует слизистые валики (феномен валообразования), колонии S. Typhi, имеющие Vi-Аг, мутные. На средах Эндо колонии всех трех сальмонелл бесцветны или розоватые, на агаре Плоскерева – бесцветные и выглядят более плотными и мутными , на висмут-сульфитном агаре – черно-коричневые с металлическим блеском, среда под колонией окрашивается в черный цвет (парататиф А – коричнево-зеленоватые). Жидкими средами обогащения при посеве крови является желчный бульон, при посеве содержащих дополнительную флору материалов (фекалий, желчи, мочи) — селенитовый бульон (пептон+NaHSeO3-ингибитор контаминирующей флоры и т. д.). На лакгозосодержащих дифференциальных средах образуют бесцветные колонии, на висмут-сульфитном агаре — колонии черного цвета.
Обладают выраженной биохимической активностью. По биохимическим свойствам род однороден. Основные биохимические свойства, необходимые для идентификации:
ф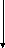
отсутствие ферментации лактозы,
— отсутствие индолообразования (в 1% пептонную воду) (среда Хисса). Среда Хисса – пептон+индикатор Андраде +набор углеводов-бесцветны, при образовании к-ты – малиновый цвет. Могут быть добавлены лошадиная или бычья сыворотка, при кислотообразовании – последняя сворачивается
S. Typhi по способности ферментировать ксилозу и арабинозу подраздиляются на 4 биохимических типа.
Антигенная структура и классификация.
— К-антигеном (Некоторые сальмонеллы) – разновидность – Vi-Аг
В связи с тем, что по основным биохимическим свойствам представители рода Salmonella однотипны, дифференциация внутри рода проводится по антигенной структуре.
Имеется несколько классификаций сальмонелл. Наиболее старой является классификация по Кауфману—Уайту. В основе этой классификации лежит подразделение сальмонелл на:
—серогруппы по общности строения О-антигена
-внутри серогруппы — на серовары, в соответствии с различиями в строении Н-антигена.
О-антиген состоит из R-ядра и боковой S-цепи. К S-цепи присоединяются сахара, которые называют рецепторами и обозначают цифрами. Критерием для объединения в серогруппу является общность конечного сахара, который по химической природе является 3,6 -д идезоксигексозой.
Н-антиген является двухфазным. Это связано с тем, что его синтез кодируется двумя независимыми генами, работа одного из которых исключает работу другого. Поэтому в каждой клетке может быть синтезирован только один белок (фаза). Первая фаза обозначается буквами, она считается специфической, вторая фаза — цифрами, ее принято считать неспецифической.
В таблице Кауфмана—Уайта (табл. 16.12) внутри серогруппы серовары расположены в алфавитном порядке. В прежних классификациях каждый серовар соответствовал виду, которых насчитывалось более 2500.
Согласно последней классификации, род Salmonella состоит из двух видов — вида S. enterica, в который включены все сальмонеллы, являющиеся возбудителями человека и теплокровных животных, и вида & bongori, который подразделяется на 10 сероваров и включает в себя сальмонеллы, изолированные от холоднокровных животных.
Вид S. enterica разделен на 6 подвидов, которые в свою очередь подразделены на серовары. Все серовары подвида enterica имеют названия, которые соответствуют прежним видовым названиям. Например: S. typhi — S. Typhi.
Некоторые серовары сальмонелл, в частности S. Typhi, имеют полисахаридный Vi-антиген, являющийся разновидностью К-антигена. Vi-антиген по химической структуре является полимером N-ацетилгалактозоаминоуроновой кислоты. Этот антиген является рецептором для бактериофагов. По спектру чувствительности к набору Vi-фагов устанавливается фаговар S. Typhi, который необходим для эпидемического анализа вспышек брюшного тифа с целью определения источника инфекции. Vi-антиген (находясь более поверхностно) может придавать бактерии явление О-инагглютинабельности. Напротив утрата Vi-антигена ведет к высвобождения О-Аг и восстановлению О-агглютинации, но при этом утрачивается Vi- агглютинация. Количественное содержания Vi-антигена может сильно варьировать, поэтому Кауфман предложил классифицировать S. Typhi по содержанию Vi-антигена на три группы:
Патогенность и патогенез. Сальмонеллы обладают множественностью факторов патогенности, многие из которых еще недостаточно изучены. Совокупность действия факторов патогенности обеспечивает сальмонеллам трансцитоз, т. е. инвазию слизистой через М-клетки, а также резистентность к фагоцитозу, позволяющую сальмонеллам сохраняться и размножаться внутри фагоцитов. Трансцитоз обеспечивается белками секреторной системы 3 типа, синтез которых детерминируется «островком патогенности 1», среди которых имеется белок наружной мембраны инвазии. Особенность синтеза этих белков заключается в том, что он индуцируется в среде с высоким осмотическим давлением, соответствующим таковому в тонком кишечнике.
Резистентность к фагоцитозу обеспечивается многими факторами. В этом процессе принимают участие продукты генов, расположенных на «островке патогенности 2», синтез которых индуцируется внутрифагоцитарным окружением. Установлено, что в формировании антифагоцитарной активности сальмонелл принимает также участие фермент су-пероксиддисмутаза, инактивирующая О2-ра-дикалы.
Все сальмонеллы обладают эндотоксином, который вызывает развитие лихорадки в случае бактериемии, вызванной сальмонеллами. При достижении критической концентрации эндотоксин активирует каскад арахидоновои кислоты в тканях. Некоторые сальмонеллы образуют белковый энтеротоксин, который обладает гомологией с холерным энтероток-сином и LT-токсином ЭТКП.
Попав после перорального заражения в тонкий кишечник, сальмонеллы инвазиру-ют трансцитозом слизистую кишечника через М-клетки без повреждения слизистой. Из М-клеток сальмонеллы транспортируются в субэпителиальное пространство, где захватываются макрофагами и привносятся в прилегающие к М-клеткам пейеровы бляшки, где, размножаясь в макрофагах, формируют первичный очаг инфекции
Резистентность. Сальмонеллы устойчивы к воздействию факторов внешней среды. Выдерживают рН в диапазоне 4—9; в водоемах, сточных водах, почве сохраняют жизнеспособность до 3 месяцев, в комнатной пыли — от 80 до 550 дней. Хорошо переносят низкие температуры. В зараженных продуктах сохраняются:
в колбасе — 3 месяца, в замороженном мясе и яйцах — до 1 года, на овощах и фруктах — 5—10 дней. При нагревании до 56 «С сальмонеллы гибнут в течение 45—60 мин, температура 100 °С убивает их мгновенно. Растворы дезинфицирующих веществ (5% фенол, 3% хлорамин, 3% лизол) убивают сальмонеллы в течение 2—3 мин. При неблагоприятных условиях сальмонеллы могут переходить в некультиви-руемую форму.
Вызываемые заболевания. В зависимости от источника инфекции, путей передачи и особенностей патогенеза и форм проявления инфекционного процесса, среди заболеваний, вызываемых сальмонеллами, различают: брюшной тиф и паратифы, сальмонеллезы, госпитальный (нозокомиальный) сальмонеллез.
Источником инфекции является больной или бактерионоситель, которые выделяют возбудитель во внешнюю среду с испражнениями, мочой, слюной. Возбудители этих инфекций, как и другие сальмонеллы, устойчивы во внешней среде, сохраняются в почве, воде. Благоприятной для них средой являются пищевые продукты (молоко, сметана, творог, мясной фарш, студень), в которых сальмонеллы способны размножаться.
1.-водным путем, играющим в настоящее время существенную роль,
Заражающая доза равняется приблизительно 1000 клеток. Естественная восприимчивость людей к возбудителям тифа и паратифа высокая.
Патогенез и клиника. Сформировав первичный очаг инфекции в пейеровых бляшках, после инвазии трансцитиозом слизистой тонкого кишечника, возбудители тифа и паратифов вызывают их воспаление с развитием лимфаденита. В результате воспаления нарушается их барьерная функция, и сальмонеллы попадают в кровь, вызывая бактериемию. Это совпадает с концом инкубационного периода, который длится 10—14 суток. Во время бактериемии, которая сопровождает весь лихорадочный период, возбудители тифа и паратифов с током крови разносятся по организму, оседая в ретикулоэндотелиальных элементах паренхиматозных органов: печени, селезенке, легких, а также в костном мозге, где размножаются в макрофагах, а также в желчном пузыре, куда они попадают по желчным протокам, диффундируя из Купферовских клеток печени. К концу 2-й недели заболевания возбудитель начинает выделяться из организма с мочой, путом, материнским молоком, слюной. Накапливаясь в желчном пузыре, сальмонеллы вызывают его воспаление и с током желчи реинфицируют тонкий кишечник. Повторное внедрение сальмонелл в сенсибилизированные пейеровы бляшки приводит к развитию в них гиперергического воспаления по типу феномена Артюса, их некрозу и изъязвлению, что может привести к кишечному кровотечению и прободению кишечной стенки. Выделяются сальмонеллы из организма с испражнениями и мочой.
Клиника брюшного тифа и паратифов характеризуется циклическим течением и проявляется лихорадкой (повышение температуры до 39—40°), интоксикацией, появлением розеолезной сыпи, нарушениями со стороны нервной системы (бред, галлюцинации) и сердечно-сосудистой системы (падение кровяного давления, коллапс и др.). Паратифы протекают в основном так же, как брюшной тиф.
Иммунитет. Иммунитет после перенесенного заболевания напряженный и длительный. Протективный иммунный ответ обеспечивается синергичным действием клеточного иммунного ответа, в котором ведущая роль принадлежит активированным макрофагам.
Гуморальный иммунитет самостоятельно не обладает протективной активностью, а является свидетелем инфекционного процесса.
-Причем первыми к концу 1-й недели заболевания появляются антитела к О-антигену, которые максимальных титров достигают к разгару заболевания, а затем исчезают.
—Антитела к Н-антигену появляются в период реконвалесценции и у привитых лиц и длительно сохраняются.
— У бактерионосителей брюшного тифа обнаруживаются антитела к Vi-антигену. Возникновение бактерионосительства связано с функциональной недостаточностью макрофагов.
Микробиологическая диагностика. Учитывая цикличность течения заболеваний, материал для исследования и метод исследования определяются стадией течения болезни.
В первые дни заболевания наблюдается бактериемия, поэтому на 1-й неделе заболевания и в течение всего лихорадочного периода используют метод гемокультуры: посев крови в желчный бульон с последующим пересе-
вом на дифференциально-элективные среды (Эндо, Плоскирева, висмут-сульфитный агар). Выделенную культуру идентифицируют по биохимическим свойствам и антигенной структуре, а выделенную культуру S. Typhi типируют Vi-фагами для определения источника инфекции. С конца 2-й недели заболевания производят выделение копро-, урино- и биликультур, т. е. материалом для исследования являются моча, испражнения, желчь.
Начиная со 2-й недели заболевания проводят серологическое исследование с целью определения наличия и типа антител. Исследование проводится постановкой РНГА. РНГА ставят с О-, Н- и Vi-диагностикумами. Положительным считают диагностический титр не менее 1:200. Ранее для серологической диагностики применяли развернутую реакцию агглютинации Видаля. В настоящее время серологическое исследование проводят также постановкой ИФА.
диагностика бактерионосительства- Диагностика бактерионосительства. Единственным доказательством бактерионосительства ляются выделение от носителя культур . Материалом исследования являются дуоденальное содержимое, испражнения и моча. Сложность проблемы чается в том, что у носителей возбудитель не всегда выделяется е этими субстратами, бывают па; и довольно продолжительные. В качестве вспомогательных методов, которые позволяют сузить обследуемых лиц, используют серологические реакции (одновременное обнаружение О, Н-, Vi-или О-, Vi-антител говорит о возможном присутствии возбудителя в организме) и аллергическую пробу с Vi-тифином. Последний содержит Vi-антиген, который при взаимодействии с Vi-aнтителом дает местную аллергическую реакцию в виде покраснения и припухлости в течение 20-30 минут Положительная реакция с Vi-тифином свидетельствует о наличии в организме Vi-антител и о возможности носительства. Исследование тампонов одновременно забрасываемых в канализационные люки населенного пункта.
Профилактика и Лечение. Для специфической профилактики брюшного тифа используют брюшнотифозную сорбированную и брюшнотифозную спиртовую, обогащенную Vi-антигеном, вакцины. Для профилактики, по эпидемическим показаниям, лицам, которые проживают совместно с больным и которые употребляли продукты и воду, зараженные или подозрительные на заражение S. Typhi, назначают сухой брюшнотифозный бактериофаг.
Лечение — этиотропная антибиотикотерапия.
Не специфическая профилактика включает: санитарно-бактериологический контроль за системами водоснабжения, соблюдение санитарно-гигиенических правил при приготовлении пищи, выявление бактерионосителей среди работников пищеблоков, торговли, своевременное выявление и изоляцию больных.
источник
Брюшной тиф и паратифы А и В — — инфекционные болезни, вызываемые соответственно Salmonella typhi, Salmonella paratyph( Salmonella schottmuelleri, сопровождающиеся сходными патогенетическими и клиническими проявлениями, характеризующиеся поражением лимфатической системы кишечника, выраженной интоксикацией. Название рода Salmonella связано с именем Д. Сальмона.
Таксономия. Возбудители брюшного тифа и паратифов А и В относятся к отделу Gracilicutes, семейству Enterobacteriaceae, роду Salmonella, включающему более 2000 видов.Морфология и тинкториальные свойства. Сальмонеллы – мелкие, длиной 2.3 мкм, шириной 0,5-0,7 мкм, грамотрицатель-ные палочки с закругленными концами (см. рис.ЮЛ). В мазках располагаются беспорядочно. Не образуют спор, имеют микрокапсулу, перитрихи.
Культивирование. Сальмонеллы – факультативные анаэробы. Они неприхотливы и растут без всяких особенностей на простых питательных средах при температуре 37ºС и рН среды 7,2-7,4. Эдективной средой является, например, желчный бульон. При диагностике брюшного тифа, как и других кишечных инфекций, используют дифференциально-диагностические среды: Эндо, Левина, висмут-сульфитный агар и др.
Ферментативная активность. Биохимическая активность сальмонелл достаточно высока, но они обладают меньшим набором ферментов, чем Е. coli, в частности не сбраживают лактозу. S. typhi менее активна, чем возбудители паратифов: она ферментирует ряд углеводов без образования газа.
Антигенные свойства. Сальмонеллы имеют О- и Н-антигены, состоящие из ряда фракций, или рецепторов. Каждый вид имеет определенный набор фракций. Ф. Кауфман и П.Уайт предложили схему классификации сальмонелл по антигенной структуре, в основу которой положено строение О-антигена. Все виды сальмонелл, имеющие общий, так называемый групповой, рецептор О-антигена, объединены в одну группу. Таких групп насчитывается в настоящее время 65. В схеме также указано строение Н-антигена. Некоторые виды сальмонелл, в том числе S. typhi, имеют поверхностный Vi-антиген – антиген вирулентности, с которым связана устойчивость бактерий к фагоцитозу.
Факторы патогенности. Сальмонеллы образуют эндотоксин, оказывающий энтеротропное, нейротропное и пирогенное действие. Белки наружной мембраны обусловливают адгезивные свойства, устойчивость к фагоцитозу связана с микрокапсулой.
Резистентность. Сальмонеллы довольно устойчивы к низкой температуре – в холодной чистой воде могут сохраняться до полутора лет; очень чувствительны к дезинфицирующим средствам, высокой температуре, УФ-лучам. В пищевых продуктах (мясе, молоке и др.) сальмонеллы могут не только долго сохраняться, но и размножаться.
Эпидемиология. Источником брюшного тифа и паратифов являются больные люди и носители. Механизм передачи инфекции – фекально-оральный. Преобладает водный путь передачи, реже встречаются пищевой и контактно-бытовой пути. Брюшной тиф и паратифы – заболевания, которые регистрируются в разных странах мира. Чаще болеют люди в возрасте от 15 до 30 лет. Наиболее высокая заболеваемость отмечается летом и осенью.
Патогенез. Возбудители попадают в организм через рот, достигают тонкой кишки, в лимфатических образованиях которой размножаются, а затем попадают в кровь. Током крови они разносятся по всему организму, внедряясь в паренхиматозные органы (селезенку, печень, почки, костный мозг). При гибели бактерий освобождается эндотоксин, вызывающий интоксикацию. Из желчного пузыря, где сальмонеллы могут длительно, даже в течение всей жизни сохраняться, они вновь попадают в те же лимфатические образования тонкой кишки. В результате повторного поступления сальмонелл может развиться своеобразная аллергическая реакция, проявляющаяся в виде воспаления, а затем некроза лимфатических образований. Выводятся сальмонеллы из организма с мочой и испражнениями.
Клиническая картина. Клинически брюшной тиф и паратифы не отличимы. Инкубационный период продолжается 12.14 дней. Заболевание обычно начинается остро с повышения температуры тела, проявления слабости, утомляемости, нарушаются сон, аппетит. Для брюшного тифа характерны помрачение сознания (от греч. typhus – дым, туман), бред, галлюцинации, наличие сыпи. Очень тяжелыми осложнениями заболевания являются перитонит, кишечное кровотечение в результате некроза лимфатических образований тонкой кишки.
Иммунитет. После перенесенного заболевания вырабатывается прочный и продолжительный иммунитет.
Микробиологическая диагностика. В качестве материала для исследования используют кровь, мочу, испражнения. Основным методом диагностики является бактериологический, завершающийся внутривидовой идентификацией выделенной чистой культуры возбудителя – определением фаговара. Применяют также серологический метод – реакцию агглютинации Видаля, РНГА.
Лечение. Назначают антибиотики. Применяют также иммуно-антибиотикотерапию (глава 7).
Профилактика. Для профилактики проводят санитарно-гигиенические мероприятия, а также используют вакцинацию в районах с неблагополучной эпидемической обстановкой. Применяют брюшнотифозную химическую и брюшнотифозную спиртовую вакцины, последняя обогащена Vi-антигеном. Для экстренной профилактики в очагах инфекции используют брюшнотифозный бактериофаг (в виде таблеток с кислотоустойчивой оболочкой и в жидком виде).
Не нашли то, что искали? Воспользуйтесь поиском:
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Брюшной тиф — тяжелое острое инфекционное заболевание, характеризующееся глубокой общей интоксикацией, бактериемией и специфическим поражением лимфатического аппарата тонкого кишечника. Интоксикация проявляется сильной головной болью, помрачением сознания, бредом (тиф от греч. typhos — туман). Брюшной тиф как самостоятельную нозологическую единицу впервые попытался выделить русский врач А. Г. Пятницкий еще в 1804 г., но окончательно это сделал в 1822 г. Р. Бретонно, который дифференцировал эту болезнь от туберкулеза кишечника и высказал предположение о контагиозной природе брюшного тифа.
Возбудитель брюшного тифа — Salmonella typhi — был обнаружен в 1880 г. К. Эбертом, а выделен в чистой культуре в 1884 г. К. Гаффки. Вскоре были выделены и изучены возбудители паратифов А и В — S. paratyphi А и S. paratyphi В. Род Salmonella включает в себя большую группу бактерий, но только три из них — S. typhi, S. paratyphi А и S. paratyphi В — вызывают заболевание у человека с клинической картиной брюшного тифа. Морфологически они неразличимы — короткие грамотрицательные палочки с закругленными концами, длиной 1-3,5 мкм, диаметром 0,5-0,8 мкм; спор и капсул не образуют, обладают активной подвижностью (перитрихи). Содержание Г + Ц в ДНК составляет 50-52 мол %.
Возбудители брюшного тифа и паратифов — факультативные анаэробы, температурный оптимум для роста 37 °С (но могут расти в диапазоне от 10 до 41 °С), рН 6,8-7,2; не требовательны к питательным средам. Рост на бульоне сопровождается помутнением, на МПА образуются нежные круглые, гладкие, полупрозрачные колонии диаметром 2-4 мм. Однако колонии S. typhi, имеющие Vi-антиген, мутные. Колонии S. paratyphi В более грубые, через несколько дней у них по периферии формируются своеобразные валики. На средах Эндо колонии всех трех сальмонелл бесцветны, на висмут-сульфитагаре — черного цвета. В случае диссоциации на плотных средах вырастают колонии R-формы. Избирательной средой для возбудителей брюшного тифа и паратифов является желчь или желчный бульон.

Возбудители брюшного тифа и паратифов дают положительную реакцию с MR, не образуют индола, не разжижают желатин, восстанавливают нитраты в нитриты, не образуют ацетоина. S. typhi не растет на голодном агаре с цитратом. Основные биохимические различия между возбудителями брюшного тифа и паратифов заключаются в том, что S. typhi ферментирует глюкозу и некоторые другие углеводы с образованием только кислоты, a S. paratyphi А и S. paratyphi В — с образованием и кислоты, и газа.
S. typhi по способности ферментировать ксилозу и арабинозу подразделяют на четыре биохимических типа: I, II, III, IV.

Сальмонеллы имеют О- и Н-антигены. По О-антигенам они разделяются на большое количество серогрупп, а по Н-антигенам — на серотипы (подробнее о серологической классификации сальмонелл см. в следующем разделе). S. typhi, S. paratyphi А и S. paratyphi В отличаются друг от друга как по О-антигенам (относятся к разным серогруппам), так и по Н-антигенам..
В 1934 г. А. Феликс и Р. Питт установили, что S. typhi помимо О- и Н-антигенов имеет еще один поверхностный антиген, который они назвали антигеном вирулентности (Vi-антигеном). По химической природе Vi-антиген отличается от О- и Н-антигенов, он состоит из трех различных фракций, но его основу составляет сложный полимер N-ацетилгалактозаминоуроновая кислота с м. м. 10 МД. Vi-антиген, как правило, обнаруживается у свежевыделенных культур, но он легко утрачивается под влиянием различных факторов (в частности, при выращивании при температуре выше 40 °С и ниже 20 °С, на средах с карболовой кислотой и т. п.), при длительном хранении культур, разрушается при температуре 100 °С в течение 10 мин. Поскольку он располагается более поверхностно, чем О-антиген, его наличие препятствует агглютинации культуры S. typhi О-специфической сывороткой, поэтому такую культуру обязательно проверяют в реакции агглютинации с Vi-сывороткой. Напротив, утрата Vi-антигена ведет к освобождению О-антигена и восстановлению О-агглютинации, но при этом утрачивается Vi-агглютинация. Количественное содержание Vi-антигена у S. typhi может сильно варьировать, поэтому Ф. Кауффманн предложил классифицировать S. typhi по содержанию Vi-антигена на три группы:
- чистые v-формы (нем. viel — много);
- чистые w-формы (нем. wenig — мало);
- промежуточные vw-формы.
Обнаружены 3 необычных мутанта S. typhi: Vi-I — R-форма, клетки лишены Н- и О-антигенов, но стойко сохраняют Vi-антиген; О-901 — лишен Н- и Vi-антигенов; Н-901 — содержит О- и Н-антигены, но лишен Vi-антигена. Все три антигена: О-, Н- и Vi- имеют выраженные иммуногенные свойства. Наличие Vi-антигенов позволяет подвергать культуры S. typhi фаготипированию. Есть 2 типа фагов, лизирующих только те культуры, которые содержат Vi-антиген: Vi-I — универсальный фаг, лизирует большинство Vi-содержащих культур S. typhi; и набор Vi-II-фагов, лизирующих избирательно культуры S. typhi. Впервые это было показано в 1938 г. Дж. Крейджем и К. Иеном. С помощью Vi-фагов II типа они разделили S. typhi на 11 фаготипов. К 1987 г. было выявлено уже 106 различных Vi-фаготипов S. typhi. Чувствительность их к соответствующим фагам является стабильным признаком, поэтому фаготипирование имеет важное эпидемиологическое значение.
Разработаны также схемы фаготипирования S. paratyphi А и S. paratyphi В, по которым они разделяются на десятки фаготипов. Существенно, что фаготипы сальмонелл могут ни по каким другим признакам не отличаться друг от друга.

Возбудители брюшного тифа и паратифов во внешней среде (вода, почва, пыль) сохраняются, в зависимости от условий, от нескольких дней до нескольких месяцев. В проточной воде могут выживать до 10 дней, в застойной — до 4 нед., на овощах и фруктах — 5-10 дней, на посуде — до 2 нед., в масле, сыре — до 3 мес, во льду — до 3 мес. и больше; нагревание при температуре 60 °С убивает через 30 мин, а кипячение — мгновенно. Обычные химические дезинфектанты убивают их через несколько минут. Содержание в водопроводной воде активного хлора в дозе 0,5-1,0 мг/л или озонирование воды обеспечивают ее надежное обеззараживание как от сальмонелл, так и от других патогенных кишечных бактерий.
Важнейшей биологической особенностью возбудителей брюшного тифа и паратифов А и В является их способность противостоять фагоцитозу и размножаться в клетках лимфоидной системы. Экзотоксинов они не образуют. Основным фактором патогенности их, помимо Vi-антигена, является эндотоксин, отличающийся необычно высокой токсичностью. Такие факторы патогенности, как фибринолизин, плазмокоагулаза, гиалуронидаза, лецитиназа и т. п., обнаруживаются у возбудителей брюшного тифа и паратифов очень редко. С наибольшей частотой встречается ДНК-аза (у 75-85 % изученных культур S. typhi и S. paratyphi В). Установлено, что штаммы S. typhi, имеющие плазмиду с м. м. 6 МД, обладают более высокой вирулентностью. Поэтому вопрос о факторах патогенности этих сальмонелл остается еще мало изученным.

Прочный, продолжительный, повторные заболевания брюшным тифом и паратифами бывают редко. Иммунитет обусловлен появлением антител к Vi-, О- и Н-антигенам, клеток иммунной памяти и повышением активности фагоцитов. Поствакцинальный иммунитет, в отличие от постинфекционного, непродолжителен (около 12 мес).
Источником брюшного тифа и паратифа А является только человек, больной или бактерионоситель. Источником паратифа В, кроме человека, могут быть и животные, в том числе птицы. Механизм заражения — фекально-оральный. Заражающая доза S. typhi 105 клеток (вызывает заболевание 50 % добровольцев), заражающие дозы сальмонелл паратифов А и В значительно выше. Заражение происходит главным образом в результате прямого или непрямого контакта, а также через воду или пищу, особенно молоко. Наиболее крупные эпидемии вызывало инфицирование возбудителями водопроводной воды (водные эпидемии).

Инкубационный период при брюшном тифе 15 дней, но он может варьировать от 7 до 25 дней. Это зависит от заражающей дозы, вирулентности возбудителя и иммунного статуса больного. Патогенез и клиническая картина брюшного тифа и паратифов А и В очень сходны. В развитии болезни четко выявляются следующие стадии:
- стадия вторжения. Возбудитель через рот проникает в тонкий кишечник;
- через лимфатические пути сальмонеллы проникают в лимфоидные образования подслизистой оболочки тонкого кишечника (пейеровы бляшки и солитарные фолликулы) и, размножаясь в них, вызывают лимфангоит и лимфаденит (своеобразные брюшно-тифозные гранулы);
- бактериемия — выход возбудителя в большом количестве в кровь. Стадия бактериемии начинается в конце инкубационного периода и может (в отсутствие эффективного лечения) продолжаться в течение всей болезни;
- стадия интоксикации наступает вследствие распада бактерий под действием бактерицидных свойств крови и высвобождения эндотоксинов;
- стадия паренхиматозной диффузии. Из крови сальмонеллы поглощаются макрофагами костного мозга, селезенки, лимфатических узлов, печени и других органов. В большом количестве возбудитель брюшного тифа накапливается в желчных ходах печени и в желчном пузыре, где он находит благоприятные условия для своего размножения и где бактерицидные свойства крови ослаблены влиянием желчи;
- выделительно-аллергическая стадия. По мере формирования иммунитета начинается процесс освобождения от возбудителя. Этот процесс осуществляют все железы: слюнные, кишечника, потовые, молочные (во время кормления ребенка), мочевыделительная система и особенно активно — печень и желчный пузырь. Выделяющиеся из желчного пузыря сальмонеллы опять поступают в тонкий кишечник, откуда часть их выделяется с испражнениями, а часть вторгается вновь в лимфатические узлы. Вторичное внедрение в уже сенсибилизированные узлы вызывает в них гиперергическую реакцию, которая проявляется в виде некроза и образования язв. Эта стадия опасна возможностью прободения стенки кишечника (язв), внутреннего кровотечения и развития перитонита;
- стадия выздоровления. Процесс заживления язв происходит без возникновения обезображивающих рубцов на местах, очистившихся от некротических налетов.
В свою очередь, в клинической картине болезни различают следующие периоды:
- I начальная стадия — stadium incrementi (1-я неделя): постепенное повышение температуры до 40-42 °С, нарастание интоксикации и других проявлений болезни.
- II — стадия максимального развития всех симптомов — stadium acme (2-3-я недели болезни): температура держится на высоком уровне;
- III — стадия спада болезни — stadium decrementi (4-я неделя болезни): постепенное снижение температуры и ослабление проявления других симптомов;
- IV — стадия выздоровления.
На 8-9-й день болезни, а иногда и позднее, у многих больных появляется розеолезная сыпь на коже живота, груди и спины. Появление сыпи (мелких красных пятен) является следствием местных продуктивно-воспалительных процессов аллергической природы в поверхностных слоях кожи около лимфатических сосудов, которые в изобилии содержат возбудителя болезни. Клиническое выздоровление не всегда совпадает с бактериологическим. Примерно 5 % переболевших становятся хроническими носителями сальмонелл тифа или паратифов. Причины, лежащие в основе длительного (более 3 мес, а иногда многие годы) носительства сальмонелл, остаются неясными. Известное значение в формировании носительства играют местные воспалительные процессы в желчевыводящих (иногда в мочевыводящих) путях, которые часто возникают в связи с тифо-паратифозными инфекциями или обостряются в результате этих инфекций. Однако не менее важную роль в формировании длительного носительства сальмонелл брюшного тифа и паратифов А и В играет L-трансформация их. L-формы сальмонелл утрачивают Н-, частично 0-и Vi-антигены, располагаются, как правило, внутриклеточно (внутри макрофагов костного мозга), поэтому становятся не доступными ни для химиопрепаратов, ни для антител и могут длительно персистировать в организме переболевшего человека. Возвращаясь в исходные формы и полностью восстанавливая свою антигенную структуру, сальмонеллы вновь становятся вирулентными, вновь проникают в желчные ходы, вызывают обострение процесса бактерионосительства, выделяются с испражнениями, а такой носитель становится источником заражения для окружающих. Не исключено также, что формирование бактерионосительства зависит от какого-то дефицита иммунной системы.
Самым ранним и основным методом диагностики брюшного тифа и паратифов является бактериологический — получение гемокультуры или миелокультуры. С этой целью исследуют кровь или пунктат костного мозга. Кровь лучше засевать на среду Рапопорт (желчный бульон с добавлением глюкозы, индикатора и стеклянного поплавка) в соотношении 1:10 (на 10 мл среды 1 мл крови). Посев следует инкубировать при температуре 37 С не менее 8 дней, а с учетом возможного наличия L-форм — до 3-4 нед. Для идентификации выделенной культуры сальмонелл используют (с учетом их биохимических свойств) диагностические адсорбированные сыворотки, содержащие антитела к антигенам 02 (S. paratyphi А), 04 (S. paratyphi В) и 09 (S. typhi). Если выделенная культура S. typhi не агглютинируется 09-сывороткой, ее необходимо проверить с Vi-сывороткой.
Для выделения S. typhi можно использовать экссудат, полученный путем скарификации розеол — вырастают розеолокультуры.
Бактериологическое исследование испражнений, мочи и желчи проводят для подтверждения диагностики, контроля бактериологического выздоровления при выписке реконвалесцентов и для диагностики бактерионосительства. В этом случае материал предварительно засевают на среды обогащения (среды, содержащие химические вещества, например селенит, которые угнетают рост Е. coli и других представителей микрофлоры кишечника, но не угнетают роста сальмонелл), а затем со среды обогащения — на дифференциально-диагностические среды (Эндо, висмутсульфитагар) с целью выделения изолированных колоний и получения из них чистых культур, идентифицируемых по указанной выше схеме. Для обнаружения О- и Vi-антигенов в сыворотке крови и испражнениях больных могут быть использованы РСК, РПГА с антительным диагностикумом, реакции коагглютинации, агрегат-гемагглютинации, ИФМ. Для ускоренной идентификации S. typhi перспективно применение в качестве зонда фрагмента ДНК, несущего ген Vi-антигена (время идентификации 3-4 ч).
С конца 1-й недели болезни в сыворотке больных появляются антитела, поэтому для диагностики брюшного тифа в 1896 г. Ф. Видалем была предложена реакция развернутой пробирочной агглютинации. Динамика содержания антител к S. typhi своеобразна: раньше всего появляются антитела к О-антигену, но титр их быстро снижается после выздоровления; Н-антитела появляются позднее, но зато сохраняются после болезни и прививок годами. С учетом этого обстоятельства реакцию Видаля ставят одновременно с раздельными О- и Н-диагностикумами (а также с паратифозными А- и В-диагностикумами) для исключения возможных ошибок, связанных с прививками или ранее перенесенным заболеванием. Однако специфичность реакции Видаля недостаточно высока, поэтому более предпочтительным оказалось применение РПГА, в которой эритроцитарный диагностикум сенсибилизирован либо О- (для обнаружения О-антител), либо Vi-антигеном (для обнаружения Vi-анти-тел). Наиболее надежной и специфической является последняя реакция (Vi-гемагглютинации).
Единственным доказательством бактерионосительства является выделение от носителя культур S. typhi, S. paratyphi А, S. paratyphi В. Материалом для исследования являются дуоденальное содержимое, испражнения и моча. Сложность проблемы заключается в том, что у носителей возбудитель не всегда выделяется с этими субстратами, бывают паузы, и довольно продолжительные. В качестве вспомогательных методов, которые позволяют сузить круг обследуемых лиц, используют серологические реакции (одновременное обнаружение О-, Н-, Vi- или О-, Vi-антител говорит о возможном присутствии возбудителя в организме) и аллергическую кожную пробу с Vi-тифином. Последний содержит Vi-антиген, который при взаимодействии с Vi-антителами дает местную аллергическую реакцию в виде покраснения и припухлости в течение 20-30 мин. Положительная реакция с Vi-тифином свидетельствует о наличии в организме Vi-антител и о возможном присутствии S. typhi. Для идентификации L-форм S. typhi предложены специальные иммунофлуоресцирующие антитела (к антигенам L-форм возбудителя). Оригинальный метод выявления бактерионосителей был предложен В. Муром. Он заключается в исследовании тампонов, одновременно забрасываемых в канализационные люки на всем протяжении канализационной сети населенного пункта.

Лечение брюшного тифа основано на применении различных антибиотиков, к которым возбудители проявляют высокую чувствительность (левомицетин, ампициллин, тетрациклины и др.). Антибиотики снижают тяжесть течения болезни и сокращают ее продолжительность. Однако перенос R-плазмид сальмонеллам от Е. coli или других энтеробактерий может привести к появлению среди них опасных эпидемических клонов.
Вместо семи различных брюшно-тифозных вакцин, применявшихся ранее, с 1978 г. в нашей стране выпускается только одна — химическая сорбированная брюшно-тифозная моновакцина. Однако в связи с тем, что брюшной тиф из эпидемического заболевания перешел в разряд спорадических (а это стало возможным, прежде всего, благодаря улучшению систем водоснабжения и канализации и повышению санитарной культуры населения), необходимость массовой иммунизации против него отпала. Поэтому прививка от брюшного тифа проводится только в случае эпидемических показаний.
источник
Брюшной тиф и паратифы А и В
Брюшной тиф (typhus abdominalis), паратифы А и В (paratyphus abdominalis А еt В) – острые инфекционные заболевания, сходные по своим клиническим проявлениям и патогенезу. Вызываются бактериями рода сальмонелл, характеризуются поражением лимфатического аппарата кишечника (главным образом тонкой кишки), бактериемией и протекают с выраженной интоксикацией, увеличением печени и селезенки и часто с розеолезной сыпью.
Исторические сведения. Заболевания тифо-паратифозной группы были известны очень давно. Описание их клинического течения имеется у Гиппократа (460—377 гг. до н.э.). Данное им название болезни происходит от слова typhos, что означает «дым», «туман». До начала XVIII в. под термином «тиф» объединяли все лихорадочные состояния, сопровождающиеся помрачением или потерей сознания. В середине XIX столетия появились описания особенностей течения брюшного тифа, но выделение его в самостоятельное заболевание произошло после открытия возбудителя болезни. Т.Брович в Кракове (1874) и Н.И.Соколов в Петербурге (1876) обнаружили палочковидные бактерии в лимфоидных (пейеровых) бляшках кишечника, а К.Эберт (1880) – в селезенке и мезентериальных лимфатических узлах людей, умерших от брюшного тифа. Г.Гаффки в 1884 г. получил возбудителя в чистой культуре, А.И.Вильчур (1887) выделил бактерию брюшного тифа из крови больного. М.Грубер (1896) открыл феномен агглютинации брюшнотифозных бактерий специфической сывороткой, Ф.Видаль в том же году разработал в диагностических целях реакцию агглютинации. Подробно описал клиническое течение болезни и характерные изменения в лимфатическом аппарате кишечника французский врач Ш.Бретано (1820—1829).
В нашей стране первое сообщение о клинической картине брюшного тифа под названием «особой» болезни в 1804 г. сделал И.И.Пятницкий. В 1857 г. клиническую и эпидемиологическую характеристику вспышки брюшного тифа в г.Николаеве дали М.Соколов и Ф.Кияковский, но эти работы остались незамеченными. Классическое, подробное описание брюшного тифа представил С.П.Боткин (1868). Большой вклад в изучение этой инфекции внесли отечественные ученые Г.А.Ивашенцев, Н.К.Розенберг, Г.Ф.Вогралик, Б.Я.Падалка, Р.П.Руднев, А.Ф.Билибин, К.В.Бунин и др.
Этиология. Возбудители брюшного тифа (Salmonella typhi) и паратифов А и В (Salmonella paratyphi А еt В) относятся к роду Salmonella (серологической группе D), семейству кишечных бактерий (Enterobacteriaceae), морфологически они не отличаются друг от друга, имеют форму палочек размером (0,5—0,8) х (1,5—3) мкм. Установлено также наличие фильтрующихся и L-форм бактерий. Спор и капсул не образуют, подвижны, имеют перитрахеально расположенные жгутики. Бактерии грамотрицательны, растут на обычных питательных средах, лучше – на содержащих желчь. Содержат эндотоксин, который освобождается при разрушении бактериальной клетки. В биохимическом отношении более активны паратифозные бактерии: они расщепляют углеводы с образованием кислоты и газа.
Брюшнотифозные бактерии содержат соматический (термостабильный) O-антиген, жгутиковый (термолабильный) Н-антиген и соматический термолабильный Vi-антиген, располагающийся более поверхностно, чем O-антиген. По отношению к бактериофагу выявлены различные типы брюшнотифозных бактерий. Определение фаготипов имеет большое значение для установления эпидемиологической связи между заболеваниями, выявления источника инфекции и идентификации культур.
Во внешней среде тифо-паратифозные бактерии относительно устойчивы. В воде и почве они могут сохраняться от нескольких дней до нескольких месяцев. Благоприятной средой для бактерий являются пищевые продукты (молоко, сметана, творог, мясной фарш, студень), в которых они не только сохраняются, но и способны размножаться. Бактерии хорошо переносят и низкие температуры, но при нагревании быстро погибают (при 60 °С через 30 мин, при 100 °С почти мгновенно). Дезинфицирующие средства (гипохлориты, хлорамины, лизол) в обычных концентрациях убивают возбудителя в течение нескольких минут.
Эпидемиология. Брюшной тиф, паратифы А и В относятся к кишечным антропонозам. Источником инфекции является только человек – больной или бактерионоситель. Из организма больного человека возбудители брюшного тифа, паратифа А и В выделяются во внешнюю среду вместе с испражнениями, мочой и слюной. Массивное выделение возбудителя из организма больного начинается после 7-го дня заболевания, достигает максимума в разгаре болезни и уменьшается в период реконвалесценции. В большинстве случаев бактериовыделение продолжается не более 3 мес (острое бактериовыделение), но иногда и всю жизнь (хроническое бактериовыделение). Хронические бактериовыделители являются основными источниками брюшнотифозной инфекции.
Для брюшного тифа и паратифов характерен фекально-оральный механизм заражения, реализация которого осуществляется водным, пищевым и контактно-бытовым путями передачи инфекции.
Передача возбудителей тифо-паратифозных заболеваний через воду, имевшая в прошлом основное значение, играет существенную роль и в настоящее время. Водные эпидемии нарастают бурно, но быстро завершаются после прекращения пользования зараженным водоисточником. Если заболевания связаны с употреблением воды из загрязненного колодца, эпидемии носят обычно локальный, очаговый характер. Спорадические заболевания в настоящее время нередко обусловлены употреблением воды из открытых водоемов, технической воды, используемой на различных промышленных предприятиях.
Опасны эпидемические вспышки, связанные с употреблением пищевых продуктов, в которых брюшнотифозные бактерии могут длительно сохраняться и размножаться. Для пищевых эпидемий характерны быстрое нарастание числа заболеваний и гнездное распространение в районах или квартирах среди лиц, употреблявших инфицированные продукты.
В заражении пищевых продуктов важную роль могут играть мухи. В ряде случаев заражение может происходить также контактно-бытовым путем, при котором факторами передачи становятся окружающие предметы.
Наиболее часто заболевают люди в возрасте 15—45 лет, преимущественно мужчины.
После перенесенной инфекции сохраняется стойкий иммунитет, однако у некоторых пациентов через несколько лет возможны повторные заболевания.
Для тифопаратифозных заболеваний характерно сезонное повышение заболеваемости в летне-осенний период, когда возникают благоприятные условия для реализации основных путей и факторов передачи возбудителя.
Патогенез и патологоанатомическая картина. При попадании в организм через рот и преодолении защитных барьеров верхних отделов пищеварительного тракта брюшнотифозные бактерии проникают в просвет тонкой кишки (фаза инфицирования). Из просвета кишки через лимфоидные образования ее слизистой оболочки (солитарные фолликулы и их скопления – групповые лимфатические фолликулы) бактерии проникают в регионарные лимфатические узлы (преимущественно брыжеечные), где интенсивно размножаются, что приводит к развитию воспалительного процесса (фаза первичной регионарной инфекции).
Указанные патогенетические фазы соответствуют инкубационному периоду. Возможно, в этот период развития болезни происходит сенсибилизация организма, в том числе и лимфатического аппарата кишечника, с чем связывают все последующие характерные для брюшного тифа патоморфологические изменения. В результате нарушения проницаемости гематолимфатического барьера бактерии поступают в кровяное русло, развивается бактериемия, с которой совпадает начало лихорадочного периода болезни.
При гибели части бактерий под влиянием бактерицидных свойств крови и вследствие фагоцитоза клетками системы макрофагов освобождаются эндотоксины, вызывающие общую интоксикацию организма (фаза бактериемии и токсинемии). Обладая выраженными нейротропными свойствами, они оказывают повреждающее действие на ЦНС и в тяжелых случаях способны вызывать status typhosus. Поражение вегетативной нервной системы приводит к появлению симптомов ваготонии, развитию метеоризма, болей в животе, к трофическим расстройствам.
Часть циркулирующих в крови бактерий поглощается клетками СМФ, но сохраняет жизнеспособность и размножается в них. Наступает фаза паренхиматозной диссеминации с соответствующими клиническими проявлениями поражения внутренних органов и экзантемой.
С момента развития инфекции возникают защитные реакции, способствующие освобождению организма от микроорганизма-возбудителя. В этом процессе немаловажная роль принадлежит специфическим антителам (опсонины, агглютинины, бактериолизины, преципитины, антиэндотоксины, комплемент-связывающие), а также нарастанию фагоцитарной активности макрофагов.
В процессе освобождения организма от бактерий брюшного тифа существенное значение имеет усиление функции выделительных систем: печени, желез кишечника (кишечные крипты, или либеркюновы железы), почек. Начиная с 8—9-го дня болезни бактерии вместе с желчью выделяются в просвет кишечника и частично выводятся из организма. Оставшиеся бактерии внедряются в первично сенсибилизированные групповые и солитарные лимфатические фолликулы дистального отдела тонкой кишки. Быстрое развитие в них некротического процесса объясняют аллергической реакцией, проявляющейся в виде гиперергического воспаления (выделительно-аллергическая фаза).
Выделение возбудителя из организма может также происходить с мочой, потом, слюной, грудным молоком. Значительное усиление выделения бактерий из организма, накопление специфических антител, повышение фагоцитарной активности клеток системы макрофагов свидетельствуют о формировании иммунитета и восстановлении физиологического равновесия. Из локализованных очагов брюшнотифозные бактерии могут прорываться в кровь с последующей генерализацией инфекционного процесса в виде рецидивов болезни.
Существенное значение в возникновении рецидивов имеет недостаточная напряженность формирующегося иммунитета вследствие приема антибиотиков, которые, ослабляя антигенное раздражение, способствуют снижению выработки специфических антител.
При брюшном тифе нередко наблюдается длительное бактериовыделение. В настоящее время оно рассматривается как хроническая форма брюшнотифозной инфекции, при которой возбудитель сохраняется в клетках СМФ. В основе формирования брюшнотифозного носительства лежит несовершенство иммунной системы. У хронических носителей выявлен дефицит макроглобулиновых O-антител (IgМ). Известно, что этому классу иммуноглобулинов принадлежит важная роль в формировании противобрюшнотифозного иммунитета.
Показано, что в случаях бактериовыделения брюшнотифозные бактерии при внутриклеточном паразитировании в клетках СМФ в костном мозге могут переходить в L-формы, которые в определенных условиях среды могут реверсировать в исходные формы бактерий и вызывать бессимптомную бактериемию с выделением возбудителя с испражнениями.
Основные патоморфологические изменения при тифопаратифозных заболеваниях наблюдаются в лимфоидной ткани подвздошной кишки. Закономерность и цикличность развития этих изменений в кишечнике послужили основанием для вы– деления пяти патоморфологических периодов. Они условны, так как не всегда полностью соответствуют клиническим периодам и тяжести болезни.
Первый период соответствует примерно 1-й неделе болезни и характеризуется значительным набуханием лимфоидной ткани тонкой кишки. Групповые и солитарные лимфатические фолликулы увеличиваются в размерах и выступают над уровнем слизистой оболочки – период мозговидного набухания. На 2-й неделе начинается некротизация центральных частей набухших лимфатических образований (период некроза). Поверхность их становится грязно-серой или зеленовато-желтой.
На 3-й неделе происходят отторжение некротизированных элементов лимфоидной ткани и образование язв (период образования язв). При этом обнажаются глубокие слои слизистой оболочки и подслизистой основы. К концу 3-й – началу 4-й недели болезни отторжение некротизированных тканей заканчивается и начинается четвертый период – период «чистых язв». Язвы с чистым, гладким дном и слегка набухшими краями образуются в области групповых и солитарных лимфатических фолликулов, располагаясь вдоль подвздошной кишки. Пятый период, соответствующий примерно 5—б-й неделе болезни, характеризуется заживлением язв без стягивающих рубцовых изменений, но с незначительной пигментацией аспидно-серого цвета.
Специфическими для брюшного тифа являются гиперпластические процессы в ретикулярной строме групповых и солитарных лимфатических фолликулов. Кроме гиперплазии, формируются брюшнотифозные гранулемы («тифомы»), состоящие из макрофагов в виде крупных, так называемых тифозных клеток с массивной светлой цитоплазмой и светлыми ядрами. Их находят в червеобразном отростке, толстой кишке, лимфатических узлах брыжейки, в печени, селезенке, костном мозге, реже в лимфоидной ткани глотки, альвеолах, мозговых оболочках.
Печень при брюшном тифе увеличенная, набухшая, на разрезе тусклая, желтоватого цвета. При микроскопическом исследовании обнаруживаются специфические гранулемы с очагами некроза, белковая и жировая, дистрофия гепатоцитов. Селезенка увеличена за счет кровенаполнения и воспалительной пролиферации ретикулярных клеток с образованием тифозных гранулем, возможно развитие инфарктов селезенки с их последующим нагноением. В почках – мутное набухание. Иногда могут встречаться некротический нефроз, геморрагический или эмболический нефрит и воспалительные процессы в лоханках, мочеточниках и мочевом пузыре. Дегенеративные изменения часто выявляются в сердечной мышце и нервных ганглиях. Такие же изменения наблюдаются в ганглиозных клетках узлов симпатической нервной системы, вегетативных сплетениях. Характерен восковидный (ценкеровский) некроз прямых мышц живота.
Пневмонии при брюшном тифе в большинстве случаев обусловлены вторичной инфекцией, но встречаются и специфические брюшнотифозные пневмонии с образованием типичных гранулем («пневмотиф»).
Розеолезная сыпь при брюшном тифе появляется в результате продуктивно-воспалительных изменений поверхностных слоев кожи по ходу кровеносных и лимфатических сосудов. В соскобах розеол обнаруживаются тифопаратифозные бактерии.
Существенных различий в патологоанатомической картине, наблюдаемой при брюшном тифе и паратифах, не отмечается.
Клиническая картина. Продолжительность инкубационного периода при брюшном тифе колеблется от 7 до 25 дней, чаще составляя 9—14 дней.
Различают типичное и атипичное течение брюшного тифа. Типичные формы протекают циклически. Это позволяет выделить четыре периода заболевания: начальный, разгара, разрешения болезни и выздоровления. По тяжести клинических проявлений различают легкую, средней тяжести и тяжелую форму брюшного тифа.
В соответствии с особенностями течения заболевания различают неосдожненный и осложненный брюшной тиф.
Начальный период болезни. Характеризуется постепенным или острым развитием интоксикационного синдрома. В прошлом преобладал вариант постепенного развития симптомов интоксикации, в настоящее время почти с равной частотой встречаются оба варианта.
При постепенном развитии симптомов заболевания в первые дни больные отмечают повышенную утомляемость, нарастающую слабость, познабливание, усиливающуюся головную боль, снижение или отсутствие аппетита. Температура тела, ежедневно ступенеобразно повышаясь, к 5—7-му дню заболевания достигает 39—40 °С. К этому времени все явления интоксикации нарастают, развиваются значительная слабость, адинамия, становится упорной головная боль, нарушается сон, возникают анорексия, обстипация, метеоризм. Иногда при погрешностях в диете наблюдается диарея. Стул редко бывает более 2—4 раз в сутки.
При остром начале заболевания в первые 2—3 дня все симптомы интоксикации достигают полного развития.
При обследовании больных в начальном периоде болезни обращают на себя внимание некоторая заторможенность и адинамия. Больные безучастны к окружающему, на вопросы отвечают односложно, не сразу. Лицо бледное или слегка гиперемировано, иногда немного пастозное.
При исследовании сердечно-сосудистой системы отмечается относительная брадикардия, иногда дикротия пульса. Артериальное давление снижено. Над легкими нередко выслушиваются везикулярное дыхание с жестким оттенком и рассеянные сухие хрипы, что свидетельствует о развитии диффузного бронхита.
Пищеварительная система закономерно вовлекается в патологический процесс, и изменения ее органов имеют большое диагностическое значение. Язык обычно утолщен, с отпечатками зубов на боковых поверхностях. Спинка языка покрыта серовато-белым налетом, края и кончик свободны от налета, имеют насыщенно-розовый или красный цвет. Зев слегка гиперемирован, иногда наблюдаются увеличение и гиперемия миндалин. Живот умеренно вздут вследствие метеоризма. При пальпации в правой подвздошной области определяются грубое, крупнокалиберное урчание в слепой кишке и мелкокалиберное урчание и болезненность по ходу терминального отдела подвздошной кишки, свидетельствующие о наличии илеита. При перкуссии отмечается укорочение перкуторного звука в илеоцекальной области (симптом Падалки), что обусловлено гиперплазией воспалительно измененных лимфатических узлов брыжейки. Об этом же свидетельствует и положительный «перекрестный» симптом Штернберга. К концу 1-й недели заболевания выявляется увеличение печени и селезенки.
В гемограмме после кратковременного (в первые 2—3 дня) умеренного лейкоцитоза с 4—5-го дня болезни отмечаются лейкопения со сдвигом лейкоцитарной формулы влево, анэозинофилия, относительный лимфоцитоз и тромбоцитопения.
СОЭ умеренно увеличена. Изменения в гемограмме являются закономерным следствием воздействия токсинов брюшнотифозных бактерий на костный мозг. Изменения в урограмме нередко укладываются в синдром инфекционно-токсической почки: протеинурия, микрогематурия, цилиндрурия.
Период разгара болезни. К концу 1-й – началу 2-й недели наступает период разгара болезни, когда все симптомы достигают максимального развития. Он продолжается 1—2 нед. Температура тела, повысившись до 39—40 °С, может иметь в дальнейшем постоянный характер (вундерлиховский тип) или носить многоволновой характер (боткинский тип), температурная кривая может также иметь одну волну – кривая типа «наклонной плоскости» (по Кильдюшевскому). В этот период болезни головная боль и бессонница нередко становятся мучительными. Развивается status typhosus, характеризующийся резкой слабостью, адинамией, апатией, нарушением сознания от оглушенности до сопора или комы. Возможно развитие инфекционного делирия.
На 8—10-й день болезни на коже появляется характерная экзантема. Она выявляется у 55—70 % заболевших брюшным тифом и локализуется преимущественно на коже живота и нижней части груди. Сыпь, как правило, скудная, число ее элементов редко превышает 6—8, по характеру розеолезная, мономорфная. Розеолы имеют вид розовых пятнышек округлой формы, с четкими контурами, диаметром около 3 мм. Нередко они слегка возвышаются над уровнем кожи (roseola elevanta) и хорошо заметны на ее бледном фоне. При надавливании или растяжении кожи по краям розеолы она исчезает, после чего появляется вновь. Каждый элемент сыпи существует 1—5 дней, чаще 3—4 дня. После исчезновения сыпи остается едва заметная пигментация кожи. Могут образовываться новые розеолы на фоне угасающих старых (феномен «подсыпания»), что связано с волнообразным течением бактериемии. У некоторых больных обнаруживается желтушное окрашивание кожи ладоней и подошв – каротиновая гиперхромия кожи (симптом Филипповича), возникающая вследствие нарушения каротинового обмена, обусловленного поражением печени.
В разгар болезни сохраняются относительная брадикардия, дикротия пульса, еще более снижается артериальное давление. Поражение сердечной мышцы проявляется умеренным смещением границ сердечной тупости влево, глухостью тонов сердца, негрубым систолическим шумом, выслушиваемым на верхушке и у основания сердца.
Над легкими продолжают выслушиваться везикулярное дыхание с жестким оттенком и рассеянные сухие хрипы. В некоторых случаях возникают симптомы очаговой пневмонии, обусловленные как самим возбудителем брюшного тифа, так и сопутствующей микрофлорой.
Симптомы поражения органов пищеварения в разгар заболевания достигают максимального развития. Губы больных сухие, нередко покрыты корочками. Язык утолщен, густо обложен серо-коричневатым налетом, края и кончик его ярко красного цвета, с отпечатками зубов («тифозный», «поджаренный» язык). У тяжелобольных язык становится сухим и принимает фулигинозный вид, живот вздут вследствие метеоризма, стул – возможен запор, в некоторых случаях жидкий, испражнения в виде горохового супа и со своеобразным кислым запахом. Отчетливыми становятся урчание и болезненность при пальпации илеоцекального отдела кишечника, сохраняются положительные симптомы Падалки и Штернберга. Печень увеличена, хорошо доступна пальпации, край ее ровный, слегка закругленный, иногда болезненный, консистенция тестоватая. Селезенка увеличена, как правило, доступна пальпации.
В разгар болезни уменьшается количество выделяемой мочи. Определяются протеинурия, микрогематурия, цилиндрурия. Возникает бактериурия, которая иногда приводит к воспалению слизистой оболочки почечных лоханок и мочевого пузыря.
В этот период заболевания могут возникать такие опасные осложнения, как перфорация брюшнотифозных язв и кишечное кровотечение. В некоторых случаях вследствие тяжелой интоксикации и опасных осложнений может наступить смерть.
Период разрешения болезни. Температура тела снижается, причем нередко перед нормализацией она начинает колебаться, приобретая амфиболический характер (различия между утренней и вечерней температурой достигают 2—2,5 °С). Прекращается головная боль, нормализуется сон, улучшается аппетит, увлажняется язык, с него исчезает налет, увеличивается диурез. Длительность периода разрешения болезни, как правило, не превышает 1 нед.
Период выздоровления. Восстанавливаются нарушенные функции организма, и происходит освобождение его от возбудителей тифа. Для данного периода типичен астеновегетативный синдром, который сохраняется 2—4 нед и зависит от тяжести перенесенного заболевания. Среди перенесших брюшной тиф 3—5 % пациентов становятся хроническими брюшнотифозными бактериовыделителями.
Рецидивы (в среднем у 7—9 % больных) чаще возникают на 2—3-й неделе нормальной температуры, но могут проявляться и в более поздние сроки (1—2 мес) независимо от формы и тяжести болезни. Они бывают однократными и многократными. Продолжительность лихорадки при рецидиве может колебаться от 1—3 дней до 2—3 нед. В предрецидивный период отмечается субфебрилитет, замедляется очищение языка от налета, сохраняются увеличенными печень и селезенка, в гемограмме отмечаются изменения, присущие периоду разгара болезни. Клинически рецидивы брюшного тифа сходны с первой волной заболевания и отличаются лишь более быстрым подъемом температуры, ранним появлением сыпи, меньшей длительностью лихорадки и обычно более легким течением.
При а типичных формах заболевания ряд характерных признаков брюшного тифа может отсутствовать. К атипичным относятся абортивная и стертая формы болезни.
Абортивная форма имеет много сходных черт с типичным течением болезни, но клиническая картина не достигает полного развития. Температура быстро (через 7—10 дней) и нередко критически снижается, исчезают другие симптомы интоксикации, наступает выздоровление.
При стертой форме («амбулаторный тиф», «легчайший тиф») интоксикация выражена незначительно. Температура субфебрильная, продолжительность ее не более 5—7 дней (иногда 2—3 дня). Экзантема возникает редко. Изменения внутренних органов выражены слабо. Больные, как правило, трудоспособны.
Иногда болезнь протекает с преобладанием симптомов поражения отдельных органов и систем: легких, мозговых оболочек, слепой кишки (так называемые пневмотиф, менинготиф, колотиф).
Осложнения. При брюшном тифе осложнения могут быть условно разделены на специфические, обусловленные патогенным влиянием возбудителя и его токсина, а также неспецифические, вызванные сопутствующей микрофлорой.
Из специфических осложнений брюшного тифа наибольшее значение для исхода заболевания имеют кишечное кровотечение, перфоративный перитонит и инфекционно-токсический шок.
Кишечное кровотечение, возникающее у 1—2 % больных, ухудшает прогноз и чаще наблюдается на 3-й неделе болезни, иногда после снижения температуры. Причиной его является аррозия сосуда (вены или артерии) в дне брюшнотифозной язвы. Кровотечение может также носить диффузный, капиллярный характер. В механизме его развития имеют значение снижение свертываемости крови и замедление тромбообразования. В зависимости от скорости эвакуации содержимого кишечника и массивности кровотечения стул больных становится дегтеобразным (мелена), содержит сгустки крови или свежую кровь.
Небольшие кровотечения обычно не влияют на состояние больного. Они обнаруживаются при осмотре стула или с помощью реакции Грегерсена спустя много часов после начала. При массивных кровотечениях температура тела внезапно снижается до нормальной или субнормальной, возникает жажда, пульс учащается, артериальное давление понижается. Небольшое кровотечение при своевременном лечении заканчивается благополучно. Массивное кровотечение может привести к развитию геморрагического шока, что всегда имеет серьезный прогноз.
Перфоративный перитонит как следствие прободения язвы кишечника – опасное осложнение брюшного тифа. Он развивается на 2—4-й неделе болезни, иногда после нормализации температуры. Встречается у 0,5—1,5 % больных и может наблюдаться не только при тяжелом, но иногда и при легком течении болезни. Наиболее часто прободение язвы происходит в подвздошной кишке на расстоянии 25—30 см от места перехода ее в слепую кишку. Перфорации способствуют метеоризм, усиленная перистальтика, резкие движения, сильный кашель, грубая пальпация живота, нарушение диеты.
Клиническая картина брюшнотифозного перфоративного перитонита имеет ряд особенностей, что необходимо учитывать при диагностике. Наличие status typhosus может маскировать симптомы перфорации. Основной симптом прободения – внезапная резкая боль – нередко отсутствует, поэтому появление даже небольших болей в животе должно привлечь внимание врача. Другой ведущий симптом развивающегося перитонита – сокращение мышц брюшной стенки – у больных с помрачением сознания может быть единственным. Не постоянным, но важным признаком перфорации является положительный симптом Щеткина – Блюмберга. Перфорация кишки иногда сопровождается тяжелым коллапсом. Спустя несколько часов после перфорации развивается выраженная картина перитонита. Появляется facies hyppocratica, присоединяются рвота, упорная икота, вздутие и сильная разлитая болезненность живота. Печеночная тупость исчезает. Однако эти симптомы развиваются слишком поздно. Больного можно спасти, если оперативное вмешательство будет произведено в первые 6 ч после перфорации. При более поздней операции прогноз почти безнадежный.
Инфекционно – токсический шок развивается, как правило, в период разгара болезни и встречается у 0,5—0,7 % больных. Возникновение его обусловлено массивным поступлением в кровь брюшнотифозных бактерий и их токсинов. В основе развития шока лежит не столько собственно токсический эффект, сколько проявление бурного иммунного конфликта в результате поступления бактериальных антигенов, образования иммунных комплексов, фиксации комплемента, реакции плазматических клеток, резкого истощения системы мононуклеарных фагоцитов, гепарин– и гистаминемии.
В клинической картине болезни инфекционно-токсическому шоку предшествуют симптомы гипертермии и нейротоксикоза. При его развитии наблюдаются резкое снижение температуры тела, повышенное потоотделение, тахикардия, тахипноэ, падение артериального давления, олигурия, в дальнейшем анурия.
К числу неспецифических осложнений относятся пневмония, тромбофлебиты, менингиты, пиелиты, паротиты, стоматиты и др.
Прогноз. При неосложненном течении брюшного тифа прогноз благоприятный. При развитии осложнений он хуже и может быть неблагоприятным (особенно при перфоративном перитоните). Летальность составляет 0,1—0,3 %.
Клиническая характеристика паратифов. По эпидемиологии, патогенезу, морфологии и клинической картине паратифы А и В в основном сходны с брюшным тифом, но имеют некоторые особенности.
Инкубационный период при паратифе А короче, чем при брюшном тифе, длительность его 8—10 дней. Начало чаще острое, иногда сопровождается насморком, кашлем. При осмотре выявляются гиперемия лица, инъекция сосудов склер, герпес на губах. Температурная кривая имеет неправильный характер, чаще волнообразный или ремитирующий. Лихорадка нередко сопровождается ознобом, а затем обильным потом. Сыпь при паратифе А появляется в более ранние сроки (4-7-й день болезни), отличается полиморфизмом; часты дополнительные высыпания. Сыпь может быть розеолезной, кореподобной и петехиальной. Интоксикация, как правило, выражена умеренно, отсутствует характерный тифозный статус. В гемограмме отмечается нормоцитоз, но может быть и лейкоцитоз с лимфомоноцитозом.
У большинства больных заболевание протекает в форме средней степени тяжести, но могут наблюдаться и тяжелые формы с осложнениями в виде кишечного кровотечения, перфорации кишки, бронхопневмонии и др. Рецидивы при паратифе А встречаются довольно часто.
Инкубационный период при паратифе В составляет 5-10 дней, но может быть и более продолжительным. Заболевание часто начинается остро, сопровождается выраженным ознобом, болями в мышцах и потливостью. В начальном периоде болезни явления интоксикации могут сочетаться с симптомами острого гастроэнтерита. Температурная реакция короткая, часто волнообразного характера. Тифозное состояние у большинства больных отсутствует, симптомы интоксикации, наблюдаемые в начальном периоде (3-5 дней), быстро исчезают. Сыпь появляется в ранние сроки, имеет полиморфный характер, часто бывает обильной. Некоторых случаях течение паратифа В может быть тяжелым, с септическими проявлениями в виде гнойного менингита, менингоэнцефалита, септикопиемии. В гемограмме наблюдается нейтрофильный лейкоцитоз. Клиническое течение тифопаратифозных инфекций может значительно варьировать в зависимости от характера эпидемической вспышки, возраста больных, сопутствующих заболеваний и предшествующих вакцинаций. Обычно заболевание длится 3-4 нед, но может быть и более коротким (5-7 дней). Повторные рецидивы и осложнения удлиняют течение болезни иногда до нескольких месяцев.
Диагностика. При брюшном тифе и паратифах наиболее важна диагностика в первые 5-7 дней болезни. Это связано с эпидемиологическими требованиями, обусловленными высокой контагиозностью больного в последующие дни болезни, а также диктуется клинико-патогенетическими особенностями заболевания.
В распознавании тифопаратифозных заболеваний большое значение имеют как клинико-эпидемиологические, так и лабораторные данные. В лабораторной диагностике используют бактериологический и серологический методы исследования, которые проводят с учетом периода инфекционного процесса.
На 1—2-й неделе заболевания возбудителя легче всего выделить из крови, со 2—3-й недели – из испражнений и мочи, в течение всего заболевания – из дуоденального содержимого (в остром периоде болезни дуоденальное зондирование противопоказано, выделение биликультуры осуществляют в периоде реконвалесценции). Можно выделить возбудителя при посеве соскоба розеол, костного мозга, гноя, экссудатов, мокроты.
Выявление бактерий в крови всегда служит показателем острого заболевания, признаком, абсолютно подтверждающим диагноз брюшного тифа. Присутствие возбудителя в фекалиях может быть результатом заболевания или бактерионосительства. В этих случаях при наличии клинических признаков вопрос решается в пользу острого заболевания брюшным тифом, при их отсутствии – в пользу бактерионосительства.
Посев крови для выделения гемокультуры можно осуществлять с 1-го дня болезни и на протяжении всего лихорадочного периода. Из вены берут стерильно 5—10 мл крови и засевают во флакон с 50—100 мл 10—20 % желчного бульона или среды Раппопорт. При посеве крови на питательную среду необходимо сохранять соотношение между кровью и средой 1:10, при меньшем объеме питательной среды кровь может оказать бактерицидное действие на микроорганизм-возбудитель.
Для получения миелокультуры можно использовать костный мозг, полученный при пункции. При выделении из крови и костного мозга L-форм бактерий применяются специальные пенициллино-сывороточные среды. Для получения копро-, били– и уринокультур используется среда Плоскирева.
Специфический антиген в крови, костном мозге и других исследуемых материалах выявляется также иммунофлюоресцентным и иммуноферментным методами. Эти методы высокочувствительны и могут быть использованы для экспрессной диагностики при эпидемических вспышках брюшного тифа.
Для серологической диагностики брюшного тифа и паратифов А и В с 5—7-го дня заболевания используется преимущественно РНГА с эритроцитарными диагностикумами (О-, Н-, Vi-антигены). Положительной считается реакция в титре 1:200 и выше. При исследовании в РНГА парных сывороток, взятых в динамике заболевания, диагностически значимым считается четырехкратное и большее нарастание титра анти– тел к возбудителям брюшного тифа и паратифов. Для выявления бактерионосителей используют РНГА с Vi-антигеном. Широко применявшаяся в прошлом реакция Видаля постепенно утрачивает диагностическое значение.
Дифференциальная диагностика. Дифференцировать тифопаратифозные заболевания приходится от сыпного тифа, малярии, бруцеллеза, листериоза, пневмонии, сепсиса, туберкулеза, лимфогранулематоза.
Лечение. Течение и исход брюшного тифа зависят от правильного ухода, диеты и своевременного назначения антибактериальных и патогенетических средств. Лечение больных тифопаратифозными заболеваниями осуществляют в условиях инфекционного стационара.
Больному необходимо обеспечить покой, удобную постель, хорошие гигиенические условия. Немаловажное значение имеет уход за полостью рта и кожей. Постельный режим необходимо соблюдать до 6– 7-го дня нормальной температуры. С 7—8-го дня разрешается сидеть, а с 10—11-го дня нормальной температуры при отсутствии противопоказаний разрешается ходить.
В лихорадочном периоде и в течение первых 7—8 дней нормальной температуры диета больных должна быть максимально механически и химически щадящей в отношении кишечника, способствовать уменьшению бродильных и гнилостных процессов и в то же время быть достаточно калорийной. Этим требованиям соответствуют диеты № 4 и 46. С выздоровлением диету постепенно расширяют (№ 4в, № 2).
Наиболее эффективным антибиотиком при тифопаратифозных заболеваниях является левомицетин. Успешно может использоваться и ампициллин. Антибиотикотерапия осуществляется в течение всего лихорадочного периода и первых 10 дней после нормализации температуры. Левомицетин назначают внутрь по 0,5 г 4 раза в сутки. Однако применение антибиотиков не всегда предупреждает рецидивы болезни и формирование хронического бактерионосительства. Рецидивы при лечении больных левомицетином, как правило, характеризуются более легким течением и наступают в более поздние сроки (на 18—25-й день нормальной температуры), чем у нелеченых больных. В случае рецидивов левомицетин назначают повторно в тех же дозах. При хроническом бактерионосительстве левомицетин не оказывает положительного действия. В случае невозможности использования левомицетина перорально (частая рвота) назначают левомицетина сукцинат растворимый внутримышечно или внутривенно. Его суточная доза для взрослого составляет 3—4 г (50 мг/кг).
Ампициллин в дозе по 1 г 4—6 раз в сутки дает хороший эффект в остром периоде брюшного тифа и в некоторых случаях острого (до 3 мес) бактериовыделения.
При устойчивости возбудителя к антибиотикам применяют бактрим (бисептол) или нитрофурановые препараты.
Для более эффективной этиотропной терапии, предупреждения рецидивов и формирования бактерионосительства она должна сочетаться со средствами, повышающими специфическую и неспецифическую реактивность организма. Для повышения неспецифической резистентности организма, кроме полноценной диеты и витаминов, используют нестероидные анаболики (метилурацил, или метацил, оротат калия).
Для дезинтоксикации организма внутривенно назначают раствор Рингера, 5 % раствор глюкозы, гемодез, реополиглюкин. Положительное действие оказывают также кортикостероиды, которые применяют только в тяжелых случаях болезни.
При кишечных кровотечениях необходим строгий постельный режим в положении на спине в течение 12—24 ч. Назначают холод на живот, запрещают прием пищи на 10—12 ч, а объем выпиваемой больным жидкости сокращают до 500 мл. В дальнейшем можно назначать небольшими порциями слизистые отвары, соки, желе, кисели, мясной или рыбный бульон. Со 2-го дня диету постепенно расширяют. При небольшом кровотечении используют хлорид кальция, витамины С и К, гипертонический раствор хлорида натрия (5—10 мл в вену), желатиноль, плазму и другие препараты крови. При борьбе с массивным кровотечением в инфузионной терапии с замести– тельной целью используют значительные количества крови (1—2 л), полиионные растворы («Трисоль», «Ацесоль», «Лактасол», «Квартасоль» и др.), коллоидные растворы (полиглюкин, реополиглюкин, желатиноль и др.) и кортикостероиды.
При перфорации стенки кишки показано срочное оперативное вмешательство.
В терапии инфекционно-токсического шока используют методику управляемой гемодилюции с введением реологически активных и комплексообразующих препаратов (коллоидов) – гемодеза, реополиглюкина, желатиноля, кристаллоидных полиионных растворов в сочетании с введением вазоактивных препаратов (например, дофамин или допамин), массивных доз глюкокортикостероидов. С целью повышения антиагрегационного эффекта кристаллоидных растворов к ним добавляют ингибиторы протеолиза – контрикал (трасилол, тзалол), в некоторых случаях применяют активаторы спонтанного фибринолиза (соли магния, никотиновая кислота).
Профилактика. Мероприятия по борьбе с тифопаратифозными заболеваниями должны быть направлены на обезвреживание источников инфекции, пресечение путей передачи, повышение невосприимчивости организма.
Большое значение в профилактике брюшного тифа имеют ранняя диагностика, своевременная изоляция и провизорная госпитализация больного, эффективная терапия с полным освобождением организма от возбудителя.
В периоде выздоровления с интервалами в 5 дней проводят трехкратное контрольное бактериологическое исследование кала и мочи и однократное исследование желчи. При обнаружении возбудителя в кале, моче или желчи реконвалесцента подвергают интенсивному лечению в стационаре в зависимости от сопутствующей патологии и реактивности организма.
Выписка бактериовыделителя возможна только с разрешения эпидемиолога. После выписки все реконвалесценты подлежат диспансерному наблюдению с систематическим обследованием для своевременного выявления рецидива болезни и формирования хронического бактерионосительства. Продолжительность и интенсивность лабораторного обследования переболевших зависят от их профессиональной принадлежности. Переболевшие состоят на учете в центре санитарно-эпидемиологического надзора в течение 2 лет, а лица, работающие на пищевых предприятиях, – 6 лет.
С целью пресечения распространения возбудителя в очаге осуществляют текущую дезинфекцию до госпитализации больного или бактериовыделителя. После госпитализации в очаге проводят заключительную дезинфекцию.
За лицами, контактировавшими с больными, устанавливается медицинское наблюдение в течение 21 дня с ежедневной термометрией. Проводится однократное, а по показаниям двукратное бактериологическое исследование кала и мочи. У ранее переболевших брюшным тифом, а также у лиц, страдающих заболеваниями печени и желчевыводящих путей, производятся посев дуоденального содержимого и исследование крови в РНГА с эритроцитарным Vi-антигеном. Специфическая профилактика в очаге включает назначение бактериофага всем контактным.
Специфическую вакцинопрофилактику брюшного тифа проводят по эпидемическим показаниям. На территориях, неблагополучных по брюшному тифу, вакцинацию осуществляют всему населению, начиная с детей 7-летнего возраста. Специфическая профилактика показана также лицам, относящимся к группам риска: работникам очистных сооружений, сотрудникам инфекционных больниц и бактериологических лабораторий. Вакцинацию проводят и лицам, выезжающим в страны Африки и Азии с высоким уровнем заболеваемости брюшным тифом. В России для активной иммунизации против брюшного тифа используют инактивированные вакцины: вакцину брюшнотифозную спиртовую сухую; вакцину брюшнотифозную спиртовую, обогащенную Vi-антигеном; вакцину брюшнотифозную У1-полисахаридную жидкую. В ответ на введение вакцин иммунитет развивается через 1—2 нед. Невосприимчивость к инфекции сохраняется в течение 2 лет.
За рубежом используют также живую брюшнотифозную вакцину. Ожидается создание конъюгированной вакцины против брюшного тифа, которая была бы пригодна для введения в том числе и детям первых 2 лет жизни.
источник