Межрегиональная ассоциация по клинической микробиологии и антимикробной химиотерапии
Институт медицинской паразитологии и тропической медицины им. Е.И. Марциновского, ММА им. И.М. Сеченова
Амёбиаз — паразитарная болезнь человека, вызываемая патогенными штаммами Entamoeba histolitica, является одной из важнейших проблем здравоохранения развивающихся стран и одной из наиболее частых причин летальных исходов при паразитарных болезнях кишечника.
В методических рекомендациях приведены основные сведения об амёбиазе, его клинических проявлениях, лечении и профилактике. Обсуждаются вопросы лечения инвазивного и неинвазивного амёбиаза.
Для врачей терапевтов, инфекционистов, педиатров, эпидемиологов, урологов, акушеров-гинекологов, клинических фармакологов.
А.М. Бронштейн
Институт медицинской паразитологии и тропической медицины им. Е.И. Марциновского, Московская медицинская академия им. И.М. Сеченова, Москва, Россия
Н.А. Малышев
Клиническая инфекционная больница N 1, Москва, Россия
В.И. Лучшев
Кафедра инфекционных болезней, тропической медицины и эпидемиологии Российского государственного медицинского университета, Москва, Россия
Александр Маркович Бронштейн
103287, Москва, ул. Писцовая 10,
ГКБ N 24 (клин. отдел ИМПиТМ)
Тел:/факс: (095)285-2669
Эл. почта: bronstein@mail.ru
Амебиаз — болезнь, вызываемая патогенными штаммами Entamoeba histolytica, имеющими широкое распространение в мире, преимущественно в странах тропического и субтропического климата. Характерный для этих районов низкий уровень санитарии обусловливает высокий уровень заболеваемости амёбиазом. В настоящее время амёбиаз представляет собой одну из крупнейших медицинских и социальных проблем населения развивающихся стран и является одной из наиболее частых причин смерти при паразитарных болезнях кишечника. После малярии данная инфекция занимает второе место в мире по частоте летальных исходов при паразитарных заболеваниях [1, 2] . Около 480 млн. людей в мире являются носителями Е.histolytica, у 48 млн. из них развивается колит и внекишечные абсцессы и у 40 тыс. — 100 тыс. заболевших наступает летальный исход [3] . Миграция, ухудшение экономического положения ряда развивающихся стран, низкий уровень санитарии способствуют распространению амёбиаза и соответственно повышению уровня заболеваемости.
В России амёбиаз встречается в южных регионах. Вместе с тем, в связи с увеличивающимся притоком мигрантов из южных регионов стран ближнего и дальнего зарубежья, увеличением въездного туризма, а также значительным увеличением зарубежного туризма, в том числе в страны жаркого климата, частота случаев амёбиаза среди граждан России, в том числе жителей Москвы существенно возросла.
Из фекалий человека можно выявить 7 видов амёб: Entamoeba histolytica, Entamoeba dispar, Entamoeba hartmanni, Entamoeba coli, Endolimax nana, Iodamoeba butschlii и Blastocystis hominis, но только Е.histolytica может вызывать инвазивные инфекции у человека.
Отмечаемый ранее диссонанс между высокой частотой выделения Е.histolytica и, в то же время, относительно низкой частотой клинических проявлений от части, как оказалось, связан с наличием в популяции Е.histolytica двух видов амёб — потенциально патогенных штаммов Е.histolytica, и непатогенной Е.dispar, различить которые можно лишь путем анализа ДНК [4] . В последние годы разработан чувствительный и специфичный метод ПЦР, позволяющий относительно просто и быстро идентифицировать в фекалиях одновременно Е.histolytica и E.dispar [5] .
Вместе с тем вопрос о различии патогенности штаммов внутри вида Е.histolytica остается недостаточно ясным. Посредством изоэнзимного анализа выявлено 9 потенциально патогенных зимодемов Е.histolytica, и 13 по-видимому непатогенных зимодемов, между которыми выявлены также отличия в ДНК [6, 7] .
Е.histolytica относится к роду Entamoeba, принадлежащему к семейству Entamoebidae, отряду Amoebida, классу Lobosea, суперклассу Rhizopoda, подтипу Sarcodina, типу Protozoa.
Цисты Е.histolytica с водой или с пищевыми продуктами попадают в желудочно-кишечный тракт. В тонком кишечнике под действием кишечных ферментов оболочка цисты растворяется и образуется восемь одноядерных амеб. В результате последующих делений они превращаются в вегетативные просветные стадии, трофозоиты размером от 10 до 60 мкм, в среднем 25 мкм, имеющими одно ядро, местом обитания которых является просвет верхних отделов толстого кишечника. По мере продвижения по кишечнику трофозоиты превращаются в одно/-четырех ядерные цисты (в среднем 12 мкм в диаметре), которые выделяются с фекалиями.
При попадании в организм человека цист Е.histolytica, вследствие воздействия ряда факторов, образуются инвазивные формы паразита. В развитии инвазивных форм имеют значение такие факторы паразита и хозяина, как: интенсивность инвазии; физико-химическая среда кишечника (характер секрета слизистой, нарушения перистальтики кишечника); иммунодефицит; голодание; стресс и др. Отмечается в частности относительно частое развитие инвазивных форм амёбиаза у беременных [1, 8, 9] . Имеются также данные, что у лиц инфицированных ВИЧ инвазивный амёбиаз развивается чаще [10, 11] .
Инвазивные или так называемые тканевые стадии амеб — больших размеров, чем просветные, могут фагоцитировать эритроциты, обладают протеолитическими свойствами и поверхностными пектинами, способствующими их прикреплению к слизистой кишечника [6, 12] .
В последнее время установлено, что основным фактором вирулентности у Е.histolytica являются цистеиновые протеиназы, отсутствующие у Е.dispar. Дальнейшие исследования в этом направлении могут способствовать разработке ингибиторов цистеин-протеиназ, которые можно будет использовать при создании новых амебоцидов [13] .
В соответствии с патоморфологическими изменениями и клинической картиной выделяют «инвазивный» амёбиаз, при котором развиваются патологические изменения, и «неинвазивный» амёбиаз [6] .
Для «инвазивного» амёбиаза характерны:
- клинические симптомы инфекционного заболевания;
- наличие трофозоитов-гематофагов в фекалиях;
- характерные изменения в слизистой кишечника при эндоскопических исследованиях;
- наличие специфических антител, выявляемых серологическими тестами.
Для «неинвазивного» кишечного амёбиаза (это состояние также определяют как «носительство» амебных цист) характерны:
- бессимптомное течение;
- отсутствие трофозоитов-гематофагов;
- отсутствие патологических изменений при эндоскопических исследованиях;
- отсутствие специфических антител.
Только у незначительной части инфицированных амёбами лиц разовьется инвазивный амёбиаз. В странах, где Е.histolytica широко распространена, у 90% инфицированных лиц имеется неинвазивный амёбиаз, которые таким образом являются «бессимптомными носителями» просветных форм амёб, и только у 10% инфицированных развивается инвазивный амёбиаз [1, 2, 3] .
Патологические изменения и клинические проявления инвазивного амёбиаза варьируют в широких пределах от колита со слабо выраженными клиническими проявлениями до фульминантного колита и амёбного абсцесса печени. Наиболее частыми клиническими проявлениями инвазивного амёбиаза являются амёбный колит и амёбный абсцесс печени, причем амёбный колит встречается в 5-50 раз чаще, чем амёбный абсцесс печени [1] .
Основной причиной летальных исходов при амёбиазе являются абсцесс печени и фульминантный колит [14, 15, 16] .
Бессимптомное нахождение (носительство) просветных форм Е.histolytica в толстом кишечнике может отмечаться в течение многих лет. Однако в любой момент просветные формы могут перейти в тканевые формы, вызывающие «инвазивный» или клинически выраженный амёбиаз.
Первичные проявления амёбиаза заключаются в образовании небольших участков некроза в слизистой толстого кишечника, которые могут прогрессировать с образованием язв. Язва может увеличиваться не только по периферии за счёт подслизистого слоя, но и вглубь, достигая мышечной и даже серозной оболочки. Глубокий некротический процесс ведет к образованию перитонеальных спаек и является причиной прободных перитонитов. Амёбные язвы могут распространяться по всему протяжению толстого кишечника, но чаще локализуются в области слепой кишки.
Типичные амёбные язвы резко отграничены от окружающих тканей, имеют неровные края. На дне язвы — некротические массы, состоящие из фибрина и содержащие трофозоиты амёб. Воспалительная реакция слабо выражена. Некротический процесс в центре, подрытые и приподнятые края язвы, реактивная гиперемия и геморрагические изменения вокруг неё составляют наиболее типичные черты изъязвлений при кишечном амёбиазе.
Наряду с изменениями слизистой и некрозом, в кишечной стенке идет регенеративный процесс, ведущий к восстановлению дефекта путем образования фиброзной ткани. Такой процесс при хроническом амёбиазе может вести к образованию стриктур и стенозу кишечного просвета, обычно в восходящем и нисходящем отделах толстого кишечника. При присоединении вторичной бактериальной инфекции образуется экссудат, содержащий нейтрофилы, лимфоциты, гистиоциты, иногда эозинофилы.
При локализации поражений в ректосигмоидальном участке толстого кишечника клиническая картина может соответствовать дизентерийному синдрому с тенезмами и, относительно нечасто, с примесью слизи, крови и гноя. При локализации поражений в слепой кишке — обычно отмечаются запоры с болями в правой подвздошной области, характерные для клинической картины аппендицита (в ряде случаев действительно развивается аппендицит). Локализация амёбных поражений в подвздошной кишке втречается значительно реже [1, 17, 18] .
Острый кишечный амёбиаз (острый амебный колит) — обычно проявляется в виде одной диареи. Реже развивается синдром амёбной дизентерии: острое начало, схваткообразные боли в животе, тенезмы, жидкий стул с кровью и слизью. Высокая лихорадка и другие системные проявления, как правило не наблюдаются. У детей младшего возраста обычно отмечается лихорадка, рвота, дегидратация [1, 6, 18] .
Молниеносный амёбный колит (фульминантный колит). Тяжело протекающая некротизирующая форма кишечного амёбиаза, характеризующаяся токсическим синдромом, тотальными глубокими повреждениями слизистой кишечника, кровотечениями, перфорацией, перитонитом. Чаще отмечается у беременных женщин и женщин в послеродовом периоде. Может развиться после назначения кортикостероидов. Показатель летальности достигает 70% [15, 16, 17] .
Затяжной кишечный амёбиаз (первично хронический амёбиаз, постдизентерийный колит). Характерно нарушение моторики кишечника, разжиженный стул, запоры (в 50% случаев) или поносы чередующиеся с запорами, боли в нижней половине живота, тошнота, слабость, плохой аппетит. В ряде случаев хронический кишечный амёбиаз является следствием перенесенной амебной дизентерии [1] .
- Перфорация кишечника, чаще в области слепой кишки, реже в ректосигмоидальном участке, которая может вести к перитониту и абсцессу брюшной полости.
- Амёбный аппендицит
- Массивное кишечное кровотечение за счёт эрозии крупной артерии язвой.
- Амебома — опухолевидное разрастание в стенке толстого кишечника, преимущественно в восходящей, слепой и прямой кишках. Состоит из фибробластов, коллагена и клеточных элементов. Содержит относительно небольшое число амёб.
- Амёбная стриктура кишечника — образуется грануляционной тканью. Стриктуры обычно единичные и расположены в области слепой или сигмовидной кишки, содержат трофозоиты амёб; часто бессимптомны; иногда способствуют развитию запоров и частичной кишечной непроходимости.
Патологические изменения при внекишечном амёбиазе могут развиться практически во всех органах, однако чаще всего поражается печень.
У пациентов с амёбным абсцессом печени указания на перенесённый ранее кишечный амёбиаз выявляются только в 30-40% случаев, а амёбы в фекалиях обнаруживаются не более чем у 20% больных. Амёбный абсцесс печени чаще развивается у взрослых, чем у детей и у лиц мужского пола чаще, чем у женского [19] . Единичные или множественные абсцессы образуются чаще в правой доле печени. Абсцесс состоит из трех зон: центральной — зона некроза, содержащая жидкие некротические массы с примесью крови, обычно стерильную (бактериальная инфекция присоединяется в 2-3% случаев); средней, состоящей из стромы и наружной зоны, содержащей трофозоиты амёб и фибрин.
Для клиники амёбного абсцесса печени характерна лихорадка с ознобом и обильным потоотделением в ночное время; увеличение размеров печени и боль в области проекции печени, умеренный лейкоцитоз. При крупных абсцессах возможно развитие желтухи, что является плохим прогностическим признаком. При вовлечении в процесс диафрагмы выявляется высокое стояние её купола, ограничение подвижности; возможно развитие ателектазов.
Относительно часто (в 10-20% случаев) отмечается длительное скрытое или нетипичное течение абсцесса (например только лихорадка, псевдохолецистит, желтуха) с возможным последующим прорывом его, что может вести к перитониту и поражению органов грудной клетки [14, 20] .
Является следствием прорыва абсцесса печени через диафрагму в лёгкие, реже за счет гематогенного распространения амёб. Проявляется развитием эмпиемы плевры, абсцессами в лёгких и печёночно-бронхиальной фистулой. Характерна боль в грудной клетке, кашель, одышка, гной и кровь в мокроте, озноб, лихорадка, лейкоцитоз [1, 14] .
Обычно развивается за счёт прорыва абсцесса печени из левой доли через диафрагму в перикард, что может вести к тампонаде сердца и летальному исходу [1] .
Форма гематогенного происхождения. Абсцессы могут быть единичные и множественные; находятся в любом участке мозга, но чаще в левом полушарии. Обычно острое начало и молниеносное течение с летальным исходом [1] .
Встречается чаще у ослабленных и истощенных больных. Язвы обычно локализуются в перианальной области, на месте прорыва абсцессов в области фистулы. У гомосексуалистов возможны в области половых органов [1] .
Наиболее простым и надёжным методом диагностики кишечного амёбиаза является микроскопическое исследование фекалий для выявления вегетативных форм (трофозоитов) и цист [21] .
Трофозоиты обычно выявляются у больных в период диареи, а цисты — в оформленном стуле. С этой целью готовят нативные препараты непосредственно из фекалий и/или из обогащённых проб.
При первичной микроскопии исследуют нативные препараты из свежих проб фекалий с физиологическим раствором. В дальнейшем для идентификации трофозоитов амёб нативные препараты из свежих проб фекалий окрашивают раствором Люголя или буферным метиленовым синим. Для идентификации цист нативные препараты, приготовленные из свежих и/или обработанных консервантом проб фекалий окрашивают йодом. Выявление амёб более эффективно при немедленном исследовании фекалий после их забора.
При малом количестве паразитов в пробе фекалий исследование нативных препаратов может их не выявить. Поэтому дополнительно следует также использовать методы обогащения. В качестве метода обогащения обычно используется эфирформалиновое осаждение. Однако методом обогащения обычно можно выявить только цисты, так как трофозоиты деформируются. Выявление только цист амёб не подтверждает наличие болезни — инвазивного амёбиаза. Поэтому исследование нативных и окрашенных препаратов является обязательным начальным этапом микроскопического исследования, а использование методов обогащения показано в случаях, когда исследование нативных препаратов дает отрицательные результаты.
При наличии сомнений в видовой принадлежности трофозоитов и цист и необходимости длительного хранения препаратов, например с целью отправления их в референтную лабораторию для экспертной оценки, можно приготовить перманентно окрашенные препараты. Для этих целей обычно используют трихромовый метод окраски.
Наиболее простым и надёжным методом диагностики кишечного амёбиаза является исследование путем микроскопирования свежих фекалий. Для микроскопии необходим высококачественный микроскоп и подготовленный персонал. Однако даже опытный лаборант может не дифференцировать непатогенные простейшие, лейкоциты, макрофаги, содержащие эритроциты или частично переваренную растительную клетчатку от трофозоитов амёб, а также идентифицировать цисты простейших. При невозможности обеспечения качественной диагностики на месте возможна консервация фекалий с последующей их транспортировкой в специализированные лаборатории [21] .
При клинических данных, указывающих на возможное поражение кишечника, рекомендуется проведение ректо- или колоноскопии. При ректо- и колоноскопии целесообразно получение биопсии из поражённых участков кишечника с целью выявления амёб и дифференциальной диагностики, в частности, с карциномой. Этими методами можно выявить наличие язв в кишечнике, амёбомы, стриктуры и другие патологические изменения. Характерной чертой изменений при амёбиазе является очаговый, а не диффузный тип поражения [6, 12] .
Диагностика внекишечного амёбиаза, в частности абсцесса печени, проводится путем ультрасонографии и компьютерной томографии, которые позволяют определить локализацию, размеры и число абсцессов, а также контролировать результаты лечения. Рентгенологическое исследование позволяет выявить высокое стояние купола диафрагмы, наличие выпота в плевральную полость, абсцессы в лёгких.
При необходимости проводят аспирацию содержимого абсцесса. Амёбы редко находятся в центре некротических масс, и обычно локализуются в наружных стенках абсцесса. Для диагностики амёбиаза можно использовать серологические тесты с целью выявления специфических антител. Эти тесты особенно полезны для диагностики внекишечного амёбиаза, поскольку в этих случаях в фекалиях инвазивные стадии Е.histolytica как правило отсутствуют.
Поскольку назначение кортикостероидов при амёбиазе может способствовать резкому ухудшению течения болезни, серологическая диагностика также рекомендуется всем больным, у которых можно подозревать амёбиаз и которым планируется назначение кортикостероидов.
В целом все препараты, используемые для лечения амёбиаза можно разделить на 2 группы: «контактные» или «просветные» (воздействующие на кишечные просветные формы) и системные тканевые амебоциды [22] .
Для лечения неинвазивного амёбиаза (бессимптомных «носителей») используют просветные амебоциды (табл. 1). Просветные амебоциды также рекомендуется назначать после завершения лечения тканевыми амёбоцидами для элиминации амёб, оставшихся в кишечнике, с целью профилактики рецидивов. В частности, имеются наблюдения о развитии амёбных абсцессов печени у лиц с кишечным амёбиазом, получивших только тканевые амёбоциды без последующего назначения просветных амебоцидов [1, 14] . В частности, описан рецидив амебного абсцесса печени у больного через 17 лет после успешно излеченного впервые выявленного абсцесса печени [23] .
В условиях, когда невозможно предотвратить повторное заражение, применение просветных амебоцидов нецелесообразно. В этих ситуациях рекомендуется назначать просветные амёбоциды только по эпидемиологическим показаниям, например лицам, чья профессиональная деятельность может способствовать заражению других лиц, в частности, сотрудникам предприятий питания.
Для лечения инвазивного амёбиаза применяют системные тканевые амебоциды (табл. 2). Препаратами выбора из этой группы являются 5-нитроимидазолы, которые используют как для лечения кишечного амёбиаза, так и абсцессов любой локализации.
Метронидазол (Трихопол ® , Флагил ® )
Тинидазол (Тиниба ® , Фасижин ® )
Помимо препаратов из группы 5-нитроимидазолов для лечения инвазивного амёбиаза и прежде всего амёбных абсцессов печени рекомендуется использовать Дегидроэметин дигидрохлорид (в РФ не зарегистрирован) и Хлорохин (табл. 3) [7, 31] .
| Амёбиаз | 5-нитро- имидазолы 1 | Просветные амебоциды | Дегидро- эметин 2 | Хлорохин 3 |
|---|---|---|---|---|
| Неинвазивный (носительство) | /+ | + | | |
| Кишечный | + | + | + | |
| Внекишечный | + | + | + | + |
1 препараты группы 5-нитроимидазолов хорошо всасываются и как правило их назначают per os. Парентеральное (в/в) введение этих препаратов применяют у тяжёлых больных, у которых невозможен их пероральный прием.
2 вследствие возможных тяжёлых нежелательных реакций, прежде всего кардиотоксического эффекта, дегидроэметин является препаратом резерва и его рекомендуется назначать путем в/м инъекций больным с обширными абсцессами; больным, у которых предыдущие курсы 5-нитроимидазолов оказались неэффективны, а также тяжёлым больным, у которых невозможен прием препаратов per os.
3 хлорохин назначают в сочетании с дегидроэметином при лечении амёбных абсцессов печени.
Метронидазол — внутрь 30 мг/кг/сутки в 3 приёма в течение 8-10 дней
Тинидазол — до 12 лет — 50 мг/кг/сутки (макс. 2г) в 1 приём в течение 3 дней;
старше 12 лет — 2 г/сутки в 1 приём в течение 3 дней
Орнидазол — до 12 лет — 40 мг/кг/сутки (макс. 2 г) в 2 приёма в течение 3 дней;
старше 12 лет — 2 г/сутки в 2 приёма в течение 3 дней
Секнидазол — до 12 лет — 30 мг/кг/сутки (макс. 2 г) в 1 приём в течение 3 дней;
старше 12 лет — 2 г/сутки в 1 приём в течение 3 дней
Метронидазол — 30 мг/кг/сутки в 3 приёма в течение 8-10 дней
Тинидазол — до 12 лет — 50 мг/кг/сутки (макс. 2 г) в 1 приём в течение 5-10 дней;
старше 12 лет — 2 г/сутки в 1 приём в течение 5-10 дней
Орнидазол — до 12 лет — 40 мг/кг/сутки (макс. 2 г) в 2 приёма в течение 5-10 дней;
старше 12 лет -2 г/сутки в 2 приёма в течение 5-10 дней
Секнидазол — до 12 лет — 30 мг/кг/сутки (макс. 2 г) в 1 приём в течение 3 дней;
старше 12 лет — 2 г/сутки в 1 приём в течение 3 дней
Дегидроэметин дигидрохлорид — 1 мг/кг/сутки в/м (не более 60 мг) в течение 4-6 дней
Одновременно или сразу же после завершения курса дегидроэметина при амёбных абсцессах печени рекомендуется хлорохин — 600 мг основания в сутки в течение 2 дней, затем по 300 мг основания в сутки в течение 2-3 недель
После завершения курса 5-нитроимидазолов или дегидроэметина с целью элиминации оставшихся в кишечнике амёб применяют просветные амёбоциды:
Этофамид — 20 мг/кг/сутки в 2 приёма в течение 5-7 дней
Паромомицин -1000 мг/сутки в 2 приёма в течение 5-10 дней
В клинически выраженных случаях при соответствующем эпидемиологическом анамнезе, когда в фекалиях обнаруживают большое число непатогенных видов амёб, также рекомендуется проводить лечение амебоцидами, так как в этих случаях высокая вероятность сопутствующей инфекции Е.histolytica [1, 22] .
Неоднородность патологического процесса и клинических проявлений при амёбиазе в разных географических регионах, наличие штаммов, резистентных к стандартным схемам химиотерапии 5-нитроимидазолами, требуют варьирования схем лечения с учётом опыта, накопленного в конкретном районе [24, 25, 26] .
После успешной химиотерапии абсцесса печени остаточные полости обычно исчезают в течение 2-4 месяцев, однако возможна персистенция полостей до 1 года.
Тяжёлым больным с амёбной дизентерией, вследствие возможной перфорации кишечника и развития перитонита рекомендуется дополнительно назначать антибактериальные препараты, активные в отношении кишечной микрофлоры [22] .
Аспирация (или чрескожное дренирование) рекомендуется при больших размерах абсцесса (более 6 см), локализации абсцесса в левой доле печени или высоко в правой доле печени, сильной боли в животе и напряжении брюшной стенки вследствие возможной угрозы разрыва абсцесса, а также при отсутствии эффекта от химиотерапии в течение 48 часов от её начала. Аспирация рекомендуется также при абсцессах неясной этиологии. При невозможности закрытого дренажа, разрыве абсцесса и развитии перитонита проводится открытое оперативное лечение [14, 27, 28, 29] .
При назначении кортикостероидов у больных амёбиазом могут развиться тяжёлые осложнения, вплоть до развития токсического мегаколона. Всвязи с этим при необходимости лечения кортикостероидами жителей эндемичных зон, у которых высок риск инфицирования Е.histolytica, необходимо предварительное обследование на амёбиаз. При сомнительных результатах целесообразно превентивное назначение амебоцидов с последующим назначением кортикостероидов [1, 17] .
В настоящее время амёбиаз является практически полностью излечиваемым заболеванием при условии ранней диагностики и адекватной терапии.
Источником инфекции является человек, выделяющий с фекалиями цисты Е.histolytica. Заражение происходит при заглатывании цист с загрязнённой водой и продуктами питания, обычно через сырые овощи и фрукты, не подвергающиеся термической обработке.
Всвязи с вышесказанным можно заключить, что основными путями профилактики амёбиаза являются: улучшение санитарных условий, включающих водоснабжение и охрану пищевых продуктов; раннее выявление и лечение больных и бессимптомных носителей; санитарное просвещение [1, 31] . Наиболее эффективными путями профилактики амёбиаза являются — обезвреживание и удаление фекалий, предотвращение загрязнения пищи и воды, защита водоёмов от фекального загрязнения (цисты амёб могут выживать в воде в течение нескольких недель). Цисты Е.histolytica исключительно устойчивы к химическим дезинфектантам, включая хлорирование. Кипячение воды является более эффективным методом обеззараживания от амёб, чем применение химических средств. Амёбы быстро погибают при высушивании, нагревании до 55°С или замораживании.
Прямой фекально-оральный путь заражения через руки или загрязнённую пищу также вполне возможен [31] . Лица, являющиеся бессимптомными носителями амёб (в частности, имеются данные, что в некоторых регионах около 33% гомосексуалистов являются носителями Е.histolytica), работающие на предприятиях питания или участвующие в приготовлении пищи в домашних условиях, должны активно выявляться и подвергаться лечению, поскольку именно они являются основными источниками заражения [1, 30, 31] .
источник
Амебиаз – это опасное заболевание, возбудителем которого являются простейшие микроорганизмы — амебы. Паразитируя в организме человека? амебы вызывают тяжелое поражение кишечника, сопровождающиеся образованием язв и абсцессов.
Лечение амебиаза следует начинать на ранних стадиях болезни, так как она способна вызывать тяжелейшие осложнения. Наиболее опасными из них являются поражения печени, легких и головного мозга.
Одним из самых важных этапов в лечении амебиаза является своевременная диагностика заболевания. Она позволяет выявить заражение амебами даже в непроявленной фазе болезни, когда другие симптомы еще отсутствуют.
На начальном этапе болезни острый амебиаз можно спутать с другими инфекциями желудочно-кишечного тракта. Отличительными признаками этого заболевания являются:
- Сильная диарея от 4 до 6 раз в стуки в первые дли болезни, от 15 до 20 при дальнейшем развитии амебиаза;
- Легкое повышение температуры до 37℃ на начальном этапе заболевания и сильный жар выше 38,5℃ в последующие дни;
- Кал имеет примеси слизи и крови, а при тяжелом течение болезни он становится похожим на красное желе. Это объясняется тем, что на поздних этапах болезни он целиком состоит из слизи, а красный цвет приобретает за счет большого содержания крови.
- Выраженные тянущие или схваткообразные боли внизу живота, которые значительно усиливаются во время опорожнения кишечника;
- Постоянные позывы к дефекации, сопровождающиеся сильными болезненными ощущениями. Чаще всего они бывают ложными и при посещении туалета у больного выделяется незначительно количество кала и слизи.
- Постоянная жажда, которая лишь ненадолго проходит после принятой жидкости;
- Сильная, слабость, сонливость, полная потеря работоспособности.

Если же болезнь не была своевременно выявлена и не подвергалась адекватному лечению, то она переходит в хроническую форму. На этом этапе болезни также можно пройти диагностику.
Хронический амебиаз проявляется следующими симптомами:
- Неприятный привкус во рту, который нельзя перебить жевательной резинкой или зубной пастой;
- Потеря аппетита, непринятие пищи, что часто приводит к истощению больного;
- Сильная общая слабость;
- Заметное увеличение размеров печени;
- Бледная кожа и анемия у больного из-за снижения гемоглобина в крови;
- Боли в подложечной области;
- Нарушение работы сердца – тахикардия, аритмия, слабые сердечные удары;
- Появление налета, чувство жжения и даже боли на языке.
Для диагностики амебиаза необходимо сдать следующие анализы:
- Анализ кала;
- Серологический анализ крови;
- Биопсия;
- Неинвазивные методы исследования.
Для получения направления на анализы для выявления амебиаза больному необходимо посетить врача-терапевта. При получении положительных результатов он направит пациента к инфекционисту.
Наибольшее значения для диагностики амебиаза имеет анализ каловых масс больного. При этом результат диагностики считается положительным если в ходе анализа в кале были обнаружены:
- Примесь крови. При поражении кишечника амебами в кале всегда присутствуют следы крови.
- Недостаточное количество нейтрофилов. Нейтрофилы – это белые кровяные тельца, количество которых может падать при тяжелых инфекционных и паразитарных заболеваниях, так как они погибают в борьбе с патогенными микроорганизмами.
- Присутствия кристаллов Шарко-Лейдена. Они находятся в цитоплазме эозинофилов – разновидности лейкоцитов, отвечающих за уничтожение паразитов.
- Нахождение в кале гематофагов, а именно взрослых особей дизентерийной амебы (трофозоитов). Такой результат анализа считается самым надежным. Он позволяет поставить окончательный диагноз больному.

Кроме того, трофозоиты гибнут при взаимодействии с водой и сернокислым барием, а также при полном высушивание. Поэтому для правильной диагностики болезни необходимо сделать по меньшей мере три анализа кала.
Для исследования кала на наличие в нем взрослых особей амеб и их цист материал окрашивают с применением раствора Люголя и трехцветной окраски.
Эффективность этого метода анализа составляет 75-95%, поэтому он часто используется для подтверждения диагноза.
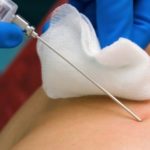
В такой ситуации можно прибегнуть к другим способам диагностики болезни, например, к биопсии краев кишечных язв при помощи колоноскопии.
Этот способ анализа дает высокие результаты, однако он может быть опасным при молниеносном амебном колите, так как может привести к прободению кишечника.
Важно отметить, что биопсия амебного абсцесса печени редко дает положительные результаты, поскольку в данном материале содержится небольшое количество трофозоитов.
Неинвазивные методы исследования – это методы диагностики заболеваний, которые осуществляются без вмешательства в организм человека. К ним относятся:
- Ультразвуковое исследование;
- Компьютерная томография;
- Магнитно-резонансная томография;
- Сцинтиграфия.
Неинвазивные методы исследования помогают установить амебный абсцесс печени. При ультразвуковом исследовании данное повреждение печени имеет вид темноного участка круглой либо овальной формы.
При относительно недолгом течение болезни у пациента, как правило, обнаруживается несколько небольших абсцессов печени. При длительном развитие внекишечного амебиаза небольшие абсцессы сливаются в один большей, образуя значительное повреждение органа.
Диагностика амебного абсцесса печени с помощью неинвазивных методов исследования помогает вовремя обнаружить тяжелые осложнения болезни такие как:
- Большой абсцесс (более 10 см), расположенный в верхней области правой стороны печени. Такой абсцесс часто приводит к прободению в плевральную полость.
- Множественные абсцессы или один большой абсцесс левой стороны печени. Нередко становятся причиной перфорации в полость перикардита.
Недостаток данного метода исследования заключается в том, что полученные данные не всегда бывают объективны и соответствую клинической картине заболевания. У многих пациентов на полное рассасывание амебного абсцесса печени уходит не менее полугода, а у некоторых почти год.
Иногда абсцесс печение может продолжать расти даже при правильном лечение болезни, что отнюдь не означает ухудшения состояния пациента.
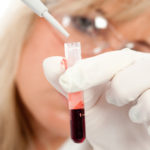
Врач-инфекционист может направить пациента на анализ крови, если после сильной диареи, сопровождающейся выделением крови, у больного появились болевые ощущения в правом подреберье, поднялась высокая температура и отмечается интоксикация. Это может говорить об образование абсцесса печени.
Серологический анализ крови не требует от пациента никакой особой подготовки. Для данного вида диагностики у больного берут кровь из вены, из которой в последствии получают сыворотку.
Именно с использованием сыворотки определяют какой титр антител присутствует у данного пациента. Этот анализ приводят в иммунологических лабораториях.
По итогам диагностики результат может быть:
- Положительный;
- Сомнительный;
- Отрицательный.
Отрицательный результат. Он говорит о полном отсутствии инфекции либо о непроявленной форме заболевания.
Сомнительный результат. При нем в крови больного выявляется низкий титр антител, который может означать неявную форму болезни или слабую работу иммунной системы пациента. Нередко такой результат выявляется у людей не больных амебиазом, но страдающих онкологией или какими-либо системными болезнями.
Положительный результат. Он характеризуется высочайшим титром антител. Такой результат анализа обычно получают люди, больные острой формой амебиаза.
Если при повторном анализе, проведенном через 14 дней, титр антител увеличился это сигнализирует о пике воспалительного процесса. Нередко данная цифра превышает первый результат в 4 и более раз. Если же титр наоборот понизился, то это означает скорое выздоровление больного.
Важно отметить, что серологический анализ крови не проводится при кишечном амебиазе, так как в этом случае он не позволит получить необходимых данных.
Елена Малышева расскажет о таком заболевании, как амебиаз в видео в этой статье.
источник
Амебиаз (амебная дизентерия) – протозойное заболевание, вызванное дизентерийной амебой (Entamoeba histolytica) характеризующееся язвенным поражением кишечника (кишечный амебиаз) и, в осложненных случаях, – формированием абсцессов печени, мозга и др. органов (внекишечный амебиаз). Кишечный амебиаз регистрируется в различных регионах мира, но наибольшую распространенность имеет в странах с тропическим и субтропическим климатом. Источником заболевания является больной человек или носитель, выделяющий цисты амеб с фекалиями. Цисты обладают высокой устойчивостью во внешней среде, что определяет водный, алиментарный и контактно-бытовой пути передачи возбудителя. Особенностью амебиаза является длительный инкубационный период (20–40 дней, в некоторых случаях до 3 месяцев).
Показания к обследованию: Пациенты с ОКИ с синдромом гемоколита.
Материал для исследований
- Образцы фекалий – микроскопические исследования, выявление ДНК E.histolytica;
- сыворотка крови – выявление АТ.
Этиологическая лабораторная диагностика включает визуальное обнаружение E.histolytica с использованием микроскопии, выявление ДНК E.histolytica, выявление АТ к АГ микроорганизма.
Сравнительная характеристика методов лабораторных исследований
Наиболее распространенным методом диагностики кишечного амебиаза является микроскопия образцов фекалий, которая позволяет выявить большую вегетативную (тканевую) форму амебы с фагоцитированными эритроцитами. Микроскопическое исследование рекомендуется проводить в два этапа. На первом этапе исследуют нативные или окрашенные препараты фекалий для выявления вегетативных форм возбудителя. При отрицательных результатах исследования необходимо провести предварительное обогащение образца, которое позволяет выявить цисты амеб.
Ложноположительные результаты исследования могут быть связаны с наличием в исследуемых образцах сапрофитных амеб. макрофагов, содержащих эритроциты, ферментированной клетчатки и др.
Обнаружение ДНК E. histolytica с использование методов АНК (преимущественно ПЦР), дает возможность с наибольшей специфичностью выявлять патоген, находит в последние годы все большее применение в диагностике кишечного амебиаза. Обнаружение ДНК методом ПЦР не позволяют дифференцировать острое заболевание от носительства просветных форм E. histolytica на фоне ОКИ другой этиологии.
Для выявления специфических АТ используют ИФА, РНИФ, РНГА. Методы определения АТ просты в применении, однако не позволяют дифференцировать текущее и недавно перенесенное заболевание и выявлять носителей просветных форм.
Для выявления амебных абсцессов при внекишечном амебиазе наиболее информативны различные формы лучевой диагностики.
Показания к применению различных лабораторных исследований
При проведении исследований в регионах с высокой распространенностью амебиаза (тропические и субтропические зоны), при наличии квалифицированных специалистов, имеющих опыт микроскопической диагностики амебиаза, целесообразно применение микроскопии как скринингового метода, обладающего большей универсальностью по отношению к спектру возбудителей, характерных для данных территорий.
При проведении исследований в неэндемичных регионах целесообразно применение комплекса методологически унифицированных тестов для выявления ДНК возбудителя методом ПЦР и исследований по выявлению специфических АТ для дифференцировки стадии заболевания и выявления носительства E. histolytica.
Применение инструментальных методов исследований является обязательным для исключения внекишечных осложнений амебиаза (наиболее частая форма – амебные абсцессы печени).
Особенности интерпретации результатов лабораторных исследований
При кишечном амебиазе безусловным подтверждением амебной этиологии поражения кишечника является обнаружение вегетативных форм амеб, фагоцитирующих эритроциты, при исследовании окрашенного или нативного препарата фекалий без их обогащения. Диагностическая чувствительность такого исследования у пациентов с подострым и хроническим течением заболевания бывает невысокой. Более высокая чувствительность достигается при использовании методов обогащения фекалий, однако они позволяют проводить концентрирование только цист амеб. Выявление цист имеет меньшее диагностическое значение и не позволяет подтвердить этиологию острых форм язвенного поражения кишечника. Результаты выявления ДНК тоже не позволяют проводить дифференцировку между вегетативными и просветными формами патогена, а также его цистами.
Выявление АТ к E.histolytica позволяет дифференцировать носительство просветных форм от заболевания, но может давать положительные результаты при недавно перенесенном заболевании. Особенно высокие уровень уровни АТ выявляют у пациентов с внекишечными осложнениями в виде амебных абсцессов.
Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.
Copyright ФБУН Центральный НИИ Эпидемиологии Роспотребнадзора, 1998 — 2019
Центральный офис: 111123, Россия, Москва, ул. Новогиреевская, д.3а, метро «Шоссе Энтузиастов», «Перово»
+7 (495) 788-000-1, info@cmd-online.ru
! Продолжая использовать наш сайт, вы даете согласие на обработку файлов cookie, пользовательских данных (сведения о местоположении; тип и версия ОС; тип и версия Браузера; тип устройства и разрешение его экрана; источник откуда пришел на сайт пользователь; с какого сайта или по какой рекламе; язык ОС и Браузера; какие страницы открывает и на какие кнопки нажимает пользователь; ip-адрес) в целях функционирования сайта, проведения ретаргетинга и проведения статистических исследований и обзоров. Если вы не хотите, чтобы ваши данные обрабатывались, покиньте сайт.
источник
Самая простая и надёжная диагностика амебиаза кишечного — микроскопическое исследование фекалий для выявления вегетативных форм (трофозоитов) и цист. Трофозоиты лучше выявлять у больных при диарее, а цисты — в оформленном стуле. При первичной микроскопии исследуют нативные препараты из свежих проб фекалий с физиологическим раствором. Для идентификации трофозоитов амёб нативные препараты окрашивают раствором Люголя или буферным метиленовым синим. Для идентификации цист нативные препараты, приготовленные из свежих или обработанных консервантом проб фекалий, окрашивают йодом. Выявление амёб более эффективно при немедленном исследовании фекалий после назначения слабительного. В практике используют также методы обогащения, в частности эфирформалиновое осаждение. Однако методом обогащения можно выявить только цисты, так как трофозоиты деформируются. Обнаружение только цист амёб не подтверждает наличия инвазивного амёбиаза. В последние годы разработан чувствительный и специфичный метод ПЦР, позволяющий относительно просто и быстро идентифицировать в фекалиях одновременно Е. histolytica и Е. dispar.
При клинических данных, указывающих на возможное поражение кишечника, рекомендуют проводить ректо- или колоноскопию с получением биопсийного материала. Этими методами можно выявить язвы в кишечнике, амебомы, стриктуры и другие патологические изменения. Характерная черта изменений при амёбиазе — очаговый, а не диффузный тип поражения. Диагностика амёбиаза внекишечного, в частности абсцесса печени, проводится с помощью УЗИ и КТ, которые позволяют определять локализацию, размеры, число абсцессов, а также контролировать результаты лечения. Рентгенологическое исследование позволяет выявить высокое стояние купола диафрагмы, наличие выпота в плевральную полость, абсцессы в лёгких. При необходимости аспирируют содержимое абсцесса печени, однако вероятность выявления амёб в некротических массах невелика, так как они обычно расположены по периферии области поражения.
Специфические противоамёбные антитела с помощью серологических методов (ИФА, НРИФ) обнаруживают у 75-80% больных инвазивным кишечным амёбиазом и у 96-100% — при внекишечных поражениях; даже у бессимптомных носителей Е. histolytica положительные результаты могут достигать 10%. Эти тесты особенно полезны для диагностики внекишечного амёбиаза. поскольку в этих случаях в фекалиях инвазивные стадии Е. histolytica, как правило, отсутствуют. В эндемических очагах серологическая диагностика амебиаза рекомендуется для всех больных с подозрением на амёбиаз, которым планируют назначить глюкокортикоиды.

Консультация хирурга при необходимости дифференциальной диагностики с хирургическими заболеваниями или подозрении на хирургические осложнения, при абсцессе печени; консультация пульмонолога — при абсцессе лёгкого.
Клинические, эпидемиологические, режим во время обострений полупостельный, стол № 2, 4.
Дифференциальная диагностика амебиаза проводится с балантидиазом, шигеллёзом, кампилобактериозом, язвенным колитом, в тропических странах — с некоторыми гельминтозами, протекающими с проявлениями гемоколита (кишечный шистосомоз, трихоцефалёз и др.).

источник
Амебиаз — протозойная инфекционная болезнь, характеризующаяся язвенным поражением толстой кишки, склонностью к образованию абсцессов в различных органах и хроническому течению.
Амебиаз — протозойная инфекционная болезнь, характеризующаяся язвенным поражением толстой кишки, склонностью к образованию абсцессов в различных органах и хроническому течению.
Амебиаз распространен преимущественно в странах тропического и субтропического климата. По данным ВОЗ, около 10% мировой популяции людей инфицировано амебами. Ежегодная заболеваемость амебиазом составляет 50 млн случаев, летальность — 0,2%. Наиболее распространена инфекция в Индии, в Южной и Западной Африке (Нигерия, Гана и др.), в Корее и Китае, в Южной и Центральной Америке. Широкому распространению амебиаза в этих странах способствуют низкий уровень санитарных условий и невысокий социально-экономический статус. Заболеваемость амебиазом в виде спорадических случаев регистрируется в Средней Азии. В связи со значительным увеличением зарубежного туризма, притоком мигрантов из стран дальнего и ближнего зарубежья в последние годы возросло число случаев амебиаза среди граждан России. Риск заболевания амебиазом выше в Закавказье и Нижнем Поволжье.
Клиника амебной дизентерии была описана еще в трудах древнегреческого целителя Гиппократа. В последующем, в средние века, Авиценна в своем «Каноне» приводит клиническую характеристику заболевания, сопровождающегося кровавым поносом и язвенным поражением толстого кишечника.
Возбудителя болезни (дизентерийную амебу) впервые обнаружил Ф. А. Леш в 1875 г. в Петербурге в кале больного, длительное время страдавшего кровавым поносом, назвав ее Amoeba coli. Ф. А. Леш описал морфологию вегетативной стадии амебы с фагоцитированными эритроцитами и изменения в кишечнике при амебиазе. Кроме того, Ф. А. Лешем были предложены методы лабораторной диагностики амебной дизентерии, актуальные и в настоящее время.
В 1883 г. Р. Кох в Египте, проводя патологоанатомическое исследование больных, впервые обнаружил амеб в гистологических срезах тканей кишечных язв и стенках абсцесса печени. В 1891 г. Каунсильмен и Леффлер выделили заболевание в самостоятельную нозологическую форму под названием амебной дизентерии. В настоящее время оно сохраняется для обозначения амебного поражения кишечника, а под названием «амебиаз» подразумевается поражение любого органа Entamoeba histolytica. Ф. Шаудин в 1903 г., изучив морфологию и биологию амеб, обитающих в кишечнике, дифференцировал их и назвал патогенную амебу Entamoeba histolytica, а непатогенную — Entamoeba coli.
В 1912 г. в практику лечения амебиаза был введен солянокислый эметин, отличающийся высокой амебоцидной активностью.
Учитывая отcутствие патологических изменений в кишечнике во многих случаях паразитирования E. histolytica, Э. Брумпт в 1925 г. разделил E. histolytica на два самостоятельных вида: патогенный (E. dysenteria) и непатогенный (E. dispar).
Большинство видов амеб, обитающих в кишечнике человека, не являются патогенными (Entamoeba dispar, Entamoeba hartmanni, Entamoeba coli, Endolimax nana, Iodamoeba butschlii и Blastocystis hominis), только Е. histolytica может вызывать инвазивные инфекции у человека.
Возбудитель амебиаза — E. histolytica относится к царству Protista, типу Amoebozoa, классу Archamoebae, семейству Entamoebidae, роду Entamoeba.
Жизненый цикл Е. histolytica включает две стадии: вегетативную (трофозоит) и стадию покоя (циста).
Цисты обеспечивают сохранение вида во внешней среде. Они обнаруживаются в испражнениях реконвалесцентов и цистоносителей.
Попав в нижние отделы тонкой кишки, цисты эксцистируются, давая поколение трофозоитов, размножающихся активных паразитов, которые мигрируют в другие отделы кишки.
Выделяют четыре формы вегетативной стадии возбудителя (трофозоитов): тканевую, Е. histolytica forma magna (эритрофаг), просветную — Е. histolytica forma minuta, предцистную. В просвете толстой кишки обитает просветная форма, питается детритом и бактериями, не причиняя вреда хозяину. Просветная форма Е. histolytica имеет округлую или овальную форму, размер 20 мкм, подвижная, в ее вакуолях содержатся бактерии. Она никогда не фагоцитирует эритроциты. Ее выявляют у лиц, перенесших острую форму кишечного амебиаза, у больных хроническим амебиазом в период ремиссии, а также у носителей.
Заболевание развивается лишь при переходе просветной формы в тканевую. Тканевые формы амеб обнаруживаются только при остром амебиазе непосредственно в пораженной ткани, в испражнениях редко. Их размеры достигают 30–40 мкм и более. Трофозоиты, внедряясь в слизистую и подслизистую оболочки толстого кишечника, приобретают при этом способность фагоцитировать эритроциты, превращаясь в эритрофаг, вызывают некроз и появление язв.
Предциста является переходной формой Е. histolytica от просветной к цисте. Ее размер 10–18 мкм. Заглоченных бактерий, эритроцитов и других клеточных элементов не содержит.
Все формы вегетативной стадии Е. histolytica быстро погибают во внешней среде.
Источником возбудителя инфекции является человек, выделяющий с фекалиями цисты амеб. Механизм передачи фекально-оральный. Пути передачи — водный, алиментарный, контактно-бытовой. Факторами передачи амебиаза могут быть пищевые продукты, почва, вода, предметы обихода. Возможна передача амеб половым путем среди гомосексуалистов. Степень пораженности населения зависит от условий быта, водоснабжения, санитарного состояния населенных пунктов. Болезнь распространена в зонах с жарким и сухим климатом и носит преимущественно спорадический характер.
Цисты Е. histolytica, попавшие в желудок с водой или пищей, поступают в кишечник без существенных изменений. В тонком кишечнике оболочка цисты растворяется, из освободившейся амебы после ее деления образуется 8 одноядерных амеб — трофозоитов, которые опускаются к месту своего паразитирования — в верхние отделы толстой кишки, где продолжают размножаться и где формируется просветная форма амеб, которые живут в просвете толстой кишки, питаясь бактериями, грибами, детритом. В этом случае развитие инвазии может протекать по типу бессимптомного носительства. Под воздействием ряда факторов (иммунодефицитное состояние, дисбиоз толстой кишки, голодание, стресс и др.), просветные формы дизентерийной амебы могут превращаться в тканевые формы паразитов. Под воздействием цитолизинов и протеолитических ферментов амеб происходит повреждение слизистой оболочки, где возбудитель интенсивно размножается, образуется первичный очаг в виде микроабсцесса, который вскрывается в полость кишки с образованием язвы. Язвы имеют неровные подрытые края, дно покрыто некротическими массами темно-серой окраски, располагаются группами или поодиночке, часто в поперечном направлении. Они могут сливаться между собой, образуя обширные, до нескольких сантиметров, поражения. На слизистой кишечника отсутствует синхронность в степени развития язв, т. е. можно одновременно обнаружить мелкие эрозии, «цветущие язвы», заживающие язвы и рубцы после заживших язв. Чаще язвенный процесс развивается в слепой и восходящей частях толстой кишки, реже в сигмовидной и прямой кишках. Возможно поражение всей толстой кишки. При хроническом амебиазе в стенке кишки скапливается большая масса грануляционной ткани в форме опухолевидного образования — амебомы.
В результате проникновения амебы в брыжеечные сосуды происходит занос паразита в другие органы, где развиваются абсцессы. Наиболее часто абсцессы формируются в печени, реже в легких, головном мозге, почках, поджелудочной железе.
Приобретенный иммунитет при амебиазе является нестойким и нестерильным, не защищает от рецидивов и реинфекции.
В зависимости от клинических проявлений выделяют следующие формы амебиаза:
а) кишечный амебиаз — острый и хронический;
б) внекишечный:
• амебный абсцесс печени;
• амебный абсцесс легких;
• амебный абсцесс мозга;
• мочеполовой амебиаз;
• кожный амебиаз.
Кишечный амебиаз, или амебная дизентерия, — основная и наиболее часто встречающаяся форма инфекции. Инкубационный период длится от 1–2 недель до нескольких месяцев. Начало болезни может быть острым или с продромальными явлениями, в виде недомогания, головной боли, понижения аппетита. Основным симптомом заболевания является расстройство стула. Вначале стул каловый, обильный, со слизью, 5–6 раз в сутки, через 4–7 дней он теряет каловый характер, представляет собой стекловидную слизь с примесью крови, приобретая вид «малинового желе». В острой фазе болезни возможны постоянные схваткообразные боли в животе. Возможны варианты преимущественного поражения разных отделов толстой кишки. Нередко наблюдается биполярный цекосигмоидный вариант. В случаях поражения прямой кишки появляются мучительные тенезмы. При амебном тифлите возможно поражение червеобразного отростка, что проявляется симптомами аппендицита.
Температура тела нормальная или незначительно повышена. Интоксикация не выражена. Живот вздут, при пальпации мягкий, болезненный по ходу толстого кишечника.
При колоноскопии обнаруживают отечность, очаги гиперемии 5–15 мм в диаметре, на складках слизистой оболочки появляются мелкие приподнятые узелки, на месте которых через 1–2 недели формируются язвы с отечными, подрытыми краями и дном с некротическими массами. Язвы окружены пояском гиперемии, слизистая оболочка вне зон поражения мало изменена.
Острые проявления кишечного амебиаза сохраняются обычно 4–6 недель. Затем состояние больных улучшается, наступает ремиссия (от нескольких недель до нескольких месяцев). При отсутствии лечения болезнь приобретает хронический характер с рецидивирующим или непрерывным течением. Длительность хронического амебиаза без специфического лечения возможна десятилетиями. Развиваются астения, анемия, похудание, вплоть до кахексии. В периферической крови наблюдаются признаки анемии, эозинофилия, моноцитоз, лимфоцитоз, увеличение СОЭ.
У ослабленных лиц, на фоне лечения глюкокортикостероидами, у беременных, у детей до двух лет наблюдается молниеносная кишечная форма амебиаза, для которой характерны обширные изъявления толстой кишки, кровотечения, перфорация, перитонит, токсический синдром.
В редких случаях у больных обнаруживают амебому — специфическую воспалительную гранулему, локализующуюся чаще в слепой и восходящей кишках. При пальпации живота ощущается как опухолевидное образование. При эндоскопии может ошибочно расцениваться как рак или саркома. Исчезает после специфической терапии.
При кишечном амебиазе могут развиться осложнения: перфорация кишечной язвы, перитонит, кишечное кровотечение, отслойка слизистой оболочки и ее гангрена, специфический аппендицит, стриктура кишки, выпадение прямой кишки, присоединение вторичной инфекции.
Из внекишечных форм амебиаза наиболее часто встречается амебный абсцесс печени. Он может развиться при остром кишечном амебиазе или спустя несколько месяцев. Однако указания на кишечный амебиаз в анамнезе имеются лишь у 30–40% больных, а амебы в фекалиях обнаруживаются в 20% случаев. Одиночные абсцессы локализуются в задней правой доле печени и в верхних отделах. Начало заболевания острое с повышения температуры тела до 39 °С и выше, интоксикации. Лихорадка ремиттирующего, гектического, постоянного или неправильного характера, сопровождается ознобами и обильным потоотделением, болями в правом подреберье. Кожные покровы приобретают землистый оттенок, черты лица заострены. Печень увеличена, болезненна в зоне повреждения. Боли усиливаются при кашле, сотрясении и перемене положения тела. Однако при глубоком расположении абсцесса боли могут отсутствовать. Иногда развивается желтуха. Продолжительность симптомов не более 10 дней. В таких случаях быстро развиваются осложнения амебного абсцесса печени: прорыв в брюшную полость с развитием перитонита или в сердечную сумку с развитием перикардита. Летальность при таком течении болезни без специфического лечения достигает 25% и выше.
Амебиаз легких развивается при гематогенном заносе амеб в легкие или при прорыве абсцесса печени в плевральную полость. Характерным для них является — лихорадка, озноб, боль в грудной клетке, кашель, кровохарканье. Рентгенологически определяется полость в пораженном легком. Абсцессы легких нередко приводят к гнойному плевриту, эмпиеме, пневмотораксу, печеночно-легочным свищам.
При возникновении амебных абсцессов в головном мозге у больных отмечают развитие очаговых и общемозговых симптомов. Неврологическая симптоматика зависит от локализации абсцессов и степени поражения мозговых центров. Прижизненная диагностика затруднена.
Описаны амебные абсцессы селезенки, почек, женских половых органов.
У истощенных и ослабленных больных встречается кожный амебиаз, который проявляется эрозиями и язвами, малоболезненными на коже перианальной области, промежности, ягодиц, живота.
Наиболее надежным методом диагностики кишечного амебиаза является ректороманоскопия с немедленной микроскопией ректального мазка. Промежуток времени от момента выделения фекалий до исследования не должен превышать 15–20 мин. В первую очередь исследованию подлежат неоформленные фекалии со слизью и кровью, так как именно в них находятся вегетативные формы амеб. Исследуемый материал помещают в чистую сухую посуду, стерилизованную только кипячением, так как вегетативные формы амеб весьма чувствительны к химическим веществам (дезсредствам).
Более точным методом диагностики является колоноскопия с биопсией язвенных поражений, где обнаруживаются гематофаги амеб.
Учитывая, что не всегда удается обнаружить амеб в кале, используются серологические методы диагностики: реакция непрямой гемагглютинации, реакция иммунофлуоресценции, иммуноферментный анализ и др.
В случаях внекишечного амебиаза необходимо комплексное инструментальное обследование (рентгенологические, ультразвуковые методы исследования, сканирование, томография) с учетом специфической локализации абсцесса, обусловленного гистолитической амебой.
Препараты, используемые для лечения амебиаза, можно разделить на две группы:
1. Просветные амебоциды: Этофамид, Клефамид, Дилоксанида фуроат, Паромомицин (упомянутые препараты в России не зарегистрированы).
Препараты этой группы используют для лечения бессимптомных носителей, а также после завершения лечения тканевыми амебоцидами с целью профилактики рецидивов.
2. Системные тканевые амебоциды (5-нитромидазолы): метронидазол, тинидазол, орнидазол, секнидазол.
Тканевые амебоциды применяют для лечения кишечного амебиаза и абсцессов любой локализации.
Хорошую переносимость продемонстрировали дилоксанида фуроат и паромомицин, которые практически не всасываются в кровь.
Применение антибиотиков показано в случае непереносимости метронидазола и при развитии перфорации кишечника с перитонитом.
Сочетания препаратов, дозы, курсы терапии зависят от формы и тяжести амебиаза.
Препаратом выбора для этиотропной терапии является метронидазол (Флагил), назначаемый по 750 мг × 3 раза в сутки внутрь, курс 10 дней.
При непереносимости метронидазола:
- тетрациклин по 250 мг × 4 раза в день, 10 дней;
- эритромицин внутрь по 500 мг × 4 раза в день, 10 дней.
При нетяжелой форме кишечного амебиаза и амебоносительстве рекомендуется:
- дилоксанида фуроат внутрь по 500 мг 4 раза в день, 10 дней;
- парамомицин внутрь по 30 мг/кг 3 раза в день, курс 10 дней;
- тинидазол (Фазижин) по 0,6 2 раза в день, 5 дней;
- орнидазол (Тиберал) по 500 мг 2 раза в день, 5–10 дней.
При амебном абсцессе печени: метронидазол по 750 мг 3 раза в день, 10 дней, или по 500 мг в/в 4 раза в день, курс 10 дней, или по 2,4 г в день внутрь, 1–2 дня. Одновременно антибиотики широкого спектра действия в течение 10 дней.
Хирургическое лечение проводится при угрозе прорыва абсцесса или при неэффективности консервативной терапии.
В комплекс лечения колитического синдрома включают Энтероседив по 2 таблетки 3 раза в день, 10 дней.
Основным подходом к профилактике амебиаза является улучшение жилищных условий и водоснабжения, повышение безопасности пищевых продуктов, раннее выявление и лечение больных и цистоносителей, санитарное просвещение.
Так как цисты E. histolytica чрезвычайно устойчивы к химическим дезинфицирующим средствам, в том числе к препаратам хлора, и могут выживать при разных уровнях pH и осмотического давления, следует употреблять кипяченную воду. В эндемичных регионах, в связи с возможной контаминацией цистами дизентерийной амебы пищевых продуктов, в частности, фруктов и овощей, лучше употреблять в пищу только термически обработанные продукты и фрукты с сохранившей целостность оболочкой.
- Ющук Н. Д., Венгеров Ю. Я. Лекции по инфекционным болезням. 3-е изд., перераб. и доп. М.: ОАО «Издательство медицина», 2007. 1032 с.
- Ющук Н. Д., Островский Н. Н., Мартынов Ю. В., Матвеева С. М., Огиенко О. Л. Инфекционные и паразитарные болезни в схемах и таблицах. М.: ФГОУ «ВУНЦ Росздрава», 2008. 444 с.
- Лысенко А. Я., Владимова М. Г., Кондрашин А. В., Майори Дж. Клиническая паразитология. ВОЗ Женева, 2002. 734 с.
- Лысенко А. Я., Горбунова Ю. П., Авдюхина Т. И., Константинова Т. И. Лабораторная диагностика кишечных протозоозов. Уч. пособие. М., 2007. 43 с.
- Бронштейн А. М., Малышев Н. А., Лучшев В. И. Амебиаз: клиника, диагностика, лечение. Методическое пособие. М.
Н. Х. Сафиуллина, кандидат медицинских наук
Н. Д. Ющук, доктор медицинских наук, профессор, академик РАМН
Г. К. Аликеева, кандидат медицинских наук
Е. В. Кухтевич, кандидат медицинских наук
источник
