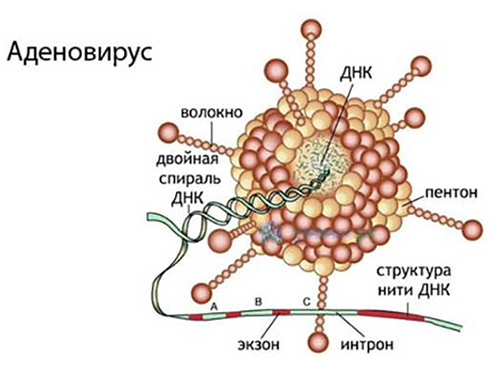
Что представляет собой аденовирус? Чем он опасен? Как от него защититься? Попробуем разобраться с поставленными вопросами.
Аденовирус (с греческого «aden» — железа и латинского «virus» — яд) впервые выделен в 1953 году группой американских учёных-вирусологов. Они обнаружили неизвестный вирус в аденоидах (увеличенная глоточная миндалина) ребёнка. Позже аденовирус находили в смывах из носоглотки у больных пневмонией, конъюнктивитом, фарингитом.
Аденовирусы — это семейство ДНК-содержащих вирусов, размножающихся в клетках животных и людей. Всего известно около 100 серотипов вируса. Серотипы 1, 2, 3, 4, 7, 14, 21, 34, 35 вызывают острую респираторную инфекцию и поражение глаз. Аденовирус 8-го серотипа связан с поражением роговицы (кератит). Тяжёлые пневмонии и бронхиты вызывают серотипы 34, 35, 7, 1, 21, 2, 5, 31.
Они являются причиной острых респираторных заболеваний (простуд) примерно в 10% случаев.
Респираторная вирусная инфекция является одним из основных факторов, способных вызывать обструкцию дыхательных путей, и может быть как триггером обострения бронхиальной астмы (БА), так и этиологическим фактором, формирующим БА у предрасположенных к ней людей.
По данным эпидемиологических исследований, 75–80% обострений БА связаны с острыми респираторными вирусными инфекциями (ОРВИ). В 89% случаев вирусная инфекция у больного астмой вызывает ее обострение [1]. То есть из десяти пациентов с астмой, заболевших респираторной вирусной инфекцией, у девяти усиливаются симптомы астмы. Существует корреляция (особенно выражена у детей) между сезонным подъемом заболеваемости ОРВИ и частотой госпитализаций в связи с обострением БА [2]. Более чем у 40% детей от четырех до 12 лет, страдавших БА, через восемь недель после ОРВИ сохранялась РНК риновируса. Речь идет о детях, у которых приступы астмы носили более тяжелый характер [3]. Кроме того, установлена связь между летальными обострениями астмы и респираторной вирусной инфекцией [4].
На фоне риновирусной инфекции ухудшаются показатели функции внешнего дыхания, повышается уровень эозинофилов в крови и эозинофильная инфильтрация слизистой бронхов [5]. Респираторная вирусная инфекция может способствовать развитию сенсибилизации. В то же время дети и подростки, страдающие аллергическими заболеваниями, склонны к частым острым респираторным заболеваниям. При этом спектр возбудителей ОРВИ у пациентов с аллергической патологией значительно шире и ассоциации вирусов более разнообразны, чем у детей без аллергии [6].
В 2008 г. эксперты Европейской академии аллергологии и клинической иммунологии (European Academy of Allergology and Clinical Immunology – ЕААCI) и Американской академии аллергологии, астмы и иммунологии (American Academy of Allergology, Asthma and Immunology – ААААI) предложили выделять четыре фенотипа БА у детей старше двух лет – аллергениндуцированную, вирусиндуцированную, астму физического напряжения и неопределенную астму. В частности, вирусиндуцированной называют астму, связанную с респираторной вирусной инфекцией. Вместе с тем необходимо понимать, что подобное деление условно, ОРВИ может вызвать обострение при любой форме астмы. В клинической практике нередки ситуации, когда у ребенка с атопией (аллергическим ринитом или атопическим дерматитом либо латентной бытовой сенсибилизацией) первый приступ удушья возникает на фоне вирусной инфекции. Впоследствии, в ближайший год или несколько лет, обострения астмы возникают только на фоне ОРВИ. В таких случаях, особенно когда не проведено аллергологическое обследование, у врача складывается впечатление, что это тип астмы, который ранее называли инфекционно-аллергическим или инфекционно-зависимым. Как следствие – неправильный выбор тактики ведения пациента.
Свистящее дыхание способны вызывать различные вирусы: респираторно-синцитиальный вирус (РСВ), риновирусы, вирусы гриппа А и В, аденовирусы, вирусы парагриппа, коронавирусы, энтеровирусы и др. Как правило, у взрослых и детей старшего возраста причиной бронхиальной обструкции становятся риновирусы – вирусы семейства Picornaviridae [7]. У детей младшего возраста основную роль в возникновении обструкции играет РСВ – РНК-вирус семейства Paramixoviridae [8]. Клинические проявления зависят от возраста, факторов риска и типа респираторного вируса (см. таблицу).
Результаты крупного проспективного исследования [9] показали, что бронхиолит, вызываемый РСВ, является самым существенным фактором риска развития не только астмы, но и атопии у детей в возрасте до трех лет. Обструкция у детей раннего возраста, спровоцированная РСВ, при повторном инфицировании не у всех вызывает свистящие хрипы, тем не менее рассматривается как фактор риска возникновения астмы. Риск максимален при отягощенном аллергологическом семейном анамнезе и генетической предрасположенности к БА. Однако РСВ провоцирует формирование астмы и в отсутствие атопии [10].
В тех случаях, когда БА дебютирует после респираторно-синцитиальной вирусной инфекции, можно выделить дополнительные предрасполагающие факторы: курение матери, наличие у нее БА, повышенный уровень общего иммуноглобулина (Ig) E в сыворотке крови [11].
Эксперты Европейского респираторного общества (European Respiratory Society – ERS) определили наиболее значимые факторы, способствующие развитию вирусиндуцированной БА:
генетические особенности, детерминирующие восприимчивость организма к тяжелым вирусным инфекциям;
нарушения во врожденном и адаптивном иммунном ответе на вирусную инфекцию [12].
В частности, наблюдается дефицит продукции эпителиальными клетками антивирусных интерферонов (ИФН) 1-го типа – ИФН-альфа и ИФН-бета. Клетки астматических пациентов продуцируют в 2,5 раза меньше ИФН-бета. Имеет также место дефицит ИФН 3-го типа – ИФН-лямбда.
Перечислим основные непосредственные механизмы обострения БА на фоне вирусной инфекции:
увеличение гиперреактивности дыхательных путей;
неспецифические и специфические иммунные механизмы. На фоне ОРВИ наблюдается усиление сенсибилизации к ингаляционным неинфекционным аллергенам, а также образование специфических противовирусных IgE. Уровень общего IgE при ОРВИ возрастает у пациентов с атопией и не изменяется у лиц, не страдающих атопическими заболеваниями [13]. В ряде случаев можно выявить только местное повышение концентрации IgE в назофарингеальных смывах и бронхоальвеолярном лаваже. Респираторные вирусные инфекции способны усиливать реакции гиперчувствительности как замедленного, так и немедленного типа в ответ на аллергенную стимуляцию;
нарушение нейрорегуляторных механизмов: повышение активности парасимпатической нервной системы за счет снижения функциональной активности M2-рецепторов и M2-независимых факторов, увеличение высвобождения нейропептидов, снижение уровня нейтральной эндопептидазы, снижение продукции NO;
структурно-механические изменения стенки бронхов (утолщение бронхиальной стенки, заполнение просвета мелких бронхов слизью, клеточным детритом).
Все указанные механизмы в большинстве случаев взаимосвязаны.
Увеличение уровня гиперреактивности бронхов при респираторной вирусной инфекции – основной фактор, приводящий к бронхообструкции. Гиперреактивность обычно развивается и у здоровых людей во время острой инфекции [14] и усиливается не только на фоне непосредственного влияния вируса, но и в результате аллергического воспаления, индуцированного ОРВИ.
В.И. Пыцкий считает, что роль вирусной, особенно респираторно-синцитиальной, инфекции в раннем детском возрасте скорее всего сводится к «отбору» и подготовке к развитию БА у детей c генетически детерминированной гиперреактивностью бронхов. Если не найдется подходящего причинно-значимого фактора или условий для реализации его действия, имеющаяся гиперреактивность будет существовать без прогрессирования в БА [15].
В настоящее время особое значение при формировании сенсибилизации придается гистогематическим барьерам, в частности нарушению барьерной функции слизистых оболочек различного генеза [16]. По мнению И.С. Гущина, состояние гистогематических барьеров, а именно кожи и слизистых оболочек, считается фактором, «делающим ненужным или, напротив, вынуждающим отреагировать аллергическим ответом». В связи с этим роль вирусной инфекции при формировании респираторной сенсибилизации может быть одной из главных. Эпителиальные клетки дыхательных путей – первая мишень респираторной вирусной инфекции. Известно выраженное цитопатическое действие на эпителий, оказываемое вирусами гриппа и РСВ, что приводит к функциональным изменениям как самого эпителия, так и дыхательной мускулатуры.
Кроме того, вследствие повреждения эпителия бронхов обнажаются окончания нервных волокон, которые под действием поллютантов и воспалительных медиаторов выделяют бронхоконстрикторные нейропептиды.
Естественно, роль дыхательного эпителия не сводится только к функции механического барьера. Эти клетки играют центральную роль в вирусной модуляции воспалительного процесса при БА, прежде всего через выход разноообразных цитокинов, хемокинов и факторов роста. В сочетании с аллергеном респираторная вирусная инфекция усиливает степень воспаления дыхательных путей.
В воспалении нижних дыхательных путей, ассоциированном с риновирусной инфекцией, участвуют эозинофилы [15]. У больных астмой эозинофилия, развивающаяся на фоне ОРВИ, сохраняется и в периоде реконвалесценции [14, 17]. Активация эозинофилов респираторным вирусом приводит к значительному выбросу медиаторов, в том числе липооксигеназных метаболитов арахидоновой кислоты – лейкотриенов (LT). Способностью активировать эозинофилы, а также увеличивать уровень LTС4 в назальном секрете больных астмой обладают риновирус и РСВ [18, 19]. В то же время повышение уровня эозинофилов после аллергенной провокации у больных астмой намного существеннее, чем при вирусиндуцированном обострении. Респираторная вирусная инфекция способствует большему притоку в дыхательные пути нейтрофилов и характеризуется нейтрофильной инфильтрацией в сочетании с дегрануляцией эозинофилов [1], то есть приводит к смешанному, эозинофильно-нейтрофильному воспалению.
Лечение вирусиндуцированного обострения БА можно разделить на два основных направления – лечение респираторной вирусной инфекции и противоастматическую терапию.
Специфических противовирусных препаратов, влияющих на респираторные вирусы, таких как ацикловир при герпетической инфекции, в настоящее время нет. Как правило, лечение вирусной инфекции заключается в создании оптимальных условий больному, его иммунной системе для естественного выздоровления. У каждого пациента и врача есть собственный набор домашних средств для лечения ОРВИ (теплое питье, чай с малиной и т.д.). При необходимости используются жаропонижающие средства. Но не следует забывать, что в случае «аспириновой» астмы или при сочетании астмы и полипозного риносинусита прием входящих в набор домашних средств нестероидных противовоспалительных препаратов, равно как и природных салицилатов, противопоказан. Надо также учитывать, что ОРВИ протекает у больного с хронической респираторной патологией (бронхиальной астмой), поэтому в некоторых ситуациях возможно применение противовирусных препаратов, иммуномодуляторов, антибактериальных средств (при развитии вторичной бактериальной инфекции).
Лечение бронхиальной астмы исходя из степени ее тяжести и клинических рекомендаций и стандартов лечения (базисная терапия, бронхолитическая, муколитическая) в большинстве случаев предусматривает повышение дозы базисного препарата (если базисная терапия проводилась до ОРВИ) либо использование более эффективного средства базисной терапии.
В настоящее время самым эффективным средством базисной противовоспалительной терапии, входящим в стандарты лечения БА, признаны глюкокортикостероиды (ГКС). Однако однозначных данных о том, что адекватная базисная терапия способна предотвратить вирусиндуцированное обострение астмы, нет. В Клиническом руководстве по ведению больных с инфекциями нижних отделов дыхательных путей ERS и Европейского общества по клинической микробиологии и инфекционным заболеваниям (European Society of Clinical Microbiology and Infectious Disease – ESCMID) сказано, что не существует доказательств эффективности регулярного приема каких-либо препаратов с целью предотвращения эпизодов вирусной бронхообструкции. Не указано и на то, что лечение обычной ОРВИ антибиотиками или противовирусными препаратами не предотвращает инфекцию нижних дыхательных путей.
Как показали результаты исследований, применение будесонида в основной группе пациентов уменьшало выраженность свистящих хрипов в дневное и ночное время по сравнению с контрольной группой, но различия были незначительны [20]. Терапия будесонидом в течение четырех месяцев не предотвращала развитие эпизодов свистящих хрипов в большей степени, чем плацебо [21].
Аналогичные данные получены для беклометазона дипропионата. По сравнению с плацебо беклометазона дипропионат улучшал легочные показатели, но не показывал клинически значимого преимущества у детей школьного возраста при вирусиндуцированном обострении БА [22].
В другом исследовании беклометазона дипропионат по сравнению с тербуталином у детей дошкольного возраста более существенно снижал выраженность дневных и ночных симптомов. Однако длительность сохранения симптомов и потребность в бронхолитической терапии при назначении беклометазона существенно не изменились [23].
Вместе с тем у некоторых пациентов антилейкотриеновые препараты более эффективны (в отношении улучшения спирометрических показателей и контроля БА), чем ингаляционные ГКС [24].
Кроме того, в 2010 г. эксперты GINA (Global Initiative for Asthma – Глобальная инициатива по лечению и профилактике БА), анализируя недостаточную эффективность ступенчатого подхода к терапии у ряда больных, выделили два основных фенотипа БА – с эозинофильным (ИГКС эффективны) и нейтрофильным (ИГКС менее эффективны) воспалением. Как уже отмечалось, при вирусиндуцированном обострении имеет место нейтрофильный компонент воспаления. По данным исследования in vitro, монтелукаст (блокатор LT-рецепторов) может влиять на нейтрофильное воспаление по механизму, не связанному с блокадой цистеиниловых LT-рецепторов, – за счет неспецифического ингибирования циклических нуклеотидных фосфодиэстераз, результатом которого является цАМФ-зависимое подавление провоспалительной активности нейтрофилов [25].
Все это говорит о том, что в лечении вирусиндуцированной астмы антилейкотриеновые препараты играют существенную роль. Наиболее удобным и часто используемым считается монтелукаст. Его можно использовать как альтернативу ингаляционным ГКС (иГКС) при нетяжелых формах астмы, а также как дополнительное средство базисной терапии к иГКС (такая комбинация позволяет уменьшить необходимую дозу ГКС). Кроме того, монтелукаст показан при стероидофобии. Поскольку препарат принимается перорально, его могут использовать пациенты, не способные пользоваться ингалятором.
Клиническая эффективность препарата Синглон
Дженериком с доказанной биоэквивалентностью оригинальному монтелукасту является Синглон (компания-производитель «Гедеон Рихтер», Венгрия). Препарат используется один раз в сутки: у детей от двух до пяти лет жевательные таблетки в дозе 4 мг, у детей 6–14 лет – также жевательные таблетки в дозе 5 мг, у подростков с 15 лет и у взрослых – в дозе 10 мг.
Эффективность Синглона была изучена в рандомизированном проспективном трехмесячном исследовании у 30 взрослых пациентов со среднетяжелым течением бронхиальной астмы [26]. Пациентам основной группы к стандартной базисной потивоастматической терапии (иГКС + бета-2-агонист длительного действия) добавляли Синглон 10 мг/сут. При сравнении с пациентами контрольной группы (только стандартная базисная терапия) отмечалось уменьшение частоты обострений астмы, увеличение продолжительности межприступного периода, а также снижение суточных колебаний пиковой скорости воздушного потока.
В педиатрической практике клиническая эффективность Синглона исследована у 250 детей с острым обструктивным бронхитом и БА в остром периоде [27]. Основную группу составляли 115 детей, принимавших Синглон. В контрольную группу были включены 135 пациентов, получавших терапию бета-2-агонистами. На фоне применения препарата Синглон в 87% случаев при обструктивном бронхите и в 67% случаев при астме сократилось количество используемых медикаментов. Эффективность Синглона, подтвержденная данными физикального обследования, лабораторными и спирографическими показателями, при БА составила 83%. Отмечалась хорошая переносимость и безопасность препарата (общее количество побочных эффектов менее 2%).
Таким образом, препарат Синглон можно рекомендовать в составе терапии БА у детей и взрослых.
источник
Аденовирусная инфекция (код по МКБ-10: A08.2, A85.1, A87.1, B30.0, B30.1, J12.0) — остро протекающее заболевание инфекционной природы, вызываемое аденовирусом различных серотипов, поражающих слизистые оболочки респираторного, гастроэнтерального, урогенитального тракта, конъюнктив глаз и лимфоидную ткань, протекающих с умеренно выраженным интоксикационным синдромом.
Аденовирусная инфекция чаще поражает детей и лиц молодого возраста. Наиболее восприимчивыми к аденовирусам являются дети 6 месяцев — 3 лет. Клиническая значимость аденовирусных заболеваний определяется широким распространением возбудителя, высоким риском возникновения эпидемических вспышек, значительным удельным весом (15-20% по разным данным) в структуре ОРВИ вирусных заболеваний верхних дыхательных путей, поражений конъюнктивы, лимфоидной ткани и кишечных расстройств. Актуальность аденовирусной инфекции также обусловлена научно доказанной онкогенной активностью ряда серотипов возбудителя и его возможностью принимать участие в образовании гибридных вирусов, имеющих особые биологические свойства, в частности, усиленную онкогенность.
О высокой восприимчивости населения и перенесенных инфекционных заболеваниях аденовирусной природы свидетельствует то, что практически у 80% взрослых людей обнаруживают антитела к аденовирусам. При этом, некоторые серотипы аденовируса могут персистировать в организме латентно без местной воспалительной реакции, так и после перенесенного типичного аденовирусного заболевания. Предполагается, что реинфицирование организма человека теми же серотипами протекает бессимптомно, что, по-видимому, и объясняет более низкую заболеваемость среди взрослых лиц.
Патогенез аденовирусной инфекции до настоящего времени изучен не полностью. В его основе — характер взаимодействия аденовируса с клетками организма человека. На сегодняшний день известно три типа взаимодействия:
- Литический инфекционный процесс, при котором вирусы в процессе репликации (размножения) покидают эпителиальную клетку и поражают новые клетки, что приводит к накоплению большого количества вирусных частиц и гибели клетки хозяина. Этот тип взаимодействия характерен для остропротекающих аденовирусных заболеваний с поражением эпителия слизистой дыхательных путей, кишечника, конъюнктив, лимфоидной ткани.
- Латентная (хроническая) инфекция. Как правило протекает в лимфоидных клетках, но механизмы латенции полностью не расшифрованы.
- Онкогенная трансформация клеток человека, при которой происходит встраивание в геном клетки ДНК аденовируса.
Местом первичной локализации (входными воротами) и первичного накопления аденовирусов являются эпителиоциты эпителия носоротоглотки, слизистой конъюнктивы или эпителия тонкого кишечника. Период накопления вирусов в эпителиоцитах и регионарных лимфатических узлах в среднем соответствует длительности инкубационного периода. Воспалительный процесс часто протекает стадийно-нисходящим путем: верхние дыхательные пути — мелкие бронхи — легкие с поражением подслизистого слоя и перибронхиальной ткани, обусловливая очаговую/интерстициальную пневмонию. Процесс в легких сопровождается увеличением трахеобронхиальных лимфоузлов. В местах поражения эпителия развивается воспалительная реакция с расширением капилляров слизистой, гиперплазией подслизистого слоя с инфильтрацией мононуклеарными лейкоцитами, зачастую с кровоизлияниями. При попадании вируса на конъюнктиву развивается кератоконъюнктивит с нарушением зрения.
Попадание аденовируса в кишечник и поражение его эпителия происходит различными путями: заглатыванием инфицированной носоглоточной слизи при наличии назофарингита и алиментарным путем, при котором эпителий кишечника поражается первично, сопровождаясь клиникой острого энтерита с поражением регионарных лимфатических узлов и мезаденита. Также возбудитель может проникать лимфогенным путём в различные регионарные лимфоузлы, что приводит к гиперплазии лимфоидной ткани и накопление вируса.
Развитие интоксикации и появление лихорадки характерно для стадии первичной вирусемии. При этом, нарушается проницаемость стенок сосудов, что вызывает выраженную экссудацию и способствует развитию отеков, а выпадение фибрина в сочетании с некрозом клеток эпителия дыхательных путей/конъюнктивы приводит к образованию на задней стенке глотки, миндалинах, конъюнктиве пленчатых налетов.
В дальнейшем аденовирусы заносятся в паренхиматозные органы (почки, печень, селезенку), нервную систему, лимфатические узлы, где происходит их дальнейшее накопление, сопровождаемое системной лимфаденопатией, увеличением печени и селезенки (гепатолиенальный синдром).
Очевидно, повторные волны вирусемии обеспечивают длительность лихорадки, ее всплески. Вирусемия может наблюдаться не только в период манифестации заболевания, но и при латентно текущей инфекции. Антитела к аденовирусам в крови обнаруживаются с 8-10-го дня, достигая максимума через 2-3 недели. При этом, уровень нейтрализующих антител практически не меняется на протяжении длительного периода (нескольких лет), обеспечивая длительный типоспецифический стойкий иммунитет.
В основу классификации АДВИ положен принцип ведущего клинического синдрома (локализации воспалительного процесса), в соответствии с которым принято выделять:
- ОРЗ аденовирусного генеза (ринит, ринофарингит, тонзиллит, ринофаринготонзиллит, трахеобронхит).
- Аденовирусная пневмония.
- Эпидемический кератоконюнктивит.
- Фарингоконъюнктивальная лихорадка.
- Аденовирусный гастроэнтерит.
- Аденовирусный геморрагический цистит.
- Поражения нервной системы (энцефалит, менингит, полирадикулоневрит) аденовирусного генеза.
- Аденовирусные заболевания при иммунодефицитах (СПИД).
По степени тяжести выделяют:
- Легкую форму. При легкой форме (острое катаральное воспаление респираторного трактата — риноларинготрахеобронхит, глотки — острый фарингит, регионарный лимфаденит, острый конъюнктивит).
- Среднетяжёлую форму. Протекает с выраженными катаральными явлениями, лимфаденопатией, гиперплазией лимфоидных ткани ротоглотки, катарально-фолликулярным конъюнктивитом.
- Тяжелую форму. Протекает на фоне генерализованного распространения вируса с попаданием в эпителиальные клетки кишечника, почек, печени, поджелудочной железы, ганглии головного мозга с выраженным воспалительным процессом, расстройством кровообращения и зачастую, с присоединением вторичной инфекции.
Аденовирусы относятся к ДНК-содержащим вирусам. Естественными хозяевами аденовирусов, являются млекопитающие и птицы. Известно около 100 сероваров вирусов и около 51 из них обнаружены у людей.
Аденовирион по форме представляет собой икосаэдр, геном которого содержит одну линейную двунитчатую ДНК и более 10 белков, образующих его структуру, в том числе и капсид вириона. Репликация вируса и его сборка осуществляется в ядре, а высвобождение вирионов происходит с разрушением эпителиальной клетки. По гемагглютинирующим свойствам и патогенности аденовирусы подразделяются на несколько подгрупп (А, В, С, D, E, F, G).
Антигенная структура аденовируса представлена тремя антигенами: групповой- общий (А-антиген), токсический, вызывающий цитопатическое действие в ткани (В-антиген) и типоспецифический, С-антиген. К важнейшим свойствам аденовирусов относится эпителиотропность – способность поражать клетки эпителия респираторного тракта, конъюнктивы, лимфоидной ткани, кишечника.
Вирус чрезвычайно устойчив в окружающей среде и может длительно (в течение 2-3 недель) сохраняться в воде и на стандартных предметах обихода при комнатной температуре (22 °С). Погибает в течение 30 минут при 56°C или под воздействием дезинфекционных хлорсодержащих препаратов в умеренных концентрациях и ультрафиолетового облучения.
Источник инфекции — вирусоноситель/больной человек, который продолжает выделять вирус во внешнюю среду с секретом верхних дыхательных путей еще на протяжении 25-28 дней после перенесенного заболевания, а с фекалиями – более 1,5 месяца. Механизм передачи аденовирусной инфекции преимущественно аэрозольный (воздушно-капельный), значительно реже — фекально-оральный (алиментарный, через инфицированные посуду, одежду, игрушки, испражнения), крайне редко — через контаминированные объекты внешней среды. Отмечается восприимчивость взрослых лиц и детей к аденовирусной инфекции. После перенесенного заболевания формируется типоспецифичный стойкий иммунитет, соответственно, могут возникать случаи повторных аденовирусных заболеваний, обусловленные другими сероварами вируса.
Входными воротами являются слизистая оболочка респираторного, кишечного тракта или конъюнктива глаз. Особенно часто АДВИ встречается у детей младшего возраста старше 6 месяцев и до 3-х лет. Дети более младшего возраста аденовирусной инфекцией практически не болеют в силу наличия у них пассивного иммунитета, полученного им от матери в виде типоспецифических антител, который после шести месяцев ослабевает, и ребенок становится восприимчив к аденовирусу.
Заболевание встречается круглогодично в виде спорадических случаев. Пик заболеваемости приходится на зимне-весенний период, в котором имеют место эпидемиологические вспышки аденовирусной инфекции в условиях тесного общения детей в организованных детских коллективах. Вспышки инфекции наиболее характерны для 3, 4, 7, 14 и 21 сероваров. Доля АДВИ составляет:
- в общей заболеваемости 0,8-1,4%;
- в инфекционной заболеваемости 10-12%;
- в группе ОРИ – 22-25%.
Разные серовары обуславливают различные клинические варианты инфекционной патологии:
- Серовары 1, 2, 5, 34, 35 группы С поражают эпителий дыхательных путей/кишечника у детей с длительной персистенцией в аденоидах и миндалинах.
- Cеровары 4, 7, 14, 21 группы B – являются возбудителями ОРВИ у взрослых лиц.
- Серовар 3 вызывает острую фарингоконъюнктивальную лихорадку.
- Серовар 3, 4 вызывает аденовирусный геморрагический конъюнктивит.
Аденовирусная инфекция у иммунокомпетентных пациентов и детей может протекать в виде манифестных форм с широким спектром клинических проявлений, а также в виде субклинических стертых и латентных форм практически без симптоматики. Инкубационный период варьирует от 1 до 12 суток.
Для аденовирусных заболеваний характерен ряд особенностей:
- Полиморфизм клинической симптоматики, что обусловлено вовлечением в воспалительный процесс различных систем/органов с появлением новых симптомов, что способствует относительно длительному течению аденовирусных заболеваний. Характерно преобладание местных симптомов относительно общих.
- Длительный период (2-14 суток) повышенной температуры тела (чаще в пределах 38-39С) с лихорадкой различного типа.
- Не выраженный интоксикационный синдром.
- При поражении дыхательной системы — преобладание экссудативного компонента над умеренной симптоматикой общей интоксикации.
- Острое начало: озноб, снижение аппетита, слабость, умеренная головная боль, возможны боли в суставах, мышцах. Со 2-3 дня — повышение температуры.
Манифестные формы АДВИ могут протекать в различных вариантах с соответствующими клиническими проявлениями:
- ОРЗ (острое респираторное заболевание). Встречается как у детей, так и у взрослых. Как правило, начинается с катарального синдрома в виде ринита — выраженной ринореи и затруднения дыхания. Серозные выделения, вскоре приобретают слизисто-гнойный характер. Продолжительность ринита может составлять 2-3 недели. Через 1-2 дня у 80-90 % пациентов появляются симптомы тонзиллита и в 50-60 % пациентов — фарингита, сопровождаемые чувством першения/жжения в области задней стенки глотки и умеренной болью при глотании. Слизистая ротоглотки отечная, мягкое небо интактно. На задней стенке глотки видны гиперплазированные фолликулы, иногда с слизистыми налетами. В ряде случаев в процесс вовлекаются низлежащие отделы дыхательных путей с развитием клиники комбинированного поражения — ринофаринготонзиллита, ларингита, трахеита, бронхита разной степени выраженности. Какие-либо специфические признаки отсутствуют за исключением экссудативного компонента, что проявляется кашлем со слизистой мокротой. Вовлечение в патологический процесс лимфоидной ткани проявляется увеличением подчелюстных, шейных регионарных лимфатических узлов, реже — системной лимфаденопатией с увеличением отдаленных лимфатических узлов. Лимфоузлы мягкоэластическаой консистенции, безболезненны, не спаяны с тканями. Часто у пациентов кроме лимфаденопатии развивается синдром гепатоспленомегалии. Длительность и выраженность интоксикационного синдрома определяются тяжестью и распространенностью воспалительного процесса. Аденовирусная пневмония, как самостоятельная нозологическая форма у иммунокомпетентных взрослых лиц встречается относительно редко. Эта форма аденовирусной инфекции чаще встречается у детей раннего возраста, имеет преимущественно диффузный характер поражения и как правило, выраженными катаральными явлениями респираторного тракта и конъюнктивитом. Аденовирусная пневмония протекает с выраженной интоксикацией (высокой температурой, слизистой мокротой, мышечными болями). Тяжесть процесса обусловлена выраженным экссудативным компонентом, что способствует нарушению проходимости бронхов. Следует учитывать и то, что клиническая симптоматика иногда отягощается за счет присоединения вторичной микробной флоры (микстинфекция с стрептококками, стафилококками).
- Фарингоконъюнктивальная лихорадка. Обычно вызывается аденовирусом серовара 3. Характеризуется острым началом, повышением температуры до 38 ºС, наличием симптомов конъюнктивита, ринита, фарингита (заложенность носа, боль в горле, глазах, ломота в теле), увеличением лимфоузлов. Продолжительность лихорадочного периода от 3-5 до 12-14 дней. Симптомы манифестируют чаще одновременно, но могут появляться и последовательно на протяжении нескольких дней. Характерным симптомом является катаральный, фолликулярный или пленчатый конъюнктивит, позволяющий отличить АДВИ от других ОРВИ. При этом, конъюнктивит будет появляться в первые дни болезни или на второй волне заболевания. Пациенты жалуются на ощущение «песка» и резь в глазах, веки отечны, глазная щель сужена, конъюнктива гиперемированная, резко отечна, отмечается скудное отделяемое. Иногда на фоне выраженной экссудации появляется пленчатый налет. Чаще поражается один глаз вначале, но зачастую позже вовлекается в процесс и второй глаз. Обычно конъюнктивит сохраняется после снижения температуры, в то время как боль в горле уже стихает. Регионарный лимфаденит сохраняется иногда на протяжении нескольких недель. Присутствует общеинтоксикационный синдром (отсутствие аппетита, слабость, мышечная и головная боль), реже явления менингизма. После перенесенного заболевания, особенно у детей отмечается длительная астения.
- Эпидемический кератоконъюнктивит. Наиболее часто заболевание вызывает аденовирус типа 8, инкубационный период может увеличиваться до 3 недель, а симптоматика конъюнктивита сохраняется до месяца. Заболевание начинается постепенно, часто поражаются сразу оба глаза. Кератит развивается, когда симптомы конъюнктивита уже затихают, но его длительность может составлять 1-3 месяца и приводить к снижению зрения. Интоксикационный синдром, выражен слабо, предушные лимфатические узлы увеличены, катаральные явления практически отсутствуют. Реже заболевание протекает в виде конъюнктивита без вовлечения/с минимальным вовлечение в процесс роговицы. Основными жалобами в таком случае слезотечение и жжение в глазах остаются. Заболевание высоко контагиозное и все лица ближайшего окружения больного подвергаются значительному риску инфицирования.
- Аденовирусный гастроэнтерит (серотип 1, 3, 40, 41). Регистрируется преимущественно у детей младшего возраста и новорожденных. Характерно бурное острое начало с частым жидким стулом, который в скором теряет каловый характер, тошнотой и периодической рвотой, вздутием живота и урчанием в кишечнике, повышением температуры до 39 С. Диарея у детей очень часто сочетается с конъюнктивитом и симптомами поражения дыхательных путей. Достаточно быстро развивается обезвоживание организма. У взрослых заболевание протекает легче — жалобы на слабость, жидкий стул, приступообразную боль в животе. Температура в пределах 38ºС, диарея у взрослых протекает без обезвоживания, обще интоксикационный синдром выражен умеренно. Длительность гастроэнтерита — 1-4 суток. Как осложнение аденовирусного гастроэнтерита можно считать появление респираторного синдрома (ринит, тонзиллит, фарингит).
- Аденовирусный геморрагический цистит. Встречается относительно редко, преимущественно у детей и лиц молодого возраста. Вызывается аденовирусами типов 11 и 21. Путь проникновения аденовируса в мочевые пути до конца еще не выяснен. Заболевание начинается внезапно с дизурической симптоматики (частые позывы, боль при мочеиспускании, макрогематурия). В дальнейшем на протяжении 10-14 суток может выявляться микрогематурия. Заболевание продолжается до 2 недель. Соответствующие симптомы у детей менее выражены, а в ряде случаев заболевание протекает в субклинический форме.
- Поражения нервной системы (энцефалит, менингит, полирадикулоневрит) при аденовирусных заболеваниях. Проявляется симптомами общемозговых расстройств (менингизм), обусловленных церебральными циркуляторными нарушениями. Как правило, симптоматика поражения ЦНС (ригидность мышц затылка, головная боль, положительный симптом Кернига) протекает на фоне клинических проявлений какого-либо аденовирусной инфекции (ОРЗ, фарингоконъюнктивальная лихорадка пневмония). Реже заболевание протекает с специфическим преимущественным аденовирусным поражением нервной системы в виде менингоэнцефалита, серозного менингита, полирадикулоневрита.
- Аденовирусные заболеваний у иммуноскомпрометированных пациентов. Вызывается аденовирусами серотипа 34 и 35. Протекает чаще по типу пневмонии, геморрагического цистита, пневмонии, гастроэнтерита. Заболевание характеризуется тяжелым течением и сопровождается высоким уровнем смертности (до 70%). К факторам риска относят длительную иммуносупрессию и нейтропению, трансплантацию солидных органов и стволовых клеток, лимфопению, реакцию «трансплантат против хозяина».
В целом, аденовирусная инфекция относится преимущественно к патологии детского возраста. При этом, у новорожденных она, если мать имеет достаточно напряженный иммунитет, протекает легко или вообще бессимптомно. Наиболее уязвимой группой являются дети 1-го года жизни, у которых респираторные проявления зачастую сочетаются с дыхательной недостаточностью, астматическим синдромом, ложным крупом, а диарейный синдром протекает с выраженным обезвоживанием. Дети старшего возраста болеют преимущественно легкими формами заболевания (ринит, фарингит).
Взрослые лица переносят заболевание сравнительно легко и болеют реже, что обусловлено как наличием специфических антител к определенному типу вируса, так и защитной ролью гетерологичных антител. По-видимому, частые инфицирования организма различными серотипами аденовирусов способствуют повышению напряженности гуморального иммунитета к гомологичным/гетерологичным видам аденовируса. В связи с чем реинфекция в большинстве случаев протекает легко или даже не приводит к заболеванию. Во многих случаях у взрослых такие формы заболевания, как тонзиллит или фарингит обусловлены активацией латентной инфекции, снижающей местную/общую реактивность организма.
Опорными признаки диагностики аденовирусной инфекции являются:
- характерный эпидемический анамнез;
- катаральный синдром поражения респираторного тракта;
- конъюнктивит;
- слабовыраженный синдромом интоксикации;
- экссудативный характер воспаления;
- лимфопролиферативный синдром;
- гепатоспленомегалия;
- волнообразное течение.
Методами экспресс-диагностики АДВИ являются иммунная электронная микроскопия и реакция иммунофлюоресценции. Вирусологическая диагностика (выделение аденовируса из биоматериала — соскоба с конъюнктивы, носоглоточных смывов, фекалий) в клинической практике ввиду сложности и длительности используется редко. Наиболее специфичной и чувствительной является полимеразно-цепная реакция, способная выявить отдельные ДНК вируса в исследуемом биоматериале.
Инструментальные методы (ренгеногарфия, фибробронхоскопия) проводятся по показаниям.
Дифференциальная диагностика проводится в зависимости от клинической формы АДВИ с гриппом, ОРВИ, конъюнктивитами/кератоконъюнктивитами различной этиологии, пневмониями, туберкулёзом.
Мы рассмотрели симптомы и теперь рассмотрим лечение аденовирусной инфекции у взрослых. Лечение проводится амбулаторно и только при тяжелом или осложненном течении заболевания показана госпитализация. В домашних условиях необходима изоляция больного и масочный режим. Назначается постельный режим, легкая диета и обильное питье. Важна гигиеническая обработка носоглотки и глаз три и более раз в день с использованием индивидуальных средств по уходу.
В целом, лечение аденовирусной инфекция у взрослых включает:
- Противовирусную терапию, эффективность которой подтверждена многими исследованиями. Она сокращает длительность течения болезни, уменьшает проявления ее и тяжесть, препятствует активации бактериальной инфекции.
- Патогенетическую терапию: дезинтоксикационные мероприятия (обильное питье), антигистаминные препараты, аскорбиновую кислоту, иммуномодулирующие препараты.
- Симптоматическую терапию: жаропонижающие средства, при выраженной заложенности носа — сосудосуживающие капли (их не стоит использовать более 5–6 дней), при наличии кашля — противокашлевые и отхаркивающие средства.
Что касается самой противовирусной терапии, то она может состоять из:
- Химиотерапевтических препаратов, оказывающих прямое воздействие на вирус — общее (при приеме внутрь или внутримышечном введении) и местное в случае конъюнктивита (глазные капли или мази и гели).
- Неспецифической иммунотерапии (интерфероны, индукторы интерферона).
Препараты прямого действия быстро купируют симптомы в период разгара аденовирусных инфекций и назначаются большей частью при средней и тяжелой степени заболевания. С целью уменьшения частоты развития осложнений (пневмонии) и развития затяжного течения с рецидивами чаще всего применяется индуктор «поздних» интерферонов Кагоцел.
Вышеперечисленные препараты прямого действия активны в отношении не только вирусов гриппа, герпеса, но и аденовирусов. Они уменьшают длительность основных симптомов в период разгара аденовирусной инфекции (интоксикация, лихорадка, боль в горле, слезотечение), но почти не влияют на частоту вирус-ассоциированных пневмоний и рецидивы заболевания. Затяжное и рецидивирующее течение, «поздние» пневмонии связаны с длительным пребыванием аденовирусов в тканях, в основном, в лимфоидной.
Кагоцел и другие индукторы интерферонов уменьшают частоту развития пневмоний, затяжного и рецидивирующего течения. Также уменьшают длительность ринита и кашля. Учитывая то, что продолжительность действия этого препарата после однократного приема составляет пять суток, его можно применять коротким курсом — достаточно 4-х дней.
Не все химические противовирусные средства можно применять беременным и детям. Препараты интерферона имеют много побочных эффектов и их регулярное применение сопряжено с риском возникновения аутоиммунных заболеваний (псориаз, красная волчанка, Синдрома Шегрена, инсулинозависимый диабет).
В случае, если противопоказан прием химических фармацевтических препаратов, для лечения применяют гомеопатические средства (Сандра, Оциллококцинум) или противовирусные средства на растительной основе. Например, препарат Гипорамин (суппозитории, таблетки, мазь) разрешен к применению у беременных и детей с 3 лет. Он индуцирует продукцию интерферона и способствует сокращению длительности проявлений (кашель, ринит, температура, хрипы, стеноз гортани). Взрослым этот препарат назначают по 1 таблетке 4-5 раз в день, детям с 3до 12 лет по 1/2–1 таблетке 2-4 раза. Курс лечения составляет 3-5 суток.
Часто аденовирусная инфекция у взрослых протекает с длительным повышением температуры до 38-39 C, которая может держаться в течение 10-14 дней. Лихорадка требует симптоматического применения жаропонижающих средств. Если цифры не превышают 38,50 С и самочувствие больного удовлетворительное, можно обойтись народными методами снижения температуры и дать организму возможность побороться с вирусом.
Такие симптомы аденовирусной инфекции у взрослых, как резь в глазах и слезотечение устраняются местным применением глазных мазей, капель и гелей с противовирусной активностью. Из индукторов интерферона второго поколения капли Полудан показали лучшие результаты при поражениях глаз аденовирусом. Препарат способствует продукции собственного интерферона, который значительно превосходит по эффективности любые препараты готового интерферона. Капли вводят в конъюнктивальный мешок до 8 раз в сутки, а по мере улучшения частоту уменьшают до 3–4 в день.
В случае присоединения гнойной инфекции при конъюнктивите дополнительно назначаются антибиотики в каплях (мазях), но не более трех раз в день. Предпочтение отдается мази Тобрекс Сигницефу, Офтаквиксу. Больным с конъюнктивитом необходимо знать о его контагиозности (заразности), поэтому важно воздержаться от контактов с детьми, не лезть руками в глаза, пользоваться индивидуальным полотенцем и отдельными ватными спонжиками для глаз.
Гиперплазия лимфоидных образований. Этот симптом чаще встречается у детей. Лимфаденопатия, иногда выраженная, становится поводом для включения гомеопатических составов с действием на лимфатические узлы — Лимфомиозот, Вокара.
Боль или першение в горле. Для устранения этих симптомов можно применять полоскания отварами трав, раствором фурацилина, однако эффективнее средства, которые имеют широкий спектр антибактериальной активности и к тому же дают обезболивающий эффект: Декатилен, Стрепсилс Интенсив, Гексорал Табс, Фарингосепт, Гексализ, Фалиминт. Многие из них содержат масло перечной мяты или эвкалипта, которые устраняют раздражение, уменьшают саднение и придают таблеткам приятный вкус.
Для местного лечения ротоглотки рациональными являются комбинированные препараты, которые оказывают комплексное действие. Например, Гексализ, который проявляет противомикробное и противовирусное действие, а также оказывает противовоспалительный и обезболивающий эффект.
Противовирусную активность обеспечивают входящие в препарат лизоцим и эноксолон. Биклотим активен в отношении бактериальной флоры, а также оказывает местноанестезирующее и противовоспалительное действие. Взрослые могут рассасывать таблетки каждые два часа (максимально восемь таблеток в день). Важно то, что препарат разрешено применять у беременных и кормящих, а также детей.
Кашель. При этой инфекции он продуктивный (с мокротой) и нет такого надсадного сухого кашля как при трахеите. В комплексной терапии применяют отхаркивающие средства растительного происхождения: Таблетки от кашля с термопсисом, сироп Алтейка, Проспан, Гербион подорожник, Бронхиал с мать и мачехой и подорожником, Сироп солодки.
Также эффективным является прием препаратов Эсперал или Эриспирус. Действующее вещество фенспирид оказывает бронхолитический и противовоспалительный эффект. Проведенные исследования доказывают высокую эффективность этих препаратов в качестве противокашлевого средства при любых респираторных инфекциях.
Если посетить форум по вопросу лечения респираторно-вирусных заболеваний у взрослых, то становится ясно, что большинство больных для симптоматического лечения пользуются комбинированными препаратами, которые отпускаются в разных формах (таблетки, порошки для приготовления растворов) и без рецепта. Удобством является то, что в их составе — от трех до пяти фармакологических веществ.
В целом они обладают жаропонижающим, противовоспалительным и обезболивающим действием (за счет Парацетамола), сосудосуживающим и антиэкссудативным (деконгестант фенилэфрин эффективно устраняет заложенность носа), антигистаминным (фенирамин или хлорфенирамин устраняют аллергический отек слизистой носа и глотки, несколько подавляют кашель) и ангиопретекторным действием (рутозид и аскорбиновая кислота, которая укрепляет стенки сосудов и рассматривается как патогенетическое средство – усиливает выработку эндогенного интерферона).
Некоторые комбинированные средства включают также кофеин, который устраняет седативное действие антигистаминных препаратов, уменьшает вялость и повышает работоспособность. К числу таких, часто употребляемых комбинированных средств, можно отнести Антифлу, Колдрекс, Милистан мультисимптомный, Инфлюнет, Фервекс, Ринза, Терафлю.
Многие препараты сочетают в себе не только вышеперечисленные эффекты, но и противовирусный и интерфероногенный, поскольку дополнительно включают Римантадин. Это препарат АнвиМакс, АнГриКапс максима, Антигриппин-максимум. Последний удобен тем, что выпускается в форме капсул с раздельным содержанием Парацетамола, если нет необходимости в снижении температуры (капсула синего цвета). Все прочие ингредиенты содержит капсула красного цвета. С лечебной целью препарат применяется не позднее 2 суток от начала появления первых симптомов. Длительность курса не должна превышать пяти дней.
Комбинированные средства целесообразно принимать тогда, когда присутствуют все симптомы заболевания. При наличии одного или двух (повышенная температура и насморк), лучше ограничиться монопрепаратами. Риск возникновения побочных эффектов в этом случае снижается.
Как лечить аденовирусную инфекцию при подозрении на осложнения бактериального характера? Наличие осложнений в виде пневмонии, отита, синусита, при обострении хронического пиелонефрита или острых инфекциях мочевыводящих путей — показание к дополнительному назначению антибиотиков. Чаще всего антибиотик при остром отите и синусите назначается эмпирически. Это связано с тем, что эти состояния требуют срочного назначения антибактериальной терапии. Назначаются аминопенициллины и цефалоспорины, поскольку к ним чувствительны основные бактериальные возбудители.
В случае их назначения рекомендуется обязательное включение в схему лечения любого пробиотика для предупреждения дисбиотических нарушений, а параллельное профилактическое назначение противогрибковых препаратов является необоснованным. Лечение аденовирусной инфекции у детей будет рассмотрено отдельно.
источник
Сегодня уже стало очевидно, что бронхиальная астма (БА) — глобальная проблема: в Европе около 30 млн человек страдают этим хроническим заболеванием, в США ежегодно более 2 млн попадают в реанимационные отделения, а 
Сегодня уже стало очевидно, что бронхиальная астма (БА) — глобальная проблема: в Европе около 30 млн человек страдают этим хроническим заболеванием, в США ежегодно более 2 млн попадают в реанимационные отделения, а 500 000 госпитализируют по поводу тяжелого обострения астмы [1]. Эпидемиологические и иммунопатофизиологические исследования показывают, что самой распространенной причиной обострений болезни — в 80–85% случаев у детей и
75% у взрослых — являются острые респираторные вирусные инфекции (ОРВИ) [2]. И хотя обострения БА зависят и от других факторов (фенотипических, анамнестических, от проводимого лечения, длительности обострения и т. д.), эти цифры указывают на колоссальную роль вирусов в этом процессе.
Известно, что сами по себе ОРВИ являются широко распространенной патологией, особенно у детей раннего возраста. Так, например, в Швейцарии симптомы респираторных инфекций отмечались у 93% детей первого года жизни (у 181 из 195 человек, включенных в исследование), причем в 46% — в тяжелой форме; длительность респираторных симптомов составила 4 недели, в 90% — менее чем 12 недель (0–23) [3]. В проспективном исследовании, недавно проведенном в Дании, дети в возрасте до одного года болели ОРВИ 6,3 раза (назальные симптомы и/или один из других симптомов: кашель, температура, свистящее дыхание, одышка, потеря аппетита) [1]. В России дети переносят ОРВИ в 3,7 раза чаще по сравнению с взрослыми, а уровень ежегодной заболеваемости этими инфекциями составляет 69 000 случаев на 100 000 населения.
Какова связь между острым инфекционным, с одной стороны, и хроническим воспалительным заболеванием дыхательных путей, с другой?
Впервые о роли «простуды» как причины обострения БА высказался W. Olser в своем учебном пособии в 1892 г., когда вирусы еще не были идентифицированы как инфекционные возбудители [4]. Сегодня к респираторным вирусам относят около 200 их разновидностей. Самые распространенные из них — человеческие риновирусы (чРВ), респираторно-синцитиальный (РС), вирусы парагриппа и гриппа, адено-, коронавирусы, а также открытые недавно бока- и метапневмовирусы человека. Доказано, что любой респираторный вирус может быть триггером обострений БА. Почему это происходит? Несмотря на интенсивное развитие молекулярной биологии, вирусологии и междисциплинарный подход в изучении этой научной проблемы, точного ответа на вопрос нет — крайне сложно исследовать механизмы воспаления дыхательных путей при вирус-индуцированном обострении БА.
Другая важная проблема — огромная разновидность не только всех возбудителей респираторных инфекций, которые вызывают грипп, ОРВИ и «простуду» (этим термином обозначают комплекс острых и обострений хронических вирусных и бактериальных инфекций верхних дыхательных путей), но и каждого по отдельности вируса в частности. Так, после открытия в 60-е годы прошлого столетия РНК чРВ описано более 100 его штаммов. Известно, что вирус гриппа состоит из 8 белков, причем 4 из них — наружные — легко мутируют, и потому уже разработанные вакцины оказываются неэффективны. Ученые уже длительное время пытаются создать вакцину, способную воздействовать на неизменившиеся «внутренние» протеины вируса гриппа. В последнее время стало ясно, что с мутацией вирусов (в том числе птиц, животных) связана чрезвычайно высокая опасность возникновения новых инфекций.
Еще одна проблема — приобретение устойчивости вирусов к вакцинам, а при несовпадении вакцинного штамма с эпидемическим — существенное снижение эффективности вакцинопрофилактики. Понятно, что создание универсальных противовирусных вакцин представляется практически невозможным. В свою очередь, БА также гетерогенное хроническое воспалительное заболевание дыхательных путей со сложными иммунопатологическими механизмами развития. Ученые признают, что при БА практически невозможно управлять тем воспалением (по выражению видного американского профессора Szefler S. — «вулканом»), которое запускается вирусной инфекцией.
Вирус-индуцированная астма — фенотип астмы?
Есть научное предположение: чем более тяжело протекает ОРВИ у детей раннего возраста, тем выше у них риск возникновения БА в последующем. Возможно, этому процессу больше способствуют ранее перенесенные бронхиолиты и/или повторные эпизоды свистящего дыхания, индуцированные респираторными вирусами. В 2008 г. в США были опубликованы результаты проспективного наблюдения за 259 детьми в возрасте 0–6 лет жизни (Childhood Origins of Asthma (COAST)) [5]. У 90% детей со свистящим дыханием в возрасте до 3 лет жизни были обнаружены вирусы (чаще всего антигены чРВ — 48%, РС-вирусы — 21%, парагриппа — 12%, других — 10%). Риск развития БА повышался, если эпизоды бронхообструкций сочетались с сенсибилизацией к аэроаллергенам. Кроме того, 90% детей (26 из 30), у которых до трех лет жизни отмечались бронхообструкции, вызванные риновирусами, к 6 годам имели диагноз БА.
В популяционном исследовании Carroll et al., также проведенном в США, среди детей, родившихся за период 1995–2000 гг. (п = 90 341 ребенок), 18% перенесли бронхиолит, который в дальнейшем у большинства трансформировался в БА; кроме того, степень тяжести бронхиолита коррелировала с риском развития БА [6].
Наиболее часто (в 2/3 случаев) при обострениях БА обнаруживают чРВ. Wos и соавт. выявили иммуногистохимическим методом в биоптате бронхов чРВ у 73% больных БА по сравнению с 22% в группе контроля здоровых лиц (p 40%, а через 6 месяцев после острого обострения — у 25% детей [8]. В другом исследовании также подтверждено наличие антигенов чРВ в циркулирующей крови новорожденных, госпитализированных по поводу обострения БА, через 6 недель после инфекции [9]. Самый высокий риск развития БА имели дети, госпитализированные по поводу тяжелой ОРВИ, вызванной недавно открытым чРВ группы С. Есть данные, которые указывают на наличие вирусов в биоптате бронхов больных даже в период ремиссии БА. С другой стороны, известно, что в 40% случаев риновирусная инфекция протекает асимптоматически.
Способны индуцировать развитие бронхообструкций/БА, возможно, также РС-вирусы, реже — метапневмовирус, коронавирус (один из серотипов последнего известен как вирус SARS, вызывающий тяжелый острый респираторный синдром с поражением легких по типу респираторного дистресс-синдрома взрослого типа; другой штамм — NL63 вызывает бронхолит). К возрасту 2 лет практически все дети имеют антитела к РС-вирусу, но немногие из них переносят бронхиолит или тяжелое течение инфекции, которое может потребовать госпитализации, однако есть убедительные данные, подтверждающие роль РС-вирусной инфекции в развитии БА у детей [10]. И хотя эпизоды свистящего дыхания у детей 1–2 года жизни больше указывают на вирусный бронхиолит, следует иметь в виду также вирус-индуцированное обострение недиагностированной БА. Примерно 50% детей, перенесших бронхиолит, имеют рецидивирующий обструктивный бронхит, а в дальнейшем, возможно, БА. Особого внимания врача требуют дети из группы «высокого риска» (наследственная отягощенность атопией/БА и/или сенсибилизация к аллергенам). Вместе с тем есть пациенты, у которых нет клинических симптомов БА во время интеркуррентной ОРВИ (соответственно, таковых примерно 20–25%).
Еще одна особенность, характерная, главным образом, для педиатрической практики: дети с аллергическими заболеваниями болеют намного чаще ОРВИ (и продолжительнее), чем неатопики [11]. Десятилетний период наблюдений позволил ученым из Осло прийти к заключению, противоречащему «гипотезе гигиены»: перенесенные в раннем возрасте ОРВИ не оказывают протективный эффект в развитии БА, аллергического ринита или сенсибилизации, а, напротив, повышают риск возникновения БА [12].
В чем причинная связь между вирусной инфекцией и БА?
В 2007 г. эксперты Европейского респираторного общества опубликовали обширный обзор, посвященный механизмам вирус-индуцированной астмы [13]. В документе детально рассмотрены следующие вопросы: экспериментальная модель вирус-индуцированной астмы; вирус-индуцированная бронхиальная гиперчувствительность; структурные клетки и внеклеточный матрикс; иммунные клетки и их функции (нейтрофилы, эозинофилы, тучные клетки, Т- и В-клетки, макрофаги); медиаторы; нейрогенные механизмы; молекулярные пути: взаимодействие между вирусной инфекцией и другими факторами (атопия, аллергены, поллютанты). Документ содержит ссылку на 162 научные публикации. Следует признать, что ведущим ученым не удалось прийти к точному заключению о том, каковы основные механизмы обострений БА при вирусных инфекциях — доказательства, подтверждающие такую причинную связь, являются слабыми, а механизмы плохо понятными. Как показывает анализ литературы, ученые выделяют наиболее значимые в этих процессах факторы, а именно: генетические особенности, детерминирующие восприимчивость организма к тяжелым вирусным инфекциям; нарушения во врожденной и адаптивной иммунной системах в ответ на вирусную инфекцию. В частности, речь идет о дефиците продукции эпителиальными клетками антивирусных интерферонов I типа — IFN-альфа и IFN-бета, которые в норме через активацию толл-подобного рецептора 3 распознают РНК вируса, что ведет к апоптозу инфицированных клеток, ограничению репликации вируса и его высвобождения. Wark et al. инфицировали эпителиальные клетки бронхов больных БА чРВ и обнаружили 50-кратное увеличение РНК вируса в супернатанте больных по сравнению со здоровыми [14]. Кроме того, клетки астматических пациентов продуцировали в 2,5 раз меньше IFN-бета. Добавление интерферона в культуру клеток частично восстанавливало иммунный ответ у больных БА.
Неспособность эпителиальных клеток бронхов продуцировать IFN-бета, когда они инфицируются чРВ, усилило предположение ученых о важной роли дефекта врожденного иммунитета как одного из основных механизмов персистирующего течения БА [1–6, 14, 15]. Недавно Хаитов М. и соавт. опубликовали в журнале Allergy оригинальную статью, в которой показано, что при вирус-индуцированном обострении БА имеет место также дефицит интерферона III типа — IFN-лямбда [16]. Респираторные вирусы инфицируют бронхиальные эпителиальные клетки и макрофаги, однако точные механизмы продукции этими клетками IFN-альфа, IFN-бета и IFN-лямбда, конечно же, до конца не ясны. Как показывают исследования in vitro, продукция интерферонов снижается у больных БА в зависимости от тяжести течения заболевания и инфицирования чРВ, в частности. Так, по данным группы авторов [17] продукция IFN-альфа и IFN-гамма лейкоцитами была в среднем ниже нормы в 5 и 11 раз соответственно. Замещение дефицита интерферонов ученые рассматривают как один из подходов к терапии БА [16].
С другой стороны, не менее важную роль играет адаптивный иммунитет: вирусные инфекции приводят к высвобождению и запуску целого каскада провоспалительных цитокинов и хемокинов Т-клеток.
Диагностика
Респираторные вирусы идентифицируют по их нуклеотидным остаткам в назальном секрете и жидкости из нижних дыхательных путей с помощью ПЦР-технологии. Следует стремиться получить материал для исследования в первые дни после инфицирования, пока количество вируса не снижено под влиянием факторов противовирусного иммунитета. В то же время аденовирусы и чРВ методом ПЦР могут быть обнаружены позже из-за способности этих вирусов длительно персистироваться в клетках эпителия дыхательных путей. Антигены наиболее часто встречаемых респираторных вирусов, таких как вирус гриппа, РС-вирус, аденовирус и вирус парагриппа, можно выявить в реакции непрямой иммунофлюоресценции или иммуноферментным анализом. Чувствительность обоих методов варьирует от 50% до > 90% [18]. При использовании пула моноклональных антител можно одновременно исследовать несколько распространенных респираторных вирусов. Однако по заключению экспертной группы Европейского респираторного общества исследования, направленные на выявление возбудителей вирусных инфекций респираторного тракта, часто не дают полезной информации [18]. Особый интерес представляют методы быстрого выявления вируса гриппа, которые дают возможность назначать противовирусные препараты своевременно.
В большинстве случаев ОРВИ сопровождает лейкоцитоз — до 10–15´109/л и выше при нормальном С-реактивном белке и другом острофазном белке — прокальцитонине выше 2 нг/мл (лейкопения характерна для гриппа). Выраженный лейкоцитоз — 15–30´109/л характерен для РС-вирусной инфекции, хотя следует помнить о бактериальном осложнении.
Диагностику БА врач проводит с учетом критериев GINA, используя клинические и лабораторные методы [19].
Вирусные инфекции при астме: клиника
ОРВИ быстро распространяются воздушно-капельным путем, при кашле, чихании, а также контактным путем через загрязненные выделениями руки. Клинически практически все ОРВИ протекают однотипно: с симптомами катара верхних дыхательных путей, а также кашлем, возможно, бронхообструкцией. Как правило, в большинстве случаев подобные симптомы легко разрешаются в течение 7–10 дней, хотя возможно развитие бактериальных и других осложнений. Встречаются тяжелые формы ОРВИ. Вирусным бронхиолитом страдают в основном дети в возрасте до двух лет. Клинические симптомы бронхиолита — сначала симптомы верхних дыхательных путей, через 2–3 дня у больных появляется кашель (иногда круп), одышка, повышение температуры, свистящее дыхание.
Как правило, при присоединении ОРВИ и гриппа большинство пациентов с БА испытывают ухудшение симптомов самой БА. Обострения БА (согласно GINA) представляют собой эпизоды прогрессирования одышки, кашля, свистящего дыхания и/или стеснения в груди, снижение пиковой скорости выдоха. На основании клинических симптомов обострение БА классифицируют как легкое, среднее, тяжелое или угрожающее жизни пациента.
Большинство исследователей находят более выраженные симптомы «простуды» на фоне обострения БА у детей и взрослых. Так, по данным Xepapadaki P. еt al. бронхиальная гиперчувствительность сохраняется у детей с БА после перенесенной ОРВИ от 5 до 11 недель [20]. У взрослых больных БА на фоне ОРВИ, индуцированной чРВ, отмечаются выраженные изменения функции внешнего дыхания, увеличение уровня эозинофилов и лейкоцитов в крови и эозинофильная инфильтрация слизистой бронхов [21]. Message et al., использовав модель экспериментальной риновирусной инфекции, выявили у больных легкой формой БА более выраженные (в 6 раз) симптомы нижних дыхательных путей, увеличение количества эозинофилов в лаважной жидкости бронхов, лейкоцитов и нейтрофилов в мокроте, по сравнению со здоровыми волонтерами [2]. Другие авторы, напротив, считают, что пациенты с легкой формой БА не отличаются по клиническим симптомам простуды от здоровых лиц [22, 23]. Powell Н. и соавт., применив у больных БА анкету по оценке симптомов нижних дыхательных путей Common Cold Questionnaire (CCQ), не подтвердили достоверность этого теста для его использования с целью правильной дифференциации вирусного и невирусного обострений БА (для этого необходимо провести конкретное вирусологическое исследование) [24].
Особенности терапии
Известно, что клинические проявления ОРВИ несколько отстают от начала репликации вируса, заканчивающейся в первые 1–3 дня болезни (при гриппе — в 1-й день). С небольшой задержкой нарастает выделение интерферонов. На репликацию вируса возможно воздействовать при начале лечения в 1–2-й дни клинических проявлений ОРВИ. В связи с этим эффективная этиопатогенетическая терапия ОРВИ представляется невозможной. Другая особенность ОРВИ — многообразие острых респираторных вирусов, вызывающих их, что не позволяет проводить активную специфическую иммунопрофилактику этих заболеваний. Не существует до сих пор также вакцин, способных предотвратить вирус-ассоциированные обострения БА. Так, формалин-инактивированная вакцина против РС-вируса (FI-RSV), разработанная в 1960 г., привела к усилению инфекции у вакцинированных детей, тогда как у неиммунизированных она протекала слабее. В лечении РС-вирусно-индуцированного бронхиолита у детей раннего возраста используют единственный препарат — рибавирин, которому приписывают также роль в превенции развития в дальнейшем БА. Уже созданы антивирусные препараты при чРВ — капсид-связывающий ингибитор (pleconaril) и ингибитор 3C протеазы (ruprintrivir), которые позволяют уменьшить клинические проявления риновирусной инфекции, однако их эффективность при БА и хронической обструктивной болезни легких детально не изучалась.
Кроме того, не существует доказательств эффективности регулярного приема каких-либо препаратов с целью предотвращения эпизодов вирусной бронхообструкции. Как известно, лечение обычной ОРВИ антибиотиками или противовирусными препаратами не предотвращает инфекции нижних дыхательных путей [18]. Однако получены стабильные доказательства, что ингибиторы нейраминидазы (в частности, осельтамивир) обладают профилактической эффективностью против вируса гриппа (хотя самым важным профилактическим методом по-прежнему остается противогриппозная вакцина). Осельтамивир разрешен для применения у детей с 1 года жизни и показывает хорошие результаты только при его приеме в первые 36 ч от начала заболевания. Хотя у детей с БА лечение осельтамивиром не оказало статистически значимого влияния на длительность заболевания, но снизило риск обострений БА и улучшило показатели функции внешнего дыхания.
Эксперты ВОЗ рекомендуют применять у детей с ОРВИ иммуномодуляторы (интерфероны, индукторы интерферонов, бактериальные лизаты и т. п.). В Кохрайновском анализе применение иммуностимуляторов позволило снизить у детей выраженность симптомов инфекций верхних дыхательных путей на 40% [25].
Учитывая ведущую роль дисфункций иммунитета в развитии повышенной восприимчивости детского организма к респираторным инфекциям с целью профилактики ОРВИ и гриппа нашел широкое применение интерферон человеческий рекомбинантный альфа-2 (Виферон). В составе Виферона содержаться человеческий рекомбинантный интерферон альфа-2, токоферола ацетат и аскорбиновая кислота. Комплексный состав Виферона обусловливает ряд новых эффектов: в присутствие аскорбиновой кислоты и токоферола ацетата возрастает специфическая противовирусная активность интерферона человеческого рекомбинантного альфа-2, усиливается его иммуномодулирующее действие на Т- и В-лимфоциты, нормализуется содержание иммуноглобулина Е, происходит восстановление функционирования эндогенной системы. Препарат производится в виде 3 различных лекарственных форм: ректальных суппозиториев, мази и геля. Ректальные суппозитории выпускаются в 4 различных дозировках: содержащие 150 000 международных единиц (МЕ) интерферона, 500 000 МЕ, 1 000 000 МЕ и 3 000 000 МЕ интерферона. Такой способ применения препарата способствует более продолжительной циркуляции интерферона в крови, чем внутривенное введение рекомбинантного интерферона альфа-2 (до 12 ч). Виферон при ОРВИ следует назначать в зависимости от возраста: новорожденным детям, в том числе и недоношенным — Виферон 150 000 МЕ по 1 свече 3 раза в сутки через 8 часов (на 1 курс — 5 дней), более старшим детям — Виферон 150 000 МЕ 2 раза в сутки 5 дней. Детям от 7 лет и взрослым больным — препарат Виферон 500 000 МЕ назначают по 1 свече в день с 12-часовым перерывом.
Получены положительные результаты применения Виферона в комплексной терапии бронхиальной астмы у детей [29]. По сравнению с общепринятой терапией включение Виферона в стадию ремиссии в схему лечения (наблюдение в течение 6 месяцев) способствовало клиническому улучшению течения заболевания: отмечалось уменьшение частоты ОРВИ в 4 раза, снижение частоты обострений бронхиальной астмы в 3,4 раза. Период ремиссии увеличивался до 4–6 месяцев, клинические приступы бронхиальной астмы протекали более легко.
Вакцинация детей с БА противогриппозной вакциной на фоне превентивного применения интерферона альфа-2 в ректальных свечах (Виферон) способствовала достоверному снижению частоты и длительности обострений БА и увеличению способности к спонтанной и индуцированной продукции эндогенного интерферона [26].
Неизбирательное назначение антихолинергических препаратов и бета2-агонистов короткого действия в лечении вирус-индуцированного эпизода бронхообструкции (при БА эти препараты назначают «по потребности») не рекомендуется. Ключевым подходом терапии БА признаны ингаляционные глюкокортикостероиды (иГКС), а при всех степенях тяжести обострения болезни (кроме легкой) — системные стероиды (уровень А по критериям доказательной медицины) [19]. Глюкокортикостероиды снижают риск обострений БА за счет торможения воспаления в дыхательных путях. Возможно использование иГКС в высоких дозах (1,6–2,25 мг/сут), однако нет достоверных данных о том, что использование перорального преднизолона или флутиказона пропионата снижает частоту риновирус-ассоциированной бронхообструкции у детей. Известно, что ни длительное (2 года и более), ни интермитирующее применение иГКС не предотвращает рецидивы бронхообструкций (в том числе вирусной этиологии) у больных БА. Вместе с тем, по данным недавно проведенного метаанализа у детей раннего и дошкольного возрастов, имеющих рецидивы бронхообструкций или БА, использование иГКС приводит к достоверному снижению эпизодов свистящего дыхания/обострений БА, улучшению клинических симптомов болезни и показателей функции внешнего дыхания (ФВД) [27]. Протективный эффект иГКС в отношении аллергенов доказан, тогда как при таких триггерах, как вирусы или поллютанты, этот эффект слабо выражен. В эксперименте у инфицированных чРВ астматических больных превентивный прием за 2 недели до инфекции иГКС способствовал снижению порога бронхиальной гиперчувствительности [28].
В последнее время появились данные о целесообразности применения у детей с вирус-индуцированным обострением БА (возможно даже при РСВ-бронхиолите у новорожденных) ингибитора лейкотриеновых рецепторов — монтелукаста. Так, регулярное применение монтелукаста позволило снизить частоту вирус-индуцированных обострений БА у детей в период сезонных ОРВИ в Канаде (сентябрь) на 32%, а использование иГКС — на 30% [29]. Возможно, здесь играет роль тормозящее влияние препарата на синтез лейкотриенов при ОРВИ, а также его терапевтический эффект на сопутствующий у большинства пациентов БА аллергический ринит. Однако это единичное исследование, и в дальнейшем необходимо провести рандомизированные клинические исследования. Использование комбинированной терапии (иГКС + длительно действующие бета-агонисты) обосновано при неконтролируемом течении БА у взрослых и подростков, что позволяет достоверно снизить частоту обострений болезни (уровень А) [19].
Сложность патогенеза вирус-индуцированного обострения БА объясняет недостаточную эффективность антиастматической терапии большинства таких случаев, что свидетельствует о крайней важности изыскания новых терапевтических подходов БА.
источник