Абсцесс – воспалительный процесс в тканях любой локации с образованием гнойной полости. Ему свойственно формироваться в костных тканях, мышцах, подкожной клетчатке. Новообразование диагностируют на органах и между ними.
Патологии свойственно развиваться самостоятельно либо формироваться на фоне травм, воспаления легких либо быть осложнением при ангине.
Чрезмерное скопление экссудата, последовательно приводит к нагнетанию на стенки капсулы, разрыву и выходу гноя наружу.
Гноеродные микроорганизмы, через очаг заносят возбудителя в лимфатическое и кровеносное русло, что в дальнейшем вполне может стать причиной сепсиса, расплавления кровеносного сосуда, под действием гноя.
Развитие процесса зависит от состояния барьерных функций организма. Чтобы выстроить защиту и не допустить распространение гноя, в очаге формируется капсула, купирующая возможности патогенной микрофлоры интенсивно проникать в здоровые ткани.
Для того, чтобы заболевание стало прогрессировать, необходимо иметь врата инфекции – рану, через которую в организм попадают гноеродные патогенные бактерии. Активная жизнедеятельность микроорганизмов в благоприятной среде, приводит к расплавлению эпидермиса и образованию капсулы, заполненной гноем. Стоит заметить, что процесс настолько стремительный, что в него втягивается полезная микрофлора и при ускоренном размножении, она увеличивает объемы выделяемого гноя.
Излюбленные места локализации микроорганизмов – слизистые ткани ротовой полости, носа, кишечника, глаз и половых органов, но стоит заметить, что выявить и идентифицировать патогенного агента сложно.
Лишь точно определив бактерию, спровоцировавшую гнойное образование, может быть назначено адекватное лечение абсцесса с положительным результатом.
Из многообразия существующих микроорганизмов, стоит рассмотреть наиболее популярные виды в практике хирургов:
- Staphylococcus aureus – золотистый стафилококк, определяют в 30% случаев при возникновении нагноений. При бактериальном посеве, наблюдают чистую культуру, без примесей сопутствующей микрофлоры.
Подобрать губительные для золотистого стафилококка антибиотики при абсцессе мягких тканей достаточно сложно, так как штаммы не всегда реагируют на медикамент.
При формировании патологического очага, ограниченный участок наполняется гноем и сопровождается воспалительным процессом рыхлой клетчатки. Такое явление можно наблюдать в следующих случаях:
- в раневых полостях герметично закрытых швами;
- в колотых ранах;
- в углублении от огнестрельного ранения;
- в месте образования гематом, лимфоэкстравазатов;
- в участках размозжения тканей;
- как следствие образования метастаз из других очагов инфекции;
- после подкожной инъекции скипидара, керосина, хлоралгидрата.
Терапевтические схемы могут быть эффективными при определении точной причины, спровоцировавшей признаки абсцесса.
Для патологии в остром течении, которая подлежат визуализации, свойственны классические проявления болезни:
- гиперемия очагов;
- местная болезненность;
- гипертермия на месте новообразования;
- отек, припухлость тканей;
- нарушение процессов и дисфункция органа;
- упадок сил;
- отсутствие аппетита;
- повышение температуры тела.
Симптоматика острого абсцесса может отличаться, так как место локации влияет на клиническую картину.
| МЕСТО ЛОКАЦИИ | ПРИЗНАКИ АБСЦЕССА |
|---|---|
| Абсцесс легкого | Кашель с выделением гнойных мокрот, боль в грудной клетке, нарушение дыхания |
| Абсцесс горла | Вызывает боль при глотании, может спровоцировать удушье; при паратонзиллярном, заглоточном абсцессе, осложнение требует срочного вмешательства врача, так как исход может быть летальным |
| Абсцесс ноги | Поверхностный абсцесс мягких тканей, легко диагностировать по внешним признакам (боль, покраснение, местная температура, симптом флюктуации); при глубоком очаге – пациент жалуется на слабость, разбитость, головную боль, озноб и высокую температуру 39+ |
| Абсцесс печени | Гипертермия до 38+; боль под ребрами с правой стороны; гепатомегалия; мышечная дрожь, асцит; отсутствие аппетита, желтуха; «гусиная кожа» |
| Абсцесс ягодицы | Если в области ягодицы развивается абсцесс после укола:
|
| Абсцесс зуба | Интенсивная ноющая, пульсирующая боль; чувствительность зуба к температурам; зловонный, гнилостный запах; гипертермия, увеличение лимфатических узлов; раны, язвы на деснах |
| Абсцесс бартолиновой железы | Характерный признак – объемное новообразование на половых губах; увеличение паховых лимфатических узлов, боль; гиперплазия слизистых тканей, отек |
| Абсцесс головного мозга | Сильные головные боли; высокое внутричерепное давление, приступы тошноты, рвота; на поздних сроках возможно развитие бреда и галлюцинаций |
| Абсцесс почки | Гипертермия до +40, озноб; болевые ощущения в пояснице; упадок сил; тошнота; болезненное мочеиспускание; потеря веса; профузная потливость |
| Абсцесс брюшной полости | В начале болезни у пациента наблюдают общие симптомы, далее проявляются признаки отравления, тошнота, рвота; паралитическая непроходимость; боль в очаге; плотность, напряженность брюшины |
| Абсцесс миндалин | Резкая односторонняя боль при глотании; иррадиация болезненности в ухо; лихорадка до 38+, упадок сил; нарушение сна; увеличение лимфатических узлов; гиперсаливация; гнилостный запах изо рта |
| Абсцесс бедра | Гной может скапливаться без локальных и общих проявлений и свойственно такое явление при определенных фазах костно-суставного туберкулеза, актиномикоза; могут образовываться свищи с крошкообразным выделением гноя |

Гнойные новообразования бывают доброкачественными — содержат густой гной. При лабораторных исследованиях в структуре содержимого выявляют большие объемы лимфоцитов.
В содержимом капсулы почти отсутствуют микроорганизмы. При диагностировании злокачественного очага, гной включает в себя большое количество микроорганизмов.
Перед назначением лечения, врач определяет место расположения пораженного участка. По локации гнойные образования классифицируют следующие абсцессы:
- мягких тканей — охватывает мышцы и жировую клетчатку;
- Бецольда — глубоко расположенный гнойник в мышцах шеи;
- мозга головы;
- легочной;
- малого таза;
- бактериальный, амебный либо печеночный;
- осложнение аппендицита в острой форме либо аппендикулярный нарыв;
- заглоточный;
- гнойный очаг между петлями кишечника и брюшиной;
- осложнение ангины — паратонзиллярный;
- поражение клетчатки, вокруг оболочки спинного мозга — спинальный эпидуральный абсцесс.
Патологию принято классифицировать по продолжительности течения на хроническую и острую.
Острая — развивается молниеносно и имеет явно выраженную, докучающую симптоматику.
Хронический абсцесс — сложно поддается лечению, создает дискомфорт и сопровождается частыми рецидивами.
Клиническое течение болезни не однозначно, так как на него влияет причина, место локации, индивидуальные особенности пациента и наличие сопутствующих патологий. Соответственно наблюдают следующие отличия:
- Холодные абсцессы — проявляются при занесении палочки Коха либо грибка актиномикоза. Особенностью течения считается медленное развитие и полное отсутствие признаков воспаления.
- Поддиафрагмальный — гнойная капсула под диафрагмой, как следствие хирургического вмешательства (послеоперационный абсцесс), травм.
- Натечный абсцесс — скопление гноя в ограниченном количестве. При таком течении не наблюдается острое воспаление.
- Горячие — дают высокую местную температуру из-за жизнедеятельности гноеродных бактерий в коже, крови, лимфе. После вскрытия абсцесса, боль устраняется, и температура приходит в норму.
Устанавливать диагноз и назначать терапевтические схемы, может только врач.
Преимущественно, проблема такого рода устраняется оперативным вмешательством.
Врач устанавливает окончательный вердикт после осмотра пациента, выслушивания жалоб. Диагностика острого абсцесса, расположенного на поверхности, не представляет сложности. Скрытые в глубоких слоях очаги обнаружить труднее. Для выявления патологии применяют:
- рентгенографию;
- ультразвук;
- КТ;
- МРТ;
- общий анализ крови;
- биохимическое исследование.
Основанием для установки точного диагноза являются результаты анализов и инструментальных исследований.
Появление подкожного абсцесса либо других видимых гнойных новообразований, сигнал требующий вмешательства хирурга.
Самостоятельно вскрывать очаги недопустимо, так как это чревато усугублением проблемы.
Медикаментозная терапия предусматривает назначение антибиотиков, введение ферментных препаратов в полость вскрытого очага.
Сформировавшийся гнойник требует оперативного вмешательства.
В зависимости от сложности случая, удалить абсцесс можно открытым и закрытым способами:
- Открытый — удаляют экссудат из очага, предварительно выполнив широкое рассечение. Для оттока жидкости устанавливают дренирующую трубку и проводят смену повязок ежедневно.
- Закрытая операция — маленькая надсечка, для удаления гноя. После устранения новообразования, в образовавшееся отверстие вставляют трубочку для дренирования. Место операции промывают дезинфицирующими препаратами, накладывают повязку.
Вскрытый абсцесс после операции требует соблюдения стерильности, периодических обработок медикаментами бактерицидного действия.
Для скорейшего созревания абсцессов народный опыт рекомендует следующие средства:
- Луковый пластырь.
Взять 2 части печеного лука и 1 часть натертого мыла. Компоненты хорошо смешать. Приготовить из смеси пластырь и приложить на больное место. Пластырь менять несколько раз в сутки. Помогает быстрому созреванию и очищению нарывов.
- Прополисная мазь.
Кусочек прополиса величиной с грецкий орех помещают в морозильную камеру холодильника, а когда застынет, измельчают.
Затем растапливают 200 г топленого сливочного масла и добавляют туда прополис. Перемешивая, греют на водяной бане минут 30 — до полного растворения прополиса. Смесь охлаждают и процеживают.
Полученную таким образом мазь намазывают на бинт и накладывают на пораженное нарывом место, забинтовывают. Повязку меняют 2-3 раза в сутки. Через несколько часов боль утихает.
Лечатся до выздоровления. Иногда достаточно 2-3 дня лечения, если болезнь не запущена.
- Солевые компрессы.
Повязка из льняной или х/б ткани (в крайнем случае из марли), смоченная в солевом прокипяченном растворе (на 1 л. воды 100 г поваренной соли) и сложенная в 4 слоя (а марля в 8 слоев) накладывается на больные места на ночь, до полного излечения.
Этот метод эффективен при лечении абсцессов, панарициев, не вскрывшихся фурункулов.
Несвоевременное обращение за помощью в медицинское учреждение при гнойном нарыве, несоблюдение рекомендаций врача, нарушение дозировок, могут спровоцировать развитие осложнений. Инфицирование при бездействии прогрессирует, распространяется, сопровождается бактериемией.
Следует понимать, что объемная гнойная капсула, может самопроизвольно разорваться как наружу, так и в соседние полости и ткани, вызвать аррозивные кровотечения.
Если дренирование проведено неадекватно либо упущено время, инфекция переходит в генерализированную форму, а воспаление преобразовывается в хроническое течение патологии.
Запущенная болезнь, приводит к дисфункции жизненно важных органов, анорексии, истощению, распаду тканей.
Не допустить развитие гнойного очага можно выполняя правила асептики и антисептики. Инъекции, обработку ран, должны осуществлять медицинские специалисты с соблюдением техник выполнения манипуляций. Травмы, раны, повреждения, следует своевременно обследовать и если необходимо, прибегнуть к помощи хирурга.
Если проблему своевременно купировать, определить и устранить причину развития патологии, после удаления абсцесса, прогноз на выздоровление — благоприятный. Запущенные формы, могут стать причиной достаточно серьезных осложнений, привести к интоксикации, сепсису и даже летальному исходу.
Гнойные абсцессы – опасное состояние, которое нельзя игнорировать, так как результат жизнедеятельности гноеродных микробов, бывает необратимым. В случае если, иммунитет ослаблен и не помогла операция, симптоматика проявляется более агрессивно, врач назначает антибиотики, симптоматическую терапию, лечение, направленное на дезинтоксикацию.
источник
Возбудителями инфекционного эндокардита обычно являются зеленящий стрептококк (50—70 %), стафилококки (10—30 %), энтерококки и др., включая грамотрицательные бактерии (синегнойная палочка, клебсиелла, кишечная палочка, грибы кандида), встречается смешанная флора. Причиной инфекционного эндокардита может быть преходящая бактериемия, которая появляется после травмы, экстракции зуба (почти в 50 %), урологические инструментальные исследования мочевого пузыря, внутривенное введение наркотиков инфицированными шприцами.
Инфекция чаще поражает клапаны сердца, эндокард, миокард. В очагах инфекции иногда образуются полиповидные выросты, суживающие просвет клапана, инфицированные тромбы, способные перемещаться с током крови в другие части тела, вызывать тромбоэмболию и образование абсцессов и инфарктов в органах, в том числе в стенке сердца, инсультов. Инфекционный процесс часто в короткий срок разрушает сердечные клапаны, чаще всего — клапаны аорты (60—70 %) или оба клапана. Ранним симптомом принято считать появление систолического шума в точке Боткина. В дальнейшем, по мере разрушения клапана, появляется недостаточность аортального клапана с характерным диастолическим шумом в V точке. Лишь у 10 % наблюдается изолированное поражение митрального клапана с последующим развитием митральной недостаточности. Встречаются случаи перфорации митрального или аортального клапана.
Клиническая картина болезни складывается из локальных и общих симптомов, характерных для инфекционного процесса: слабость, ознобы с повышением температуры тела, боли в суставах. При объективном исследовании отмечают появление шумов в сердце или изменение их характера, увеличенную селезенку, анемию, лейкоцитоз, резкое повышение СОЭ, патологические изменения в моче. В типичных случаях сочетание лихорадки с ознобами, появлением шумов в сердце, увеличением селезенки и изменениями в моче дают основание для диагностики септического эндокардита. Диагноз уточняется с помощью специальных методов исследования сердца (ЭКГ, ультразвуковая допплерография, бактериологическое исследование крови).
Лечение. Основой терапии септического эндокардита является антибактериальная терапия современными препаратами и их сочетаниями с учетом чувствительности выделенного из крови возбудителя к антибиотикам.
В последние годы по жизненным показаниям применяют хирургическое лечение. Противопоказанием к операции являются необратимые изменения во внутренних органах, вызванные септическим эндокардитом и генерализованной инфекцией. Оперативное вмешательство производится на сухом сердце с использованием аппарата для искусственного кровообращения. Оперативный доступ — правосторонняя переднебоковая торакотомия в IV или V межреберьях с пересечением 1—2 хрящей верхних ребер. Основная задача вмешательства — ликвидировать очаги инфекции. Для этого используют: 1) механическую санацию — иссечение пораженных клапанов и пораженных внутрисердечных структур (вегетации на пристеночном эндокарде, инфицированные тромбы, абсцессы, отложение кальция), 2) химическую санацию — обработку полостей сердца антибактериальными препаратами, 3) физическую санацию — обработку полостей сердца низкочастотным ультразвуком для воздействия на недоступные для иссечения очаги поражения. Используется также санирующий эффект искусственного кровообращения. Для этой цели в перфузат, используемый во время искусственного кровообращения, добавляют суточную дозу 2—3 антибиотиков с разным механизмом и спектром действия, большую дозу глюкокортикоидов, ингибиторов протеаз, глюкозу и инсулин, увеличивают максимально оксигенацию перфузата. Операция во всех отношениях тяжелая, послеоперационная летальность около 20 %.
источник
Абсцесс (нарыв, гнойник) – это гнойное воспаление, сопровождающееся расплавлением тканей и образованием заполненной гноем полости. Он может образовываться в мышцах, подкожной клетчатке, костях, во внутренних органах или в окружающей их клетчатке.
Причиной абсцесса является гноеродная микрофлора, которая проникает в организм пациента через повреждения слизистых оболочек или кожных покровов, или же заносится с током крови из другого первичного очага воспаления (гематогенный путь).
Возбудителем в большинстве случаев становится смешанная микробная флора, в которой преобладают стафилококки и стрептококки в сочетании с различными видами палочек, например, кишечной палочкой. В последние годы значительно возросла роль анаэробов (клостридий и бактероидов), а также ассоциации анаэробных и аэробных микроорганизмов в развитии абсцессов.
Иногда бывают ситуации, когда полученный при вскрытии абсцесса гной при посеве на традиционные питательные среды не дает роста микрофлоры. Это свидетельствует о том, что в данных случаях заболевание вызывается нехарактерными возбудителями, обнаружить которые обычными диагностическими приемами невозможно. В определенной мере это объясняет случаи абсцессов с атипичным течением.
Абсцессы могут возникать как самостоятельное заболевание, но чаще являются осложнением какой-либо другой патологии. Например, пневмония может осложниться абсцессом легкого, а гнойная ангина – паратонзиллярным абсцессом.
При развитии гнойного воспаления защитная система организма стремится локализовать его, что и приводит к образованию ограничивающей капсулы.
В зависимости от места расположения:
- поддиафрагмальный абсцесс;
- заглоточный;
- паратонзиллярный;
- окологлоточный;
- мягких тканей;
- легкого;
- головного мозга;
- предстательной железы;
- пародонтальный;
- кишечника;
- поджелудочной железы;
- мошонки;
- дугласова пространства;
- аппендикулярный;
- печени и подпеченочный; и др.
Абсцессы подкожной клетчатки обычно заканчиваются полным выздоровлением.
По особенностям клинического течения выделяют следующие формы абсцесса:
- Горячий, или острый. Сопровождается выраженной местной воспалительной реакцией, а также нарушением общего состояния.
- Холодный. Отличается от обычного абсцесса отсутствием общих и местных признаков воспалительного процесса (повышение температуры тела, покраснение кожи, боль). Данная форма заболевания характерна для определенных стадий актиномикоза и костно-суставного туберкулеза.
- Натечный. Образование участка скопления гноя не приводит к развитию острой воспалительной реакции. Образование абсцесса происходит на протяжении длительного времени (до нескольких месяцев). Развивается на фоне костно-суставной формы туберкулеза.
Клиническая картина заболевания определяется многими факторами и, прежде всего, местом локализации гнойного процесса, причиной абсцесса, его размерами, стадией формирования.
Симптомами абсцесса, локализованного в поверхностных мягких тканях, являются:
- отечность;
- покраснение;
- резкая болезненность;
- повышение местной, а в некоторых случаях и общей температуры;
- нарушение функции;
- флюктуация.
Абсцессы брюшной полости проявляются следующими признаками:
- перемежающаяся (интермиттирующая) лихорадка с гектическим типом температурной кривой, т. е. подверженной значительным колебаниям в течение суток;
- сильные ознобы;
- тахикардия;
- головная боль, мышечно-суставные боли;
- отсутствие аппетита;
- резкая слабость;
- тошнота и рвота;
- задержка отхождения газов и стула;
- напряжение мышц брюшной стенки.
При локализации абсцесса в поддиафрагмальной области пациентов могут беспокоить одышка, кашель, боль в верхней половине живота, усиливающаяся в момент вдоха и иррадиирующая в лопатку и плечо.
При тазовых абсцессах происходит рефлекторное раздражение прямой кишки и мочевого пузыря, что сопровождается появлением тенезмов (ложных позывов на дефекацию), поноса, учащенного мочеиспускания.
Забрюшинные абсцессы сопровождаются болью в нижних отделах спины, интенсивность которых усиливается при сгибании ног в тазобедренных суставах.
Симптомы абсцесса головного мозга схожи с симптомами любого другого объемного образования (кисты, опухоли, гематомы) и могут варьировать в очень широком пределе, начиная от незначительной головной боли и заканчивая тяжелой общемозговой симптоматикой.
Для абсцесса легкого характерно значительное повышение температуры тела, сопровождаемое выраженным ознобом. Пациенты жалуются на боли в области грудной клетки, усиливающиеся при попытке глубокого вдоха, одышку и сухой кашель. После вскрытия абсцесса в бронх возникает сильный кашель с обильным отхождением мокроты, после чего состояние больного начинает быстро улучшаться.
Абсцессы в области ротоглотки (заглоточный, паратонзиллярный, окологлоточный) в большинстве случаях развиваются как осложнение гнойной ангины. Для них характерны следующие симптомы:
- сильная боль, отдающая в зубы или ухо;
- ощущение инородного тела в горле;
- спазм мышц, препятствующий открыванию рта;
- болезненность и припухлость регионарных лимфатических узлов;
- повышение температуры тела;
- бессонница;
- слабость;
- гнусавость голоса;
- появление изо рта неприятного гнилостного запаха.
Поверхностно расположенные абсцессы мягких тканей затруднений в диагностике не вызывают. При более глубоком расположении может возникнуть необходимость в выполнении УЗИ и/или диагностической пункции. Полученный во время пункции материал отправляют на бактериологическое исследование, позволяющее выявить возбудителя заболевания и определить его чувствительность к антибиотикам.
Абсцессы ротоглотки выявляют во время проведения отоларингологического осмотра.
Абсцессы могут возникать как самостоятельное заболевание, но чаще являются осложнением какой-либо другой патологии. Например, пневмония может осложниться абсцессом легкого, а гнойная ангина – паратонзиллярным абсцессом.
Значительно сложнее диагностика абсцессов головного мозга, брюшной полости, легких. В этом случае проводится инструментальное обследование, которое может включать:
- УЗИ органов брюшной полости и малого таза;
- магниторезонансную или компьютерную томографию;
- рентгенографию.
В общем анализе крови при любой локализации абсцесса определяют признаки, характерные для острого воспалительного процесса (повышение количества лейкоцитов, сдвиг лейкоцитарной формулы влево, увеличение СОЭ).
В начальной стадии развития абсцесса поверхностных мягких тканей назначается противовоспалительная терапия. После созревания гнойника производится его вскрытие, обычно в амбулаторных условиях. Госпитализация показана только при тяжелом общем состоянии пациента, анаэробном характере инфекционного процесса.
В качестве вспомогательного средства при лечении, а так же для профилактики осложнений абсцессов подкожно-жировой клетчатки, рекомендуется использовать мазь Илон. Мазь следует наносить на пораженный участок под стерильную марлевую повязку или пластырь. В зависимости от степени нагноения, менять повязку необходимо один или два раза в день. Срок лечения зависит от тяжести воспалительного процесса, но, в среднем, для получения удовлетворительного результата нужно применять мазь не менее пяти дней. Мазь Илон К продается в аптеках.
Лечение абсцесса легкого начинается с назначения антибиотиков широкого спектра действия. После получения антибиотикограммы проводят коррекцию антибиотикотерапии с учетом чувствительности возбудителя. При наличии показаний с целью улучшения оттока гнойного содержимого выполняют бронхоальвеолярный лаваж. Неэффективность консервативного лечения абсцесса является показанием к хирургическому вмешательству – резекции (удалению) пораженного участка легкого.
Лечение абсцессов головного мозга в большинстве случаев хирургическое, так как они могут привести к дислокации мозга и стать причиной летального исхода. Противопоказанием к удалению абсцессов является их локализация в глубинных и жизненно важных структурах (подкорковые ядра, ствол мозга, зрительный бугор). В таком случае прибегают к пункции полости абсцесса, удалению гнойного содержимого аспирационным способом с последующим промыванием полости раствором антисептика. Если требуется многократное промывание, катетер, через который оно проводится, оставляют в полости на некоторое время.
При абсцессах головного мозга прогноз всегда очень серьезный, летальный исход наблюдается в 10% случаев, а у 50% пациентов развивается стойкая утрата трудоспособности.
Абсцессы брюшной полости удаляют хирургическим путем.
Абсцессы при несвоевременном лечении могут приводить к тяжелым осложнениям:
- неврит;
- остеомиелит;
- флегмона;
- гнойное расплавление стенки кровеносного сосуда с возникновением угрожающего жизни кровотечения;
- гнойный менингит;
- эмпиема плевры;
- перитонит;
- сепсис.
Прогноз зависит от локализации абсцесса, своевременности и адекватности проводимого лечения. Абсцессы подкожной клетчатки обычно заканчиваются полным выздоровлением. При абсцессах головного мозга прогноз всегда очень серьезный, летальный исход наблюдается в 10% случаев, а у 50% пациентов развивается стойкая утрата трудоспособности.
Профилактика развития абсцессов направлена на предупреждение попадания патогенной гноеродной микрофлоры в организм пациента и включает следующие мероприятия:
- тщательное соблюдение асептики и антисептики при проведении медицинских вмешательств, сопровождающихся повреждением кожных покровов;
- своевременное проведение первичной хирургической обработки ран;
- активная санация очагов хронической инфекции;
- повышение защитных сил организма.
Видео с YouTube по теме статьи:
Образование: окончила Ташкентский государственный медицинский институт по специальности лечебное дело в 1991 году. Неоднократно проходила курсы повышения квалификации.
Опыт работы: врач анестезиолог-реаниматолог городского родильного комплекса, врач реаниматолог отделения гемодиализа.
Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья!
источник
Инфекционный эндокардит — одна из наиболее частых причин возникновения приобретенного порока сердца — дефекта клапанов, который нарушается нормальную насосную функцию сердца по «перекачке» крови.
Что же такое инфекционный эндокардит? Это серьезный инфекционный процесс в организме с преимущественным поражением эндокарда — внутренней оболочки сердца, которая и образует клапаны. Это системное (распространенное) заболевание, по сути — сепсис (заражение крови), при котором страдают многие внутренние органы, не только сердце.
Как и при любой инфекции, для возникновения инфекционного эндокардита необходимо наличие двух факторов:
- Возбудитель. Наиболее часто причиной инфекционного эндокардита являются стафилококк, энтерококк, зеленящий стрептококк. Реже встречаются кишечная, синегнойная палочки, протей, микоплазмы, хламидии, грибы (кандиды, аспергиллы) и пр.
- Нарушение (ослабление) иммунитета, которое может быть вызвано каким-либо предшествующим хроническим заболеванием, неблагоприятной экологией, алкоголизмом и т.д.
Для того чтобы вызвать эндокардит, патогенные микроорганизмы должны попасть в системный кровоток. Кровь в норме у человека стерильна, т.е. в ней нет никаких микробов. На их пути стоит множество заслонов.
Как же бактерии, вирусы или грибы проникают внутрь? Либо с так называемого «первичного очага инфекции», например гнойный отит, либо при выполнении медицинских обследований, манипуляций и операций. А как же использование стерильного одноразового инструментария, спросите вы? Иногда бывают такие ситуации, когда даже самое тщательное выполнение принципов асептики (стерильности) может не помочь предотвратить попадание инфекции. Эти ситуации носят название факторов риска.
- Все стоматологические процедуры, особенно удаление кариозных зубов. Почему? Во рту полно микробов. И рот невозможно стерилизовать при всем желании. При удалении зуба повреждаются сосуды, через эти повреждения могут проникнуть свои же микробы.
- Удаление миндалин (тонзилэктомия).
- Операции на пищеводе, кишечнике.
- Урологические манипуляции и операции, особенно при мочекаменной болезни и сопутствующем пиелонефрите, необходимость установки мочевого катетера на длительный срок и пр.
- Гинекологические вмешательства, особенно аборты.
- Длительная катетеризация вены.
- Искусственная вентиляция легких (ИВЛ), интубация (установка дыхательной трубки в трахею).
При всех этих ситуациях невозможность добиться полной стерильности сочетается с повреждением тканей и сосудов. Если в защите организма есть «брешь», то вероятность заноса инфекции и развития заболевания многократно возрастает.
Также выделяют еще один мощный фактор риска эндокардита — наличие предшествующего заболевания сердца, крупных сосудов (например, аневризма аорты) или порока сердца ревматического, атеросклеротического происхождения. На таких измененных, уже затронутых болезнью клапанах и эндокарде, легко гнездится инфекция. Возникает так называемый вторичный инфекционный эндокардит. Поражает он и искусственные клапаны.
Бактерии с кровью заносятся в сердце, где оседают на клапанах и активно размножаются, формируя вторичный инфекционный (септический) очаг. Их масса образует вегетации (разрастания) на клапанах. Клапаны «съедаются» инфекционным процессом, деформируются, перестают полностью смыкаться (возникает недостаточность с обратным током крови) либо наоборот, срастаются и клапан не может открыться полностью, когда нужно пропустить необходимый объем крови (стеноз). Особенно часто страдает аортальный клапан, хотя другая локализация или поражение нескольких клапанов также не исключается.
Вегетации бактерий могут отрываться и переноситься в другие органы: сосуды селезенки, кишечника, почек, глаз. При этом они перекрывают кровоток в органах (эмболия) и там возникает инфаркт (гибель ткани от недостатка кислорода и питания). Если заносятся мелкие «кусочки» вегетаций, то инфаркта не будет, а разовьется инфекция в этих органах.
Один из главных и первых симптомов — это длительное повышение температуры как бы без видимой причины. Лихорадка может быть постоянной и высокой, а может — волнообразной с периодическими подъемами в течение суток. Температура не снижается при применении жаропонижающих и обычных коротких курсов антибиотиков, сопровождается сильными ознобами и потливостью. В некоторых случаях лихорадка небольшая, либо отсутствует совсем.
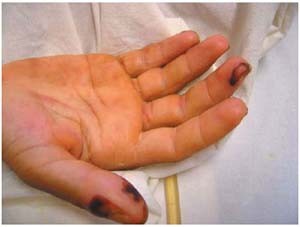
У трети пациентов страдает нервная система из-за эмболии вегетациями. Это проявляется слабостью в правой или левой половине тела, нарушениями зрения, сильными головными болями.
В первую очередь она базируется на совокупности симптомов и выявлении предшествующих заболеванию факторов риска (см. выше). Если у пациента ранее уже имелся порок сердца, то очень часто при присоединении эндокардита меняется аускультативная картина, т.е. шумы либо усиливаются, либо начинают «звучать» по-другому.
Для подтверждения диагноза врачом-кардиологом назначаются:
- неоднократный посев крови для выявления возбудителя, определения его вида и чувствительности к антибиотикам;
- ЭХОКС, которая позволяет «увидеть» разрастания на клапанах, изменения самых клапанов, оценить степень нарушения тока крови в сердце, обратного заброса (регургитации);
- анализы крови. Характерным для большинства пациентов являются анемия, увеличение лейкоцитов и СОЭ. Биохимические показатели (белок, билирубин, трансаминазы и пр.) меняются у всех по-разному;
- анализы мочи;
- УЗИ;
- ЭКГ.
Лечение проводят в стационаре. Основная терапия, это конечно, применение антибиотиков. Выбирают препараты широкого спектра действия в зависимости от вида возбудителя:
- Пенициллины (ампициллин, амоксициллин с клавулановой кислотой);
- Цефалоспорины III, IV поколений (цефтриаксон, цефотаксим, цефтазидим);
- Аминогликазиды (гентамицин, амикацин);
- Ванкомицин, даптомицин.
Длительность первого курса лечения индивидуальна, от 3 до 8 недель большими дозировками, внутривенно и внутримышечно. Часто используют комбинацию двух антибактериальных препаратов.
В дополнение используют жаропонижающие и антигистаминные (противоаллергические) средства, глюкокортикоиды, иммунокорректоры, препараты для лечения сердечной недостаточности. Помогают в выздоровлении плазмаферез и облучение крови ультрафиолетом, активная дезинтоксикационная терапия.
Если клапаны необратимо разрушены и сердечная недостаточность нарастает, не корригируется медикаментозно, то выполняют операцию на сердце по удалению зараженных участков и протезированию клапанов.
Выздоровление (с формированием порока) наблюдается приблизительно в половине процентов случаев. В 15-30% болезнь переходит в хроническую форму, с периодами обострения инфекции и ремиссии. К сожалению, несмотря на усилия врачей, часто бывает и летальный исход — в 20-30%.
источник
Возбудителями инфекционного эндокардита обычно являются зеленящий стрептококк стафилококкиэнтерококки и др., включая грамотрицательные бактерии (синегнойная палочка, клебсиелла, кишечная палочка, грибы кандида), встречается смешанная флора. Причиной инфекционного эндокардита может быть преходящая бактериемия, которая появляется после травмы, экстракции зуба (почти в 50%), урологические инструментальные исследования мочевого пузыря, внутривенное введение наркотиков инфицированными шприцами.
Инфекция чаще поражает клапаны сердца, эндокард, миокард. В очагах инфекции иногда образуются полиповидные выросты, суживающие просвет клапана, инфицированные тромбы, способные перемещаться с током крови в другие части тела, вызывать тромбоэмболию и образование абсцессов и инфарктов в органах, в том числе в стенке сердца, инсультов. Инфекционный процесс часто в короткий срок разрушает сердечные клапаны, чаще всего — клапаны аорты или оба клапана. Ранним симптомом принято считать появление систолического шума в точке Боткина. В дальнейшем, по мере
разрушения клапана, появляется недостаточность аортального клапана с характерным диастолическим шумом в V точке. Лишь у 10% наблюдается изолированное поражение митрального клапана с последующим развитием митральной недостаточности. Встречаются случаи перфорации митрального или аортального клапана.
Клиническая картина болезни складывается из локальных и общих симптомов, характерных для инфекционного процесса: слабость, ознобы с повышением температуры тела, боли в суставах. При объективном исследовании отмечают появление шумов в сердце или изменение их характера, увеличенную селезенку, анемию, лейкоцитоз, резкое повышение СОЭ, патологические изменения в моче. В типичных случаях сочетание лихорадки с ознобами, появлением шумов в сердце, увеличением селезенки и изменениями в моче дают основание для диагностики септического эндокардита. Диагноз уточняется с помощью специальных методов исследования сердца (ЭКГ, ультразвуковая допплерография, бактериологическое исследование крови).
Лечение. Основой терапии септического эндокардита является антибактериальная терапия современными препаратами и их сочетаниями с учетом чувствительности выделенного из крови возбудителя к антибиотикам.
В последние годы по жизненным показаниям применяют хирургическое лечение. Противопоказанием к операции являются необратимые изменения во внутренних органах, вызванные септическим эндокардитом и генерализованной инфекцией. Оперативное вмешательство производится на сухом сердце с использованием аппарата для искусственного кровообращения. Оперативный доступ — правосторонняя переднебоковая торакотомия в IV или V межреберьях с пересечением хрящей верхних ребер. Основная задача вмешательства — ликвидировать очаги инфекции. Для этого используют: 1) механическую санацию — иссечение пораженных клапанов и пораженных внутрисердечных структур (вегетации на пристеночном эндокарде, инфицированные тромбы, абсцессы, отложение кальция), 2) химическую санацию — обработку полостей сердца антибактериальными препаратами, 3) физическую санацию — обработку полостей сердца низкочастотным ультразвуком для воздействия на недоступные для иссечения очаги поражения. Используется также санирующий эффект искусственного кровообращения. Для этой цели в перфузат, используемый во время искусственного кровообращения, добавляют суточную дозуантибиотиков с разным механизмом и спектром действия, большую дозу глюкокортикоидов, ингибиторов протеаз, глюкозу и инсулин, увеличивают максимально оксигенацию перфузата. Операция во всех отношениях тяжелая, послеоперационная летальность около 20% .
Атеросклеротическое поражение венечных артерий является прогрессирующим заболеванием. На ранней стадии развития липиды инкорпорируются в интиме, образуя атеросклеротические бляшки, окруженные фиброзной тканью. Это сопровождается постепенным сужением и уменьшением просвета коронарных артерий, а следовательно, и снижением кровоснабжения миокарда. В ряде случаев фиброзная ткань содержит отложения кальция. В более поздней стадии наступает разрыв ткани над бляшкой, изъязвление ее. Над поврежденной бляшкой образуется тромбоцитарный сгусток, дающий начало тромбу, дальнейшему уменьшению просвета артерий, инфаркту миокарда. По мере сужения венечных артерий наступает несоответствие между потребностью миокарда в кислороде и возможностями его доставки. В связи с этим возникают приступы стенокардии.
По статистическим данным, около одной трети населения умирает от атеросклеротического заболевания коронарных артерий. В начале ишемической болезни сердца преобладает спазм венечных артерий, сопровождающийся ишемическими болями при физической нагрузке (стенокардия напряжения) или в покое (стенокардия покоя). В последующем очень часто возникает инфаркт миокарда.
Атеросклеротическое поражение венечных артерий может быть ограниченным или диффузным. Обтурация их просвета приводит к очаговой ишемии миокарда, которая может быть обратимой или необратимой (инфаркт миокарда). Важнейшим симптомом ишемии являются загрудинные боли, стенокардия.
Клиническая картина и диагностика. Больных беспокоят приступы загрудинных болей, которые прекращаются после приема нитроглицерина; нарушение ритма, приступы сердцебиения. Клинические проявления весьма вариабельны. Согласно классификациисердечной ассоциации (NYHA), тяжесть загрудинных болей и течения хронической ишемической болезни сердца подразделяют на четыре класса. I класс — отчетливых симптомов болезни нет; П класс — появление стенокардии после тяжелой физической нагрузки; III класс — появление стенокардии после легкой физической нагрузки; IV класс — стенокардия в покое. Пациенты, отнесенные кклассу, не испытывают тяжких приступов стенокардии, болезнь не мешает им вести нормальный образ жизни (стабильная стенокардия). В случае нарастания класса болезни в течение короткого периода времени имеется основание говорить о прогрессирующей стенокардии, которая существенно ухудшает прогноз. В поздней стадии ишемия возникает в покое и становится рефрактерной к применяемому медикаментозному лечению (нестабильная стенокардия). Прогноз при этой стадии болезни существенно ухудшается, возникает опасность инфаркта или внезапной смерти. У значительной части больных болезнь развивается не по приведенным классам, а может сразу проявиться инфарктом или внезапной смертью. Иногда наблюдается бессимптомная ишемия миокарда, тогда болезнь распознается только в поздней стадии.
Важную информацию дает электрокардиограмма, полученная в покое и при дозированной физической нагрузке на велоэргометре. Анализ электрокардиограммы позволяет определить выраженность и локализацию (очаги) ишемии миокарда, степень нарушения проводимости, характер аритмии.
Большое значение имеет цветное ультразвуковое допплерографическое и эхокардиографическое исследование. Оно позволяет определить изменения сократительной способности миокарда. По характеру движений стенок желудочков сердца можно выявить очаг и распространенность ишемии миокарда по зонам гипокинезии, акинезии или дискинезии в зоне, снабжаемой суженной ветвью венечной артерии. Замедление скорости движения стенок желудочка при сокращении миокарда называют гипокинезией, отсутствие движения стенки желудочка — акинезией. При аневризме сердца в момент сокращения непораженного миокарда участок выпячивается (дискинезия). Эхокардиографическое исследование позволяет определить систолический, конечнодиастолический и остаточный объемы левого желудочка, фракции выброса, минутный объем и сердечный индекс и другие показатели гемодинамики. Наиболее точную информацию о состоянии коронарного кровообращения даеттомография.
Для уточнения степени и локализации сужения венечных артерий, состояния периферического и коллатерального кровообращения в сердечной мышце производят селективную коронарографию, в том числе кинорентгенографию. Это важно для определения локализации и протяженности сужения перед и во время операции.
Радионуклидные исследования позволяют уточнить обширность очага поражения миокарда по степени накопления нуклида в миокарде.
Прогрессирующее сегментарное сужение венечных артерий неизбежно приводит к инфаркту миокарда. Судьба больного зависит от обширности и локализации инфаркта, степени нарушения функции сердца и внутренних органов.
Лечение. Хирургическое лечение показано при стенозе главного ствола левой коронарной артерии на 75%, при стенозеветвей артерии и клинических проявлениях поклассу NYHA, снижении фракции выброса левого желудочка менее 50% .
Неотложным показанием к операции реваскуляризации миокарда является нестабильная
«предынфарктная ангина», не поддающаяся консервативному лечению, а также резко выраженный стеноз левой венечной артерии, стеноз проксимального участка передней межжелудочковой ветви левой венечной артерии, так как закупорка их сопровождается обширным инфарктом миокарда. При стабильной стенокардии, поддающейся медикаментозному лечению, операцию производят в плановом порядке. Результатом операции является восстановление коронарного кровообращения, у больных после операции исчезают явления стенокардии, резко снижается опасность возникновения инфаркта миокарда.
Рис. 17.6. Аортокоронарное шунтирование.
1 — аортокоронарное шунтирование веной; 2 — правая коронарная ар терия; 3 — левая коронарная артерия; 4 — огибающая ветвь (ramus cir cumflexus); 5 — межжелудочковая ветвь (ramus interventricularus).
Основным способом хирургического лечения атеросклеротических поражений венечных артерий является аортокоронарное шунтирование (bypass — байпас). Операция заключается в создании одного или нескольких анастомозов между восходящей аортой и венечной артерией и ее ветвями дистальнее места окклюзии (рис. 17.6). В качестве шунта используют участок
вены голени (v. saphena magna). В 1964 г. В. И. Колесов впервые сделал анастомоз между внутренней грудной и коронарной артерией ниже ее сужения анастомоз). Эта операция при определенных показаниях производится в ряде учреждений. В настоящее время мобилизованные участки артерий (a. thoracicaa. epigastrica и др.) нередко используются для ангиопластики. По ряду показателей ангиопластика с применением артерии превосходит аортокоронарное шунтирование с применением сегмента вены. Предпосылками для успешной реваскуляризации миокарда являются: 1) стеноз венечных артерий (50% и более) при хорошей проходимости их периферических отделов; 2) достаточный диаметр (не менее 1 мм) периферического участка венечных артерий; 3) сохранение сократительной способности миокарда («живой» миокард) листальнее стеноза артерий.
В последние годы с развитием эндоваскулярной рентгенохирургии для лечения сужений венечных сосудов стали применять их дилатацию с помощью специальных зондов с баллонами, которые вводят в просвет артерии. Наполняя баллон контрастным веществом, добиваются растяжения суженного сегмента просвета артерии и восстановления ее проходимости. Достигнутый при дилатации успех можно закрепить установкой стента.
Выбор метода операции зависит от характера поражения коронарных артерий и состояния пациента по NYHA классу. Делаются попытки разрушения атеросклеротической бляшки лучом лазера. При развитии у больного предынфарктного состояния вследствие тромбоза суженной венечной артерии для обнаружения локализации тромба выполняют экстренную коронарографию. Затем в венечную артерию к месту ее закупорки вводят через катетер стрептокиназу. Таким путем добиваются реканализации венечной артерии, уменьшения зоны ишемии. Впоследствии выполняют аортокоронарное шунтирование в плановом порядке.
Аневризма в большинстве случаев развивается после обширного инфаркта миокарда, сопровождающегося некрозом мышечной ткани и замещением ее рубцовой. Редко причиной аневризмы может быть врожденный дефект развития или травма. Различают также ложные аневризмы, возникающие после ранее перенесенных операций или бактериального эндокардита. Аневризма сердца развивается убольных, перенесших инфаркт миокарда, в большинстве случаев в первые 6 мес, а иногда
источник
Возбудителями инфекционного эндокардита обычно являются зеленящий стрептококк (50-70 %), стафилококки (10-30 %), энтерококки и др., включая грамотрицательные бактерии (синегнойная палочка, клебсиелла, кишечная палочка, грибы кандида), встречается смешанная флора. Причиной инфекционного эндокардита может быть преходящая бактериемия, которая появляется после травмы, экстракции зуба (почти в 50 %), урологические инструментальные исследования мочевого пузыря, внутривенное введение наркотиков инфицированными шприцами.
Инфекция чаще поражает клапаны сердца, эндокард, миокард. В очагах инфекции иногда образуются полиповидные выросты, суживающие просвет клапана, инфицированные тромбы, способные перемещаться с током крови в другие части тела, вызывать тромбоэмболию и образование абсцессов и инфарктов в органах, в том числе в стенке сердца, инсультов. Инфекционный процесс часто в короткий срок разрушает сердечные клапаны, чаще всего — клапаны аорты (60-70 %) или оба клапана. Ранним симптомом принято считать появление систолического шума в точке Боткина. В дальнейшем, по мере разрушения клапана, появляется недостаточность аортального клапана с характерным диастолическим шумом в V точке. Лишь у 10 % наблюдается изолированное поражение митрального клапана с последующим развитием митральной недостаточности. Встречаются случаи перфорации митрального или аортального клапана.
Клиническая картина болезни складывается из локальных и общих симптомов, характерных для инфекционного процесса: слабость, ознобы с повышением температуры тела, боли в суставах. При объективном исследовании отмечают появление шумов в сердце или изменение их характера, увеличенную селезенку, анемию, лейкоцитоз, резкое повышение СОЭ, патологические изменения в моче. В типичных случаях сочетание лихорадки с ознобами, появлением шумов в сердце, увеличением селезенки и изменениями в моче дает основание для диагностики септического эндокардита. Диагноз уточняется с помощью специальных методов исследования сердца (ЭКГ, ультразвуковая допплерография, бактериологическое исследование крови).
Лечение. Основой терапии септического эндокардита является антибактериальная терапия современными препаратами и их сочетаниями с учетом чувствительности выделенного из крови возбудителя к антибиотикам.
В последние годы по жизненным показаниям применяют хирургическое лечение. Противопоказанием к операции являются необратимые изменения во внутренних органах, вызванные септическим эндокардитом и генерализованной инфекцией. Оперативное вмешательство производится на сухом сердце с использованием аппарата для искусственного кровообращения. Оперативный доступ — правосторонняя переднебоковая торакотомия в IV или V межреберье с пересечением 1-2 хрящей верхних ребер. Основная задача вмешательства — ликвидировать очаги инфекции. Для этого используют:
- механическую санацию — иссечение пораженных клапанов и пораженных внутрисердечных структур (вегетации на пристеночном эндокарде, инфицированные тромбы, абсцессы, отложение кальция),
- химическую санацию — обработку полостей сердца антибактериальными препаратами,
- физическую санацию — обработку полостей сердца низкочастотным ультразвуком для воздействия на недоступные для иссечения очаги поражения.
Используется также санирующий эффект искусственного кровообращения. Для этой цели в перфузат, используемый во время искусственного кровообращения, добавляют суточную дозу 2-3 антибиотиков с разным механизмом и спектром действия, большую дозу глюкокортикоидов, ингибиторов протеаз, глюкозу и инсулин, увеличивают максимально оксигенацию перфузата. Операция во всех отношениях тяжелая, послеоперационная летальность около 20 %.
источник
Гнойный перикардит – инфекционное воспаление серозной оболочки сердца, сопровождающееся образованием гнойного выпота в околосердечной сумке. Гнойный перикардит протекает с выраженными симптомами интоксикации (ознобами, лихорадкой, проливными потами, отсутствием аппетита) и нарушения гемодинамики (одышкой, цианозом, приступами сердцебиения и болей в области сердца). Диагноз гнойного перикардита устанавливается по данным рентгенологического обследования, эхокардиографии, пункции перикарда. Лечение гнойного перикардита включает антибиотикотерапию, дренирование полости перикарда или перикардэктомию.
Гнойный перикардит – бактериальный экссудативный перикардит, характеризующийся накоплением гнойного экссудата в перикардиальном мешке. Гнойный перикардит чаще носит вторичный характер и осложняет течение ряда заболеваний в кардиологии, пульмонологии, гастроэнтерологии, травматологии. Гнойные перикардиты составляют 7,4—8,8% от числа всех перикардитов. В настоящее время частота развития гнойных перикардитов значительно снизилась, что связано, главным образом, с широким применением антибиотиков. Между тем, летальность при гнойном перикардите крайне высока.
При гнойном перикардите экссудат может заполнять всю перикардиальную полость, однако чаще он осумковывается в одном или нескольких синусах. Количество гнойного экссудата при перикардите может составлять от 100 мл до 1 л.
Гнойный перикардит, как правило, носит вторичный характер и является следствием распространения первичной инфекции любой локализации. В большинстве случаев гнойный перикардит развивается у больных с эмпиемой плевры, медиастинитом, пневмонией, абсцессом легкого, поддиафрагмальным абсцессом, миокардитом, инфекционным эндокардитом. В этих случаях имеет место контактное распространение инфекции на перикард из соседних анатомических областей.
Метастатические (гематогенные и лимфогенные) гнойные перикардиты встречаются у пациентов с остеомиелитом, перитонитом, рожистым воспалением, ангиной, дифтерией, одонтогенной флегмоной полости рта, перитонзиллярным абсцессом, пародонтозом, абсцессом мягких тканей, сепсисом. При некоторых вирусных инфекциях (гриппе, ветряной оспе, кори) снижение иммунобиологической реактивности организма приводит к присоединению бактериальной инфекции и развитию гнойного перикардита кокковой природы.
Гнойный перикардит может являться осложнением пункции перикарда, торакальных и кардиохирургических операций, огнестрельных и ножевых ранений сердца. В литературе имеются сведения о возникновении бактериальных перикардитов на фоне аневризмы брюшной аорты микотической этиологии, рака пищевода, вследствие выполнения операции фундопликации по Ниссену, резекции желудка и др.
Наиболее распространенным патогенном, вызывающим гнойный перикардит, остается золотистый стафилококк (22–31% случаев). Реже встречаются гнойные перикардиты, обусловленные стрептококками, пневмококками, протеем, энтерококком, клебсиеллой, микоплазмой, микробактерией туберкулеза, гонококком. Среди анаэробных возбудителей выявляются превотеллы, пептострептококи, пропионовые бактерии акне и др.
Патоморфологические изменения при перикардите проходят стадии фибринозного, серозного, и гнойного воспаления. При умеренной экссудации всасывательная способность перикардиальных листков сохраняется, поэтому изменения перикарда характеризуются гиперемией, набуханием и десквамацией мезотелия, выпадением фибрина между листками перикарда. При попытке отделения перикарда от эпикарда фибринозные тяжи создают феномен «волосатого» или «ворсинчатого» сердца.
При значительно выраженных экссудативных процессах в перикардиальном мешке вначале накапливается серозный выпот, содержащий хлопья фибрина, слущенный мезотелий, клетки крови. При инфицировании содержимого околосердечной сумки, на стадии гнойного перикардита, в выпоте дополнительно обнаруживаются патогенные микроорганизмы, простейшие, грибы и пр.
В стадии организации выпота и последующего рубцевания может отмечаться обызвествление и оссификация рубцовой ткани, что приводит к иммобилизации сердца. Рубцовые изменения могут захватывать не только перикард и эпикард, но иногда и все сердце, распространяясь до эндокарда («панцирное сердце»). Рубцевание и обызвествление листков перикарда и эпикарда ограничивает силу и амплитуду сердечных сокращений; в этих условиях насосная функция сердца осуществляется только благодаря движениям межжелудочковой перегородки (констриктивный перикардит).
Преобладающими синдромами в клинике гнойного перикардита являются интоксикация и выраженные гемодинамические нарушения. Тяжелое состояние больных усугубляется проявлениями первичного очага инфекции.
Практически у всех пациентов с гнойным перикардитом отмечается гектическая лихорадка, потрясающие ознобы, общая слабость, адинамия, проливные поты, отсутствие аппетита. По мере накопления гнойного экссудата в перикардиальной полости возникают симптомы нарушения сердечной деятельности: цианоз, одышка, тахикардия, ощущения тяжести и болей в области сердца. Боли могут иррадиировать в левую руку, напоминая клинику стенокардии. Мучительная одышка вынуждает пациента с гнойным перикардитом принимать положение полусидя, облегчающее дыхание.
Компрессионный синдром, обусловленный сдавлением сосудов, трахеи и пищевода находит проявление в набухании вен шеи, кашле, дисфагии. Затруднение венозного кровообращения сопровождается похолоданием кожных покровов головы, шеи, верхней части туловища, верхних конечностей.
При гнойном перикардите рано возникает тампонада сердца, характеризующаяся артериальной гипотонией, нарастанием венозного давления, появлением давящих болей в сердце, в эпигастральной области, увеличением и резкой болезненностью печени, чувством страха смерти. При тампонаде сердца критическое падение сердечного выброса приводит к нарушениям мозгового кровообращения; в этом случае только лишь экстренно предпринятая разгрузка полости перикарда от экссудата позволяет спасти жизнь больного. Частота развития тампонады сердца при гнойном перикардите варьирует от 42 до 80%.
Исходом гнойного перикардита могут являться адгезивный или фиброзный перикардиты, требующие выполнения перикардэктомии.
При осмотре больного с гнойным перикардитом выявляется припухлость поверхностных тканей прекардиальной области, сеть венозных коллатералей на груди, болезненность в эпигастральной области, увеличенная печень. При аускультации обнаруживается шум трения перикарда, глухость сердечных тонов; перкуторно определяется увеличение сердечной тупости в форме треугольника. Пульс учащенный, слабый, АД снижено. Изменения в общем анализе крови характеризуются признаками выраженного воспаления — нейтрофильным лейкоцитозом, высокой СОЭ.
При рентгенографии органов грудной клетки определяется интенсивная треугольная тень в области сердца, обусловленная заполнением гноем наддиафрагмальных и передневерхнего заворотов перикардиальной полости.
Информативным инструментальным методом обследования при гнойном перикардите является ЭхоКГ, позволяющая выявить даже незначительное количество выпота в полости перикарда, определить признаки тампонады сердца. С помощью эхокардиографии с высокой степенью точности можно судить о гнойном характере экссудата по наличию гиперэхогенных включений, хлопьев, взвеси, внутриперикардиальных тяжей, утолщенного перикарда. Большое значение в диагностике гнойного перикардита имеют компьютерная и магнитно-резонансная томография сердца.
Окончательно диагноз гнойного перикардита подтверждается при проведении пункции перикарда. С целью профилактики ранения сердца пункция осуществляется под контролем УЗИ и электрокардиограммы. В процессе чрескожного перикардиоцентеза получают густой мутный экссудат, содержащий множество нейтрофильных лейкоцитов, фибрина, белка и нередко бактерии. Для уточнения этиологии гнойного перикардита производится культуральное исследование выпота.
Дифференциальная диагностика гнойного перикардита проводится с левосторонним экссудативным плевритом и расширением границ сердца.
Лечение гнойного перикардита осуществляется в специализированном кардиохирургическом стационаре. В острой фазе проводятся консервативные мероприятия: назначаются антибиотики с учетом чувствительности возбудителя, проводится симптоматическая терапия (анальгетики, сердечные препараты, мочегонные, оксигенотерапия).
Пациентам с гнойным перикардитом выполняются лечебные пункции или чрезкожное дренирование перикарда с целью эвакуации гнойного выпота. Наряду с системной противомикробной терапией, осуществляется внутриперикардиальное введение антибиотиков и ферментов (урокиназы, стрептокиназы).
При отсутствии эффекта от консервативного ведения гнойного перикардита решается вопрос о проведении хирургического дренирования — перикардиотомии, позволяющей опорожнить полость перикарда от гноя. При наличии плотных спаек, локализованного гнойного выпота, повторяющейся тампонады сердца, сохраняющейся инфекции показана перикардэктомия.
При отсутствии специального лечения гнойный перикардит в 100% случаев приводит к летальному исходу из-за тампонады сердца и интоксикации. Медикаментозное лечение гнойного перикардита сопровождается гибелью больных в 66-82% случаев. Комплексный подход к ведению гнойного перикардита в условиях специализированного кардиохирургического стационара позволяет снизить показатели летальности до 20-36%. В связи с последующим констриктивным перикардитом в дальнейшем нередко развивается сердечная недостаточность. Пациентам, перенесшим гнойный перикардит, требуется наблюдение кардиолога и кардиохирурга.
Профилактика гнойного перикардита требует предупреждения и своевременного лечения заболеваний, осложняющихся воспалением перикарда (ангины, гнойных заболеваний легких, плевры, средостения), соблюдения хирургических техник при операциях на грудной полости, правильной обработки ран сердца и перикарда.
источник