- Боль в деснах
- Боль в лимфоузлах на шее
- Выделение гноя из свища
- Гной в десневых карманах
- Головная боль
- Кровоточивость десен
- Нарушение сна
- Невозможность нормально пережевывать пищу
- Обнажение корня зуба
- Отечность десны
- Повышенная температура
- Повышенная чувствительность зуба
- Повышенное слюноотделение
- Покраснение слизистой рта
- Потеря аппетита
- Расшатывание зубов
- Рвота
- Свищ на десне
- Тошнота
- Увеличение лимфоузлов на шее
Пародонтальный абсцесс — воспалительный процесс в десне, на фоне которого формируется образование с размерами от небольшой горошины до грецкого ореха, а внутри очага гнойная жидкость. Мужчины и женщины страдают от патологии в равной степени.
Главными причинами возникновения абсцесса служат обострение воспалительно-деструктивного процесса в пародонте, наличие глубоких десневых карманов и твердых отложений, скапливающихся под десной.
Симптомы заболевания выделяют специфичные (патологическая подвижность зубных единиц) и общие (повышение температуры тела и ухудшение общего состояния).
Диагностика основывается на лабораторно-инструментальных обследованиях, которые в обязательном порядке дополняются манипуляциями, выполняемыми непосредственно стоматологом, в частности физикальным осмотром ротовой полости.
Лечить абсцесс десны принято только хирургическими методиками, которые направлены на предупреждение развития непоправимых осложнений и достижение стойкой ремиссии.
В международном классификаторе заболеваний десятого пересмотра абсцесс не обладает отдельным шифром, а относится к категории «Другие повреждения пародонта». Из этого следует, что код по МКБ-10 будет К05.2.
Как известно, в ротовой полости проживает большое количество условно-патогенных микроорганизмов, составляющих нормальную микрофлору рта. Однако под влиянием негативных факторов бактерии могут увеличивать свою численность, приникая в десневые карманы и приводя к воспалительному процессу в десне.
Таким образом, пародонтальный абсцесс может быть сформирован на фоне таких патологий:
- пародонтит;
- гингивит;
- пародонтоз;
- неправильно подобранные зубные протезы;
- механическое травмирование или ожог десны;
- некачественная работа стоматолога, установившего пломбу, которая постоянно соприкасается и травмирует десну;
- частое протекание инфекций;
- попадание постороннего предмета в десневой карман;
- нарушение обмена веществ;
- наличие у человека патологий эндокринной системы;
- любые иммунодефицитные состояния.
Среди местных причин развития абсцесса стоит выделить:
- сохранившаяся циркулярная связка зубной единицы;
- глубоко расположенные зубные отложения;
- неполный отток гнойной жидкости;
- течение хронического пародонтита, особенно средней или тяжелой степени.
Нередко абсцесс формируется после удаления зуба, особенно в тех ситуациях, когда возникли осложнения после процедуры или при неадекватной работе стоматолога.
Основную роль в возникновении болезни играют такие микроорганизмы:
- Prevotella intermedia;
- Porphyromonas gingivalis;
- Bacteroides forsythus;
- Treponema denticola.
Группу риска составляют лица преклонного возраста, однако это вовсе не означает, что абсцесс не может развиваться на десне у ребенка или у людей средней возрастной категории.
По характеру протекания десневой абсцесс бывает:
- острый — отличается ярким проявлением клинических признаков и резким нарастанием болевых ощущений;
- хронический или холодный — характеризуется стертой симптоматикой, на первый план выходят такие симптомы, как повышенная кровоточивость и болезненность десен.
Опираясь на локализацию воспалительно-гнойного процесса, абсцесс может быть расположен в таких зонах:
- апикальная область корней зубных единиц;
- в середине корня;
- район пришеечной части зуба.
Пародонтальный абсцесс может быть единичным и множественным.
Первыми клиническими признаками абсцесса выступают сильнейший болевой синдром и отечность пораженной части десны. По мере прогрессирования патологического процесса в острой форме будут возникать следующие внешние проявления:
- покраснение слизистой;
- гиперемия;
- глубокие пародонтальные карманы, наполненные грануляциями;
- патологическая подвижность зубных единиц 2 или 3 степени тяжести протекания;
- проблемы с пережевыванием пищи;
- оголение корней зубов;
- увеличение и болезненность регионарных лимфатических узлов;
- усиление болевых ощущений при надавливании на очаг;
- повышенная чувствительность зубов к горячим или холодным напиткам и блюдам.
Когда пародонтальный абсцесс увеличивается в размерах, клиническая картина будет дополняться такими признаками:
- сильнейшие головные боли;
- постоянная тошнота, изредка приводящая к рвотным позывам;
- возрастание температуры;
- нарушения сна;
- снижение аппетита.
Симптомы хронического пародонтального абсцесса представлены таким перечнем:
- кровоточивость десен;
- умеренно выраженные болевые ощущения;
- пародонтальные карманы полностью наполняет гнойный экссудат;
- повышенное слюнотечение;
- трудности с пережевыванием пищи.
Возможно формирование свища, через который вытекает гнойная жидкость. Тем не менее, это вовсе не означает, что человеку не нужна консультация работников стоматологических учреждений.
При возникновении одного или нескольких вышеуказанных признаков следует как можно быстрее обратиться за квалифицированной помощью к стоматологу. Однако если боль высокой интенсивности, можно немного унять ее самостоятельно.
Таким образом, доврачебная помощь объединяет:
- полоскание ротовой полости антисептическими растворами или отварами на основе ромашки, зверобоя или шалфея;
- прикладывание льда к проблемной области — использовать теплые компрессы категорически запрещено;
- осторожное очищение больного зуба и окружающего пространства от частичек пищи;
- прием слабодействующих анальгетиков — недопустимо самостоятельно использовать антибиотики и противовоспалительные вещества.
Поставить диагноз «пародонтальный абсцесс» может стоматолог-терапевт или пародонтолог. Помимо назначения лабораторных тестов и инструментальных обследований, клиницист должен в обязательном порядке самостоятельно выполнить несколько манипуляций.
Таким образом, первичная диагностика включает:
- изучение истории болезни — для поиска острого или хронического патологического процесса, который мог привести к формированию абсцесса на десне у ребенка или взрослого;
- сбор и анализ жизненного анамнеза;
- пальпация проблемного участка десны;
- оценка состояния зубов и их подвижности;
- детальный опрос — для установки первого появления и степени выраженности клинических признаков.
Лабораторные тесты при диагностировании представлены такими анализами:
- общеклинический анализ крови;
- биохимия крови;
- ПЦР-пробы;
- цитологическое изучение гнойной жидкости;
- исследование слюны методом хемилюминесценции.
Среди инструментальных процедур выделяют:
- дентальная рентгенография;
- ортопантомография;
- КТ.
Пародонтальный абсцесс в обязательном порядке следует дифференцировать от таких патологий:
- острое течение или обострение хронического периодонтита;
- нагноение челюстной кисты;
- периостит;
- остеомиелит.
В дополнение может потребоваться консультация стоматолога-хирурга.
Устранение абсцесса осуществляется только хирургическими методами. Перед началом специфического лечения необходима определенная подготовка:
- удаление зубных отложений;
- терапия кариеса и его осложнений;
- полоскание рта антисептиками;
- пероральный прием лекарств, среди которых антибиотики, противопротозойные и противовоспалительные вещества.
Чтобы гнойная жидкость смогла беспрепятственно выходить, осуществляют промывание проблемной области антисептическими растворами под давлением.
При неэффективности вышеописанных процедур проводят хирургическое вскрытие пародонтального абсцесса, что может быть выполнено полулунным или точечным путем.
Такая процедура включает несколько этапов:
- Кюретаж пародонтальных карманов.
- Иссечение грануляций.
- Сглаживание поверхности корня.
- Формирование слизисто-надкостничного лоскута с последующей репозицией.
- Наложение швов.
После операции показаны применение пародонтологической повязки на протяжении 10 суток, фотодинамическая терапия с применением лазера.
Для предупреждения осложнений пациентам рекомендуют:
- отказаться от вредных привычек;
- не переедать;
- принимать в пищу пюреобразные блюда;
- не принимать медикаменты — в случае крайней необходимости разрешены сильнодействующие обезболивающие;
- при любых признаках ухудшения обратиться к лечащему врачу.
Лечение в домашних условиях народными средствами категорически запрещено, поскольку это может привести к увеличению размеров абсцесса и развитию осложнений.
Во избежание появления пародонтального абсцесса необходимо придерживаться несложных общих правил профилактики:
- отказ от пагубных пристрастий;
- рациональное питание;
- избегание травм десны;
- своевременное выявление и лечение любых аномалий, которые могут привести к формированию гнойника;
- соблюдение рекомендаций клинициста после удаления зуба;
- адекватный подбор зубных протезов;
- регулярное посещение стоматолога.
В случаях своевременного обращения за квалифицированной помощью и осуществления комплексной терапии прогноз будет благоприятным: патологический процесс удается полностью купировать или достичь длительной ремиссии.
Однако абсцесс имеет серьезные последствия — необратимую деструкцию костной ткани и высокую вероятность рецидива или обострения.
источник
Мы рады сообщить вам об открытии нового филиала Клиники Доброго Стоматолога в Кировском районе на углу Ленинского проспекта и проспекта Народного Ополчения!
Высококачественные четкие рентгеновские изображения, улучшающие работу персонала и повышающие комфорт пациента, это отличительная черта визиографа DEXIS.
Уважаемые коллеги, пациенты, друзья! Мы рады представить вашему вниманию долгожданную новую главу «Записок Доброго Стоматолога» в разделе «Мои путешествия». Глава посвящена поездке автора на круглый стол в Мюнхене по приглашению 3М ESPE. Читать далее
Перевод предоставлен Александром Островским
Настоящая статья отображае точку зрения на системное применение антибиотиков при лечении заболеваний пародонта. Документ состоит из трех разделов: 1) концепция применения антибиотиков при проведении пародонтологического лечения; 2) эффективность антибактериального пародонтологического лечения; 3) практические аспекты антибактериального пародонтологического лечения. Заключение, данное в настоящей статье, отражает точку зрения Американской Академии Пародонтологии и предназначено для широкого круга специалистов в области стоматологии.
Микробная этиология воспалительных заболеваний пародонта объясняет необходимость использования антибиотиков при проведении пародонтологического лечения.
Антибиотики и другие лекарственные средства назначались пациентам, страдающим пародонтологическими заболеваниями, не поддающимся традиционной механической терапии, пациентам с острыми воспалительными заболеваниями пародонта, ассоциированного с системными проявлениями, с целью профилактики, а также в качестве дополнительной терапии при проведении хирургического и нехирургического пародонтологического лечения. Недавно был опубликован обзор, представляющий медицинские показания для использования антибиотиков.(1) Настоящая статья посвящена использованию антибиотиков при лечении патологии пародонта.
Концепция применения антибактериального пародонтологического лечения основывается на знаниях о патогенных микроорганизмах, пациенте и препарате. Все эти компоненты рассматриваются отдельно.
Рациональное использование антибиотиков при лечении пародонтита основывается на знании возможных патогенов. В пародонтальных карманах было обнаружено более 500 видов микроорганизмов.(2) Однако, в настоящее время относительно небольшое количество штаммов ассоциируется с развитием пародонтита (Таблица 1). Наиболее вероятными возбудителями являются постоянные представители флоры ротовой полости, но могут обнаруживаться микроорганизмы (энтеробактерии, псевдомонады, стафилококки, грибы), вызывающие суперинфекцию, которые не имеют постоянного представительства в полости рта. Повреждение пародонта чаще вызывается не монокультурой, а микстовыми формами.
Наиболее обычными пародонтальными патогенами являются грам-отрицательные анаэробные палочки. Однако, иногда патогенами могут быть грам-положительные факультативные и анаэробные кокки и палочки, а также грам-отрицательные факультативные палочки. Факультативные пародонтальные патогены значительно варьируют по степени чувствительности к различным антимикробным препаратам, что создает определенные трудности при подборе антибактериальной терапии.(4)
Основными кандидатами для проведения системной антимикробной терапии являются пациенты, у которых не удается справиться с активностью процесса, происходит продолжающаяся потеря пародонтального прикрепления, несмотря на тщательно проводимую традиционную механическую терапию. Рефрактерный пародонтит часто вызывается сапрофитными поддесневыми микроорганизмами и, вероятно, обусловлен ослабленным состоянием макроорганизма.(5) Антибактериальная терапия показана пациентам с локализованным ювенильным пародонтитом и другими типами рано возникающего пародонтита(6) или имеющих факторы, предрасполагающие к развитию пародонтита(7). Пациентам с острыми или тяжелыми пародонтальными инфекциями (пародонтальный абсцесс, острый некротизирующий гингивит/пародонтит) также показано лечение антибиотиками.(8) Пациенты, страдающие гингивитом или имеющие компенсированный пародонтит взрослых, обычно хорошо поддаются механической пародонтальной терапии и не получают или почти не получают преимуществ при использовании антибактериальных препаратов.(9)
Эффективность антибактериального пародонтологического лечения зависит от антимикробного спектра и фармакокинетических характеристик препарата(10) и от местных факторов(11), включающих: 1) накопление препарата в тканях; 2) резистентность патогенов, которая осуществляется посредством связывания, потребления или разрушения препарата микроорганизмами, не входящими в спектр действия антибиотика; 3) феномен образования в налете биопленки, защищающей возбудителей; 4) количество микробов, при котором концентрация антибиотика будет достаточна для обеспечения подавляющего эффекта; 5) эффективность защиты макроорганизма; 6) наличие патогенов в пародонтальных карманах, на поверхностях корней и других участках полости рта, не подвергающихся лечению.
Системная антибиотикотерапия имеет ряд преимуществ перед местными аппликациями антибактериальных агентов. Антибиотики действуют на микроорганизмы, с помощью плазмы достигая их в основаниях глубоких пародонтальных карманов, зонах фуркации, в эпителиальных и соединительных тканях. Кроме того, системные антибиотики способны влиять на бактерии, населяющие слизистую полости рта в удаленных от зубов зонах.(12–14) Вероятность значительного подавления или элиминации пародонтальных патогенов полости рта может снизить риск повторной колонизации пародонтальных карманов и прогрессирования заболевания. Более того, системная антибиотикотерапия имеет относительно низкую стоимость для пациента.
К недостаткам системной антибиотикотерапии по сравнению с местным их применением можно отнести невозможность достижения высокой концентрации препаратов в пародонтальной жидкости,(15) наличие побочных эффектов,(16) формирование полирезистентных штаммов микроорганизмов(4) и сомнительная переносимость.(17)
При вовлечении в патологический процесс нескольких штаммов с различной чувствительностью к антибиотикам может быть полезным применение комбинации антибактериальных препаратов. Комбинация должна включать препараты, которые действуют синергично или обладают аддитивным действием in vitro. Например, метранидазол-амоксициллин и метранидазол-ципрофлоксацин действуют синергично по отношению к Actinobacillus actinomycetemcomitans и другим пародонтальным патогенам.(18) Однако, некоторые антибиотики при их применении в комбинации действуют антагонистично и ведут к снижению антимикробной активности. Антагонизм проявляется при комбинации бактериостатичных тетрациклинов и бактерицидных бета-лактамных антибиотиков.(19)*
Проведение контролируемых клинических исследований необходимо для определения эффективности антибиотикотерапии в пародонтологии.20 Данные многих проведенных на настоящий момент исследований трудно интерпретировать вследствие того, что открытые исследования не включают достаточного количества клинических случаев, проводятся в короткие периоды времени, включают неоднородные группы пациентов, не учитывают активность пародонтологического заболевания, не дифференцируют патогенную флору, варьируют режим применения антибиотиков и не осуществляют достаточного контроля за поддесневым налетом.(9) Поскольку многие клинические исследования эффективности антибиотиков при заболеваниях пародонта проводились у пациентов с невысокой или неизвестной степенью активности процесса, могла быть недооценена потенциальная ценность системной антибиотикотерапии при лечении прогрессирующего пародонтита.
Исследования некоторых форм пародонтита оценивали эффективность системных антибиотиков в качестве дополнительной терапии к кюретажу и снятию наддесневых и поддесневых отложений. Нормы эталонной медицинской практики гласят о том, что бактериальная нагрузка должна быть максимально снижена до назначения антибиотикотерапии. В дополнение, настоящее исследование преследует цель выяснить возможный дополнительный клинический и/или микробиологический эффект антимикробных средств в сравнении с плацебо или без применения антибиотиков.
В таблице 2 перечислены исследования, в которых оценивался эффект антимикробной терапии взрослых пациентов с клинической симптоматикой активной стадии пародонтита. В большинстве исследований сделаны выводы о преимуществах антибактериального лечения больных с прогрессирующим пародонтитом в качестве дополнения к традиционной механической пародонтологической терапии, особенно у пациентов, страдающих рефрактерным пародонтитом.
Таблица 3 представляет данные преимуществ применения системных антимикробных средств при лечении локализованного ювенильного пародонтита (ЛЮП). Однако, форма открытого исследования использовалась при оценке ЛЮП в основном из-за ограниченного количества пациентов. Хотя подавление поддесневой Actinobacillus actinomycetemcomitans до минимально определяемого уровня является важнейшей целью лечения локализованного ювенильного пародонтита, 52 других вероятных патогенных микроорганизма, ассоциированных с ЛЮП, также необходимо подавить.
Выбор пациента
Антибиотикотерапия обычно назначается пациентам, у которых пародонтологическое заболевание возникает повторно после проведения традиционной механической терапии. Однако, некоторым категориям больных с высоким риском возникновения заболеваний пародонта, например, страдающих ювенильным пародонтитом или другой формой рано возникающего пародонтита, тоже показано применение антибиотиков во время первоначальной механической терапии.
Микробиологическая диагностика
Микробиологическую диагностику поддесневой флоры можно выполнять после завершения традиционной механической терапии с целью решения вопроса о необходимости проведения дополнительных методов лечения, например, такого как антибиотикотерапия. Для верификации элиминации возбудителя или его значительного подавления и с целью выявления суперинфекции (грам-отрицательные кишечные палочки, псевдомонады и грибки) может проводиться повторное обследование, проводимое с применением микробиологических тестов через 1–3 месяца после окончания антибактериального лечения. При использовании антибиотиков для лечения заболеваний пародонта стоматолог должен знать чувствительность микроорганизмов к антимикробным препаратам, вид возможного возбудителя во избежание назначения препаратов, к которым неизвестные патогены резистентны. Применение неадекватно подобранного антимикробного препарата может привести к размножению возбудителей и недостаточному клиническому эффекту.(53)
Процедуры забора образцов
Микробные образцы могут быть получены из отдельных карманов с недавней патологической активностью или из больших поддесневых очагов. В большом поддесневом патологическом очаге можно обнаружить широкий спектр возбудителей заболеваний пародонта, требующий адекватной антибиотикотерапия.(54) Показательный поддесневой образец может быть получен при заборе материала из одного глубокого кровоточащего или экссудатирующего кармана из каждого квадранта полости рта. Поддесневой материал собирают с помощью стерильных бумажных полосок или кюреты. Для культивирования образцы помещают в транспортную среду, соответствующую условиям поддержания жизнедеятельности выделенных микроорганизмов.
Культуральные методики
Культивирование анаэробных микроорганизмов предоставляет наиболее полноценную информацию о флоре пародонта. Может быть определено общее количество клеток, соотношение возбудителей и наличие необычных поддесневых микроорганизмов. В настоящее время культуральные исследования используют для определения чувствительности микроорганизмов к антибиотикам. К недостаткам этого метода выявления возбудителей относятся значительная продолжительность, необходимость присутствия опытного технического персонала, относительно высокие финансовые затраты, невозможность культивирования некоторых микроорганизмов и ограниченное время выживания высеянных возбудителей.
Некультуральные методиких
Молекулярные генетические методики для определения пародонтальных бактерий включают определение видоспецифичной ДНК и полимеразную цепную реакцию.(55) Эти методики не требуют присутствия живых клеток и являются высоко чувствительными и высоко специфичными. Кроме того, с их помощью можно определить высоко и низко вирулентные штаммы одного и того же вида. Молекулярные генетические тесты относительно легко и быстро выполняются и недороги. Недостатком является ограниченное количество видов, которые могут быть идентифицированы, невозможность проведения тестов на определение чувствительности микроорганизмов к антибиотикам.
Поликлональные и моноклональные антитела могут быть использованы для выявления возбудителя непосредственно в мазках из налета.(55) Большинство иммуно-серодиагностических тестов основано на иммунофлюоресценции и связанной с энзимами иммуносорбции. К недостаткам иммуно-серодиагностических методов относятся ограниченное количество определяемых возбудителей и невозможность проведения тестов на определение чувствительности микроорганизмов к антибиотикам.
Определение чувствительности к антибиотикам
Резистентность возбудителей к антибиотикам постоянно возрастает.(4) Таким образом, определение чувствительности к антибиотикам очень важно при назначении антимикробных средств для лечения пациентов, страдающих рефрактерным пародонтитом. Параметры Ухода Американской Академии Пародонтологии, опубликованные в 1995 году,(56) гласят: При постановке диагноза рефрактерного пародонтита должно быть сделано следующее:
1)Забор поддесневого микробного материала из различных очагов с целью проведения анализов, по возможности, определение чувствительности к антибиотикам;
2)Выбор и назначение адекватного режима антибиотикотерапии;
3)При назначении антибиотикотерапии может быть использована традиционная пародонтологическая терапия;
4)Повторный осмотр и микробиологические исследования по показаниям.
В некоторых клинических ситуациях определение чувствительности к антибиотикам не дает значительной информации, которая могла бы повлиять на способ лечения заболевания. Например, полость рта пациентов с классическими симптомами локализованного ювенильного пародонтита, обычно, колонизирована Actinobacillus actinomycetemcomitans, которая почти всегда чувствительна к тетрациклину in vitro.(16) Кроме того, некоторые возбудители пародонтологических заболеваний (например, Porphyrimonas gingivalis и Campylobacter rectus) обычно чувствительны к широкому спектру антибактериальных средств и их лечение противомикробными препаратами достаточно эффективно.(16)
Выбор aнтибиотика
Относительно небольшое количество исследований было посвящено выбору антибиотика для лечения пациентов с рефрактерным пародонтитом на основании микробиологического исследования поддесневой флоры. Кроме того, оптимальная дозировка антибиотиков остается неясной(10) поскольку большинство режимов применение антимикробных средств было разработано эмпирически, а не посредством тщательных систематизированных исследований.(20) Данные, представленные в таблицах 2 и 3, могут помочь выбрать оптимальный режим антибиотикотерапии. В таблице 4 перечислены наиболее часто назначаемые антибактериальные препараты для лечения пародонтита.(57)
Тетрациклины показаны для лечения пародонтологических инфекций, основным возбудителем которых является Actinobacillus actinomycetemcomitans; однако, при смешанных инфекциях эти препараты могут не обеспечивать достаточного подавления поддесневых патогенов, что не позволит купировать развитие патологического процесса.(11)
Метронидазол может остановить прогрессирование рефрактерного пародонтита, вызванного Porphyrimonas gingivalis и/или Prevotella intermedia при отсутствии других патогенов.(58)
Клиндамицин продемонстрировал эффективность при лечении рефрактерного пародонтита и заболеваний, вызванных Peptostreptococcus и бета-гемолитическим стрептококком и различными грам-отрицательными анаэробными палочками.(34) Клиндамицин должен назначаться с осторожностью из-за возможности возникновения псевдомембранозного колита в результате размножения в кишечнике Clostridium difficile. Другие антибиотики иногда тоже могут вызывать развитие псевдомембранозного колита.
Амоксициллин-клавулановая кислота могут быть альтернативой клиндамицину.(30) При направленной тканевой регенерации системное применение амоксициллина-клавулановой кислоты использовалось для подавления пародонтальных патогенов и увеличения уровня клинического прикрепления.(59)
Ципрофлоксацин эффективен против энтеробактерий, псевдомонад, стафилококков, A. Actinomycetemcomitans и других патогенных микроорганизмов.(60) Ципрофлоксацин может комбинироваться с метронидазолом или бета-лактамными антибиотиками для лечения смешанных пародонтологических инфекций.(57)
Метронидазол плюс амоксициллин обеспечивают относительно эффективное подавление в периодонте A. Actinomycetemcomitans и P. gingivalis при формах пародонтита, возникающих в молодом возрасте, и рефрактерном пародонтите взрослых.(18, 38, 61) Ципрофлоксацин может заменить амоксициллин при лечении пациентов старше 18 лет с аллергией к бета-лактамным антибиотикам.
Антибиотикотерапия может быть показана при хирургическом вскрытии и дренировании острого пародонтального абсцесса, сопровождающегося системной симптоматикой (лихорадка, слабость, лимфоаденопатия). В таблице 5 описаны режимы антибактериальной терапии для взрослых при остром пародонтальном абсцессе.
Последовательность антибактериальной терапии
Антибиотики должны рассматриваться в качестве дополнения к механической пародонтологической терапии. Назначению эффективных антибиотиков предшествует постановка адекватного клинического диагноза, тщательная механическая терапия, а при необходимости, и микробиологические анализы. Ниже представлена практическая последовательность назначения пародонтологического антибактериального лечения.
1)Первоначальное пародонтологическое лечение должно включать тщательную механическую санацию пародонтального очага, при необходимости, с хирургическим обеспечением доступа.
2)Антибиотики могут быть назначены для улучшения эффекта дальнейшего лечения, на основании данных микробиологических исследований, медицинского состояния пациента и принимаемых пациентом в настоящее время лекарственных средств.
3)Клинический эффект должен быть оценен через 1–3 месяца после окончания механической терапии. При прогрессировании пародонтологического заболевания или отсутствии разрешения симптомов воспаления микробиологическое обследование поддесневой флоры может помочь выявить наличие и количество присутствующих пародонтальных патогенов.
4)Если клиническая ситуация того требует, через 1–3 месяца после системной антибактериальной терапии, могут быть проведены дополнительные микробиологические исследования для верификации уничтожения поддесневых патогенов и определения возможных возбудителей суперинфекции. Высокий уровень Streptococcus sangui.v/mitis, Veillonella и актиномицет говорит о здоровом состоянии пародонта или минимальной степени развития заболевания.(62)
5)После разрешения пародонтальной инфекции пациенту должна быть предложена индивидуально разработанная программа поддерживающего пародонтологического лечения. Контроль за состоянием наддесневого налета при проведении поддерживающего пародонтологического лечения может предотвратить повторную колонизацию пародонтальных патогенов.63 При повторном прогрессировании заболевания может понадобиться дополнительное микробиологическое обследование и последующая антибиотикотерапия, направленная на специфический патогенный микроорганизм.
Системная антибиотикотерапия в пародонтологии основывается на том, что специфические микроорганизмы инициируют развитие деструктивных заболеваний пародонта и что антибактериальные средства in vivo способны достичь концентраций, необходимых для подавления патогенов.
Системная пародонтологическая антибактериальная терапия предназначена для увеличения эффективности механического пародонтологического лечения и для поддержания защитных сил организма, борющихся с инфекцией, подавляя поддесневые микроорганизмы, которые остаются после проведения традиционного механического лечения. Патогены могут избежать эффекта механической терапии благодаря своей способности проникать в пародонтальные ткани, оставаясь в анатомических образованиях, недоступных для пародонтологического инструмента, или в результате снижения защитных сил организма хозяина.
Системная антибиотикотерапия показана пациентам, страдающим пародонтитом, неподдающемуся традиционному пародонтологическому механическому лечению. Должны учитываться медицинский статус пациента и возможные перекрестные реакции между принимаемыми лекарственными средствами. У некоторых пациентов является целесообразным провести тесты на определение чувствительности микроорганизмов к антибиотикам. Применение антибактериальной монотерапии позволяет подавить поддесневые патогены в течение продолжительного времени, зависящего от способности защитных систем организма и обеспечения гигиены полости рта. Для лечения пародонтологических заболеваний, вызванных смешанной флорой, показано применение комплексной антибиотикотерапии с целью расширения антимикробного спектра и создания синергичного эффекта от действия антибиотиков.
Увеличение количества бактерий, резистентных к наиболее часто применяющимся антибиотикам, заставляет использовать ограниченный и консервативный подход при назначении системной антибактериальной терапии.
* бета-лактамные антибиотики — антибиотики четырех групп: пенициллины, цефалоспорины, монобактамы и карбапенемы. Антибиотики двух последних групп в основном применяются при лечении госпитальных инфекций. Для бета-лактамных антибиотиков характерно возникновение перекрестных аллергических реакций — иными словами при аллергии к любому препарату из перечисленных выше групп нельзя использовать никакой другой антибиотик, относящийся к бета-лактамным.
Таблица 1 . Взаимосвязь между условно патогенными бактериями пародонта и прогрессирующим пародонтитом*
* Модифицированные данные Sokransky и Haffajee.(3)
Таблица 2 . Клинические исследования системной антибиотикотерапии при лечении пародонтита взрослых в активной стадии заболевания
Таблица 3 . Клинические исследования системной антибиотикотерапии при лечении пациентов с локализованным ювенильным пародонтитом
Таблица 4 . Обычные режимы антибиотикотерапии при лечении пародонтита*
* Данные Slots и Van Winkellhoff.(57)
Таблица 5 . Режимы антибиотикотерапии при лечении острого пародонтального абсцесса*
* Данные Pallasch.(16)
источник
Пародонтальный абсцесс — это довольно распространенное заболевание в области пародонтологии.
Любой абсцесс — это гнойник, расположенный в мягких тканях, который лечится только хирургическим путем. Поэтому при первых признаках появления опухоли лучше сразу показаться стоматологу.
Если затянуть с визитом к врачу, инфекция может проникнуть глубоко внутрь корня и поразить костную структуру челюсти.
Наибольшую опасность возникновение патологического процесса представляет для женщин в период гестации, или в детском возрасте из-за не до конца сформировавшегося иммунитета.
Для ослабленного организма даже легкая инфекция может закончиться заражением всего организма.
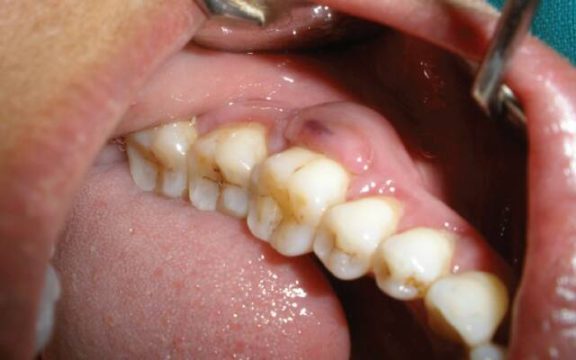
Пародонтальный или периодонтальный абсцесс – это гнойное новообразование, которое возникает на фоне развития деструктивных процессов в тканях десны.
Согласно международной классификации 10-го пересмотра (МКБ-10) болезнь проходит под кодом К05.2, который включен в группу «Острый пародонтит».
Заболевание различается по форме, степени тяжести и месту локализации.
Чтобы определить развитие абсцесса в ротовой полости нужно знать его симптомы, иметь представление, что спровоцировало проблему и как это лечится.
Эффективность лечения напрямую зависит от стадии развития гнойного воспаления. Чем раньше вы отреагируете на его появление, тем легче и быстрее избавитесь от проблемы.
В норме, в микрофлоре полости рта постоянно обитает масса бактерий и микробов, которые содействуют бесперебойной работе функций организма.
Однако под воздействием провоцирующих факторов, колония патогенных микроорганизмов начинает активно размножаться.
Проникая в пародонтальные карманы десны, вредоносные бактерии вызывают воспалительные процессы слизистой, вплоть до образования гнойного нарыва.
Причины, провоцирующие образование абсцесса в мягких тканях пародонта, бывают двух типов — экзогенные (внешние) и эндогенные (внутренние).
- Воспаление десны на фоне стоматологических заболеваний (гингивита, пародонтита, пародонтоза, периодонтита).
- Механические повреждения — травмы, химические и термические ожоги слизистой оболочки.
- Ошибки врачей — неправильно подобранный или установленный протез, брекет-система, нависающие пломбы, нарушение прикуса.
- Часто нарыв появляется на фоне сложного удаления зуба, особенно 8-го моляра.
- Попадание инородного тела в десневой карман (частицы пищи, зубной осколок и т. д.).
- Переохлаждение или перегрев организма.
- Склонность к частым инфекционным заболеваниям.
- Хронические болезни зубов, например, запущенный кариес, средняя или тяжелая стадия пародонтита.
- Нарушения на фоне гормонального сбоя или обмена веществ.
- Дисфункции эндокринной системы, иммунодефицитное состояние любой этиологии.
- Глубокое расположение зубных отложений.
- Недостаточный отток гнойного экссудата.
- Бруксизм — скрежет зубов во сне, вызывающий расшатывание зубов.
По скорости развития, интенсивности болевого синдрома и выраженности симптоматики различают два вида парадонтального абсцесса.
- симптомы выражены и очевидны;
- отмечается резкое усиление болевых и прочих ощущений;
- в десневых карманах образуются гнойные очаги;
- появляются признаки интоксикации.
- абсцесс быстро прогрессирует, в течение короткого срока происходит сильное ухудшение самочувствия человека.
Хронический (или холодный) абсцесс:
- клиническая картина стертая;
- болевой синдром и геморрагия (кровоточивость) слизистой проявляется периодически;
- отмечается возможность спонтанного обострения.
По месту локализации абсцесс может располагаться в следующих зонах:
- на верхушке корневого канала;
- в средней части корня;
- в области пришеечного участка дентина.
При этом воспаление может охватить один зуб, несколько соседних участков или разные зоны челюстной области.
Острый периодонтальный абсцесс даже в начальной стадии имеет яркую клиническую картину, которая выражается следующими симптомами:
- появление небольшого шарика (капсулы) в мягких тканях;
- отечная, гиперемированная десна;
- сильные болевые ощущения, особенно при жевании, пальпации или перкуссии;
- образование парадонтальных карманов, наполненных гнойным экссудатом.
При прогрессировании абсцесса клиника усиливается:
- заметнообнажаются зубные корни, при этом просматривается гнойник;
- появляется гиперестезия (чувствительность на внешние раздражители);
- боль становится нестерпимой;
- при нажатии на пораженное место может выделяться гной, пошатываться зуб.
- рост опухоли может привести к изменению контура челюстей;
- отмечается увеличение лимфоузлов.
А также при развитии воспаления появляются признаки интоксикации и общего недомогания:
- может подскочить температура тела;
- наблюдаются наплывы тошноты, иногда вызывающие рвоту;
- мучительные пульсирующие боли в голове со стороны пораженного участка;
- расстройство сна, потеря аппетита.
При выбухании нарыва может произойти разрыв капсулы с гноем, после чего последует некоторое облегчение.
Однако это не означает, что нужно отменить визит к врачу. Внутри полости может остаться инфекция, которая послужит фактором для рецидива.
Даже при первичном осмотре стоматолог-терапевт может диагностировать развитие пародонтального абсцесса.
Назначение забора крови на увеличение уровня лейкоцитов и анализ ПЦР (полимеразная цепная реакция) на наличие инфекции — подтвердит предварительный диагноз.
Чтобы точно определить глубину, степень тяжести, причину возникновения и возможных осложнений необходимо проведение полноценной диагностики дополнительными методами.
Инструментальное обследование включает следующие процедуры:
- рентген пораженного участка;
- цитологическое исследование гнойного инфильтрата;
- УЗИ, КТ, МРТ — для определения точного места расположения и размеров абсцесса.
Важно дифференцировать новообразование от других воспалительных процессов или заболеваний (периодонтит, нагноение челюстной кисты, остеомиелит) со схожими признаками.
При появлении признаков пародонтального абсцесса больному требуется срочная квалифицированная помощь.
В домашних условиях невозможно справиться с проблемой такого рода. Самолечением можно спровоцировать ухудшение своего состояния и массу серьезных осложнений.
Однако допускаются доврачебные меры, которые помогут на время снять интенсивность болевого синдрома:
- прополоскать рот антисептическими средствами — эффективно применение раствора фурацилина, мирамистина или хлоргексидина;
- аналогичное действие окажет полоскание отварами лекарственных растений (зверобой, ромашка, шалфей);
- приложить наружный холодный компресс с больной стороны, хорошо поможет лед, обернутый в ткань или тонкое полотенце;
- попробуйте аккуратно почистить зубы, чтобы очистить ротовую полость от пищевых частиц;
- можно принять обезболивающие — безрецептурные анальгетики (кетопрофен, нимесулид, ибупрофен).
Категорически запрещается по личной инициативе:
- принимать антибиотики или НВПС (нестероидные противовоспалительные средства);
- прокалывать нарыв или выдавливать гной;
- прогревать место воспаления.
Схема и стратегия лечения зависит от степени тяжести и повреждения зубных коронок на пораженном участке.
Периодонтальный абсцесс начальной стадии начинают лечить предварительными терапевтическими методами:
- профессиональная очистка зубов от налета, камня, отложений;
- при наличии запущенных кариозных очагов проводится соответствующее лечение;
- санация ротовой полости с помощью ирригатора антисептическими растворами для свободного выхода гноя;
- назначение препаратов (антибиотики, НВПС, противопротозойные).
Если методы не оказывают эффективного воздействия, хирург-стоматолог проводит периостомию — вскрытие пародонтального абсцесса.
Оперативный метод включает следующие процедуры:
- делают анестезирующую блокаду больного участка;
- вскрывают нарыв — делают надрез капсулы с гноем;
- проводят кюретаж лунки — выскабливание гнойного экссудата, удаление глубоких поддесневых отложений, резекция пораженных тканей;
- дренирование полости для полного выведения остатков гноя;
- санация раны и слизистой антисептиками;
- для устранения карманов формируют лоскут из мягких тканей надкостницы, который имплантируют на место резекции ткани;
- в завершение накладывают шов.
Для защиты открытой раны, комфорта больного и фиксации лоскута в определенном положении, в течение 7-10 дней после операции применяют пародонтологические повязки на основе оксида цинка.
Гигиенист обучает пациента правильному уходу за полостью рта. При этом поясняет, по каким параметрам рекомендуется выбирать пасты с лечебным эффектом, зубную щетку и прочие принадлежности.
Для стабилизации восстановительного процесса и регенерации тканей в послеоперационный период врачи назначают следующие препараты и процедуры:
- прием таблетированных или в виде инъекций антибиотиков (амоксиклав, сумамед, линкомицин, амоксициллин);
- наружные аппликации или втирания (метрогилдента, асепта, холисал);
- полоскания антисептическими препаратами;
- витаминотерапия (группы В, комплекс С, А, Е, РР), микроэлементы — магний, кальций, селен, железо;
- физиотерапия — ультра- и электрофорез, ультразвуковое и лазерное излучение, магнитотерапия;
- применение народных средств — лекарственные травы для приготовления рецептов для втираний и ротовых ванночек (алоэ, хлорофилл, кора дуба и т. д.);
- гомеопатическая терапия — в качестве противовоспалительной терапии применяют аконит, апис, меркуриус, нукс вомика.
Несмотря на эффективность народных методов и гомеопатии все средства должны быть одобрены врачом.
- воздержание от переедания, курения, алкоголя;
- не злоупотреблять седативными или успокоительными препаратами;
- сильнодействующие анальгетики принимать в крайнем случае;
- исключить из рациона твердое, кислое, острое, сладкое;
- с аккуратностью проводить полоскания и чистку зубов.
При первых признаках дискомфорта или ухудшения состояния (сильная боль, отек, температура) незамедлительно показаться лечащему врачу.
Запущенный периодонтальный абсцесс, самолечение или игнорирование проблемы может закончиться тяжелыми последствиями.
Таблица наиболее распространенных осложнений:
| Название | Основные симптомы | Прогноз врача |
| Свищевой ход | Отек, гиперемия, образование белого или красного пятна с четкими границами, выделение гноя | Удаление зуба в 50% |
| Утрата зуба | Расшатывание коронки 2-3 степени, обнажение корня на 1/3 | Протезирование |
| Абсцесс головного мозга | Устойчиво-высокая температура, сильная цефалгия, заложенность носа, спутанность сознания, раскоординация | Кома, инвалидизация, летальный исход |
| Синусит | Заложенность и гноетечение из носа, боли в области лица | Удаление зуба |
| Ангина Людвига | Инфицирование дыхательных путей, удушье, синюшность лица | При отсутствии лечения возможен летальный исход |
Для предотвращения появления или рецидива воспалительного процесса необходимо систематизировать выполнение рекомендаций врача.
Профилактика пародонтального абсцесса:
- Строгое соблюдение правил гигиены — чистка зубов пастой с лечебным эффектом утром и вечером не менее 3-5 минут + применение ополаскивателя, хороший пример — Listerine «Сильные зубы здоровые десны» или Splat «Лечебные травы».
- Использовать зубную щетку, жесткость которой позволяет эффективно очищать пространства между зубов.
- После каждого приема пищи применять флосс (зубную нить) или ершик, дополнительно проводить полоскание рта, после грубой пиши повторно чистить зубы.
- Старайтесь избегать травмирования слизистой, даже легких проколов или царапин.
- При первых признаках дискомфорта, боли или изменений в тканях ротовой полости сразу покажитесь врачу.
- Раз в полгода проходите плановый осмотр в кабинете стоматолога.
- Сбалансированный рацион с включением максимального количества полезных продуктов и витаминов — это залог здоровья ваших зубов.
источник
Антибиотики в сочетании со скейлингом и сглаживанием корней (scaling and root planing -SRP) могут дать дополнительное преимущество по сравнению только SRP при лечении пародонтита с точки зрения проблемы потери клинического прикрепления, изменения глубины кармана и снижения риска дополнительной потери клинического прикрепления. Однако антибиотики не являются безобидными препаратами. Их использование должно быть оправдано на основе четко выраженной потребности и не должно заменять адекватное местное лечение.
Целью этого обзора является обсуждение обоснования, правильного выбора, дозировки и продолжительности терапии антибиотиками, чтобы оптимизировать медикаментозную терапия пациентов.
Антибиотики определяются как природные или синтетические органические вещества, которые в низких концентрациях ингибируют или убивают некоторые виды микроорганизмов. В течение последних двух десятилетий стоматологи и микробиологи применяли пародонтальную антибиотикотерапию как мощное дополнение к традиционной механической обработке для терапевтического лечения заболеваний пародонта.
Концепция антибиотической пародонтальной терапии сосредотачивается на патогенной микробиоте, пациенте и препаратах. Существует множество антибиотиков, которые можно применять для лечения пародонтальных инфекций, но часто неясно, какой антибиотик будет оказывать наибольшую пользу пациенту с определенной пародонтальной инфекцией и с минимальными побочными эффектами.
Механическое и хирургическое лечение в сочетании с надлежащими мерами гигиены полости рта могут останавливать или предотвращать дальнейшую потерю клинического прикрепления у большинства людей путем уменьшения общей над- и подддесневой бактериальной массы. Однако, несмотря на добросовестную стоматологическую терапию, у некоторых людей продолжается разрушение пародонта, возможно, из-за способности крупных пародонтальных патогенов, таких как Porphyromonas gingivalis, Aggregatibacter actinomycetemcomitans, Fusobacterium nucleatum, Treponemadenticola bacteroids, вторгаться в ткани пародонта или находиться в фуркациях или других структур зуба вне досягаемости для пародонтальных инструментов или из-за слабых механизмов защиты хозяев. Кроме того, предполагаемые пародонтальные патогены («красный комплекс»), как правило, находятся в биопленки, прикрепленной к эпителиальной поверхности пародонтального кармана, и пациент не может достичь этого места во время мероприятий по гигиене полости рта.
Первыми кандидатами на системную антимикробную терапию являются те пациенты, которые проявляют потерю прикрепления после кажущейся адекватной традиционной терапии или пациенты с агрессивными формами пародонтита, имеющие заболевания, предрасполагающие к развитию пародонтита. Пациентам с острыми или тяжелыми пародонтальными инфекциями (пародонтальный абсцесс, острый язвенно-некротический гингивит / пародонтит) также может быть полезно применение антибиотиков.
Системная пародонтальная антибиотикотерапия направлена на усиление механического пародонтологического лечения и поддержку системы защиты хозяев в преодолении инфекции путем уничтожения поддесневых патогенов, которые остаются после обычной механической пародонтальной терапии. Восприимчивость бактерий к антибиотикам может быть ключом к эффективности системных антибиотиков при лечении заболеваний пародонта. Другие химиотерапевтические агенты также могут уменьшить разрушение коллагена и кости за счет их способности ингибировать ферментацию коллагеназы. Пациенты с гингивитом или стабильным взрослым пародонтитом обычно хорошо реагируют на механическую пародонтальную терапию и практически не получают дополнительного эффекта от антибактериальной терапии.
1. Клинический диагноз и ситуация диктуют необходимость возможной антибактериальной терапии в качестве дополнения к контролю активного пародонтального заболевания, поскольку диагноз пациента может изменяться в течение времени.
2. Продолжающаяся активность болезни является показателем для пародонтального вмешательства и возможного микробного анализа путем отбора проб бляшек. Кроме того, случаи устойчивого или агрессивного пародонтита могут указывать на необходимость антимикробной терапии.
3. При использовании для лечения заболеваний пародонта антибиотики выбираются на основании медицинского и стоматологического статуса пациента, приема текущих лекарств и результатов микробного анализа, если таковые проводились.
4. Микробные образцы могут быть получены из отдельных карманов с недавней активностью заболевания или из «объединенных» поддесневых участков. «Объединенный» поддесневой образец может обеспечить хорошее представление о диапазоне пародонтальных патогенов, на которые должна быть нацелены антибиотикотерапия.
5. Отбор проб бляшек может проводиться при начальном обследовании, сглаживании поверхностей корня, повторных осмотрах или при вспомогательном назначении периодонтальной терапии.
6. Также было показано, что антибиотики имеют ценность в снижении необходимости в пародонтальной хирургии у пациентов с хроническим пародонтитом.
7. Системная антибактериальная терапия должна быть дополнением к комплексному плану лечения пародонта. Концентрация антибиотика, в 500 раз превышающая системную терапевтическую дозу, может потребоваться, чтобы быть эффективной против бактерий, расположенных в биопленках. Поэтому важно нарушить эту биопленку физически, чтобы антибиотики могли получить доступ к пародонтальным патогенам.
8. Slots и соавторы описали серию опытов с использованием антимикробных средств для улучшения результатов лечения. Они рекомендуют начинать антибиотики за 1-2 дня до операции и продолжать в течение как минимум 8 дней, однако достоинства этого режима не были хорошо документированы.
9. Haffajee и соавторы пришли к выводу, что данные подтверждают аналогичные эффекты для большинства антибиотиков. Риски и преимущества, связанные с антибиотиками в качестве дополнения к пародонтальной терапии, должны обсуждаться с пациентом до использования антибиотиков.
Установив необходимость использования антибиотика у пациента, часто бывает трудно решить, какой из них выбрать из большого количества доступных. Факторами, определяющими решение о выборе антибиотиков, являются следующие пункты.
1. Возраст пациента. Он может влиять на фармакокинетику многих антибиотиков, например, тетрациклины накапливаются в развивающихся зубах и костях.
2. Почечная и печеночная функция. Осторожное использование и модификация дозы антибиотика становится необходимым, когда есть проблемы в органах выведения.
3. Местные факторы. Условия, преобладающие в месте заражения, сильно влияют на действие антибиотиков, таких как наличие гноя и секретов, некротический материал и инородное тело, низкий уровень рН.
4. Аллергия на лекарственные средства. Должна быть получена история предыдущего воздействия антибиотика и возможности любой аллергической реакции.
5. Нарушение защиты хозяина. У человека с нормальной защитой бактериостатический антибиотик может помочь достичь полного излечения, в то время как интенсивная терапия бактерицидными препаратами является обязательной для пациентов с нарушенной защитой.
6. Беременность. Применение антибиотиков следует избегать во время беременности из-за риска для развивающегося плода.
7. Вопросы, связанные с организмом. Хотя терапия является эмпирической в большинстве случаев, необходимо учитывать вероятность присутствие того или иного патогена.
8. Факторы лекарственного средства. Включают специфические свойства антибиотиков, такие как спектр активности (узкий / широкий), тип активности (бактерицидный / бактериостатический), чувствительность организма (минимальные значения ингибирующей концентрации), относительная токсичность, фармакокинетический профиль, путь введения, доказательства клинической эффективности и стоимость препарата.
Микробная композиция поддесневой бляшки значительно варьируется от пациента к пациенту.
Описание реакции окрашивания по Граму и потребностей инфекционной пародонтальной микробиоты дало первые рекомендации по выбору антимикробной терапии.
Разграничение типа парододонтальной инфекции (экзогенного / эндогенного) может иметь важное значение при выборе правильной стратегии антимикробной терапии в пародонтологии.
При выборе системного антибиотика при терапии пародонта следует особо учитывать два важных фактора: концентрацию в десневой жидкости и минимальную ингибирующую концентрацию.
1. Концентрация десневой жидкости (C GCF ) дает информацию о пиковых уровнях, достигаемых системной доставкой в первичную экологическую нишу. Для пародонтальных патогенов это- пародонтальный карман.
2. Минимальная ингибирующая концентрация 90% (MIC 90 ) представляет собой определение in vitro концентрации, которая будет ингибировать рост 90% бактериальных штаммов исследуемого вида. Противомикробная активность может быть определена как взаимосвязь между C GCF и MIC 90
100 (C GCF / MIC 90 ) = антимикробная активность, выраженная в процентах для каждого антибиотика и каждого организма.
Антибиотики, которые могут достичь 90% -ного ингибирования роста организма, появляются на 100% -ной линии. Наиболее эффективными антибиотиками для лечения определенного пародонтального возбудителя являются те, которые равны или превышают 100% значение.
1. Хронический пародонтит. Антибактериальная терапия обычно рекомендуется для пациентов, имеющих прогрессирующую деструкцию пародонта даже после обычной механической обработки, пациенты не реагирующих на пародонтальную терапию (невосприимчивый, устойчивый пародонтит) и больным с рецидивами заболевания.
В обзоре соответствующей литературы было предложено использовать следующие антибиотики: тетрациклин, доксициклин, метронидазол, клиндамицин, амоксициллин + клавулановая кислота (аугментин), азитромицин, метронидазол + амоксициллин, спирамицин.
2. Агрессивный пародонтит: локализованный агрессивный пародонтит, в основном вызванный Aggregatibacter actinomycetemcomitan, контролируется или устраняется системной комбинированной терапией метронидазол-амоксициллин. Другие антибиотики, рекомендуемые как для локализованного, так и для генерализованного агрессивного пародонтита: тетрациклин, доксициклин, миноциклин, метронидазол, амоксициллин + клавулановая кислота (аугментин), метронидазол + амоксициллин.
3. Некротические пародонтальные заболевания. Пациенты с умеренным или тяжелым ЯНГ или язвенно-некротическим пародонтитом (ЯНП), местной лимфаденопатией и системными проявлениями нуждаются в антибактериальной терапии. Рекомендуемыми антибиотиками являются амоксициллин, метронидазол и комбинация амоксициллина + метронидазола.
4. Пародонтальный абсцесс. Антибиотики показаны для пародонтальных абсцессов с системными проявлениями (лихорадка, недомогание, лимфаденопатия). Антибиотики для лечения абсцессов следует назначать в сочетании с хирургическим разрезом и дренажом.
Схемы приема для взрослых пациентов с острыми пародонтальными абсцессами.
1. Амоксициллин: ударные дозы 1,0 г с последующей поддерживающей дозой 500 мг / день в течение 3 дней с последующей оценкой пациента для определения необходимости дополнительной антибиотикотерапии или корректировки дозы.
2. При аллергии на β-лактамные препараты: азитромицин: ударная доза 1,0 г в день 1, затем 500 мг / ежедневно 2 или 3 дня; или клиндамицин: ударная доза 600 мг в день 1, затем 300 мг / день в течение 3 дней.
1. Используйте высокие дозы в течение короткой продолжительности: успех антибиотика зависит от поддержания концентрации крови и ткани выше минимальной ингибирующей концентрации для целевого организма. Высокие концентрации являются более критическими для аминогликозидов, метронидазола и хинолонов (зависимы от концентрации антибиотика), тогда как длительное воздействие организма на противомикробный агент более критично для бета-лактамов (зависимы от времени воздействия антибиотика).
2. Используйте пероральную ударную дозу для введения антибиотика: без ударной дозы требуется 6-12 часов для достижения максимального терапевтического уровня в крови и в тканях при пероральном введении.
3. Достижение уровня антибиотика в крови в 2-8 раз ниже минимальной ингибирующей концентрации. Такие уровни в крови необходимы для компенсации тканевых барьеров, которые препятствуют проникновению антибиотиков на участки инфекции.
4. Используйте небольшие интервалы между приемами. Это важно для более старых бета-лактамных антибиотиков, таких как пенициллин V и цефалоспорины первого поколения (цефалексин, цефрадин), чтобы поддерживать относительно постоянный уровень в крови.
5. Определите продолжительность терапии путем создания условий для ремиссии заболевания. Прием антибиотика прекращается, когда защитные силы организма получают контроль над инфекцией, достаточный для разрешения процесса. Системно назначенные бактериостатические антибиотики характерно требуют более длительных периодов введения, чтобы быть эффективными по сравнению с их бактерицидными аналогами.
Восемь основных видов антибиотиков были широко изучены и описаны для лечения заболеваний пародонта: тетрациклин, миноциклин, доксициклин, эритромицин, клиндамицин, ампициллин, амоксициллин и метронидазол.
1. Тетрациклин
Фармакология
1. Производится естественным путем из определенных видов Streptomyces или полусинтетических производных.
2. Бактериостатические препараты, эффективнее против быстро размножающихся бактерий и грамположительных бактерий, чем против грамотрицательных бактерий.
3. Концентрация в десневой борозде в 2-10 раз больше, чем в сыворотке.
4. Обладают уникальными не-антибактериальными характеристиками — ингибированием коллагеназы, ингибированием хемотаксиса нейтрофилов, противовоспалительным эффектом, ингибированием микробной адгезии.
Механизм действия
Действуют путем ингибирования синтеза белка путем связывания с 30 S рибосомами в восприимчивом организме.
Клиническое использование
1. Вспомогательный препаратпри лечении локализованного агрессивного пародонтита.
2. Останавливает потерю кости и подавляет уровни A. actinomycetemcomitans в сочетании с скейлингом и сглаживанием корней.
Тетрациклин, миноциклин и доксициклин являются полусинтетическими членами группы тетрациклина, которые использовались при терапии пародонта.
Режим дозирования — 250 мг четыре раза в день.
2.Миноциклин
1. Эффективен против широкого спектра микроорганизмов.
2. Подавляет спирохеты и подвижные палочки так же эффективно, как скейлинг и сглаживание корней, с подавлением до 3 месяцев после терапии.
3. Можно принимать два раза в день, что облегчает соблюдение правил приема.
4. Хотя сопровождается меньшей фототоксичностью и почечной токсичностью, чем тетрациклин, может вызвать обратимое головокружение.
5. Увеличивает уровень препарата десневой жидкости в 5 раз.
6. За исключением влияния миноциклина на актиномицеты, ни один из тетрациклинов по существу не ингибирует рост оральных грамположительных организмов путем системной доставки.
3. Доксициклин
1. Тот же спектр активности, что и у миноциклина.
2. Удобен в приеме, поскольку его необходимо принимать один раз в день, абсорбция из желудочно-кишечного тракта лишь слегка может быть изменена кальцием, ионами металлов или антацидами.
3. Рекомендуемая доза составляет 100 мг 2 раза в день в первый день, затем 100 мг. Чтобы уменьшить желудочно-кишечные расстройства, 50 мг можно принять 2 раза в день.
Сравнение биологических эффектов, пиковых концентраций тетрациклинов после системного введения в обычной дозе для взрослых показано в таблице 1.
4. Метронидазол
Фармакология
1. Синтетическое нитроимидазольное соединение с бактерицидными эффектами в основном применяются против облигатных грамположительных и грамотрицательных анаэробов. Campylobacterrectus является единственным факультативным анаэробным и вероятным пародонтальным возбудителем, который восприимчив к низким концентрациям метронидазола.
2. Спектр активности препарата : превосходное лечение инфекций, вызванных Fusobacterium и Selenomonas , лучший препарат, воздействующий на инфекции Peptostreptococcus , средняя эффективность воздействия на инфекции, вызванные P. gingivalis, Pintermedia и C. rectus , низкая эффективность воздействия на инфекции, вызванные A. actinomycetemcomitans и инфекций E. corrodens , существенно не влияет на подавление роста полезных видов бактерий
3. Концентрации, измеренные в десневой жидкости, обычно немного меньше, чем в плазме.
Способ действия
Метронидазол действует путем ингибирования синтеза ДНК.
Клиническое использование
1. Для лечения гингивита, острого некротического язвенного гингивита, хронического периодонтита и агрессивного пародонтита.
2. В качестве монотерапии метронидазол является не эффективным, его следует использовать в сочетании с обработкой поверхности корня, хирургическим вмешательством или с другими антибиотиками. Наиболее часто назначаемый режим составляет 250 мг трижды в день в течение 7 дней.
3. В исследовании, проведенном Haffajee et al обследовались пациенты с глубиной кармана ≥6 мм. Пациенты, получавших метронидазол или азитромицин, показали значительно большее уменьшение глубины кармана и большее усиление прикрепления , чем пациенты, получавше доксициклин.
5.Пенициллин
Фармакология
1. Природные и полусинтетические производные бульонных культур Penicillium mould.
2. Узкий спектр и бактерицидный характер. Основная активность в грамположительном спектре. Только широкого спектра пенициллины, такие как ампициллин и амоксициллин, обладают значительной антибактериальной антимикробной активностью для грамотрицательных видов.
Способ действия
Вмешивается в синтез клеточной стенки бактерий, ингибируют транспептидазы, так что перекрёстное сшивание не происходит.
Клиническое использование
1. В лечении пациентов с агрессивным пародонтитом, как в локализованных, так и в генерализованных формах. Рекомендуемая доза составляет 500 мг трижды в день в течение 8 дней.
2. Показывает высокую антимикробную активность по отношению к бактериям, которые встречаются в зубодесневой жидкости, за исключением E. corrodens, S. sputigena и Peptostreptococcus, ингибирует рост грамположительных факультативных анаэробов.
Исследования показывают, что более 60% взрослых пациентов с пародонтитом, у которых брали пробы на анализ пародонтльной бляшки, проявили β-лактамазную активность. По этой причине введение чувствительных к β-лактамазе пенициллинов, включая один амоксициллин, обычно не рекомендуется, а в некоторых случаях может ускорять разрушение пародонта.
Амоксициллин-клавуланат (Augmentin). Общепринятой стратегией является введение амоксициллина с ингибитором бета-лактамазы, такой как клавулановая кислота. Аугментин может быть полезен при лечении пациентов с невосприимчивым или локализованным агрессивным пародонтитом.
При направленной тканевой регенерации систематическая терапия амоксициллин-клавулановой кислотой использовалась для подавления пародонтальных патогенов и увеличения усиления клинического прикрепления.
6.Цефалоспорины
Фармакология
1. Используется против инфекций, которых в противном случае можно было бы лечить с помощью пенциллина.
2. Устойчив к ряду β-лактамаз, обычно активных против пенициллина.
Способ действия
Тот же способ действия, что и у пенициллинов, т. е. ингибирование синтеза клеточной стенки бактерий. Однако они связываются с другими белками, чем те, с которыми связываются пенициллины.
Клиническое использование
Цефалексин является цефалоспорином, доступным для введения в пероральной лекарственной форме.
1. Достигает высоких концентраций в зубодесневой жидкости.
2. Эффективно тормозит рост грамотрицательных облигатных анаэробов, не препятствует грамотрицательным факультативным анаэробам.
3. Более новые цефалоспорины с повышенной грамотрицательной эффективностью могут быть полезны при лечении заболеваний пародонта.
7.Клиндамицин
Фармакология
Эффективен против анаэробных бактерий и у пациентов, имеющих аллергию на пенициллин.
Способ действия
Ингибирование синтеза белка путем связывания с 50 S рибосомой.
Клиническое использование
1. Клиндамицин достигает более высоких уровней антимикробной активности, чем другие антибиотики.
2. Gordon и соавторы наблюдали средний прирост клинического прикрепления 1,5 мм и снижение активности болезни у пациентов через 24 месяца после дополнительной терапии клиндамицином.
3. Walker и соаворы показали, что клиндамицин помогает в стабилизации процесса у трудноподдающихся лечению пациентов. Дозировка составляла 150 мг 4р./день в течение 10 дней.
4. Jorgensen и соавторы рекомендовали режим 300 мг 2р./день в течение 8 дней
8.Ципрофлоксацин
Фармакология
1. Фторхинолоновый антибиотик, доступный для перорального введения.
2. Мощный ингибитор грамположительных бактерий (все факультативные и некоторые анаэробные предполагаемые пародонтальные патогены), включая Pseudomonas aeruginosa , с величинами MIC 90 в диапазоне от 0,2 до 2 мкг / мл.
Способ действия
Ингибирование репликации и транскрипции бактериальной ДНК путем ингибирования фермента ДНК-гиразы, фермента, уникального для прокариотических клеток .
Клиническое использование
1. Способствует созданию микрофлоры, связанной с пародонтальным здоровьем, с минимальным воздействием на виды стрептококков, которые связаны с пародонтальным здоровьем.
2. В настоящее время ципрофлоксацин является единственным антибиотиком в пародонтальной терапии, к которому чувствительны все штаммы A. actinomycetemcomitans .
3. Также используется в сочетании с нитроимидазолами (метронидазолом и тинидазолом).
9.Макролиды
Фармакология
1. Содержит полилактонное кольцо, к которому прикреплены один или несколько дезоксисахаров.
2. Может быть бактериостатическим или бактерицидным, в зависимости от концентрации препарата и природы микроорганизма.
3. Макролидные антибиотики, используемые для лечения пародонта, включают эритромицин, спирамицин и азитромицин.
4. Основным ограничением эритромицина является его плохая абсорбция тканями. Препараты для системного введения доступны в качестве пролекарств (эритромицинэстолат, стеарат эритромицина или этилсукцинат эритромицина) для облегчения абсорбции. Пролекарство обладает незначительной антибактериальной активностью до тех пор, пока не будет гидролизовано эстеразами в сыворотке.
Способ действия
Ингибирование синтеза белка путем связывания с 50 S рибосомными субъединицами чувствительных микроорганизмов и препятствование трансляции.
Эритромицин
Клиническое использование
1. Очень безопасный препарат, который часто рекомендуется в качестве альтернативы пенициллину для пациентов с аллергией.
2. Уровни десневой жидкости указывают на то, что лишь небольшая часть достигает пародонтального кармана оральным путем.
Спирамицин
Он выводится с высокой концентрацией через слюну . Результаты различных клинических испытаний показали хорошую эффективность спирамицина в лечении пародонтита, и метаанализ этих исследований показал высокие уровни доказательств, подтверждающих его эффективность . Было показано, что он уменьшает количество зубодесневой жидкости, глубину кармана и спирохет на поддесневом уровне. Herrera и соавторы в мета-анализе, оценивающем спирамицин, амоксициллин совместно с метронидазолом, и метрамидазол показали статистически значимый дополнительный эффект спирамицина по сравнению с другими антибиотиками в отношении уменьшения глубины зондирования кармана для участков с начальной глубиной зондирования более 6 мм
Клиническое использование
Эффективен против грамположительных организмов, оказывает минимальное влияние на увеличение уровня прикрепления.
Азитромицин
Клиническое использование
1. Эффективен против анаэробов и грамотрицательных палочек.
2. После пероральной дозы 500 мг в течение 3 дней в большинстве тканей в течение 7-10 дней могут быть обнаружены значительные уровни азитромицина.
3. Было высказано предположение, что азитромицин проникает в фибробласты и фагоциты в концентрациях, в 100-200 раз превышающих концентрации внеклеточного компартмента. Азитромицин активно переносится в места воспаления фагоцитами, а затем непосредственно высвобождается в местах воспаления как разрыв фагоцитов при фагоцитозе .
4. Терапевтическое применение требует разовой дозы 250 мг / день в течение 5 дней после начальной загрузочной дозы 500 мг.
10.Аминогликозиды
1. Ингибируют синтез белка путем связывания необратимым с конкретным белком или белками 30 S-рибосомной субъединицы.
2. Неактивны в анаэробных условиях, потому что внутриклеточный перенос сильно нарушен в отсутствие кислорода. Поэтому все анаэробные бактерии очень устойчивы, хотя они содержат рибосомы, чувствительные к этим антибиотикам.
Сравнение биологических эффектов, пиковых концентраций тетрациклинов после системного введения в обычной дозе для взрослых (все значения в мкг / мл)
Есть пять проблем, которые замедляют ход антибактериальной терапии:
1. Пародонтальные заболевания гетерогенны;
2. Клинические диагнозы производятся на основании клинических признаков, а не молекулярной патологии;
3. Фактический причинный фактор (ы) не определен окончательно;
4. Нет микробиологической выборки.
5. Существует множество различных протоколов приема антибиотиков, но мало хорошо спланированных рандомизированных контролируемых испытаний, которые проверяют эффективность этих протоколов.
Пародонтальные инфекции могут рассматриваться как смешанные инфекции, в которых участвуют различные аэробные, микроаэрофильные и анаэробные бактерии, как грамотрицательные, так и грамположительные, чувствительные к различным лекарственным средствам. Поэтому лучше использовать более одного антибиотика для охвата всех пародонтальных патогенов в некоторых клинических ситуациях.
Комбинация антибиотиков может помочь
1. Расширить антимикробный диапазон терапевтического режима, выходящий за рамки любого антибиотика.
2. Не допустить или предотвратить возникновение бактериальной резистентности с использованием агентов с перекрывающимися антимикробными спектрами.
3. Уменьшить дозу отдельных антибиотиков, используя возможную синергию между двумя препаратами против целевых организмов.
Недостатками сочетания антибиотиков являются:
1. Повышенные побочные реакции
2. Антагонистические взаимодействия с неправильно подобранными антибиотиками.
Побочные эффекты выбранных антибиотиков, используемых при лечении заболеваний пародонта, приведены в таблице 2.
Антибиотики, которые являются бактериостатическими (например, тетрациклин), обычно эффективны против микроорганизмах, способных к быстрому делению. Они плохо работают, если одновременно назначают бактерицидный антибиотик (например, амоксициллин или метронидазол). Когда требуются оба типа лекарств, их лучше всего назначать поочередно, а не в сочетании, чтобы избежать неблагоприятного взаимодействия, но получить результат от обоих.
В одном из исследований шесть пациентов с рецидивирующим прогрессирующим пародонтитом получали обычную взрослую дозу доксициклина в течение 4 дней с последующим амоксициллином с клавуланатом в течение 5 дней. Пять подобных пациентов получали доксициклин в течение 10 дней. Через 25 недель пациенты, получавшие последовательную комбинацию, имели значительно большее уменьшение глубины кармана, чем те, которые получали только доксициклин.
В другом исследовании все пациенты с рецидивирующим пародонтитом получали регулярное двухмесячное снятие отложений и последовательную дозу доксициклина и метронидазола. В комбинированной группе антибиотикотерапии у 9% наблюдался рецидивирующий пародонтит, тогда как у 42% группы плацебо наблюдались признаки рецидивирующего заболевания. Хотя эти различия статистически значимы, через 7 месяцев после метронидазола не было обнаружено различий в микробиоте между группами.
Сочетание метронидазола и амоксициллина (МА) показало, что это эффективный антибактиериольный режим для борьбы с Aggregatibacter actinomycetemcomitans и Porphyromonas gingivalis-связанными с пародонтальными инфекциями.
Одно из важных клинических исследований было проведено Winkel et al . Наблюдения показали, что пациенты с поддесневым P. gingivalis на исходном уровне, которые получали лечение метронидазолом + амоксициллином, имели в два раза меньше пародонтальные карманы размером> 5 мм после терапии по сравнению с P . gingivalis -положительными пациентами, которые получали плацебо.
Guerreo et al использовали сопоставимый протокол лечения у пациентов с агрессивным пародонтитом и показали значительное улучшение всех параметров пародонта у пациентов, получавших антибиотики, по сравнению с пациентами, получавшими плацебо, через 6 месяцев после лечения.
Эти исследования показали, что при хроническом, а также при агрессивном пародонтите антибиотики приводят к лучшему разрешению воспаления пародонта, улучшению глубины зондирования и уменьшению потери прикрепления.
Метронидазол и азитромицин, по-видимому, более эффективны в деле искоренения анаэробных пародонтопатогенных бактерий, чем доксициклин или механическая терапия.
Комбинация метронидазола и ципрофлоксацина эффективна против A. actinomycetemcomitans . Метронидазол нацелен на облигатные анаэробы, а ципрофлоксацин нацелен на факультативные анаэробы. Это мощная комбинация против смешанных инфекций. Исследования этой комбинации лекарств при лечении трудноподдающегося лечению пародонтита подтвердили значительное клиническое улучшение.
Пациенты с неконтролируемым диабетом, трансплантацией органов, трансплантацией костного мозга, заменой протезного сустава, лейкемией, нейтропенией, тромбоцитопенией подвергаются большему риску развития инфекции после стоматологических процедур из-за иммуносупрессии или уменьшения количества иммунных клеток. Хронические заболевания почек также требует антибиотикопрофилактику для предотвращения эндартериита артериовенозной свищей или шунтов. Для профилактики инфекционного эндокардита у пациентов с предшествующей историей инфекционного эндокардита, с искусственными сердечными клапанами, основными врожденными пороков сердца (тетралогия Фалло, транспозиции больших артерий, хирургически сконструированных системных легочных шунтов или каналов), приобретенной клапанной функцией (например, ревматическая болезнь сердца ), гипертрофической кардиомиопатией, пролапсом митрального клапана, рекомендуется профилактика антибиотиками.
Пародонтальные процедуры, рассматриваемые как процедуры высокого риска у этих пациентов, — это зондирование, скейлинг и сглаживание корней, поддесневое размещение антибиотических препаратов, интралигаментарная анестезия, профилактическая чистка зубов или имплантатов с предполагаемым кровотечением, пародонтальная хирургия, утсановка зубного имплантата.
Амоксициллин используется чаще всего для антибиотикопрофилактики. Рекомендуемая доза составляет 2 г у взрослых и 50 мг / кг у детей, перорально за час до процедуры. Для пациентов, которые не могут использовать пероральные препараты, ампициллин вводят внутримышечно или внутривенно в дозе 2,0 г у взрослых и 50 мг / кг у детей в течение 30 минут до процедуры. У пациентов, страдающих аллергией на пенициллин, предпочтительными антибиотиками являются клиндамицин (взрослые, 600 мг, дети, 20 мг / кг перорально за час до процедуры), цефалексин или цефадроксил (взрослые, 2,0 г, дети 50 мг / кг перорально за час до процедуры ), азитромицин или кларитромицин (взрослые, 500 мг, дети, 15 мг / кг перорально за час до процедуры). Пациентам с аллергией на пенициллин и неспособных принимать пероральные препараты, назначают клиндамицин (взрослым — 600 мг; дети, 15 мг / кг в/в за час до процедуры) или цефазолин (взрослым, 1,0 г, детям, 25 мг / кг в/м или в/в в течение 30 минут до процедуры).
Клинические причины возникновения неудачи антибиотикотерапии следующие:
1. Неправильный выбор антибиотика
2. Появление антибиотикорезистентных микроорганизмов
3. Слишком низкая концентрация антибиотика в крови
4. Медленный темп роста микроорганизмов
5. Нарушенная защита хозяина
6. Несоблюдение режима лечения пациентом
7. Антагонизм антибиотиков
8. Невозможность проникновения антибиотика в место заражения
9. Сосудистые ограничения или снижение кровотока
10. Неблагоприятные местные факторы (снижение рН ткани или кислородного напряжения)
11. Неспособность искоренить источник инфекции (отсутствие разреза и дренажа)
Установлено, что системные антибиотики могут значительно усилить эффекты механической пародонтальной терапии в сочетании с мерами, которые улучшают гигиену полости рта. Клинические исследования системной антибиотикотерапии при пародонтите взрослых, устойчивым к лечению пародонтите, пациентах с агрессивным пародонтитом приведены в таблице 3.
Как было предложено Herrera et al и Haffajee et al средний прирост клинического прикрепления может составить 0,3-0,4 мм.
В качестве контроля выступили пациенты с пародонтитом, прошедшие мониторинг после лечения и поддерживающей пародонтальной терапии в течение примерно 12 лет. Все они испытывали только среднегодовую потерю прикрепления в 0,042 мм до 0,067 мм. Таким образом, «уровень укрепления » клинического прикрепления в 0,3 мм будет эквивалентен изменению 4-7 лет прогрессирования заболевания у вылеченного и «поддерживаемого» пациента.
Клинические исследования системной антибиотикотерапии у взрослых пациентов с пародонтитом с недавней активностью заболевания
Все антибиотики, используемые в пародонтальной терапии, ингибируют рост основных пародонтопатогенов P. gingivalis, C. rectus и Capnocytophaga.
Прямо противоположно ни один из них не особенно эффективен при ингибировании E. corrodens (лучше всего подходят миноциклин и доксициклин).
Миноциклин, по-видимому, является наиболее эффективным антибиотиком, который достигает уровней, которые должны быть полностью ингибирующими (активность антибиотика = 600%) для большинства патогенных патогенов, но также может ингибировать рост полезных видов. Амоксициллин проявляется почти так же эффективно, как и миноциклин. Тетрациклин, наиболее часто используемый антибиотик, но, по-видимому, является относительно плохим выбором для A. actinomycetemcomitans -инфекции, для которых он использовался чаще всего. Эритромицин, по-видимому, является плохим выбором для любой патогенной инфекции полости рта. Метронидазол уникально эффективен при лечении инфекций Selenomonassputigena и Peptostreptococcus и равен миноциклину при лечении инфекций Fusobacterium .
Пародонтальные инфекции могут включать различные патогены с различными антимикробной чувствительностью и резистентностью. В пародонтальных инфекциях тканевые барьеры и биопленки следует удалять механической очисткой до или с помощью антибиотиков. Состояние пародонтальной болезни и антимикробный режим необходимо тщательно определить, чтобы добиться успеха с помощью антимикробной терапии. Если антимикробные агенты против пародонтальной болезни не используются разумно, мы можем вскоре столкнуться с новым видом оральных микроорганизмов с повышенной защитой, которая обеспечит выживание вида, позволяет увеличить патогенность и передавать генетический материал, кодирующий повышенную вирулентность и устойчивость к антибиотикам.
Статья «Systemic antibiotic therapy in periodontics» Anoop Kapoor, Ranjan Malhotra, Deepak Grover переведена редакцией «Современная пародонтология»
источник