Спинальный эпидуральный абсцесс — редкое заболевание. Встречается с частотой 0,2-1,2 случая на 10000 поступлений в больницы. Редкость болезни, а также неспецифичность его клинических проявлений часто приводят к запоздалой диагностике.
Этиология и патогенез. Патогенез спинального эпидурального абсцесса несколько отличается от патогенеза внутричерепного абсцесса. Во-первых, имеется различие в возбудителях (преобладание стафилококков – 50-60% от всех случаев — и грамотрицательных бактерий при спинальном абсцессе). Во-вторых, твердая оболочка спинного мозга не прикреплена к костным структурам. Это позволяет инфекции интенсивно распространяться рострально и каудально. Спинальный эпидуральный абсцесс может быть острым и хроническим. Большинство острых случаев является результатом гематогенного заноса. Обычные источники инфекции: фурункулы, урогенная инфекция, заболевания зубов, хронические заболевания легких, септикопиемия. На их долю приходится 1/3 все острых случаев. Контактные абсцессы при заболеваниях прилежащих к позвоночнику тканей составляют еще 1/3 острых и половину хронических гнойников. Причины хронических абсцессов: остеомиелит позвоночника, фарингеальная инфекция, ретроперитонеальный абсцесс, абсцесс поясничной мышцы, пролежни, нагноение после хирургических вмешательств. Источники абсцесса у детей: кожная инфекция в промежности, эндокардит, фарингит, урогенная инфекция. Нередко причина заболевания остается невыясненной. Удивительно часто (20-30%) встречается предшествующая травма спины. Эпидуральный абсцесс чаще развивается в среднегрудном и нижнепоясничном отделах, где эпидуральное пространство лучше всего выражено. Как правило, он образуется в заднем пространстве, так как переднее относительно узко и аваскулярно. Реже встречающиеся передние абсцессы обычно развиваются при инфекции глотки, перитонзиллярных пространств, средостения, при остеомиелите позвоночника. Для спинального эпидурального абсцесса, как правило, нехарактерно разрушение твердой оболочки и развитие гнойного менингита, хотя в очень запущенных случаях при переднем гнойнике такой ход событий возможен.
Клиника. Выделяют четыре стадии развития острого абсцесса. Первая стадия характеризуется наличием боли в спине на уровне поражения, высокой лихорадкой, ознобом и местной ригидностью мышц. На второй стадии боль приобретает корешковый характер и сопровождается изменением рефлексов соответственно уровню поражения. Третья стадия наступает с появлением парезов, которым часто сопутствуют парестезии и расстройства тазовых функций. Затем быстро развиваются параличи, что соответствует переходу в четвертую стадию. Скорость прогрессирования по этим стадиям различна. В острых случаях паралич может развиться через несколько дней, в хронических — спустя несколько недель. Обычны оболочечные симптомы и головная боль. В зоне гнойника возможны гиперемия и отек. При хроническом эпидурите, как правило, нет лихорадки и общих явлений, очаговые знаки могут нарастать месяцами.
В крови отмечается высокий лейкоцитоз и увеличенная СОЭ. В половине случаев положительны посевы крови. Цереброспинальная жидкость стерильна, в ней обычно повышено содержание белка, преимущественно лимфоцитарный плеоцитоз по 200 клеток в 1мм. Содержание глюкозы нормальное. На рентгенограмме иногда имеются признаки остеомиелита. Высокоинформативны КТ и МРТ. При миелографии обнаруживают полный (80%) или частичный блок. Миелография помогает дифференцировать хронический эпидуральный абсцесс от арахноидита или эпидуральной опухоли.
Диагностика. Быстрое установление диагноза, несмотря на всю его необходимость, нередко по субъективным или объективным причинам непросто. Это объясняется относительной неспецичностью симптомов. Острый эпидуральный абсцесс часто принимают за менингит, околопочечный абсцесс, ревматоидный спондилит, банальную острую боль в спине, острый полиомиелит, подкожную гематому, гематомиелию, полиневрит, остеомиелит позвоночника, поперечный миелит. Дифференциация с поперечным миелитом наиболее трудна из-за схожести симптомов. При поперечном миелите неврологический дефект иногда развивается без боли в спине; о возможности развития абсцесса следует помнить при сопутствующем остеомиелите, недавней пиогенной инфекции, положительных посевах крови. Во всех сомнительных случаях при малейшем подозрении на эпидурит показана субокципитальная миелография с водорастворимым контрастом. При возможности надежную диагностику эпидурита обеспечат КТ и МРТ.
Хронический абсцесс обычно принимают за опухоль спинного мозга, остеомиелит позвоночника, болезнь Потта с компрессионным миелитом. Другие ошибочные диагнозы: протрузия диска, пиелонефрит, истерия, инфекция позвоночного диска, опоясывающий лишай. Нужные исследования обычно не выполняются, пока правильный диагноз не удается заподозрить.
Первые диагностические тесты — спондилограмма и миелография. На рентгеновском снимке можно увидеть признаки остеомиелита, но и нормальная картина не исключает диагноз абсцесса. Особого внимания заслуживает при подозрении на эпидурит поясничный прокол. Нет другой неврологической ситуации, где эта рутинная процедура была бы столь реальной угрозой развития гнойного менингита. Пункция эпидурального пространства с целью верификации абсцесса ушла в прошлое. Поясничная пункция показана только при эпидурите, располагающемся выше нижнегрудного уровня, одновременно проводят восходящую миелографию. Подозрение на эпидурит нижнегрудной или пояснично-крестцовой локализации — абсолютное противопоказание к поясничному проколу! Риск внесения гноя с иглой в подпаутинное пространство с развитием гнойного менингита при этой локализации исключительно велик. Показана субокципитальная пункция с введением водорастворимого контраста. При возможности — КТ или МРТ, заменяющие поясничную пункцию. Обязателен посев крови.
Лечение. Срочное хирургическое вмешательство с дренированием очага. При операции очаг занимает в среднем 4-5 сегментов. Возможны и тяжелые случаи с распространением гнойника едва ли не по всему длиннику эпидурального пространства.
В половине случаев возбудителем является золотистый стафилококк. Вторые по частоте возбудители — грамнегативные бактерии (эшерихии, псевдомонады). Антибиотик должен соответствовать высеянному возбудителю. Когда возбудитель неизвестен, терапия должна быть направлена и против пенициллинрезистентных стафилококков и иных возбудителей, которые могут быть заподозрены как причина заболевания. Антибиотики должны вводиться не менее 2-4 нед. При наличии остеомиелита лечение необходимо проводить как минимум б нед.
Прогноз. Без операции болезнь заканчивается смертью. Степень восстановления после операции зависит от длительности и тяжести болезни. Большинство больных после операции полностью выздоравливают. У других возможен остаточный дефект. Часто разрушение спинного мозга оказывается более значительным, чем этого можно было ожидать по степени компрессии, это связано с окклюзией сосудов в области абсцесса и спинальным инсультом.
Не нашли то, что искали? Воспользуйтесь поиском:
источник
• следует подозревать у пациента с болью в спине, ↑ Т и болезненностью позвоночника
• основные факторы риска: диабет, в/в злоупотребление наркотиками, хроническая почечная недостаточность, алкоголизм
• может приводить к значительной миелопатии, иногда с резким ухудшением
• часто наблюдаются лихорадка, профузное потоотделение, сильный озноб
• классический вариант с кожным фурункулом встречается только в ≈15% случаев
Хотя следующие временные классификации спинального эпидурального абсцесса (СЭА) используются, но корреляция с истинной продолжительностью инфекционного процесса является неопределенной:
• острый (продолжительность , чем при остром СЭА): грануляционная ткань в эпидуральном пространстве. Может существовать в течение нескольких мес
СЭА часто наблюдается на фоне остеомиелита позвоночника (в одной серии из 40 случаев СЭА остеомиелит позвоночника наблюдался во всех случаях переднего СЭА, в 85% окутывающего СЭА и ни в одном случае заднего СЭА) и межпозвокового дисцита.
Частота: в начале 70-х гг. частота была 0,2-1,2 случая на 10.000 госпитализаций/год. Средний возраст составил 57,5±16,6 лет.
Наиболее частая локализация, указываемая в литературе, — грудной уровень (≈50%), затем поясничный (35%), затем шейный (15%). В серии из 39 пациентов в 82% случаев была задняя локализация и в 18% — передняя.
Клинические проявления
Обычно проявляется очень сильной болью в позвоночнике, болезненностью при перкуссии. Наблюдаются радикулярные симптомы, к которым затем присоединяются симптомы дистального поражения СМ, часто начинающиеся с нарушений функций мочевого пузыря или кишечника, вздутия живота, мышечной слабости, которая затем может прогрессировать до пара- или тетраплегии. Средний срок от возникновения боли до появления корешковых симптомов – 3 д; от корешковых симптомов до возникновения мышечной слабости – 4,5 д; от слабости до параплегии – 24 ч.
Часто наблюдаются лихорадка, профузное потоотделение и сильный озноб. Фурункул удается обнаружить только в 15% случаев.
Может наблюдаться энцефалопатия средней или тяжелой степени, что может привести к задержке постановки диагноза. Могут быть положительные менингеальные симптомы.
В случае послеоперационного СЭА помимо местной боли может быть min кол-во симптомов (напр., отсутствие лейкоцитоза, лихорадки и т.д.).
Патофизиология нарушений функций спинного мозга
Хотя некоторые симптомы со стороны СМ могут быть обусловлены его прямой компрессией (включая случаи с коллапсом тела позвонка), обнаруживается она далеко не всегда. Предполагается, что определенную роль могут иметь сосудистые механизмы; описаны различные варианты артериальной и венозной патологии (в одной серии аутопсийных наблюдений было показано незначительное нарушение артериального кровоснабжения, но значительная венозная компрессия и тромбозы, тромбофлебит эпидуральных вен и самого СМ, с возможным распространением на мягкую мозговую оболочку.
Подозрение на СЭА должно возникать в случаях боли в спине, лихорадки и болезненности позвоночника.
1. менингит
2. острый поперечный миелит (паралич обычно наступает быстрее, данные рентгенологического обследования в норме)
3. выпадение межпозвонкового диска
4. опухоль СМ
5. послеоперационный СЭА может выглядеть как псевдоменингоцеле
• гематогенное распространение является наиболее частым (в 26-50% случаев) или непосредственно в эпидуральное пространство или в позвонок с последующим распространением в него. Упоминаемые источники:
A. кожная инфекция (наиболее частая причина): фурункул удается обнаружить в 15% случаев
B. парентеральная инфекция, особенно при в/в злоупотреблении наркотиками
C. бактериальный эндокардит
D. мочевая инфекция
E. дыхательная инфекция (включая отит среднего уха, синуситы и пневмонию)
F. зубной и глоточный абсцессы
• прямое распространение из:
A. пролежня
B. абсцесса поясничной мышцы: большая поясничная мышца прикрепляется к поперечным отросткам, телам позвонков (ТП) и межпозвонковым дискам, начиная с нижнего края тела Т12 и до верхней части тела L5
C. при проникающей травме, включая раны брюшной полости, раны шеи
D. глоточной инфекции
E. медиастенита
F. околопочечного абсцесса в результате пиелонефрита
• после операций на позвоночнике (у 3 из 8 таких пациентов уже до операции были установлены следующие источники инфицирования: периодонт, мочеиспускательный тракт и артерио-венозная фистула)
A. открытые операции: особенно поясничная дискэктомия (частота ≈0,67%)
B. закрытые вмешательства: напр., установка эпидурального катетера для спинальной эпидуральной анестезии, ЛП и т.д.
• в анамнезе часто имеется указание на недавнюю травму спины (вплоть до 30%)
• в некоторых сериях источник инфицирования не удалось установить вплоть до 50% случаев
В серии из 40 больных в 65% случаев имелись сопутствующие хронические заболевания, которые сопровождались нарушениями иммунитета. Среди них: сахарный диабет – 32%, в/в злоупотребление наркотиками – 18%, ХПН – 12%, алкоголизм – 10%, рак, повторные мочевые инфекции, болезнь Потта, положительная реакция на ВИЧ – у 1-2 больных.
Наиболее надежным способом определения возбудителей являются посевы, взятые во время операции. Эти посевы могут быть отрицательными (вероятно чаще в тех случаях, когда пациенты до операции получали АБ), но в этих случаях положительными могут быть посевы крови. Негативные результаты могут наблюдаться в 29-50% случаев.
1. золотистый стафилококк: наиболее частый возбудитель (высевается в >50% случаев), вероятно в результате того, что он чаще вызывает образование абсцессов, его распространенности, способности заражать как здоровых людей, так и лиц с нарушениями иммунитета (эти факты позволяют объяснить, почему во многих случаях СЭА возникает в результате первичного кожного очага)
2. аэробный и анаэробные стрептококки: второй наиболее частый вид возбудителя
8. хронические инфекции:
A. наиболее частой является ТБ. Хотя он стал менее распространенным в США, все равно на его долю приходится 25% случаев СЭА; обычно он сочетается с остеомиелитом позвоночника (болезнь Потта)
B. грибковая: криптококкоз, аспергиллез, бруцеллез
C. паразитарная: эхинококкоз
9. множественные возбудители в ≈10% случаев
10. анаэробы высеваются в ≈8% случаев
Развернутый анализ крови: при остром СЭА часто наблюдается лейкоцитоз (в среднем кол-во лейкоцитов =16.700/мм3), при хроническом кол-во лейкоцитов часто нормальное (в среднем =9.800/мм3).
СОЭ: в большинстве случаев повышена, обычно >30.
ЛП: производится с осторожностью в подозрительных случаях на уровне, отдаленном от клинически подозреваемого (для проведения миелографии может потребоваться пункция промежутка С1-2) с постоянной аспирацией для обнаружения гноя по мере продвижения к дуральному мешку (опасность распространения инфекции в САП). При обнаружении гноя следует сразу же остановиться, послать жидкость на посев и прекратить процедуру. Кол-во белка и лейкоцитов в ЦСЖ обычно повышены, кол-во глюкозы нормальное (показатель параменингеальной инфекции). В 5 из 19 случаев был получен рост тех же организмом, что и в абсцессе.
Посев крови: в некоторых случаях может быть полезен для определения возбудителя.
Анализы анэргии: (напр., при паротите или кандидамикозе) для оценки состояния иммунной системы
Краниограммы: обычно нормальные, за исключением случаев остеомиелита прилежащих ТП (чаще при инфекционных процессах, локализующихся впереди ТМО); проверьте есть ли литические очаги, деминерализация, фестончатость костных пластинок (для появления этих изменений может потребоваться 4-6 нед).
МРТ: метод выбора. Исключает необходимость ЛП, чувствительность соответствует чувствительности КТ-миелографии, позволяет дифференцировать другие состояния (особенно поперечный миелит и инфаркт СМ) лучше, чем КТ-миелография. Типичные признаки: в режиме Т1 → гипо- или изотензивное эпидуральное объемное образование; остеомиелит позвоночника проявляется в виде понижения сигнала в кости; в режиме Т2 → эпидуральное объемное образование высокой интенсивности, которое часто накапливает КВ (гадолиниум). Могут наблюдаться 3 типа КУ: 1)плотное, гомогенное, 2)негомогенное с разбросанными областями, не накапливающими КВ, 3)тонкий ободок периферического КУ. В острой фазе, когда абсцесс состоит из одного гноя с небольшим кол-вом грануляционной ткани, КУ может быть min. Остеомиелит позвоночника дает повышение сигнала в кости, сопутствующий дисцит вызывает ↑ сигнала в диске и исчезновение внутриядерного расщепления. При бесконтрасной МРТ в некоторых случаях можно не обнаружить СЭА, использование гадолиниума несколько повышает чувствительность исследования.
Миелография: обычно выявляются признаки экстрадуральной компрессии (напр., «вид кисточки» в случае полного блока). В случае полного блока для определения его верхнего уровня требуется С1-2 пункция (если только на КТ после миелографии не будет видно КВ выше очага поражения). См. предосторожности, касающиеся проведения ЛП.
КТ: есть описание обнаружения газа внутри позвоночного канала на обычных КТ. КТ может быть особенно информативна после миелографии.
В тех случаях, когда неврологические нарушения отсутствуют до появления деформации позвоночника возможно проведение иммобилизации (при инфекции в шейном отделе с помощью головного обруча и грудного корсета, для остальных отделов с помошью грудного-поясничного-крестцового корсета) и АБ. Некоторые авторы рекомендуют оперативную эвакуацию очага в сочетании с АБ в качестве метода выбора на основании сообщений о том, что в случаях только АБ лечения (даже соответствующими имеющейся у больного флоре АБ) возможно развитие быстрого и необратимого ухудшения у пациентов, не имевших неврологического дефицита. Рекомендуется применять консервативное лечение у следующих больных:
1. с повышенными факторами риска для хирургического лечения
2. при большой продолжительности зоны поражения спинномозгового канала
3. полным параличом >3 д
4. при отсутствии выраженного неврологического дефицита (NB: это положение спорно)
Целями являются установление диагноза и возбудителя, удаление гноя и грануляционной ткани, при необходимости костная стабилизация. В большинстве случаев СЭА располагается кзади от дурального мешка, поэтому для доступа к нему требуется обширная ламинэктомия. В случае заднего расположения СЭА и при отсутствии признаков остеомиелита позвоночника после проведения простой ламинэктомии и АБ терапии нестабильности обычно не наступает. Рану закрывают ограниченными проволочными швами. В тех случаях, когда имелась только грануляционная ткань и не было гноя, оставление дренажа не требуется. При повторной инфекции может потребоваться реоперация и установка приточно-отточной промывной системы.
У пациентов с остеомиелитом позвоночника после проведения ламинэктомии может развиться нестабильность позвоночника, особенно если имеется существенная деструкция кости. Поэтому при передних СЭА, который обычно наблюдается на фоне остеомиелита (болезнь Потта), всегда, когда это возможно, показан задне-боковой внеполостной доступ (у ослабленных больных следует избегать трансабдоминального или трансторакального доступов) с удалением нежизнеспособной кости с последующей задней инструментальной фиксацией. В случае болезни Потта в качестве распорки можно использовать трансплантат, взятый у пациента (ребро или мальберцовая кость), с небольшим риском его инфицирования.
Если возбудитель и источник СЭА неизвестны, то наиболее вероятен золотистый стафилококк. Эмпирические АБ:
1. цефалоспорин-3, напр., цефотаксим (Claforan®)
И
2. ванкомицин: пока не будет исключен МУЗС. После его исключения можно перейти на синтетический пенициллин (напр., нафциллин или оксациллин)
И
3. рифамипин РО
АБ меняют в зависимости от результатов посевов или обнаружения источника [напр., у лиц, злоупотребляющих в/в наркотиками, чаще встречаются Грам(-) организмы].
При СЭА после 3-4 нед лечения в/в АБ обычно достаточно 4 нед курса РО АБ. При сопутствующем остеомиелите позвоночника в/в курс должен составлять 6-8 нед (хотя некоторые авторы отмечают, что гистологически остеомиелит имеется практически во всех случаях, даже если его не удается обнаружить рентгенологически; поэтому лечение в обеих группах должно быть одинаковым). Повторные анализы СОЭ также могут влиять на продолжительность лечения (при отсутствии снижения СОЭ следует предполагать повторную инфекцию). Во время лечения АБ требуется иммобилизация в течение по крайней мере 6 нед.
Летальные исходы наблюдаются в 18-23% случаев (возможно чаще у пожилых больных и с парализацией до операции). Улучшение выраженного неврологического дефицита наблюдается редко, даже если операция производится в течение 6-12 ч после его возникновения. Обратное развитие парализации сакральных сегментов СМ, существующей более нескольких часов, наблюдается редко (исключение: 50% восстановление при болезни Потта). Смертность обычно обусловлена первичным очагом инфекции или осложнениями параплегии (напр., ТЭЛА).
источник
Абсцесс головного или спинного мозга — ограниченное скопление гноя в полости черепа или позвоночного канала. В зависимости от локализации абсцессы могут быть внутримозговыми (скопление гноя в веществе мозга) , субдуральными (расположенными под твёрдой мозговой оболочкой) либо эпидуральными (локализованными над твёрдой мозговой оболочкой) . Абсцессы мозга встречают с частотой около 0,7 на 100 000 населения в год.
Основные пути проникновения инфекции в полость черепа и позвоночного канала следующие:
• гематогенный;
• открытая проникающая ЧМТ или спинальная травма;
• гнойно-воспалительные процессы в придаточных пазухах носа;
• инфицирование раны после нейрохирургических вмешательств.
Условия формирования абсцесса при проникновении инфекции — характер возбудителя (вирулентность патогена) и снижение иммунитета больного. В развитых странах наиболее типичны гематогенные абсцессы. В развивающихся странах абсцессы мозга чаще всего формируются на фоне хронических воспалительных процессов в прилежащих тканях, что связано с неадекватным лечением последних.
Приблизительно в 25% случаев установить источник, приведший к формированию абсцесса мозга, не представляется возможным.
При гематогенных абсцессах источником бактериальных эмболов наиболее часто бывают воспалительные процессы в лёгких (абсцесс лёгкого, бронхоэктатическая болезнь, эмпиема плевры, хроническая пневмония) . Бактериальный эмбол представляет собой фрагмент инфицированного тромба из сосуда на периферии воспалительного очага. Тромб попадает в большой круг кровообращения и током крови заносится в сосуды мозга, где фиксируется в сосудах небольшого диаметра (артериоле, прекапилляре или капилляре). Меньшее значение в патогенезе абсцессов имеют острый бактериальный эндокардит, хронический бактериальный эндокардит, сепсис и инфекции жкт.
Причиной абсцесса мозга у детей часто становятся «синие» пор оки сердца, в первую очередь тетрада Фалло, а также лёгочные артерио-венозные шунты (50% из них ассоциировано с синдромом Рандю-Ослера — множественными наследственными телеангиэктазиями) . Риск развития абсцесса мозга у таких больных составляет около 6%.
При гнойно-воспалительных процесс ах в придаточных пазухах носа, среднем и внутреннем ухе распространение инфекции может происходить либо ретроградно по синусам твёрдой мозговой оболочки и мозговым венам, либо при непосредственном проникновении инфекции через твёрдую мозговую оболочку (при этом сначала формируется отграниченный очаг воспаления в мозговых оболочках и затем — в прилежащем отделе мозга) . Реже встречают одонтогенные абсцессы.
При проникающей и открытой черепно-мозговой травме абсцессы мозга могут развиваться вследствие прямого попадания инфекции в полость черепа. В мирное время доля таких абсцессов не превышает 15%. В условиях боевых действий она значительно возрастает (огнестрельные и минно-взрывные ранения).
Абсцессы мозга могут формироваться также на фоне интракраниальных инфекционных осложнений после нейрохирургических вмешательств (менингиты, вентрикулиты) . Как правило, они возникают у тяжёлых, ослабленных больных.
Выделить возбудитель инфекции и з содержимого абсцесса мозга удаётся далеко не всегда. Приблизительно в 25% случаев посевы содержимого абсцесса оказываются стерильными. Среди выделенных возбудителей гематогенных абсцессов преобладают стрептококки (аэробные и анаэробные), часто в ассоциации с бактероидами (Bacteroides spp.) . При гематогенных абсцессах вследствие абсцесса лёгкого часто встречают Enterobacteriaceae (в частности, Proteus vulgaris). Эти же возбудители характерны для отогенных абсцессов.
При проникающей ЧМТ в патогенезе абсцессов мозга преобладают стафилококки (в первую очередь, St. aureus) . Обнаруживают также возбудители рода Enterobacteriaceae.
У больных с различными иммунодефицитными состояниями (приём иммуносупрессоров после трансплантации органов, БИЧ-инфекция) среди патогенов преобладают Aspergillus fumigatus.
Формирование абсцесса мозга проходит несколько этапов. Первоначально развивается ограниченное воспаление мозговой ткани — энцефалит («ранний церебрит», по современной англоязычной терминологии). Длительность этой стадии составляет до 3 сут. На этом этапе воспалительный процесс обратим и может разрешиться либо спонтанно, либо на фоне антибактериальной терапии.
При недостаточности защитных механизмов и в случае неадекватного лечения воспалительный процесс прогрессирует, и к 4-9-м сут В его центре возникает полость, заполненная гноем, способная увеличиваться. К 1 0-13-м сут вокруг гнойного очага начинает формироваться защитная соединительнотканная капсула, препятствующая дальнейшему распространению гнойного процесса. К началу 3-й нед капсула становится более плотной, вокруг неё формируется зона глиоза.
Дальнейшее течение абсцесса мозга обусловлено вирулентностью флоры, реактивностью организма и адекватностью лечебно-диагностических мероприятий.
Иногда абсцесс подвергается обратному развитию, но чаще происходит либо увеличение его внутреннего объёма, либо формирование новых воспалительных очагов по периферии капсулы.
Абсцессы мозга могут быть одиночными и множественными (рис. 31-8) . Абсцессы в субдуральном или эпидуральном пространстве формируются реже, чем внутримозговые. Такие абсцессы обычно бывают вызваны местным распространением инфекции из прилежащих гнойных очагов в околоносовых придаточных пазухах, а также возникают при открытой ЧМТ, остеомиелите костей черепа.
Как и при внутримозговых абсцессах, при субдуральных и эпидуральных абсцессах может формироваться плотная соединительнотканная капсула (рис. 31-9). Если этого не происходит, развивается разлитое гнойное воспаление в соответствующем пространстве. Такой процесс, как и в общей хирургии, называют субдуральной или эпидуральной эмпиемоЙ.
Клиническая картина при абсцессах головного и спинного мозга соответствует клинической картине объёмного образования. Патогномоничных симптомов абсцесса мозга не существует. Как и при других объёмных образованиях, клинические симптомы могут варьировать в широких пределах — от головной боли до развития тяжёлых общемозговых симптомов с угнетением сознания и выраженных очаговых симптомов поражения мозга. Первым проявлением болезни может стать эпилептиформный припадок. При субдуральных абсцессах и эмпиеме чаще присутствуют менингеальные симптомы. Эпидуральные абсцессы практически всегда ассоциируются с остеомиелитом костей черепа. Типично прогредиентное нарастание симптоматики. В части случаев оно может быть очень быстрым.
Рис. 31 -8. Абсцесс правой лобной доли ; кт без контрастного усиления (а). Грибковый многокамерный абсцесс правой теменно-затылочной области; МРТ, Т1 -взвешенное изображение с контрастным усилением (б).
Рис. 31 -9. Абсцесс правой задне-лобнотеменной области, М РТ: а — Т 1 — взвешенное изображение; б — Т 1 — взвешенное изображение с контрастным усилением; в — Т2-взвешенное изображение.
При постановке диагноза большое значение имеет тщательный сбор анамнеза.
Появление и нарастание неврологических симптомов у больного с диагностированным воспалительным процессом — повод для проведения нейровизуализационного обследования.
Компьютерная томография. Точность диагноза абсцесса мозга при КТ зависит от стадии развития процесса. При инкапсулированных абсцессах точность диагноза приближается к 100%. Абсцесс имеет вид округлого объёмного образования С чёткими, ровными, тонкими контурами повышенной плотности (фиброзная капсула) и зоной пониженной плотности в центре (гной, рис. 31-10) . В части случаев в полости абсцесса определяют чёткий уровень жидкости. По периферии капсулы видна зона отёка. При введении контрастного вещества оно накапливается в виде тонкого кольца, соответствующего фиброзной капсуле с небольшой прилежащей зоной глиоза. При повторении КТ через 30-40 мин накопление контрастного вещества не определяют.
Диагностика в более ранних стадиях менее надёжна. В стадии раннего энцефалита (1-е-3-и сут) при КТ выявляют зону сниженной плотности, часто неправильной формы. При введении контрастного вещества его накопление происходит неравномерно, преимущественно в периферических отделах очага, но иногда и в его центре.
Рис. 31 — 10. Абсцесс левой лобной доли, неправильная форма затрудняет дифференциальную диагностику с опухолью; МРТ: а — Т1 -взвешенное изображение; б — режим диффузии, выявлен харак· терный для абсцесса высокий МР-сигнал; в — протонная МР-спектроскопия, выявлены характерные для абсцесса пики метаболитов — ацетата (Ас), лактата (Lac) и аминокислот (АА).
В стадии позднего энцефалита (4-9-е сут) контуры очага становятся более ровными и округлыми, а накопление контрастного вещества по периферии очага — более интенсивным и равномерным. Рентгеновская плотность центральной зоны очага непосредственно после введения контрастного вещества не изменяется, но при повторной КТ через 30-40 мин можно обнаружить диффузию контраста в центр очага, а также сохранение его в периферической зоне, что не характерно для опухолей.
При анализе компьютерной томограммы следует иметь в виду, что глюкокортикоиды, часто используемые в лечении, значительно уменьшают накопление контрастного вещества в энцефалитическом очаге.
Магнитно-резонансная томография. МРТ служит более точным методом диагностики абсцессов, чем КТ. Энцефалитический очаг выглядит гипоинтенсивным на T l — и гиперинтенсивным — на Т2-взвешенных изображениях.
Инкапсулированный абсцесс на ТI -взвешенных изображениях выглядит как зона пониженнога сигнала в центре и на периферии, в зоне отёка, с кольцевидной зоной умеренно гиперинтенсивного сигнала между ними, соответствующей капсуле абсцесса. На Т2-взвешенных изображениях центральная зона абсцесса бывает изо- или гипоинтенсивной, периферическая зона отёка — гиперинтенсивной, между этими зонами прослеживается чётко очерченная капсула.
Дифференциальную диагностику абсцесса следует проводить с первичными глиальными и метастатическими опухолями мозга. При сомнении в диагнозе и необходимости дифференцировки абсцесса исключительную роль играет МР-спектроскопия (дифференциальная диагностика основана на различном содержании лактата и аминокислот в абсцессах и опухолях) .
При подозрении н а абсцесс мозга необходимо тщательно обследовать больного, чтобы выявить все возможные очаги воспаления, способные стать источником внутричерепного инфицирования.
Другие способы диагностики и дифференциальной диагностики абсцесса мозга малоинформативны. Лихорадка, увеличение СОЭ, лейкоцитоз, повышение содержания С-реактивного белка в крови бывают при любых воспалительных процессах, в том числе при внечерепных. Посевы крови при абсцессах мозга обычно бывают стерильными. Люмбальную пункцию в диагностике внутричерепных абсцессов сегодня не применяют в связи с низкой информативностью (в большинстве случаев воспалительный процесс в мозге бывает отграниченным и не сопровождается менингитом) и опасностью дислокации мозга.
Лечение абсцессов мозга может быть консервативным и хирургическим. Способ лечения зависит в первую очередь от стадии развития абсцесса, его размера и локализации.
В стадии формирования энцефалитического очага (длительность анамнеза — до 2 нед), а также при небольших « 3 см в диаметре) абсцессах показано консервативное лечение. Обычной тактикой становится эмпирическая антибактериальная терапия. Некоторые хирурги предпочитают проведение стереотаксической биопсии для окончательной верификации диагноза и выделения возбудителя.
Абсолютными показаниями к хирургическому вмешательству считают абсцессы, вызывающие повышение внутричерепного давления и дислокацию мозга, а также расположенные около желудочковой системы (прорыв гноя в желудочковую систему часто становится фатальным) . При травматических абсцессах, расположенных около инородного тела, хирургическое вмешательство также становится методом выбора, поскольку такой воспалительный процесс невозможно вылечить консервативно. Показанием к операции считают также грибковые абсцессы, хотя прогноз в этой ситуации бывает крайне неблагоприятным независимо от метода лечения.
При абсцессах, расположенных в жизненно важных и глубинных структурах (стволе мозга, зрительном бугре, подкорковых ядрах), прямое хирургическое вмешательство противопоказано. Б таких случаях методом выбора может быть стереотаксический метод — пункция абсцесса и его опорожнение с однократным или повторным (через установленный на несколько суток катетер) промыванием полости и введением антибактериальных препаратов.
Тяжёлые соматические заболевания не считаются абсолютным противопоказанием к хирургическому вмешательству, так как стереотаксическую операцию можно выполнить под местной анестезией.
Больным в крайне тяжёлом состоянии (терминальной коме) любое хирургическое вмешательство противопоказано.
Эмпирическая (до получения результата посева или при невозможности идентификации возбудителя) антибактериальная терапия должна покрывать максимально возможный спектр возбудителей. Поэтому используют следующий алгоритм.
• Больным без ЧМТ или нейрохирургического вмешательства в анамнезе назначают одновременно следующие препараты:
— ванкомицин (взрослым — 1 г 2 раза в сут в/в; детям — 15 мг/кг 3 раза в сут);
— цефалоспорин III поколения (например, цефотаксим);
— метронидазол (взрослым — 30 мг/кг В сут на 2-4 введения; детям — 10 мг/кг 3 раза в сут) .
• Больным с посттравматическими абсцессами метронидазол заменяют рифампицином в дозе 9 мг на 1 кг массы тела 1 раз в сут внутрь.
• у больных с иммунодефицитом (кроме БИЧ) наиболее вероятным возбудителем абсцесса мозга бывает Cryptococcus neoformans, реже Aspergillus spp. или Candida spp. Б связи с этим им назначают амфотерицин Б в дозе 0,5-1,0 мг/кг в сут внутривенно или липосомальный амфотерицин Б — 3 мг /кг в сут внутривенно с постепенным повышением дозы до 15 мг /кг в сут. Б случае исчезновения абсцесса по данным нейровизуализационных методов назначают флуконазол по 400 мг/сут внутрь до 10 нед, а затем пациентов переводят на постоянную поддерживающую дозу 200 мг/сут.
• у больных с БИЧ наиболее вероятным возбудителем абсцесса мозга является Toxoplasma gondii, поэтому в эмпирическом лечении таких больных применяют сульфадиазин с пириметамином.
Если получена культура возбудителя, лечение изменяют с учётом антибиотикограммы. При стерильном посеве продолжают эмпирическую антибактериальную терапию.
Продолжительность интенсивной антибактериальной терапии — не менее 6 нед, после чего целесообразно назначить пероральные антибактериальные препараты ещё на 6 нед.
Применение глюкокортикоидов при водит к уменьшению выраженности и более быстрому обратному развитию фиброзной капсулы абсцесса, что хорошо при адекватной антибактериальной терапии, но в противном случае может вызвать распространение воспалительного процесса за пределы первичного очага.
Поэтому назначение глюкокортикоидов оправдано лишь при нарастающем отёке и дислокации мозга, в остальных случаях вопрос требует обсуждения.
Основным методом лечения большинства внутримозговых абсцессов мозга в настоящее время служит простое или приточно-отточное дренирование. Суть метода заключается в установке в полость абсцесса катетера, через который осуществляют эвакуацию гноя и введение антибактериальных препаратов. При возможности в полость на несколько суток устанавливают второй катетер меньшего диаметра, через него проводят инфузию раствора для промывания (обычно используют 0,9% раствор натрия хлорида, эффективность добавления к нему антибактериальных препаратов не доказана) . Дренирование абсцесса подразумевает обязательную антибактериальную терапию (сначала эмпирическую, затем — с учётом чувствительности выделенного патогена к антибиотикам).
Альтернативным методом служит стереотаксическая аспирация содержимого абсцесса без установки дренажа. Достоинство метода — меньший риск вторичного инфицирования и более снисходительные требования к квалификации медицинского персонала (контроль за функционированием приточно-отточной системы требует специальных знаний и пристального внимания). Однако при использовании этого метода приблизительно в 70% случаев возникает необходимость в повторных аспирациях.
При множественных абсцессах в первую очередь дренируют очаг, наиболее значимый в клинической картине или наиболее опасный в отношении осложнений (дислокации мозга, прорыва гноя в желудочковую систему и т.д.).
При субдуральных абсцессах или эмпllеме применяют дренирование, приточноотточную систему не используют.
Операции тотального удаления абсцесса вместе с капсулой, без вскрытия последней, в настоящее время не применяют в связи с высокой травматичностью. Исключения составляют грибковые и нокардиозные (вызванные Nocardia asteroides, реже Nocardia brasiliensis) абcuессы, развивающиеся у иммунодефицитных больных. Радикальное удаление абсцессов в таких ситуациях несколько улучшает выживаемость.
Хирургическое лечение эпидуральных абсцессов такое же, как при остеомиелите.
Прогноз при абсцессах мозга заВИСI1Т от многих факторов. Большое значение имеет возможность определять возбудитель и его чувствительность к антибактериальным препаратам, что позволяет про водить направленную патогенетическую терапию. Важную роль в исходе заболевания играют реактивность организма, количество абсцессов, своевременность и адекватность лечебных мероприятий. Летальность при абсцессах мозга составляет около 10%, инвалидизация — около 50%. Почти У трети выживших больных развивается эпилептический синдром.
Субдуральные эмпиемы прогностически менее благоприятны, чем абсцессы мозга, поскольку отсутствие границ гнойного очага свидетельствует либо о высокой вирулентности возбудителя, либо о крайне низкой сопротивляемости больного. Летальность при субдуральных эмпиемах составляет около 50%. При грибковых эмпиемах у иммунодефицитных больных она приближается к 100%.
Эпидуральные абсцессы и эмпиемы обычно имеют благоприятный прогноз. Инфекция практически никогда не проникает через неповреждённую твёрдую мозговую оболочку, и санация остеомиелитического очага позволяет ликвидировать эпидуральную эмпиему.
источник
Спинальный эпидуральный абсцесс (G06.1) — это гнойное очаговое воспаление эпидуральной клетчатки в области спинного мозга.
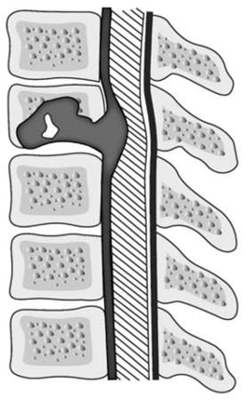
Возбудители инфекции: чаще — золотистый стафилококк, реже — грамотрицательные палочки, стрептококки, анаэробные микроорганизмы и грибы. Источники инфекции: фурункулы, урогенная инфекция, хронические заболевания легких, заболевания зубов, остеомиелит позвоночника, ретроперитонеальный абсцесс, абсцесс большой поясничной мышцы, пролежни.
Факторы риска: сахарный диабет, алкоголизм, употребление наркотиков, хроническая почечная недостаточность. Предрасполагающими факторами являются предшествующая травма спины, хирургические операции на спинном мозге.
Чаще развивается в среднегрудном (50%) и нижнепоясничном (35%) отделах позвоночника.
Первые симптомы — интенсивная боль в спине на уровне поражения, высокая лихорадка, озноб (на протяжении нескольких дней, недель). Отмечается разлитая интенсивная боль в области поражения с распространением в ноги, возникают чувства онемения или покалывания в течение 3–5 дней (80%). В последующем постепенно нарастает слабость в ногах (60%). Появлению слабости в конечностях, отсутствию движений в них часто сопутствуют онемение и расстройство тазовых функций (50%).
При объективном исследовании выявляют изменения:
- Общеинфекционный, общемозговой и менингеальные синдромы.
- В результате исследования чувствительности — болезненность при перкуссии остистых отростков позвоночника на уровне поражения и при пальпации соответствующих паравертебральных точек, симптомы натяжения (Нери, Ласега), гипестезия или анестезия по сегментарному типу, проводниковые нарушения чувствительности.
- Парез нижних конечностей до развития плегии, тазовые дисфункции.
- Локальные изменения в виде гиперемии и отека в области патологического образования.
-
Общий анализ крови: высокий лейкоцитоз, увеличенная скорость оседания эритроцитов.
- Посев крови (определение возбудителя).
- Исследование ликвора: цереброспинальная жидкость стерильна, белково-клеточная диссоциация, лимфоцитарный плеоцитоз до 200 клеток в 1 мкл, содержание глюкозы нормальное.
- Рентгенография позвоночника (признаки остеомиелита позвоночника).
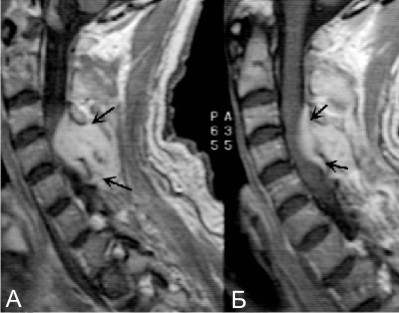
- Магнитно-резонансная томография спинного мозга (визуализация образования).
- Миелография (признаки экстрадуральной компрессии — полный или частичный блок).
- Компьютерная томография (обнаружение газа внутри позвоночного канала, особенно информативна после миелографии).
- Острый поперечный миелит.
- Вторичный гнойный лептоменингит.
- Острое нарушение спинального кровообращения.
- Кистозный спинальный арахноидит.
Лечение назначается только после подтверждения диагноза врачом-специалистом. Необходимо срочное хирургическое вмешательство с дренированием очага инфекции, проводится антибактериальная терапия.
Имеются противопоказания. Необходима консультация специалиста.
- Ванкомицин (антибиотик группы гликопептидов). Режим дозирования: взрослым в/в 1 г 2 раза в сутки; детям — 15 мг/кг 3 раза в сутки. Длительность курса лечения определяется индивидуально.
- Цефтриаксон (цефалоспориновый антибиотик III поколения). Режим дозирования: для взрослых и детей старше 12 лет доза составляет 1-2 г 1 раз/сут. или по 0,5-1 г каждые 12 ч. Максимальная суточная доза — 4 г. Препарат вводят в/м и в/в (струйно или капельно). Длительность курса лечения определяется индивидуально.
- Рифампицин (антибактериальное средство широкого спектра). Режим дозирования: внутрь, за 30-60 мин. до еды, 900-1200 мг/сут. в 2 приема, после исчезновения симптомов лечение продолжают еще в течение 2-3 дней.
Рекомендуется консультация нейрохирурга, магнитно-резонансная томография спинного мозга.
источник
Спинальный эпидуральный абсцесс — ограниченное гнойное воспаление эпидурального спинномозгового пространства. Проявляется острой болью в спине, трансформирующейся в корешковый синдром, появлением и прогрессированием парезов, тазовых расстройств и чувствительных нарушений в соответствии с топикой абсцесса. В ходе диагностики оптимальным является проведение МРТ спинного мозга, при отсутствии такой возможности — спинальной пункции и миелографии. Лечение состоит в как можно более ранней оперативной декомпрессии спинного мозга с дренированием абсцесса, проводимой на фоне массивной антибиотикотерапии.
Спинальный эпидуральный абсцесс — локальный гнойно-воспалительный процесс, возникающий в эпидуральном пространстве. Последнее представляет собой щель, располагающуюся между твердой (дуральной) спинальной мозговой оболочкой и стенками позвоночного канала. Эпидуральное пространство заполнено рыхлой клетчаткой и венозными сплетениями. По нему гнойное воспаление может распространяться в церебральном или каудальном направлении, занимая пространство, соответствующее нескольким позвоночным сегментам.
В литературе по неврологии спинальный эпидуральный абсцесс можно встретить под синонимичным названием «ограниченный гнойный эпидурит». Частота встречаемости эпидурального абсцесса спинного мозга в среднем составляет 1 случай на 10 тыс. госпитализаций. Наиболее часто, примерно в половине случаев, наблюдается абсцесс среднегрудного отдела позвоночника. Около 35% приходится на эпидуральные абсцессы поясничного отдела, 15% — на шейный отдел. Заболевают преимущественно люди в возрасте от 40 до 75 лет с пониженной сопротивляемостью иммунной системы. Современная тенденция к росту заболеваемости, по всей видимости, обусловлена увеличением численности пожилого населения и количества лиц с пониженным иммунитетом.
Спинальный эпидуральный абсцесс является следствием попадания в субдуральное пространство инфекции. В качестве инфекционных агентов могут выступать стафилококки (50-60% случаев), стрептококковая инфекция, анаэробные микроорганизмы, специфические возбудители (например, палочка туберкулеза), грибы. Занос инфекции в эпидуральное пространство возможен гемато- и лимфогенным способом из существующих в организме удаленных инфекционных очагов, таких как фурункулез, заглоточный абсцесс, нагноившаяся киста средостения, инфекционный эндокардит, пиелонефрит, гнойный цистит, периодонтит, гнойный отит, пневмония и пр.
Спинальный эпидуральный абсцесс может возникнуть в результате распространения гнойного воспаления из рядом расположенных структур при остеомиелите или туберкулезе позвоночника, абсцессе поясничной мышцы, пролежнях, ретроперитонеальном абсцессе. Примерно до 30 % случаев эпидурального абсцедирования связаны с проникновением инфекции вследствие травмы позвоночника, например, перелома позвонка с вклинением его частей или осколков в клетчатку эпидурального пространства. Возможно образование посттравматической гематомы с ее последующим нагноением. В редких случаях спинальный эпидуральный абсцесс формируется как осложнение эпидуральной анестезии, люмбальных пункций или хирургических операций на позвоночнике.
Немаловажное значение в развитии абсцедирования имеет иммунокомпрометированное состояние организма больного, при котором проникающие в субдуральное пространство микроорганизмы не получают достойного отпора иммунной системы. Причинами снижения иммунного ответа могут быть пожилой возраст, хронический алкоголизм, наркомания, ВИЧ-инфекция, сахарный диабет и др.
Формирование абсцесса в спинальном эпидуральном пространстве сопровождается развитием ликвороциркуляторного блока и нарастающей компрессией спинного мозга. В отсутствие быстрой ликвидации абсцесса в спинном мозге на фоне сдавления происходят необратимые дегенеративные процессы, влекущие за собой формирование стойкого неврологического дефицита.
Спинальный эпидуральный абсцесс манифестирует соответствующей его локализации разлитой болью в спине, подъемом температуры тела до высоких цифр, ознобами. Отмечается локальная ригидность позвоночных мышц, болезненность перкуссии остистых отростков, положительные симптомы натяжения. Затем наступает 2-я стадия болезни — боль трансформируется в корешковый синдром, что сопровождается снижением сухожильных рефлексов в соответствии с уровнем поражения. На 3-ей стадии возникают парезы и тазовые нарушения, свидетельствующие о компрессии проводящих спинальных путей, зачастую наблюдаются парестезии. Переход в 4-ую стадию сопровождается быстрым нарастанием парезов вплоть до полных параличей, проводниковыми нарушениями чувствительности.
Неврологическая картина неспецифична. Периферические вялые параличи отмечаются на уровне локализации субдурального абсцесса, а ниже этого уровня определяются проводниковые расстройства: центральные параличи и сенсорные нарушения. В проекции абсцесса на поверхности спины может наблюдаться гиперемия кожи и отечность подлежащих тканей.
Скорость развития клиники в соответствии с указанными выше стадиями вариативна. Острый субдуральный абсцесс характеризуется формированием параличей спустя несколько суток от дебюта болезни, хронический — через 2-3 недели. При хроническом абсцессе высокая лихорадка зачастую отсутствует, чаще наблюдается субфебрилитет. Трансформация острого абсцесса в хронический сопровождается снижением температуры тела и некоторой стабилизацией клиники, иногда уменьшением выраженности симптомов спинальной компрессии. Течение хронического абсцесса представляет собой смену обострений и затуханий клинических симптомов.
Неспецифичность симптомов и данных неврологического статуса не позволяют неврологу и нейрохирургу достоверно диагностировать спинальный субдуральный абсцесс. Заподозрить его можно при наличии инфекционного процесса в области позвоночного столба или удаленного очага гнойной инфекции. При остром процессе возникают соответствующие изменения в клиническом анализе крови (ускорение СОЭ, лейкоцитоз), хронический абсцесс характеризуется слабой выраженностью островоспалительных изменений крови. Данные о характере возбудителя может дать бакпосев крови.
Проведение рентгенографии позвоночника помогает выявить или исключить остеомиелит и туберкулезный спондилит. Люмбальная пункция возможна только при расположении абсцесса выше нижнегрудных сегментов. Поражение ниже грудного уровня является противопоказанием для ее проведения, поскольку существует опасность внесения пункционной иглой инфекции в арахноидальное пространство с развитием гнойного менингита. В таких случаях возможна субокципитальная пункция.
Люмбальную или субокципитальную пункцию совмещают с проведением соответственно восходящей или нисходящей миелографии. Последняя выявляет экстрадуральное (частичное или полное) сдавление спинного мозга, однако малоинформативна в отношении дифференциации вызвавшего компрессию объемного образования, т. е. не может различить абсцесс, гематому и опухоль спинного мозга. Наиболее надежным и безопасным способом диагностировать спинальный субдуральный абсцесс является проведение КТ, оптимально — МРТ позвоночника.
Спинальный эпидуральный абсцесс является показанием к срочному хирургическому вмешательству. Проводится декомпрессия спинного мозга путем ламинэктомии и дренирование субдурального пространства. При наличии остеомиелита в ходе операции производится удаление нежизнеспособных костных тканей с последующей фиксацией позвоночника. Своевременно проведенная операция предотвращает развитие парезов или уменьшает их степень.
Антибиотикотерапия начинается эмпирически (до получения результатов бакпосева) еще на стадии предоперационной подготовки с парентерального введения препаратов широкого спектра (амоксициллина, рифампицина, ванкомицина, цефотаксима), их комбинации или комбинированных антибактериальных препаратов (например, амоксициллин+клавулановая кислота). Затем переходят на пероральный прием антибиотиков. Продолжительность лечения антибиотиками составляет от 1 до 2 мес. При диагностике туберкулеза проводится консультация фтизиатра и назначается противотуберкулезная терапия.
От 18% до 23% случаев субдурального абсцесса спинного мозга заканчиваются смертельным исходом в результате сепсиса, ТЭЛА и др. осложнений. Наиболее неблагоприятный прогноз у пожилых пациентов при осуществлении хирургического вмешательства после развития параличей. При ранней диагностике и проведении оперативного лечения до возникновения парезов прогноз благоприятный. После операции отмечается остановка прогрессирования неврологических нарушений. Однако при выраженном характере неврологического дефицита его регресс не происходит даже в случаях, когда оперативное лечение проводилось в первые 6-12 ч его появления.
источник

Это заболевание считается довольно редким в наши дни, но никто не застрахован от его развития.
Современные достижения медицины (в виде антибиотиков и нейрохирургического лечения) могут избавить от абсцесса и предотвратить появление осложнений.
Но это возможно только при своевременном обращении к специалисту.
Поэтому стоит повнимательнее рассмотреть симптоматику патологии, причины развития заболевания, а также способы избавления от него.
Эпидуральный абсцесс — это гнойный воспалительный процесс локального характера, который возникает в эпидуральном пространстве позвоночного столба. Эпидуральное пространство в свою очередь представляет собой своеобразную щель, которая располагается между дуральной (твёрдой) оболочкой спинного мозга и стенками позвоночного канала.

На локальном уровне выявляются отеки, гипертонус мышц в пораженной зоне. Может развиться парез нижних конечностей, дисфункция органов малого таза.
Видео: «Анатомия спинного мозга»
Эпидуральный абсцесс может возникнуть в любом отделе позвоночника. Хотя наиболее частыми случаями абсцесса являются поясничный и грудной абсцессы. Патология может иметь острый характер или же хронический.
Самыми частыми возбудителями эпидурального абсцесса являются патогенные микроорганизмы, т.е. стафилококки, стрептококки и т.д. Именно они вызывают гнойные воспаления в организме вне зависимости от тяжести и локализации. Инфекция попадает в эпидуральное пространство через кровь и лимфу или через ближайшие ткани.
Источники, способные вызвать острый эпидуральный абсцесс:
- Заболевания легких;
- Урогенные инфекции;
- Фурункулы и фурункулёз;
- Септикопиемия;
- Стоматологические заболевания.
Причиной возникновения хронической формы эпидурального абсцесса могут стать:
Острая форма эпидурального абсцесса отличается от хронической тем, что в случае с острым воспалением инфекция не может проникнуть в спинной мозг, поскольку ей преграждает путь твердая оболочка спинного мозга. Хроническая же форма способна разрушать эти твердые стенки и вызывать изменения в клетчатке эпидурального пространства.
Факторами риска развития эпидурального абсцесса можно считать:
- Алкоголизм;
- Употребление наркотиков;
- Гнойная инфекция в организме;
- Операционные вмешательства на спинном мозге;
- Сахарный диабет;
- Посттравматические проблемы спины;
- Возрастные изменения.

Размеры гнойной инфекции могут дать прогноз о вероятном летальном исходе. И хотя современные достижения медицины могут справляться даже с серьезным сепсисом, иммунная система пациента может не справиться с тем количеством стероидов, которым будут ее «кормить».
Если размеры сепсиса были не слишком большими, то шансы избавления от заболевания высоки. В медицинской практике имеются случаи рецидива абсцесса. Поэтому нужно внимательно относится к своему здоровью и проходить регулярное обследование, чтобы избежать повторной инфекции.
Основными симптомами, служащими сигналом о наличии абсцесса, являются:
- Острая боль в зоне поражения, не затихающая и не прекращающаяся на протяжении нескольких недель;
- Высокая температура, также не спадающая на протяжении нескольких недель;
- Озноб;
- Болевые ощущения, распространяющиеся на нижние конечности;
- Гипертонус мышц в зоне поражения.
Эти симптомы характеризуют первую стадию заболевания.
Для второй стадии характерно развитие корешкового синдрома, что в свою очередь влечет за собой снижение сухожильных рефлексов в зоне поражения
На третьей стадии развиваются парезы нижних конечностей, возникает дисфункция малого таза.
Четвертая стадия характеризуется нарастаниями парезов, вплоть до полного паралича, потерей чувствительности в конечностях.
На внешнем уровне можно увидеть отечность тканей и гиперемию кожи в зоне поражения.
Острая форма эпидурального абсцесса характеризуется развитием параличей уже спустя несколько суток после первого симптома болезни. Хронической форме для этого требуется несколько недель (2-3).
Кода остра форма перерастает в хроническую, температура тела снижается, несколько снижается выраженность симптомов. Для хронической формы свойственно периодическое обострение и затухание симптомов заболевания.
Диагностировать эпидуральный абсцесс довольно непросто, поскольку симптоматика заболевания неспецифична.
Если у пациента имеется ярко выраженный инфекционный процесс в области позвоночника или очаг гнойной инфекции в удаленной от позвоночника области, то невролог или нейрохирург могут заподозрить спинальный эпидуральный абсцесс.

Дополнительно к общему анализу крови назначается бакпосев крови, рентгенография позвоночника (для выявления остеомиелита и туберкулезного спонндилита).
Если врач заподозрил грудной или шейный эпидуральный абсцесс, то он может назначит люмбальную пункцию, которую можно совместить с миелографией. Миелография поможет выявить частичное или полное сдавливание спинного мозга.
Из стандартных мероприятий пациенту назначается КТ и МРТ позвоночника.
Видео: «Абсцесс мозга — что делать?»
Диагноз «спинальный эпидуральный абсцесс» требует немедленного оперативного вмешательства. Только своевременно проведенная операция гарантирует избежание летального исхода.
Прием антибиотиков начинается еще до получения результатов бакпосева, на стадии подготовки к операции. Препараты вводятся пациенту парентерально. Обычно назначаются такие препараты, как Амоксициллин, Рифампицин, Цефотаксим. Медикаменты могут вводиться как в индивидуальном порядке, так и в комбинации с другими антибиотиками.
После этого начинается пероральный прием препаратов. Лечение антибиотиками должно длиться около 2 месяцев.
Пациенту с эпидуральным абсцессом проводят декомпрессию спинного мозга при помощи ламинэктомии и дренирования субдурального пространства.
Если у пациента имеется остеомиелит, то по ходу операции хирург удаляет отмершие костные ткани и фиксирует позвоночник. Если операция была проведена своевременно, то это предотвратит развитие парезов или уменьшит их степень (если заболевание было запущено).

Летальный исход в случае с эпидуральным абсцессом регистрируется в 15-20% случаев. Чаще всего в эти цифры входят пожилые люди с дооперационным параличом. Улучшение выраженного неврологического дефицита происходит редко, даже если операционное вмешательство было осуществлено в течение первых 6-13 часов после его появления.
Спинальный эпидуральный абсцесс — это заболевание серьезное и опасное.
Поэтому каждому нужно помнить о некоторых особенностях этой патологии:
- Причиной возникновения эпидурального абсцесса может быть снижение иммунитета на фоне наличия инфекционного воспаления или гнойной инфекции. Возбудителями гнойной инфекции обычно являются различные «кокки»: стафилококки, стрептококки и т.д. Поэтому стоит внимательнее относиться к гигиене и питанию, чтобы поддерживать иммунитет в норме;
- Эпидуральный абсцесс имеет 4 стадии развития, а также две формы протекания: острую и хроническую. Хроническая форма отличается от острой по симптоматике и причинам возникновения;
- Лечение эпидурального абсцесса проводится только хирургическим путем и антибиотической терапией. При чем операцию нужно проводить как можно раньше, чтобы предотвратить риск развития паралича или летальный исход.
источник
 Общий анализ крови: высокий лейкоцитоз, увеличенная скорость оседания эритроцитов.
Общий анализ крови: высокий лейкоцитоз, увеличенная скорость оседания эритроцитов.


.%20%D0%9E%D0%BA%D0%BE%D0%BB%D0%BE%2030-35%%20%D0%BF%D1%80%D0%B8%D1%85%D0%BE%D0%B4%D0%B8%D1%82%D1%81%D1%8F%20%D0%BD%D0%B0%20%D0%B0%D0%B1%D1%81%D1%86%D0%B5%D1%81%D1%81%20%D0%BF%D0%BE%D1%8F%D1%81%D0%BD%D0%B8%D1%87%D0%BD%D0%BE%D0%B3%D0%BE%20%D0%BE%D1%82%D0%B4%D0%B5%D0%BB%D0%B0,%20%D0%B2%20%D1%82%D0%BE%20%D0%B2%D1%80%D0%B5%D0%BC%D1%8F%20%D0%BA%D0%B0%D0%BA%20%D1%81%D0%B0%D0%BC%D1%8B%D0%B9%20%D0%BC%D0%B0%D0%BB%D1%8B%D0%B9%20%D0%BF%D1%80%D0%BE%D1%86%D0%B5%D0%BD%D1%82%20%E2%80%94%2015%%20%E2%80%94%20%D0%BF%D1%80%D0%B8%D1%85%D0%BE%D0%B4%D0%B8%D1%82%D1%81%D1%8F%20%D0%BD%D0%B0%20%D1%88%D0%B5%D0%B9%D0%BD%D1%8B%D0%B9%20%D0%BE%D1%82%D0%B4%D0%B5%D0%BB%20%D0%BF%D0%BE%D0%B7%D0%B2%D0%BE%D0%BD%D0%BE%D1%87%D0%BD%D0%BE%D0%B3%D0%BE%20%D1%81%D1%82%D0%BE%D0%BB%D0%B1%D0%B0.</p>%0A<p>%D0%A7%D0%B0%D1%89%D0%B5%20%D0%B2%D1%81%D0%B5%D0%B3%D0%BE%20%D0%B7%D0%B0%D0%B1%D0%BE%D0%BB%D0%B5%D0%B2%D0%B0%D0%BD%D0%B8%D0%B5%20%D1%84%D0%B8%D0%BA%D1%81%D0%B8%D1%80%D1%83%D1%8E%D1%82%20%D1%83%20%D0%BB%D1%8E%D0%B4%D0%B5%D0%B9%20%D0%B2%20%D0%B2%D0%BE%D0%B7%D1%80%D0%B0%D1%81%D1%82%D0%B5%20%D0%BE%D1%82%2045%20%D0%B4%D0%BE%2075%20%D0%BB%D0%B5%D1%82%20%D1%81%20%D0%BD%D0%B8%D0%B7%D0%BA%D0%B8%D0%BC%D0%B8%20%D0%BF%D0%BE%D0%BA%D0%B0%D0%B7%D0%B0%D1%82%D0%B5%D0%BB%D1%8F%D0%BC%D0%B8%20%D0%B8%D0%BC%D0%BC%D1%83%D0%BD%D0%B8%D1%82%D0%B5%D1%82%D0%B0.</p>%0A<p><strong>%D0%9F%D0%B5%D1%80%D0%B2%D0%BE%D0%BE%D1%87%D0%B5%D1%80%D0%B5%D0%B4%D0%BD%D1%8B%D0%BC%D0%B8%20%D1%81%D0%B8%D0%BC%D0%BF%D1%82%D0%BE%D0%BC%D0%B0%D0%BC%D0%B8%20%D0%B2%20%D1%81%D0%BB%D1%83%D1%87%D0%B0%D0%B5%20%D1%81%20%D1%8D%D0%BF%D0%B8%D0%B4%D1%83%D1%80%D0%B0%D0%BB%D1%8C%D0%BD%D1%8B%D0%BC%20%D0%B0%D0%B1%D1%81%D1%86%D0%B5%D1%81%D1%81%D0%BE%D0%BC%20%D1%8F%D0%B2%D0%BB%D1%8F%D1%8E%D1%82%D1%81%D1%8F%20%D0%BE%D1%81%D1%82%D1%80%D1%8B%D0%B5%20%D0%B8%20%D0%B8%D0%BD%D1%82%D0%B5%D0%BD%D1%81%D0%B8%D0%B2%D0%BD%D1%8B%D0%B5%20%D0%B1%D0%BE%D0%BB%D0%B8%20%D0%B2%20%D1%81%D0%BF%D0%B8%D0%BD%D0%B5%20%D0%B2%20%D0%B7%D0%BE%D0%BD%D0%B5%20%D0%BF%D0%BE%D1%80%D0%B0%D0%B6%D0%B5%D0%BD%D0%B8%D1%8F,%20%D0%BF%D1%80%D0%B8%20%D1%8D%D1%82%D0%BE%D0%BC%20%D1%83%20%D0%BF%D0%B0%D1%86%D0%B8%D0%B5%D0%BD%D1%82%D0%B0%20%D0%B4%D0%B5%D1%80%D0%B6%D0%B8%D1%82%D1%81%D1%8F%20%D0%B2%D1%8B%D1%81%D0%BE%D0%BA%D0%B0%D1%8F%20%D1%82%D0%B5%D0%BC%D0%BF%D0%B5%D1%80%D0%B0%D1%82%D1%83%D1%80%D0%B0,%20%D0%B5%D0%B3%D0%BE%20%D0%B1%D1%8C%D0%B5%D1%82%20%D0%BF%D0%BE%D1%81%D1%82%D0%BE%D1%8F%D0%BD%D0%BD%D1%8B%D0%B9%20%D0%BE%D0%B7%D0%BD%D0%BE%D0%B1</strong>.</p>%0A<p>%D0%91%D0%BE%D0%BB%D0%B5%D0%B2%D1%8B%D0%B5%20%D0%BE%D1%89%D1%83%D1%89%D0%B5%D0%BD%D0%B8%D1%8F%20%D0%BF%D1%80%D0%B8%20%D1%8D%D1%82%D0%BE%D0%BC%20%D0%BE%D1%82%D0%B4%D0%B0%D1%8E%D1%82%20%D0%B2%20%D0%BD%D0%B8%D0%B6%D0%BD%D0%B8%D0%B5%20%D0%BA%D0%BE%D0%BD%D0%B5%D1%87%D0%BD%D0%BE%D1%81%D1%82%D0%B8,%20%D0%B2%D0%BE%D0%B7%D0%BD%D0%B8%D0%BA%D0%B0%D0%B5%D1%82%20%D0%BE%D1%89%D1%83%D1%89%D0%B5%D0%BD%D0%B8%D0%B5%20%D0%BE%D0%BD%D0%B5%D0%BC%D0%B5%D0%BD%D0%B8%D1%8F,%20%D0%BF%D0%BE%D1%82%D0%B5%D1%80%D0%B8%20%D1%87%D1%83%D0%B2%D1%81%D1%82%D0%B2%D0%B8%D1%82%D0%B5%D0%BB%D1%8C%D0%BD%D0%BE%D1%81%D1%82%D0%B8.%20%D0%A7%D0%B5%D0%BC%20%D0%B4%D0%B0%D0%BB%D1%8C%D1%88%D0%B5%20%D0%B1%D1%83%D0%B4%D0%B5%D1%82%20%D1%80%D0%B0%D0%B7%D0%B2%D0%B8%D0%B2%D0%B0%D1%82%D1%8C%D1%81%D1%8F%20%D0%B1%D0%BE%D0%BB%D0%B5%D0%B7%D0%BD%D1%8C,%20%D1%82%D0%B5%D0%BC%20%D0%B1%D0%BE%D0%BB%D1%8C%D1%88%D0%B5%20%D0%BF%D0%B0%D1%86%D0%B8%D0%B5%D0%BD%D1%82%20%D0%B1%D1%83%D0%B4%D0%B5%D1%82%20%D0%BE%D1%89%D1%83%D1%89%D0%B0%D1%82%D1%8C%20%D1%81%D0%BB%D0%B0%D0%B1%D0%BE%D1%81%D1%82%D1%8C%20%D0%B2%20%D0%BA%D0%BE%D0%BD%D0%B5%D1%87%D0%BD%D0%BE%D1%81%D1%82%D1%8F%D1%85,%20%D0%BF%D0%BE%D1%8F%D0%B2%D0%B8%D1%82%D1%81%D1%8F%20%D1%80%D0%B0%D1%81%D1%81%D1%82%D1%80%D0%BE%D0%B9%D1%81%D1%82%D0%B2%D0%BE%20%D1%82%D0%B0%D0%B7%D0%BE%D0%B2%D1%8B%D1%85%20%D1%84%D1%83%D0%BD%D0%BA%D1%86%D0%B8%D0%B9.</p>%0A<p><strong>%D0%9F%D1%80%D0%B8%20%D0%B8%D1%81%D1%81%D0%BB%D0%B5%D0%B4%D0%BE%D0%B2%D0%B0%D0%BD%D0%B8%D0%B8%20%D0%B2%D1%8B%D1%8F%D0%B2%D0%BB%D1%8F%D1%8E%D1%82%20%D1%82%D0%B0%D0%BA%D0%B8%D0%B5%20%D0%B8%D0%B7%D0%BC%D0%B5%D0%BD%D0%B5%D0%BD%D0%B8%D1%8F,%20%D0%BA%D0%B0%D0%BA</strong>:</p>%0A<ul>%0A<li>%D0%9E%D0%B1%D1%89%D0%B5%D0%BC%D0%BE%D0%B7%D0%B3%D0%BE%D0%B2%D0%BE%D0%B9%20%D1%81%D0%B8%D0%BD%D0%B4%D1%80%D0%BE%D0%BC;</li>%0A<li>%D0%9C%D0%B5%D0%BD%D0%B8%D0%BD%D0%B3%D0%B5%D0%B0%D0%BB%D1%8C%D0%BD%D1%8B%D0%B9%20%D1%81%D0%B8%D0%BD%D0%B4%D1%80%D0%BE%D0%BC;</li>%0A<li>%D0%9E%D0%B1%D1%89%D0%B5%D0%B8%D0%BD%D1%84%D0%B5%D0%BA%D1%86%D0%B8%D0%BE%D0%BD%D0%BD%D1%8B%D0%B9%20%D1%81%D0%B8%D0%BD%D0%B4%D1%80%D0%BE%D0%BC.</li>%0A</ul>%0A<p%20style=)