При этом образующиеся спайки отграничивают скопление гноя от свободных отделов брюшной полости. Вначале образуется воспалительный инфильтрат, в состав которого могут входить петли кишок, сальник, стенки мочевого пузыря, матки и прямой кишки. С затиханием воспалительной реакции образуется пиогенная капсула. При абсцессе всегда имеют место интоксикация и опасность вскрытия капсулы в брюшную полость, прямую кишку или во влагалище. Абсцессы формируются на 5—8-е сутки после операции и позже.
Клиническая картина характеризуется повышением температуры (постоянного или гектического типа) с 4—6-х суток послеоперационного периода, болями внизу живота, нарастающими изменениями в крови (повышение СОЭ, лейкоцитоз и др.). При вскрытии абсцесса и попадании гноя в брюшную полость возникают симптомы раздражения брюшины и другие симптомы перитонита.
С целью диагностики используются пункция брюшной полости через задний свод, УЗИ, компьютерная томография, лапароскопия.
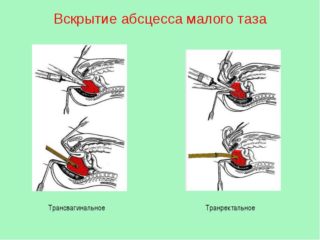
Лечение оперативное. Если раньше предпочтение отдавалось вскрытию абсцессов через задний свод, то в настоящее время операции выполняются трансабдоминально. Дренирование брюшной полости осуществляется через дополнительные разрезы в подвздошных областях и через задний свод влагалища.
Послеоперационные абсцессы малого таза, брюшной полости и забрюшинных пространств в гинекологической практике в настоящее время встречаются редко. Чаще из них наблюдаются абсцессы полости малого таза. Возникают они у женщин в основном после операций по поводу гнойно-воспалительных процессов, реже — по другим причинам.
Основным условием развития послеоперационных абсцессов является снижение неспецифической резистентности организма и иммунных механизмов.
Чаще они возникают при невозможности радикального удаления очагов воспалительного процесса.
Межпетельные абсцессы — это ограниченное скопление гноя между петлями тонкой и толстой кишок. В гинекологической практике встречаются редко. Развиваются они при гинекологических операциях по поводу заболеваний, сопровождающихся общим или диффузным перитонитом.
Возникновению межпетельных абсцессов способствует недостаточная санация брюшной полости, неадекватное дренирование. Чаще они наблюдаются в илеоцекальной области, в правом или левом боковых каналах.
Клинически заболевание вначале проявляется парезом кишечника при субфебрильной температуре. В последующем симптомы становятся более выраженными: появляются сильные боли в животе, высокая (38—39°С) темперетура, типичные для воспалительного процесса изменения показателей крови. Возможно развитие кишечной непроходимости, как паралитической (из-за раздражения нервных окончаний кишки), так и механической (за счет сдавления кишки инфильтратом, образованием изгибов). При нескольких межпетельных абсцессах клиника напоминает разлитой перитонит. Выявлению межпетельных абсцессов помогают рентгенологические, ультразвуковые исследования и компьютерная томография.
Лечение в стадии инфильтратов может быть консервативным (холод, дезинтоксикационная, антибактериальная терапия), при образовании абсцессов — оперативное. Вскрытие абсцессов, опорожнение от гноя и дренирование производятся трансабдоминально или через разрезы, произведенные экстраперитонеально непосредственно над областью гнойника.
Реже в гинекологической практике встречаются послеоперационные поддиафрагмальные абсцессы (в верхнем этаже брюшной полости, ограниченные сверху диафрагмой), забрюшинные, абсцессы печени, селезенки и других локализаций.
источник
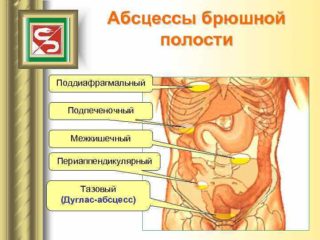
Абсцессы малого таза возникают в местах, где имеются благоприятные условия. К располагающим факторам относится застой воспалительного экссудата или выливание крови. Жидкость скапливается в самом низком месте брюшной полости — дугласовом пространстве. У женщин очаг болезни располагается между маткой и прямой кишкой, у мужчин в углублении между мочевым пузырем и прямой кишкой. Воспаление тканей с гнойной полостью возникает как осложнение хирургических вмешательств, аппендицита, гинекологических инфекций.
- травмы и операции на органах брюшной полости;
- острый аппендицит;
- несоблюдение правил асептики;
- недостаточное дренирование и санирование брюшной полости;
- гнойные гинекологические воспаления.
Предрасположенность к патологии наблюдается у пациентов с сахарным диабетом, болезнью Корна, а также беременных.
Патология характерна для любого пола и возраста, наблюдается у детей как форма осложнения после операции.

- ухудшение общего состояния;
- сильные боли внизу живота;
- проблемы с мочеиспусканием;
- позывы к дефекации;
- тенизмы;
- жажда;
- учащение пульса;
- тошнота;
- слизистые выделения из прямой кишки, влагалища.
Клиническая картина не одинакова для всех пациентов, патология может иметь минимальные проявления или совсем не проявляться до определенного момента. Симптоматика зависит от локализации очага нагноения. Пока капсула целая, брюшина не раздражается. Перфорация абсцесса в кишечник приводит к появлению свищей. Обычно они наблюдаются в толстой кишке.
В процессе сбора анамнеза врач учитывает недавние хирургические вмешательства и гинекологические проблемы. При подозрении на абсцесс проводится ректальное (для мужчин) и вагинальное (для женщин) обследование. Пальпаторно определяется плотный инфильтрат с размягченным участком в центре. Образование болезненное, при разрастании давит на прямую кишку. Возникают ложные позывы к дефекации.
Консистенция инфильтрата различается в зависимости от продолжительности формирования. Вначале образование плотное, с появлением гноя размягчается. У женщин шейка матки смещается в сторону. Более полную картину патологии дает инструментальное обследование и лабораторные анализы:
- УЗИ малого таза;
- КТ или МРТ для уточнения локализации очага нарыва;
- общий и биохимический анализ крови;
- анализ мочи — при вовлечении мочевого пузыря выявляются лейкоциты, белок.
Если при пальпации обнаружена флюктация (образование гноя), показана пункция. Она проводится через прямую кишку или задний свод влагалища. Для процедуры используется шприц с пункционной иглой. После извлечения жидкости проводится бактериологическое исследование.
Лечение абсцесса проводится оперативно, с госпитализацией пациента. На стадии плотного инфильтрата назначаются клизмы и спринцевание теплыми отварами лекарственных трав. Процедуры способствуют скорейшему образованию гноя и размягчению абсцесса. Также на этой стадии проводится консервативная терапия по снятию интоксикации. Пациенту прописываются антибиотики широкого спектра действия. Препараты подавляют аэробные и анаэробные бактерии.
В процессе консервативного лечения возможен произвольный прорыв абсцесса. Пациенты замечают вытекание гноя с мочой или калом. Их состояние улучшается. В большинстве случаев прибегают к дренированию очага нагноения. Перед операцией больному ставят очистительную клизму. Хирургическое лечение проходит под общим наркозом. Выбор метода зависит от пола пациента:
- У мужчин производится вскрытие стенки прямой кишки. Для проведения операции выполняется расширение ануса. В наиболее мягком месте происходит вскрытие по игле. Процесс контролируется с помощью аппарата УЗИ. Разрез увеличивают корнцангом. Происходит опорожнение и санирование полости нарыва. Вставляется трубка для дренажа.
- У женщин тазовые абсцессы вскрываются через задний свод влагалища. Слизистая разрезается скальпелем, полость нарыва расширяется зажимам для лучшего оттока содержимого. На 3-4 суток вставляется трубка дренажа.
При выборе места доступа хирург ориентируется по данным о локализации нарыва. Операционный разрез может выполняться в промежности или над лоном. Установка вагинального дренажа не рекомендуется девственницам. В отсутствии возможности сделать пункцию под контролем УЗИ, добраться до патологического образования трансректально и трансвагинально, проводится лапаротомия.
Продолжительность периода восстановления зависит от выбранного метода операции и возраста пациента. Дренажную трубку удаляют через 2-3 дня, после прекращения оттока гноя. Больного располагают в полусидящем положении для обеспечения оттока жидкости. Антибактериальная терапия продолжается. Температура и общее самочувствие быстро приходит в норму.
В первые дни рекомендуется питание бульонами и жидкой кашей. Дальше назначается бесшлаковая диета. В период реабилитации запрещен подъем тяжестей, продолжительная ходьба.
Среди медиков патология считается менее опасной, чем нагноение в других отделах брюшной полости – поддиафрагмальном и межкишечном. Степень угрозы зависит от размеров гнойника. В некоторых случаях он может быть объемом до 500 мл. Существует риск прорыва абсцесса, который приведет к перитониту. Расплавление тканей ближайших органов обернется попаданием гноя в кишечник, мочевой пузырь или матку. Дальнейшее развитие событий: прорыв в матку и мочевой пузырь ведет к их воспалению, вытекание в прямую кишку способствует улучшению состояния пациента.
Меры по предотвращению возникновения и развития абсцессов:
- качественное удаление экссудата, сгустков крови, гноя во время операций;
- правильный выбор наркоза, позволяющий выполнить хирургическое вмешательство в полном объеме;
- своевременное лечение гинекологических и проктологических болезней, связанных с гнойными образованиями;
- проведение ректального и влагалищного обследования пациентов после удаления аппендицита.
Профилактические мероприятия касаются медицинских работников. От их профессионализма и ответственности зависит здоровье пациентов.
Патология успешно лечится, прогноз благоприятный. Это касается одиночных очагов воспаления. Своевременность вмешательства играет значимую роль. Грамотное лечение нагноения предотвращает распространение патологии на ближайшие органы.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Гнойно-воспалительные заболевания органов малого таза — инфекции репродуктивных органов женщины. Репродуктивные органы включают матку, маточные трубы, яичники и шейку матки. Инфекции могут быть вызваны различными видами бактерий. Распространенные симптомы — боль в низу живота, выделения из влагалища, повышение температуры, жжение и боль при мочеиспускании или нарушение менструального цикла.

В основе развития и формирования гнойных ВЗОМТ лежит множество взаимосвязанных процессов, начиная от острого воспаления и заканчивая сложными деструктивными изменениями тканей. Основным пусковым механизмом развития воспаления считают бактериальную инвазию. И если в патогенезе неосложненного острого гнойного воспаления (острый эндомиометрит, сальпингит) основную роль играет бактериальная инвазия «сексуальной инфекции нового типа» (гонококки, хламидии, микоплазмы, вирусы, условно-патогенные штаммы аэробных и анаэробных возбудителей), то при осложненных формах гнойного воспаления микрофлора более агрессивна и включает ассоциации следующих патогенных возбудителей: грамотрицательные неспорообразующие анаэробные бактерии (strongacteroides fragilis, Prevotella spр., Prevotella bivius, Prevotella disiens и Prevotella melaninogenica), грамположительные анаэробные стрептококки (Pep tostreptococcus spp.), аэробные грамотрицательные бактерии семейства Enterobacteriacea (E. coli, Proteus), аэробные грамположительные кокки (энтеро-, стрепто- и стафилококки).
В настоящее время основной причиной развития деструктивных, осложненных форм гнойного воспаления, в том числе и генерализованных, считают длительное использование ВМК, приводящее к возникновению тубоовариальных, а в отдельных случаях — множественных экстрагенитальных абсцессов с крайне неблагоприятным септическим клиническим течением, обусловленным Actinomycetes Israeli и анаэробами.
Далее в порядке убывания (по частоте) идут тяжелые гнойные послеродовые заболевания, затем гнойные осложнения на фоне обострения длительно существующих хронических заболеваний, далее — послеоперационные осложнения. Более редкие причины: нагноение гематом и плодного яйца при эктопической беременности, нагноение опухолей, первичный деструктивный аппендицит с тазовой флегмоной и прочие.

Кроме бактериальной инвазии, в этиологии гнойного процесса значительную роль играют так называемые провоцирующие факторы. Данное понятие включает физиологическое (менструацию, роды) или ятрогенное (аборты, ВМК, гистероскопию, гистеросальпингографию, операции) ослабление или повреждение барьерных механизмов, способствующее формированию входных ворот для патогенной микрофлоры и дальнейшему ее распространению.
Основные факторы, способствующие прогрессированию заболевания и формированию осложненных форм гнойного воспаления:
- необоснованно длительное консервативное ведение гнойных гинекологических больных;
- использование с целью лечения паллиативных вмешательств, не ликвидирующих очаг деструкции (пункции, дренирование).

Особенности течения гнойных ВЗОМТ в настоящее время:
- Повышение вирулентности и резистентности микрофлоры, преимущественно ассоциативной, в которой анаэробные и грамотрицательные микроорганизмы относят к основным патогенам. В это же время гонококк как возбудитель гнойного процесса не только не утратил своего значения, но и повысил степень своей агрессии за счет сопутствующей микрофлоры, в частности ИППП.
- Изменение клинического течения гнойных заболеваний внутренних половых органов: на современном этапе они изначально протекают как первично хронические и характеризуются длительным, рецидивирующим течением при крайней неэффективности медикаментозной терапии. Например, у большинства женщин, применяющих ВМК, манифестация заболевания происходит тогда, когда уже имеется тяжелое инфильтративное поражение гениталий.
Чаще всего гнойный сальпингит начинается остро, с повышения температуры (иногда сопровождается ознобами), появления болей внизу живота (типичная локализация болей — левая и правая гипогастральные области, при наличии сопутствующего эндомиометрита наблюдают так называемые «срединные» боли), обильных гнойных белей и резей при мочеиспускании. Вскоре у больных отмечают симптомы гнойной интоксикации (слабость, тахикардия, мышечные боли, чувство сухости во рту), присоединяются диспептические, эмоционально-невротические и функциональные расстройства. Нарушения функции прямой кишки проявляются чаще в виде симптома «раздраженной» кишки (частый жидкий стул). Частая жалоба — наличие выраженной диспареунии.
При влагалищном исследовании выявляют болезненность при движении за шейку матки, пастозность или наличие пальпируемого образования небольших размеров с нечеткими контурами в области придатков, а также чувствительность при пальпации бокового и заднего сводов.
Лабораторные исследования: у больных выявляют лейкоцитоз с умеренным сдвигом лейкоцитарной формулы влево (палочкоядерных лейкоцитов 6–9%), повышенная СОЭ (20–40 мм/ч), наличие резко положительного C-реактивного белка, гиперфибриногенемия.
Эхографические признаки острого гнойного сальпингита: наличие «расширенных, утолщенных, вытянутых маточных труб, характеризующиеся повышенным уровнем звукопроводимости, у каждой второй больной в прямокишечно-маточном углублении отмечают скопление свободной жидкости».
Высокоинформативной лечебно-диагностической процедурой при гнойном сальпингите (особенно при невозможности проведения лапароскопии) до настоящего времени считают пункцию заднего свода влагалища. Манипуляция позволяет получить гнойный экссудат для микробиологического исследования и провести дифференциальный диагноз с другой ургентной ситуацией, например с внематочной беременностью, апоплексией яичника.
По мнению G. strongalbi и соавт., классические признаки острого гнойного сальпингита: наличие болей в животе, болезненность при движении за шейку матки и чувствительность в области придатков в сочетании, по крайней мере, с одним из следующих дополнительных признаков (температура >38 °С; лейкоцитоз >10,5 9 /л и наличие гноя, полученного при пункции заднего свода влагалища).
- Нарастание симптомов гнойной интоксикации (появление гектической лихорадки, тошноты, рвоты, постоянного чувства сухости во рту, резкой мышечной слабости).
- Появление преимущественно в нижних отделах живота симптомов раздражения брюшины (пельвиоперитонит). Влагалищное исследование у больных пельвиоперитонитом малоинформативно из-за выраженной болезненности при пальпации. Определяют умеренное нависание и резкую болезненность сводов, особенно заднего, резко усиливающуюся при малейшем движении за шейку матки. Пропальпировать небольшие объемные образования в малом тазе обычно не удается.
- Появление «чувства резкого давления на прямую кишку» и учащенной дефекации (свидетельствует о формирующемся на фоне пельвиоперитонита абсцессе маточно-прямокишечного углубления). При гинекологическом осмотре в соответствующей анатомической области выявляют патологическое образование неравномерной консистенции, без четких контуров, пролабирующее через задний свод и переднюю стенку прямой кишки, резко болезненное при пальпации (так называемый «крик Дугласа»).
Относят все осумкованные воспалительные придатковые опухоли — пиосальпинкс, пиовар, гнойные тубоовариальные образования и их дальнейшие осложнения, обусловленные рядом факторов: длительностью заболевания, стадией воспаления, глубиной деструктивного процесса и характером поражения органов и систем. Основной клинический симптом у данного контингента больных, кроме болей и температуры, — наличие изначально тяжелой гнойной эндогенной интоксикации. Гнойные бели наблюдают у послеродовых, послеабортных больных и пациенток с ВМК (гнойный эндомиометрит). Следует отметить наличие у больных выраженных невротических расстройств, при этом наряду с симптомами возбуждения (повышенной раздражительности) на фоне интоксикации появляются и симптомы угнетения ЦНС: слабость, быстрая утомляемость, нарушение сна и аппетита.

Течение гнойного процесса на фоне ношения ВМК отличается особой тяжестью, при этом консервативное, даже интенсивное лечение малоэффективно. Извлечение ВМК даже на самых ранних этапах развития гнойного воспаления придатков матки не способствует купированию воспаления, выскабливание полости матки после удаления ВМК резко усугубляет тяжесть процесса.
Для больных с гнойными послеоперационными осложнениями характерно наличие преходящего пареза кишечника, сохранение или нарастание основных признаков интоксикации на фоне проводимой интенсивной терапии, а также их возобновление после короткого «светлого» промежутка.
Для акушерских больных основной клинический симптом — наличие прогрессирующего гнойного (некротического) эндомиометрита, не купирующегося даже при адекватно проводимой терапии: размеры матки не соответствуют срокам нормальной послеродовой инволюции, отсутствует тенденция к формированию шейки матки: шейка свободно в виде «паруса» свисает во влагалище, свободно пропускает один или два пальца. Наличие гематом (инфильтратов) в параметрии и/или позадипузырной клетчатке — неблагоприятный клинический признак, резко снижающий шансы на благоприятный исход консервативного лечения у данных больных.
Одной из отличительных особенностей клинического течения хронических гнойных ВЗОМТ считают волнообразность процесса. В стадии ремиссии воспалительного процесса клинические проявления выражены не резко, из всех симптомов сохраняется интоксикация легкой или средней степени тяжести. В стадии обострения проявляются основные признаки острого гнойного воспаления, при этом часто происходит появление новых осложнений.
Чаще всего обострению сопутствует острый пельвиоперитонит, характеризующийся ухудшением самочувствия и общего состояния больной, гипертермией, нарастанием явлений интоксикации, появлением в нижних отделах живота болей и слабоположительных симптомов раздражения брюшины. Острый пельвиоперитонит у больных с гнойными тубоовариальными образованиями может в любой момент привести к дальнейшим серьезным осложнениям, таким как перфорация гнойника в соседние органы, бактериальный шок, разлитой гнойный перитонит.
Разлитой гнойный перитонит развивается достаточно редко (3,1%), поскольку хронический гнойный процесс, как правило, ограничен полостью малого таза за счет многочисленных плотных сращений, брюшины и связок малого таза, сальника и прилежащих органов, т.е. превалирует гнойно-инфильтративный, «конгломератный» тип воспаления.
Чаще при прогрессировании заболевания появляются такие осложнения гнойного процесса, как параметрит, межкишечные абсцессы, гнойные свищи. О наличии параметрита у больных с гнойными тубоовариальными образованиями могут свидетельствовать клинические признаки:
- боли при мочеиспускании, пиурия (передний параметрит);
- запоры, затруднения при дефекации (задний параметрит);
- нарушение функции почек: появление мочевого синдрома, отеки, снижение диуреза (боковой параметрит);
- появление инфильтрата и гиперемии кожи над пупартовой связкой (передний параметрит);
- явления перифлебита наружной подвздошной вены (отек и цианоз кожи бедра, распирающие боли в ноге) — верхний боковой параметрит;
- проявления паранефрита (на ранних стадиях характерны проявления псоита: вынужденное положение больной с приведенной ногой) — верхний боковой параметрит.
Появление болей в мезогастральных отделах брюшной полости, сопровождающихся явлениями преходящего пареза кишечника или частичной кишечной непроходимости (тошнота, рвота, задержка стула), может свидетельствовать о формировании межкишечных абсцессов.
Появление на стороне поражения болей в грудной клетке, болезненности в области реберной дуги и шеи в месте проекции диафрагмального
нерва может косвенно свидетельствовать о формировании поддиафрагмального абсцесса.
Перфорацию тазового абсцесса (гнойное тубоовариальное образование, абсцесс маточно-прямокишечного пространства) в полые органы наблюдают у больных с длительным и рецидивирующим течением гнойного процесса. Ей предшествует так называемое состояние «предперфорации»:
- ухудшение общего состояния на фоне ремиссии имеющегося гнойного воспалительного процесса;
- повышение температуры до 38–39 °С, ознобы;
- появление болей внизу живота «пульсирующего», «дергающего» характера;
- появление тенезмов, жидкого стула (угроза перфорации в дистальные отделы кишечника, реже — в прилежащие к абсцессу отделы тонкой кишки);
- появление учащенного мочеиспускания, микрогематурии или пиурии (угроза перфорации в мочевой пузырь);
- появление инфильтрата и болей в области послеоперационно го шва.
Многократная перфорация в прилежащий отдел кишечника приводит к формированию генитальных свищей. Наиболее часто свищи формируются в различных отделах толстой кишки, чаще в верхнеампулярном отделе или ректосигмоидном углу, реже в слепой и сигмовидной кишке. Придатково-пузырные свищи встречают значительно реже, так как брюшина пузырно-маточной складки и предпузырная клетчатка расплавляются значительно медленнее. Свищи чаще диагностируют на стадии их формирования по клинике так называемой угрозы перфорации в мочевой пузырь.
При проведении влагалищного исследования гнойные тубоовариальные образования в стадии обострения характеризуются нечеткими контурами, неравномерной консистенцией, полной неподвижностью и выраженной болезненностью. При этом они всегда находятся в едином конгломерате с маткой, пальпация и определение которой крайне затруднены. Размеры гнойных образований придатков весьма вариабельны, но в острой стадии воспаления они всегда несколько больше истинных. В стадии ремиссии конгломерат имеет более четкие контуры, хотя сохраняет неравномерность консистенции и полную его неподвижность.
При сопутствующем параметрите у больных определяют инфильтраты различной (в зависимости от стадии воспалительного процесса) консистенции — от деревянистой плотности в стадии инфильтрации до неравномерной, с участками размягчения при нагноении. Воспалительные инфильтраты могут иметь различные размеры. В тяжелых случаях они достигают костей таза (боковые отделы таза, крестец, лоно) и могут распространяться на переднюю брюшную стенку и даже паранефральную клетчатку. Поражение параметрия, особенно задних его отделов, особенно хорошо выявляют при прямокишечно-влагалищном исследовании, при этом косвенно оценивают степень поражения воспалительным инфильтратом прямой кишки (слизистая подвижна, ограниченно подвижна, неподвижна).
За рубежом применяют в основном классификацию G. Monif (1982), включающую острые воспалительные процессы внутренних половых органов:
- острый эндометрит и сальпингит без признаков воспаления тазовой брюшины;
- острый эндометрит и сальпингит с признаками воспаления брюшины;
- острый сальпингоофорит с окклюзией маточных труб и развитием тубоовариальных образований;
- разрыв тубоовариального образования.
В Женевской международной статистической классификации болезней, травм и причин смерти (ВОЗ, 1980) имеются следующие нозологические формы воспалительных заболеваний внутренних половых органов.
- Острый сальпингит и оофорит:
- абсцесс: маточной трубы, яичника, тубоовариальный;
- оофорит;
- пиосальпинкс;
- сальпинит;
- воспаление придатков матки (аднекстумор).
- Острый параметрит и тазовая флегмона.
- Хронический или неуточненный параметрит и тазовая флегмона:
- абсцесс: широкой связки матки, прямокишечно-маточного углубления, параметрия, тазовая флегмона.
- Острый или неуточненный тазовый перитонит.
С практической точки зрения удобной считают классификацию, предложенную В.И. Краснопольским и соавт., позволяющую определять тактику ведения и прогноз развития и исхода заболевания. По клиническому течению заболевания и на основании патоморфологических исследований авторы выделяют две клинические формы гнойных воспалительных заболеваний гениталий: неосложненные и осложненные.
- К неосложненным формам относят острый гнойный сальпингит. При своевременной диагностике и целенаправленной терапии процесс может ограничиться поражением эндосальпинкса с последующей регрессией воспалительных изменений и выздоровлением. В случае запоздалой или неадекватной терапии острый гнойный сальпингит ос ложняется пельвиоперитонитом с частичным отграничением гнойного экссудата в маточно-прямокишечном углублении (Дуглас-абсцесс) или переходит в хроническую или осложненную форму — пиосальпинкс или гнойное тубоовариальное образование. В этих случаях изменения всех слоев маточной трубы и стромы яичника носят необратимый характер, что подтверждается результатами морфологических иссле дований.
- К осложненным формам относят все осумкованные воспалительные придатковые опухоли: пиосальпинкс, пиовар, гнойные тубоовариальные образования, при этом перспектива на последующее деторождение резко снижена или проблематична, а выздоровление больной может наступить только после хирургического лечения. При запоздалом хирургическом вмешательстве и дальнейшем прогрессировании процесса развиваются тяжелые гнойные осложнения, угрожающие жизни больной: простые и сложные генитальные свищи, микроперфорации абсцесса в брюшную полость с образованием межкишечных и поддиафрагмальных абсцессов, гнойно-инфильтративный оментит. Конечный исход гнойного процесса — сепсис.

Даже при возможности использования самых современных методов исследования основным способом диагностики, определяющим профессиональную квалификацию и клиническое мышление врача, является клинический. Все гнойные заболевания имеют специфические симптомы, отражающиеся в субъективных жалобах или данных объективного исследования. Развитие осложнений также «проходит» последовательные стадии и их четко отражают все больные при сборе информации об истории заболевания при условии знания врачом возможного течения заболевания и постановке направленных вопросов. Даже если заболевания в определенной степени имеют сходную клиническую картину (например, гнойный сальпингит и гнойные тубоовариальные образования в стадии обострения), всегда имеются клинические признаки (инициация заболевания, его продолжительность, степень интоксикации, симптоматика), позволяющие уточнить первичный клинический диагноз.
У больных с гнойными воспалительными заболеваниями внутренних половых органов целесообразна 3-этапная система обследования.
- При неосложненных формах:
- первый этап — клиническое обследование, включающее бимануальное исследование, бактериологическую и лабораторную диагностику;
- второй этап — трансвагинальная эхография органов малого таза;
- третий этап — лапароскопия для гинекологических больных (гистероскопия для послеродовых больных).
- При осложненнных формах:
- первый этап — клиническое обследование, включающее бимануальное и ректовагинальное исследование, бактериологическую и лабораторную диагностику;
- второй этап — трансабдоминальная и трансвагинальная эхография органов малого таза, брюшной полости, почек, печени и селезенки, эхокардиография, эхография с дополнительным контрастированием прямой кишки;
- третий этап — рентгенологическое исследование легких, дополнительные инвазивные методы обследования: цисто- и колоноскопия, фистулография.
В настоящее время даже при наличии тяжелых форм гнойного воспаления часто наблюдают «стертую» лабораторную симптоматику, обусловленную, в том числе, применением массивной антибактериальной терапии и местной санации. Поэтому нецелесообразно ориентироваться на лейкоцитоз как на основной маркер гнойного процесса (наблюдают только у 1/3 больных). Кроме того, лейкопению отмечают у 11,4% больных с тяжелыми формами гнойных ВЗОМТ у женщин. Она сопряжена с персистенцией в крови патологических аутоантитела к мембранам нейтрофилов.
В целом для данных пациенток наиболее характерно повышение СОЭ, наличие лимфопении и анемии. Анемию считают интоксикационной и степень ее коррелирует с тяжестью состояния больных.
Показатели периферической крови отражают стадию гнойного процесса. В стадии обострения чаще выявляют лейкоцитоз, повышение СОЭ (до 60–70 мм/ч), C-реактивный белок. При ремиссии гнойного процесса наблюдают снижение числа эритроцитов и гемоглобина, лимфопению и повышенную СОЭ.
Длительное течение гнойного процесса сопровождается нарушением белкового (гипо- и диспротеинемия), минерального, липидного обмена и ферментативной функции печени.
Выраженные нарушения системы гемостаза (с преобладанием процессов гиперкоагуляции) отмечают у 35,7% пациенток с осложненными формами гнойного воспаления, нарушения системы кровообращения — у 69,4% (гипокинетический тип кровообращения у 22% больных, снижение сократительной функции миокарда у 13% и нарушение скорости мозгового кровотока у 52% больных).
Основной дополнительный метод диагностики — эхография. Для гнойных тубоовариальных образований характерно:
- форма их чаще бывает неправильной, но все-таки приближается к овоидной;
- внутренняя структура отличается полиморфизмом: неоднородна и, как правило, представлена среднедисперсной эхопозитивной взвесью на фоне повышенного уровня звукопроводимости;
- контуры гнойного тубоовариального образования могут быть представлены: эхопозитивной толстой капсулой с четкими контурами, капсулой с участками неравномерной толщины и участками резкого истончения, а также образованием без четких контуров; при этом выявляют отсутствие сосудистой сети внутри образования.

Острый сальпингит дифференцируют.
- Острый аппендицит. Нехарактерна связь заболевания с перечисленными ранее факторами риска; заболевание возникает внезапно, ранний признак — приступообразная боль, вначале локализующаяся в области пупка или в эпигастрии, затем в области слепой кишки. Решающее значение в диагностике острого аппендицита — выявление симптомов Ситковского (усиление болей в правой подвздошной области при положении больного на левом боку) и Ровсинга (усиление болей в области слепой кишки при толчкообразном надавливании в левой подвздошной области). Для острого аппендицита также характерно почасовое нарастание количества лейкоцитов в анализе крови при исследовании в динамике.
- Эктопическая беременность, особенно в случае формирования и нагноения заматочных гематом, когда присоединяющиеся вторичные воспалительные изменения маскируют исходное заболевание. Для эктопической беременности характерны: нарушения менструального цикла (чаще задержка менструации с последующими длительными кровянистыми выделениями мажущего характера), наличие болей с иррадиацией в прямую кишку, периоды кратковременного на рушения сознания (головокружение, обморок и т.д.). Проведению дифференциального диагноза помогает определение ХГТ в крови и моче (в лаборатории или методом экспресс-тестов). В сложных случаях проведение пункции заднего свода или лапароскопии решает диагностическую проблему.
Гнойные тубоовариальные образования следует дифференцировать:
- при правосторонней локализации — с аппендикулярным инфильтратом;
- при преимущественно левосторонней локализации процесса — с дивертикулитом;
- с первичной карциномой трубы;
- с раком яичника;
- с инфильтративными формами эндометриоза.

В отдельных случаях есть показания для консультации хирурга, уролога, нефролога, сосудистого хирурга (см. 3-й этап обследования при осложненных формах).

Цель лечения гнойно-воспалительных заболеваний органов малого таза – ликвидация гнойного процесса (очага) в брюшной полости: сохранение жизни, здоровья, по возможности – детородной, менструальной и гормональной специфических женских функций. Отсутствие лечения у всех больных с гнойными ВЗОМТ приводит к тяжелым осложнениям (гнойный перитонит, сепсис) и летальности.
Абсолютные. Все пациентки с гнойными ВЗОМТ или подозрением на наличие данных заболеваний (см. группы риска и клинику) должны быть госпитализированы. Промедление с госпитализацией, проведение амбулаторного лечения, отсутствие своевременного оперативного вмешательства лишь усугубляет состояние пациенток и ограничивает в дальнейшем проведение органосберегающего лечения.
У данных больных из-за тяжести патологии не имеет решающего значения.
Ввиду тяжести общих и местных изменений у больных с гнойными заболеваниями органов малого таза и чрезвычайном риске генерализации процесса важными считают следующие тактические положения: при любой форме гнойного воспаления лечение может быть только комплексным, консервативно-хирургическим, состоящим из:
- патогенетически направленной предоперационной подготовки;
- своевременного и адекватного объема хирургического вмешательства, направленного на удаление очага деструкции;
- интенсивного и рационального ведения послеоперационного периода, причем чем раньше выполнена хирургическая санация очага, тем лучше исходы заболевания.
Предоперационная подготовка у больных с гнойным сальпингитом направлена на купирование острых проявлений воспаления и подавление агрессии микробного возбудителя. Для лечения больных с острым гнойным сальпингитом целесообразно использовать антибиотики (или их комбинации) с обязательным интраоперационным (во время лапароскопии) внутривенным их введением и продолжением антибактериальной терапии в послеоперационном периоде в течение 5–7 сут.
- Ингибиторозащищенные пенициллины, например амоксициллин + клавулановая кислота (клавуланат). Разовая доза препарата 1,2 г в/в, суточная доза 4,8 г, курсовая доза 24 г с интраоперационным (при проведении лапароскопии) внутривенным введением 1,2 г препарата.
- Фторхинолоны (хинолоны II поколения) в комбинации с нитроимидазолами (метронидазолом), например ципрофлоксацин или офлоксацин в разовой дозе 0,2 г в/в капельно (суточная доза 0,4 г, курсовая доза 2,4 г) с интраоперационным внутривенным введением 0,2 г препарата.
- Цефалоспорины III поколения в комбинации с нитроимидазолами (метронидазолом).
- проведение инфузионной терапии (кристаллоиды, корректоры электролитного обмена, плазмозамещающие и белковые препараты) в объеме трансфузий 1000–1500 мл/сут. Продолжительность терапии индивидуальна (в среднем 3–5 сут);
- назначение десенсибилизирующих и антигистаминных препаратов;
- применение НПВС, обладающих противовоспалительным, анальгетическим и антиагрегационным эффектом (препараты назначают после отмены антибиотиков);
- использование иммунокорректоров с первых суток лечения. С этой целью целесообразно применять аминодигидрофталазиндион натрия по следующей схеме: в 1-й день 0,2 г в/м, затем 3 дня ежедневно по 0,1 г в/м, с 5-х суток лечения — по 0,1 г 5 инъекций через день (на курс 10 инъекций препарата). Всем пациенткам, не получившим иммунокорригирующую терапию в стационаре, при выписке следует рекомендовать ее проведение в амбулаторных условиях с целью профилактики рецидива гнойного процесса.
На фоне проводимого консервативного лечения в первые 2–3 сут необходимо эвакуировать гнойный экссудат (хирургический компонент лечения). Наиболее эффективным методом хирургического лечения гнойного сальпингита на современном этапе считают лапароскопию, особенно у молодых, нерожавших пациенток.
При гнойном сальпингите адекватный объем вмешательства — адгезиолизис, санация и трансвагинальное (через кольпотомное отверстие) дренирование малого таза. В случаях гнойного сальпингоофорита и пельвиоперитонита с образованием осумкованного абсцесса в прямокишечно-маточном углублении адекватным пособием считают мобилизацию придатков матки, опорожнение абсцесса, санацию и активное аспирационное дренирование через кольпотомное отверстие. При сформировавшемся пиосальпинксе необходимо удалять маточную трубу или трубы. При пиоваре небольших размеров (до 6–8 см в диаметре) и сохранении интактной яичниковой ткани целесообразно произвести вылущивание гнойного образования. При абсцессе яичника проводят удаление яичника. Показанием к удалению придатков матки служит наличие в них необратимых гнойно-некротических изменений. Все операции необходимо заканчивать повторным тщательным промыванием малого таза и ревизией надпеченочного пространства для исключения затекания гноя и крови. С целью создания благоприятных условий для репарации и активной эвакуации экссудата целесообразно проводить активную аспирацию при помощи аппарата ОП-1 [19]. Это особенно важно у пациенток с выраженными гнойно-некротическими изменениями, когда после разъединения сращений образуются большие раневые поверхности, что приводит к продуцированию значительного количества раневого секрета и способствует образованию серозных или гнойных полостей, т.е. затяжному течению заболевания и его рецидивам.
Для проведения аспирационно-промывного дренирования (АПД) одну или две двухпросветные трубки из силиконовой резины диаметром 11 мм подводят к зонам наибольшей деструкции в малом тазе и выводят наружу через кольпотомное отверстие (или, при отсутствии условий для кольпотомии, через дополнительные контрапертуры в гипогастральных отделах). Подключают хирургический отсос (ОП-О1). АПД осуществляют введением раствора фурацилина (1:5000) по узкому просвету трубки со скоростью 20 капель в минуту и аспирацией под давлением 30 см вод.ст. в течение 2–3 сут в зависимости от тяжести процесса с периодическим струйным промыванием трубок при наличии гнойных «пробок».
Данный способ является методом патогенетической терапии, который воздействует на первичный очаг. При этом:
- осуществляется активное вымывание и механическое удаление инфицированного и токсичного содержимого брюшной полости;
- гипотермическое действие охлажденного фурацилина приостанавливает дальнейшее нарастание микробной инвазии, способствует снятию отека в пораженном органе и окружающих тканях, предотвращает поступление токсинов и микроорганизмов в кровеносную и лимфатическую системы;
- надежный отток промывной жидкости при отрицательном давлении исключает возможность накопления раствора в брюшной полости, позволяет очистить брюшину от фибрина, некротического детрита и уменьшить отек и инфильтрацию тканей;
Альтернативой служит методика проведения динамических лапароскопий, начиная со 2-х суток послеоперационного периода с периодичностью в 2 дня. Методика позволяет осуществить контроль за динамикой воспалительного процесса, разделить формирующиеся спайки, подводить лекарственные препараты непосредственно к очагу инфекции, проводить программированную санацию брюшной полости.
В послеоперационном периоде (до 7 дней) рекомендовано проведение антибактериальной, инфузионной и рассасывающей терапии. Необходимо подчеркнуть, что больные с гнойным сальпингитом после купирования острого воспаления нуждаются в длительной реабилитации, направленной на профилактику рецидива заболевания и восстановление фертильности.
Базовый компонент — хирургическое лечение. «Точки приложения» антибактериальной терапии у больных с осложненными формами гнойных ВЗОМТ определены особыми временными отрезками сложного и длительного течения заболевания. Применение антибиотиков целесообразно в следующих клинических ситуациях:
- у всех больных с острой гнойной инфекцией (манифестация заболевания);
- при клинических проявлениях активизации подострой или хронической гнойной инфекции и возникновении угрозы перфорации абсцесса или генерализации инфекции;
- интраоперационно у всех пациенток с целью периоперационной защиты и профилактики септического шока (препарат вводят в максимальной разовой дозе);
- в послеоперационном периоде у всех больных.
При генерализованных формах инфекции (перитонит, сепсис) антибактериальную терапию назначают немедленно, продолжительностью в интраоперационном (профилактика бактериального шока и послеоперационных осложнений) и в послеоперационном периоде.
Несмотря на существенный прорыв в микробиологической диагностике за последние 10–15 лет, первоначальный выбор антибактериальной терапии остается эмпирическим. В зависимости от тяжести заболевания препараты назначают в средней или максимальной разовой и суточной дозе. Для лечения данных больных целесообразно использовать следующие препараты.
- Ингибиторозащищенные пенициллины, например тикарциллин + клавулановая кислота (тиментин), пиперациллин + тазобактам (тазоцин). Преимущество этих препаратов заключается в их высокой активности в отношении аэробных и анаэробных бактерий, в том числе энтерококков и микроорганизмов, продуцирующих β-лактамазу.
- Цефалоспорины III поколения в комбинации с нитроимидазолами (метронидазолом). Обладают высокой активностью в отношении грамотрицательных бактерий, а также стафилококков, однако они имеют низкую антианаэробную активность, что требует их комбинации с антианаэробными препаратами.
- Ингибиторозащищенные цефалоспорины III поколения (цефоперазон + сульбактам). Препарат широкого спектра действия, обладающий, в числе прочего, и высокой антианаэробной активностью.
- Комбинацию линкозамидов и аминогликозидов, например комбинацию клиндамицин + аминогликозиды. Линкозамиды высокоактивны в отношении анаэробной и грамположительной кокковой флоры, аминогликозиды — в отношении грамотрицательных бактерий, при этом «пульс-терапия» аминогликозидами (введение суточной дозы за один прием) имеет преимущество перед традиционными схемами назначения (2–3 раза в сутки) как в плане клинической эффективности, так и более низкой нефро- и ототоксичности.
- Карбапенемы: имипенем + циластин (тиенам) или меропенем (меронем) — препараты, обладающие наиболее широким спектром антимикробной активности, в том числе против штаммов грамотрицательных бактерий, устойчивых к цефалоспоринам. Первостепенное значение в проведении предоперационной подготовки имеет дезинтоксикационная и детоксикационная терапия. Эффект детоксикации и подготовки больных к операции значительно повышается при эвакуации гнойного экссудата.
Показания для проведения дренирующих паллиативных операций (пункция или кольпотомия) у больных с осложненными формами гнойного воспаления:
- угроза перфорации абсцесса в брюшную полость или полый орган (с целью предупреждения перитонита или формирования свищей);
- наличие острого пельвиоперитонита, на фоне которого хирургическое лечение наименее благоприятно;
- тяжелая степень интоксикации.
По достижении ремиссии пациенток необходимо оперировать. Проведение повторных пункций заднего свода и кольпотомий нецелесообразно, поскольку это способствует формированию придатково-влагалищных свищей. Продолжительность предоперационной подготовки определяется индивидуально. Оптимальной для операции считается стадия ремиссии гнойного процесса.
Интенсивное консервативное лечение должно продолжаться не более 5 дней, а при развитии клинических проявлений угрозы перфорации — не более 12–24 ч, если нельзя провести паллиативного вмешательства с целью устранения угрозы перфорации.
В случае появления экстренных показаний к операции в течение 1,5–2 ч проводят предоперационную подготовку, включающую катетеризацию подключичной вены и трансфузионную терапию под контролем ЦВД в объеме как минимум 1200 мл коллоидов, белков и кристаллоидов в объеме 1:1:1.
Показания к экстренному вмешательству:
- перфорация абсцесса в брюшную полость с развитием разлитого гнойного перитонита;
- перфорация абсцесса в мочевой пузырь или ее угроза;
- септический шок.
Отличается характер хирургического лечения от тактики ведения больных с неосложненными формами. Таким пациенткам показана только лапаротомия.
Объем хирургического вмешательства индивидуален и зависит от следующих основных моментов: характера процесса, сопутствующей патологии гениталий и возраста больных. Представления об объеме операции должны складываться еще до операции после получения данных обследования и выявления степени поражения матки, придатков, определения характера осложнений и наличия экстрагенитальных гнойных очагов. Показания к выполнению реконструктивной операции с сохранением матки в первую очередь — отсутствие гнойного эндомиометрита или панметрита, множественных экстрагенитальных гнойных очагов в малом тазу и брюшной полости, а также сопутствующей тяжелой генитальной патологии (аденомиоз, миома). При наличии двусторонних гнойных тубоовариальных абсцессов, осложненных генитальными свищами, выраженного обширного гнойно-деструктивного процесса в малом тазу со множественными абсцессами и инфильтратами тазовой и параметральной клетчатки, подтверждении гнойного эндомиометрита или панметрита необходимо производить экстирпацию матки с сохранением, по-возможности, хотя бы части неизмененного яичника.
Основной принцип дренирования — установление дренажей по основным путям миграции жидкости в брюшной полости и малом тазе, т.е. основная часть дренажей должна находиться в латеральных каналах и позадиматочном пространстве, что обеспечивает полное удаление патологического субстрата. Целесообразно использование аспирационно-промывного дренирования с введением двухпросветных дренажных трубок:
- трансвагинально через открытый купол влагалища после экстирпации матки (дренажи диаметром 11 мм);
- посредством задней кольпотомии при сохраненной матке (целесообразно использовать дренаж диаметром 11 мм или два дренажа диаметром 8 мм);
- трансабдоминально (дополнительно трансвагинальному) через контрапертуры в мезо- или эпигастральных областях при наличии подпеченочных или межкишечных абсцессов — дренажи диаметром 8 мм.
Оптимальным режимом разряжения в аппарате при дренировании брюшной полости считают 30–40 см вод.ст. Средняя продолжительность дренирования 3 сут. Критериями прекращения дренирования служит улучшение состояния больной, восстановление функции кишечника, купирование воспалительного процесса в брюшной полости, тенденция к нормализации клинических анализов крови и температуры тела.
- Применение адекватного обезболивания. Оптимальный метод — применение длительной эпидуральной анестезии. Если по каким-либо причинам, не связанным с наличием противопоказаний, во время операции не проводилась комбинированная анестезия, то в послеоперационном периоде следует применить данный метод обезболивания и лечения. При наличии противопоказаний к использованию метода ДЭА в течение первых 3 сут обезболивание следует проводить наркотическими анальгетиками. Для потенцирования действия их следует сочетать с антигистаминными и седативными препаратами.
- Инфузионная терапия. Для коррекции нарушений в послеоперационном периоде важно как качество инфузионных сред, так и объем инфузии. Показано введение коллоидов (400–800 мл/сут), белковых препаратов из расчета 1–1,5 г нативного белка на 1 кг массы тела (при тяжелом течении процесса доза белка может быть увеличена до 150–200 г/сут); остальной объем замещают кристаллоидами. Количество вводимой жидкости, при условии сохраненной функции почек, составляет 35–40 мл/кг/сут. При тяжелых формах осложнений (перитонит, сепсис) количество вводимой жидкости может быть увеличено до 4–6 л (режим гиперволемии) с регуляцией мочеотделения (форсированный диурез). При септическом шоке количество вводимой жидкости не должно превышать количество выделенной мочи более чем на 800–1000 мл.
- Стимуляция кишечника. Адекватна «мягкая», физиологическая стимуляция кишечника за счет применения в первую очередь эпидуральной блокады, во вторую — адекватной инфузионной терапии в объеме нормо- или незначительной гиперволемии, в третью — за счет преимущественного использования препарата метоклопрамида, оказывающего регулирующее влияние на моторику ЖКТ. В лечении пареза кишечника немаловажную роль также играет коррекция гипокалиемии. Вводить препараты калия необходимо под контролем его содержания в сыворотке крови медленно, в разведенном виде, лучше в отдельную вену. В среднем в сутки вводят 6–8 г калия с учетом его содержания в других растворах (свежезамороженная плазма, гемодез и прочие).
- Целесообразно применять ингибиторы протеаз.
- У всех больных при отсутствии противопоказаний целесообразно использовать низкомолекулярный гепарин — надропарин кальция в дозе 0,3 мл (285 ME анти-Ха активности соответственно) под кожу живота в течение 5–7 дней, а также средств, улучшающих реологические свойства крови. Необходимо использование компрессионных чулков (эластичных бинтов), а также пневматической манжеточной компрессии с первых суток послеоперационного периода.
- Лечение глюкокортикоидами. Целесообразно использование преднизолона в суточной дозе 90–120 мг/сут (в зависимости от массы тела) с постепенным снижением и отменой препарата через 5–7 дней.
- Показано применение НПВС (назначают после отмены антибиотиков).
- По показаниям проводят терапию органных нарушений гепатотропными [фосфолипиды + поливитамины (эссенциале)] и кардиологическими средствами, применяют спазмолитики, экстракорпоральные методы детоксикации (плазмаферез).
- Иммунокоррекция. Целесообразно использование препарата аминодигидрофталазиона натрия, обладающего также выраженным противовоспалительным и антиоксидантным действием. Препарат применяют по следующей схеме: в первые сутки 0,2 г в/м, затем 3 дня ежедневно по 0,1 г в/м, далее через день 5 инъекций; затем 2 раза в неделю по 0,1 г в/м (курс лечения — 20 инъекций).
Все пациентки, перенесшие гнойно-воспалительные заболевания органов малого таза, нуждаются в длительной реабилитации.
источник
УЗИ-диагностика кистозных образований (кист) яичников
В клинической практике различают кисты и кистомы яичников. Киста – ретенционное опухолевидное образование – полость, заполненная жидкостью. При этом отсутствует пролиферация клеточных элементов, характерная для истинных опухолей (кистом). Нет убедительных данных о возможности развития рака яичников из ретенционных образований. Однако трудно провести дифференциальную диагностику их со злокачественным процессом.
К ретенционным, или простым кистам относятся фолликулярные кисты, кисты желтого тела (лютеиновые, тека-лютеиновые при пузырном заносе и хорионкарциноме), эндометриодные «шоколадные», паровариальные кисты.
В тех случаях, когда при гинекологическом исследовании выявляется то или иное патологическое образование в полости малого таза с помощью УЗИ можно решить ряд вопросов:
1) визуализировать пальпируемое образование на эхограмме;
2) установить его характер (жидкостное или мягкотканное);
3) точно локализовать относительно матки, яичников;
4) указать число и размеры образования, а также сделать точное описание эхографических характеристик объекта.
В распознавании кист и кистом яичников УЗИ органов малого таза имеет особую значимость, т.к. клиническая картина многих заболеваний бывает идентична, а данные гинекологического осмотра неспецифичными. Врач УЗИ должен исключить наличие вариантов нормы, воспалительных изменений, опухолей матки и, главное, провести дифференциальную диагностику между различными видами кист и опухолей яичников. Основным УЗИ-признаком кисты является обнаружение жидкостного образования в проекции яичника.
Фолликулярная киста развивается из зрелых или антральных фолликулов, часть сочетается с воспалительными заболеваниями матки и придатков, миомой матки. Это однокамерное, тонкостенное кистозное образования, наполненное прозрачным и светлым содержимым. Обычно к основанию кисты прилежит ткань макроскопически неизмененного яичника. Встречается в любом возрасте. При УЗИ малого таза визуализируется как эхонегативная структура.
Киста желтого тела встречается редко и возникает при воспалительных или гормональных изменениях в яичниках. Строение кисты сходно со строением желтого тела, отличается от него лишь размерами. Внутренняя поверхность кисты складчатая, содержимое – прозрачная жидкость. Чаще всего претерпевают обратное развитие.
В 50 % случаев пузырного заноса наблюдаются двусторонние лютеиновые кисты яичников, которые могут достигать больших размеров. После удаления пузырного заноса кисты исчезают в первые месяцы.
Эндометриодная («шоколадная») киста яичника – одно- или двустороннее образование, сине-багрового цвета с темно-геморрагическим содержимым. На эхограмме визуализируются нечетко, образуя множество эхо-сигналов. Эти кисты относятся к наружному перитонеальному эндометриозу и лечатся оперативно (лапараскопия, удаление кисты).
Паровариальная киста обычно небольших размеров, овоидной формы, гладкая, ограничена в подвижности. Протекает бессимптомно, при больших размерах могут быть боли внизу живота. Диагностика затруднена, в большинстве случаях при УЗ-исследовании такие кисты принимаются за кисты яичника. На УЗИ-органов малого таза виден здоровый яичник отдельно от паровариальной кисты.
Таким образом, ультразвуковое исследование органов малого таза на 5-7 день менструального цикла позволяет выявить, провести дифференциальную диагностику различных кистозных образований яичников.
Идентификация абсцессов на УЗИ. Диагностика абсцесса на узи.
При наличии у пациента участка отека, уплотнения, болезненности и покраснения бывает трудно дифференцировать целлюлит и абсцесс. Для дифференциальной диагностики этих состояний традиционно использовали аспирацию через иглу. Однако такая манипуляция болезненна и может увеличить риск инфекции. 1. Имеется ли абсцесс? 2. Имеются ли рядом с абсцессом сосуды? Важно распознать нормальную картину подкожных тканей и кожи (обсуждалось в предыдущем разделе). Часто при переходе от ткани с целлюлитом к здоровой ткани наблюдаются очевидные различия, относительная толщина различных тканей может указать на локализацию воспаления и инфекции. Абсцесс выглядит как гипоэхогенное или темное скопление жидкости, часто с серым гетерогенным содержимым внутри. Такие скопления жидкости нарушают архитектуру тканей. Они являются сжимаемыми, так как содержат жидкость. Также у них может наблюдаться эффект заднего акустического усиления, потому что звуковые волны, проходящие через наполненное жидкостью образование будут меньше ослабляться, чем волны, проходящие через окружающие ткани. Исследования поверхностных мягких тканей проводится с использованием высокочастотного (5—10 МГц) линейного датчика. Расположите пациента как для стандартного проведения манипуляции. Проведите сканирование над местом наибольшей флюктуации или над любой подозрительной областью. Отметьте наличие или отсутствие полости абсцесса, а также наличие расположенных рядом сосудов, которые могут помешать безопасному выполнению разреза и дренирования. Также отметьте любое расположенное глубже или латеральнее продолжение скопления жидкости. УЗИ иногда может выявить, что воспаление в поверхностных тканях является только «верхушкой айсберга» и заставит оператора провести дополнительную визуализацию или получить консультацию перед принятием решения о глубоком разрезе. Используя метки аппарата УЗИ, проведите измерение глубины от поверхности кожи до полости абсцесса. Можно использовать маркер, чтобы отметить локализацию полости. абсцессы на узи Оставшуюся часть манипуляции можно провести без использования УЗИ. В качестве альтернативы можно использовать ультразвуковой контроль в реальном времени при проведении иглы для аспирации, используя методику продольного доступа, описанную в нашей статье. Методика визуализации перитонзилярного абсцесса такая же, как и для других абсцессов. Единственным отличием является то, что для их идентификации лучше всего подходит высокочастотный внутриполостной датчик, так как благодаря его маленькой толщине датчик можно расположить в заднем глоточном пространстве, а высокая частота делает получаемые изображения легко читаемыми. На кончик датчика наносят гель, а стерильный колпачок служит барьером между датчиком и пациентом. Абсцесс выглядит в виде гипоэхогенного пространства под областью наибольшего отека. Использование УЗИ в этих условиях имеет несколько потенциальных преимуществ. Первое, можно избежать дискомфорта «сухого прокола», когда имеется уплотнение, но нет абсцесса. Второе, можно использовать цветовой допплер для определения глубины и локализации сонной артерии, чтобы не травмировать ее при проведении разреза и дренирования. На рисунке визуализирована игла при дренировании полости абсцесса. Как и при пункции сосуда, возможно использование статической локализации или контроля аспирации полости абспесса в реальном времени. Это зависит от способности больного вытерпеть длительную УЗ-визуализацию. УЗИ является более точным методом выявления абсцесса, чем только физикальное обследование (способность подтвердить диагноз 93 % против 81 %, способность опровергнуть диагноз 97 % и 77 % соответственно). Таким образом, при использовании УЗИ можно снизить число ненужных разрезов и дренирований. Другое исследование инфекции мягких тканей в ОР показало, что применение УЗИ изменило ведение около 50 % пациентов. Изменения ведения включали: распознавание скрытых абсцессов в случаях, когда ожидалось обнаружение только целлюлита, отмена вскрытия и дренирования, когда не было обнаружено абсцесса и проведение дополнительных обследований и консультаций.
Дата добавления: 2017-02-11 ; просмотров: 1244 | Нарушение авторских прав
источник