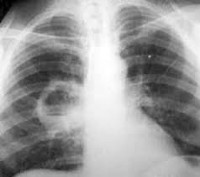
Осложнения ВИЧ-инфекции — вторичные заболевания, развивающиеся на фоне иммунодефицита. Механизм их возникновения связан либо с угнетением клеточного и гуморального иммунитета (инфекционные болезни и опухоли), либо с прямым воздействием вируса иммунодефицита человека (например, некоторые неврологические нарушения).

Примерно у 65% больных ВИЧ-инфекцией диагностируют туберкулёз как впервые возникшее заболевание, у остальных пациентов обнаруживают реактивацию процесса. ВИЧ существенно влияет на состояние иммунной системы (и на иммуно-реактивность) при туберкулёзе, нарушает дифференцировку макрофагов и препятствует образованию специфической гранулёмы. В то время как на ранних стадиях ВИЧ-инфекции морфология специфического воспаления существенно не меняется, на стадии СПИДа гранулёмы просто не формируются. Особенность туберкулёза лёгких у больных ВИЧ-инфекцией — тяжёлое течение заболевания с поражением бронхов и образованием свищей плевры, перикарда и лимфатических узлов. Как правило, в 75-100% случаев у больных ВИЧ-инфекцией возникает лёгочная форма туберкулёза, однако, по мере нарастания иммунодефицита, у 25-70% пациентов отмечают диссеминацию и развитие внелёгочных форм заболевания. Туберкулёз — одна из основных причин смерти пациентов (на стадии СПИДа) в Украине. Процессы, происходящие в лёгких больных СПИДом людей, — формирование корневой аденопатии и милиарных высыпаний; возникновение преимущественно интерстициальных изменений и образование плеврального выпота. При этом отмечают снижение количества случаев, сопровождающихся распадом лёгочной ткани, а следовательно, и числа больных, в мокроте которых при микроскопии и посеве обнаруживают микобактерии туберкулёза. Весьма характерным считают частое развитие туберкулёзной микобактериемии у больных СПИДом, как правило осложнённой септическим шоком и нарушением функций различных органов. Нередко наблюдают поражение лимфатических узлов (особенно шейных), костей, ЦНС, мозговых оболочек и органов пищеварительной системы: описаны абсцессы простаты и печени. Примерно у 60-80% ВИЧ-инфицированных пациентов туберкулёз протекает только с поражением лёгких, у 30-40% выявляют изменения других органов.
Группу возбудителей «нетуберкулёзных» микобактериозов составляют представители различных видов микобактерии (свыше сорока). Заболевания у человека вызывают восемнадцать разновидностей микобактерии. четыре вида микроорганизмов обладают сравнительно высокой патогенностью для людей, а четырнадцать видов относят к условно-патогенным. Атипичный микобактериоз, вызванный М. avium (входят в состав комплекса М. avium complex — MAC), — суперинфекция. составляющая группу СПИД-ассоциированных оппортунистических инфекций. До пандемии ВИЧ-инфекции атипичный микобактериоз диагностировали крайне редко, как правило, у лиц с выраженной иммуносупрессией (например, при трансплантации органов и тканей, после длительной кортикостероидной терапии, у онкологических больных). У пациентов, страдающих ВИЧ-инфекцией, иногда развивается диссеминированная форма МАС-инфекции. В терминальной стадии регистрируют локализованную или генерализованную формы заболевания. При локализованной МАС-инфекции обнаруживают абсцессы кожи и поражения лимфатических узлов, а при генерализованной — общеинтоксикационный и желудочно-кишечный синдромы, а также синдром экстрабилиарной обструкции. Признаки общеинтоксикационного синдрома — лихорадка, астенизация, снижение массы тела, тяжёлая анемия, лейкопения, повышение активности аланиновои трансаминазы в сыворотке крови. При желудочно-кишечном синдроме возникает хроническая диарея, боли в животе: отмечают гепатоспленомегалию, мезаденит и синдром мальабсорбции. Экстрабилиарная обструкция обусловлена перипортальным и перипанкреатическим лимфаденитом, приводящим к билиарному блоку и токсическому гепатиту. Основой диагностики атипичных микобактериозов считают выделение гемокультуры микобактерии.
Ранее возбудителя этого заболевания относили к простейшим, но генетический и биохимический анализ P. carinii показал его таксономическую принадлежность к дрожжевым грибам. Существуют три морфологические формы P. carinii — спорозоит (внутрицистное тельце диаметром 1-2 мкм). трофозоит (вегетативная форма), циста с толстой стенкой диаметром 7-10 мкм (состоит из восьми грушевидных спорозоитов).
В природе пневмоцисты обнаруживают у крыс, мышей, собак, кошек, свиней, кроликов и других млекопитающих, но заражение человека возможно только при контакте с человеком. Инфицирование происходит воздушно-капельным, аэрогенным, ингаляционным и трансплацентарным путём (редко). Пневмоцисты обладают высокой тропностью к лёгочной ткани, поэтому даже в фатальных случаях патологический процесс редко выходит за пределы лёгких (это связывают с крайне низкой вирулентностью возбудителя). Микроорганизмы прикрепляются к пневмоцитам, вызывая их десквамацию. Основные клинические признаки пневмоцистоза — интерстициальная пневмония и реактивный альвеолит. Симптомы неспецифичны. Продолжительность инкубационного периода пневмоцистной пневмонии варьирует от 8-10 дней до 5 нед. Начало заболевания невозможно отличить от банальных инфекций респираторного тракта. Клинические симптомы у больных СПИДом развиваются медленнее, чем у пациентов с гемобластозами. Одышка возникает очень быстро (частота дыхательных движений до 30-50 в минуту) и сопровождается сухим или влажным кашлем со скудной, вязкой (иногда пенистой) мокротой, цианозом, повышением температуры тела. Плевральные боли и кровохарканье возникают редко. При аускультации выслушивают жёсткое или ослабленное дыхание (локально или над всей поверхностью лёгких), сухие хрипы. По мере прогрессирования пневмонии могут нарастать симптомы дыхательной и сердечно-сосудистой недостаточности. Рентгенологическая картина в начале неспецифическая, затем обнаруживают прикорневое снижение пневматизации лёгочной ткани и усиление интерстициального рисунка. Более чем в половине случаев визуализируют билатеральные облаковидные инфильтраты (симптом «бабочки»), а в разгаре заболевания — обильные очаговые тени («ватное» лёгкое). В начале заболевания нормальную рентгенологическую картину обнаруживают у трети пациентов. Раннее вовлечение ацинусов создает на рентгенограммах картину так называемой воздушной бронхограммы (нередко ошибочно связывают с интерстициальным поражением). Однако в дальнейшем на рентгенограммах определяют преимущественно паренхиматозную природу пневмонии. В 10-30% случаев отмечают асимметричные, как правило, верхнедолевые инфильтраты. При проведении КТ обнаруживают периферические инфильтраты (иногда с очагами распада), снижение прозрачности («матовое стекло») и эмфизематозные участки. Пневмоторакс — наиболее часто возникающее осложнение.
При исследовании крови определяют гипохромную анемию, лейкоцитоз (до 50х10 9 /л) и эозинофилию. При проведении биохимического анализа крови обнаруживают повышение активности ЛДГ до 700-800 МЕ/л. Определение РаО2 позволяет выявить артериальную гипоксемию. Обнаружение антител к P. carinii — неспецифичный тест; культуральные методы отсутствуют. Поэтому диагноз ставят на основании прямой морфологической визуализации пневмоцист в биологическом материале с помощью различных методов (иммунофлюоресценция, методы окрашивания образцов Романовского-Гимзы и Грама, использование реактива Шиффа и др.), а также проводят ПЦР-диагностику.
Открытую биопсию лёгкого выполняют при прогрессирующем течении заболевания. Макроскопически во время операции лёгкое больного выглядит увеличенным, уплотнённым, консистенция его напоминает резину; отмечают буллёзные и эмфизематозные изменения, обнаруживают полости распада. Интраальвеолярный пенистый экссудат, диффузные альвеолярные повреждения, эпителиоидные гранулёмы, десквамативный интерстициальный пневмонит, интерстициальные лимфоидные инфильтраты — гистологические изменения в ткани лёгкого при пневмоцистной пневмонии. Выживаемость больных СПИДом при развитии пневмоцистной пневмонии не превышает 55%. Прогноз значительно ухудшается, если лечение начинают на фоне острой дыхательной недостаточности, тяжёлой гипоксии или при лейкопении. Летальность вследствие пневмонии и острой дыхательной недостаточности у больных СПИДом составляет, по разным данным, от 52,5 до 100%, а при осуществлении ИВЛ — 58-100%.
Цитомегаловирусная инфекция, как правило, протекает латентно. Однако иногда диагностируют клинически выраженные формы заболевания, обусловленные первичным инфицированием цитомегаловирусом, а также реинфекцией или реактивацией вируса в заражённом организме. Генерализованная цитомегаловирусная инфекци, сопровождающаяся возникновением клинических симптомов, занимает важное место в структуре оппортунистических заболеваний ВИЧ-инфицированных пациентов. Данную патологию регистрируют у 20-40% больных СПИДом, не принимающих антиретровирусные препараты. Цитомегаловирусная инфекция — непосредственная причина смерти 10-20% ВИЧ-инфицированных пациентов. Вероятность возникновения и тяжесть течения цитомегаловирусной инфекции связывают со степенью иммуносупрессии. Если количество СД4+-лимфоцитов в крови составляет 100-200 клеток в 1 мкл, то манифестную цитомегаловирусную инфекцию диагностируют у 1,5% ВИЧ-инфицированных людей. При уменьшении числа СД4+-лимфоцитов до 50-100 клеток в 1 мкл вероятность развития цитомегаловирусной инфекции увеличивается почти в четыре раза. При тотальном исчезновении СД4+-лимфоцитов (менее 50 клеток в 1 мкл) заболевание регистрируют практически у половины инфицированных пациентов.
Если содержание СД4+-лимфоцитов в крови достаточно велико (более 200 клеток в 1 мкл), то манифестацию цитомегаловирусной инфекции отмечают редко. Данное заболевание, как правило, развивается постепенно, при этом обнаруживают симптомы-предвестники. предшествующие формированию выраженных органных нарушений. У взрослых отмечают длительную волнообразную лихорадку неправильного типа с подъёмами температуры тела выше 38,5 °С. слабость, быструю утомляемость, потерю аппетита, существенное снижение веса; реже — потливость (преимущественно по ночам), артралгии или миалгии. При поражении лёгких указанные симптомы дополняет постепенно усиливающийся сухой или со скудной мокротой кашель. При вскрытии умерших пациентов, страдавших цитомегаловирусным поражением органов дыхания, нередко обнаруживают фиброателектаз лёгких с кистами и инкапсулированными абсцессами. Наиболее тяжёлый признак цитомегаловирусной инфекции — ретинит (диагностируют у 25-30% пациентов). Больные жалуются на плавающие пятна перед глазами, затем происходит снижение остроты зрения. Потеря зрения необратима, поскольку данный процесс развивается в результате воспаления и некроза сетчатки. При офтальмоскопии на сетчатке обнаруживают экссудаты и периваскулярные инфильтраты. При цитомегаловирусном эзофагите у больного при глотании возникает боль за грудиной. При эндоскопии в типичном случае визуализируют обширную поверхностную язву слизистой оболочки пищевода или желудка. Гистологические методы позволяют обнаружить клетки цитомегалии в биоптате: с помощью метода ПЦР можно определить ДНК вируса. Цитомегаловирусная инфекция может поражать различные органы пищеварительной системы, но чаще всего развивается колит. Пациента беспокоят боли в животе, жидкий стул, похудание и потеря аппетита. Перфорация кишки — наиболее грозное осложнение. Как возможные клинические симптомы цитомегаловирусной инфекции диагностируют также восходящий миелит и полиневропатию (подострого течения): энцефалит, характеризующийся деменцией; цитомегаловирусный гепатит с одновременным поражением жёлчных путей и развитием склерозирующего холангита; адреналит. проявляющийся резкой слабостью и снижением артеирального давления. Иногда возникает эпидидимит, цервицит. панкреатит.
Специфическое поражение сосудов преимущественно микроциркуляторного русла и сосудов мелкого калибра — морфологическая особенность патологического процесса при цитомегаловирусной инфекции. Для постановки клинического диагноза цитомегаловирусной инфекции необходимо проводить лабораторные исследования. Как показали исследования, наличие в крови больного антител класса IgM (или высоких титров антител класса IgG), a также присутствие вирионов в слюне, моче, сперме и вагинальном секрете недостаточно ни для установления факта активной репликации вируса, ни для подтверждения диагноза манифестной цитомегаловирусной инфекции. Обнаружение вируса (его антигенов или ДНК) в крови имеет диагностическое значение. Достоверным критерием высокой активности цитомегаловируса, доказывающим его этиологическую роль в развитии тех или иных клинических симптомов, служит титр ДНК цитомегаловируса. При повышении концентрации ДНК вируса в плазме в 10 раз вероятность развития цитомегаловирусного заболевания возрастает в три раза. Определение высокой концентрации ДНК вируса в лейкоцитах крови и плазме требует безотлагательного начала этиотропной терапии.

Токсоплазмоз — заболевание, вызываемое Т. gondii, чаще всего возникающее у ВИЧ-инфицированных пациентов на фоне СПИДа. Попадание токсоплазм в организм человека приводит к формированию объёмных образований в ЦНС (в 50-60% случаев) и развитию первичных эпилептических припадков (в 28% случаев). Токсоплазма — внутриклеточный паразит; заражение человека происходит при употреблении в пищу продуктов (мясо и овощи), содержащих ооцисты или тканевые цисты. Полагают, что развитие токсоплазмоза — реактивация латентной инфекции, поскольку при наличии в сыворотке крови антител к токсоплазме вероятность возникновения токсоплазмоза увеличивается в десять раз. Однако примерно у 5% ВИЧ-инфицированных пациентов на момент постановки диагноза токсоплазмоза антитела к Т. gondii отсутствуют. Заражение обычно происходит в детском возрасте. Цисты представляют собой очаги тлеющей инфекции, обострение или рецидив которых может наступить через несколько лет или даже десятилетий после инфицирования ВИЧ. В форме цист токсоплазмы сохраняются до 10-15 лет. преимущественно в тканях головного мозга и органа зрения, а также во внутренних органах. Патоморфологические изменения при токсоплазмозе имеют фазовый характер. В паразитемической фазе токсоплазмы поступают в регионарные лимфатические узлы, затем проникают в кровеносное русло и распространяются по органам и тканям. Во второй фазе происходит фиксация токсоплазмы в висцеральных органах, приводящая к развитию некротических и воспалительных изменений и образованию мелких гранулём. В течение третьей (заключительной) стадии токсоплазмы формируют в тканях истинные цисты; воспалительная реакция исчезает, очаги некроза подвергаются обызвествлению. Хотя токсоплазмы могут поражать все органы и ткани, но, как правило, у ВИЧ-инфицированных пациентов регистрируют церебральную форму заболевания. Отмечают лихорадку, головные боли, возникновение в 90% случаев разнообразной очаговой неврологической симптоматики (гемипарез, афазия, психические и некоторые другие нарушения). При отсутствии адекватного лечения наблюдают спутанность сознания, оглушённость, сопор и кому в результате отёка головного мозга. При выполнении МРТ или КТ с контрастированием обнаруживают множественные очаги с кольцевидным усилением и перифокальным отёком, реже — единичный очаг. Дифференциальный диагноз проводят с лимфомой головного мозга, опухолями другой этиологии, СПИД-дементным синдромом, мультифокальной лейкоэнцефалопатией и туберкулёмами. Почти в каждом случае диагностируют преимущественное поражение определённых органов и систем. Иногда токсоплазмоз протекает без формирования объёмных образований в головном мозге (по типу герпетического энцефалита или менингоэнцефалита). Внемозговые локализации токсоплазмоза (например, интерстициальная пневмония, миокардит, хориоретинит и поражение органов пищеварительной системы) у больных СПИДом регистрируют в 1,5-2% случаев. Максимальное количество очагов внемозговых локализаций обнаруживают при исследовании зрительного аппарата глаза (примерно в 50% случаев). Диссеминацня (по меньшей мере две локализации) происходит в 11,5% случаев. Диагностировать токсоплазмоз крайне сложно. Ликвор при спинномозговой пункции может быть интактным. Диагноз ставят на основании клинической картины, данных МРТ или КТ, а также при наличии антител к токсоплазме в сыворотке крови. Биопсию головного мозга выполняют при невозможности правильно установить диагноз. При биопсии в поражённых участках наблюдают воспаление с зоной некроза, расположенной в центре.
Саркома Капоши — многоочаговая сосудистая опухоль, поражающая кожу, слизистые оболочки и внутренние органы. Развитие саркомы Капоши связывают с вирусом герпеса человека 8-го типа, который впервые обнаружили в коже больного с этой опухолью. В отличие от эндемического и классического вариантов заболевания, эпидемическую форму саркомы регистрируют только у ВИЧ-инфицированных пациентов (преимущественно у гомосексуалистов). В патогенезе саркомы Капоши ведущую роль отводят не злокачественному перерождению клеток, а нарушению продукции цитокинов, контролирующих клеточную пролиферацию. Инвазивный рост для данной опухоли нехарактерен.
При гистологическом исследовании саркомы Капоши обнаруживают усиленную пролиферацию веретенообразных клеток, сходных с эндотелиальными и гладкомышечными клетками сосудов. Саркома у ВИЧ-инфицированных пациентов протекает неодинаково. У одних больных диагностируют лёгкую форму заболевания, у других — более тяжёлую. Клинические признаки саркомы Капоши разнообразны. Чаще всего развиваются поражения кожи, лимфатических узлов, органов пищеварительной системы и лёгких. Разрастание опухоли может приводить к лимфатическому отёку окружающих тканей. В 80% случаев поражение внутренних органов сочетается с вовлечением в патологический процесс кожи. На начальных стадиях заболевания на коже или слизистой оболочке формируются небольшие возвышающиеся красно-лиловые узлы, нередко возникающие на месте травмы. Вокруг узловых элементов иногда обнаруживают мелкие тёмные пятна или желтоватый ободок (напоминают синяки). Диагноз саркомы Капоши ставят с учётом гистологических данных. При биопсии поражённых участков отмечают пролиферацию веретенообразных клеток, диапедез эритроцитов; обнаруживают содержащие гемосидерин макрофаги, а также воспалительные инфильтраты. Одышка — первый признак поражения лёгких при саркоме Капоши. иногда наблюдают кровохарканье. На рентгенограммах грудной клетки определяют двусторонние затемнения в нижних долях лёгких, сливающиеся с границами средостения и контуром диафрагмы; нередко обнаруживают увеличение прикорневых лимфатических узлов. Саркому Капоши следует дифференцировать с лимфомами и микобактериальной инфекцией, протекающей с поражением кожи. У 50% больных диагностируют поражение органов пищеварительной системы, а в тяжёлых случаях возникает кишечная непроходимость или кровотечение. Вовлечение в патологический процесс жёлчных путей приводит к развитию механической желтухи.
Смерть больных ВИЧ-инфекцией наступает либо от прогрессирования вторичных заболеваний, либо от любых других сопутствующих заболеваний, не связанных с ВИЧ. Генерализованный туберкулёз — основная причина гибели больных СПИДом. Кроме того, причиной смерти считают лёгочную патологию (с последующим развитием дыхательной недостаточности) и манифестную цитомегаловирусную инфекцию. В последнее время регистрируют увеличение летальности вследствие цирроза печени, обусловленного развитием вирусного гепатита С на фоне хронической алкогольной интоксикации. Прогрессирование хронического гепатита в цирроз у таких пациентов происходит в течение 2-3 лет.
источник
Абсцесс легкого – это неспецифическое воспаление легочной ткани, в результате которого происходит расплавление с образованием гнойно-некротических полостей. В период формирования гнойника отмечается лихорадка, торакалгии, сухой кашель, интоксикация; в период вскрытия абсцесса — кашель с обильным отхождением гнойной мокроты. Диагноз выставляется на основании совокупности клинических, лабораторных данных, рентгенологической картины. Лечение подразумевает проведение массивной противомикробной терапии, инфузионно-трансфузионной терапии, серии санационных бронхоскопий. Хирургическая тактика может включать дренирование абсцесса или резекцию легких.
Абсцесс легкого входит в группу «инфекционных деструкций легких», или «деструктивных пневмонитов». Среди всех нагноительных процессов в легких на долю абсцесса приходится 25-40%. Абсцессы легочной ткани в 3-4 раза чаще регистрируются у мужчин. Типичный портрет пациента — мужчина среднего возраста (40-50 лет), социально неустроенный, злоупотребляющий алкоголем, с длительным стажем курильщика. Более половины абсцессов образуется в верхней доле правого легкого. Актуальность проблематики в современной пульмонологии обусловлена высокой частотой неудовлетворительных исходов.
Возбудители проникают в полость легкого бронхогенным путем. Золотистый стафилококк, грамотрицательные аэробные бактерии и неспорообразующие анаэробные микроорганизмы являются наиболее распространенной причиной абсцесса легких. При наличии воспалительных процессов в полости рта и носоглотке (пародонтоз, тонзиллит, гингивит и др.) вероятность инфицирования легочной ткани возрастает. Аспирация рвотными массами, например, в бессознательном состоянии или в состоянии алкогольного опьянения, аспирация инородными телами тоже может стать причиной абсцесса легких.
Варианты заражения гематогенным путем, когда инфекция попадает в легочные капилляры при бактериемии (сепсисе) встречаются редко. Вторичное бронхогенное инфицирование возможно при инфаркте легкого, который происходит из-за эмболии одной из ветвей легочной артерии. Во время военных действий и террористических актов абсцесс легкого может образоваться вследствие прямого повреждения или ранения грудной клетки.
В группу риска входят люди с заболеваниями, при которых возрастает вероятность гнойного воспаления, например больные сахарным диабетом. При бронхоэктатической болезни появляется вероятность аспирации зараженной мокротой. При хроническом алкоголизме возможна аспирация рвотными массами, химически-агрессивная среда которых так же может спровоцировать абсцесс легкого.
Начальная стадия характеризуется ограниченной воспалительной инфильтрацией легочной ткани. Затем происходит гнойное расплавление инфильтрата от центра к периферии, в результате чего и возникает полость. Постепенно инфильтрация вокруг полости исчезает, а сама полость выстилается грануляционной тканью, в случае благоприятного течения абсцесса легкого происходит облитерация полости с образованием участка пневмосклероза. Если же в результате инфекционного процесса формируется полость с фиброзными стенками, то в ней гнойный процесс может самоподдерживаться неопределенно длительный период времени (хронический абсцесс легкого).
По этиологии абсцессы легких классифицируют в зависимости от возбудителя на пневмококковые, стафилококковые, коллибациллярные, анаэробные и пр. Патогенетическая классификация основана на том, каким образом произошло заражение (бронхогенным, гематогенным, травматическим и другими путями). По расположению в легочной ткани абсцессы бывают центральными и периферическими, кроме того они могут быть единичными и множественными, располагаться в одном легком или быть двусторонним. Некоторые авторы придерживаются мнения, что гангрена легкого — это следующая стадия абсцесса. По происхождению выделяют:
- Первичные абсцессы. Развиваются при отсутствии фоновой патологии у ранее здоровых лиц.
- Вторичные абсцессы. Формируются у лиц с иммуносупрессией (ВИЧ-инфицированных, перенесших трансплантацию органов).
Болезнь протекает в два периода: период формирования абсцесса и период вскрытия гнойной полости. В период образования гнойной полости отмечаются боли в области грудной клетки, усиливающиеся при дыхании и кашле, лихорадка, порой гектического типа, сухой кашель, одышка, подъем температуры. Но в некоторых случаях клинические проявления могут быть слабо выраженными, например, при алкоголизме болей практически не наблюдается, а температура редко поднимается до субфебрильной. С развитием болезни нарастают симптомы интоксикации: головная боль, потеря аппетита, тошнота, общая слабость. Первый период абсцесса легкого в среднем продолжается 7-10 дней, но возможно затяжное течение до 2-3 недель или же наоборот, развитие гнойной полости носит стремительный характер и тогда через 2-3 дня начинается второй период болезни.
Во время второго периода абсцесса легкого происходит вскрытие полости и отток гнойного содержимого через бронх. Внезапно, на фоне лихорадки, кашель становится влажным, и откашливание мокроты происходит «полным ртом». За сутки отходит до 1 литра и более гнойной мокроты, количество которой зависит от объема полости. Симптомы лихорадки и интоксикации после отхождения мокроты начинают снижаться, самочувствие пациента улучшается, анализы крови так же подтверждают угасание инфекционного процесса. Но четкое разделение между периодами наблюдается не всегда, если дренирующий бронх небольшого диаметра, то отхождение мокроты может быть умеренным.
Если причиной абсцесса легкого является гнилостная микрофлора, то из-за зловонного запаха мокроты, пребывание пациента в общей палате невозможно. После длительного стояния в емкости происходит расслоение мокроты: нижний густой и плотный слой сероватого цвета с крошковидным тканевым детритом, средний слой состоит из жидкой гнойной мокроты и содержит большое количество слюны, а в верхних слоях находится пенистая серозная жидкость.
Если в процесс вовлекается плевральная полость и плевра, то абсцесс осложняется гнойным плевритом и пиопневмотораксом, при гнойном расплавлении стенок сосудов возникает легочное кровотечение. Также возможно распространение инфекции, с поражением здорового легкого и с образованием множественных абсцессов, а в случае распространения инфекции гематогенным путем – образование абсцессов в других органах и тканях, то есть генерализация инфекции и бактериемический шок. Примерно в 20% случаев острый гнойный процесс трансформируется в хронический.
При визуальном осмотре, часть грудной клетки с пораженным легким отстает во время дыхания, или же, если абсцесс легких носит двусторонний характер, движение грудной клетки асимметрично. В крови ярко выраженный лейкоцитоз, палочкоядерный сдвиг лейкоцитарной формулы, токсичная зернистость нейтрофилов, повышенный уровень СОЭ. Во второй фазе абсцесса легкого анализы крови постепенно улучшаются. Если процесс хронизируется, то в уровень СОЭ увеличивается, но остается относительно стабильным, так же присутствуют признаки анемии. Биохимические показатели крови изменяются – увеличивается количество сиаловых кислот, фибрина, серомукоида, гаптоглобинов и α2- и у-глобулинов; о хронизации процесса говорит снижение альбуминов в крови. В общем анализе мочи – цилиндрурия, микрогематурия и альбуминурия, степень выраженности изменений зависит от тяжести течения абсцесса легкого.
Проводят общий анализ мокроты на присутствие эластических волокон, атипичных клеток, микобактерий туберкулеза, гематоидина и жирных кислот. Бактериоскопию с последующим бакпосевом мокроты выполняют для выявления возбудителя и определения его чувствительности к антибактериальным препаратам. Рентгенография легких является наиболее достоверным исследованием для постановки диагноза, а так же для дифференциации абсцесса от других бронхолегочных заболеваний. В сложных диагностических случаях проводят КТ или МРТ легких. ЭКГ, спирография и бронхоскопия назначаются для подтверждения или исключения осложнений абсцесса легкого. При подозрении на развитие плеврита осуществляется плевральная пункция.
Тяжесть течения заболевания определяет тактику его терапии. Возможно как хирургическое, так и консервативное лечение. В любом случае оно проводится в стационаре, в условиях специализированного отделения пульмонологии. Консервативная терапия включает в себя соблюдение постельного режима, придание пациенту дренирующего положения несколько раз в день на 10-30 минут для улучшения оттока мокроты. Антибактериальная терапия назначается незамедлительно, после определения чувствительности микроорганизмов возможна коррекция антибиотикотерапии. Для реактивации иммунной системы проводят аутогемотрансфузию и переливание компонентов крови. Антистафилакокковый и гамма-глобулин назначается по показаниям.
Если естественного дренирования не достаточно, то проводят бронхоскопию с активной аспирацией полостей и с промыванием их растворами антисептиков (бронхоальвеолярный лаваж). Возможно также введение антибиотиков непосредственно в полость абсцесса легкого. Если абсцесс расположен периферически и имеет большой размер, то прибегают к трансторакальной пункции. Когда же консервативное лечение абсцесса легкого малоэффективно, а также в случаях осложнений показана резекция легкого.
Благоприятное течение абсцесса легкого идет с постепенным рассасыванием инфильтрации вокруг гнойной полости; полость теряет свои правильные округлые очертания и перестает определяться. Если процесс не принимает затяжной или осложненный характер, то выздоровление наступает через 6-8 недель. Летальность при абсцессе легкого достаточно высока и на сегодняшний день составляет 5-10%. Специфической профилактики абсцесса легкого нет. Неспецифической профилактикой является своевременное лечение пневмоний и бронхитов, санация очагов хронической инфекции и предупреждение аспирации дыхательных путей. Так же важным аспектом в снижении уровня заболеваемости является борьба с алкоголизмом.
источник
S. aureusу больных с ВИЧ-инфекцией заселяет преимущественно области крупных складок кожи (подмышечные впадины, промежность) и слизистую носа.
К провоцирующим факторам развития пиококковой инфекции относят: наличие мелких травм кожи (возникают при бритье, эпиляции), ссадин; повышенную мацерацию кожи (при применении окклюзионных повязок, использовании лейкопластыря, под протезом); пренебрежение правилами личной гигиены; переохлаждение и перегревание организма, отрицательно влияющие на обменные процессы кожи; нерациональное применение кортикостероидных мазей, антибиотиков. В роли провоцирующего фактора также могут выступать такие климатические условия, как жаркий и влажный климат.
Все эти причины в условиях иммунодефицитного состояния приводят к тому, что пиодермии возникают значительно легче и быстрее.
Поражения кожи при стафилококковой инфекции могут иметь несколько клинических форм. Клинические проявления остиофолликулита, фолликулита, фурункула, фурункулеза описаны выше (см. раздел 16.1.4.1). Как правило, у больных ВИЧ-инфекцией на участках пораженной кожи длительно сохраняется эритема, имеющая синюшно-красную окраску, или остаются мелкие рубчики, часто отмечается абсце-дирование фурункулов.
Вульгарный сикоз — хроническое рецидивирующее воспаление фолликулов в зоне роста коротких толстых волос (борода, усы, брови, лобок, аксиллярные ямки). У больных ВИЧ-инфекцией процесс носит выраженный агрессивный характер и необычайную стойкость к лечению.
Карбункул — острое гнойно-некротическое воспаление нескольких волосяных фолликулов с образованием сливного воспалительного инфильтрата, локализованного в дерме и подкожной жировой клетчатке, и нескольких гнойно-некротических стержней.
На фоне ВИЧ-инфекции карбункулы могут носить множественный характер, а также приводить к развитию тромбофлебита лицевых вен, сепсису.
Вульгарное импетиго относится к смешанным стрептостафилодермиям, цра котором в 80% случаев выделяется стафилококк преимущественно фагогруппы Ц, фаготипа71.
На фоне ВИЧ-инфекции клиническая картина вульгарного импетиго характеризуется образованием везикул и пузырей, локализующихся в паховой и подмышечной областях. Элементы заполнены желтой, прозрачной или слегка мутной жидкостью, по периферии их иногда имеется красный венчик. Лопнувшие пузыри спадаются или вскрываются с образованием поверхностных красных мокнущих эрозий.
Абсцесс — ограниченное скопление гноя в тканях, сопровождающееся некрозом. Чаще всего причиной абцессов является S. aureus, хотя на фоне ВИЧ-инфекции в роли этиологического фактора может выступать и любой другой микроорганизм. Глубина поражения различна вплоть до подкожной жировой клетчатки, мышц.
Возникает болезненный узел ярко-красного цвета. Через несколько днер, недель в центре происходит расплавление тканей и образуется полость с гнойным содержимым. Для сформировавшегося абсцесса характерна флюктуация.
Абсцесс является исходом фурункула, карбункула и других форм пиодермии, так как при ВИЧ-инфекции они приобретают деструктивный характер и воспаление «уходит» в глубьлежащие ткани.
Синдром «ошпаренной кожи» [син.: болезнь Риттера, дерматит эксфоллиатив-ный] — тяжелая инфекция, возбудителем которой является золотистый стафилококк (фагогруппа II, фаготип 71). Заболевание характерно для детей, но при ВИЧ-инфекции может наблюдаться и среди взрослого контингента.
Клиническая картина связана с продукцией S. aureusэксфолиативного токсина, который образуется в первичном очаге инфекции (например, инфекция носоглотки). В большинстве случаев заболевание начинается с резкого подъема температу ры, ухудшения общего самочувствия. На следующий день на коже вокруг естест
венных отверстий на лице, шее, подмышечных впадинах, в паховой области, затем и на любом участке кожного покрова, появляется крупная пятнистая сыпь, переходящая в сливную эритему; дряблые пузыри заполнены прозрачным содержимым при вскрытии которых образуются влажные эрозии красного цвета (имеют вид о
паренной кожи). Эрозии сливаются, занимая обширные поверхности. Выявляя положительный симптом Никольского как в области высыпаний, так и на неизмененной коже.
Диагноз стафилококковой инфекции ставится на основании клинической картины и дополнительных микробиологических методов исследования.
источник
Пневмония при ВИЧ возникает в 60-75% случаев. Это заболевание настолько опасно, что может стать причиной летального исхода пациента. В данном случае важно своевременное реагирование и начало лечения.
Пневмония при ВИЧ уже сама по себе определяется болезнетворным состоянием организма. Ослабленная иммунная система становится причиной высокого риска возникновения воспалительных процессов, так как пациента окружают живущие в естественной среде патогенные микроорганизмы. Если для здорового человека они не всегда представляют опасность, то для ВИЧ-инфицированного лица встреча с ними чаще всего заканчивается развитием болезни. Пневмония в данном случае возникает при попадании в организм бактерий Pneumocystis carinii, которые как раз таки обитают в воздухе в достаточно большом количестве.
На быстрое развитие воспаления легких при ВИЧ могут оказать влияние следующие факторы:
- Вирусные заболевания. Например, ветрянка, ОРВИ;
- Инфекции, вызванные пневмококками, синегнойной и гемофильной палочкой;
- Аллергические реакции;
- Грипп.
На самом деле множество иных патологических состояний могут стать толчком к развитию пневмонии у больного, зараженного ВИЧ, поэтому это достаточно частое явление. В некоторых случаях пневмоцистоз может стать признаком, благодаря которому у пациента обнаруживается ранее не выявленный вирус иммунодефицита.
Еще несколько десятков лет назад пневмоцистная пневмония при ВИЧ уносила жизни более чем 60% людей, которые с ней сталкивались. Современные способы диагностики и лечения позволили снизить этот показатель до 10-25%.

Симптоматика, вызванная проявлением заболевания, выглядит следующим образом:
- Наличие инкубационного периода. Его продолжительность может варьироваться от 7 до 28 дней;
- Одышка. Характеризуется нарастающим эффектом. Если в начале болезни она возникает только при каких-либо физических нагрузках, то впоследствии она наблюдается даже в спокойном состоянии;
- Повышенная температура. Причем она не всегда достигает очень высоких показателей;
- Непродуктивный кашель, часто обладающий приступообразным характером;
- Возможны жесткое дыхание и прослушиваемые сухие хрипы;
- Признаки лихорадки;
- В некоторых случаях изо рта может выделяться слизь, больше похожая на пену.
Как видно, признаки воспаления легких при ВИЧ не сильно отличаются от проявления иных заболеваний дыхательных путей, в том числе обычного ОРВИ. Все это затрудняет выявление патологического процесса на ранних стадиях.
Диагностика пневмонии при ВИЧ инфекции включает в себя следующие процедуры:
- Физикальный осмотр. Врачом могут быть обнаружены хрипы или измененное дыхание, но не во всех случаях;
- Рентгенография. Демонстрирует изменения в легких в виде затемненных пятен на снимке. В 30% случаев данный метод не может диагностировать болезнь на ранней стадии;
- Анализ крови. Позволяет выявить повышенное количество лейкоцитов и тромбоцитов, а также признаки анемии;
- Бронхоальвеолярный лаваж. Позволяет получить материал в виде мокроты и жидкости для дальнейшего его лабораторного исследования на предмет наличия патогенных микроорганизмов.
Помимо перечисленных методов подтверждения инфицирования, могут применяться полимеразная цепная реакция, трансбронхиональная биопсия, иммунофлюоресцентная диагностика.
Такие методы, как обследования мокроты позволяют не только диагностировать пневмонию, но и определить антибиотики, которые имеют устойчивость к патогенным возбудителям.
Лечебная терапия пневмонии при ВИЧ определяется врачом индивидуально в каждом случае. Категорически запрещается самолечение, поскольку оно может привести не только к ухудшению состояния больного, но и к его возможному летальному исходу. Легко вылечить пневмонию при вирусе иммунодефицита, к сожалению, не всегда получается. Болезнь требует внимательного подхода и правильно подобранных препаратов.

Возможные способы лечения:
- Ко-тримоксазол. Он представляет собой сочетание Триметоприма и сульфометаксозола. Курс обычно продолжается 3 недели. При осложненном варианте болезни способ ввода препарата может быть назначен внутривенным, в иных случаях допускается использование таблеток при условии 3-4-разовом приеме в сутки. Побочными эффектами могут быть: сыпь, нарушение работы печени, проявления лихорадки;
- Пентамидин. Данное средство вводится только паренторально, а именно внутримышечно или внутривенно. Среди возможных побочных эффектов отмечаются: дисфункция почек, артериальная гипотония, нейтропения;
- Комбинация Клиндамицина и Примахина. Лечение может привести к кожной сыпи или поносу;
- Атоваквон. Не самый сильный препарат, но в то же время он имеет меньшее количество побочных эффектов в сравнении с иными лекарственными средствами;
- Триметрексат. Такое лечение оправдано при осложненном течении болезни, когда иные препараты не оказали положительного результата. Данное лечебное средство вводится в виде внутривенной инфузии.
Лечение пневмоцистной пневмонии может быть дополнено применением глюкокортикоидов. Они необходимы при среднетяжелом и тяжелом характере болезни, так как способны противостоять возникновению дыхательной недостаточности, которая может стать причиной смерти пациента.
Как было указано выше, современные способы лечения пневмонии в купе с антиретровирусной терапией заболевания иммунодефицита дают достаточно положительный прогноз, так как позволяют снизить риск летального исхода практически до 10-25%. В случае поздней диагностики пневмонии данный риск увеличивается до 40%. При полном отсутствии лечения или его неправильном осуществлении прогноз совсем неутешительный, болезнь не проходит самостоятельно, а ее результатом становится смерть пациента.
Конечно, редко болезнь проходит без тех или иных последствий для организма. Среди возможных осложнений на фоне пневмоцисткой пневмонии можно выделить следующие явления:
- Острый плеврит;
- Серьезное нарушение процесса газообмена;
- Признаки гипоксии;
- Абсцесс легкого.
Среди симптоматических признаков чаще всего имеют место:
- Аллергические реакции, выражаемые, как правило, в кожных высыпаниях;
- Нарушения работы желудочно-кишечного тракта. Это могут быть понос, запор, тошнота и прочие проявления.

В случае если болезнь возникает повторно, то на благоприятный исход могут надеяться только 40% пациентов. Такой низкий процент обуславливается частым развитием сильных побочных явлений на фоне приема лечебных препаратов при рецидиве.
Осуществлять профилактику воспаления легких при пневмонии достаточно сложно. Но пациентам все же рекомендуется вести максимально возможный здоровый образ жизни, придерживаться правильного сбалансированного питания, заниматься допустимыми видами спорта. Очень важно соблюдать все предписания врача в рамках лечебной терапии против ВИЧ.
источник
Абсцесс легкого определяется, как некроз легочной ткани с образованием полостей, содержащих некротические остатки тканей и жидкость – продукты жизнедеятельности микробной инфекции. Формирование многочисленных мелких (менее 2 см) абсцессов иногда называют некротической пневмонией или гангреной легких.
Обе этих патологии имеют весьма сходное проявление и патогенетическую картину. Отсутствие своевременного диагноза и лечения абсцесса легких связано с неблагоприятным клиническим исходом, чаще всего – смертью пациента.
Что это такое? Основной причиной абсцесс легкого является ситуация, при которой легочная ткань полностью теряет кислород. Больные очаговой пневмонией находятся в группе риска. Гнойно-некротические процессы в легочных тканях могут возникнуть по причине попадания в полости верхних дыхательных путей инородных тел, рвотных масс. Посторонние предметы, попадая в легкие, полностью закрывают бронх, препятствуя поступлению к нему воздуха в должном количестве. Именно в таком пространстве быстро развиваются гнойники.
Абсцесс легкого может стать последствием перенесенной бронхоэктатической болезни, сниженного иммунитета. Эти причины достаточно существенные для развития заболевания и возникновения последующих рецидивов. Гнойный воспалительный процесс может возникнуть, когда в кровеносную систему попадают определенные микробы из уже существующих очагов воспаления.
Абсцесс легкого может быть вызван болезненной микрофлорой у людей, страдающих воспалением десен. Болезнетворные бактерии из полости рта попадают в дыхательные пути, что провоцирует скоротечное развитие инфекции и воспаление легочных тканей. В дальнейшем без надлежащего осмотра врача и приема лекарств некроз прогрессирует и приводит к образованию абсцесса.
Абсцесс лёгкого в острой форме по статистике чаще поражает сильный пол в возрасте 20-50 лет. Правое лёгкое, из-за его больших параметров, воспаляется чаще. При этом абсцессы возникают в разных частях органа, хотя верхняя доля лёгких подвержена болезни сильнее.
Симптомы заболевания выявляемые в 1 период:
- Боль со стороны пораженного легкого, усиливающаяся в момент глубокого вдоха и при кашле.
- Сухой кашель.
- Увеличение частоты дыхания до 30 дыхательных движений в минуту и более.
- Повышение температуры до 39 °C и выше.
- Головная боль.
- Резкое снижение аппетита.
- Тошнота.
- Общая слабость.
Симптоматика, появляющиеся во 2 период:
- Влажный кашель.
- Выделение мокроты при кашле «полным ртом».
- Зловонный запах отделяемого (если инфекционным агентом выступила гнилостная микрофлора).
- От 1000 мл и более гнойного отделяемого в сутки (чем больше полостной процесс, тем выше объем отделяемого).
- Уменьшение температуры тела и общей интоксикации.
В зависимости от хода развития болезни и возможностей рецидива принято делить абсцесс на хронический и острый.
В случае когда гной прорвало в бронхи, но при этом инфекционный процесс получилось остановить, то у человека наступает стадия выздоровления. Если же больной не обратился за медицинской помощью, то его состояние значительно ухудшается и наступают осложнения абсцесса. Они выражены в виде:
- болевого шока;
- сепсиса;
- эмпиемы плевры;
- воспалительно-некротического очага;
- пиопневмотораксе;
- легочном кровотечении.
Как правило, именно легочное кровотечение является наиболее распространенным осложнением абсцесса легкого.
Возникает в том случае, если острый процесс не завершается за 2 месяца. Этому способствуют особенности самого абсцесса – большие размеры (больше 6 см в диаметре), плохой дренаж мокроты, локализация очага в нижней части легкого; ослабление организма – нарушение в работе иммунитета, хронические заболевания и так далее; ошибки при лечении острого абсцесса – неправильно подобранный антибиотик или слишком маленькие дозы, поздно начатое или недостаточное лечение.
При хроническом абсцессе больного мучают одышка, кашель с отделением зловонной мокроты, чередование ухудшения и нормализации состояния, повышенная утомляемость, слабость, истощение, потливость. Постепенно, из-за нехватки кислорода и постоянной интоксикации организма, развивается бронхоэктазия, пневмосклероз, эмфизема легких, дыхательная недостаточность и другие осложнения. Меняется внешний вид больного – грудная клетка увеличивается в размерах, кожные покровы бледные, цианотичные, конечные фаланги пальцев утолщаются, приобретают вид «барабанных палочек».
Диагноз ставится по результатам обследования пациента. Существует несколько методов проведения обследования больного. Одним из них является пальпация больного участка. При этом обнаруживается болезненность.
- При проведении рентгена и на КТ можно увидеть образование воспалительного инфильтрата, который характеризуется гомогенным затемнением. Если абсцесс прорывается в область бронхиального дерева, то обнаруживается гнойная мокрота в большом количестве, которая имеет неприятный запах, иногда имеется примесь крови.
- Чаще всего при прорыве абсцесса наблюдается облегчение состояния пациента, температура начинает понижаться. При этом на рентгене можно увидеть, что в легких образуется просветление. Большое значение имеет состояние пациента, развитие заболевания, а также данные, которые были получены в результате лабораторных, функциональных, иммунологических и рентгенологических исследований.
- Хронический абсцесс легкого очень часто имеет схожие симптомы с гангреной легких, поэтому различить их бывает достаточно сложно. Поэтому чаще всего диагноз ставится после проведения рентгенологического обследования. Большое значение имеет проведение КТ, которая позволяет определить степень поражения легочной ткани. Кроме того, при подозрении на полостные формы онкологии, необходимо пройти пункционную биопсию.
Абсцесс правого легкого нередко напоминает туберкулез.
В таком случае для уточнения необходимо сдать мокроту на посев палочки, а также иммунологическое обследование. Существуют похожие симптомы с эмфиземой и пневмотораксом, нагноившимися легочными кистами.
При возникновении абсцесса легкого начало лечения зависит от его причины, характера течения (острый, хронический), микроорганизма-возбудителя и его чувствительности к антибиотикам, наличия сопутствующих легочных заболеваний.
- Стандартно лечение начинают с назначения пенициллина по 500000—1000000 ЕД лучше внутривенно 6—8 раз в день (до 8000000—10000000 ЕД в сутки). При отсутствии эффекта после определения чувствительности бактериальной флоры к антибиотикам назначают наиболее эффективный препарат. Лечебный эффект могут дать морфоциклин, эритромицин, метициллин, левомицетин, сигмамицин, олеадомицин и другие антибиотики.
- Весьма эффективной бывает бронхоскопия с отсасыванием гнойного содержимого абсцесса и последующим введением в полость антибиотика, подобранного согласно антибиотикограмме. При этом пенициллин вводят по 300 000—800 000 ЕД каждые 2—3 дня (всего 15 введений), стрептомицин — по 500000 ЕД.
- Нередко бывает высокоэффективной комбинация антибиотиков с сульфаниламидами (сульфадиметоксин по 1 г в день, норсульфазол или сульфадимезин — по 1 г 6—8 раз в день). Назначают отхаркивающие средства. Большое значение имеет обеспечение дренажа, для чего больному (в зависимости от локализации абсцесса) придают определенное положение.
- При множественных двусторонних или центрально расположенных абсцессах, а также абсцессах, осложненных кровотечением, наряду с другими методами лечения применяют инфузию антибиотиков в легочную артерию. В качестве основы для приготовления смеси лекарственных препаратов обычно используют раствор хлорида натрия (1 л), в котором растворяют суточную дозу одного из антибиотиков, 5000—10000 ЕД гепарина, 1000 мг витамина С, 25— 30 мг гидрокортизона. Раствор вводят капельно непрерывно со скоростью 12—15 капель в минуту.
- Необходима общеукрепляющая терапия: повторные переливания крови (по 100—200 мл каждые 4—5 дней), витамины А, С, О и группы В, высококалорийная диета (3000—4000 калорий) с высоким содержанием белка.
Если в течение 1 1/2 — 2 мес консервативная терапия не дает эффекта, больного направляют на операцию.
Хирургическое лечение абсцесса легкого осуществляется несколькими методами:
- Путем дренирования абсцесса (торакоцентез, торакотомия и пневмотомия).
- С помощью резекции легкого.
Оно направлено на быстрое и максимально полное удаление гноя и омертвевших участков ткани легкого.
Специфической профилактики абсцесса легкого нет. Неспецифической профилактикой является своевременное лечение пневмоний и бронхитов, санация очагов хронической инфекции и предупреждение аспирации дыхательных путей.
Так же важным аспектом в снижении уровня заболеваемости является борьба с алкоголизмом.
источник
ВИЧ-инфекция сама по себе человека не убивает, а разрушает его иммунитет своего носителя, открывая его для всех остальных микроорганизмов.
Пневмония – смертельно опасное поражение лёгких какой-либо инфекцией. Является одним из самых распространённых заболеваний при ВИЧ-инфекции. Собственно, благодаря ей ВИЧ и СПИД впервые и были обнаружены, так как врачей смутило скоропостижное поражение дыхательной системы практически безвредными организмами отдельных, с виду абсолютно здоровых людей, которое не поддавалось лечению.
Процент поражения пневмонией у ВИЧ-инфицированных составляет 80% всего числа больных. Это обусловлено тем, что при вирусе иммунодефицита больные не способны справляться даже с практически непатогенной микрофлорой, попадающей в организм через кровь, пищеварительную систему, систему дыхания и кожу.
Заболевания кожи довольно легко исцеляются как быстрой регенерации кожного покрова, так и при помощи препаратов местного применения и очень редко проникают внутрь. Получить ещё что-то через кровь ВИЧ-инфицированные тоже умудряются довольно редко, так как теперь им приходится очень внимательно следить за целостностью своего кожного покрова и, получив горький опыт, вести аккуратный образ жизни. Пищеварительная система имеет помимо иммунитета свои защитные механизмы в виде слюны, убивающей безобидные бактерии и желудочного сока, эффективно растворяющего практически всё без участия иммунных клеток.
Легкие же являются своеобразным фильтром воздуха окружающей человека атмосферы, который содержит в себе миллиарды различных пылинок, микроорганизмов и вирусов. Их защита целиком и полностью возложена на иммунные клетки, в большом количестве находящиеся в постоянно циркулирующей в них крови, без каких-либо дополнительных инструментов. При поломке естественного иммунитета, лёгкие становятся доступны для любого воздействия и являются открытыми воротами в организм больного, что и объясняет такой огромный процент пневмонии при ВИЧ.
Пневмония – воспалительное поражение лёгочной ткани с большим отёком и иногда с гнойными абсцессами. Этот недуг может провоцироваться сильными аллергическими реакциями, гемофильной инфекцией, пневмококковыми бактериями, гриппом, простой ветрянкой и другими вирусами, а также такими тяжёлыми патогенными организмами, как синегнойная палочка и многими другими.
Однако, при всём разнообразии возбудителей, пневмония при ВИЧ почти всегда вызвана Pneumocystis carinii – безобиднейшим микроорганизмом, находящимся на промежуточной стадии между грибком и бактерией. Pneumocystis carinii – одноклеточный организм, официально причисленный после долгих споров в научных кругах к царству грибов, имеющий грибковую РНК и размножающийся спорообразованием, но, в отличие от грибка, он чувствителен к антибиотикам и имеет некоторые особенности поведения бактерий. Этот организм является условно патогенным и не причиняет вреда людям, в большом количестве находясь в воздухе и органах дыхательной системы.
При нормальном уровне иммунитета популяция возбудителей пневмоцистоза уравновешивается иммунными клетками, при ВИЧ же никто не мешает им свободно размножаться и использовать лёгкие как питательную среду.
ВИЧ и пневмония, вызванная Pneumocystis carinii, являются сопутствующими практически неразлучными заболеваниями. Эффективное лечение пневмонии при ВИЧ-инфекции было скоординировано сравнительно недавно. Ранее, до двухтысячных годов, для заболевших ВИЧ и пневмонией прогноз выносился неутешительный — довольно быстрый летальный исход 60-80% пациентов, вызванный острой дыхательной недостаточностью. Сейчас современное лечение пневмоцистоза позволяет значительно продлить жизнь больного и снизить летальность до 10-30% случаев.
Пневмоцистоз часто рассматривают как признак ВИЧ-инфекции, а иногда и вовсе её начальной стадией, так как это заболевание появляется в первую очередь после заражения.
При единовременном заболевании пневмонией и ВИЧ лечение требует приёма огромного количества препаратов. Сам пневмоцистоз в среднем длиться 21 день и если совместить два вида терапии, то эффект будет намного лучше, однако, совместное применение такого количества лекарств вызывает сильнейшую интоксикацию организма, поэтому в некоторых странах лечат сначала пневмоцистоз, а потом переходят на противовирусную терапию.
Симптоматика и течение пневмонии при ВИЧ такая же, как и у неинфицированного, однако, пневмоцистоз имеет ряд особенностей:
- Длительный инкубационный период от 7 до 28 дней.
- Способность протекать в виде ОРЗ, бронхита или ларингита
- Практически всегда хроническая форма с рецидивами.
- Во время скрытой болезни изо рта больного может выделяться белая слизистая пена.
- Длительная несильная лихорадка может послужить признаком пневмоцистоза.
Выявить это заболевание довольно сложно, так как оно может прогрессировать, выдавая себя лишь небольшим сухим кашлем в течение нескольких месяцев, а потом очень резко перейти в очень острую фазу.
Основой лечения пневмоцистоза ВИЧ-инфицированных пациентов заключается в первую очередь в подавлении вируса ВИЧ-инфекции и незначительном подъёме иммунитета, при котором возбудители недуга (цисты) очень быстро выселяются из организма. Специализированные же препараты (бактрим, бисептол, пентамидин и др.) направлены на прекращение их размножения.
Профилактика пневмоцистоза начинается с трёхмесячного возраста предполагаемого ВИЧ-инфицированного пациента и продолжается до конца жизни. До первого заболевания она заключается в пожизненном приёме раз в три дня бисептола после падения количества лимфоцитов до 300 шт на 1 мл крови, а после первого перенесённого пневмоцистоза – ежедневном приёме препарата.
Последствия пневмоцистоза могут быть представлены в виде острого плеврита или абсцесса лёгкого, но в основном они выражены очень сильным и резким нарушением газообмена и ярко выраженной гипоксией на фоне сильного токсического воздействия препаратов, которые, в свою очередь, могут вызвать как кожные реакции и реакции желудочно-кишечного тракта, так и острые аллергические реакции, являющиеся причиной одной из разновидностей пневмонии и способные сильно усугубить болезнь.
Самой главной профилактикой любого вида пневмонии будут правильный образ жизни и полноценное питание с занятиями спортом вместе с идеальнейшим соблюдением всех предписаний врача и назначенной им терапии против ВИЧ-инфекции поможет надолго отсрочить первое заболевание пневмонией и сделать промежутки между рецидивами как можно больше. Это очень важно не только для минимизации последствий болезни, но и для избежания или максимального оттягивания смертельного исхода.
источник
Абсцесс легкого – воспаление участка ткани самого органа, образованное из-за гнойного расплавления. В нем образуется заполненная этой жидкостью полость. При появлении первых признаков заболевания требуется срочный вызов терапевта на дом.
В роли возбудителя заболевания обычно выступают болезнетворные бактерии, особо часто — золотистый стафилококк. Заболевание может развиться на фоне общего снижения иммунитета и слабости организма в результате попадания в дыхательные пути и легкие различных инородных тел. В состоянии сильного опьянения или без сознания рвотные массы, слизь и другие вещества могут проникнуть в легкие, провоцируя развитие абсцесса. На фоне хронических заболеваний и инфекций, при длительном курсе приема антидепрессантов или глюкокортикоидов, при нарушении дренажа бронхов абсцесс легких развивается достаточно часто. Еще один способ заражения – гематогенный. В этом случае инфекция проникает в легкие при сепсисе. Такой путь заражения крайне редок. Вторичное инфицирование может произойти на фоне инфаркта легкого. Еще одна довольно часто встречающаяся причина заболевания – ранение в область груди.
Первый этап абсцесса отличается инфильтрацией ткани легкого на ограниченном участке. Потом гнойник расплавляется, постепенно образуя полость. На следующем этапе болезни инфильтрация по краям полости пропадает. Полость в это время покрывается грануляционной тканью. Если болезнь проходит в легкой форме, полость закрывается, а на ней образуется участок пневмосклероза. Если полость имеет фиброзные стенки, то внутри процессы образования гноя склонны к самоподдерживанию. В этом случае развивается хронический абсцесс легкого. Такой этап болезни более свойственен мужчинам, чем женщинам. При этом почти половина заболевших употребляли алкоголь в больших дозах.
2. Попадание какого-либо инородного тела в легкие или бронхи.
3. Инфекция миндалин и придаточных пазух.
4. Многочисленные абсцессы в анамнезе, возникающие на фоне септикопиемии.
5. Эмболы, проникающие в легкие из различных очагов заболеваний: простатита, онита; а при лимфогенном способе – из инфицированной полости рта, фурункулов с губ.
6. Распад раковой опухоли в легком или осложнение инфаркта легкого.
Признаки абсцесса легкого, как правило, не заставляют себя долго ждать. Заболевание развивается стремительно – больной чувствует боль в грудине, у него повышена температура, появляется озноб. Мокрота при абсцессе легкого выделяется через ротовую полость после прорыва бронха. Мокрота неприятно пахнет, могут быть вкрапления крови. При прослушивании ясно, что дыхание ослаблено, после прорыва оно становится бронхиальным с сопутствующими влажными хрипами. Образование тонкостенной кисты или пневмосклероза – подход к благоприятному завершению болезни. Его следует ждать примерно через 2 месяца после инфицирования. Может возникнуть хронический абсцесс легкого, причины этого кроются в неправильном лечении или его отсутствии.
Первый этап болезни длится около недели. Начало болезни может затянуться и до трех недель. Бывает, что гнойной полости на развитие нужно только 2 дня, такое начало заболевания считают стремительно быстрым.
Второй этап абсцесса характеризуется разрывом полости и ее гнойного содержимого. Развивается лихорадка, сухой кашель уступает место влажному отхаркивающему. Больной постоянно кашляет и отхаркивает гной в больших количествах. Количество гноя варьируется в зависимости от объема полости и может достигать 1 и более литра.
Завершающий этап заболевания характеризуется снижением симптомов интоксикации и лихорадки. Больной чувствует себя значительно лучше. Анализы крови, взятые на этом этапе, указывают на отступление инфекции.
Сложность состоит в том, что этапы заболевания четко разграничить возможно не всегда. В случае маленького размера дренирующего бронха мокрота не будет отходить большими объемами, как это должно быть. Хотя если собранная мокрота будет стоять какое-то время в стеклянной емкости, она расслоится. Верхний слой станет пенистым, средний – жидким, а нижний – густым и серым.
При привлечении плевры либо ее области к течению болезни могут возникнуть осложнения абсцесса. Осложнения болезни протекают на фоне гнойного плеврита. Легочное кровотечение может возникнуть в случае гнойного расплавления сосудистых стенок. Инфекция может беспроблемно распространиться на здоровые участки легкого, образуя многочисленные гнойные очаги. Возможен переход инфекции и на соседнее здоровое легкое. Если распространение инфекции происходит гематогенным способом, очаги абсцесса могут возникнуть на других органах, что может вызвать бактериемический шок и распространение болезни по всему организму. Абсцесс легкого приводит к летальному исходу в пяти процентах случаев из ста.
При первых признаках такого заболевания, как абсцесс легкого, диагностика проводится в полном объеме, необходимо сдать все анализы: кровь, мочу. В анализе крови врач увидит выраженный лейкоцитоз, повышение допустимого уровня СОЭ, токсичную зернистость нейтрофилов. Анализируемая кровь улучшается к началу второго этапа абсцесса. Когда болезнь переходит к хронической форме, заметно понижается уровень гемоглобина в крови. Изменяется биохимия крови: количество серомукоида, гаптоглобинов, фибрина растет, а количество альбумина в крови падает.
Анализ мочи покажет, как изменяются показатели альбуминурия и микрогематурия.
Для правильной постановки диагноза обязательно проводят анализ отделяемой мокроты. Ее проверяют на наличие жирных кислот, атипичных клеток, эластичных волокон, а также на наличие туберкулезных бактерий.
Возбудитель заболевания выявляется с помощью бактериоскопии мокроты. Затем выявляется чувствительность и реакция на антибиотики.
Самый верный и быстрый способ постановки данного диагноза – проведение рентгеноскопии легких. При затруднении диагностики выполняют МРТ легких, КТ легких, бронхоскопию и другие процедуры, предписанные врачом. При подозрении на плеврит обязательна пункция плевры.
Если по результатам анализов подтвердился абсцесс легкого, лечение производится незамедлительно. В зависимости от степени тяжести абсцесса врач назначает целесообразную терапию. Возможен консервативный либо хирургический путь лечения. Оба способа терапии ведутся в стационаре под наблюдением специалистов-пульмонологов.
Чтобы победить абсцесс легкого, лечение заболевания проводят консервативно, что подразумевает обязательный дренаж мокроты, т.е. больной несколько раз в сутки должен принимать положение, удобное для отхода мокроты. Соблюдение постельного режима необходимо для благоприятного исхода болезни. Как только лаборантом определена чувствительность микроорганизмов, врач назначает лечение антибиотиками. Назначается переливание необходимых компонентов донорской крови. В отдельных случаях пациенту переливается его собственная кровь, взятая заблаговременно. Данные процедуры назначаются с целью восстановления функций иммунной системы. Также лечащий врач принимает решение о целесообразности назначения больному глобулинов.
В отдельных случаях, когда естественный дренаж незначительно улучшает состояние больного и отход мокроты, ему назначается бронхоскопия с аспирацией полостей. Во время данной процедуры полость промывается и антисептически обрабатывается. В трудных случаях антибиотик вводится непосредственно в гнойную полость. Гнойный абсцесс легкого в 75-80 процентах случаев бывает одиночным и локализуется в сегментах правого легкого.
При отсутствии результатов консервативного лечения или возникновении опасных для жизни осложнений прибегают к хирургическому пути решения проблемы: врач удаляет часть больного легкого под наркозом.
Абсцесс и гангрена легкого являются наиболее частыми острыми нагноительными заболеваниями легких.
Профилактические меры в случае данного заболевания не всегда эффективны. Но следует знать о некоторых правилах:
— нужно вовремя лечить пневмонию, бронхит и другие заболевания органов дыхания;
— предупреждение попадания инородных тел в легкие и бронхи;
-своевременное лечение гнойных заболеваний, фурункулов на теле и особенно абсцессов в полости рта;
— не злоупотреблять алкогольными напитками.
Прогноз этого заболевания при правильном и своевременном лечении благоприятный. Часто абсцесс легкого со времен проходит: инфильтрация вокруг полости истончается. Со временем полость уже не определяется. В течение 8 недель заболевание проходит (если не затягивается или не переходит в хроническую форму).
В случае отсутствия должного лечения острый абсцесс легкого станет хроническим с соответствующими обострениями и ремиссиями. Данная нозологическая форма отличается формированием в пораженном органе некой полости, а вокруг нее происходит необратимый процесс изменения паренхимы и бронхиального дерева. Данные метаморфозы приобретают форму деформирующего бронхита, пролиферации соединительной ткани, а в будущем они могут перетечь в бронхоэктазы. Переход острой формы абсцесса легкого в хроническую наблюдается в 2,5–8% случаев.
Если подтверждается хронический абсцесс легкого, история болезни пациента начинается еще задолго до него. Хронические абсцессы возникают из-за тех же возбудителей, которые провоцируют острые нагноения в легких. К ним можно причислить стафилококк с преобладанием штаммов, имеющих устойчивость к большинству антибиотиков, самых современных в том числе. Есть также подобные, в плане устойчивости к медицинскому воздействию, микроорганизмы со значительной ролью в этиологии хронических абсцессов легких. Это такие грамотрицательные палочки, как протея, эшерихий, псевдомонад и пр. Микологическое исследование, имеющее четкую направленность, выявляет у большей доли больных наличие возбудителей глубоких микозов, которые выделяются из мокроты. Причем только выявив серологические маркеры активной грибковой инфекции, получается доказать их этиологическое значение. Данные условия делают этиотропную терапию хронических абсцессов нелегкой задачей.
Переход от острой формы легочного абсцесса к хронической обусловлен следующими основными факторами:
- в легком находится либо слишком большая деструкция (больше 5 см), либо их слишком много;
- процесс дренирования полости деструкции был неэффективен или прошел неадекватно, в связи с чем в окружающей паренхиме развилась соединительная ткань, а также сформировалась фиброзная капсула, которая впоследствии будет препятствовать уменьшению размеров полости;
- в полости абсцесса есть секвестры, которые загораживают устья дренирующих бронхов, а также постоянно поддерживают нагноение внутри полости и воспаление вокруг нее;
- консервативное лечение острого абсцесса легкого спровоцировало образование сухой остаточной полости, а также ее эпителизацию из устьев дренирующих легких;
- неспецифический характер резистентности организма и скомпрометированный иммунитет;
- в пораженных абсцессом сегментах легких образовались плевральные сращения, из-за чего не происходит ранний спад и облитерация полости.
Из-за хронической гипоксии и гнойной интоксикации, из-за дефицита негазообменных легочных функций и из-за сбоя в работе эндокринной, нервной и других регуляционных систем организма длительному хроническому нагноительному процессу сопутствуют разнообразные нарушения:
- компенсаторные и резервные возможности кровообращения снижаются;
- наблюдается легочная гипертензия;
- микроциркуляция в органах и тканях нарушается;
- приобретается вторичный иммунодефицит;
- происходят изменения в энергетическом и белковом обмене.
Хронический абсцесс легкого симптомы имеет следующие:
- постоянный кашель;
- боли в грудной клетке;
- длительное ощущение нехватки воздуха;
- хроническая гнойная интоксикация;
- возможны осложнения со стороны других органов и систем организма.
Сложно точно определить хронический абсцесс легкого, симптомы могут быть выражены в любой степени, это зависит от тяжести или стадии заболевания, фазы его течения (ремиссия или обострение), характера изменений легочной ткани, степени нарушения бронхиальной дренирующей функции. Примечательно, что за последние 20 лет методы лечения острых легочных нагноений усовершенствовались настолько, что частота переходов в хроническую форму существенно снизилась, к тому же их клинические проявления стали гораздо слабее.
Чаще всего хронический абсцесс легкого сопровождаются следующими осложнениями:
- легочное кровотечение;
- вторичные бронхоэктазии;
- сепсис.
Они в большинстве случаев проявляются при обострении болезни или ее длительном лечении. За последнее время амилоидоз паренхиматозных органов стал встречаться значительно реже.
Если диагностирован хронический абсцесс легкого, лечение происходит только путем хирургического вмешательства.
Консервативный метод лечения львиной доли больных состоит в предоперационной подготовке. Эти мероприятия могут стать даже единственным возможным путем лечения, если оперативное вмешательство невозможно по каким-либо причинам. Этому методу характерны следующие мероприятия:
- санация трахеобронхиального дерева и полости деструкции;
- купирование обострения гнойной деструкции;
- коррекция нарушенных функций организма для повышения его резервных возможностей, которые помогут противостоять хирургической агрессии.
Очень сложным и трудоемким является послеоперационное лечение людей, которые перенесли хронический абсцесс легкого. Такие больные требуют особого внимания, так как может возникнуть целая цепь взаимообусловленных осложнений после оперативного вмешательства. Послеоперационные осложнения у данной категории больных могут быть всевозможными:
- Общими: декомпенсация кровообращения, осложнения тромбоэмболического характера.
- Легочными и бронхоплевральными, такими как пневмония, плевральная эмпиема, бронхиальные свищи, несостоятельность культи бронха.
- Общехирургического характера: инфицирование послеоперационной раны, послеоперационное кровотечение.
В послеоперационный период, длящийся сутки–двое, главным образом необходимо обеспечить все условия для восстановления и поддержания главных жизнеобеспечивающих систем организма, ослабленных перенесенной болезнью и оперативным вмешательством. К ним относятся дыхательная система и система кровообращения. Когда дыхательный процесс стабилизировался, наладилась гемодинамика, пора переключать интенсивную терапию на профилактику инфекционных осложнений. Она должна сопровождаться терапией корригирующего и поддерживающего характера. Ранняя стадия послеоперационного периода считается удачно завершенной, если оперированное легкое расправилось, показатели крови нормализовались, а больной уже легко встает и ходит. Через большее время после операции, после проведения симптоматической терапии приступают к местному лечению и устранению осложнений, которые не удалось ликвидировать ранее. Вместе с этим дыхательная и кровеносная системы стабилизируются, а обменные процессы приходят в норму.
Хирургическое вмешательство у пациентов с хроническими абсцессами легких за последние несколько десятков лет стало показывать гораздо лучшие результаты. Но даже успешное хирургическое лечение легких не исключает летальных исходов. К сожалению, процент смертности пациентов данной категории по-прежнему высок и достигает 15%. Чаще всего больные гибнут из-за кровотечений, сердечной и дыхательной недостаточности, а также в связи с эмпиемой плевры. Анализируя статистику летальных исходов пациентов с хроническими абсцессами легких после резекций, можно сделать вывод о методах улучшения результатов лечения. Для этого нужно максимально тщательно готовить пациентов к операции, сделать технику оперативного вмешательства более совершенной, а также своевременно предупреждать и лечить развивающиеся послеоперационные осложнения.
источник