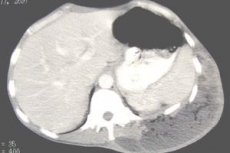
Ультразвуковое исследование брюшной полости является ведущим методом диагностики при панкреатите и вспомогательным при остальных перечисленных здесь патологиях.
Абсцесс — гнойное воспаление с образованием полости.
На УЗИ абсцесс — это ограниченное жидкостное образование, часто имеющее отчетливую стенку (капсулу); содержимое неоднородное, в виде эхогенной взвеси или нитевидных структур. Наличие газа сопровождается эффектом реверберации (процесс постепенного уменьшения интенсивности звука при его многократных отражениях).
Перфорация — прободение с выходом содержимого полого органа наружу. Прямой признак — пневмоперитонеум (свободный воздух в брюшной полости). Однако с помощью УЗИ его выявление затруднительно. Иногда свободный воздух обнаруживается под передней брюшной стенкой и вызывает патогномоничный (специфичный) эффект — реверберацию. В ряде случаев в брюшной полости определяется свободная жидкость.
Является признаком асцита (водянки) или острой абдоминальной патологии с вовлечением в процесс брюшины; в ряде случаев сопровождает закрытую травму органов брюшной полости. Места локации (присутствия) жидкости типичны: околопеченочное, околоселезеночное пространство, малый таз, правый и левый боковые каналы. Жидкость определяется в виде участков низкой эхогенности без четких контуров, изменяющих форму при перемене положения тела. На практике имеет значение количество свободной жидкости. На самом деле точное измерение затруднительно. Обычно используется приблизительное определение объема жидкости в месте наибольшего ее скопления.
- послеоперационное скопление жидкости (кровь, выпот),
- наличие внутрибрюшных абсцессов (межкишечных, поддиафрагмальных, подпеченочных, абсцессов дугласова пространства). УЗИ может подтвердить, но не исключает наличие абсцесса.
Перитонит — воспаление брюшины. Клинически проявляется выраженной болью в животе, мышечной защитой, отсутствием перистальтики. Имеет место лихорадка, озноб.
На УЗИ при перитоните определяются:
- расширение петель кишечника и заполнение их жидкостью,
- свободная жидкость в брюшной полости,
- утолщение стенок кишечника в связи с отеком,
- наличие межпетлевых или поддиафрагмальных абсцессов.
Острый панкреатит — воспаление поджелудочной железы. Сопровождается острой, мучительной болью в животе с иррадиацией в спину или левый бок; имеет место сильная рвота. Из лабораторных показателей специфичны резкое повышение уровня амилазы и липазы в крови.
На УЗИ в большинстве случаев поджелудочная железа увеличена, контур может быть нечетким. При отечной форме структура может оставаться нормальной. В случае деструктивного панкреатита отмечается неоднородность структуры, вплоть до жидкостных образований в самой железе или в проекции сальниковой сумки. Также определяется свободная жидкость в брюшной или плевральных полостях. В исходе формируются псевдокисты.
Роль УЗИ при остром панкреатите — установление его природы (билиарный, алиментарно-токсический) и степени тяжести, а также определение перипанкреальных изменений, наличия и объема жидкости при асцит-перитоните.
Характерных признаков нет. Клиническая картина варьирует от отсутствия симптомов до опоясывающих болей; в крови может быть повышение уровня амилазы, лейкоцитоз.
Ультразвуковая картина при повреждении поджелудочной железы:
- увеличение размеров части или всего органа.
В ряде случаев УЗИ неинформативно. В исходе тяжелых травм образуются посттравматические псевдокисты.
- Богданович Б. Б. (10-я городская клиническая больница г. Минска). «Использование ультразвукового исследования в экстренной абдоминальной хирургии».
источник
При эхографическом исследовании внутриорганные абсцес- , сы (печени и селезенки) лоцируются в виде образований ок- ¦’,lt; руглой формы с четким, неровным, как бы «рваным» внутрен-
А
¦ ‘ ч*
Рис. 4.1. Продольное сканирование через межре- берные промежутки справа. Абсцесс VII сегмента печени размером 5,5×3,5×3 см. Четкий неровный внутренний контур, анэхогенное содержимое. Зона перифокально- го воспаления повышенной эхогенности.
ним контуром, что особенно хорошо видно при увеличении масштаба (рис. 4.1).
Внутренняя структура и эхогенность содержимого во многом зависят от флоры и давности существования абсцессов.
В раннем периоде, на стадии инфильтрации, лоцируется зона без четких контуров пониженной эхогенности со смазанной внутренней структурой. В дальнейшем зона превращается в образование, четко отграничиваясь от здоровых тканей. Эхогенность понижается. Структура становится неоднородной за счет мелких жидкостных включений. Это соответствует II стадии формирования абсцесса, названной В.А.Быковским «стадией пресептических изменений» [Быковский В.А. и др., 1994]. На первых двух стадиях возможно обратное развитие процесса при адекватной общей и антибактериальной терапии.
Динамика развития абсцессов выглядит следующим образом: в стадии экссудации возникают выраженные деструктивные изменения, что проявляется еще большим снижением эхогенности, неоднородностью структуры за счет тяжистых включений средней эхогенности или зернистых — высокой эхогенности. Мелкие жидкостные анэхогенные включения проявляют тенденцию к слиянию. Степень неоднородности зависит от соотношения жидкостного компонента и тканевого детрита в полости абсцесса. По периферии очага наблюдается зона перифокального воспаления в виде ободка от 2 до 16 мм толщиной, пониженной или повышенной эхогенности.
При преобладании жидкого гноя в полости абсцесса можно проследить эффекты усиления задней стенки, краевого ослабления эхосигнала и дистального усиления, которые характерны для жидкостных образований. В случае преобладания детрита
Рис. 4.2. Косое сканирование из правого подреберья. Абсцесс VI сегмента печени размером 3,4x4x3,3 см в стадии деструктивных изменений.
анэхогенные компоненты в полости абсцесса могут не визуализироваться. В этом случае эхографическое отображение полости гнойника может напоминать структуру печеночной ткани (рис. 4.2).
Достоверных различий соотношения экссудат/тканевый детрит в зависимости от давности существования абсцесса в стадии деструктивных изменений нами отмечено не было. В некоторых случаях внутри крупных полостей формируются соединительнотканные перегородки, делающие абсцессы многокамерными (рис. 4.3).
Диагностика абсцессов паренхиматозных органов брюшной полости у детей в послеоперационном периоде сводится к обнаружению очаговых образований в печени или селезенке. В абсолютном большинстве наблюдений абсцессы сопровождаются клинической картиной воспалительного процесса в брюшной полости. Печень и селезенка при соблюдении методики исследования доступны для УЗИ во всех отделах. Для более детального осмотра поддиафрагмальных отделов используют приемы «полипозиционности». Больные укладываются на правый или левый бок, руку запрокидывают вверх с небольшим сгибанием туловища. Выдох после глубокого вдоха увеличивает обзор.
Исследование проводят секторным датчиком по межребер- ным промежуткам по подмышечным линиям. При обнаруже-
Рис. 4.3. Продольное сканирование по передней подмышечной линии. Сформированный многокамерный абсцесс VIII сегмента печени. В полости лоцируется соединительнотканная перегородка.
нии патологического образования проводят топический диагноз для дифференцирования внутриорганных абсцессов с абсцессами брюшной полости (табл. 4.1).
Таблица 4.1
Дифференциальный диагноз абсцессов печени, селезенки и поддиа- фрагмальных абсцессов
| Признаки | Абсцессы печени | Поддиафрагмальные |
| и селезенки | абсцессы | |
| Увеличение органа | Отмечается всегда | Редко встречается |
| Размер | Вариабелен | Вариабелен |
| Форма | Округлая | Серповидная |
| Структура | Неоднородная | Более однородна |
| Эхогенность | Низкая или средняя | Низкая |
| Контур | Четкий, неровный | Четкий, ровный, ги- перэхогенный |
| Изменения окру | Зона перифокального | Нет зоны перифо |
| жающих тканей | воспаления | кального воспаления |
| Рентгенологичес | Только при крупных га | Присутствует почти |
| кая семиотика | зосодержащих абсцессах всегда | |
Подпеченочные абсцессы чаще всего небольшого размера, округлой или полициклической формы, неоднородной структуры. Эхогенность их снижена. Контур четкий и неровный. Хорошо выражена капсула высокой эхогенности. Подпеченочные абсцессы чаще, чем внутрипеченочные, сопровождаются выпотом в правых отделах брюшной полости.
При подозрении на абсцессы селезенки (учитывая их редкость) в сомнительных случаях необходимо принимать во внимание, что УЗ-картины абсцесса селезенки и дна желудка сходны. Для этого УЗИ выполняют в динамике через 30 мин после обильного питья. В случаях, когда наполнение желудка бывает противопоказано, в желудочный зонд вводят 20,0 мл глюкозы. Диагноз уточняют по наличию или отсутствию передвижения вводимой жидкости в образовании.
Мелкие, до 15 мм в диаметре, абсцессы печени дифференцируют с септическими очагами. Последние отличают небольшой диаметр (до 10—15 мм), правильная форма, ровные, четкие контуры, однородная структура и несколько сниженная эхогенность, а также отсутствие эхогенной капсулы и зоны перифокального воспаления. Они могут быть единичными и множественными. Но главное их отличие от абсцессов печени заключается в быстроте появления и обратного развития при адекватной антибиотикотерапии. Мы наблюдали септические очаги в печени у 4 больных • — у 2 с сепсисом и абсцессами брюшной полости и у 2 с разлитым гнойным перитонитом. Ни в одном случае трансформации в абсцесс не произошло.
Из сопутствующих изменений у больных с внутриорганны- ми абсцессами отмечено: увеличение пораженного органа; закругление нижнего края печени; диффузное повышение эхогенности паренхимы печени; реактивное утолщение и повышение эхогенности стенки желчного пузыря; реактивный выпот в плевральной полости (у больных с абсцессами VII и VIII сегментов печени). У 1 ребенка лоцировались увеличенные лимфатические узлы по ходу воротной вены.
У первично неоперированных больных проводился дифференциальный диагноз между абсцессом и гематомой. УЗ-симп- томатика этих заболеваний очень схожа. При гематомах в зависимости от срока существования эхогенность содержимого варьирует от низкой до ее полного отсутствия, структура более однородна, отсутствует зона перифокального воспаления.
Чувствительность метода для внутриорганных абсцессов, по нашим данным, составила 95,5 %, точность — 97,2 %, прогностическое значение положительного результата — 95,5 %, прогностическое значение отрицательного результата •—98,1 %, эффективность метода УЗИ равнялась 96,9 %.
источник
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Абсцессом брюшной полости является воспаление органов брюшной полости гнойного характера с дальнейшим их расплавлением и образованием в них гнойной полости различного размера с наличием пиогенной капсулы. Он может сформироваться в любой части брюшной полости с формированием целого ряда клинических синдромов: септического, интоксикационного, лихорадочного.

Количество проводимых хирургических вмешательств на органах брюшной полости постоянно растет. Это, применение огромного числа самых разнообразных антибиотиков, а также сильное ослабление иммунной системы организма вследствие быстрой урбанизации приводит к частому развитию послеоперационных абсцессов брюшной полости. По статистике, послеоперационный осложнения в виде образования абсцессов развиваются у 0,8% пациентов после плановых полостных оперативных вмешательств и у 1,5% — после экстренных операций.

Как правило, абсцессы брюшной полости развиваются после получения различных травм, перенесения инфекционных заболеваний ЖКТ, воспалительных процессов в органах, которые находятся в брюшной полости, а также вследствие перфорации дефекта при язве желудка или двенадцатиперстной кишки.
- Следствие вторичного перитонита, (перфоративный аппендицит; несостоятельность анастомозов после полостных операций, панкреонекроз после операции, травматические повреждения) и т. д.
- Воспаления внутренних женских половых органов гнойного характера (сальпингиты, воспаление придатков яичников, гнойные параметриты, пиосальпинксы, тубоовариальные абсцессы).
- Острый панкреатит и холецистит, неспецифический язвенный колит.
Остеомиелит позвоночника, спондилит туберкулезной этиологии, воспаление околопочечной клетчатки.
Основными возбудителями абсцессов являются аэробная (Escherichia coli, протеи, Staphylococcus и Streptococcus и др.) и анаэробная (Clostridium, Bacteroides fragilis, Fusobacteriales) бактериальная флора.

Очень часто абсцессы органов брюшной полости развиваются вследствие хирургических вмешательств на органах брюшной полости (чаще всего, после операций на желчных путях поджелудочной железы, кишечнике). Бывают случаи, когда брюшина инфицируется уже после проведения вмешательства, особенно, при несостоятельности анастомоза.
В 70% случаев абсцесс развивается в внутрибрюшинно или в забрюшинной области, в 30% он локализуется внутри какого-либо органа.

Абсцесс брюшной полости развивается вследствие гиперреактивности иммунной системы при активном росте и размножении стрептококковой и стафилококковой флоры, а также кишечной палочки (аппендикулярный абсцесс). Возбудители проникают в брюшную полость лимфогенным или гематогенным путем, а также контактно через фаллопиевые трубы, когда происходит деструктивное воспаление органов или органа, ранение, перфорация, несостоятельность швов, которые были наложены в процессе хирургического вмешательства.
Основным отличием абсцесса брюшной полости является тот факт, что очаг воспаления четко ограничивается от здоровых тканей, которые его окружают. Если пиогенная оболочка разрушается, развивается сепсис и гнойные затеки. Гнойники могут быть как одиночными, так и многочисленными.

Первые признаки абсцесса брюшной полости варьируются, но в большинстве случаев у пациентов наблюдаются:
- Резкая лихорадка, озноб, которое сопровождается слабо выраженными тянущими ощущениями в области живота, которые усиливаются при пальпации.
- Частые позывы к мочеиспусканию (так как брюшная полость находится недалеко от мочевого пузыря.
- Запоры.
- Тошнота, которая может сопровождаться рвотой.
Также другими объективными симптомами абсцесса брюшной полости являются:
- Тахикардия, повышенное артериальное давление.
- Напряжение мышц передней стенки живота.
Если абсцесс поддиафрагмальный, то среди основных симптомов также присутствуют:
- Болевые ощущения в районе подреберья, которые могут усиливаться во время вдоха и иррадиировать в лопатку.
- Изменением в ходьбе пациента, он начинает наклонять туловище в сторону дискомфорта.
- Высокая температура тела.

Если не диагностировать абсцесс брюшной полости вовремя и не начать правильное лечение, могут возникнуть достаточно серьезные последствия:
Именно поэтому, если вы почувствовали какой-либо дискомфорт или боль в области живота, необходимо сразу же обратиться за помощью к гастроэнтерологу или терапевту.

Основными методами диагностики являются:
- Рентген органов грудной и брюшной полости.
- Ультразвуковое исследование.
- КТ и МРТ как вспомогательные методы диагностики.
- Взятие пункции из заднего свода влагалища или передней стенки прямой кишки (если существует подозрение на развитие абсцесса дугласовой зоны).

Если диагностировать абсцесс не удается из-за отсутствия каких-либо симптомов, на могут быть назначены анализы, в том числе и общий анализ крови. При этом заболевании у пациента практически всегда наблюдается лейкоцитоз, иногда нейтрофиллез (резкий сдвиг лейкоцитарной формулы влево), а также увеличение СОЭ.

С помощью рентгена органов грудной полости можно заметить, что на пораженной стороне купол диафрагмы высоко стоит. В плевральной зоне можно увидеть реактивный выпот. При поддиафрагмальном абсцессе на рентгенологических снимках можно заметить газовый пузырь и уровень жидкости под ним.
«Золотым» стандартом диагностики абсцессов брюшной полости различной локализации является ультразвуковое исследование. УЗИ-признаками являются: четко очерченное жидкостное образование в капсуле, содержимое которого неоднородное и имеет вид нитевидной структуры или эхогенной взвеси. Имеет место так называемый эффект реверберации из-за газов, когда многократные отражения звука постепенно уменьшают его интенсивность.
Лечение заключается в проведении хирургической операции, целью которой является устранение гнойника и дренирование с помощью катетера.
Медикаментозное лечение не дает возможности вылечить абсцесс брюшной полости, но с помощью различных антибиотиков можно ограничить распространение инфекции. Именно поэтому врачи назначают их пациентам до и после хирургического вмешательства. Преимущественно используют препараты, которые способны подавить развитие кишечной микрофлоры. В некоторых случаях также рекомендованы антибиотики, которые проявляют активность по отношению к анаэробным бактериям, в том числе и к Pseudormonas.
Метронидазол. Эффективное противомикробное и противопротозойное средство. В лекарстве находится активное вещество метронидазол. Он способен восстанавливать 5-нитрогруппу внутриклеточными протеинами у простейших и анаэробных бактерий. После восстановления данная нитрогруппа взаимодействует с ДНК бактерий, вследствие чего происходит угнетение синтеза нуклеиновых кислот возбудителей и они погибают.
Метронидазол эффективен в борьбе с амебами, трихомонадами, бактероидами, пептококками, фузобактериями, эубактериями, пептострептококками и клостридиями.
Метронидазол обладает высокой абсорбцией и эффективно проникает в пораженные ткани и органы. Дозировка является индивидуальной и устанавливается лечащим врачом в зависимости от состояния пациента. Больным с непереносимостью метронидазола, эпилепсией в анамнезе, заболеваниями центральной и периферической нервной системы, лейкопенией, неправильной работой печени использовать препарат запрещено. Также нельзя назначать во время беременности.
В некоторых случаях применение средства может вызывать: рвоту, анорексию, диарею, глоссит, панкреатит, мигрени, вертиго, депрессию, аллергию, дизурию, полиурию, кандидоз, частое мочеиспускание, лейкопению.
Профилактические меры основываются на адекватном и своевременном лечении различных заболеваний органов, которые находятся в брюшной полости. Также очень важно вовремя поставить правильный диагноз при остром аппендиците и сделать операцию по его удалению.

Смертность при абсцессе брюшной полости составляет от 10 до 40%. Прогноз в большой мере зависит от того, насколько серьезная фоновая патология, какое состояние больного, где локализован гнойник.

источник
Абсцесс брюшной полости – это ограниченный гнойник в брюшной полости, заключенный в пиогенную капсулу. Особенности клиники зависят от локализации и величины гнойного очага; общими проявлениями абсцесса брюшной полости служат боль и локальное напряжение мышц живота, лихорадка, кишечная непроходимость, тошнота и др. Диагностика абсцесса включает обзорную рентгенографию органов брюшной полости, УЗИ и КТ брюшной полости. Лечение заключается во вскрытии, дренировании и санации гнойника; массивной антибактериальной терапии.
В широком смысле к абсцессам брюшной полости в абдоминальной хирургии относят внутрибрюшинные (интраперитонеальные), забрюшинные (ретроперитонеальные) и интраорганные (внутриорганные) абсцессы. Внутрибрюшинные и забрюшинные гнойники, как правило, располагаются в области анатомических каналов, карманов, сумок брюшной полости и клеточных пространствах ретроперитонеальной клетчатки. Внутриорганные абсцессы брюшной полости чаще образуются в паренхиме печени, поджелудочной железы или стенках органов.
Пластические свойства брюшины, а также наличие сращений между ее париетальным листком, сальником и органами, способствуют отграничению воспаления и формированию своеобразной пиогенной капсулы, препятствующей распространению гнойного процесса. Поэтому абсцесс брюшной полости еще называют «отграниченным перитонитом».
В 75% случаев абсцессы располагаются внутри- или забрюшинно; в 25% — внутриорганно. Пиогенная флора абсцессов чаще полимикробная, сочетающая аэробные (кишечную палочку, протей, стафилококки, стрептококки и др.) и анаэробные (клостридии, бактероиды, фузобактерии) микробные ассоциации. Причины абсцесса:
- Перитонит. В большинстве случаев формирование абсцессов брюшной полости связано с вторичным перитонитом, развивающимся вследствие попадания в свободную брюшную полость кишечного содержимого при перфоративном аппендиците; крови, выпота и гноя при дренировании гематом, несостоятельности анастомозов, послеоперационном панкреонекрозе, травмах и т. д. Типичными местами локализации служат большой сальник, брыжейка, малый таз, поясничная область, поддиафрагмальное пространство, поверхность или толща тканей паренхиматозных органов.
- Инфекционные процессы в малом тазу. Причиной абсцесса могут выступать гнойные воспаления женских гениталий – острый сальпингит, аднексит, параметрит, пиовар, пиосальпинкс, тубоовариальный абсцесс.
- Заболевания органов ЖКТ. Встречаются абсцессы брюшной полости, обусловленные панкреатитом: в этом случае их развитие связно с действием ферментов поджелудочной железы на окружающую клетчатку, вызывающим выраженную воспалительную реакцию. В некоторых случаях абсцесс брюшной полости развивается как осложнение острого холецистита или прободения язвы желудка и 12-перстной кишки, болезни Крона.
- Инфекции забрюшинного пространства. Псоас-абсцесс может являться следствием остеомиелита позвоночника, туберкулезного спондилита, паранефрита.
По ведущему этиофактору различают микробные (бактериальные), паразитарные и некротические (абактериальные) абсцессы брюшной полости.
В соответствии с патогенетическим механизмом выделяют посттравматические, послеоперационные, перфоративные и метастатические гнойники.
По расположению относительно брюшины абсцессы делятся на забрюшинные, внутрибрюшинные и сочетанные; по количеству гнойников — одиночные или множественные.
По локализации встречаются:
- поддиафрагмальные,
- межкишечные,
- аппендикулярные,
- тазовые (абсцессы дугласова пространства),
- пристеночные
- внутриорганные абсцессы (внутрибрыжеечные, абсцессы поджелудочной железы, печени, селезенки).
В начале заболевания при любом виде абсцесса брюшной полости превалирует общая симптоматика: интоксикация, интермиттирующая (перемежающаяся) лихорадка с гектической температурой, ознобами, тахикардией. Часто отмечается тошнота, нарушение аппетита, рвота; развивается паралитическая кишечная непроходимость, определяется выраженная болезненность в зоне гнойника, напряжение брюшных мышц. Симптом напряжения мышц живота наиболее выражен при абсцессах, локализующихся в мезогастрии; гнойники поддиафрагмальной локализации, как правило, протекают со стертой местной симптоматикой. При поддиафрагмальных абсцессах может беспокоить боль в подреберье на вдохе с иррадиацией в плечо и лопатку, кашель, одышка.
Симптомы тазовых абсцессов включают абдоминальные боли, учащение мочеиспускания, понос и тенезмы вследствие рефлекторного раздражения мочевого пузыря и кишечника. Для забрюшинных абсцессов характерна локализация боли в нижних отделах спины; при этом интенсивность боли усиливается при сгибании нижней конечности в тазобедренном суставе. Выраженность симптоматики связана с величиной и локализацией гнойника, а также с интенсивностью проводимой противомикробной терапии.
Обычно при первичном осмотре абдоминальный хирург обращает внимание на вынужденное положение пациента, которое он принимает для облегчения своего состояния: лежа на боку или спине, полусидя, согнувшись и т. д. Язык сухой, обложен сероватым налетом, живот незначительно вздут. Пальпация живота обнаруживает болезненность в отделах, соответствующих локализации гнойного образования (в подреберье, глубине таза и др.). Наличие поддиафрагмального абсцесса характеризуется асимметрией грудной клетки, выпячиваем межреберий и нижних ребер. В общем анализе крови обнаруживаются лейкоцитоз, нейтрофилез, ускорение СОЭ.
Решающая роль в диагностике абсцесса брюшной полости отводится рентгенологическому обследованию. Как правили, обзорная рентгенография брюшной полости позволяет выявить дополнительное образование с уровнем жидкости. При контрастном исследовании ЖКТ (рентгенографии пищевода и желудка, ирригоскопии, фистулографии) определяется оттеснение желудка или петель кишечника инфильтратом. При несостоятельности послеоперационных швов контрастное вещество поступает из кишечника в полость абсцесса. УЗИ брюшной полости наиболее информативно при абсцессе верхних ее отделов. При сложностях дифференциальной диагностики показано проведение КТ, диагностической лапароскопии.
Хирургическое лечение проводится под прикрытием антибактериальной терапии (аминогликозидов, цефалоспоринов, фторхинолонов, производных имидазола) для подавления аэробной и анаэробной микрофлоры. Принципы оперативного лечения всех видов абсцессов заключаются во вскрытии и дренировании, проведении адекватной санации. Доступ определяется локализацией гнойника: поддиафрагмальные абсцессы вскрывают внебрюшинно или чрезбрюшинно; абсцессы дугласова пространства – трансректально или трансвагинально; псоас-абсцесса – из люмботомического доступа и т. д.
При наличии множественных абсцессов выполняется широкое вскрытие брюшной полости. После операции оставляют дренаж для активной аспирации и промывания. Небольшие одиночные поддиафрагмальные абсцессы могут быть дренированы чрезкожно под ультразвуковым наведением. Однако при неполной эвакуации гноя велика вероятность рецидива гнойника или его развития в другом месте субдиафрагмального пространства.
При одиночном абсцессе прогноз чаще благоприятный. Осложнениями абсцесса может явиться прорыв гноя в свободную плевральную или брюшную полость, перитонит, сепсис. Профилактика требует своевременного устранения острой хирургической патологии, гастроэнтерологических заболеваний, воспалительных процессов со стороны женской половой сферы, адекватного ведения послеоперационного периода после вмешательств на органах брюшной полости.
источник
Наиболее трудными для диагностики и грозными по своим последствиям являются абсцессы брюшной полости.
При подозрении на развитие абсцессов брюшной полости необходимо тщательное динамическое УЗИ. По нашему мнению диагностика остаточных скоплений выпота, гнойников брюшной полости должна быть следствием активного и целенаправленного поиска, а не случайной находкой.
Необходимо сделать правилом проведение УЗИ на 3 4 сутки после операций, произведенных по поводу деструктивного аппендицита, осложненного диффузным или разлитым перитонитом, а так же, после операций по поводу острого аппендицита с атипичным расположением червеобразного отростка.
Такая диагностическая тактика позволяет выявлять и устранять пункционным способом ограниченные скопления жидкости в брюшной полости до развития абсцессов.
В ультразвуковом изображении жидкостные скопления имеют вид объемных эхонегативных или гипоэхогенных образований различной формы. При скоплении жидкости под диафрагмой или в подпеченочном пространстве скопления жидкости выглядят в виде серповидных или овальных образований (рисунок 15). При этом обычно бывает реактивный выпот в плевральном синусе (рисунок 16). Не менее важным диагностическим признаком служит уменьшение подвижности диафрагмы на стороне поражения.
Аналогичные скопления выпота в полости малого таза визуализируются либо в виде анэхогенной полоски жидкости различной толщи ны, либо в виде округлого гипоэхогенного образования, которое может выглядеть неоднородным, в связи с присутствием сгустков фибрина и гноя.
Скопления жидкости в межкишечных пространствах определяются как объемные, полиморфные, не имеющие четких контуров гипоэхогенные образования, отличить которые от содержимого в просвете прилежащих петель кишки помогает отсутствие перистальтических движений и перемещения в них содержимого (рисунок 17).
При трансформации скоплений жидкости в абсцессы, в их окружности происходит формирование различной степени плотности и толщины пиогенной капсулы.
Оптимальным вариантом устранения патологических скоплений жидкости, а также дренирования абсцессов брюшной полости является их пункция и дренирование под контролем ультразвука.
Подготовка к проведению чрескожного вмешательства предусматривает четкую локализацию полостного образования, определение кратчайшего пути к нему, на котором не должны находиться свободные плевральные синусы, кровеносные сосуды, по возможности паренхиматозные органы и кишечные петли.
При ограниченных жидкостных скоплениях бывает достаточно пункционного метода. Под ультразвуковым наведением производится пункция полостного образования, аспирация его содержимого, промывание полости антисептическим растворами (диоксидин, хлоргексидин) с аспирацией промывных вод. В последующем осуществляется динамический ультразвуковой контроль. Порой требуется 2-3 пункции, производимые через два-три дня до полного спадения стенок полости.
Для дренирования рецидивирующих внутрибрюшных жидкостных скоплений и сформированных абсцессов требуется использовать специальные стилет — катетеры, пункции под контролем УЗИ троакаром с последующим проведением через его просвет в полость абсцесса дренажной трубки. Может быть использован метод введения катетера по Сельдингеру. При необходимости длительного дренирования целесообразно использовать двухпросветные дренажи, что позволяет обеспечить проточно-аспирационное лечение по Н.Н.Каншину.
При наличии многокамерных полостных образований необходимо проведение фистулографии, для уточнения взаимоотношений этих полостей, наличия или отсутствия сообшения между ними. В последних случаях, для обеспечения адекватного дренирования необходимо введение дополнительных дренажей.
Примером успешного использования описанного пункционного метода лечения остаточных гнойников может служить следующее наблюдение.
Больная Д. 52 лет доставлена в клинику 13.10-97. через 7 дней от начала заболевания. При поступлении в стационар клиническая картина распространенного перитонита, полиорганной недостаточности. После предоперационной подготовки произведена средняя срединная лапаротомия. Диагностирован острый гангренозный перфоративный аппендицит, разлитой гнойный перитонит, множественные абсцессы брюшной полости (межкишечные, поддиафрагмальные, подпеченочный, тазовый). Произведена аппендэктомия, промывание брюшной полости с частичным удалением массивных фибринозных наложений, назоинтестинальная интубация. Операционная рана ушита редкими лавсановыми швами через все слои брюшной стенки, завязанными на «бантики» Произведено наружное дренирование грудного лимфатического протока.
В послеоперационном периоде проводилась массивная этиотропная антибактериальная терапия со сменой препаратов через 5-6 суток (цефалоспорины 111 поколения/метронидазол; амикацин/метронидазол; карбапенемы). С интервалом в сутки произведено 4 ревизии и санации брюшной полости. Интенсивная детоксикационная терапия включала лимфосорбцию (3-3,5 л/сут), УФО крови. Были обеспечены парентеральное питание, постоянная декомпрессия и лаваж тонкой кишки, санационные бронхоскопии, ГБО.
Состояние больной оставалось крайне тяжелым, сохранялись проявления печеной, почечной, дыхательной и сердечной недостаточности После прекращения хирургических санаций брюшной полости ежедневно производилось динамическое УЗИ. На 3 сутки после последней ревизии и санации брюшной полости обнаружено скопление жидкости в правом поддиафрагмальном пространстве и двухсторонний плеврит. Под контролем УЗИ выполнены плевральные пункции с удалением серозного транссудата. При пункции поддиафрагмального пространства получено 18 мл сливкообразного гноя. С интервалом 2 суток, с учетом результатов УЗИ, трижды производились пункции поддиафрагмального пространства с аспирацией содержимого и промыванием полости диоксидином.
Постепенно состояние больной улучшилось. Операционная рана зажила первичным натяжением. Выписана на амбулаторное лечение по поводу пролежня в области крестца.
В заключение следует отметить, что УЗИ не может решить всех проблемы диагностики острого аппендицита и его осложнений. Нужно помнить о том. что, как и при других методах исследования, при УЗИ можно получить как ложноположительные, так и ложноотрицательные данные. Только тщательная оценка всей совокупности данных анамнеза, физикального обследования, лабораторных данных, порой результатов нескольких инструментальных исследований выполненных неоднократно, позволяет прийти к правильному диагнозу.
И все же, на пути этих кропотливых исканий иногда не хватает малой толики, нюанса, «изюминки». Иногда этой «изюминкой» может стать неприметная, но очень важная деталь, выявленная при ультразвуковом исследовании, выполненным опытным исследователем.
Д.Г. Кригер, А.В.Федоров, П.К.Воскресенский, А.Ф.Дронов
источник
УЗИ-диагностика кистозных образований (кист) яичников
В клинической практике различают кисты и кистомы яичников. Киста – ретенционное опухолевидное образование – полость, заполненная жидкостью. При этом отсутствует пролиферация клеточных элементов, характерная для истинных опухолей (кистом). Нет убедительных данных о возможности развития рака яичников из ретенционных образований. Однако трудно провести дифференциальную диагностику их со злокачественным процессом.
К ретенционным, или простым кистам относятся фолликулярные кисты, кисты желтого тела (лютеиновые, тека-лютеиновые при пузырном заносе и хорионкарциноме), эндометриодные «шоколадные», паровариальные кисты.
В тех случаях, когда при гинекологическом исследовании выявляется то или иное патологическое образование в полости малого таза с помощью УЗИ можно решить ряд вопросов:
1) визуализировать пальпируемое образование на эхограмме;
2) установить его характер (жидкостное или мягкотканное);
3) точно локализовать относительно матки, яичников;
4) указать число и размеры образования, а также сделать точное описание эхографических характеристик объекта.
В распознавании кист и кистом яичников УЗИ органов малого таза имеет особую значимость, т.к. клиническая картина многих заболеваний бывает идентична, а данные гинекологического осмотра неспецифичными. Врач УЗИ должен исключить наличие вариантов нормы, воспалительных изменений, опухолей матки и, главное, провести дифференциальную диагностику между различными видами кист и опухолей яичников. Основным УЗИ-признаком кисты является обнаружение жидкостного образования в проекции яичника.
Фолликулярная киста развивается из зрелых или антральных фолликулов, часть сочетается с воспалительными заболеваниями матки и придатков, миомой матки. Это однокамерное, тонкостенное кистозное образования, наполненное прозрачным и светлым содержимым. Обычно к основанию кисты прилежит ткань макроскопически неизмененного яичника. Встречается в любом возрасте. При УЗИ малого таза визуализируется как эхонегативная структура.
Киста желтого тела встречается редко и возникает при воспалительных или гормональных изменениях в яичниках. Строение кисты сходно со строением желтого тела, отличается от него лишь размерами. Внутренняя поверхность кисты складчатая, содержимое – прозрачная жидкость. Чаще всего претерпевают обратное развитие.
В 50 % случаев пузырного заноса наблюдаются двусторонние лютеиновые кисты яичников, которые могут достигать больших размеров. После удаления пузырного заноса кисты исчезают в первые месяцы.
Эндометриодная («шоколадная») киста яичника – одно- или двустороннее образование, сине-багрового цвета с темно-геморрагическим содержимым. На эхограмме визуализируются нечетко, образуя множество эхо-сигналов. Эти кисты относятся к наружному перитонеальному эндометриозу и лечатся оперативно (лапараскопия, удаление кисты).
Паровариальная киста обычно небольших размеров, овоидной формы, гладкая, ограничена в подвижности. Протекает бессимптомно, при больших размерах могут быть боли внизу живота. Диагностика затруднена, в большинстве случаях при УЗ-исследовании такие кисты принимаются за кисты яичника. На УЗИ-органов малого таза виден здоровый яичник отдельно от паровариальной кисты.
Таким образом, ультразвуковое исследование органов малого таза на 5-7 день менструального цикла позволяет выявить, провести дифференциальную диагностику различных кистозных образований яичников.
Идентификация абсцессов на УЗИ. Диагностика абсцесса на узи.
При наличии у пациента участка отека, уплотнения, болезненности и покраснения бывает трудно дифференцировать целлюлит и абсцесс. Для дифференциальной диагностики этих состояний традиционно использовали аспирацию через иглу. Однако такая манипуляция болезненна и может увеличить риск инфекции. 1. Имеется ли абсцесс? 2. Имеются ли рядом с абсцессом сосуды? Важно распознать нормальную картину подкожных тканей и кожи (обсуждалось в предыдущем разделе). Часто при переходе от ткани с целлюлитом к здоровой ткани наблюдаются очевидные различия, относительная толщина различных тканей может указать на локализацию воспаления и инфекции. Абсцесс выглядит как гипоэхогенное или темное скопление жидкости, часто с серым гетерогенным содержимым внутри. Такие скопления жидкости нарушают архитектуру тканей. Они являются сжимаемыми, так как содержат жидкость. Также у них может наблюдаться эффект заднего акустического усиления, потому что звуковые волны, проходящие через наполненное жидкостью образование будут меньше ослабляться, чем волны, проходящие через окружающие ткани. Исследования поверхностных мягких тканей проводится с использованием высокочастотного (5—10 МГц) линейного датчика. Расположите пациента как для стандартного проведения манипуляции. Проведите сканирование над местом наибольшей флюктуации или над любой подозрительной областью. Отметьте наличие или отсутствие полости абсцесса, а также наличие расположенных рядом сосудов, которые могут помешать безопасному выполнению разреза и дренирования. Также отметьте любое расположенное глубже или латеральнее продолжение скопления жидкости. УЗИ иногда может выявить, что воспаление в поверхностных тканях является только «верхушкой айсберга» и заставит оператора провести дополнительную визуализацию или получить консультацию перед принятием решения о глубоком разрезе. Используя метки аппарата УЗИ, проведите измерение глубины от поверхности кожи до полости абсцесса. Можно использовать маркер, чтобы отметить локализацию полости. абсцессы на узи Оставшуюся часть манипуляции можно провести без использования УЗИ. В качестве альтернативы можно использовать ультразвуковой контроль в реальном времени при проведении иглы для аспирации, используя методику продольного доступа, описанную в нашей статье. Методика визуализации перитонзилярного абсцесса такая же, как и для других абсцессов. Единственным отличием является то, что для их идентификации лучше всего подходит высокочастотный внутриполостной датчик, так как благодаря его маленькой толщине датчик можно расположить в заднем глоточном пространстве, а высокая частота делает получаемые изображения легко читаемыми. На кончик датчика наносят гель, а стерильный колпачок служит барьером между датчиком и пациентом. Абсцесс выглядит в виде гипоэхогенного пространства под областью наибольшего отека. Использование УЗИ в этих условиях имеет несколько потенциальных преимуществ. Первое, можно избежать дискомфорта «сухого прокола», когда имеется уплотнение, но нет абсцесса. Второе, можно использовать цветовой допплер для определения глубины и локализации сонной артерии, чтобы не травмировать ее при проведении разреза и дренирования. На рисунке визуализирована игла при дренировании полости абсцесса. Как и при пункции сосуда, возможно использование статической локализации или контроля аспирации полости абспесса в реальном времени. Это зависит от способности больного вытерпеть длительную УЗ-визуализацию. УЗИ является более точным методом выявления абсцесса, чем только физикальное обследование (способность подтвердить диагноз 93 % против 81 %, способность опровергнуть диагноз 97 % и 77 % соответственно). Таким образом, при использовании УЗИ можно снизить число ненужных разрезов и дренирований. Другое исследование инфекции мягких тканей в ОР показало, что применение УЗИ изменило ведение около 50 % пациентов. Изменения ведения включали: распознавание скрытых абсцессов в случаях, когда ожидалось обнаружение только целлюлита, отмена вскрытия и дренирования, когда не было обнаружено абсцесса и проведение дополнительных обследований и консультаций.
Дата добавления: 2017-02-11 ; просмотров: 1243 | Нарушение авторских прав
источник
Доступная эффективность. Универсальный ультразвуковой сканер высокого класса, компактный дизайн и инновационные возможности.
Абсцесс печени — отграниченное гнойнодеструктивное нагноение ее паренхимы с очагом литического расплавления в центре, возникающее в результате заноса инфекции гематогенным, лимфогенным, холангиогенным или контактным путем, а также инфицирования интрапаренхиматозных и подкапсульных гематом. Впервые абсцесс печени был описан Гиппократом за 400 лет до н.э. Он предположил, что тяжесть течения заболевания может зависеть от характера содержимого абсцесса. В начале ХIХ века R. Bright впервые высказал предположение о возможности формировании абсцессов печени при амебиазе, а в 1890 г. W. Osler первым обнаружил амеб в абсцессе печени и каловых массах одного и того же пациента. P. Dieulafoy и H. Fitz среди различных причин формирования абсцессов печени рассматривали нагноительные болезни органов брюшной полости [1]. В 1926 г. впервые описан пилефлебитический абсцесс печени у больного дивертикулитом. В 1903 г. L. Rogers отметил связь между гнойным холангитом, обструкцией желчных протоков и абсцессами печени. До появления антибактериальных препаратов в 30-х годах прошлого века поздно диагностированный деструктивный аппендицит являлся основной причиной развития пилефлебитических абсцессов печени. В 1938 г. A. Ochsner и M. DeBakey, проанализировав протоколы операций и аутопсийный материал, установили, что в 35% наблюдений причиной формирования абсцессов печени являлся аппендицит [1].
Обычно абсцесс печени — вторичное заболевание, которое развивается на фоне уже имеющихся воспалительных изменений печени. Но встречаются абсцессы, которые являются проявлением первичного заболевания (паразитарной этиологии). Существует несколько классификаций абсцессов печени, единая классификация отсутствует. Наиболее ёмкой, на наш взгляд, является классификация абсцессов печени Б.И. Альперовича [2].
- Первичные абсцессы печени:
- бактериальные (кокковые, бациллярные, смешанные);
- паразитарные (амебные, аскаридные, эхинококковые, описторхозные, лямблиозные и др.).
- Вторичные нагноения печени:
- нагноения патологических новообразований печени (непаразитарной кисты печени, распадающегося рака, сифилитической или туберкулезной гранулемы);
- посттравматические нагноения печени (раны или гематомы, нагноение вокруг инородного тела печени).
- По количеству:
- одиночные;
- множественные.
Эпидемиология абсцессов печени изучена недостаточно. В разных странах показатели заболеваемости могут сильно отличаться, и составляют от 2,3 на 100 тыс. населения в Северной Америке до 275,4 на 100 тыс. на Тайване [3]. До начала эры антибактериальной терапии основной причиной развития абсцессов печени являлся острый аппендицит. Летальность была крайне высокой и составляла около 80%. С внедрением в клиническую практику антибиотиков и хирургических методов лечения этот показатель значительно снизился, оставаясь, однако, на уровне 10-40%. Параллельно изменилась и структура этиологических факторов абсцессов печени. На первый план стали выходить заболевания желчевыводящих путей и печени, злокачественные новообразования и осложнения инвазивных медицинских процедур [4, 5].
Этиология абсцессов печени гетерогенна. В качестве основных причин выделяют инфекционно-воспалительные заболевания, злокачественные новообразования, ятрогенные состояния и тупые травмы печени (см. таблицу). В развитых странах преобладают абсцессы бактериальной этиологии, в то время как в Юго-Восточной Азии и Африке наиболее частой их причиной остается амебиаз [3].
| Гематогенные абсцессы (портальные и артериальные) | Холангиогенные абсцессы | Абсцессы при заболеваниях печени | Ятрогенные причины и травмы |
|---|---|---|---|
| Сепсис | Холангит как следствие холедохолитиаза, стриктур, новообразований желчевыводящих путей, хронического описторхоза | Первичные злокачественные образования печени (аденокарцинома и др.) и метастатическое поражение печени | Чрескожные инъекции этанола Химиоэмболизация печеночной артерии Радиочастотная абляция образований печени |
| Воспалительные заболевания органов брюшной полости, ведущие к пилефлебиту: — аппендицит; — острый холецистит; — панкреатит; — дивертикулит; — болезнь Крона; — язвенный колит; — перитонит | Билиодигестивные анастомозы, свищи | Гранулемы печени | Оперативные вмешательства и эндоскопические процедуры на желчевыводящих путях и печени: — стентирование; — папиллосфинк-теротомия; — холедоходуоденостомия; — резекция печени; — ортотопическая трансплантация печени |
| Нарушение целостности кишечной стенки с последующим развитием бактериемии: — эндоскопическая полипэктомия; — неметастатический рак толстой кишки | Острый холецистит (гематогенный или прямой путь распространения инфекции) | Гематомы печени | Тупые травмы печени |
| Амебиаз |
Основными факторами риска развития печеночных абсцессов служат сахарный диабет, цирроз печени, иммунодефицитные состояния, пожилой возраст, мужской пол [4].
Несмотря на значительный прогресс медицины, критически важной остается ранняя и точная диагностика абсцессов печени. Трудности при трактовке клинической картины, результатов лабораторных и инструментальных методов исследования могут стать причиной поздней диагностики, несвоевременного начала лечения, развития тяжелых осложнений и, как следствие, неблагоприятного исхода заболевания. Так, по данным T. Pang и соавт., диагноз абсцесса печени удавалось установить в среднем через неделю после появления его первых симптомов [6].
Клинические проявления абсцессов печени неспецифичны и могут зависеть от их размера, количества и локализации. Большинство пациентов предъявляют жалобы на боль в правом подреберье, лихорадку и другие симптомы интоксикации (озноб, миалгию, слабость, потливость, тахикардию, тошноту, анорексию). Боль нередко усиливается при глубоком вдохе, перемене положения тела, может иррадиировать в правое плечо, лопатку, надплечье. При объективном обследовании может быть выявлена гепатомегалия. Иногда имеют место желтуха и асцит. На первый план часто выходит клиническая картина заболевания, приведшего к развитию абсцесса [2, 5-8].
Лабораторные показатели мало специфичны и отражают наличие активного воспалительного процесса. В общем анализе крови отмечаются лейкоцитоз, ускорение СОЭ. При биохимическом исследовании повышен уровень С-реактивного белка, билирубина, АЛТ, АСТ [1, 4].
Основными методами диагностики абсцессов печени являются УЗИ и КТ органов брюшной полости. Чувствительность этих методов составляет 96-100%. В то же время, по данным A. Lin и соавт., при обращении у 25% пациентов результаты УЗИ дают неопределенные результаты, а у 14% — ложноотрицательные [9].
Для определения этиологии абсцессов печени большое значение имеет бактериологическое исследование содержимого абсцесса и крови.
В ультразвуковой картине абсцесса печени имеется ряд особенностей, связанных со временем его существования. В фазе формирования при наличии соответствующих клинико-лабораторных данных в паренхиме печени можно выявить зону сниженной эхогенности с неоднородной структурой и нечеткими, переходящими в нормальную ткань контурами. В центральной части этой зоны сниженной эхогенности (зона интенсивного отека паренхимы) обычно выявляется анэхогенный бесструктурный участок, являющийся участком некроза ткани, пока без жидкостного компонента. Такая картина может наблюдаться непродолжительный отрезок времени (несколько часов). Впоследствии при параллельном нарастании клинических проявлений формируется жидкостьсодержащая анэхогенная полость с внутренним эхогенным содержимым, обусловленная наличием гноя и тканевого детрита. Помимо характерных для жидкостной структуры эхографических признаков (эффект усиления задней стенки, эффект боковых теней, эффект дистального псевдоусиления эхосигнала), наблюдаются некоторые особенные признаки: разделение содержимого полости абсцесса с образование границы «жидкость-жидкость» с горизонтальным уровнем, где более густая часть находится внизу; возможное появление в полости пузырьков воздуха (при наличии газпродуцирующей флоры, например род Klebsiella) в виде гиперэхогенных структур у верхней стенки, дающих эффект реверберации «хвост кометы»; перемещение всего внутреннего содержимого при изменении положения тела пациента; формирование четкого отграничения полости абсцесса от окружающей паренхимы печени в виде несколько неоднородного ободка (пиогенной оболочки) повышенной эхогенности толщиной 0,5-1,5 см [10].
В литературе нам встретилось описание ультразвуковой картины абсцесса печени в зависимости от преобладания инфильтративных или деструктивных изменений [11]. Авторы выделили два типа изображений абс цесса. Абсцессы I типа располагаются, как правило, в задних сегментах правой доли (VI, VII) и представляют собой участки паренхимы повышенной эхогенности различных размеров с нечеткими контурами неоднородной структуры с наличием очагов пониженной эхогенности или жидкостных образований неправильной формы, соответствующих участкам некроза. Такие абсцессы являются следствием воспалительной инфильтрации паренхимы при обострениях описторхозного холангита. Как показал опыт, учитывая преимущественно инфильтративный характер поражения, незначительный деструктивный компонент, эти абсцессы при своевременном обнаружении и адекватной антибактериальной терапии (лучше при внутрипортальном введении) могут быть излечены без оперативного вмешательства.
Абсцессы II типа являются следствием гнойного холангита, представляют собой неравномерно расширенные внутрипеченочные желчные протоки с утолщенными и уплотненными стенками, с наличием в просвете неоднородного эхогенного содержимого (гной, детрит). Для этих абсцессов характерны множественная локализация, небольшие размеры, связь с желчными протоками, стенки которых и являются стенками абсцессов. Абсцессы II типа развиваются из холангиоэктазов при длительной желчной гипертензии, обусловленной обструкцией протоков в результате склеротических изменений, стеноза большого дуоденального сосочка, обтурации описторхозным детритом.
Некоторые отличия может иметь эхографическая картина паразитарного абсцесса при амебиазе [10]. При попадании амеб развивается воспалительная инфильтрация с последующим формированием очагов некроза и лизиса печеночной ткани. При УЗИ вначале наблюдается умеренная, а затем и выраженная диффузно-очаговая неоднородность паренхимы печени со смешанной и преимущественно сниженной эхогенностью. Затем на этом фоне формируются гипоэхогенные участки неправильной формы различных размеров с неровными нечеткими контурами. В дальнейшем они образуют одну или несколько полостей, практически аналогичных по ультразвуковым признакам бактериальным абсцессам, но с рядом отличий: контуры обычно неровные с наличием «карманов», эхогенная оболочка вокруг абсцессов выражена нечетко, в полости абсцесса визуализируется неоднородное содержимое вплоть до наличия секвестров печеночной ткани и большого количества газов.
При прорывах абсцессов в брюшную, а иногда и плевральную полость, в забрюшинное пространство внепеченочно определяются скопления жидкости, аналогичной содержимому гнойника, может быть виден дефект капсулы печени.
Основным методом лечения абсцессов печени является их оперативное или чрескожное дренирование в сочетании с парентеральным введением антибиотиков [12-14]. Терапией первой линии обычно является комбинация цефалоспорина III поколения с метронидазолом. При небольших размерах абсцессов (менее 3 см) может применяться только системная антибиотикотерапия. При амебных абсцессах препаратами выбора являются метронидазол и тинидазол [1, 2, 4].
Ключом к успешному ведению пациентов с абсцессами печени часто являются своевременная диагностика и лечение заболеваний, ставших причиной их развития.
Для иллюстрации приведенного выше краткого обзора представляем клиническое наблюдение.
Пациент А., 1971 года рождения, инструктор по лечебной гимнастике. Обратился с жалобами на озноб, жар, слабость, отсутствие аппетита, незначительный неопределенный дискомфорт в правом подреберье.
Заболел за неделю до обращения в поликлинику, когда без видимой причины возникла острая «стреляющая» боль в надплечье и под лопаткой справа, усиливающаяся при дыхании. Пациент расценил боль как «мышечную». Провел сеанс лечебной гимнастики. Боль стихла. На следующий день возникла ноющая и колющая боль в правом подреберье с иррадиацией под правую лопатку, усиливающаяся при дыхании и движении. Температура тела повысилась до 37,8 °C.
На 3-й день после появления первых симптомов пациент обратился в поликлинику по месту жительства. При УЗИ органов брюшной полости выявлены признаки умеренной гепатомегалии, преимущественно правой доли печени, а в общем анализе крови отмечены лейкоцитоз до 14,6 • 109 /л и ускорение СОЭ до 59 мм/ч.
В последующие 4 дня боли в животе не возникали, однако нарастали слабость, анорексия, часто беспокоили жар и озноб. Сохранялась субфебрильная лихорадка. Принимал парацетамол. Обратился в нашу поликлинику.
Из анамнеза жизни известно, что пациент ведет здоровый образ жизни, не имеет вредных привычек. Три месяца назад выезжал в Японию, а около трех лет назад посещал Индию. Во время поездок и после них ничем не болел.
На момент обращения состояние средней тяжести. Температура тела 38,4 °C. Кожные покровы бледно-розового цвета. Подкожножировая клетчатка развита умеренно. Отеков нет. Периферические лимфатические узлы не пальпируются. В легких дыхание везикулярное, ослаблено справа в нижних отделах, хрипов нет. Тоны сердца ритмичные, ясные. АД 120/75 мм рт.ст. Пульс 102 уд/мин.
Живот не увеличен, участвует в акте дыхания, при поверхностной пальпации мягкий, безболезненный. Нижний край печени перкуторно у края реберной дуги. При пальпации печень мягкоэластической консистенции, безболезненная. Симптомы Ортнера и Мерфи отрицательные. Однако при глубокой пальпации в правом подреберье возникала колющая боль в правом надплечье. Френикус-симптом отрицательный с обеих сторон.
Стул один раз в день, оформленный, коричневого цвета, без патологических примесей. Мочеиспускание свободное, безболезненное.
Для уточнения диагноза пациенту было выполнено УЗИ органов гепатобилиарной зоны с ультразвуковой ангиографией:
Печень увеличена в размерах: переднезадний размер правой доли 14,3 см (N до 12,5 см), вертикальный размер правой доли 19,0 см (N до 15,0 см), переднезадний размер левой доли 9,3 см (N до 7,0 см). Диафрагмальный край ровный. Структура паренхимы печени неоднородная с наличием в правой доле в проекции V сегмента образования сниженной эхогенности, с несколько нечеткими контурами, размерами до 6,5 х 4,6 х 4,8 см, выраженно неоднородной структуры с наличием в центральных отделах участка умеренно повышенной эхогенности неоднородной структуры размерами 5,8 х 4,8 х 4,2 см, аваскулярного (рис. 1). По периферии образования — деформация сосудистого рисунка (рис. 2). Эхогенность печени обычная. Внутри- и внепеченочные желчные протоки не расширены, стенки их уплотнены. Диаметр воротной вены 1,2 см.
Рис. 1. В-режим. В правой доле печени в проекции V сегмента визуализируется образование сниженной эхогенности с нечеткими контурами выраженно неоднородной структуры с наличием в центральных отделах участка умеренно повышенной эхогенности неоднородной структуры.
источник